Технология производства акролеина
Министерство Образования и Науки РФ
Казанский Государственный
Технологический Университет
Кафедра: "Общей химической
технологии"
Курсовая работа
На тему: "Технология
производства акролеина"
КАЗАНЬ
2008
ПЛАН
1.
Технологическая
схема производства акролеина
2.
Материальный
баланс сложной параллельной необратимой реакции
3.
Технологические и
технико-экономические показатели
Реклама
Список литературы
1. Технологическая схема
производства акролеина
Из ненасыщенных алифатических альдегидов широкое применение в
промышленности получил акролеин.
Физические свойства: акролеин 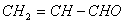 -
бесцветная жидкость с острым запахом. Температура кипения =
-
бесцветная жидкость с острым запахом. Температура кипения = 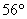 С, а температура плавления =
С, а температура плавления = 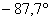 С. Плотность акролеина составляет 0,841
г/см
С. Плотность акролеина составляет 0,841
г/см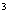 . Акролеин частично растворим в воде.
Так же он токсичен (пары его сильно раздражают слизистые оболочки глаз и
дыхательных путей), но опасность отравления им сравнительно невелика вследствие
легкости его обнаружения.
. Акролеин частично растворим в воде.
Так же он токсичен (пары его сильно раздражают слизистые оболочки глаз и
дыхательных путей), но опасность отравления им сравнительно невелика вследствие
легкости его обнаружения.
Акролеин является сырьем для промышленного синтеза аллилового
спирта, акрилонитрила и его производных. Значительное количество акролеина
расходуется на производство метионина (аминокислота, добавка которой в корм
домашней птицы ускоряет ее рост). Акролеин и его производные применяются в
синтезе полиуретанов, полиэфиров, различных пластификаторов и химикатов для
текстильной промышленности. Из способов получения акролеина практическое
значение имеют два:
1)
конденсация
формальдегида с ацетальдегидом
HCOH + CH3—CHO → CH2=CH—CHO
2)
прямое
окисление пропилена.
Метод прямого окисления пропилена является более перспективным
ввиду большей доступности и дешевизны сырья. Формально кинетическую схему этого
процесса можно представить следующим образом:
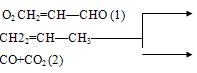
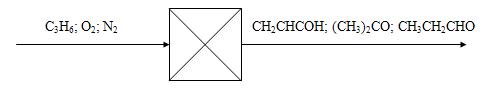
Технологическая схема одностадийного окисления пропилена в
реакторе с восходящим потоком катализатора представлена на рисунке 1. Реактор 2
изготовлен в виде трубы (высота 25 м, диаметр 0,75 м), соединенной
непосредственно с дозатором 1, где находится катализатор — молибдат висмута на
силикагеле. Температура в дозаторе около 420 °С, в реакторе 435 °С; давление
0,7—3 МПа. Температуру регулируют, охлаждая стенки реактора испаряющейся водой
и подавая воду с паром в дозатор 1. Кислород подают в нижнюю часть реактора и
дополнительно в несколько точек по его высоте. Пропилен вместе с
рециркулирующим газом тоже поступает в нижнюю часть реактора 2 и проходит снизу
вверх вместе с паром, кислородом и суспензированным катализатором. Реакционная
смесь, поступающая в реактор, имеет следующий состав [в % (мол.)]:
кислорода—7,5, пропилена — 21,5, водяного пара — 38; остальное — азот и
незначительное количество оксидов углерода. Скорость движения смеси в реакторе
составляет 6,1—7,6 м/с.
Парогазовый поток из реактора поступает в сепаратор 3 циклонного
типа, куда подают воду для "закалки" продуктов реакции (их
температура снижается до 290 °С). Катализатор в сепараторе 3 отделяют от продуктов
реакции и в горячем состоянии возвращают в дозатор 1. Часть пара, образующегося
за счет отвода выделяющегося тепла, по мере необходимости подают из
паросборника 4 в сепаратор 3, а основное количество пара вводят в нижнюю часть
дозатора 1. Газовый поток из сепаратора 3 после охлаждения в холодильнике (на
схеме не показан) поступает в сепаратор 5, где отделяются сконденсировавшиеся
вода и высококипящие продукты, а также катализатор, возвращаемый на окисление.
Несконденсировавшиеся продукты реакции из сепаратора 5 после холодильника 6 поступают
в газосепаратор 7, из которого парогазовый поток направляется в орошаемый водой
абсорбер 8. Газ из абсорбера возвращают на окисление (часть его периодически
сбрасывают в атмосферу во избежание накопления инертных примесей). Жидкие
продукты из сепаратора 7 и раствор из абсорбера 8 смешивают и подают в отпарную
колонну 9, с верха которой отбирают акролеин-сырец, направляемый на
ректификацию, а снизу — воду, подаваемую в дозатор 1 или сбрасываемую из
системы.
Выход акролеина составляет 71% в расчете на пропилен, при 50%-ной
степени конверсии пропилена и 91%-ной степени конверсии кислорода.
При двухстадийном окислении пропилена выход акролеина составляет 69—70%;
степень превращения пропилена — 95%.
Рисунок 1. Технологическая схема одностадийного окисления
пропилена:

1 —дозатор;
2 — реактор;
3, 5 — сепараторы циклонного типа;
4— паросборник;
6 — холодильник;
7 — газосепаратор;
9
— абсорбер;
9 — отпарная колонна.
2. Материальный баланс сложной
параллельной необратимой реакции
Задача:
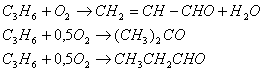
Исходные данные:
1. Производительность установки 80 т/сутки.
2. Состав безводной реакционной смеси (% мольных):
Акролеин 80
Ацетон 15
Масляный альдегид 5
3. Молярное соотношение "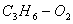 "
5:1
"
5:1
4. Концентрация  в смеси "
в смеси "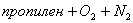 " (% об) 4,8
" (% об) 4,8
5. Потери пропилена % масс. От производительности установки 1,0
6. Концентрация технического 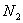 (%
об.) 100
(%
об.) 100
7. Концентрация технического  (%об.)
(примесь-азот) 95
(%об.)
(примесь-азот) 95
8. Конверсия пропилена (%) 100
Решение:
Материальный баланс:
|
приход
|
расход
|
|
кг/ч
|
кмоль/ч
|
кг/ч
|
кмоль/ч
|
|
C3H6
CH2CНСОН
(СН3)2СО
СН3СН2СНО
О2
N2
Н2О
|
2507,4
-
-
-
1702,24
26115,32
-
-
-
-
53,195
932,69
-
|
25,07
2647,66
514,33
171,33
-
26115,32
851,04
|
0,6
47,28
8,87
2,95
-
932,69
47,28
|
|
Σ1=30324,96
|
Σ2 = 30324,75
|
Молярные массы веществ:
Mr(C3H6)=12*3+1*6=42
кг/кмоль
Mr(CH2СНСОН)=12*3=1*4+16=56 кг/кмоль
Mr((CH3)2СО)=12*3+1*6+16=58кг/кмоль
Mr(CH3СН2СОН)=12*3+1*6+16 = 58кг/кмоль
Mr(О2)=16*2 = 32 кг/кмоль
Mr(N2) = 14*2 = 28 кг/кмоль
m(смеси) = 80 *100/24= 3333,33 кг/ч
Состав безводной реакционной смеси:
CH2СНСОН – 80 % моль Mr(CH2СНСОН) = 56 кг/моль
(CH3)2СО – 15 % моль Mr((CH3)2СО) = 58 кг/моль
CH3СН2СОН – 5 % моль Mr(CH3СН2СОН) = 58 кг/моль
Найдем массовый процентный состав
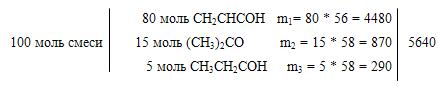
wмас (CH2СНСОН) = 4480/5640 * 100% = 79,43 %
wмас((CH3)2СО) = 870/5640 * 100% = 15,43 %
wмас (С2Н5СОН) = 290/5640 * 100% = 5,14 %
Состав
3333,33 реакционной смеси
CH2СНСОН – 79,43 % масс m1(CH2СНСОН) = 2647,66 кг/ч
CH3СН2СОН – 15,43 % масс m2 (CH3СН2СОН) = 514,33 кг/ч
С2Н5СОН
– 5,14 % масс m3(С2Н5СОН) = 171,33 кг/ч
ν(CH2СНСОН) = 2647,66/56 = 47,28 кмоль/ч
ν(CH3СН2СОН) = 514,33/58 = 8,87 кмоль/ч
ν(С2Н5СОН)
= 171,33/58 = 2,95 кмоль/ч
1
реакция
ν1(C3Н6) = ν(CH2СНСОН) = 47,28 кмоль/ч
ν1(O2) = ν1(C3Н6) = 47,28 кмоль/ч
ν1(H2O) = ν1(C3Н6) = 47,28 кмоль/ч
m(H2O) = 4747,28 * 18 = 851,04 кг/ч
2
реакция
ν2(C3Н6) = ν(CH3СН2СОН) = 8,87 кмоль/ч
ν2(O2) = 1/2 ν2(C3Н6) = 4,44 кмоль/ч
3
реакция
ν3(C3Н6) = ν(С2Н5СОН) = 2,95 кмоль/ч
ν3(O2) = 1/2 ν(С2Н5СОН)
= 1,475 кмоль/ч
Общее
количество затраченного кислорода
ν0(O2) = ν1+ν2+ν3 = 53,195 кмоль/ч
m0 (O2) =53,1995* 32 = 1702,24 кг/ч
Общее количество прореагировавшего пропилена
ν0(C3Н6) = 59,1 кмоль/ч m0 (C3Н6) = 59,1*42 = 2482,2 кг/ч
Конверсия
пропилена 100 % поэтому весь пропилен реагирует и его не остается. Количество
пропилена с учетом потерь 1 % масс
m0 (C3Н6) – (100-1)%
m (C3Н6) – 100 %
m (C3Н6) = 2482,2 * 100/99 = 2507,27кг/ч
ν(C3Н6) = m/Mr = 2507,27/42
59,7 кмоль/ч
Потери
пропилена
m (C3Н6) = 2507,27 – 2482,2 = 25,07 кг/ч
ν(C3Н6) = 25,07/43 = 0,6 кмоль/ч
V(O2) = ν0(O2)/22.4 = 1191.56 м3/ч
1191.56 – 4.8 %
V(C3Н6) – х %
V(C3Н6) = ν (C3Н6) * 22.4 = 1337,28 м3/ч
х =
1337,28 * 4.8/1191.56 = 5,38 %
Концентрация
C3Н6 в смеси C3Н6+О2+N2 = 5,38 %
отсюда
концентрация N2 = 100 – 5,38 – 4,8 = 89,82 %
Объем
азота в смеси всего:
191,56 –
4,8 %
х – 89,82
%
х = V1( N2) = 1191,56 * 89,82/4,8 = 22297,06 м3/ч
w1( N2) = V1( N2)/22,4 = 995,4 кмоль/ч
Количество
азота который поступает с техническим кислородом:
V(O2) – 95 %
V2( N2) – 5 %
V2( N2) = 1191/56 * 5/95 = 62,71 м3/ч
ν2( N2) = V2( N2)/22,4 = 62,71 кмоль/ч
Всего технического азота:
ν( N2) = ν1( N2) - ν2( N2) = 932,69 кмоль/ч
m( N2) = 932,69 * 28= 26115,32 кг/ч
Технологические
и технико-экономические показатели процесса
1. Пропускная
способность установки: 30324,96 кг/час.
2. Конверсия или степень
превращения пропилена: 100%.
3. Теоретические
расходные коэффициенты:
по С3Н6:
sтС3Н6 = Mr(C3H6) / Mr(CH2CНСОН) = 42 / 56 = 0,75 кг/кг;
по О2:
sтО2 = Mr(О2) / Mr(CH2CНСОН) = 32 / 56 = 0,57 кг/кг.
4. Фактические
расходные коэффициенты:
по С3Н6:
sфС3Н6 = m(C3H6) / m(CH2CНСОН) = 2507,4 / 2647,66 = 0,95 кг/кг;
по О2:
sфО2 = m(О2техн) /m(CH2CНСОН) = 1702,24+26115,32 / 2647,66 =
0,065 кг/кг.
Выход на
поданное сырье:
1)
Фактический выход
CH2CНСОН:
QФ = m (CH2CНСОН) = 2647,66 кг;
2)
Теоретический
выход CH2CНСОН:
Mr(С3Н6)
¾ Mr(CH2CНСОН),
42 ¾ 56,
m(С3Н6)
¾ QТ; 2507,4 ¾ QТ
;
QТ = (2507,4 * 56) / 42 = 3343,2 кг;
Выход CH2CНСОН по пропилену:
bС3Н6 = QФ / QТ * 100% = 2647,66 / 3343,2 * 100% = 79 %
РЕКЛАМА

СПИСОК ЛИТЕРАТУРЫ
1. Лебедев Н.Н. Химия и технология основного органического и
нефтехимического синтеза. Изд. 2-е, пер. М., "Химия", 2005, 736 с.
2. Юкельсон И.И. Технология основного органического синтеза.
М.: "Химия", 2008, 846 с.
3. Общая химическая технология /Под ред. А.Г.Амелина. М.: "Химия",
2007, 400 с.
4. Расчеты химико-технологических процессов /Под ред.
И.П.Мухленова. Л.:Химия, 2006, 300 с.