|
0,71
Для того чтобы исследование качества протеина
рыбной муки было эффективным, необходимо одновременно анализировать в ней сырой
и перевариваемый протеин и содержание небелкового азота. Так, если рыбная мука
имеет высокий протеин, но была сфальсифицирована за счет добавления азотистых
неорганических веществ, то коэффициент перевариваемости такого протеина будет
тоже высоким, так как в ходе анализа небелковая часть азота попадает с
перевариваемым протеином в одну фракцию. Эта мука будет казаться качественной,
однако действительную ценность ее протеина можно выявить только при дополнительном
исследовании на содержание небелкового азота. И наоборот, если в рыбной муке
количество небелкового азота оказалось в норме, то нельзя, основываясь только
на одном этом показателе, утверждать, что такая рыбная мука доброкачественная,
так как она могла быть приготовлена из трудноусваиваемого сырья. Качество такой
рыбной муки можно выявить при дополнительном анализе ее протеина на
перевариваемость.
Следовательно, для того чтобы всесторонне
оценить биологическую полноценность протеина рыбной муки, необходимо проводить
комплексное исследование ее по вышеперечисленным показателям.
.4 Принцип метода Къельдаля по определению
содержания общего азота
В зависимости от финансовых возможностей
предприятия и наличия специального оборудования, метод Къельдаля применяют в
ручном, полуавтоматическом и автоматическом режимах. Принцип метода остается
одним и тем же, но при автоматизации в два-три раза возрастает
производительность труда оператора, при этом уменьшается влияние человеческого
фактора на конечный результат. Кроме того, снижаются в два раза энергозатраты и
в три-четыре раза - количество вредных выбросов в окружающую среду.
Определение общего азота по методу Къельдаля
проводится в три основных этапа: минерализация (разложение) образца;
нейтрализация кислоты концентрированной щелочью с последующей перегонкой
(дистилляцией) водяным паром; титрование перегнанного дистиллята раствором
кислоты или щелочи известной концентрации (титрантом).
Минерализацию (разложение) образца проводят при
температуре 400-440ºС в концентрированной
серной кислоте в присутствии катализатора. Азот (N) из образца в виде аммиака
связывается с серной кислотой с образованием сульфата аммония ((NH4)2SO4).
Минерализат охлаждают, а затем разбавляют водой и нейтрализуют
концентрированной натриевой щелочью, в результате чего образуется гидроокись
аммония.
OH + H2SO4 => (NH4)2SO4 + H2O
(NH4)2SO4 + 2NaOH => 2NH4OH +
Na2SO4
Это нестойкое соединение, которое распадается на
аммиак и воду при нагревании. В нашем случае - при обработке обычным водяным
паром.
Дальше наступает этап перегонки (дистилляции)
паром. Аммиак вместе с паром попадают в приемную колбу, где аммиак связывается
со специальным раствором - ресивером. Таковым может служить серная, редко -
соляная, кислота, но чаще всего используют раствор борной кислоты, особенно в
полуавтоматических и автоматических системах.(См. рис 1,2)
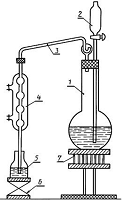
Рис.1 Установка типа Кьельдаля
- колба вместимостью 1000 см3;
- капельная воронка вместимостью 100 см3;
- каплеуловитель;
- холодильник;
- приемная колба вместимостью 250 см3;
- подъемный столик;
- колбонагреватель или электроплитка с
регулятором температуры, или газовая горелка.
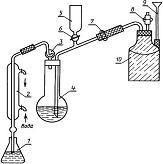
Рис. 2 Аппарат для отгонки аммиака с водяным
паром
- приемная колба;
- холодильник;
- каплеуловитель;
- отгонная колба;
, 9 - воронки;
, 7, 8 - краны;
- парообразователь
Затем дистиллят (ресивер со связанным аммиаком)
титруют. Прямое титрование (кислотой) проводят, если в качестве ресивера
применялась борная кислота, если же ресивером служили другие кислоты, то
проводят обратное титрование (щелочью). По количеству реагента, который был
истрачен на титрование связанного аммиака, определяют содержание общего азота.
Это значение умножают на 6,25 и получают массовую долю сырого протеина
.5 Причины расхождения результатов испытаний в
разных лабораториях
Существует несколько основных причин, по которым
результаты по одним и тем же образцам корма или сырья, исследованным в разных
лабораториях по методу Къельдаля, показывают различное содержание сырого
протеина. Это: гомогенность образца, масса навески, объем кислоты для
минерализации, соотношение катализатор/кислота, тип катализатора, время и
температура минерализации, оборудование для перегонки и титрования. Все эти факторы
влияют на достоверность исследований.
.5.1 Гомогенность образца
Этот фактор особенно критичен для образцов с
высоким содержанием протеина, таких как рыбная, мясная/мясокостная и перьевая
мука. После размола в каждой единице объема такого продукта все его
составляющие (кости, мышечная ткань, а для мясокостной муки из птицы -
дополнительно перо и содержимое кишечника) должны содержаться в тех же
пропорциях, что и в самом образце. Если в пробу, предназначенную для
определения сырого протеина, попадет больше костей, результат будет занижен,
если больше пера и/или мышечной ткани - завышен. В обоих случаях он будет
недостоверен.
Подобную картину можно наблюдать и при анализе
образцов с низком содержанием протеина, но с высоким содержанием пленок/лузги
(оболочек, шелухи) - ячменя и овса. Если в пробу попадет больше пленок (при
размоле они обычно как бы всплывают наверх), результат будет занижен.
Аналогичная ситуация может сложиться и с рассыпной готовой продукцией, особенно
при ее расслоении при транспортировке. В связи с этим размалывать навеску
образца необходимо так, чтобы размер частиц по возможности не превышал 1 мм,
хотя это и проблематично для мясной и мясокостной муки, особенно с высоким
содержанием жира.
.5.2 Масса навески
Оптимальной навеской при определении азота по
методу Къельдаля является навеска продукта, содержащего от 10 до 100 мг азота.
Например, в рыбной муке, согласно сопроводительным документам поставщика,
содержится 65% сырого протеина. Это значит, что в 1 г рыбной муки должно
содержаться 650 мг сырого протеина или 104 мг общего азота (при делении на
коэффициент 6,25). Таким образом, нам подходит навеска рыбной муки в диапазоне
от 0,1 г (10,4 мг азота) до 0,96 г (99,8 мг азота). При этом следует помнить,
что очень маленькая навеска не будет репрезентативной, что снизит достоверность
результатов, особенно для образцов с низкой гомогенностью. В то же время при
взятии очень большой навески, хотя и репрезентативной, увеличиваются
продолжительность ее сжигания, а возможно даже неполное сжигание, объем
используемого титранта и время титрования. Таким образом, для данного образца
рыбной муки с ожидаемым содержанием сырого протеина на уровне 65% оптимальной
можно считать навеску 0,6-0,8 г.
Для жмыхов, шротов, дрожжей, полножирной сои,
БВМК мы обычно берем навеску 0,7-0,9 г; для зерновых, молочной сыворотки,
премиксов - 1,0-1,2 г; для кровяной муки - 0,3-0,4 г, для комбикормов - 0,8-1,0
г.
1.5.3Объем кислоты для минерализации
При применении метода Къельдаля в классическом
(ручном) варианте требуемый объем концентрированной серной кислоты для
минерализации навески составляет 25 мл, в полуавтоматическом или автоматическом
(на специальном оборудовании) - 12 мл. (Принцип расчета этой цифры обычно
указывают в руководствах для пользователей, прилагаемых к оборудованию для
определения сырого протеина.) При недостаточном объеме кислоты разложение
образца будет неполным, а результат исследования - неверным (часто заниженным).
Соотношение катализатор/кислота носит
принципиальный характер и влияет на скорость и полноту минерализации образца.
Чистая концентрированная серная кислота кипит при температуре 338°С, а
разложение образца начинается при 373°С. Для того чтобы повысить температуру
кипения кислоты до необходимого уровня (иначе она частично испарится до начала
процесса минерализации), добавляют катализаторы - соли различных металлов. В
зависимости от вида катализатора соотношение кислота/катализатор колеблется в
диапазоне от 1,4 до 2,0.
.5.4Вид катализатора
При определении азота методом Къельдаля чаще
применяют так называемые медные, селеновые и ртутные катализаторы. Наиболее
эффективным признан катализатор на основе окиси ртути (HgO), так как по
сравнению с другими катализаторами в его присутствии разложение всех видов
образцов происходит в 1,5-2 раза быстрее. Однако с экологической точки зрения
от ртутного катализатора отказываются в пищевой и комбикормовой промышленности
по всему миру. Селеновый и медный катализаторы по своей эффективности
приблизительно одинаковы. Наиболее доступен, надежен и безопасен в работе
медный катализатор, представляющий собой смесь 7 г сернокислого калия и 0,8 г
сернокислой меди. Его в основном и используют при проведении исследований
методом Къельдаля.
.5.5 Время и температура минерализации
При использовании медного катализатора время,
необходимое для полной минерализации (разложения) при температуре 420°С, обычно
составляет 50-60 мин для всех видов сырья и готовой продукции при условии
правильного выбора размера навесок.
Процесс минерализации условно разделим на два
этапа: на первом этапе, когда минерализат становится прозрачным, восстановление
азота составляет 95-100% (в зависимости от вида образца); на втором -
восстанавливается оставшийся азот. При недостаточных времени и температуре
минерализации результаты исследования могут быть занижены из-за неполного
восстановления азота. Поэтому после осветления раствора процесс минерализации
следует продолжить еще как минимум 10-15 мин. Однако если сильно превысить
необходимые для разложения образца время (в 1,5-2 раза) и температуру (более
440°С), возможны потери азота уже от излишнего испарения кислоты, особенно при
большой мощности вытяжной системы. Также возможны потери в самом начале
процесса разложения из-за повышенного пенообразования, когда образец остается
на стенках колбы или даже выплескивается из нее, а также активного испарения
при излишне мощной работе вытяжной системы. Пенообразование характерно для
образцов с повышенным содержанием жира, а также для жидких образцов. Для
гашения пены используют октанол.
Все перечисленное выше может привести к
искажению результатов, обычно - к занижению.
.5.6 Перегонка (дистилляция) и титрование
При работе ручным, или классическим, методом
Къельдаля возможен ряд типичных ошибок. Например, при неправильной сборке
перегонного устройства концентрированную щелочь для нейтрализации минерализата
иногда приливают не в собранную перегонную систему, а в отдельную колбу для
перегонки, которую только потом присоединяют к системе. В этом случае в колбе
происходит термическая реакция (взаимодействие концентрированной кислоты и
щелочи), при которой часть азота испаряется. Кроме того, часто трубка
холодильника перегонной системы не погружена в ресивер (как это указано в
ГОСТ), то есть висит над горлышком приемной колбы. Поэтому пар с аммиаком не
«пробулькивает» через ресивер, а просто капает в приемную колбу. Потери азота в
этом случае неизбежны (испарение аммиака в окружающую среду) и могут достигать
10% от его общего содержания в образце.
Очень важно внимательно относиться к
концентрации (титру) кислот или щелочей, которыми оттитровывается дистиллят.
Если раствор для титрования будет приготовлен даже изгосударственного
стандарт-титра с действующим сроком годности, его необходимо обязательно
перепроверять, так как не всегда он соответствует заявленной концентрации.
.6 Конструкция Vapodest 20
Корпус (1) изготовлен из химически устойчивого
пластика и отличается исключительной долговечностью. Сенсорная панель
управления (2), стойкая к агрессивным средам, обеспечивает легкость управления
прибором. Информация обо всех стадиях выполнения программы, а также сообщения
об ошибках воспроизводятся на дисплее (3). В рабочем пространстве располагаются
реакционный сосуд (4), каплеуловитель (5), холодильник (6), приемная колба (7)
и тефлоновые трубки для подачи реагента (8) и водяного пара (9).
Защитная дверца (10) из плексигласа предохраняет
от брызг и позволяет наблюдать за ходом процесса. В качестве реакционного
сосуда применяются колбы Къельдаля с широким горлом. Для дозирования реагента и
снабжения парогенератора дистиллированной водой используются специальные
насосы. Генератор пара оснащен контроллером давления и защитой от перегрева,
которые обеспечивают полную безопасность. Его мощность может варьироваться в
диапазоне 40-100%, что существенно расширяет аналитические возможности прибора.
Фиксация зажимным устройством пробирки с
анализируемой пробой в приборе (11). Добавление определенного количества
реагента в реакционный сосуд через тефлоновую трубку (8) согласно
активированной программе. Подача перегретого пара из парогенератора через
заданное программой время по трубке (9) для быстрой отгонки определяемого
вещества в приемную колбу (7). По окончанию дистилляции прибор сразу готов для
дальнейшей работы. Оператор должен лишь сменить реакционный сосуд и приемную
колбу.

Рис.3 Внешний вид Vapodest 20
1.7 Фотометрический индофенольный метод
определения азота
Сущность метода заключается в разложении
органического вещества пробы концентрированной серной кислотой с образованием
солей аммония и последующем фотометрическом определении азота в виде
окрашенного индофенольного соединения, образующегося в щелочной среде при
взаимодействии с салицилатом и гипохлоритом натрия и имеющего максимум
светопоглощения при 655 нм. Концентрация азота в фотометрируемых растворах
должна быть 0,01-0,14 мг/см3.
1.8 Титриметрический или объемный метод анализа
1.8.1 Сущность метода и его достоинства
Титриметрический или объемный метод анализа
является одним из методов количественного анализа. В основе этого метода лежит
точное измерение объемов растворов двух веществ, реагирующих между собой.
Количественное определение с помощью титриметрического метода анализа
выполняется довольно быстро, что позволяет проводить несколько параллельных
определений и получать более точное среднее арифметическое. В основе всех
расчетов титриметрического метода анализа лежит закон эквивалентов. По
характеру химической реакции, лежащей в основе определения вещества, методы
титриметрического анализа подразделяют на следующие группы: метод нейтрализации
или кислотно-основного титрования; метод окисления- восстановления; метод
осаждения и метод комплексообразования.
Титрование - это постепенное прибавление
титрованного раствора реагента (титранта) к анализируемому раствору для
определения точки эквивалентности. Титриметрический метод анализа основан на
измерении объема реагента точно известной концентрации, затраченного на реакцию
взаимодействия с определяемым веществом.
Точка эквивалентности - момент титрования, когда
достигнуто эквивалентное соотношение реагирующих веществ. Достигнув точки
эквивалентности, титрование заканчивают и отмечают объем раствора, пошедший на
данную реакцию. Следовательно, в титриметрическом методе анализа первостепенное
значение имеет точное определение точки эквивалентности. Точку эквивалентности
определяют по изменению окраски индикатора (химического индикатора) или с
помощью инструментальных индикаторов, приборов фиксирующих измене какого-то
свойства среды в процессе титрования.
Индикаторы - это вещества, которые изменяют свое
строение и физические свойства при изменении среды. В области точки
эквивалентности индикатор изменяет свой цвет, образует осадок или вызывает
какой-то другой наблюдаемый эффект.
.8.2 Методы титрования
В титриметрическом методе анализа используются
различные типы химических реакций. В зависимости от характера применяемой
химической реакции различают следующие методы титриметрического анализа:
- кислотно-основное титрование;
осадительное титрование или осаждение;
- комплексонометрическое титрование или
комплексонометрия;
окислительно-восстановительное титрование или
редоксиметрия.
По применяемым реагентам титриметрические методы
анализа подразделяются на следующие виды:
- алкалиметрическое титрование (титрант - щелочь
- NaOH или Ba(OH)2);
перманганатометрическое титрование (титрант -
KМnO4);
хроматометрическое титрование (титрант -
K2Cr2O7);
йодометрическое титрование (титрант I2 или KI) и
т.д.
.8.3 Метод кислотно-основного титрования
Метод объемного анализа, заключающийся в
постепенном прибавлении раствора известной концентрации (стандартный раствор) к
анализируемому раствору.
Основан на реакции нейтрализации. Результат
титрования вычисляют по объему и концентрации рабочего раствора в точке
эквивалентности. Рабочими растворами при определении кислот служат щелочи КОН,
NaOH (алкалиметрия); при определении оснований - сильные кислоты НС1, H2S04
(ацидиметрия). В процессе титрования имеет место постепенное изменение рН раствора
с особо резким скачком вблизи точки эквивалентности. Для фиксирования точки
конца титрования используются индикаторы химические (лакмус, фенолфталеин,
тимолфталеин, метилоранж, метилрот и др.).
Важно правильно выбрать индикатор; точка
эквивалентности должна попадать в интервал перехода окраски индикатора.
Например, при титровании слабого основания сильной кислотой точка
эквивалентности достигается в кислой среде. В этом случае титрование следует
вести в присутствии метилоранжа, изменяющего свой цвет в диапазоне рН 3,0-4,4;
фенолфталеин и лакмус дадут большую индикаторную ошибку (раствор будет
перетитрован). При титровании слабой кислоты сильным основанием точка
эквивалентности достигается в щелочной среде - нужно использовать фенолфталеин.
При титровании сильной кислоты сильным основанием и наоборот точка
эквивалентности соответствует рН 7; в качестве индикатора выбирают лакмус или
фенолфталеин.
.9 Техника безопасности в химической лаборатории
За состояние охраны труда и техники безопасности
в лаборатории отвечает руководитель лаборатории. Он может назначать
ответственных за технику безопасности в целом по лаборатории, ответственных за
противопожарное состояние каждого лабораторного помещения, включая подсобные
помещения и лабораторные склады, ответственных за соблюдение техники
безопасности при выполнении отдельных видов работ, однако основная
ответственность в конечном счете лежит на нем. При этом остальные сотрудники
лаборатории также несут персональную ответственность за обеспечение
безопасности на собственном рабочем месте и на рабочих местах своих
непосредственных подчиненных.
Старшие научные сотрудники или руководители
групп осуществляют надзор за исправным состоянием оборудования, индивидуальных
защитных средств и средств пожаротушения, проводят инструктажи по отдельным
видам работ и обучение безопасным методам работы, присутствуют при выполнении
опасных работ.
Ответственными за технику безопасности в
лаборатории назначается наиболее опытный и квалифицированный химик, хорошо
знакомый с методикой и техникой всех выполняемых в лаборатории работ. В
обязанности ответственного за технику безопасности входит:
. Проведение регулярных инструктажей по
технике безопасности (с ведома и по поручению руководителя лаборатории).
. Осуществление периодических проверок
состояния приборов и оборудования, запрещение работы на неисправном
оборудовании.
. Контроль за соблюдением персоналом
лаборатории правил техники безопасности, обсуждение всех случаев
нарушения правил с ответственными за это лицами.
. Оказание консультативной помощи сотрудникам
лаборатории при выборе наиболее безопасных способов проведения тех или иных
работ, при конструировании и установке лабораторного оборудования
. Анализ совместно с руководителем
лаборатории всех происшествий, связанных с нарушениями правил техники
безопасности.
. Разработка программ обеспечения
безопасности и плана мероприятий в рамках комплексной программы охраны труда,
контроль за реализацией программ.
К работе в химических лабораториях допускаются
лица, прошедшие медицинское освидетельствование и инструктаж по технике
безопасности. Прохождение инструктажа обязательно для всех работников,
независимо от их образования, стажа работы или должности, а также для
командированных и проходящих производственное обучение или практику.
По характеру и времени проведения инструктаж
подразделяют на вводный, первичный на рабочем месте, повторный, внеплановый и
текущий. Вводный инструктаж проводится инженером по охране труда (технике
безопасности), а остальные виды инструктажа - заведующим лабораторией или
непосредственно руководителем работ. Вводный инструктаж помимо прочих вопросов
обязательно должен включать подробное рассмотрение основных опасных и вредных
производственных факторов, ознакомление с характерными причинами несчастных случаев
в лаборатории и со средствами индивидуальной защиты. Отдельно должны быть
рассмотрены общие меры по обеспечению пожарной безопасности и правила
пользования первичными средствами тушения пожаров, а также вопросы оказания
первой помощи пострадавшему.
Первичный инструктаж на рабочем месте должен
включать ознакомление с условиями работы в лаборатории, с конкретными опасными
и вредными производственными факторами, с безопасной организацией и содержанием
рабочего места. Инструктируемый должен быть ознакомлен с безопасными и наиболее
рациональными приемами и методами работы, с тем, как надо действовать при
возникновении опасной ситуации, со средствами индивидуальной защиты на данном
рабочем месте, а также с имеющимися в лаборатории средствами пожаротушения.Целью
повторного инструктажа является проверка и повышение уровня знаний правил и
инструкций по технике безопасности.
Внеплановый инструктаж проводится индивидуально
или с группой в случаях изменения инструкций, необходимости проведения нового
вида работ, незнакомых операций, перед работой с новыми веществами, а также в
случаях нарушения работниками правил техники безопасности или после несчастных
случаев.
В химических лабораториях нельзя работать при
плохом самочувствии, в болезненном состоянии, а также при сильной усталости. К
работе с химическими веществами нельзя приступать при наличии незащищенных
царапин или ссадин на руках, тем более при экземе или воспалительных процессах
кожи.
Любые работы в химической лаборатории надо
выполнять тщательно, аккуратно, без спешки. На рабочем месте должны находиться
только необходимые для выполнения конкретной работы реактивы, приборы и
оборудование. Беспорядок на рабочем месте недопустим.
К выполнению любой работы можно приступать
только тогда, когда все ее этапы понятны и не вызывают никаких сомнений. Если
возникают какие-либо неясности, следует до начала работы обратиться к
руководителю. Операции, связанные с повышенной опасностью, необходимо проводить
только под непосредственным наблюдением руководителя или опытного работника.
План работы должен быть заранее обдуман, а лучше
всего - обсужден. Если какая-либо операция не может быть выполнена в течение
рабочего дня, следует заранее решить, на какой стадии работа может быть
прервана до следующего дня.
Фиксация условий и результатов каждого опыта в
рабочем журнале должна проводиться в ходе выполнения работы или сразу же после
ее окончания. Ведение черновиков не допускается; в рабочем журнале должны
проводиться и все необходимые расчеты. При описании экспериментов особо следует
выделять все замеченные отклонения от описанного в методике хода процесса, а
также возможные источники опасности - бурное выделение газа, самопроизвольное
повышение температуры и т. п.
При воспроизведении описанных в литературе
синтезов следует по крайней мере первый опыт проводить с рекомендованными
количествами веществ и строго придерживаться условий, указанных в прописи.
Исследовательские работы, результат которых невозможно предсказать заранее,
нельзя проводить сразу с большими количествами веществ. Даже когда пробные
опыты с малыми количествами реактивов проходят гладко, при переходе к
препаративным синтезам следует соблюдать осторожность. Ведь если, например,
выделение теплоты или вспенивание массы в небольших объемах не вызывает
осложнений, то при значительных загрузках они могут послужить причиной аварии.
Емкости с реактивами должны быть снабжены
надежно наклеенными этикетками с разборчивыми надписями, где указаны название
соединения и его химическая формула Запрещается исправлять надписи на этикетках,
наклеивать новые этикетки, не удалив старых, наносить на емкости с реактивами
легко смывающиеся надписи. Запрещается пользоваться реактивами без этикеток или
с сомнительными надписями на них: в подобных случаях необходимо точно
установить формулу вещества с помощью химического анализа. Если определение
состава реактива не представляется возможным, он подлежит уничтожению.
Этикетками с указанием формулы вещества и номера опыта по рабочему журналу
должны непременно снабжаться также емкости с промежуточными продуктами в
многостадийных синтезах, если они не используются немедленно.
Необходимо внимательно следить за сохранением
чистоты реактивов. Ни в коем случае нельзя путать пробки от банок с реактивами,
доставать вещество из банки грязным шпателем и т. д. Загрязнение реактивов
может не только привести к искажению результатов работы, но и вызвать
нежелательные и опасные побочные процессы вследствие, например, каталитических
эффектов. Так, присутствие случайных примесей солей или оксидов железа, то есть
ржавчины, солей хрома, цинка и т. п. при работе с концентрированной перекисью
водорода может вызвать ее самопроизвольное бурное разложение.
Запрещается выбрасывать в раковины отходы
химических реактивов, сливать органические растворители, водные растворы химических
веществ. Отходы подобного рода следует в конце рабочего дня выносить специально
отведенные для сливов места с целью последующего централизованного их
уничтожения. Отходы органических растворителей собирают отдельно от водных
растворов и от неорганических веществ. Практика выбрасывания в раковину даже,
казалось бы, безвредных и безопасных химических веществ, во-первых, приводит к
ускоренной коррозии и выходу из строя канализационных труб; во-вторых, при
взаимодействии отходов могут образоваться ядовитые газы. Результаты
взаимодействия, как правило, труднопредсказуемы, поскольку в канализационной
сети смешиваются стоки из разных лабораторных помещений.
Химические вещества также нельзя выбрасывать
вместе с мусором на помойку.
Все сотрудники лаборатории обязаны владеть
приемами оказания первой (доврачебной) помощи при несчастных случаях - уметь
накладывать повязки для остановки кровотечения, проводить искусственное
дыхание, непрямой массаж сердца и т. д. В каждом рабочем помещении на видном
месте должна находиться полностью укомплектованная аптечка первой помощи.
Состав аптечки зависит от характера работ, выполняемых в лаборатории, и должен
быть согласован с врачом. По мере расходования и окончания срока годности
медикаментов аптечку необходимо без промедления пополнять.
Запрещается работать в условиях, при которых
невозможно оказание немедленной помощи в случае аварии: при работе в вечернее и
ночное время, независимо от характера работ, а также при выполнении операций,
связанных с какой-либо опасностью, в любое время суток, в рабочем помещении
должно находиться не менее двух человек. К числу опасных относятся любые работы
с токсичными, едкими, горючими и взрывоопасными веществами (см. приложения 2 и
3), с движущимся оборудованием, с использованием повышенного давления, вакуума,
высоких температур, сильного охлаждения, электрического тока, а также все
нестандартные операции.
Запрещается оставлять без присмотра работающие
установки, включенные электронагревательные приборы, газовые горелки. Если
необходимо ненадолго отлучиться от работающей установки, следует поручить
присмотр за ней досрочно квалифицированному сотруднику, подробно
проинструктировав его. Нельзя поручать другим лицам присмотр за установкой,
если она не вышла на рабочий режим, работает нестабильно или имеет
какие-либо отклонения от нормы
Перед уходом из лаборатории следует убедиться
что на каждом рабочем столе и в вытяжных шкафах отключены вода и электрические
приборы, перекрыты газовые линии, в смонтированных приборах закончились все
химические процессы, а из водяных холодильников слита вода. Каждый работник
лаборатории должен иметь в индивидуальном пользовании средства
индивидуальной защиты - очки или маску для защиты глаз и лица респираторы
для работы с пылящими веществами заранее подогнанный и проверенный на
герметичность противогаз, резиновые перчатки, а также спецодежду - халат,
а в некоторых случаях головной убор и прорезиненный фартук.
Раздел 2. ПРАКТИЧЕСКАЯ ЧАСТЬ
2.1 Титриметрический метод определения азота по Кьельдалю
Сущность метода заключается в разложении
органического вещества пробы кипящей концентрированной серной кислотой с
образованием солей аммония, переведении аммония в аммиак, отгонке его в раствор
кислоты, количественном учете аммиака титриметрическим методом и расчете
содержания азота в исследуемом материале.
2.2 Отбор точечных проб
Точечные пробы продуктов отбирают с
транспортеров, из-под силосов, бункеров, весов или технологического
оборудования путем пересечения падающей струи ковшом, автоматическим или
механическим пробоотборником через равные промежутки времени. Время отбора
точечных проб устанавливают в зависимости от скорости перемещения продукта, но
с таким расчетом, чтобы общая масса объединенной пробы от партии составила для
муки животного происхождения и рыбной муки не менее 2 кг; для остальных
продуктов - не менее 4 кг.
Точечные пробы рассыпных и гранулированных
продуктов с автотранспорта отбирают щупом с укороченной ручкой и широким
конусом из пяти различных мест по всей глубине насыпи, отступая 0,5 м от
бортов, и в середине.
Точечные пробы рассыпных продуктов, хранящихся в
складе, отбирают вагонным щупом при высоте насыпи до 1,5 м, а при высоте насыпи
свыше 1,5 м применяют щуп с навинчивающимися штангами.
Перед отбором проб поверхность насыпи разделяют
на 6 условно равных секций. В каждой секции точечные пробы отбирают из пяти
различных мест по схеме конверта. При высоте насыпи до 0,75 м из двух слоев: из
верхнего слоя на глубине 10-15 см от поверхности насыпи и нижнего слоя - у самого
пола. При высоте насыпи свыше 0,75 м - из трех слоев: из верхнего - на глубине
10-15 см от поверхности насыпи, среднего и нижнего - у самого пола.
Во всех случаях точечные пробы отбирают сначала
из верхнего, затем среднего, и, наконец, нижнего слоя. Точечные пробы
гранулированных продуктов отбирают ковшом или щупом с укороченной ручкой и
широким конусом на глубине не менее 30 см.
Точечные пробы рассыпных продуктов, упакованных
в тканевые мешки, отбирают мешочным щупом из верхней и нижней частей мешка.
Перед введением щупа в мешок выбранное место должно быть очищено мягкой щеткой.
Щуп вводят желобком вниз, затем поворачивают на 180° и вынимают. Отверстие в
ткани мешка затягивают при помощи щупа.
Точечные пробы рассыпных продуктов, упакованных
в бумажные мешки или тканевые мешки с полиэтиленовым вкладышем, а также
точечные пробы гранулированных продуктов отбирают из предварительно расшитых
мешков.
Из расшитых мешков точечные пробы рассыпных
продуктов отбирают щупом с укороченной ручкой и широким конусом в трех местах:
вверху, в середине и в нижней части мешка, а точечные пробы гранулированных
продуктов отбирают ковшом из верхней части расшитых мешков.
2.3 Составление объединённой пробы
Для составления объединенной пробы отобранные
точечные пробы продукта помещают в чистую тару и перемешивают. В тару
вкладывают этикетку с указанием наименования продукта, рецепта, массы партии, а
для упакованного продукта - количества мешков в партии, даты и места отбора
точечных проб, наименования предприятия-изготовителя и номера транспортного
документа.
.4 Выделение средней пробы
Среднюю пробу рассыпного и гранулированного
продукта выделяют из объединенной пробы с помощью делителя ДЗК-1 или вручную
путем квартования. Для выделения средней пробы объединенную пробу высыпают
вручную на деревянный поднос или поднос из органического стекла с гладкой
поверхностью и разравнивают в виде квадрата двумя деревянными планками со
скошенными ребрами. Затем одновременно с двух противоположных сторон продукт
подгребают к середине таким образом, чтобы получился валик. После этого продукт
захватывают с концов валика и также подгребают к середине. Перемешивание
повторяют три раза, после чего объединенную пробу разравнивают тонким слоем и
планкой делят по диагонали на четыре треугольника. Продукт, находящийся в двух
противоположных треугольниках, удаляют, а в двух оставшихся - соединяют вместе
и перемешивают. Деление продукта продолжают до тех пор, пока масса оставшейся
части (средняя проба) составит: для муки животного происхождения и рыбной муки
не менее 1 кг, для остальных продуктов - не менее 2 кг.
Среднюю пробу продукта делят по п.4.1 на две
равные части. Одну из них используют для анализа, а другую помещают в чистую
сухую банку с плотно закрывающейся крышкой. Банку опечатывают или пломбируют и
хранят не менее одного месяца на случай разногласий в оценке качества
контрольных испытаний.
К банке со средней пробой продукта прикрепляют
этикетку, на которой должны быть обозначены: наименование продукта, рецепт,
наименование предприятия-изготовителя, номер транспортного документа, масса
партии, дата отбора пробы и подпись лица, отбиравшего пробу.
В лаборатории среднюю пробу регистрируют в
специальном журнале и нумеруют. Присвоенный номер проставляют на всех
документах, относящихся к данной партии продукта.
.5 Аппаратура, материалы и реактивы
Весы лабораторные с пределом допускаемой
абсолютной погрешности взвешивания не более ± 0,01 г. по ГОСТ OIML.R 76-1-2011
или по нормативным документам, действующим на территории государства, принявшего
стандарт.
Электроплитка бытовая по ГОСТ 14919-83 или
газовые горелки.
Холодильник шариковый по ГОСТ 25336-82.
Воронка капельная по ГОСТ 25336-82.
Бюретка по ГОСТ 29251-91, вместимостью 50 см3.
Каплеуловитель по ГОСТ 25336-82.
Колбы для сжигания по ГОСТ 25336-82,
вместимостью 100 см3.
Колбы плоскодонные и круглодонные по ГОСТ
25336-82, вместимостью 500-700 см3.
Колбы плоскодонные по ГОСТ 25336-82,
вместимостью 250-300см3.
Капельница по ГОСТ 25336-82.
Вода дистиллированная по ГОСТ 6709-72.
Кислота серная по ГОСТ 4204-77,
концентрированная и раствор 0,05 моль/дм3(0,1н).
Медь сернокислая 5-водная по ГОСТ 4165-78.
Калий сернокислый по ГОСТ 4165-74.
Индикатор смешанный (Таширо).
2.6 Проведение анализа
Навеску муки массой 0,2-0,3 г. взвешивают с
абсолютной погрешностью не более 0,0005 г в закрытую с одной стороны трубочку
из фильтровальной бумаги или из станиоля, помещают в колбу для сжигания
вместимостью 100 см3, добавляют несколько мелких кристаллов медного купороса
(0,2-0,3 г.) и приливают 10-20 см3 серной кислоты, плотностью 1840 кг/м3.
Колбу с содержимым осторожно нагревают в
вытяжном шкафу, не допуская разбрызгивания жидкости. Когда содержимое колбы
станет однородным, прекращают нагревание, дают остыть, добавляют 0,5 г.
сернокислого калия и продолжают нагревание до тех пор, пока жидкость в колбе не
станет прозрачной, зеленовато-голубой окраски без бурого оттенка. Внутренние
стенки колбы должны быть совершенно чистыми. Это достигается осторожным взбалтыванием
содержимого колбы для смывания со стенок темных, обугленных частиц муки.
По окончанию сжигания содержимое колбы охлаждают
и количественно переносят в отгонную колбу, вместимостью 500-750 см3.
Колбу для сжигания тщательно ополаскивают,
проверяя полноту смывания добавлением 1-2 капель раствора метилового красного.
Общий объем раствора в отгонной колбе должен
быть равен не более 250-300 см3.
Приемником служит коническая колба вместимостью
250-300см3, в которую из бюретки налито 25-30 см3 раствора серной кислоты 0,05
моль/дм3. Конец трубки холодильника должен быть погружен в раствор серной
кислоты.
В отгонную колбу осторожно, по стенкам, избегая
смешивание жидкостей, приливают 50-70 см3 раствора гидроксида натрия 330 г/дм3,
бросают кусочек лакмусовой бумаги и быстро закрывают ее пробкой, соединенной
посредством каплеуловителя с холодильником, осторожно перемешивают содержимое и
нагревают. Реакция жидкости в колбе должна быть резко щелочной.
После закипания жидкости в колбе преемник
опускают так, чтобы конец трубки холодильника находился на некотором расстоянии
от поверхности раствора и продолжают отгонку до тех пор, пока не отгонится не
менее 2/3 жидкости.
Конец отгонки определяют по лакмусовой бумаге.
Если отгонка закончена, капля дистиллята не должна вызывать посинения красной
лакмусовой бумаги. При появлении в конце отгонки при кипении толчков отгонку
прекращают.
По окончанию отгонки конец трубки холодильники
обмывают водой в приемную колбу и содержащийся в ней избыток серной кислоты
оттитровывают раствором гидроксида натрия 0,1 моль/дм3 в присутствии метилового
красного или смешанного индикатора.
Одновременно проводят контрольный анализ без
навески исследуемого образца.
2.7 Обработка результатов
Массовую долю белковых веществ (Х37) в процентах
вычисляют по формуле:
Х37= 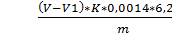 ,
(1) ,
(1)
где- объем раствора гидроксида натрия
0,1моль/дм3, израсходованный на титрование серной кислоты в контрольном
анализе, см3;-объем раствора гидроксида натрия 0,1моль/дм3, израсходованный на
титрование избытка серной кислоты в рабочем анализе, см3;- коэффициент
пересчета на точный раствор гидроксида натрия 0,1моль/дм3, г;
,0014 - количество азота, эквивалентное 1 см3
раствора гидроксида натрия 0,1моль/дм3, г;
,25 - коэффициент пересчета количества азота на
белковые вещества;- навеска муки, г.
За окончательный результат принимают
среднеарифметическое значение результатов трёх параллельных определений,
допускаемые расхождения между которыми не должны превышать 0,5% для кормовой
муки и 0,2% для остальной продукции.
Вычисления проводят до второго десятичного
знака.Все расчеты выполнялись с помощью ПК в программе MicrosoftExsel.
Таблица 4.
|
Масса
навески, г
|
1,00
|
1,00
|
1,00
|
|
V
(NaOH), мл
|
65,50
|
65,50
|
65,48
|
Х37= 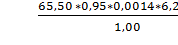 =
54, 45% =
54, 45%
Х37= 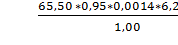 =
54, 45% =
54, 45%
Х37= 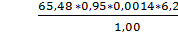 =
54, 43% =
54, 43%
Х37(ср) = 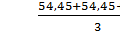 =
54, 44% =
54, 44%
ЗАКЛЮЧЕНИЕ
1. Некоторые аспекты происхождения и контроля
качества рыбной муки
На современном рынке помимо рыбной муки
представлен целый ряд товаров на ее основе. В большинстве случаев это смеси
рыбной муки с животными и/или растительными компонентами, с добавлением
синтетических аминокислот, витаминов, микроэлементов. Состав такой смеси
искусственно приближен к натуральной рыбной муке и проходит под названием
«аналог рыбной муки». Реже встречаются так называемые «протеиновые (белковые)
концентраты на основе рыбной муки» и «комбинированные продукты на основе рыбной
муки», в состав которых входит около 50% рыбной муки и смесь растительных и
животных белков. В отличие от аналогов рыбной муки здесь обычно не применяют
добавок аминокислот или микроэлементов, так как не стремятся повторить
компонентную формулу натуральной рыбной муки.
Рассмотрим основных производителей и экспортеров
рыбной муки. Самым крупным экспортером в мире является Перу - это мука,
произведенная из рыбы, которая называется анчоус. При производстве используется
два способа сушки: паровой или огневой. При паровой сушке не происходит
пережигание протеина, что характерно для огневой сушки, но энергозатраты
намного выше, что сказывается и на цене рыбной муки. Огневая мука имеет черный
цвет и сильно отличается от привычного коричневого (при паровой сушке). Доля
импорта в РФ рыбной муки огневой сушки составляет порядка 80%. Анчоус сама по
себе рыба жирная и, соответственно, в рыбной муке большая доля рыбьего жира,
так как на транспортировку и перевалку уходит до двух месяцев. Чтобы мука не
испортилась, в ней содержится большое количество антиоксиданта, обычно это
ионол или агидол.
Лаборатории тщательно контролируют все
закупаемое сырье, независимо от страны производителя. Одним из важнейших видов
сырья является рыбная мука как главный источник высокоперевариваемого и
полноценного протеина, а также лизина в комбикорме.
Аналоги рыбной муки, протеиновые (белковые)
концентраты на основе рыбной муки и комбинированные продукты на основе рыбной
муки - это самостоятельные продукты, которые имеют полное право на
существование, не являются фальсификацией рыбной муки и имеют свою нишу на
рынке - они значительно дешевле натуральной рыбной муки. Однако все чаще
встречаются случаи, когда, пользуясь несовершенством существующих ГОСТ и других
нормативных документов, данные товары пытаются продать под маркой и по цене
натуральной рыбной муки.
Специалистами были рассмотрены причины появления
на рынке фальсифицированной рыбной муки, а так же схема комплексного
исследования протеина рыбной муки с целью выявления фальсификации. В схему
предложено включить следующие исследования: сырой протеин, перевариваемый
протеин, карбамид (мочевина), протеин по Барштейну, содержание четырех основных
аминокислот (лизин, метионин, цистин, триптофан). Однако основное внимание было
уделено качеству протеина в рыбной муке, контролю его перевариваемости,
натуральности и полноценности. Этот показатель, действительно, очень важен для
потребителя, но не только он определяет доброкачественность и натуральность
рыбной муки.
. Виды добавок, обнаруженные при фальсификациях
рыбной муки
Мочевина (карбамид) и/или другие неорганические
источники азота (селитра, аммонийные соли).Добавление 1% мочевины «увеличивает»
содержание сырого протеина на 3,06%. Но по ГОСТ 2116-82 в рыбной муке
допускается содержание мочевины до 0,3%. Для других источников неорганического
азота можно также рассчитать «вклад» в сырой протеин, исходя из процента ввода
в рыбную муку и содержания азота в самом соединении (соли).
Мука животного происхождения (морские
млекопитающие, наземные животные, мука из шерсти), свиные шкварки. Содержание и
питательные свойства «сырого протеина» в данных продуктах ниже, чем в
натуральной рыбной муке, но они в два раза дешевле.
Перьевая мука. В основном используют как дешевый
источник сырого протеина, так как перьевая мука может содержать его до 80%.
Степень усвоения такой муки значительно ниже, чем у рыбной, и зависит от
степени гидролиза пера.
Мука из ракообразных (креветки, крабы), мидий,
прочих морских организмов. Содержит азот в недоступной форме (хитин панциря
ракообразных, раковины моллюсков).
Соевый шрот. Обычно используют как наполнитель в
комбинациях с перьевой мукой.
Отруби. Добавляют в незначительных количествах в
составе витаминных и минеральных премиксов при балансировании состава смеси.
Карбонат кальция. При добавлении мясной муки
снижается содержание кальция в смеси, которое восполняют минеральным кальцием.
Часто встречающиеся комбинации на основе рыбной
муки: рыбная и перьевая мука, соевый шрот, отруби, минеральный источник
кальция; рыбная и перьевая мука, мука из криля и креветок, мясная мука
(свиная), минеральный источник кальция; рыбная и перьевая мука, мясная мука
(свиная), свиные шкварки, минеральный источник кальция; рыбная мука с низким
содержанием протеина (из костей, плавников, голов), карбамид и/или соли
аммония, селитра.
. Ценность протеина в кормах
Общеизвестно, что под протеином понимают все
азотосодержащие соединения, входящие в состав корма, - белки и небелковые
азотистые вещества: амины, аминокислоты, пурины, пиримидины, алкалоиды и т.д. В
связи с неоднородностью протеина нет единого метода определения его
биологической ценности, поэтому необходимо проводить комплексные исследования,
то есть анализировать корма на содержание сырого и перевариваемого протеина,
истинного белка (белка по Барнштейну), небелкового азота, растворимой фракции
белка, аминокислот. Такой подход дает возможность наиболее эффективно оценить
биологическую ценность корма.
Разносторонние исследования протеина кормов
позволяют создать схему для выявления, например, недоброкачественной и
фальсифицированной рыбной муки. Этот корм животного происхождения является
одним из наиболее богатых протеином и полноценных по аминокислотному составу,
имеет высокий коэффициент перевариваемости. С вводом рыбной муки улучшается
качество протеина в рационах сельскохозяйственных животных и птицы.
Для получения рыбной муки с высокими
показателями питательности необходимо использовать качественное сырье и точно
соблюдать технологию ее приготовления. Это требует больших затрат, поэтому
рыбная мука на сегодняшний день является наиболее дорогим сырьем на рынке
кормов. Снижение содержания протеина в рыбной муке даже на 2 - 3% уменьшает ее
стоимость. В связи с этим у продавцов рыбной муки появляется соблазн повысить
уровень протеина за счет ввода неорганических азотосодержащих соединений
(карбамида, аммонийных солей и т.д.). Подобного рода замена недопустима в
рационах птиц и свиней, так как может вызвать симптомы аммиачного отравления.
Использование для производства рыбной муки недоброкачественного
сырья (трудноперевариваемых частей рыбы - костей, голов, плавников) также
приводит к снижению биологической ценности протеина, что связано с низкой его
перевариваемостью.
Список использованных источников
Законы и законодательные акты
1.
ГОСТ 13496.0-80 Комбикорма, сырье. Методы отбора проб.
.
ГОСТ 13496.4-93. Корма, комбикорма, комбикормовое сырье. Методы определения
содержания азота и сырого протеина.
Печатная литература
3. Лурье.Ю.Ю. Справочник по аналитической химии:
Справ.изд. - 6-е изд., перераб. и доп. - М.: 1989 - 448 с.: ил.
.Технология производства кормов/Авт.-сост. Т38
С.Н. Александров. - М.: ООО «Издательство ACT»; Донецк: «Сталкер», 2003. - 235,
[5] с: ил. - (Приусадебное хозяйство).
. Васильев В.П. Аналитическая химия. В 2 ч.
Часть I. Гравиметрический и титриметрический методы анализа - М.: Высш. школа,
1989 - 320 с.
. Руководство по эксплуатации автоматической
установки для перегонки с водяным паром«VAPODEST-20».
. Захаров Л. Н.Техника безопасности в химических
лабораториях: Справ, изд.-2ое изд., перераб. и доп.- Л.; ‘ Химия, 1991.-336 с.:
ил.
. Сборник Национальных стандартов. «Рыба и
рыбные продукты». Методы анализов. Маркировка. Упаковка. ИПК. Издательство
Стандартов. 2004 Москва.
Похожие работы на - Определение содержания белка в пищевой продукции
|