|
Продукт
|
Год
|
|
1970
|
1975
|
1980
|
1987
|
|
Ацетилен
|
228
|
294
|
311
|
-
|
|
Метанол
|
1004
|
1477
|
1900
|
3333
|
|
Пропилен
|
302
|
580
|
824
|
-
|
|
Уксусная кислота
|
146
|
190
|
239
|
-
|
|
Фенол
|
347
|
413
|
496
|
521
|
|
Этилен
|
799
|
1366
|
1773
|
2971
|
|
Этанол синтетический (миллионов
декалитров)
|
90
|
92,4
|
-
|
Одновременно с увеличением общего объема
продукции промышленность основного органического синтеза, начиная с 1960 года,
по темпам роста начинает значительно опережать химическую и нефтехимическую
промышленность в целом. [14]
. Основные тенденции развития
промышленного органического синтеза
Основные тенденции развития промышленности ООС,
направленного на повышение экономической эффективности производства и качества
продукции, связаны с экономией сырья, энергии и снижением капитальных затрат.
Важнейшими из них являются следующие:
. Создание новых технологических
процессов, базирующихся на более доступном и дешевом сырье. Например, переход
от дорогого ацетилена к ароматическим углеводородам, алкенам, алканам и,
наконец, синтез-газу в соответствии со шкалой их ценности:
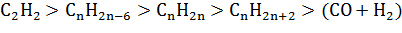
. Переход к прямым методам синтеза,
исключающим потребление неорганических реагентов. Например, замена сернокислотной
гидратации этилена прямой каталитической в производстве этанола.
. Повышение селективности процессов за
счет оптимизации параметров, выбора аппаратуры и подбора высокоселективных
катализаторов.
. Сокращение числа стадий производства.
Например, замена двухстадийного процесса синтеза ацетальдегида из этилена через
этанол одностадийным окислительным процессом:
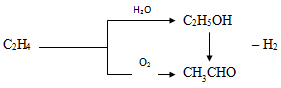
5. Увеличение единичной мощности аппаратов
и снижение за счет этого капитальных затрат. Например, в производстве метанола
до 300-500 тыс. т/год.
. Экономия энергии и повышение
коэффициента полезного действия агрегатов, в частности за счет использования
вторичных энергоресурсов и внедрения энерготехнологических схем. [14]
2.1 Синтез-газ как альтернатива
нефти
После 1945 года в связи с бурным развитием
нефтедобычи и падением цен на нефть отпала необходимость синтеза органических
веществ из СО и Н2. Наступил нефтехимический бум. Однако в 1973 году
разразился нефтяной кризис - нефтедобывающие страны ОПЕК (организация стран -
экспортеров нефти - Organization of Petroleum Exporting Countries) резко
повысили цены на сырую нефть, и мировое сообщество вынуждено было осознать
реальную угрозу истощения в обозримые сроки дешевых и доступных нефтяных
ресурсов. Энергетический шок 70-х годов возродил интерес ученых и
промышленников к использованию альтернативного нефти сырья, и здесь первое
место, бесспорно, принадлежит углю. Мировые запасы угля огромны, они, по
различным оценкам, более чем в 50 раз превосходят нефтяные ресурсы, и их может
хватить на сотни лет. Нет никаких сомнений, что в обозримом будущем
использование синтез-газа будет играть ключевую роль для целей органического
синтеза. В настоящее время в промышленном масштабе по методу Фишера-Тропша
получают бензин, газойль и парафины только в Южной Африке. На установках фирмы
"Sasol" производят около 5 млн т в год жидких углеводородов. [8]
Отражением интенсификации исследований по
синтезам на основе СО и Н2 является резкое возрастание публикаций,
посвященных химии одноуглеродных молекул (так называемая С1-химия).
С 1984 года начал издаваться международный журнал "C1-Molecule
Chemistry". Таким образом, мы являемся свидетелями наступающего ренессанса
в истории углехимии [10]. Рассмотрим некоторые пути превращения синтез-газа,
приводящие к получению как углеводородов, так и некоторых ценных
кислородсодержащих соединений. Важнейшая роль в превращениях СО принадлежит
гетерогенному и гомогенному катализу [9].
Получение синтез-газа
Первым способом получения синтез-газа была
газификация каменного угля, которая была осуществлена еще в 30-е годы XIX века
в Англии с целью получения горючих газов: водорода, метана, монооксида
углерода. Этот процесс широко использовался во многих странах до середины 50-х
годов XX века, а затем был вытеснен методами, основанными на использовании
природного газа и нефти. Однако в связи с сокращением нефтяных ресурсов
значение процесса газификации снова стало возрастать.
В настоящее время существуют три основных
промышленных метода получения синтез-газа.
. Газификация угля. Процесс основан на
взаимодействии угля с водяным паром:
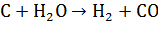
Эта реакция является эндотермической, равновесие
сдвигается вправо при температурах 900-1000℃.
Разработаны технологические процессы, использующие парокислородное дутье, при
котором наряду с упомянутой реакцией протекает экзотермическая реакция сгорания
угля, обеспечивающая нужный тепловой баланс:
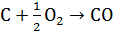
2. Конверсия метана. Реакция взаимодействия
метана с водяным паром проводится в присутствии никелевых катализаторов (Ni-Al2O3)
при повышенных температурах (800-900℃)
и давлении:
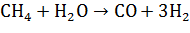
В качестве сырья вместо метана может быть
использовано любое углеводородное сырье.
. Парциальное окисление углеводородов.
Процесс заключается в неполном термическом окислении углеводородов при
температурах выше 1300℃:

Способ применим к любому углеводородному сырью,
но наиболее часто в промышленности используют высококипящую фракцию нефти -
мазут.
Соотношение СО : Н2 существенно
зависит от применяемого способа получения синтез-газа. При газификации угля и
парциальном окислении это соотношение близко к 1 : 1, тогда как при конверсии
метана соотношение СО : Н2 составляет 1 : 3. В настоящее время разрабатываются
проекты подземной газификации, то есть газификации угля непосредственно в
пласте. Интересно, что эта идея была высказана Д.И. Менделеевым более 100 лет
назад. В перспективе синтез-газ будут получать газификацией не только угля, но
и других источников углерода вплоть до городских и сельскохозяйственных
отходов. [8]
Синтез на основе монооксида углерода
Многочисленные синтезы на базе монооксида
углерода и водорода представляют громадный как практический, так и
теоретический интерес, так как позволяют из двух простейших веществ получать ценнейшие
органические соединения. И здесь определяющую роль играет катализ переходными
металлами, которые способны активировать инертные молекулы СО и Н2.
Активация молекул - это перевод их в более реакционноспособное состояние. Особо
следует отметить, что в превращениях синтез-газа широкое развитие получил новый
тип катализа - катализ комплексами переходных металлов или металлокомплексный
катализ. [10]
Катализ
Отметим несколько важных ключевых реакций в
металлокомплексном катализе. Это прежде всего реакции окислительного
присоединения и восстановительного элиминирования. Окислительное присоединение
- это реакции присоединения нейтральных молекул А-В, например H2 или
галогена, к металлическому центру комплекса. При этом металл окисляется, что
сопровождается повышением его координационного числа. Такое присоединение
сопровождается расщеплением связи А-В.
Очень важна реакция окислительного присоединения
молекулы водорода, в результате которой происходит её активация. Широкую
известность получила открытая Васко и Дилюцио реакция окислительного
присоединения водорода к плоскоквадратному комплексу одновалентного иридия. В
результате степень окисления иридия возрастает от I до III.
Реакция, обратная окислительному присоединению,
называется восстановительным элиминированием, при этом степень окисления и
координационное число металла уменьшаются на два.
Отметим также реакцию миграционного внедрения,
которая заключается во внедрении ненасыщенных соединений по связи
металл-углерод и металл-водород. Реакция внедрения СО является ключевой для
многих процессов с участием синтез-газа.
Внедрение олефина - важнейшая реакция среди
каталитических превращений олефинов: гидрирования, гидроформилирования и др.
[9]
Синтез фишера-тропша
Синтез Фишера-Тропша может рассматриваться как реакция
восстановительной олигомеризации монооксида углерода, при которой образуются
углерод-углеродные связи, и в общем виде она представляет собой сложную
комбинацию ряда гетерогенных реакций, которую можно представить суммарными
уравнениями:

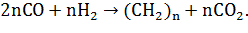
Продуктами реакции являются алканы, алкены и
кислородсодержащие соединения, то есть образуется сложная смесь продуктов,
характерная для реакции полимеризации. Первичными продуктами синтеза Фишера-Тропша
являются a- и b-олефины, которые превращаются в алканы в результате
последующего гидрирования. Природа применяемого катализатора, температура,
соотношение СО и Н2 существенно сказываются на распределении
продуктов. Так, при использовании железных катализаторов велика доля олефинов,
тогда как в случае кобальтовых катализаторов, обладающих гидрирующей
активностью, преимущественно образуются насыщенные углеводороды.
В настоящее время в качестве катализаторов
синтеза Фишера-Тропша в зависимости от поставленных задач (повышение выхода
бензиновой фракции, увеличение выхода низших олефинов и др.) используются как
высокодисперсные железные катализаторы, нанесенные на оксиды алюминия, кремния
и магния, так и биметаллические катализаторы: железо-марганцевые,
железо-молибденовые и др.
Гидроформилирование олефинов
Одним из наиболее важных примеров промышленных
процессов с участием синтез-газа является реакция гидроформилирования
(оксо-синтез). В 1938 году Релен, исследуя механизм синтеза Фишера-Тропша,
открыл эту замечательную реакцию, значение которой трудно переоценить. В этом
процессе алкены в присутствии катализаторов, главным образом кобальтовых или
родиевых, при давлениях свыше 100 атм и температурах 140-180℃
взаимодействуют с синтез-газом и превращаются в альдегиды - важнейшие
полупродукты в производстве спиртов, карбоновых кислот, аминов, многоатомных
спиртов и др. В результате реакции гидроформилирования получаются альдегиды с
прямой и разветвленной цепью, содержащие на один атом углерода больше, чем в
исходной молекуле:
Наиболее ценными являются нормальные альдегиды,
тогда как альдегиды изо-строения можно рассматривать как нежелательные побочные
продукты. Мировое производство альдегидов по процессу гидроформилирования
достигает 7 млн т в год, при этом около половины приходится на н-масляный
альдегид, из которого получают н-бутиловый спирт. Альдольной конденсацией с
последующим гидрированием получают 2-этилгексанол, используемый для
производства пластификаторов поливинилхлорида.
В качестве катализаторов гидроформилирования
наиболее широко используются карбонилы кобальта, в последнее время описано
применение родиевых катализаторов, которые позволяют проводить процесс в более
мягких условиях. [9]
Перспективы
Огромное значение имеет освоенный в 20-е годы процесс
получения из синтез-газа метанола - важнейшего продукта химической
промышленности. В то же время прямой синтез других кислородсодержащих
соединений из синтез-газа также представляется весьма привлекательным. Описано
применение синтез-газа для получения спиртов состава С1-С4
(низших спиртов), из которых затем дегидратацией получают низшие олефины. В
70-е годы были предложены катализаторы сложного состава, состоящие из оксидов
меди, кобальта, хрома, ванадия, марганца и солей щелочных металлов, которые позволили
получить из синтез-газа спирты нормального строения состава С1-С4
при температуре 250℃ и давлении всего 6
атм.
В литературе описано образование из синтез-газа
самых различных кислородсодержащих соединений, например: ацетальдегида,
уксусной кислоты, этиленгликоля и др.
Все эти реакции представляются вполне реальными.
К сожалению, эти способы в настоящее время не могут конкурировать с уже
освоенными промышленными процессами, поскольку протекают в очень жестких
условиях и с небольшой селективностью. Можно надеяться, что поиски новых
эффективных методов промышленного использования синтез-газа будут интенсивно
продолжаться, и нет сомнения, что у этой области большое будущее. [8]
2.2 Получение этанола прямой
каталитической гидратацией этилена
Этанол принадлежит к числу многотоннажных и
широко применяемых продуктов органического синтеза. Он является хорошим, хотя и
огнеопасным растворителем; в больших количествах используется в пищевой и
медицинской промышленности. Служит горючим в жидкостных ракетных двигателях,
антифризом и т. д. Как промежуточный продукт органического синтеза этанол имеет
важное значение для получения сложных эфиров: хлороформа, хлораля, диэтилового
эфира, ацетальдегида и уксусной кислоты.
В России процесс производства синтетического этанола
посредством гидратации этилена осуществляется двумя способами: сернокислотной и
прямой гидратацией. Первый способ внедрен в промышленном масштабе с 1952 г.,
второй получил широкое распространение в последние десятилетия. [15]
Прямая гидратация этилена - более совершенный
процесс, при котором происходит непосредственное присоединение воды к этилену в
присутствии катализатора. Он является более прогрессивным, что послужило
поводом считать сернокислотный метод устаревшим и не имеющим перспективного развития.
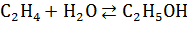
Синтез этилового спирта удалось осуществить лишь
после того, как были изысканы достаточно активные катализаторы процесса. При
газофазной гидратации в качестве катализаторов применяются фосфорная кислота
или окись вольфрама на носителях. На последнем катализаторе процесс проводят и
в жидкой фазе.
Газофазная реакция прямой гидратации олефинов
обратима и идёт с выделением тепла. Тепловой эффект зависит от строения
исходных олефинов и их молекулярного веса:

Поскольку реакция идёт с выделением тепла и
уменьшением объёма, ей благоприятствуют пониженные температуры и повышенные
давления. Константа равновесия реакции равна:
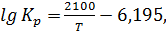
где Т - температура, К.
Практический выбор условий связан со скоростью
реакции и, следовательно, с активностью катализатора. Реакцию удаётся
реализовать при температурах от 200 до 300 ℃,
но эти условия термодинамически неблагоприятны для этилена. Поэтому на
промышленных катализаторах степень конверсии олефинов в спирт низка.
Исходные вещества и образующийся этиловый спирт
находятся при этой температуре в газообразном состоянии - это
гетерогенно-каталитическая реакция. Фосфорная кислота постепенно улетучивается,
падает активность катализатора, что вызывает коррозию реактора. Нейтрализация
газопаровой смеси по выходе из реактора приводит к значительной потере тепла и
неполностью устраняет коррозию аппаратуры, особенно в случаях резких отклонений
от режима с конденсацией воды на катализаторе. Ведутся поиски катализаторов, не
обладающих этими недостаткоми. К ним относится оксид вольфрама, нелетучий в
условиях синтеза этилового спирта.
Эти недостатки могут быть устранены при
использовании нейтральных катализаторов - вольфрамовых и кремний-вольфрамовых.
Эти процессы разработаны в жидкой фазе при 250 - 300 ℃
и 300 кг*с/см2 и при 300 ℃
и 140 кг*с/см2. В этих случаях процесс ведут в колонне высокого
давления, где на тарелках помещён катализатор - окислы вольфрама на силикагеле.
Этилен и воду подают в верхнюю часть колонны, а снизу отводят 20% спирт. При
этом процессе не требуется расходовать большое количество тепла на испарение
воды и перегрев водяного пара.
Вольфрамовые катализаторы помимо уже указанных
преимуществ более активны, чем фосфорнокислотные и могут работать в более
мягких условиях. Однако они значительно дороже, ибо вольфрам дефицитный
материал. [13]
При прямой гидратации серная кислота не
применяется, благодаря этому отпадает сложная система кислотного хозяйства,
уменьшается коррозия аппаратуры и трубопроводов. [17]
Недостатками прямой гидратации являются частая
замена катализатора и использование более дорогих концентрированных фракций
олефинов. По этим причинам в промышленности сосуществуют оба метода, причем в
США для гидратации олефинов преобладает сернокислотный метод. В России этанол
получают прямой гидратацией, а изопропиловый спирт - сернокислотным способом.
[16]
Дальнейшее усовершенствование этого метода
связано с подбором наиболее активных катализаторов и изысканием путей
осуществления жидкофазного процесса гидратации; при этих условиях можно будет
снизить температуру процесса и увеличить конверсию этилена. [17]
По масштабам производства ацетальдегид, наряду с
формальдегидом, стоит на первом месте среди альдегидов, что обусловлено его
большой ценностью в качестве промежуточного продукта органического синтеза.
Окислением ацетальдегида получают уксусную кислоту, уксусный ангидрид,
надуксусную кислоту. Реакцией с синильной кислотой и последующими превращениями
циангидрина получают молочную кислоту, акрилонитрил и эфиры акриловой кислоты.
Другие методы переработки ацетальдегида состоят в процессах типа альдольной
конденсации (получение пентаэритрита, бутандиола-1,3, кротонового альдегида и
др.).
Ацетальдегид в промышленности получают:
· жидкофазной гидратацией ацетилена в
присутствии ртутьсодержащих и парофазной гидратацией в присутствии
кадмийкальцийфосфатных катализаторов;
· каталитическим окислительным
дегидрированием этанола;
· окислением легких насыщенных С3
- С4 углеводородов;
· прямым каталитическим окислением
этилена. [20]
Из всех методов получения ацетальдегида наиболее
перспективным является процесс прямого окисления этилена в присутствии хлорида
палладия [19]. Он получил наибольшее распространение.
Реакция окисления этилена в ацетальдегид
сопровождается выделением значительного количества тепла [20]:
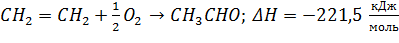
Условия проведения синтеза:
· температура: 100 - 130 ℃,
· давление: 0,3 - 1,0 МПа,
· катализаторы: PlCl2,
CuCl2.
[21]
Процесс получения ацетальдегида окислением
этилена может осуществляться на твёрдом катализаторе
(гетерогенно-каталитический процесс). Однако это сопряжено с трудностями,
связанными с отводом значительного количества тепла. Применение жидкого
катализатора (гомогенно-каталитический процесс) позволяет проще решать проблему
отвода тепла - путем испарения части воды, содержащейся в катализаторном
растворе. Непрерывный процесс получения ацетальдегида состоит из двух стадий:
. Карбонилирование
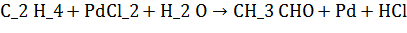
Установлено, что промежуточным соединением при
введении этилена в водный раствор хлорида палладия является комплекс этилен -
палладийхлорид.

который при взаимодействии с водой очень быстро
разрушается с образованием ацетальдегида и металлического палладия:

. Окисление
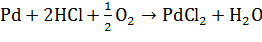
Скорость реакции окисления значительно ниже, чем
реакции карбонилирования, поэтому активность катализатора быстро падает.
Для повышения скорости окисления палладия применяются
водные растворы хлоридов меди и железа, играющие роль переносчиков кислорода:
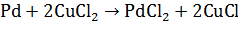
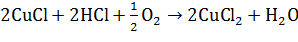
В качестве побочных продуктов при окислении
этилена в ацетальдегид образуются уксусная кислота, муравьиная кислота,
хлорсодержащие соединения (метилхлорид, этилхлорид, ацетальдегидхлорид),
продукты конденсации (кротоновый альдегид), диоксид углерода. [20]
В промышленности существует 2 варианта процесса
окисления С2Н4 в ацетальдегид:
. Окисление осуществляется катализаторным
раствором в одном реакторе, а в другом реакторе проводят реакцию регенерации
катализаторного раствора воздухом. Таким образом, в этом варианте узел
окисления этилена отделен от реактора, в котором используется О2 воздуха
для регенерации катализатора. Это делает процесс более взрывобезопасным,
используется дешевый окислитель-воздух.
. Окисление С2Н4 и
регенерация катализаторного раствора протекают в одном и том реакторе. При этом
процессе используется избыток этилена, чтобы избежать образования взрывоопасных
смесей. В данном процессе мы вынуждены держать рецикл С2Н4,
отсюда в качестве окислителя применяется технический О2 и необходимо
держать полную конверсию О2.
Преимущества процесса: дает экономию в
капитальных вложениях и в расходе энергии.
Недостатки: большая взрывоопасность, более
дорогой окислитель.
.4 Создание органических молекул с заданными
структурными характеристиками
Создание новых типов органических молекул с
заданными структурными характеристиками, получившее название "молекулярный
дизайн", приобретает всё большее и большее значение. О впечатляющих
успехах в данной области говорит синтез органических молекул в виде правильных
многогранников (призман, кубан, тетраэдран, додекаэдран), необычных
молекулярных конструкций типа катенанов, ротоксанов, узлов. Имеются сообщения о
создании молекулярных структур, обладающих формой листа Мёбиуса. Получение
молекулярных структур различных типов, с одной стороны, обогащает теоретическую
органическую химию новыми идеями, с другой стороны, может иметь практический
выход, например, в решении задач по синтезу биологически активных препаратов,
органических катализаторов, материалов для регистрации информации и т.д.
Выделяют два направления, сложившиеся в этой
области:
· "структурно-ориентированным
дизайн"
· "функционально-ориентированным
дизайн".
К структурно-ориентировавнному дизайну относятся
работы по созданию молекул с необычными структурными характеристиками, причем
не обязательно в связи с какими-то полезными свойствами получающихся новых
веществ. Такое направление немедленно ассоциируется с множеством классических
исследований, таких, как синтезы цик- лоокгатетраена, бензола Дьюара или
астерана, новые синтезы додекаэдрана и производных теграэдрана. Цель
исследований в этой области состоит в том, чтобы придумать и затем
синтезировать некоторые нетривиальные молекулы, имеющие определенные уникальные
особенности. Очень часто уникальность целевых структур состоит в общей форме
молекул (таких, как додекаэдран или катенаны), которые во всех остальных
отношениях построены в соответствии с классическими концепциями структурной
теории. В то же время целый ряд беспрецедентных по структуре соединений
появился недавно в результате исследований, направленных на выяснение пределов
применимости классического описания структуры молекул органических соединений.
Нельзя, однако, упускать из виду того, что работы в области
структурно-ориентированного дизайна в действительности проводятся вблизи
границы, которая в органической химии отделяет известное от неизвестного. Таким
образом, их непосредственным результатом является существенное расширение
многообразия объектов, изучаемых этой наукой. Еще более важно, что
проникновение в эту область новых соединений и новых структурных типов
оказывается исключительно плодотворным, приносящим множество неожиданных
открытий с важными последствиями как для академической, так и прикладной науки.
Функционально-ориентированный дизайн решает
задачу синтеза соединений, которые должны обладать набором четко определенных,
заранее заданных свойств. Здесь конечная цель состоит в оптимизации структуры
целевого соединения с тем, чтобы добиться максимальной эффективности в
выполнении им требуемой функции. Это могут быть такие важные физические
свойства, как электропроводность (создание органических металлов) или
способность образовывать жидкие кристаллы; химические свойства, как, например,
каталитическая активность, подобная активности биологических катализаторов
(ферментов), или просто определенная реакционная способность, отвечающая тем
или иным нуждам синтеза; биологическая активность, в конечном счете
направленная на лечение определенных болезней или на борьбу с
насекомыми-вредителями. Здесь снова можно сказать, что все это - наиболее
обычные задачи, с которыми органическая химия имела дело уже в течение
столетия, задолго до появления термина "молекулярный дизайн". Однако
традиционный поиск полезных соединений ранее шел в основном методом проб и
ошибок, а потому поглощал огромное количество труда и времени на синтез тысяч
аналогов, необходимых для нахождения одного из них, отвечающего поставленной
задаче. В настоящее время ясно обнаруживается тенденция двигаться в этой
области гораздо более экономными путями. Достаточно часто еще в начале подобных
проектов теперь применяют разнообразные методы молекулярного моделирования,
позволяющее с разумной вероятностью установить тот набор структурных
параметров, наличие которых должно обеспечить целевому соединению способность
выполнять заданную функцию. Результаты первоначальных экспериментов используют
далее для корректировки исходных планов и более точного фокусирования
направлений исследования. При этом иной раз удается сузить область поиска
целевой структуры до всего нескольких многообещающих кандидатов. При этом
сплошь и рядом функционально-ориентированный дизайн получает плодотворные
импульсы от своего структурно-ориентированного собрата в виде открытий новых
классов структур с набором новых, потенциально полезных свойств (как это имело
место, например, в случае жидких кристаллов или органических металлов).
2.5 Использование наноматериалов и
нанотехнологий в современном нефтегазохимическом синтезе
В настоящее время глубина переработки нефти на
предприятиях России составляет в среднем 70%. Однако значительная доля (свыше
20%) ежегодно добываемых попутных газов не находит квалифицированной
переработки и сгорает в промысловых факелах, что, по оценке экспертов, приводит
к потере порядка 2 млрд долл. в год и связано с разрушительным воздействием на
экологию.
Внедрение новых технологий требует согласованных
усилий государства, частного бизнеса и науки. И примеры таких партнерских
отношений есть. Это уже накопившийся положительный опыт поддержки разработки и
освоения новых технологий через систему долевого финансирования важнейших
инновационных проектов со стороны государства и компаний.
Одно из новых направлений в технологии
осуществления химических превращений - мембранно-каталитические методы
переработки попутных нефтяных газов в высокоценные химические продукты.
Имеющийся отечественный научно-технологический
потенциал должен быть использован для создания принципиально новых, гибких
(например, мембранно-каталитических) процессов, поддающихся легкому
масштабированию для интенсификации переработки углеводородного сырья (в первую
очередь - попутных нефтяных газов), расширения сырьевой базы для производства
моторных топлив и основных продуктов промышленности тяжелого органического
синтеза, повышения селективности, снижения затрат энергии на производство
единицы продукции, обеспечивающих прорыв в важнейших направлениях технологий
переработки нефти и природного газа.
Примером может служить создание
наномембранно-каталитических реакторов, являющихся базовым, легко встраиваемым
элементом в комплексные технологические процессы нефтегазового комплекса для получения
широкого класса высокотехнологичной продукции, например, олефинов (этилен,
пропилен, бутилены) и ароматических углеводородов (бензол, толуол и др.).
Таким образом, стратегически необходимо
сосредоточиться на новых высокоскоростных и избирательных технологиях
переработки органического сырья, элементы которых уже созданы российскими
специалистами.
К настоящему времени в России выполнен
значительный объем научных разработок и на базе Ассоциации "АСПЕКТ"
создано опытно-промышленное производство отечественного высокотехнологичного
продукта - металлокерамических пластичных нанопористых материалов (торговая
марка TrumemЄ).
Одновременно с этим учеными Института
нефтехимического синтеза (ИНХС РАН) обнаружен эффект асимметрии селективности
реакций в наномембранно-каталитических структурах на основе мембран TrumemЄ и
способность наноразмерных каналов изменять селективность процессов окисления
протекающих по ним углеводородов. В комбинации с достижениями в производстве
нанопористых структур это обеспечивает прорыв в промышленной реализации задач
высокоэффективного синтеза ценных органических продуктов. Иными словами,
наномембранно-каталитические структуры позволяют одновременно осуществить
скоростные селективные реакции (со скоростью и селективностью на порядки выше,
чем в обычных условиях) за счет каталитической компоненты и размерных эффектов
в нанокапиллярах, и обеспечить эффективное разделение и очистку получаемых
продуктов при низком энергопотреблении за счет мембранной компоненты. При этом
каждая пора наномембранно-каталитической структуры выполняет роль
микрореактора, в котором осуществляется единый цикл химических превращений и
разделения продуктов реакций. В этом состоит принципиально новый подход к
решению задач крупнотоннажной промышленной химии, который позволяет легко
масштабировать наномембранно-каталитические процессы для интенсификации и
существенного снижения затрат в процессах переработки органического сырья.
В качестве первого шага на этом стратегическом
направлении по инициативе Правительства России (Госзаказчик - Федеральное
агентство по науке и инновациям) в рамках формирования государственно-частного
партнерства обеспечена разработка отечественной технологии переработки
факельных попутных газов в ценную товарную продукцию - ароматические углеводороды.
В течение 2005-2006 гг. за счет бюджетных средств (более 300 млн руб.) и
частных инвестиций (около 300 млн руб.) разработаны и поставлены на
производство (ОАО "Новосибирский завод химконцентратов" концерна
"ТВЭЛ" Росатома) новые катализаторы для этого процесса; создана
пилотная установка (ОАО "НИПИГазпереработка" г. Краснодар, компания
"Сибур") мощностью 500 тыс. м3 газа/год (1000 тн/год),
полномасштабные испытания которой будут завершены к октябрю с.г.
В качестве основных исполнителей проекта были привлечены:
Ассоциация предприятий атомной промышленности "АСПЕКТ" (управляющая
компания); институты РАН (Институт проблем химической физики РАН, Институт
катализа СО РАН), обеспечившие решение фундаментальных проблем осуществления
химических и каталитических процессов превращения попутных газов; отраслевые
организации (ГНЦ "Курчатовский институт", ОАО "ВНИПИНефть",
ЗАО "ВНИИОС НК", ОАО "НИПИГазпереработка"), обеспечившие
технологические испытания созданных процессов и их проектно-конструкторскую
разработку; вузы (Московская государственная академия тонкой химической
технологии, Московский институт стали и сплавов), которые ведут подготовку
специалистов для промышленности по производству катализаторов и применению
создаваемых процессов, и, наконец, промышленные предприятия, осуществившие
освоение производства создаваемых катализаторов и практическую реализацию
промышленных процессов (ОАО "Новосибирский завод химконцентратов",
ЗАО "Самарский завод катализаторов") и процессов переработки попутных
газов (ОАО "Татнефтехиминвест-холдинг").
Новая технология глубокой переработки попутных
нефтяных газов в ароматические углеводороды обеспечит в период до 2009 г. вклад
в приращение ВВП 2,1 млрд руб. При этом выбросы СО2 в атмосферу
сокращаются в 3,5 раза, что будет способствовать выполнению Россией требований
Киотского протокола.
Разработанная технология обеспечивает
превращение предельных углеводородов (пропана, бутанов) в ароматические
углеводороды (бензол, толуол, ксилолы) - процесс ароматизации. Это чрезвычайно
актуально, поскольку в ближайшие годы в России прогнозируется значительный рост
производства продуктов, исходным сырьем для которых является бензол. Основными
сферами применения бензола в мире являются: производство стирола, капролактама,
этилбензола, фенола, кумола, циклогексана и малеинового ангидрида.
Среднегодовой прирост производства стирола и сополимеров стирола составит
10,4%, капролактама - 5,8%, фенола - 9,9%. В связи с этим ожидается увеличение
спроса на бензол. Толуол используется в нефтеперерабатывающей промышленности
при производстве смазочных масел и присадок, в качестве растворителя в
производстве лаков и красок, синтетических каучуков, а также в оборонной
промышленности. Ожидается, что объем потребления толуола в экономике России
возрастет в период 2006-2010 гг. примерно в полтора раза. Основной областью
использования ксилола является изготовление полиэфирных волокон и нитей. Другая
перспективная область использования ксилола - производство гранулированного
ПЭТФ, из которого изготовляются пластиковая упаковка для пищевых продуктов,
косметических и фармацевтических средств, видео- и аудиопленок и других
изделий. Прогнозируется увеличение спроса на ксилол в России в период с 2006 по
2015 гг. примерно в 2,6 раза.
Следовательно, в результате реализации проекта
разработанная технология позволит получить смесь ароматических углеводородов,
потребность в которой будет возрастать в ближайшие 10 лет. Реализация проекта
позволит удовлетворить растущую потребность экономики России в ароматических
соединениях.
Разработанная технология получила полную
поддержку на организованном правительством Татарстана совещании руководителей
нефтедобывающих и нефтеперерабатывающих компаний. Технология прошла
международную экспертизу и к ней проявлен интерес со стороны ведущих инжиниринговых
компаний. В частности, компания "Linde" (Германия) рассматривает
данную технологию как основу для своего участия в переработке попутных газов в
России, включая поставку оборудования и сдачу установки "под ключ".
Ведущие развитые страны (США, Япония, Германия,
Англия, Франция), на государственном уровне, и крупнейшие мировые компании по
добыче и переработке нефти и газа (Шелл, Бритиш Петролеум, Шеврон, Мобайл и
др.), на частном уровне, осуществляют многомиллиардные ивестиции в разработку
новых эффективных и энергосберегающих технологий переработки нефти и газа.
Несмотря на столь высокий конкурентный уровень развития этих технологий, Россия
имеет сегодня уникальный шанс вырваться вперед за счет активного использования
своих прорывных разработок, в частности, в области производства нанопористых
материалов и новых открытий в области протекания каталитических процессов в
нанопористых структурах. [22]
Заключение
В данной работе мы ознакомились с некоторыми
наиболее многообещающими перспективами промышленного органического синтеза. К
сожалению, невозможно описать все направления развития данной области, так как
количество их огромно и растёт с каждым днём. Число известных органических
соединений близко к 10 миллионам и не ограничено число тех соединений, которые
могут быть получены. В химических лабораториях каждый день синтезируются сотни
новых веществ. Открываются новые реакции, разрабатываются новые способы
получения органических веществ, внедряются новые методы стимулирования
химических реакций и новые методы исследования химических соединений.
Продуктами органического синтеза, осуществляемого в промышленных масштабах,
являются пластмассы, химические волокна, красители, лекарственные препараты,
сельскохозяйственные химикаты, моющие средства, душистые вещества и многие
другие вещества и материалы, необходимые человеческому обществу. Современная
органическая химия располагает огромным экспериментальным и теоретическим
материалом, а уровень развития органического синтеза может служить мерилом
научно-технического прогресса. Интенсивно развиваются как синтетическая, так и
теоретическая органическая химия.
Всё острее и острее глобальная сырьевая
проблема. Уже в этом веке все запасы нефти и газа будут исчерпаны, а это грозит
не только энергетическим кризисом, но и утратой самого главного источника
сырья. Большинство синтетических материалов, используемые человечеством
производятся из нефтехимического сырья. Поэтому, огромное значение имеет
разработка новых перспективных направлений в промышленном органическом синтезе.
Развитие человечества не смогло не затронуть и
состояние биосферы Земли. К сожалению, одним из самых сильных её загрязнителей
является промышленный органический синтез, а также продукты его деятельности.
Человек и человеческое общество являются открытыми системами и любое изменение
в окружающей среде неизбежно сказывается на всех её обитателях. Даже небольшие
выбросы опасных веществ способны привести к необратимым последствиям. Мы не
имеем право забывать об этом и обязаны искать новые экологически чистые пути
решения данных проблеем. И тут нам не обойтись без виновника данной проблемы,
промышленного органического синтеза.
Промышленный органический синтез стал
неотъемлемой частью человеческого общества и перспективы развития человечества
зависят от перспектив развития промышленного органического синтеза.
Список используемой литературы
1. Катализ в Cl-химии. Под
редакцией Л. Кайма. Л.: Химия, 1987. 296 с.
. Современные направления в
органическом синтезе. Под редакцией X. Нодзаки. М.: Мир, 2006. 558 с.
Книга: однотомное издание с автором
. Глущенко Н.Н., Плетенева Т.
В., Попков В. А. Фармацевтическая химия: учебник для студентов средних
профессиональных учебных заведений. Под ред. Т. В. Плетеневой. М.: Издательский
центр "Академия", 2011. 384 с.
. Смит В.А., Дильман А.Д.
Основы современного органического синтеза: учебное пособие. М.: Издательство
"Бином. Лаборатория знаний", 2009. 752 с.
. Теддер Д., Нехватал А.,
Джубб А. Промышленная органическая химия. М.: Мир, 1977. 700 с.
. Тейлор Ф.С. "История промышленной
химии"
Статья: из сборника статей или
журнала
. Денисов В.Я., Ткаченко
Т.Б., Чуйкова Т.В. Органический синтез - основа современной органической химии
// Успехи современного естествознания. 2011. № 2. С. 118-120