Взаимодействие альдегидов с тетрацианоэтиленом
Содержание
Введение
.
Литературный обзор
.1
Взаимодействие тетрацианоэтилена с карбонильными соединениями
.2
Основные направления взаимодействия тетрацианоэтилена с карбонильными
соединениями
.3
Алифатические и жирноароматические кетоны и тионы в реакциях с ТЦЭ
.
Обсуждение результатов
.Экспериментальная
часть
Выводы
Метрология
Техника
безопасности
Вопросы
экологии
Гражданская
оборона
Список
литературы
Введение
В связи с все возрастающим ростом потребности
современной науки (медицинская химия [1], нанотехнология [2] и молекулярная
электроника [3]) в соединениях, имеющих достаточно сложное строение, перед
химиками-синтетиками встала задача создания прикладных методов синтеза таких
веществ, в том числе и с использованием комбинаторной химии. Очевидно, что
усложнение строения и функционального обрамления молекул увеличивает
стадийность и сложность методов его синтеза [4]. Надо отметить, что при этом
наблюдается резкое снижение выхода конечного соединения, связанное с
вышеуказанным фактом и побочными процессами. Кроме того, это ведет к
возрастанию количества отходов, что экологически неприемлемо. Поэтому
специалисты и ведущие фирмы мира ведут активный поиск идеологий, лишенных
указанных недостатков.
Высокий синтетический потенциал в этой области
показали непредельные нитрилы [5-15]. Нитрилы, как класс соединений и
нитрильная группа, как функциональная играют особую роль в органической химии.
Действительно, трудно найти другую функциональную группу, которая столь легко
вводилась бы в молекулу и обладала такой высокой активностью, обусловленной
сочетанием поляризуемости и ненасыщенности. Не случайно в основе одной из
наиболее серьезных концепций возникновения добиологической Жизни лежит
рекомбинация молекул синильной кислоты [2]. Сравнительно недавно, было обнаружено,
что накопление нитрильных групп в одной молекуле взаимно активирует их, приводя
к “взрыву” реакционной способности и, как следствие, каскадам уникальных
химических превращений.
Тетрацианоэтилен (ТЦЭ) - один из ярких
представителей класса пернитрильных алкенов [7,12,13,15]. Интенсивно
развивающимся направлением химии тетрацианоэтилена в последнее время стало
синтез и изучение свойств его аддуктов c кетонами [17-21]. Среди аддуктов и их
производных найдены перспективные противораковые препараты [22], получены
комплексы с переносом заряда [23] и соли с плоским органическим анионом имеющие
перспективу использования в качестве элементов молекулярной электроники
[24-26].
Несмотря на большое количество сообщений о
взаимодействии ТЦЭ с карбонильными соединениями, все они относятся к кетонам, а
альдегиды обойдены вниманием исследователей.
Гетероциклические соединения на протяжении всей
истории развития органической химии постоянно находятся в центре внимания
исследователей - на их долю приходится около 80% всех публикаций по этой
области химии, что связано, прежде всего, с широким спектром биологической
активности их производных и другими видами практического применения [1]. В
конце прошлого столетия из 1500 наиболее регулярно применяемых медицинских
препаратов свыше 10% приходится на долю соединений, имеющих пиридиновое кольцо.
Среди них: витамины (B3, B6, PP), анальгетики, антисептики, антидепрессанты;
препараты противотуберкулезного, противоопухолевого и других видов действия
[2]. В недавно опубликованной монографии [3] констатируется, что пиридин и его
гомологи относятся к числу важнейших синтонов тонкого и промышленного
органического синтеза.
Впервые начато исследование взаимодействия
тетрацианоэтилена с альдегидами. Установлено что, варьируя молярное соотношение
реагентов, вид и количество катализатора, удается осуществить синтез ранее
неизвестных
3,8-диалкил-6-имино-2,7-диоксабицикло[3.2.1]октан-4,4,5-трикарбонитрилов а так
же изучать их взаимодействие с другими соединениями
1. Литературный обзор
.1. Взаимодействие тетрацианоэтилена с
карбонильными соединениями
Непридельные нитрилы с момента синтеза наиболее
яркого представителя данного класса - тетрацианоэтилена стали объектом для
всестороннего изучения [5-15]. Наличие электроно-дефицитной кратной связи
обеспечивает использование их в качестве π-кислот
в реакциях циклоприсоединения [13]. Кроме широко используемого [4+2]
циклоприсоединения по Дильсу-Альдеру [13,27-29] для них характерны реакции
[2+2] присоединения [30-44], реализуемые, как правило, через образование
цвиттер-ионного интермедиата [42-46]. Именно данная схема предлагается нами в
качестве основной для описания взаимодействия тетрацианоэтилена с карбонильными
соединениями.
Цианогруппа не только активирует кратную связь,
но и сама обладает рядом уникальных свойств, которые делают ее идеальным
перкурсором в органической химии. Ее линейное строение и компактность не
создают пространственных затруднений, что исключает стерические затруднения при
нуклеофильных и электрофильных реакциях по СºN связи. Благодаря
своему сильному электроноакцепторному эффекту она способна активировать
соседние функциональные группы и связи. На ее основе восстановлением различными
реагентами могут быть получены амино-, оксо-, иммногруппы; гидролизом -
карбоксильная, сложноэфирная, амидная группы, в результате децианирования можно
получить алкены, а декарбоксилирования - алканы и т.д. Многообразие превращений
полинитрильных соединений раскрыто в ряде обзоров [7,12,13,15] на примере ТЦЭ.
Предметом настоящего обзора являются схемы
реакций между ТЦЭ и карбонильными соединениями, а также свойства
«тетрацианоэтилированных» кетонов.
.2 Основные направления взаимодействия
тетрацианоэтилена с карбонильными соединениями
Исторически первым методом вовлечения
тетрацианоэтилена (1) во взаимодействие с кетонами была реакция получения
тетрацианоалканонов (2) с использованием в качестве катализатора «молекулярного
серебра» [47,48]. Однако более эффективным оказался катализ водными растворами
сильных кислот [49]. При использовании газообразного хлористого водорода выход
целевого продукта не высокий. Оптимальным можно считать использование
концентрированного водного раствора хлористого водорода. Количество взятой
кислоты влияет на время реакции, однако выход меняется незначительно. При катализе
20% водного раствора серной кислоты время реакции увеличивается в 3-4 раза.
Уксусная кислота эффективна в виде 50% водного раствора при температуре
40-50°С, в то время как трифторуксусная (99.5%) активна при комнатной
температуре. К кислотному типу катализа можно отнести реакции и в присутствии
диоксида серы [12,37].
Другими катализаторами указанного процесса
являются спирты или вода, взятые в больших количествах, чем кислоты, что сильно
влияет на выход целевого вещества [50].
Схема взаимодействия тетрацианоэтилена с
кетонами описана в работе [49].
Схема 1.
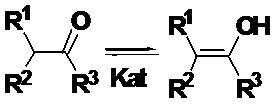
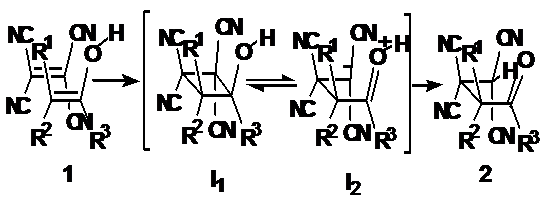
Под действием кислот или спиртов
скорость достижения равновесия между кетонной и енольной формами оксосоединений
возрастает. Затем енол образует π-комплекс с
тетрацианоэтиленом, который далее превращается в циклобутан (I1) по схеме [2+2]
циклоприсоединения, описанной для виниловых эфиров (3) [30-39,42-44]. В ряде
работ было показано, что циклобутан (3) может существовать в виде цвиттер-иона
(I3) [32-35,38,44] и в связи с этим предложена схема образования
тетрацианоалканона (2) включающая образование интермедиата (I2) [49]. Раскрытие
циклобутана (3) наблюдается при взаимодействии с метанолом и приводит к кеталям
тетрацианоалканонов (4) [42-46].
Схема 2
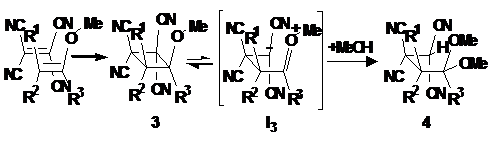
В подобные реакции вступает и ацилированная
енольная форма ацетона. Продукт реакции после гидролиза превращается в
тетрацианоалканон (2) [49].
Схема 3.
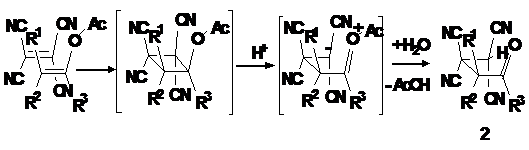
Следует отметить, что образующиеся
4-оксоалкан-1,1,2,2-тетракарбонитрилы (2) обладают наибольшей стабильностью в
ряду полинитрильных аналогов [12,13], однако в ряде случаев их выделение
невозможно вследствие дальнейших превращений. Путь протекающих преобразований
определяется как строением карбонильных соединений, так и условиями проведения
реакции.
Схема 4.
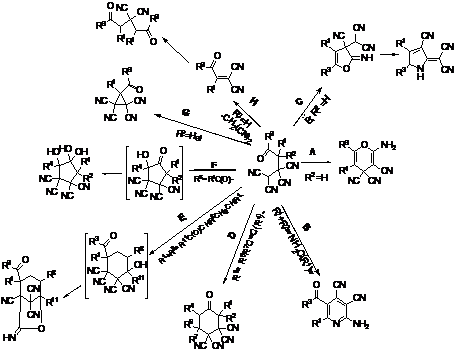
Наиболее распространенным
направлением превращений 4-оксоалкан-1,1,2,2-тетракарбонитрилов (2) является
внутримолекулярная циклизация с участием OH или NH-нуклеофильного центра
кетонов и цианогрупп дицианометиленового фрагмента, приводящая к образованию
шестичленных гетероциклов (направления A и B [сх.4]). В присутствии оснований (пиперидин)
цианогруппы при атоме С1 дезактивируются вследствие образования солеобразных
соединений, и происходит «вынужденная» циклизация на цианогруппы при С2,
приводящая к пятичленным гетероциклам (направление C [сх.4]). В случае
непредельных кетонов и дикарбонильных соединений реализуется внутримолекулярное
присоединение СН-кислотного центра по кратной связи, приводящее к пяти или
шестичленным алициклам (направления D, E и F [сх.4]). От α-галогензамещенных
тетрацианоалканонов может отщепляться HHal, что приводит к образованию
циклопропанов (направление G [сх.4]).
Проведение реакций в более жестких
условиях может привести к дедицианометилированию (направление H [сх.4]). Данное
направление часто используется для введения в молекулу малонодинитрильного фрагмента
и представляет собой ретро-Михаэлевское превращение [51,52]. Если скорость
отщепления малонодинитрила значительно выше скорости образования аддукта (2)
или карбонильное соединение взято в избытке, то может происходить
взаимодействие со второй молекулой карбонильного соединения.
Схема 5.
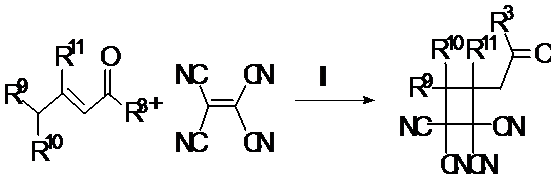
Направление I (образование
циклобутана, сх.5) необычно тем, что на этапе тетрацианоэтилирования
задействуется γ-СН кислотный
центр непредельного альдегида, а сама реакция завершается присоединением СН
кислотного центра дицианометиленового фрагмента по двойной связи
углерод-углерод.
Кроме описанного выше часто
реализуемой для карбонильных соединений имеющих в своем строении элемент
1,3-диеновой системы, является реакция диенового синтеза [13].
.3 Алифатические и
жирноароматические кетоны и тионы в реакциях с ТЦЭ
Взаимодействие тетрацианоэтилена с
алифатическими и жирноароматическими кетонами, способными к кенолизации
представляют собой модификацию конденсации по Михаэлю [15]. Образующиеся при
этом аддукты -4-оксоалкан-1,1,2,2-тетракарбонитрилы достаточно стабильны и
могут быть выделены и охарактеризованы [12,13].
4-Оксоалкан-1,1,2,2-тетракарбонитрилы (2) были
впервые получены Мидделтоном в 1957 году реакцией кетонов, содержащих a-водородный
атом, с тетрацианоэтиленом (1) в течение 8-170 часов, в качестве катализатора
использовалось «молекулярное серебро». Выход по данному методу составил 50-90%
[47,48]. Позднее были найдены более доступные кислотные и слабоосновные
катализаторы тетрацианоэтилирования, и на многочисленных примерах было показано
управляемое внедрение тетрацианоэтилена по a-метиленовому и a-метильному
звеньям кетонов [50,53]. Показано, что взаимодействие тетрацианоэтилена (1) с
метилалкилкетонами (5) при катализе «молекулярным серебром» или спиртами
протекает с участием α-метильной
группы и селективным синтезом аддуктов (6) [50].
Схема 6.

В случае кислотного катализа
активируется метиленовое звено и образуются изомерные соединения (7) [50].
Строение тетрацианоалканонов (6,7) было подтверждено их циклизацией под
действием кислот в пиридины и пираны [54].
Было обнаружено, что циклические
кетоны (например, циклогексанон) реагируют значительно энергичнее, чем
ациклические (например: ацетон, метилэтилкетон и диэтилкетон). В идентичных
условиях полнота протекания процессов для циклических (циклогексанон) достигается
за 1-2 мин. в то время как для линейных (ацетон, метилэтилкетон и диэтилкетон)
- 6-24 ч [47,55].
Сообщалось о тетрацианоэтилировании
дигидроэпиандростерона (8) в присутствии галогеноводородной кислоты в качестве
катализатора с выходом 85% [56]. Вышеуказанное показало возможность
распространения тетрацианоэтилирования на сложные полициклические объекты
природного происхождения.
Схема 7.
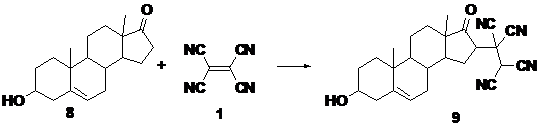
Неустойчивые замещенные
тетрацианоэтаны (11) получены взаимодействием ТЦЭ с
4-оксо-4,5,6,7-тетрагидроиндолами (10) - представителями циклических кетонов,
содержащих гетероциклический фрагмент [57].
Схема 8.
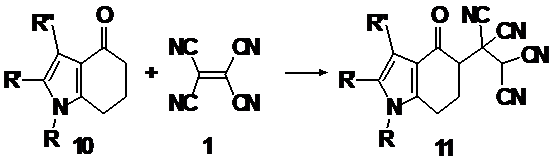
Кроме катализа «молекулярным»
серебром, спиртами и различными кислотами имеются сведения о
тетрацианоэтилирование циклогексанона в присутствии оксида серы (IV) с выходом
95% [12,37].
В некоторых системах возможно так же
взаимодействие ТЦЭ с кетонами без катализатора, однако в этом случае требуются
жесткие условия, приводящие к дальнейшим превращениям аддуктов по направлению H
(сх.4.). Так, процесс дедицианометилирования с последующим взаимодействием
образовавшегося α,β-непредельного
динитрила (13) со второй молекулой кетона обнаружен при тетрацианоэтилировании
2-инданона (12) [58 68].
Схема 9.
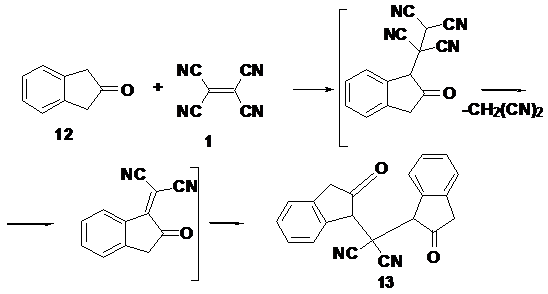
Исследование взаимодействия α-разветвленных
кетонов с ТЦЭ представлено единичной публикацией [59]. В ней описано получение
аддуктов (15, 18) на основе 2-метилициклогексанона (14, 17) и ментона.
Различное направление атаки для этих соединений объясняется затруднением
подхода ТЦЭ к метиновому звену ментона вызванного объемным изопропильным
заместителем. Продолжительность реакции составила 24 ч, а выход достигал 90%.
Схема 10.
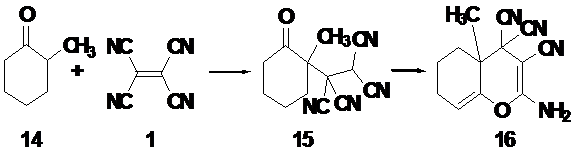
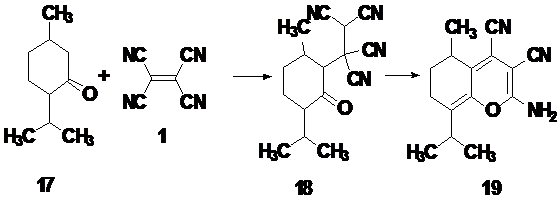
Полученные аддукты оказались
малостабильными веществами и самопроизвольно превращаются при комнатной
температуре в течение 1-2 дней в гидрированые хромены (16, 19) с
количественными выходами [59].
Схема 11.

Следует отметить, что взаимодействие
ТЦЭ с карбонильными соединениями позволило впервые осуществить синтез ранние не
доступных диоксабициклов.
2. Обсуждение результатов
Получение
3,8-диалкил-6-имино-2,7-диоксабицикло[3.2.1]октан-4,4,5-трикарбонитрилов
В результате реакций тетрацианоэтилена с
алифатическими кенолизирующимися альдегидами 1a,б в присутствии каталитических
количеств хлороводородной кислоты образуются
3,8-диалкил-6-имино-2,7-диоксабицикло[3.2.1]октан-4,4,5-трикарбонитрилов 2а,б с
выходами 40-72%.
Данное превращение представляет собой трех
компонентную реакцию, в которой в качестве третьего компонента выступает вторая
молекула альдегида.
Схема 1

1а,
2а:
R1=Me, R2=Me 1б,
2б:
R1=Et, R2=Et;
Процесс формирования бициклов 2а,б
включает две последовательные реакции. Первая, начинается с енолизации
альдегидов. Далее енолы вступают во взаимодействие с тетрацианоэтиленом с
образованием промежуточного биполярного иона, которая затем напрямую реагирует
со второй молекулой альдегида, образуя циклическую структуру I1.
Необходимо отметить, что
синтезированные ранее структурные аналоги данного типа соединений, например,
1-R1-3-R2-8-R3-6-имино-2,7-диоксабицикло[3.2.1]октан-4,4,5-трикарбонитрилы
обнаружили способность подавлять рост опухолевых клеток, а для некоторых линий
клеток рака прямой кишки, мелономы и рака почек наблюдалось цитотоксическое действие
[22], что делает проведенные нами исследования перспективными.
Результаты исследования влияния
структуры альдегидов на процесс образования диоксабициклов 2а,б полностью
совпадают с представлениями об активности исходных альдегидов. Так, наиболее полно
и быстро (в течение 1 ч) реакция происходит для изомасленного альдегида. Менее
активные алифатические альдегиды, не имеющие заместителей в a-положении, такие как
масляный и капроновый, взаимодействует значительно медленнее и с меньшими
выходами.
Необходимо отметить, что
присоединение тетрацианоалканаля к альдегиду протекает стереоселективно с
образованием только одного из возможных диастереомеров, у которого алкильный
заместитель при атоме С3 лежит в транс-положении к оксаиминному мостику (сх.
2). Вероятно, эта реакция чувствительна к стерическим затруднениям. Так,
например, 4-оксоалкан-1,1,2,2-тетракарбонитрилы не реагируют с кетонами [49].
Схема 2
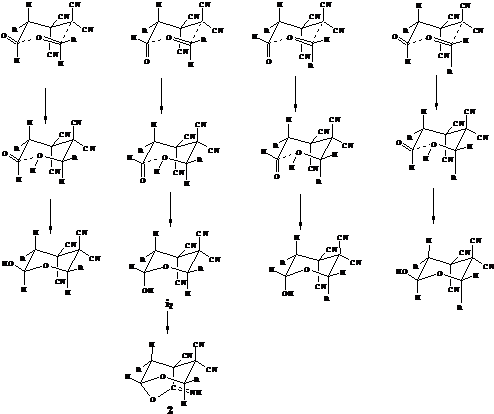
Строение соединения 2а определено методом
рентгеноструктурного анализа монокристаллов (Рис.1). В пределах стандартных
отклонений соответствующие расстояния и углы в молекуле 2а одинаковы и не
выходят за пределы значений для соответствующих типов связей [67]. Как это
видно из рисунка1 для молекулы 2а наблюдаются многочисленные межмолекулярные
взаимодействия атомов водорода метильных групп и атомов азота цианогрупп, что и
определяет упаковку молекул 2а в кристалле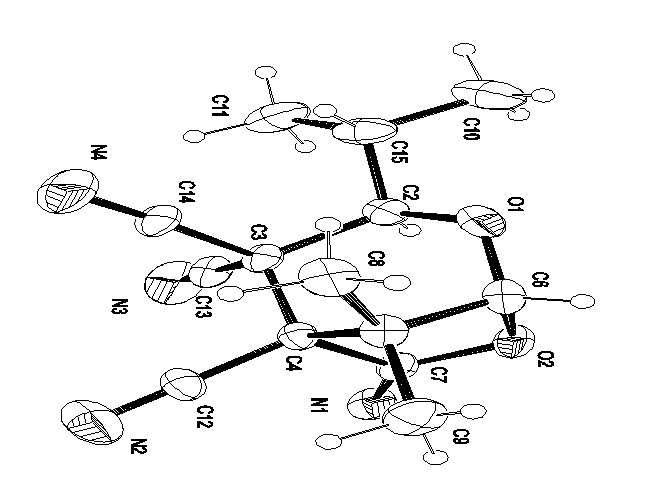
Рисунок 1. Молекулярная структура соединения 2а
Таблица 1. ИК, ЯМР 1Н и масс-спектры
соединений 2а,б
|
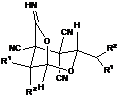
|
|
|
|
Соединение
|
R1
|
R2
|
ИК
спектр, см-1
|
Масс-спектр,
m/z (EI, %)
|
Спектр
ЯМР 1Н (ДМСО-d6), d, м.д.
|
|
2а
|
Me
|
Me
|
3280
(n NH), 2260
(n СºN), 1690 (n С=N)
|
257
([M-15]+, 0.1), 229 (1)
|
9.78
с (1Н, NH), 5.82 с (1Н, СНО2), 4.03 д (1Н, J 8.55, ОСНСН), 2.19 м (1Н, J
6.71, 8.55, i-Pr), 1.42 с (3Н, СН3С), 1.24 с (3Н, СН3С), 1.17 д (3Н, J 6.71,
СН3СН), 1.12 д (3Н, J 6.71, СН3СН)
|
|
|
2б
|
Et
|
Et
|
3280
(n NH), 2260
(n СºN), 1690 (n С=N)
|
257
([M-71]+, 0.9)
|
9.79
с (1Н, NH), 5.93 с (1Н, СНО2), 4.10 д (1Н, J 6.71, О-СН), 2.00 м (1Н,
СН-СНEt2), 0.9-1.9 м (20Н, J 6.71, 7.32, 4Et)
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Структура соединения 2а,б подтверждена ИК, 1Н
ЯМР и масс-спектроскопией (см. табл.1).
Для спектров ЯМР 1Н соединений 2а,б характерны
сигналы протона иминной группы в виде синглета в области с δ
9.8-9.6
м.д. и протона при ацетальном атоме углерода в виде синглета в области с δ
6.6-5.8
м.д. В ИК спектрах соединений 2а,б наблюдаются интенсивные полосы поглощения в
области 3280-3300 см-1, характерные для связи N-H иминогруппы, а также полосы
валентных колебаний группы С=N в области 1685-1700 см-1. Колебания
несопряженной нитрильной группы проявляются в виде полосы слабой интенсивности
при 2260 см-1.
Масс-спектр соединений 2а,б представлен ионами,
соответствующими потере алкильного заместителя диоксабициклического кольца с
интенсивностью 0.1-10%.
Реакции
3-алкил-6-имино-8,8-диалкил-2,7-диоксабицикло[3.2.1]октан-4,4,5-трикарбонитрилов
с ацетальдоксимом
Взаимодействие 3-алкил-6-имино-8,8-диалкил-2,7-диоксабицикло[3.2.1]-
октан-4,4,5-трикарбонитрилов (2а,б) с избытком оксима ацетальдегида приводит к
образованию
6-[1-(гидроксиламино)этокси]-3-имино-4,7,7-триалкил-1-оксатетрагидропирано[3,4-c]пиррол-3a,7a(1Н,4Н)-дикарбонитри-лов(3а,б).
Схема 4

3a: R1=Me,
R2=Me; 3б:
R1=Et, R2=Et.
Согласно предлагаемой нами схемы
электрофильный углерод ацетального фрагмента подвергается атаке нуклеофильной
гидроксильной группы оксима, что приводит к интермедиату I1. Далее, по-видимому,
происходит образование I2 за счет отшепления ацетонитрила.
В пиране I2, как мы считаем,
карбоксамидная группа и вошедший заместитель находятся в транс положение друг
относительно друга. А поскольку лишь экваторилальное положение карбоксамидной
группы обеспечивает ее взаимодействие с вицинальным нитрильным заместителем,
что приводит к формированию пиррольного цикла. Переход карбоксамидной группы в
экваториальное положение в результате обращения цикла предполагает переход
алкильного заместителя цикла в аксиальное положение. Далее гидроксильная группа
выступает в качестве нуклеофила, а α-С оксима в качестве
электрофильного центра в реакции приводящей к конечному продукту 3.
Процесс образования 3 может
протекать и без образования интермедиата (I2) с гидроксильной группой, как
результат одновременного образования нитрила и присоединения оксима.
Расположение вводимого заместителя в
аксиальном или экваториальном положении нами определено не было, однако на
основании данных спектров 1Н ЯМР мы считаем, что образуется лишь один из
возможных изомеров. Это показывает протекание превращений под строгим
стерическим контролем, что можно соотнести с протеканием реакции по схеме,
включающей реализацию бимолекулярного механизма замещения.
Для доказательства строения
соединений 3а,б были использованы методы ИК, масс, ЯМР 1Н спектроскопии (табл.
2).
В ИК- спектре соединения 3а,б
присутствуют полосы поглощения при 1690 см-1 С=N связи, при 1725 см-1 С=О связи
карбонильной группы, при 2260 см-1 несопряженных нитрильных групп, и широкая
полоса поглощения NH и ОН в области 3300-3400 см-1.
|
Таблица
2. ИК и ЯМР 1Н спектры соединений 3а,б
|
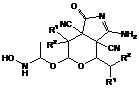
|
|
|
Соединение
|
R1
|
R2
|
ИК
спектр, см-1
|
Спектр
ЯМР 1Н (ДМСО-d6), d, м.д.
|
|
|
|
n N-H
|
n CºN
|
n C=O, C=N
|
|
|
3а
|
Me
|
Me
|
3300-3400
|
2260
|
1700,
1725
|
8.06
с (1Н, NH), 7.35 с (1Н, OH), 6.46 с (2Н, NH2), 5.5 с (1Н, O-CH-O), 4.91 м
(1Н, O-СH-N), 4.21 д (1Н, J=9.15 Гц, O-СH-СН), 2.0 м (1Н, J=6.77, 8.54 Гц,
O-СН-СН(СН3)2), 1.63 с (3Н, Me), 1.5 д (3Н, J=6.10 Гц, NН-СНСН3), 1.06 д (3Н,
J=6.71 Гц, O-СН-СН(СН3)2), 0.94 с (3Н, Me), 0.85 д (3Н, J=6.71 Гц,
O-СН-СН(СН3)2)
|
|
3б
|
Et
|
3300-3400
|
2260
|
1700,
1725
|
8.1
с (1Н, NH), 7.30 с (1Н, OH), 6.5 с (2Н, NH2), 5.7 с (1Н, O-CH-O), 4.85 м (1Н,
O-СH-N), 4.4 д (1Н, O-СH-СН), 2.3 м (1Н, O-СН-СН(СН2)2], 2.0-1.3 м (8Н+3Н,
4CH2+CH3), 1.0-0.70 м (12Н, 4СН3)
|
|
|
|
|
|
|
|
|
|
Масс-спектры соединений 4 представлены
молекулярным ионом [М]+ 5-10%, дальнейший распад происходит с потерей метильной
группы [М-15]+ 1%.пектр ЯМР 1Н соединений 4 представлен синглетом с δ
8.0-8.1
м.д. HONH группы (1Н), синглетом с δ 7.3-7.4
м.д гидроксильной группы гидроксиламина (1Н), синглетом с δ
6.4-6.5
м.д N=C-NH2 группы (2Н), синглетом с δ 5.5-5.7
м.д O-CH-O группы (1Н), мультиплетом с δ 4.8-4.9
м.д O-СH-N группы (1Н), дуплетом с δ 4.2
м.д O-СH-СН группы (1Н), мультиплетом с δ 2.0-2.3
м.д O-СН-СН(Alk)2 группы (1Н) и сигналами соответствующие протонам алкильных
групп.
Взаимодействие с оксимами кетонов
В случае реакции
3-алкил-6-имино-8,8-диалкил-2,7- диоксабицикло[3.2.1]октан-4,4,5-трикарбонитрилов
(2а,б) с оксимами кетонов (метилэтилкетона, цилогексанона и ацетона) в среде
ацетонитрила происходит образование
2-алкил-5,5-диалкил-6-алкилиденаминоокси-3,3,4-трицианотетрагидро-2H-пиран-4-карбоксамидов
(4а,б) с выходами 65-75%.
Схема 5
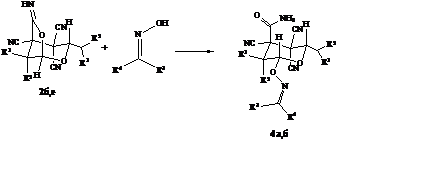
4а:
R1=Me, R2=Me, R3=Me, R4=Me; 4б: R1=Et, R2=Et, R3=Me, R4=Me;
Как и с оксимами альдегидов реакция
с оксимами кетонов, по-видимому, начинается с атаки нуклеофила по
электрофильному углероду ацетального фрагмента диоксабицикла. Однако в отличие
от процессов, описанных на сх.4, в этом случае вводимый заместитель
располагается в экваториальном, а карбоксамидная группа в аксиальном положении.
Причиной этого мы считаем больший объем вводимого фрагмента по сравнению с
оксимом ацетальдегида, а тем более объемнее, чем гидроксильный заместитель. Так
как карбоксамидная группа в полученном соединении занимает аксиальное
положение, то взаимодействие ее с вицинальной нитрильной группой не возможно. В
дальнейшем отщепление нитрила для оксима кетона не возможно, поэтому реакция
заканчивается на стадии образования
2-алкил-5,5-диалкил-6-алкилиденаминоокси-3,3,4-трицианотетрагидро-2H-пиран-4-карбоксамидов
(4а,б).
Строение соединений 4a,б было
установлено по данным ИК, масс, ЯМР 1Н спектроскопии (табл. 4). В ИК-спектрах
соединений 4a,б присутствуют полосы поглощения С=N связи при 1690 см-1 , при
1725 см-1 С=О связи карбоксамидной группы, при 2260 см-1 несопряженных
нитрильных групп, а широкая полоса поглощения связей N-H при 3170, 3300 и 3415 см-1.
Масс-спектр соединения 4 представлен
молекулярным ионом [М]+ 3-10%, дальнейший распад которого происходит с потерей
оксимного фрагмента [М-NСR2]+ 5-12%, затем и изоалкильного фрагмента
[М-NСR2-CHR2]+ 5-15%.
Спектр ЯМР 1Н соединений 4
представлен двумя синглетами с δ 7.8-7.6 м.д. и 7.6-7.4 м.д.
карбоксамидной группы (2Н), синглетом с δ 5.1-4.9 м.д.
O-CH-O группы (1Н), дуплетом с δ 4.6-4.4 м.д. O-СH-СН группы (1Н),
мультиплетом с δ
2.4-2.3
м.д O-СН-СН(Alk)2 группы (1Н) и сигналами протонов алкильных заместителей.
|
Таблица
3. ИК и ЯМР 1Н спектры соединений 4а,б
|
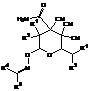
|
|
Соедине-ние
|
R1
|
R2
|
R3,
R4
|
ИК
спектр, см-1
|
Спектр
ЯМР 1Н (ДМСО-d6), d, м.д.
|
|
|
|
|
n N-H
|
n CºN
|
n C=O, C=N
|
|
|
4а
|
Me
|
Me
|
Me,
Et
|
3170,
3300, 3415
|
2260
|
1700,
1725
|
7.66
с (1Н, С(O)NH2), 7.47 с (1Н, С(O)NH2), 4.91 с (1Н, O-CH-O), 4.43 д (1Н,
J=10.98 Гц, O-СH-СН), 2.41 м (1Н, J=6.71, 10.37 Гц, O-СН-СН(СН3)2), 2.26 к
(2Н, J=7.32 Гц, N=CCH2CH3], 1.87 с (3Н, N=C-CH3), 1.28 с (3Н, CH3), 1.17 с
(3Н, CH3), 1.16 д (3Н, J=6.71 Гц, O-СН-СН(СН3)2), 1.04 д (3Н, J=6.71 Гц,
O-СН-СН(СН3)2), 1.03 т (3Н, J=7.32 Гц, N=CCH2CH3)
|
|
4б
|
Et
|
Et
|
Me,
Me
|
3170,
3300, 3415
|
2260
|
1700,
1725
|
7.76
с (1Н, С(O)NH2), 7.6 с (1Н, С(O)NH2), 5.06 с (1Н, O-CH-O), 4.6 д (1Н,
O-СH-СН), 2.36 м (1Н, O-СН-СН(СН3)2), 1.9 с (6Н, N=C(CH3)2), 1.8-1.5 м (8Н,
4CH2), 0.95-0.8 м (12Н, 4 CH3)
|
|
|
|
|
|
|
|
|
|
.Экспериментальная часть
Контроль полноты протекания реакций и чистоты
синтезированных соединений проводили методом тонкослойной хроматографии (ТСХ)
на пластинках “Silufol UV-254”, проявитель - УФ-облучение, пары иода,
термическое разложение. ИК спектры снимали на приборе UR-20 в слое вазелинового
масла. Спектры ЯМР записывали на спектрометре Bruker DRX500 с рабочей частотой
для ЯМР 1Н - 500,13 МГц, а для ЯМР 13С - 125.76 МГц, растворитель - ДМСО-d6.
Масс-спектры снимали на приборе Finnigan mat.incos 50 (электронный удар 70eV).
Параметры элементарных ячеек и интенсивности отражений для рентгеноструктурного
анализа измеряли на дифрактомерах Enraf-Nonius CAD-4 и Bruker SMART 1000 CCD.
Все расчеты проведены на ЭВМ по программе SHELXTL97. Молекулярная графика по
программам DIAMOND (Brandenburg 2000) и ORTEP-3 (Farrugia, 1997).
Квантово-химические расчеты проводились с помощью Gaussian98 (Frisch, 1998) в
B3LYP/6-311G** приближении.
Синтез тетрацианоэтилена
(Этентетракарбонитрил)
тетрацианоэтилен альдегид
карбонильный реакция
4CH2(CN)2 + 8Br2 + KBr → KBr[Br2C(CN)2]4 +
HBr[Br2C(CN)2]4 + 4Cu → 2(CN)2C=C(CN)2 + 4CuBr2 + KBr
А. В колбу, помещенную в баню со льдом и водой,
добаляли 900 мл холодной воды, 99 г (1,5 моля) нитрила малоновой кислоты и 75 г
(0,63 моля) бромистого калия, постоянно при этом перемешивая. При температуре
смеси 5-10°С в течение 2,5 ч приливали 488 г (158 мл, 3,05 моля) брома.
Перемешивание продолжали еще 2 часа, придерживая при этом температуру 5-10°С.
Выпавший твердый комплекс отфильтровывали на воронке Бюхнера, промывали 150 мл
ледяной воды. Зернистый препарат сушили до постоянного веса в
вакуум-эксикаторе. Выход 88%.
В. К смеси 254 г (0,25 моля) комплекса
диброммалонинитрила и бромистого калия и 1 л сухого бензола прибавляли 100 г
(1,57 г-атома) осажденной порошкообразной меди. Смесь кипятили в течение 10
часов, при этом не прекращали перемешивание. Затем в горячем состоянии
фильтровали ее через складчатый бумажный фильтр. Фильтрат выпаривали до объема
около 350 мл. Кристаллы фильтровали с отсасыванием, промывали двумя порциями по
25 мл холодного бензола, сушили в вакуум-эксикаторе. Выход 62%. Тпл=197-199°С.
Синтез
3,8-диалкил-6-имино-2,7-диоксабицикло[3.2.1]октан-4,4,5-трикарбонитрилов
(2а,б).
К раствору 0.64 г (0.005 моль) тетрацианоэтилена
в 10 мл 1,4-диоксана добавляли 0.01 моль соответствующего альдегида (1а,б) и
одну каплю концентрированного раствора хлороводородной кислоты. После
завершения реакции (ТСХ, проба с гидрохиноном) реакционную массу разбавляли
водой, выделившийся осадок отфильтровывали, промывали водой.
Перекристаллизовывали из 2-пропанола.
Выходы, т. пл., время реакции, данные
элементного анализа приведены в таблице 4.
Таблица 4. Время реакции, выходы, т.пл. соединений
2а,б.
|
Соединение
|
Время
реакции
|
Выход,
%
|
Т
пл. °С
|
|
|
|
|
|
2а
|
7-14
д
|
38
|
72
|
|
2б
|
1,5-3
ч
|
58
|
103
|
6-[1-(гидроксиламино)этокси]-3-имино-4,7,7-триалкил-1-оксатетрагидропирано[3,4-c]пиррол-3a,7a(1Н,4Н)-дикарбонитрил.
(3а,б).
.25 мМоль диоксобицикла 2а,б растворяли в 0.1 мл
ацетальдоксима. Через 5-6 ч реакционную массу разбавили водой, выделившиеся
осабок отфильтровывали, промывали водой. Перекристаллизовывали из ацетонитрила.
Выходы, т. пл., данные элементного анализа
приведены в таблице 6. Данные ИК и 1Н ЯМР спектроскопии приведены в таблице 2
-алкил-5,5-диалкил-6-алкилиденаминоокси-3,3,4-трицианотетрагидро-2H-пиран-4-карбоксамид.
(4а,б)
Выходы, т. пл., данные элементного анализа
приведены в таблице 7. Данные ИК и 1Н ЯМР спектроскопии приведены в таблице. 3
Таблица 5. Выходы, т.пл. соединений 3а,б
|
Соединение
|
Выход,
%
|
Т
пл. °С
|
|
3а
|
64
|
170-3
|
|
3б
|
52
|
180-1
|
Таблица 6. Выходы, т.пл.соединений 4а,б.
|
Соединение
|
Выход,
%
|
Т
пл. °С
|
|
4а
|
65
|
140-1
|
|
4б
|
76
|
168-9
|
Выводы:
1.Показали, что при реакции
3,8-диалкил-6-имино-2,7-диоксабицикло[3.2.1]октан-4,4,5-трикарбонитрилов с
избытком оксима проходит с раскрытием дигидрофуранимидного фрагмента.
.Установлено, что взаимодействие
3-алкил-6-имино-8,8-диалкил-2,7-диоксабицикло[3.2.1]-
октан-4,4,5-трикарбонитрилов с избытком оксима приводит к образованию 6-[1-(гидроксиламино)этокси]-3-имино-4,7,7-триалкил-1-оксатетрагидропирано[3,4-c]пиррол-3a,7a(1Н,4Н)-дикарбонитрилов.
.Выяснили, что при взаимодействии
3-алкил-6-имино-8,8-диалкил-6-имино-2,7-диоксабицикло[3.2.1]октан-4,4,5-трикарбонитрила
с оксимами кетонов в среде ацетонитрила происходит образование
2-алкил-5,5-диалкил-6-алкилиденаминоокси-3,3,4-трицианотетрагидро-2H-пиран-4-карбоксамидов.
Метрология
Метрология - наука об измерениях, методах
достижения их единства и требуемой точности. Все технические средства, с
помощью которых выполняются измерения, называются измерительной техникой.
Метрологическая служба представляет собой сеть
государственных метрологических органов, задачами которых является обеспечение
единства измерений и единообразия средств измерения в стране.
Метрологическая служба призвана осуществлять
стандартизацию единиц физических величин, их воспроизведение с помощью
государственных этанолов, передачу размеров единиц средствами измерения,
государственные испытания новых образцов средств измерений, надзор за
соблюдением стандартов и качеством выпускаемой продукции, за эксплуатируемыми
средствами измерений путем их периодической проверки и ревизионного контроля,
метрологическую экспертизу стандартов, нормативно-технической и проектной документации.
Для достижения единства измерений необходимо
производить правильную градуировку и периодическую проверку всех средств
измерений. Все приборы, инструменты, использованные при выполнении данной
работы, соответствуют утвержденным ГОСТам. Приборы, находящиеся в лаборатории,
прошли проверку в I, II кварталах текущего года. Работы по определению
физико-химических параметров проводились согласно утвержденным ГОСТам и
инструкциям.
|
Измеряемая
величина
|
Предел
допустимых погрешностей
|
Количественный
показатель погрешности
|
Наимено
-вание прибора
|
Нормированная
метрологическая характеристика
|
Средство
обработки результатов измерений
|
|
Масса
1 - 200, г
|
±
0,005
|
±
0,0001
|
ВЛА
200 Г - М
|
Точность
измерения массы
|
Разновесы
|
|
Масса
1 - 500, г
|
±
0,005
|
±
0,05
|
ВЛК-
500
|
Точность
измерения массы
|
Шкала
|
|
Длина
волны ИК-спектров поглощения, 400 - 4000,см-1
|
±
0,005
|
-
|
ИР
- 20
|
Точность
измерения длины волны
|
Кювета
из кристаллов KBr, LiF
|
|
Показатель
преломления
|
±
0,0001
|
±
0,0001
|
Рефракто-метр
ИРФ 4546
|
Точность
измерения показателя преломления
|
Шкала
|
|
Температура,
оС
|
±
0,5
|
±
0,5
|
Термометр
|
Точность
измерения температуры
|
Шкала
|
Техника безопасности
Выполнение правил техники безопасности играет
значительную роль при выполнении работ в химической лаборатории. Работа часто
связана с некоторой опасностью, вызываемой потребностью применять в ходе
синтезов едкие, ядовитые, раздражающие, канцерогенные, пожаро- и взрывоопасные
вещества, из чего следует необходимость знания физико-химических свойств
используемых в работе веществ и правил техники безопасности.
Многие нитрилы очень ядовиты, особенно нитрилы
алифатического ряда предельных кислот с малыми молекулярными массами.
Токсичность цианосодержащих соединений зависит от их превращений в организме,
ведущих к освобождению синильной кислоты. Нитрилы вызывают тканевое удушие
вследствие связывания нитрильной группы с одним из дыхательных ферментов. В
первый момент решающим оказывается кислородное голодание тканей, в дальнейшем
могут возникнуть изменения, развивающиеся в центральной нервной системе после
перенесенного отравления. Многие нитрилы подвергаются гидролизу в кислой среде
с выделением циановодорода, бурное выделение которого возможно при прямом
контакте растворов кислот с нитрилами, а так же в ряде синтезов с замещением
CN-группы.
Для нитрилов характерна способность всасываться
через кожу, вызывая при этом отравление организма. При отравлениях цианистым
водородом высоких концентраций почти мгновенно теряется сознание, наступает
паралич дыхательного центра, сердечных мышц и в результате наступает смерть.
При отравлении цианистым водородом в небольших концентрациях наблюдается
жгуче-горький вкус во рту, слюнотечение, мышечная слабость, затруднение речи,
острая головная боль.
Нитрилосодержащие соединения должны храниться в
вытяжных шкафах в плотно закрытых банках. Все работы должны производиться
только при хорошо работающей вентиляции. Со всеми неизвестными нитрилами надо
обращаться, как с ядами. Переливание нитрилов, мытье посуды и уничтожение
остатков производить только в резиновых перчатках.
Особую осторожность необходимо соблюдать при
обращении с электрическим током, так как его действие на живую ткань носит
своеобразный и разносторонний характер. Проходя через организм, электрический
ток оказывает термическое, электролитическое и биологическое действия. Чтобы
избежать электротравматизма, корпусы электродвигателей, трансформаторов и
других металлических нетоковедущих частей, которые могут оказаться под
напряжением, должны быть заземлены.
В лаборатории должны быть необходимые средства
пожаротушения: ящик с песком, асбестовое одеяло и огнетушители типа ОУ - 5.
Все работы должны проводиться под вытяжным
шкафом.
Легковоспламеняющиеся жидкости (диэтиловый эфир,
ацетон, спирт) нельзя перегонять на открытом огне. Переливать их из одной
посуды в другую можно лишь при выключенных электроплитках. При перегонке
органических веществ, при отгонке растворителя и других работах, связанных с
нагреванием при атмосферном давлении, не допускается работа в герметично
закрытых сосудах. При проведении вакуумной перегонки необходимо работать в
защищающих глаза очках или маске из органического стекла.
Многие работы в лабораториях требуют применения
термометров и манометров. Необходимо знать правила безопасной работы с этими
приборами, а в случае боя знать методы и средства сбора и нейтрализации
пролившейся ртути.
Обязательно наличие в лаборатории средств первой
помощи таких, как стерильные бинты и вата, сердечные средства, обезболивающие и
обеззараживающие препараты.
Вопросы экологии
Экологические исследования, проведённые в последние
десятилетия во многих странах мира, показали, что всё возрастающее
разрушительное воздействие антропогенных факторов на окружающую среду привело
её на грань кризиса. Среди различных составляющих экологического кризиса
(истощение сырьевых ресурсов, нехватка чистой пресной воды, возможные
климатические катаклизмы и т. д.) наиболее угрожающий характер приняла проблема
загрязнения незаменимых природных ресурсов - воздуха, воды, почвы - отходами
промышленности и транспорта.
В связи с этим в современном обществе резко
возрастает роль и задачи технической экологии, призванной на основе оценки
степени вреда, приносимого природе индустриализацией производства,
разрабатывать и совершенствовать инженерно-технические средства защиты
окружающей среды, всемерно развивать основы создания замкнутых и безотходных
технологических циклов и производств.
Важное место в деле охраны окружающей среды
отводится воспитанию всех членов общества, в том числе и инженерно-технических
кадров, в духе бережного отношения к окружающей среде.
Гражданская оборона
Гражданская оборона представляет собой систему
общегосударственных оборонительных мероприятий, направленных на защиту
населения, создание необходимых условий работы объектов народного хозяйства в
военное время, а в случае применения противником оружия массового поражения -
на проведение спасательных работ.
В военных условиях важное значение для целей
разведки имеет объективное восприятие химического оружия. Различают следующие
виды восприятия и ощущения: раздражение органов дыхания, глаз и кожи, ощущение
запаха и вкуса, обнаружение тумана в воздухе и капель ОВ на растительности и
почве.
В связи с появлением в конце 1945 года различных
фосфорорганических ОВ, обладающих высокой токсичностью, распознать ОВ по запаху
стало невозможно. Такие вещества, как зарин, зоман, V-газы и другие даже в
очень малых концентрациях токсичны. Для обнаружения ОВ высокой токсичности
пользуются только объективными методами индикации. В полевых условиях для
быстрого обнаружения и определения ОВ на различных поверхностях и их паров в
воздухе имеются разнообразные методы: применение индикаторных порошков,
карандашей, бумаг и другое.
Высокая токсичность БОВ и их способность
проникать через неповрежденную кожу вынуждают применять индивидуальные средства
защиты органов дыхания и кожных покровов.
Для проведения дегазации нужны средства,
способные поглощать или нейтрализовать ОВ, переводя их в простые нетоксичные
вещества. К средствам дегазации относятся моющие, адсорбирующие соединения и
другие. Для грамотного проведения дегазации необходимо оперативно и точно
определить ОВ.
Список литературы
Граник
В.Г. Основы медицинской химии. М.: Вузовская Химия. -2001. -384 с.
Анцеферов
В.Н., Бездудный Ф.Ф. и др. Новые материалы / под. науч. ред. Ю.С.Карабасова.
М.: МИСИС. -2002. -736 с.
Гусев
А.И. Нанокристаллические материалы: методы получения и свойства. Екатиринбург:
УрО РАН -1998. -199 с.
Смит
В., Бочков А., Кейпл Р. Органический синтез. Наука и искусство. М.: Мир. -2001.
-572 с.
Cairns
T.L., McKusick B.C. Cyankolenstoffchemie // Angew. Chem.
-1961. -Bd. 73. -S. 30-35.
Ремон
Ж. Новое семейство органических соединений - циануглеводороды // Усп. химии.
-1962. -Т.31. -С.1257-1264.
Винклер
Р. Химия тетрацианоэтилена // Усп. химии. -1963. -Т. 31. -С. 1525-1536.
Kuban
V., Janak J. Molecularni komplexy tetracyanoethyleny // Chem. Listy. -1969.
-Sv.63. -S.639-678. E., Linn W.J., Webster O.W. Cyanocarbon and
polycyanocompaunds // The Chemistry of the cyano group / Ed. Z.Rappoport.
London: Intersc. Pupl. -1970. -Ch. 9. -P. 423-638.
Зильберман
Е.Н. Реакции нитрилов. М.: -Химия. -1972. -448 с.
Зефиров
Н.С., Махонькое Д.И. Успехи химии пернитрилов // Усп. химии. -1980. -Т. 49. -С.
637-678.
Fatiadi
A.J. New applications of the tetracyanoethylene in organic chemistry //
Syntesis. -1986. -N 4. -P. 249-284.A.J. Addition and cycloaddition reaction of
tetracyanoethylene in organic chemistry // Syntesis. -1987. -N 9. -P.
749-789.F. Reactions of Malononitrile Derivatives // Syntesis. -1987. -N 12.
-P. 925-954
Шаранин
Ю.А., Гончаренко М.П., Литвинов В.П. Взаимодействие карбонильных соединений с α,β-нередельными
нитрилами - удобный путь синтеза карбо- и гетероциклов // Успехи химии. -1998.
-Т.67 -Вып.5. -С.442-472.
Гудман
М., Морхауз Ф. Органические молекулы в действии. М.: Мир. -1977. -С. 12-13.
Каюков
Я.С. Синтез полицианозамещенных гидрированных производных пиридина
взаимодействием 4-оксоалкан-1,1,2,2-тетракарбонитрилов с
1,3,5-триарил-2,4-диаза-1,4-пентадиенами и изучение их свойств // Автореф. дис.
канд. хим. наук. - Москва.- 1997.- 22с.
Ершов
О.В. Взаимодействие тетрацианоэтилена с a,b-непредельными,
b-гидрокси-
и a-хлоркетонами.
// Автореф. дис. канд. хим. наук.- Чебоксары. -2000. -21с.
Булкин
В.В. Синтез, реакционная способность и биологическая активность
тетрацианоциклоалканов // Автореф. дис. канд. хим. наук.- Чебоксары.- 2004.-
21с.
Чернушкин
А.Н. Синтез и свойства 4-оксоалкан-1,1,2,2-тетракарбонитрилов // Автореф. дис.
канд. хим. наук.- Москва.- 2006.- 21с.
Николаев
А.Н. Синтез и превращения
6,6-диметил-5,7-диоксо-4,8-диоксаспиро[2.5]октан-1,1,2,2-тетракарбонитрилов //
Автореф. дис. канд. хим. наук. -Москва. -2006. -21с.
Лыщиков
А.Н., Насакин О.Е., Шевердов В.П. и др. Противоопухолевая активность
производных полинитрилов // Хим.-фарм. журнал. -2000. -Т.34. -N 4 -C. 11-23
Junek
H., Fischer-Colbrie H., Anigner H., Braun A.M. Synthesen mit Nitrilen.
Phenylhydrazone des Dicyanmethylenindandions: Struktur und Farbe// Helv. Chem.
Acta. -1972. -Vol. 55. -P.1459-1466. V.A., Nikolaev A.N., Peschar R., Kajukova
O.V., Schenk H, Aslanov L.A. N-methylpyridinium
3-cyano-4-(dicyanomethylene)-5-oxo-4,5-dihydro-1H-pyrrol-2-olate // Acta
Crystallogr. -2004. -С60.
-o297 -o299. V.A., Peschar R., Kajukova O.V., Schenk H., Aslanov L.A.
N-Methylpyridinium 3-cyano-4-(dicyanomethylene)-5-oxo-4,5-dihydro-1H-pyrrol-2-
olate // Acta Crystallogr. -2004. -С60.
-o62-o64. V. A., Peschar R., Kajukov Y. S., Kornilov K. N., Aslanov L. A..
Ammonium 3-cyano-4-(dicyano- methylene)-5-oxo-4,5-dihydro-1H- pyrrol-2-olate
monohydrate // Acta Cryst. -2005. -C61. -o366-o368G., De Lucchi O., Fabris F.,
Lucchini V., Pasqualotti M., Zambon A. Synthesis of the syn and anti isomer of
1,4,5,8,9,12-hexahydro-2,3,6,7,10,11-hexamethylidene-1,4:5,8:9,12-trimethanotriphenylene
and Diels-Alder reactivity of the syn isomer // Tetrahedron Letters. -2003.
-Vol. 44. -P. 561-563.K., Kohler F., Meier B. Synthesis and reactions of the
first cyclopentadienyl isonitriles // Tetrahedron Letters. -2003. -Vol. 44. -P.
3781-3783.R., Tappanchai S., Bandmann H. a(E)-1-Methoxy-1,3-butadiene and
1,1-dimethoxy-1,3-butadiene in (4 + 2) cycloadditions. A mechanistic comparison
// J. Am. Chem. Soc. -1996. -Vol. 118. -P. 12555-12561J.K., Wiley D.W.,
McKusick B.C. Cyanocarbon chemistry. 19. Tetracyanocyclobutanes from
tetracyanoethylene and electron-rich alkenes // J. Am. Chem.
Soc.-1962.-Vol.84.-P.2210-2215.P.D. Mechanisms of cycloaddition // Q. Rev.
Chem. Soc. -1970. -Vol. 24. -P.473-497.G., Huisgen R. Tetracyanoethylene and enol
ethers. Rates of 2+2 => 4 cycloadditions and structural variation of the
enol ether // Tetrahedron Letters. -1973. -Vol. 13. -N 39. -P.3763-3768.G.,
Huisgen R. 2+2 => 4 cycloadditions of tetracyanoethylene to enol ethers;
activation parameters as mechanistic criteria // Tetrahedron Letters. -1973.
-Vol. 13. -N 39. -P.3769-3772.G., Huisgen R. Tetracyanoethylene and enol
ethers. Dependence of cycloaddition rate on solvent polarity // J. Am. Chem.
Soc. -1973. -Vol. 95. -P.5056-5058R. Tetracyanoethylene and enol ethers. A
model for 2 + 2 cycloadditions via zwitterionic intermediates // Acc. Chem.
Res. -1977. -Vol.10. -№4. -P.117-124.R. Can tetramethylene intermediates be
intercepted? // Acc. Chem. Res. -1977. -Vol. 10. -P.199-206.D., Reuman M. E.,
Rogic M. M. Ene-type reaction through the intermediacy of the 1,4-dipolar ion
in the reaction of tetracyanoethylene with nucleophilic double bonds in liquid
sulfur dioxide // J. Org. Chem. -1980. -Vol. 45. -№ 23. -P.4602-4605.N., Padias
A.B., Hall H.K. Zwitterionic tetramethylenes as the common intermediates in the
cycloaddition and polymerization reactions of n-vinylcarbazole with
electrophilic tetrasubstituted ethylenes: a new explanation for
"charge-transfer" initiation // J. Am. Chem. Soc. -1986. -Vol. 108.
-P.4920-4931 .E.L., Lewis K.K. The unexpected regioselectivity in the
singlet oxygen cycloadditions to electron-rich 1,3-butadienes // J. Am. Chem.
Soc. -1987. -Vol. 109. -N. 8. -P.2475-2478.H., Sharon O., Frimer A.A.
Surprising exocyclic regioselectivity in electrophilic additions to
alkylidenecyclobutenes // Tetrahedron. -2002. -Vol. 58. -P.3199-3205.G.,
Orfanopoulos M. Remote ε-secondary
isotope effect in the reaction of tetracyanoethylene with
2,5-dimethyl-2,4-hexadiene. A step-wise mechanism // Tetrahedron Letters.
-1996. -Vol. 37. -P.3075-3078.R., Steiner G. Nonstereospecifity in [2+2]
cycloadditions of tetracyanoethylene to enol ethers // J. Am. Chem. Soc. -1973.
-Vol.95. -P.5054-5055.R., Steiner G. Reversibility of zwitterion formation in
the [2 + 2] cycloaddition of tetracyanoethylene to enol ethers // J. Am. Chem.
Soc. -1973. -Vol. 95. -P.5055-5056.J., Flippen J., Huisgen R., Schug R. [2+2]
Cycloaddition of tetracyanoethylene to enol ethers. Structure of the product of
interception with alcohol // J. Am. Chem. Soc. -1975. -Vol. 97. -P.
5285-5287.R., Schug R., Steiner G. Trapping of the 1,4-dipole formed in the 2 +
2-cycloaddition of tetracyanoethylene to enol ethers // Angew. Chem. Int. Ed.
Engl. -1974. -Vol. 13. -N 1. -P.80-81.R., Huisgen R. 1,4 -Dipolar cycloadditions
as trapping reactions for zwitterionic intermediates of 2 +2 cycloadditions //
J. Chem. Soc. Chem. Commun. -1975. -P.60-61.W.I., Heckert R.E., Little E.L.,
Krespas C.G. Cyanocarbon chemistry. III. Addition reactions of
tetracyanoethylene // J. Am. Chem. Soc. -1958. -Vol. 80. -N 11. -P.
2783-2788.W.I. Alpha-(1,1,2,2-tetracyanoetyl)-ketones and their preparation //
U.S. Patent 2,762,837 (1956).
Николаев
Е.Г. Синтез, реакционная способность и биологическая активность
тетрацианэтилированных кетонов и их производных // Автореф. дис. канд. хим.
наук. - Москва. -1985. -23с.
Николаев
Е.Г., Насакин О.Е., Терентьев П.Б., Хаскин Б.А., Петров В.Г. Взаимодействие
тетрацианоэтилена c метил(алкил)кетонами // Журн. органич. химии. -1984. -Т.
20. -Вып. 1. -С.205-206.
Fatiadi
A.J. New application of malononitrile in organic chemistry - part I //
Synthesis. -1978. -P.165-204. A.J. New application of malononitrile in organic
chemistry - part II // Synthesis. -1978. -P.241-282.
Насакин
О.Е., Кухтин В.А., Петров В.Г., Николаев Е.Г., Алексеев В.В., Сильвестрова С.Ю.
Способ получения b,b,g,g-тетрацианокетонов
// А.С. 759507 (1979). -Б.И. -1980. -№32.
Насакин
О.Е., Николаев Е.Г., Терентьев П.Б., Булай А.Х., Лаврентьева И.В. Синтез
замещенных пиридинов взаимодействием тетрацианоэтилированных кетонов с
хлористо- и бромистоводородными кислотами // ХГС. -1987. -№8. -С.653-656
Насакин
О.Е., Лукин П.М., Николаев Е.Г. Химия полицинсодержащих соединений. Чебоксары:
ЧГУ. -1985. -44 c.
Шевердов
В.П., Ершов О.В., Насакин О.Е., Чернушкин А.Н., Ефимов Р.Н., Тафеенко В.А.
Тетрацианоэтилирование циклододеканона и дигидроэпиандростерона до β,β,γ,γ-тетрацианоалканонов
и их взаимодействие с акролеином // Журн. общ. химии. -2002. -Т.72. -Вып.5.
-С.877-878.
Клемон
Д.П. Синтез и реакции производных 4-оксо-4,5,6,7-тетрагидроиндола // Автореф.
дис. канд. хим. наук. -М. -1984. -24с.
Wolfbeis
O.S., Zacharias G., Junek H. Die Reactionen von 2-Indanon mit Malonitrile bzw.
Cyanessigester und Tetracyanoathylen // Monatsh. Chem. -1975.
-Bd. 106. -S. 1207-1212.
Шевердов
В.П., Ершов О.В., Насакин О.Е., Чернушкин А.Н., Тафеенко В.А. Взаимодействие
тетрацианоэтилена с 2-замещенными циклогексанонами // Журн. органич. химии.
-2002. -Т.38. -Вып. 7. -C. 1043-1046.
Lown
J.W., Koganty R. R. Formation of novel 1,2-oxathietanes from 2-chloroethyl
sulfoxide precursors and their reactions in solution, including formal [ σ2s
+ σ
2a] cycloreversions and rearrangements // J. Am. Chem. Soc. -1986. -Vol. 108.
-P.3811-3818.
Насакин
О.Е.,
Николаев
Е.Г.,
Терентьев
П.Б.,
Булай
А.Х.,
Хаскин
Б.А.,
Дагер
К.
Взаимодействие
тетрацианэтилированных
кетонов
с
альдегидами.
Синтез
3-имино-2,6-диоксабицикло-[2,2,2]октанов // ХГС. -1984. -N. 11. -С.1462-1466.
Каюков
Я. С., Лукин П.М., Насакин О.Е., Хрусталев В.Н., Нестеров В.Н., Шевердов В.П.
Уточнение структуры продуктов взаимодействия
4-оксоалкан-1,1,2,2-тетракарбонитрилов с альдегидами // ХГС. -1997. -N 4. -С.
497-499.
В.
А. Смит, М. И. Лазарева, Р. Кэйпл. Методология «сборки» полифункциональных
соединений из простых предшественников на основе контролируемой
последовательности трех AdE реакций. Общность, механизм, стереохимия // Рос.
хим. ж. (Ж. Рос. хим. об-ва им. Д.И.
Менделеева).
-2001. -Т.
XLV. -N. 4. -C.3-14.
Но
Т.-L.
Таndеm
rеасtions
in organic synthesis // N.Y. Wiley-Interscience. -1992.P.A., Miller B.P.
Organic synthesis: theory and applications. Ed. T. Hudlicky. Greenwich: JAP
Press, CT. -1993. -Vol. 2. -P. 27.P. Cojugate addition reactions in organic
synthesis. Tetrahedron Organic Series. Oxford: Pergamon. -1992. -373 р.F.H.,
Kennard O., Watson D.G., Brammer L., Orpen A.G., Taylor R. Tables of bond
lengths determined by X-ray and neutron diffraction. Part 1. Bond lengths in
organic compounds // J. Chem. Soc. Perkin Trans 2. - 1987. -P.S1-19.
Шевердов
В.
П.,
Ершов
О.
В.,
Еремкин
А.В.,
О.Е.
Насакин,
Бардасов
И.Н.,
Тафеенко
В.А.
Синтез
4-формил-3-циклопентен-1,1,2-трикарбонитрилов.
// Журн.
органич.
химии.
-2005. -Т.
41. -№ 12. -С. 1795-1801.