Использование метода полимеразной цепной реакции в реальном времени для детекции хантавирусной РНК
Использование метода полимеразной цепной реакции в реальном
времени для детекции хантавирусной РНК
В настоящее время метод полимеразной
цепной реакции (ПЦР) в реальном времени широко используется для диагностики
различных, в том числе и вирусных, заболеваний. Предлагаемая методика позволит
проводить диагностику ГЛПС за довольно непродолжительное время. Методика
включает в себя ПЦР в реальном времени, совмещенную с предварительной реакцией
обратной транскрипции вирусной РНК и построением кДНК. Особенностью методики
является проведение обеих реакций с помощью одного фермента - термостабильной
ДНК-полимеразы Thermus thermophilus, которая обладает обратнотранскрибирующей активностью в
присутствии ионов Mn І+ и полимеразной активностью в присутствии ионов MgІ+.
Башкортостан был и остается одним из
самых крупных в мире районов-очагов ГЛПС. Возбудителями ГЛПС являются вирусы
рода Hantavirus (семейство Bunyaviridae), которые подразделяются на несколько различных серотипов.
Изоляты, выделенные в Башкортостане (Tkachenko et al., 1984), относятся к серотипу Puumala, представители которого
вызывают менее тяжелые формы ГЛПС, нежели, например, серотип Hantaan. Однако, за последние
несколько десятилетий (с момента регистрации ГЛПС в 1957 г.), эпидемиологическая
картина мало изменилась. ГЛПС по заболеваемости занимает первое место среди
природно-очаговых инфекций в РФ. Число зарегистрированных случаев в отдельные
годы может достигать 20 тысяч и более, нередки летальные исходы (Морозов, 2001;
Ткаченко, Дроздов, 2002). Поэтому разработка быстрых и эффективных
диагностических тестов является актуальной проблемой.
Полимеразная цепная реакция в
реальном времени имеет несколько преимуществ перед обычной ПЦР (Klein, 2002; Tse, Capeau, 2003, Mackay, 2004):
1. возможность наблюдения за
накоплением целевого продукта в данный момент на любой из стадий реакции
амплификации
2. отсутствие постреакционных
манипуляций для детекции образования целевого продукта (электрофоретический
анализ и пр.), и, вследствие этого
. сокращение времени от
начала проведения ПЦР до получения конечного результата.
При этом, с использованием новой
термостабильной ДНК-полимеразы Thermus thermophilus (Tth-полимеразы), появилась возможность проводить построение кДНК и
последующую ее амплификацию в одной пробирке (Myers, Gelfand, 1991), опять же,
значительно сокращая время проведения реакции.
Материалы и методы
Рибоолигонуклеотид. Для постановки модельных экспериментов был синтезирован 35-членный
рибоолигонуклеотид HVIRNA (НПФ «СИНТОЛ», Москва.), соответствующий консервативному участку S-сегмента РНК хатавируса штамма CG-1820 / Уфа-83 (серотип Puumala):
’ - UGGCAUUUACAUCAAGGACAUUUCCAUACCUAAGG-3’
Праймеры. Для проведения синтеза кДНК использовался 16-членный праймер HV1, соответствующий
участку с 288 по 303 нуклеотид «+» цепи кДНК S-сегмента штамма CG-1820 / Уфа-83:
’ - TAGGTATGGAAATGTC-3’,
или соответствующий тому же участку
кДНК праймер HV1-FAM (или его 21-членный аналог HV11-FAM), меченый
флуоресцентным красителем карбоксифлуоресцеином (место модификации указано
заглавной буквой):
’ - taggTatggaaatgtc-3’ (5’ - aggcttaggTatggaaatgtc-3’).
Для последующей амплификации
полученной кДНК использовались пары праймеров HV1/HV3 и HV1-FAM/HV3-ROX соответственно. Праймер
HV3
комплементарен участку с 304 по 320 нуклеотид «+» цепи кДНК S-сегмента штамма CG1820 / Уфа-83:
’ - TGGCATTTACATCAAG-3’.
Праймер HV3-ROX комплементарен тому же
участку кДНК и мечен флуоресцентным красителем карбокси-Х-родамином:
’ - tggcaTttacatcaag-3’.
Праймеры HV1 и HV3 были синтезированы в
нашей лаборатории, праймеры с флуоресцентной меткой - НПФ «СИНТОЛ», Москва.
Ферменты. Синтез кДНК и последующая ПЦР проводились с помощью фермента
термостабильной ДНК-полимеразы Thermus thermophilus - Tth-полимеразы («Сибэнзим», Новосибирск). Важным моментом является
способность Tth-полимеразы вести обратную транскрипцию. Нужно отметить, что этой
способностью Tth-полимераза обладает только в присутствии ионов Mn І+, а для полимеразной
активности необходимы ионы MgІ+(Гребенникова и др., 1995). Поэтому, при проведении реакции,
после стадии построения кДНК в буферной системе, содержащей ионы Mn І+, в реакционную смесь
добавлялись ионы MgІ+ в достаточной для полимеразной активности фермента
концентрации.
Синтез кДНК и ПЦР в
реальном времени. Синтез комплементарной
модельному рибоолигоонуклеотиду ДНК и последующую амплификацию полученной кДНК
проводили в приборе iCycler iQ фирмы Bio-Rad (USA), в 30 мкл реакционной смеси, содержащей буфер для реакции
обратной транскрипции (1 х 50мМ Tris-HCl, pH=8,5/25єС; 100мM KCl, 0,5мM MnCl2), 0,25 ммоль смеси dNTP, 40 пкмоль каждого праймера (т.к. обе реакции идут друг за
другом, то в реакционную смесь добавляется сразу пара праймеров), 1 пкмоль
рибоолигонуклеотида и 1-2 ед. Tth-полимеразы. Критической стадией при проведении данной реакции
является стадия отжига праймера-затравки на рибоолигонуклеотидной матрице и
последующее построение кДНК. Поэтому время для проведения этих операций было
сознательно завышено и составило 5 мин. на каждую стадию: первая стадия - отжиг
праймера при 32єС - 5 мин., синтез кДНК при 50єС - 5 мин., затем в реакционную
смесь добавляли MgCl2 до конечной концентрации 10мМ и проводили вторую стадию - 25
циклов - 80єС -4 с., 32єС - 8 с. Вся реакция, включая и время на добавление в
реакционную смесь ионов MgІ+, занимает менее одного часа.
Параллельно для наглядности и
сравнения эффективности методов проводились ПЦР в реальном времени с кДНК,
полученной с помощью двух обратных транскриптаз: M-MLV-обратная транскриптаза,
фирмы «Силекс» и AMV Reverse Transcriptase, фирмы «Promega». Синтез кДНК проходил на той же самой рибоолигонуклеотидной
матрице в общем объеме 20 мкл при разбавлении ее в 10 раз. Реакционная смесь
состояла из буфера (для M-MLV - обратной транскриптазы: 1 х 70мМ Tris-HCl, pH=8,3/25єС, 16,6мМ (NH4) 2SO4, 75мM MgCl2; для AMV - обратной
транскриптазы: 1 х 25мМ Tris-HCl, pH=8,3/25єС, 25мМ KCl, 5мМ MgCl2, 0,25мМ спермидин, 5мМ DTT), 0,25 ммоль смеси dNTP, 10 пкмоль праймера HV1 или HV1-FAM (HV11-FAM), 1 пкмоль рибоолигонуклеотида и 10 ед. обратной транскриптазы.
Подготовленную смесь прогревали при 65єС в течение 2 мин, затем медленно
охлаждали до комнатной температуры и проводили синтез кДНК при 37єС в течение
30 мин. Далее брали по 1 мкл полученного раствора в качестве матрицы для ПЦР в
реальном времени со следующим режимом: 20 циклов - 32єС - 8 с., 80єС - 4 с.
Время проведения реакции: синтез кДНК - 1 час, ПЦР - 40 минут.
Результаты и обсуждение
В результате проводимых модельных
реакций обратной транскрипции и амплификации мы получали ДНК-продукты размером
32 пн, которые для наглядности анализировали в 10% полиакриламидном геле (рис.
1а). На рис. 1б представлена кривая накопления ДНК-продукта в реальном времени
в зависимости от количества циклов реакции. Видно, что количество наработанного
продукта можно было детектировать уже с 15 цикла, и далее его накопление
увеличивалось экспоненциально.
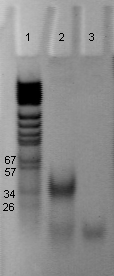

Рис. 1а Рис. 1б
Рис. 1а: Рис. 1б:
- маркер pBSK/Hpa II 1 - амплификат с
праймерами HV1/HV3
- амплификат с праймерами HV1/HV3 2 - минус-контроль
- минус-контроль
Т. к. система флуоресцентных
красителей FAM-ROX обладает большей чувствительностью, чем краситель SYBR Green I, то, хотя накопление ПЦР-продукта
начинается несколько позже (рис. 2б), оно идет быстрее, поэтому для реакции с
такими праймерами достаточно 20-22 циклов, что значительно сокращает время на
проведение анализа.


Рис. 2а Рис. 2б
- маркер pBSK/Hpa II 1 - амплификат с
праймерами HV1F/HV3R
- амплификат с праймерами HV1F/HV3R 2 - амплификат с праймерами
- минус-контроль HV11F/HV31R
- амплификат с праймерами 3 и 4 -
минус-контроль
HV11F/HV31R
- минус-контроль

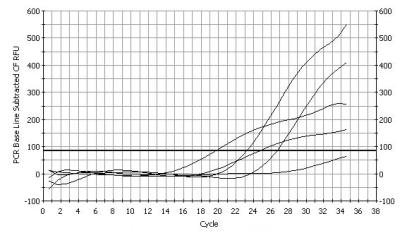
Рис. 3а, б:
и 2 - амплификаты кДНК, полученной
обратной транскриптазой M-MLV:
- с праймерами HV1F/HV3R, 2- с праймерами HV11F/HV31R
и 4 - амплификаты кДНК, полученной
обратной транскриптазой AMV:
- с праймерами HV1F/HV3R, 2- с праймерами HV11F/HV31R
- минус-контроль, 6 - маркер pBSK/Hpa II
Таким образом, проведенные модельные
эксперименты показали возможность использования Tth-полимеразы и метода
полимеразной цепной реакции в реальном времени для создания быстрого и
эффективного диагностического теста - детекции хантавирусной РНК.
Литература
полимеразный цепной
диагностика вирусный
1. Морозов В.Г.
Применение индуктора эндогенного интерферона амиксина для лечения
геморрагической лихорадки с почечным синдромом. /РМЖ - 2001, т. 9, №15, с.
656-660/.
2. Ткаченко Е.А.,
Дроздов С.Г. Хантавирусы и хантавирусные лихорадки. /Эпидемиология и
вакцинопрофилактика - 2002, №6, с. 14-18/.
. Гребенникова
Т.В., Глюков А.И., Чистякова Л.Г., Киселев В.И., Северин Е.С. Использование
термостабильной ДНК-полимеразы из Thermus thermophilus KTP в комбинированной реакции обратной транскрипции и амплификации
для детекции РНК интерлейкина 2-б и определения экспрессии гена множественной
устойчивости к антибиотикам (MDR-1). /Молекулярная биология - 1995, т. 29, №4, с. 930-941/.
4. Klein D.
Quantification using real-time PCR technology: applications and limitations.
/Trends Mol. Med. - 2002, V. 8 (6), p. 257-260/.
. Mackay
I.M. Real-time PCR in microbiology laboratory. /Clin. Microbiol. Infect. -
2004, V. 10 (3), p. 190-212/.
. Myers
T.W., Gelfand D.H. Reverse transcription and DNA amplification by a Thermus
thermophilus DNA polymerase. /Biochemistry - 1991, V. 30 (31), p. 7661-7666/.
. Tse C.,
Capeau J. Real time PCR methodology for quantification of nucleic acids. /Ann.
Biol. Clin. - 2003, V. 61 (3), p. 279-293/.