Свойства и превращения соединений производных бензольного и гетероциклического рядов
Контрольная
работа
по
органической химии
1. Приведите схему
реакции получения анилина из нитробензола. Напишите для анилина схемы следующих
реакций:
а) с уксусным ангидридом;
б) с хлороводородной кислотой;
в) с азотистой кислотой.
Получение анилина из нитробензола реакцией
Зинина (в лаборатории):
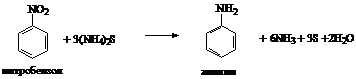
Каталитическим гидророванием
нитробензола (промышленный способ):
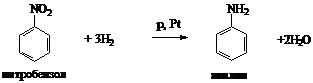
а) анилин с уксусным ангидридом (реакция
ациллирования);
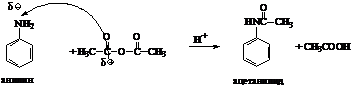
б) с хлороводородной кислотой;
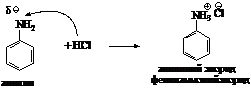
в) с азотистой кислотой (реакция
диазотирования):

. Напишите схему азосочетания
диазотированной сульфаниловой кислоты с N,N-диметиланилином. При каких
значениях рН протекает эта реакция?
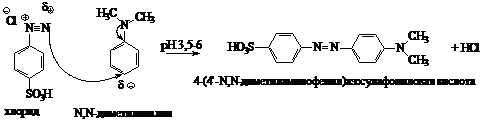
С аминами, активными в
непротонированной форме, азосочетание проводят при рН 3,5-6. Кроме того, в
кислой среде предотвращается диссоциация водорода в сульфогруппе.
. Приведите схему промышленного
получения салициловой кислоты. Охарактеризуйте свойства салициловой кислоты как
гетерофункционального соединения
В промышленности салициловую кислоту
обычно получают карбоксилированием фенолята натрия углекислым газом при 150-180
°C и давлении 5 атм (реакция Кольбе-Шмидта):
Гетерофункциональные карбоновые
кислоты - бифункциональные соединения, обладающие свойствами карбоновых кислот
и свойствами того класса органических соединений, который определяет
заместитель в углеводородном радикале.
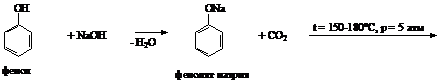
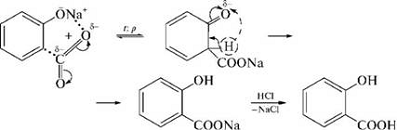
салициловая кислота
Салициловая кислота - бифункциональное
соединение, обладающее свойствами фенолов и карбоновых кислот.

В реакцию с гидрокарбонатом натрия вступает
только карбоксильная группа, и как следствие - образуется мононатриевая соль
салициловой кислоты, а при действии щелочей - динатриевая соль салициловой
кислоты.
Из-за близости функциональных групп в молекуле
салициловая кислота, в отличие от ее изомеров, взаимодействует с гидроксидом
меди (II):

С участием карбоксильной группы протекают
реакции со спиртами, галогенирующими реагентами:

При взаимодействии салициловой кислоты с
уксусным ангидридом образуется ацетилсалициловая кислота (т.е. происходит
ациллирование фенольной группы):

Салициловая кислота по кислотным свойствам
превосходит бензойную кислоту, а также о- и п-гидроксибензойные кислоты. Это
можно объяснить тем, что происходит дополнительная стабилизация салицилат-иона
за счет образования внутримолекулярной водородной связи:
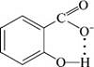
Итак, указанные химические свойства салициловой
кислоты характерны только для гетерофункциональных соединений.
4. Дайте определение таутомерии. Из предложенных
соединений - 4-гидроксибутандиовая кислота, оксобутандиовая кислота, пропанон -
выберите то, для которого возможна кето-енольная таутомерия. Приведите схему
таутомерного равновесия, назовите таутомерные формы. Напишите схемы реакций,
доказывающих наличие таутомерных форм.
Таутомерия - явление обратимой изомерии, при
которой два или более изомера легко переходят друг в друга. При этом
устанавливается таутомерное равновесие, и вещество одновременно содержит
молекулы всех изомеров (таутомеров) в определённом соотношении. Процесс такого
взаимопревращения таутомеров называют таутомеризацией. Она протекает с
обязательным разрывом одних хим. связей и образованием др. связей между атомами
одной молекулы (внутримолекулярная таутомерия) или агрегата молекул
(межмолекулярная таутомерия).
Для решения поставленной задачи рассмотрим
структурные формулы указанных соединений:

Итак, для 4-гидроксибутановой
кислоты кето-енольная таутомерия невозможна, так как гидрокси- и карбокси-
группы не проявяют подобных свойств (явление характерно для альдегидов и
кетонов).
Пропанон (ацетон) формально образует
таутомерные формы, однако их количества в растворах ничтожно малы - равновесие
практически полностью смещено в сторону кетонной формы, а содержание енольной
формы в ацетоне составляет всего 0,00025%.

Это объясняется тем, что в
соединении отсутствуют другие электроноакцепторые группы, поэтому длина
сопряжения связи, а следовательно, и устойчивость енольной формы незначительна.
Кето-енольная таутомерия в
значительной степени возможна у 2-оксобутандиовой кислоты. Это связано с тем,
что соединение обладает более длинной цепью сопряжения заряда (электронная
плотность с двойной связи углерод-углерод распределяется в том числе и на
электроноакцепторный карбоксильный атом углерода (1)), вследствие чего растет и
и термодинамическая устойчивость енольной формы (в условиях равновесия ее
количество составляет 80%). Кроме того, дополнительным стабилизирующим фактором
является образование водородной связи между водородом гидроксигруппы и атомом
килорода карбоксильной группы.

. Приведите структурные формулы
фурана и пиримидина с нумерацией атомов в циклах. Перечислите все условия, по
которым эти соединения удовлетворяют критериям ароматичности. Выделите и
изобразите электронное строение атомов азота пиррольного и пиридинового типов.
Сравните реакционную способность пиримидина и фурана в реакциях электрофильного
замещения. Приведите схему бромирования фурана.
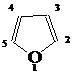 - фуран
- фуран
 - пиримидин
- пиримидин
Рассмотрим критерий ароматичности. Ароматичной
может называться ненасыщенная циклическая молекула, если все атомы цикла входят
в полностью сопряженную систему таким образом, что в основном состоянии все π-электроны
располагаются только на связывающих молекулярных орбиталях аннулярной
(замкнутой) оболочки.
Итак, фуран- гетероароматическое соединение,
свойства которого определяются наличием кольцевого секстета π-электронов,
образованных 4 π-электронами
двух связей С=С и неподеленной электронной пары гетероатома; другая
неподеленная пара электронов атома кислорода остается свободной и может
участвовать в образовании оксониевых соединений. Молекула ненасыщенна, имеет
сопряженную устойчивую систему.
Для пиримидина, подобно пиридину, характерна 6π-электронная
сопряженная ароматическая система, образованных 2 π-электронами
связи С=С и 4 π-электронами двух
связей С=N. Поэтому его цикл
обладает повышенной устойчивостью. Пиримидин содержит в своей структуре два
пиридиновых атома азота.
Выделим атомы азота пиридинового типа в
пиримидине.
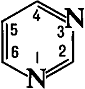
В пиридине на s-орбитали
располагается неподелённая пара электронов, не участвующая в образовании
связей. Из трёх электронов, располагающихся на рх, ру, рzорбиталях,
два участвуют в образовании сигма-связей с атомом углерода, а один - в
образовании шестиэлектронной π-системы:

Следовательно, данная система
является электронодифицитной.
В пирроле: на s-орбитали
располагается электрон, участвующий в связи с атомом водорода. Из четырёх
электронов, располагающихся на рх, ру, рz-орбиталях,
два участвуют в образовании сигма-связей с атомом углерода, а оставшиеся два
(неподелённая пара) - в образовании шестиэлектронной ароматической π-системы:
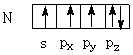
Следовательно, данная система
является электрононасыщенной.
Для фурана, являющегося электрононасыщенным
соединением из-за наличия в ароматической системе неподеленной электронной пары
с атома кислорода, характерны реакции электрофильного замещения:
галогенирование, нитрование, сульфирование, ацилирование, меркурирование и др,
протекающие в мягких условиях. Повышенная реакционная способность фурана в
сравнении с пиримидином связана с положительным мезомерным эффектом гетероатома.
С одной стороны, он приводит к появлению
частичного отрицательного заряда на атомах углерода в составе гетероцикла и
обуславливает большее сродство к электрофилу, а с другой стороны, приводит к
более эффективной стабилизации катионного интермедиата этой реакции - π-комплекса
и, следовательно, к снижению энергии переходного состояния реакции.
Реакционная способность в реакциях
электрофильного замещения у электронодефицитного (как видно из вышесказанного)
пиримидина значительно ниже, чем у фурана из-за снижения электронной плотности
в положениях 2, 4, 6, вызванного наличием двух атомов азота в цикле. Так,
пиримидин не нитруется и не сульфируется, однако в виде соли бромируется в
положение 5.
Электрофильное замещение становится возможным
только при наличии электронодонорных заместителей и направляется в наименее
дезактивированное положение 5.
анилин пиримидин барбитал папаверин
6. Сравните реакционную способность бензола и
пиридина в реакциях нуклеофильного замещения. Напишите схемы реакций пиридина со
следующими реагентами:
а) пропилхлоридом;
б) гидроксидом натрия
По каким механизмам протекают эти реакции?
Опишите механизм последней реакции
Пиридин же, напротив, в реакции нуклеофильного
замещения вступает значительно легче, чем в реакции электрофильного замещения,
потому что кольцо его значительно обеднено электронной плотностью по сравнению
с бензолом (вследствие наличия в кольце сопряжения атома азота, приводящего к
значительному перераспределению электронной плотности в сторону азота и
дефициту электронной плотности во всей системе). Введение же в систему
нуклеофила снижает дефицит электронной плотности. Для пиридина характерны
реакции ароматического нуклеофильного замещения, протекающие преимущественно по
орто-пара положениям кольца.
а) Пиридин - основание, поэтому N-алкилирование
пиридина галоидными алкилами, приводит к алкилпиридиниевым солям.
Следовательно, реакция пиридина с пропилхлоридом идет по атому азота.

б) При нагревании до 400 °С пиридин
реагирует с NaОН с
образованием α-гидроксипиридина

7. Приведите схему таутомерных
превращений барбитала, назовите таутомерные формы. Какая таутомерная форма
барбитала принимает участие в образовании соли? Приведите схему реакции
взаимодействия барбитала с гидроксидом натрия
В отличие от барбитуровой кислоты,
барбитал не способен образовывать таутомеры по механизму кето-еольной
таутомерии (так как атом углерода связан с двумя этильными группами). Поэтому
единственный тип изомерии барбитала - лактим-лактатная.
В образовании соли при
взаимодействии со щелочью принимает участие лактимная форма барбитуровой
кислоты.

8. Приведите строение папаверина. Напишите схемы
реакций взаимодействия папаверина со следующими реагентами:
а) йодоводородной кислотой при нагревании;
б) разбавленной серной кислотой.
Структурная формула папаверина
(1-(3,4-диметоксибензил)-6,7-диметоксиизохинолин) имеет
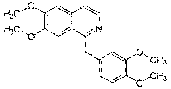
а) Реакция папаверина с йодоводородной кислотой
при нагревании:
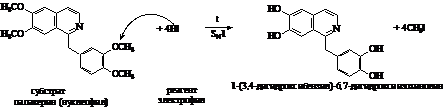
б) Реакция папаверина с разбавленной
серной кислотой:
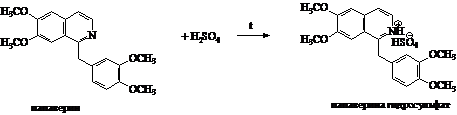
. Заполните схему превращений,
назовите продукты реакций, укажите механизмы отдельных реакций:
а)
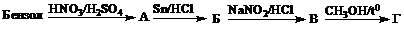
. Нитрование бензола нитрующей
смесью:
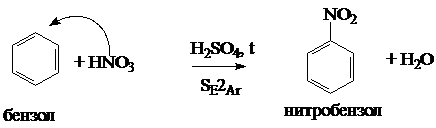
. Восстановление нитробензола до
анилина:
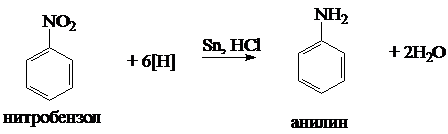
. Диазотирование анилина

. Взаимодействия
фенилдиазонийхлорида с метанолом:

б)
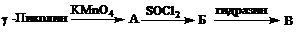
. Окисление γ-пиколина до
γ-карбоксипиридина

. Получение соответствующего
хлорангидрида

. Получение соответствующего
гидразида

Список использованной литературы
1. Березин
Б.Д., Березин Д.Б. Курс современной органической химии. Учебное пособие для
вузов. - М.: Высшая школа,2001.-768с.
2. Гауптман
З., Грефе Ю., Ремане Х. Органическая химия, Москва, "Химия", 1979,
832с.
. Левитина
Т.П. Справочник по органической химии: Учебное пособие. - СПб: «Паритет», 2002.
- 448с.
. Начала
органической химии. В 2 кн. Несмеянов А.Н., Несмеянов Н.А. М.: Изд.
"Химия", 1969. - 664с.; 1970 - 824с.
. Нейланд,
О.Я. Органическая химия: Учеб. для хим. спец.вузов.- М.:Высш.шк., 1990.- 751 с.
. Петров
А.А., Бальян Х.В., Трощенко А.Т. Органическая химия. СПб.: «Иван Федоров»,
2008. - 624 с.