|
Соединение
|
Дипольный момент, µ, [D]
|
pKBH+ 25oC
|
ЕИ [еВ] Me=Et
|
Длина связи [пм]
|
Угол [град]
|
|
|
|
|
N-H
|
N-C
|
CNH
|
HNH
|
CNC
|
|
NH3
|
|
9.245
|
|
101
|
|
|
107
|
|
|
NH2CH3
|
1,23 ←+
|
10.627
|
8,9
|
101
|
147
|
112
|
106
|
|
|
HOCH3
|
1,69 ←+
|
|
10,8
|
|
|
|
|
|
|
NH(CH3)2
|
|
10.730
|
8,0
|
100
|
146
|
112
|
|
111,8
|
|
N(CH3)3
|
|
9.81
|
|
145
|
|
|
110,6
|
|
PhNH2
|
1,53 ←+
|
4.63
|
7,7
|
100
|
140
|
|
113
|
|
|
PhOH
|
1,60 ←+
|
|
8,6
|
|
|
|
|
|
|
PhH
|
|
|
9.24
|
|
|
|
|
|
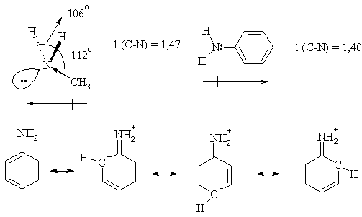
В аминах, как и в молекуле аммиака,
атом азота находится в sp3-гибридном состоянии. Аминогруппа в
алифатических аминах имеет пирамидальное строение. В ароматических аминах
аминогруппа почти плоская вследствие сопряжения несвязывающей электронной пары
и p-электронной системы бензольного кольца. Так, в анилине связь C-N короче
(140 пм), чем в метиламине (147 пм), а угол HNH (113о) больше, чем в
метиламине (106о) и аммиаке (107 о).
Молекулы аминов полярны, при этом в
алифатических аминах вектор дипольного момента направлен от углеводородного
радикала к аминогруппе, а в ароматических аминах наоборот.
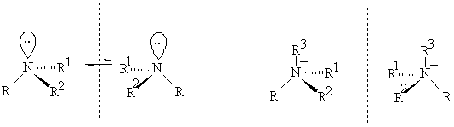
В молекулах аминов атом
азота, связанный с тремя различными заместителями, является асимметрическим
(подобно атому углерода, соединенному с четырьмя разными радикалами), т.к.
четвертая sp3-гибридная орбиталь занята неподеленной электронной
парой. Т.о. эти амины должны существовать в виде пары энантиомеров, однако
зафиксировать подобные стереоизомеры в индивидуальном состоянии, как правило,
не удается. Такие энантиомеры легко взаимопревращаются, этот процесс называется
инверсией азота. Энантиомеры четвертичных аммониевых солей, атом азота которых
связан с четырьмя разными заместителями - вполне устойчивые соединения, т.к. в
них инверсия азота невозможна.
4. Свойства
Образование водородных
связей
Амины могут образовывать
водородные связи друг с другом или с другими полярными молекулами, например, с
водой. Но эти связи менее прочные, чем водородные связи в спиртах. Так,
температуры кипения повышаются в ряду: C4H10 - 0oC;
C4H9NH2 - 49oC; C4H9OH
- 97oC.
Прочность водородных
связей уменьшается в ряду первичные амины > вторичные амины > третичные
амины, что связано с экранированием неподеленной электронной пары атома азота
углеводородными радикалами. Например, температуры кипения триметиламина (CH3)3N
- 3.5oC и изобутана (CH3)3CH - -12oC.
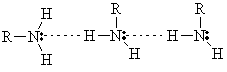
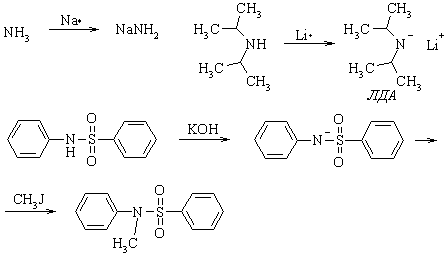
Кислотность первичных и
вторичных аминов
Первичные и вторичные
амины - очень слабые NH-кислоты. Так, рКа аммиака ≃
35, рКа диизопропиламина ≃
40. N-Анионы аминов (амид-анионы), напротив, очень сильные основания. Так, диизопропиламид
лития (ЛДА), часто используется в органическом синтезе в качестве сильного
основания, практически не обладающего нуклеофильными свойствами.Кислотность
повышается, если при атоме азота в аминах находятся электронакцепторные
заместители. Например, кислотность NH - связи в сульфамидах повышается
настолько, что они реагируют со щелочами, а возникающие N-анионы значительно
легче вступают в реакции нуклеофильного замещения с алкилгалогенидами, чем
исходные сульфамиды.
Основность аминов
Алкиламины - более
сильные основания, чем аммиак. В газовой фазе основность аминов увеличивается в
ряду NH3 < RNH2 < R2NH < R3N,
что является следствием +I эффекта алкильных групп. Но в водных растворах этот
ряд изменяется: R2NH > RNH2 ≃
R3N, что связано со стерическими препятствиями для переноса протона
и сольватацией в случае третичных аминов.
Ароматические амины
менее сильные основания, чем аммиак и алкиламины. Делокализация неподеленной
электронной пары по бензольному кольцу уменьшает электронную плотность на атоме
азота, и, следовательно, понижается способность к связыванию протона.
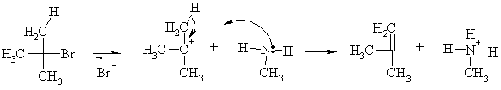
Как основания алкил- и
ариламины реагируют с минеральными кислотами с образованием четвертичных
аммониевых солей. Алкиламины выступают в роли оснований (но не нуклеофилов) в
реакциях третичных галогеналканов, например реакция отщепления бромоводорода от
трет-бутилбромида.
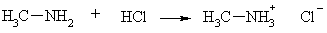
Нуклеофильность аминов
Амины проявляют свойства
нуклеофильных реагентов, вступая в реакции замещения при sp3 -
(алкилирование) и sp2-гибридных атомах углерода (ацилирование,
арилирование); в реакции присоединения-отщепления с карбонильными соединениями
(образование иминов, енаминов, оснований Шиффа); в реакции замещения при атоме
серы в сульфонилгалогенидах (синтез сульфониламидов).
Алкилирование
Алкиламины алкилируются
галогеналканами, давая смесь трех соединений - вторичного и третичного аминов и
четвертичной аммоневой соли. При действии гидроксида серебра на галогениды
тетраалкиламмония образуются соответствующие гидроксиды, нагревание которых
приводит к образованию алкенов (см. расщепление гидроксидов тетраалкиламмония
по Гофману). Ариламины можно превратить в N,
N-диалкилариламины действием диалкилсульфатов или спиртов.

Арилирование
Подвижность галогена в
галогенаренах невысока, поэтому реакции арилирования аминов протекают с большим
трудом. Например, синтез дифениламина осуществляют нагреванием реагентов в
нитробензоле в присутствии в качестве катализатора мелкодисперсной меди.

Ацилирование и защита
аминогруппы
Ацилирование первичных и
вторичных аминов карбоновыми кислотами и их производными (ангидридами,
галогенангидридами, сложными эфирами) протекает по аминогруппе с образованием
N-замещенных амидов карбоновых кислот.

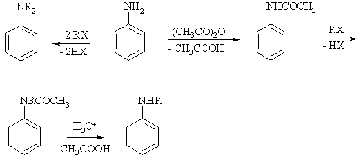
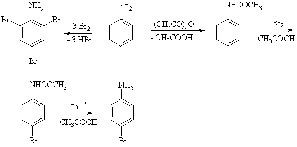
Реакцию ацилирования в
некоторых случаях используют для дезактивации аминогруппы (один из вариантов
защиты аминогруппы). Например, для получения N-алкилариламинов или
монобромариламинов ариламины предварительно ацилируют, затем проводят целевую
реакцию (алкилирование или бромирование) и снимают защитную функцию, как
правило, кислотным гидролизом.
Другой пример
использования ацилирования для защиты аминогруппы - реакция нитрования ариламинов.
При действии азотной кислоты аминогруппа легко окисляется, поэтому нитруют
ацильные производные аминов.
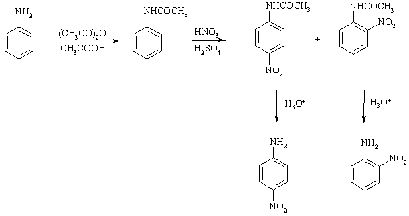
Другие функции,
используемые для защиты аминогруппы - формил (СНО), трифторацетил (CF3CO),
тозил (п-толуолсульфонил, 4-СН3-С6Н4-SO2),
бензилоксикарбонил (карбобензокси, С6Н5СН2-О-СО),
трет-бутоксикарбонил (ВОС, (СН3)3С-О-СО). Например,

Конденсация с
карбонилами
Первичные амины
реагируют с карбонильными соединениями, образуя имины или, в случае
ароматических аминов - основания Шиффа. Вторичные амины с карбонильными
соединениями образуют енамины.


Синтез сульфониламидов
Первичные и вторичные
амины реагируют с сульфонилхлоридами с образованием сульфониламидов. Эта
реакция широко используется в фармацевтической промышленности, поскольку многие
сульфониламиды обладают антибактериальной активностью (сульфаниламидные
антибиотики). Например, сульфаметоксазол входит в состав широко используемого
комбинированного антибиотика «бисептол».
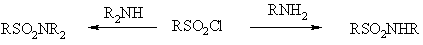

Реакция с азотистой
кислотой
Реакция с азотистой
кислотой - качественная реакция на первичные, вторичные и третичные,
алифатические и ароматические амины.
Неустойчивая азотистая
кислота генерируется непосредственно в процессе реакции из нитрита натрия и
сильной минеральной кислоты (серной, соляной). В кислой среде она дает ион
нитрозония, который и является нитрозирующим агентом.
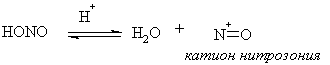
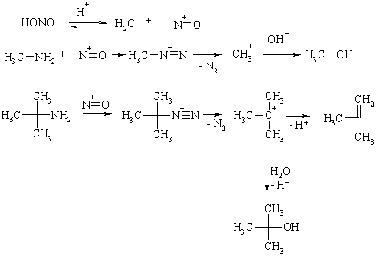
Первичные амины
Первичные алифатические
амины при нитрозировании превращаются в крайне неустойчивые соли алкилдиазония,
которые отщепляют молекулу азота, превращаясь в карбокатионы. Последние
стабилизируются несколькими способами: 1) за счет взаимодействия с водой, давая
спирты; 2) реагируя с другими нуклеофилами, например, с галогенид анионами,
если реакция проводится в присутствии галогеноводородных кислот; 3) за счет
отщепления протона. Поэтому в результате реакции обычно образуется смесь
нескольких соединений.
Первичные ароматические
амины при действии азотистой кислоты превращаются в соли диазония.
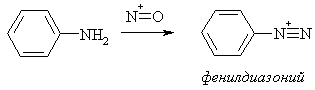
Вторичные амины
Вторичные алифатические
и ароматические амины нитрозируются с образованием N-нитрозоаминов.
Ароматические N-нитрозоамины при действии минеральных кислот
перегруппировываются в п-нитрозо-N-алкилариламины. Примечательно, что
перегруппировка протекает исключительно по пара-положению бензольного
кольца.
Третичные амины
Третичные алифатические
амины при нитрозировании образуют крайне неустойчивые N-нитрозоаммонийные соли.
Ароматические третичные амины подвергаются электрофильному нитрозированию по пара-положению
бензольного кольца.
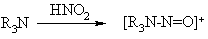
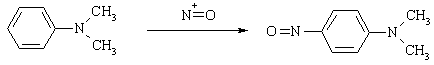
Превращения
углеводородного радикала
Разложение четвертичных
аммониевых оснований
При нагревании сухих
гидроксидов тетраалкиламмония происходит образование алкена, третичного амина и
воды.
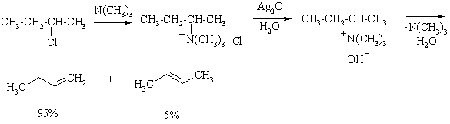
Механизм реакции -
бимолекулярное Е2-элиминирование, протекающее в соответствии с правилом
Гофмана. Т.е. при отщеплении амина от солей тетраалкиламмония преимущественно
образуется наименее замещенный алкен. В переходном состоянии, имеющем
трансоидную конфигурацию, более выгодной оказывается атака основания с менее
экранированной стороны.
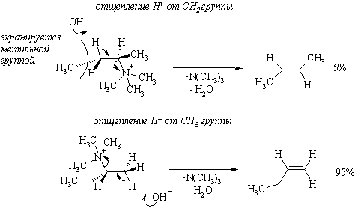
В пользу
пространственного фактора говорит следующий факт. Доля олефина с концевой
двойной связью возрастает, при увеличении объема уходящей группы. Например,
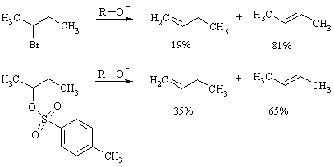
Реакции ароматического
кольца
Аминогруппа, обладающая
+М и - I эффектами (+М >> - I), активирует бензольное кольцо по отношению
к электрофилам. Реакции электрофильного замещения в ариламинах протекают без
катализатора, зачастую в мягких условиях и под действием даже очень слабых
электрофилов.
Галогенирование
Независимо от количества
используемого галогена (хлора или брома) реакция протекает сразу по всем
свободным орто- и пара-положениям бензольного кольца. О
моногалогенировании
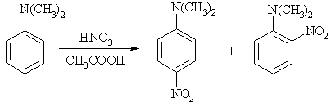
Нитрование
Первичная аминогруппа в
ариламинах легко окисляется под действием азотной кислоты, поэтому для
получения нитрозамещенных ариламинов требуется Защита аминогруппы. В отличие от
них, третичные ароматические амины нитруются азотной кислотой в уксусной
кислоте до орто- и пара-нитроариламинов, а в конц.H2SO4
- мета-нитросоединения. Образование последних является следствием
протонирования аминогруппы, которая превращаясь в аммониевую группу NH3+
становится ориентантом 2-ого рода и направляет вступление нитрогруппы в мета-положение.
Сульфирование
Аминогруппа при действии
конц. серной кислоты протонируется, а образующаяся аммониевая группа - NH3+
является электроноакцепторным заместителем, поэтому сульфирование ариламинов в
этих условиях протекает по мета-положениям бензольного кольца. Для
получения орто- и пара-аминобензолсульфокислот используют
«реакцию спекания». Действуя на амин эквимольным количеством конц. серной
кислоты получают твердый гидросульфат ариламмония, который нагревают до 180-200оС.
При этом первоначально образуется арилсульфаминовая кислота, которая далее
изомеризуется в орто- и пара-аминобензолсульфокисоты. Увеличение
времени проведения реакции приводит к образованию более термодинамически стабильного
пара-изомера - сульфаниловой кислоты.

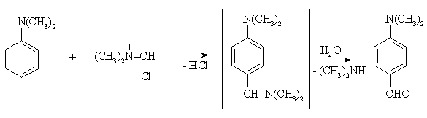
Формилирование
Третичные ароматические
амины реагируют с N, N-диметилфорамидом в присутствии хлорокиси фосфора,
образуя пара-замещенные бензальдегиды (реакция Вильсмайера-Хаака).
Формилирующий агент в этом превращении - иминиевая соль, получаемый in situ
из ДМФА и хлорокиси фосфора.

Азосочетание
Ароматические амины
вступают в реакцию азосочетания с солями диазония. Ниже приведен пример
получения индикатора метиловый оранжевый.

Литература
1. Органическая химия: в 4 ч. / О.А. Реутов, А.Л. Курц, К.П.
Бутин. - 2-е изд., испр. - М.: БИНОМ. Лаборатория знаний. - (Классический
университетский учебник). Ч. 4: 2011. - 726 с.: ил.
2. Кодопозитивы. ХИМИЯ. Рецензент Мельник А.С., кооператив
«Форма», Свердловск, 2000 г.
. Хомченко Г.П. Химия (для подготовительных отделений).
Учебник. - 3-е изд., испр. - М.: Высш. шк., 2003. - 368 с., ил.
. Вайзман Ф.Л. Основы органической химии: Учебное пособие
для вузов: Пер. с англ. / Под ред. А.А. Потехина. - СПб: Химия, 2005. - 464 с.
- Пер. изд.: США, 2008. ил.
. Слета Л.А. Химия: Справочник. - Харьков: Фолио; Ростов
н/Д: Феникс, 2007. - 496 с.
. Кузьменко Н.Е. и др. Химия. Для школьников ст. кл. и
поступающих в вузы: Учеб. пособие/ Н.Е. Кузьменко, В.В. Ерёмин, В.А. Попков. -
М.: Дрофа, 2007. - 528 с.: ил.