Лечение боли при ревматоидных заболеваниях суставов
Лечение боли при ревматоидных
заболеваниях суставов
При проведении Международной
декады заболеваний костей и суставов (2000–2010) выделены следующие
заболевания, имеющие наиболее важное медико-социальное значение для общества:
остеоартроз, остеопороз, боль в нижней части спины, ревматоидный артрит,
травматические повреждения.
Наиболее распространенным
ревматическим заболеванием является остеоартроз (ОА). Это хроническое
невоспалительное заболевание суставов (суставных хрящей) и окружающих их
тканей. По статистике от остеоартроза страдает от 10 до 16% населения Земного
шара. Частота ОА прогрессирующе увеличивается с возрастом (5). Ревматоидный
артрит (РА) - хроническое системное заболевание соединительной ткани, при
котором в результате иммуновоспалительного процесса преимущественно поражаются
периферические суставы с развитием в них эрозивно-деструктивных изменений (2).
Распространенность ревматоидного
артрита в популяции достигает 1,0 %, а экономические потери для общества
сопоставимы с таковыми при ишемической болезни сердца (1).
Возраст, в котором у большинства
пациентов начинается ревматоидный артрит, составляет 30 - 50 лет. Женщины
страдают РА и ОА примерно в три раза чаще. С возрастом распространенность
заболевания увеличивается, а ее половые различия сглаживаются. У женщин 60 - 64
лет РА возникает в 6 раз чаще, чем у женщин 18 - 29 лет. В отсутствие
эффективной терапии продолжительность жизни у больных РА ниже на 3 года у
женщин и на 7 лет у мужчин (1).
Согласно современным
стандартам лечения ревматоидного артрита, непосредственной целью терапии
является достижение состояния продолжительной ремиссии, а также уменьшение боли
в суставах, улучшение их подвижности, улучшение общего состояния больного,
уменьшение повышенной температуры тела (25).
Нефармакологические
методы лечения. Социальная
поддержка больных
В последние годы
обращается внимание на социальную поддержку и образование больных. Так,
различные советы и общества по артритам в Великобритании, США, Канаде издают
брошюры, обучающие больных справляться с болью (20), и организуют локальные
группы самопомощи. Такие мероприятия должны являться существенной частью любого
лечебного плана для больных ОА, тем более что приводятся доказательства
эффективности образовательных программ для больных, таких как “Arthtritis Self-Management Course”, в
уменьшении боли, числа визитов к врачу, улучшении качества жизни и поддержании
функции суставов. Недавно проведенный сравнительный метаанализ образовательных
программ и применения НПВП показал, что образовательные программы весьма
существенно помогают больным справиться с болью (21).
Физическая терапия
Физическая терапия играет
важную роль в лечении ОА. Она включает аэробные, двигательные и силовые
упражнения для определенных мышечных групп, тепловые методы, ультразвук,
чрескожную электростимуляцию нервов (ЧЭСН) и т.д. Так, укрепление четырехглавой
мышцы бедра и аэробные упражнения в течение 6 мес. уменьшали боль и улучшали
функцию коленных суставов. Результаты проведенного W.Ettinger и соавт.
многоцентрового исследования (22) длительностью 18 мес. показали, что аэробные
или изометрические упражнения дают лучший результат, чем комбинация
фармакотерапии с образовательными программами у больных с ОА коленных суставов.
Данные клинических исследований подтверждают полезность физических упражнений.
ЧЭСН применяют для получения анальгетического действия, но результаты двойных
слепых исследований ЧЭСН с плацебо (23) и напроксеном неоднозначны. При
поражении суставов нижних конечностей для уменьшения нагрузки рекомендуется
хождение с палочкой, которая почти на 50% уменьшает нагрузку на тазобедренный
сустав, ношение надколенников и супинаторов. Использование подпяточных клиньев
полезно при ОА медиального отдела коленного сустава, особенно у больных с
легким течением заболевания.
Медикаментозное
лечение ревматоидного артрита основано на четырех традиционных подходах
Первый - заключается в
использовании аспирина и других нестероидных противовоспалительных препаратов
(НПВС), а также анальгетиков. Эти препараты быстро уменьшают проявления
заболевания, но почти не влияют на скорость его прогрессирования.
Второй - предусматривает
прием низких доз глюкокортикоидов внутрь. Недавно показано, что они не только
подавляют воспаление, но и замедляют деструкцию костной ткани.
Третий подход основан на
использовании так называемых средств базисной терапии, приостанавливающих
прогрессирование ревматоидного артрита. Кроме иммунодепрессантов и
цитостатиков, в эту группу входят и другие препараты, некоторые из которых
снижают уровень белков острой фазы воспаления, что говорит об их способности
предотвращать повреждение тканей.
Четвертый подход -
внутрисуставное введение глюкокортикоидов - позволяет добиться временного
улучшения в тех случаях, когда не помогают препараты для системного применения
(11).
Пятый подход –
использование биологических агентов, что является наиболее существенным
достижением ревматологии последнего десятилетия.
Наиболее широко
применяемыми в клинической практике являются нестероидные противовоспалительные
препараты – НПВП.
Таблица 1. Основные
механизмы влияния неселективных и селективных ингибиторов ЦОГ – 2
|
Влияние
|
Неселективные ингибиторы ЦОГ
|
Ингибиторы ЦОГ - 2
|
|
Артрит
|
Ингибируют ЦОГ - 2↓
Ингибируют ПГЕ 2 ↓
Уменьшают боль и отечность
|
Ингибируют ЦОГ - 2↓Ингибируют ПГЕ2↓Уменьшают
боль и отечность
|
|
Желудок
|
Ингибируют ЦОГ - 2
Ингибируют ПГЕ2
Уменьшают гастропротекцию
|
Не вызывают эффекта на ЦОГ - 1
|
|
Тромбоциты
|
Ингибируют ЦОГ - 1 и ЦОГ - 2
|
Не вызывают эффект на ЦОГ - 2
|
|
Сосуды
|
Ингибируют ЦОГ - 1 и ЦОГ - 2
|
Ингибируют ЦОГ - 2↓
Ингибируют ПГЕ2↓
Уменьшают антитромбоцитарный эффект
|
Вместе с тем фармакоэпидемиологические
данные показывают не только их широкое использование, но часто и неправильное
применение у больных, и поэтому, чаще имеющих различные побочные реакции.
В настоящее время
выделяют несколько десятков НПВП, близким по химическим и фармакологическим
свойствам. Рассмотрим некоторые из них.
Нимесулид - это НПВП с уникальной химической структурой; принадлежит к
классу сульфонамидов, обладает выраженным эффектом ингибирования
циклооксигеназы (ЦОГ)-2 и меньшим воздействием на ЦОГ-1. Во многих исследованиях
продемонстрировано, что нимесулид в стандартной дозе 100 мг дважды в сутки
эффективен для симптоматического лечения ОА.
На сегодняшний день в
клинической практике в Украине используется несколько десятков (30) разных по
производителю и фармацевтическим формам препаратов нимесулида. Накоплен
позитивный опыт фармакотерапии этим препаратом, причем в разных
фармацевтических формах при остеоартрозе (В.Н. Коваленко. Н.М. Шуба, А.К.
Галицкая, 2001). Достаточно высокую эффективность выявили исследования растворимой
формы нимесулида – препарата Нимесил. Следует отметить, что благодаря своим
фармацевтическим и фармакокинетическим свойствам данной фармацевтической формы
нимесулид сравнительно с другими НППВ, диклофенаком натрия, например, проявляет
более ранний обезболивающий эффект уже после первого приема. Использование 100
мг нимесулида провоцирует более выраженный и быстрый терапевтический эффект,
чем 200 мг целекоксиба или 25 мг рофекоксиба на протяжении 3-х часов. У больных
с остеоартрозом обезболивание происходит через 15 минут после приёма
нимесулида, тогда как эффект целекоксиба и рофекоксиба развивается намного
медленнее. Лечение нимесулидом гораздо дешевле, чем использование упомянутых
выше препаратов со схожими фармакотерапевтическими препаратами. (8).
Целекоксиб (Ревмоксиб) –
это сульфонамид, принадлежащий к группе селективных ингибиторов ЦОГ-2. В
клинических исследованиях показано, что целекоксиб в дозировке 200 мг способен
устранять симптомы ОА.
За период между сентябрем
2004 г. и ноябрем 2005 г. в исследование отобрали 44 пациента (6 мужчин и 38
женщин), у 24 из которых был болевой синдром в коленном суставе без
синовиального выпота и у 20 – с выпотом.
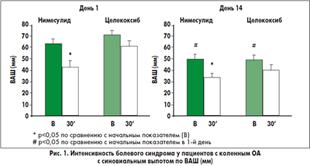
У пациентов с
синовиальным выпотом анальгетический эффект нимесулида был более выраженным,
чем целекоксиба. В группе пациентов, получавших нимесулид, показатели по ВАШ
через 30 мин после приема лекарства были достоверно ниже, чем до приема
препарата (рис. 1), тогда как в группе целекоксиба эта разница не была
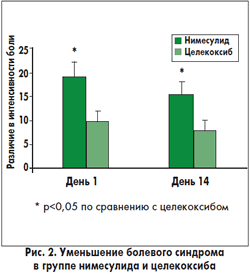
статистически значимой. Болевой синдром в группе нимесулида уменьшался
значительно больше, чем в группе целекоксиба (рис. 2). С другой стороны,
эффективность лечения обоими препаратами была сравнимой у пациентов без
синовиального выпота.
В последний день лечения
у всех пациентов перед приемом препаратов оценивали интенсивность болевого
синдрома по ВАШ. В обеих группах исследования интенсивность боли была ниже, чем
до начала лечения. Такие результаты наблюдали и у пациентов с синовиальным
выпотом, и без выпота (рис. 1 и 2). Через 30 мин после приема препаратов
интенсивность боли в группе нимесулида была достоверно ниже, чем до приема
лекарства, тогда как статистически достоверной разницы в группе целекоксиба не
обнаружено. Также уменьшение между аналогичными показателями болевого синдрома
было достоверно выше в группе нимесулида (рис. 2).(7)
L-лизина эсцинат - это препарат выбора
в профилактике и лечении отечно-болевого синдрома, который, начиная с 1998 г. используют в Институте травматологии и ортопедии АМН Украины (11). Эсцин понижает активность
лизосомальных гидролаз, что предупреждает расщепление мукополисахаридов в
стенках капилляров и в соединительной ткани, которая их окружает, и таким
образом нормализует повышенную сосудисто-тканевую проницаемость и оказывает
антиэкссудативное (противоотечное), противовоспалительное и обезболивающее
действие. Препарат повышает тонус сосудов, оказывает умеренный
иммунокорригирующий и гипогликемический эффекты (12).
Суточная выраженность
боли под влиянием лечения L-лизина
эсцинатом

Обозначения :
Красным цветом - до
лечения;
Зеленым – после.
1-ходьба по ровной
поверхности;
4-ходьба по ступенькам
вниз;
7-постоянная боль;
10-ночная боль;
13-боль при
продолжительной ходьбе;
16-стартовая боль.
Таблица. Сравнительная
анальгетическая активность и переносимость классических НПВП на модели
ацетилхолинового абдоминального теста у мышей
|
Препарат
|
ЕД 50, мг/кг
|
УД 50, мг/кг
|
ИП, УД 50/ЕД 50
|
Относительная безопасность по
диклофенаку натрия
|
|
АСК
|
50(28±90)
|
4,8
|
0,8
|
|
Динклофенак натрия
|
8(5±14)
|
48(33±71)
|
6
|
1
|
|
Индометацин
|
4(3±6)
|
10(5±19)
|
2,5
|
0,42
|
|
Ибупрофен
|
20(11±38)
|
310(230±419)
|
15,5
|
2,6
|
|
Кетопрофен
|
53(28±101)
|
62(36±108)
|
1,2
|
0,2
|
|
Пироксикам
|
36(23±57)
|
36(25±53)
|
1
|
0,17
|
Пометки: ЕД-эффективная
доза, ИП- индекс переносимости. (17).
Побочные эффекты
нестероидных противовоспалительных препаратов
Наиболее главным побочным
эффектом НПВП является поражение слизистой оболочки желудка, что проявляется в
виде так называемой гастропатии, вплоть до появления язвенной болезни и ее
осложнений в виде перфорации. Это связано с тем, что при приеме внутрь НПВП
вызывают раздражение слизистой желудка. Чтобы снизить этот эффект НПВП эти
препараты назначаются обычно только после еды. Кроме того, существуют
таблетированные формы с оболочкой, которая растворяется не в желудке, а в
кишечнике.
Также, снизить
раздражение слизистой желудка можно и путем назначения инъекций этих
препаратов.
Среди признаков
осложнений со стороны желудка во время приема НПВП можно отметить:
-тошноту,
-диспепсию,
-желудочно-кишечное
кровотечение,
-диарею.
Побочные эффекты,
наблюдавшиеся в контролируемых клинических испытаниях (результаты 12
исследований), при применении целекоксиба в дозах 100–200 мг ежедневно у
пациентов с ОА или РА (безотносительно причинной связи с приемом препарата)
представлены в таблице.
Побочные реакции,
отмеченные с частотой ≥2% случаев в премаркетинговых контролируемых
испытаниях у пациентов с артритом, получавших целекоксиб, по сравнению с
плацебо.
|
Системы организма / побочные
эффекты
|
Частота побочных реакций
|
|
Боль в животе
|
4,1
|
2,8
|
|
Диарея
|
5,6
|
3,8
|
|
Диспепсия
|
8,8
|
6,2
|
|
Метеоризм
|
2,2
|
1
|
|
Тошнота
|
3,5
|
4,2
|
|
Организм в целом
|
|
|
|
Боль в спине
|
2,8
|
3,6
|
|
Периферические отеки
|
2,1
|
1,1
|
|
Случайная травма
|
2,9
|
2,3
|
|
Нервная система
|
|
|
|
Головокружение
|
2
|
1,7
|
|
Головная боль
|
20,2
|
|
Инсомния
|
2,3
|
2,3
|
|
Респираторные
|
|
|
|
Фарингит
|
2,3
|
1,1
|
|
Ринит
|
2
|
1,3
|
|
Синусит
|
5
|
4,3
|
|
Инфекция верхних дыхательных путей
|
8,1
|
6,7
|
|
Кожа
|
|
|
|
Сыпь
|
2,2
|
2,1
|
В результате применения
НПВП не часто встречаются отек лица и ног, внезапное снижение мочеиспускания.
Эти эффекты обычно встречаются у пожилых больных и людей с другими серьезными
заболеваниями.
НПВП вызывают в организме
задержку солей и воды, что приводит как к отекам, так и к повышению
артериального давления (артериальная гипертензия).
Сравнительно редко
возникают следующие осложнения со стороны почек: интерстициальный нефрит,
нефротический синдром, острая почечная недостаточность и острый сосочковый
некроз.
Кроме того, многие НПВП
вызывают уменьшение свертываемости крови, что также нужно учитывать больным со
склонностью к кровотечениям.
Кортикостероиды – это
группа препаратов противовоспалительного свойства. Они являются производными
естественного гормона человека – кортизола. Их эффект заключается в устранении
воспаления. Данные препараты не обладают непосредственно обезболивающим
эффектом, но, разрешая воспаление, они тем самым устраняют и боль.
Применяются эти препараты
в тех случаях, когда нестероидные противовоспалительные препараты и мышечные релаксанты
оказываются неэффективными.
Побочные эффекты
кортикостероидов
Среди умеренно выраженных
побочных эффектов этих препаратов отмечаются:
-Головная боль, иногда
выраженная
-Головокружение
-Усиление боли в спине
или ноге
В редких случаях могут
быть более серьезные побочные эффекты:
-Воспаление в области
спинномозгового нерва или другой ткани
-Дегенерация ткани в
месте постоянного введения препарата
-Повреждение
спинномозговых корешков (14).
Хондропротекторы. Согласно рекомендациям Ассоциации
ревматологов Украины они, наряду с нестероидными противовоспалительными
препаратами (НПВП), являются основой терапевтического подхода у больных
остеоартрозом. Основными хондропротекторами являются глюкозамин и хондроитин
сульфат. Они являются естественными компонентами суставного хряща, входят в
состав протеогликанов и гликозаминогликанов хрящевой ткани.
В многочисленных
исследованиях фармакологических эффектов глюкозамина установлено благоприятное
влияние на метаболизм хряща — усиление анаболических и ослабление катаболических
процессов. Установлены стимуляция глюкозамином синтеза протеогликанов и
коллагена, повышение продукции компонентов внеклеточного матрикса, при этом
свойства гликозаминогликанов и протеогликанов (по данным хроматографического
анализа) были близки к физиологическим. В большинстве проведенных краткосрочных
(4-6 недель) клинических исследований эффективность глюкозамина в дозах
800-1500 мг/сут у больных остеоартрозом превышала таковую плацебо и была
эквивалентна эффективности ибупрофена и диклофенака. Глюкозамин несколько
уступал НПВП по скорости наступления обезболивающего и противовоспалительного
действия, однако обладал отчетливым последействием. Заметное улучшение
клинических симптомов (по оценке в баллах боли при ходьбе и в покое, выраженности
синовита, функционального индекса Лекена) проявлялось через 2-3 недели от
начала лечения с сохранением эффекта в течение месяца и более после отмены
лечения, что позволяет проводить прерывистые курсы лечения.
В длительных
исследованиях, когда терапия глюкозамином в дозе 1500 мг/сут у больных
остеоартрозом продолжалась в течение 1-3 лет, хороший и отличный результат был
получен у 50-60% больных, удовлетворительный — у 25-30% больных. При этом
отмечено, что для четкой оценки результатов лечения следует принимать
глюкозамин не менее 6-12 недель, что вполне объяснимо с учетом особенностей
кровоснабжения суставов и темпов обмена веществ в тканях сустава.
В исследованиях,
посвященных переносимости глюкозамина, установили отсутствие токсичности и
наличия тяжелых побочных эффектов, а также клинических, биохимических или
гематологических изменений при длительном его приеме.
В клинических
исследованиях продемонстрирована эффективность хондроитин сульфата в отношении
влияния на болевой синдром и функциональное состояние суставов.
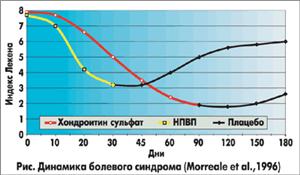
В большинстве клинических
исследований, в которых сравнивался эффект хондроитин сульфата и НПВП
отмечалось, что хондроитин сульфат в дозе 1200 мг/сут так же эффективен, как
диклофенак и ибупрофен в терапевтических дозах, и более эффективен, чем плацебо
в отношении уменьшения боли и увеличения подвижности суставов у больных
остеоартрозом. Хотя эффект хондроитин сульфата наступал несколько позже (на
6-8-й неделе лечения) по сравнению с действием НПВП (на 1-2-й неделе лечения),
он держался более длительно после прекращения лечения (см. рис.).
Немаловажным
преимуществом препарата является хорошая переносимость, побочные проявления при
его приеме незначительны и нечасты — около 1-3% случаев, тогда как при приеме
НПВП они более серьезны (прежде всего, желудочно-кишечные кровотечения,
изъязвления и т.п.) и встречаются у 30-40% лиц. Как правило, переносимость
хондроитин сульфата и плацебо была одинаковой (16).
Особенное внимание среди хондропротекторов
заслуживает ХС – 4,6, зарегистрированный в Украине как препарат Структум
производства компании «Пьер Фабр», Франция. Препарат проявляет высокую
биодоступность по отношению к хрящу, хорошо переносится больными (17). Структум принадлежит к
препаратам замедленного действия. Эффект наступает не одномоментно, а по мере накопления
хондроитин сульфата в хряще. Уменьшение боли наблюдается на протяжении 1 мес.
лечения и в последующие месяцы вначале стихает боль в состоянии покоя, а затем
– боль при движениях. Это дает возможность уменьшить дозу анальгетиков или НПВП
(18). При постановке диагноза ОА показано
проводить 14-дневный курс НПВП до начала действия структурно-модифицирующих
препаратов, после чего рекомендуется постоянная и длительная терапия
хондропротекторами (17).
Биологические агенты. В
отличие от традиционных БПВП и глюкортикоидов, для которых характерны
неспецифические противовоспалительные и/или иммуносупрессивные эффекты,
биологические агенты оказывают более селективное действие на гуморальные и
клеточные компоненты воспалительного каскада, лежащего в основе
иммунопатогенеза РА.
Среди чрезвычайно
широкого спектра противовоспалительных медиаторов, принимающих участие в
развитии РА, особое внимание привлечено к фактору некроза опухоли (ФНО-а),
который рассматривается как основная мишень для терапии некоторых
воспалительных реакций человека. Это послужило основанием для разработки
препаратов, блокирующих биологическую активность именно ФНО-а.
Существует ряд
стандартных биологических агентов, предназначенных для лечения ревматоидного
артрита:
-Ембрел
-Хумира
-Кинерет
-Ремикад
-Ритуксан
-Оренция
Остальные биологические
агенты подвергаются клиническим испытаниям относительно их воздействия на
различные формы артрита.
Адалимубаб (Хумира, «Эббот Лэбораториз»)
является первым и пока единственным препаратом, представляющим собой полностью
человеческие рекомбинантные моноклональные антитела к ФНО-а. В настоящее время
лечение адалимубабом получают свыше 110 000 пациентов более чем в 67
странах мира. При тяжелом или среднетяжелом РА его применяют в режиме
монотерапии или в комбинации с метотрексатом (МТ) или другими базисными
противовоспалительными препаратами. Кроме того, адалимубаб можно применять как
препарат первого ряда у пациентов с ранним быстро прогрессирующим тяжелым РА, а
также псориатическим артритом и анкилозирующим спондилитом (1).
Было проведено
многоцентровое рандомизированное, двойное слепое клиническое исследование по
оценке эффективности препарата Adalimumab (Humira), моноклонального антитела,
действующего на фактор некроза опухоли, для раннего лечения 799 пациентов с
ревматоидным артритом (РА) средней и тяжелой степени. Исследование было
организовано компанией-производителем Abbot Laboratories (CША). Через 1 год
лечения значительное улучшение состояния наблюдалось у больных, получавших
комбинированную терапию Adalimumab и метотрексатом, по сравнению с группами
пациентов, находившихся на монотерапии Adalimumab или метотрексатом: 62, 41 или
46% соответственно. Через 2 года достигнутые результаты сохранялись: 59, 37 или
43% соответственно. Не было различий в количестве наблюдавшихся серьезных
побочных явлений. Исследователи считают, что у пациентов с прогрессирующим РА,
никогда не получавших метотрексат, можно достичь хороших терапевтических
результатов при раннем комбинированном лечении препаратом Adalimumab и
метотрексатом (24).
Побочные действия
адалимубаба. Очень часто сообщалось о реакциях в месте введения (большинство
реакций были легкими и не требовали прекращения введения); часто сообщалось об
инфекциях верхних и нижних дыхательных путей, кандидозе, бактериальных
инфекциях (включая инфекции мочевого тракта), лимфопении, головокружении,
головной боли, расстроиствах чувствительности (включая парастезию), раздражении
или воспалении глаз,диарее,боли в животе, стоматите, тошноте, повышении уровней
печеночных ферментов, сыпи, дерматите, зуде, скелетно-мышечной боли. Сообщалось
о развитии тяжелых инфекций (редко с фатальным исходом) – туберкулеза и
инвазивных оппортунистических инфекций, анафилаксии, ангионевротическом отеке.
К сожалению, ревматоидный
артрит продолжает оставаться заболеванием, при котором все еще отсутствуют
методы, позволяющие добиться полного излечения.
Чем раньше будет
назначено лечение ревматоидного артрита, направленное на подавление воспаления
в суставе (базисная терапия), тем больше надежды на сохранение функции суставов
и внутренних органов и возможностей продления активных лет жизни человека.
Пациенты, которые хорошо
информированы о своем заболевании и ведут правильный образ жизни, ощущают
меньше симптомов, реже посещают врачей, больше уверены в себе и более активны,
несмотря на продолжающуюся болезнь (25).
Литература
1.
Е.Л. Насонов. Перспективы применения полностью
человеческих моноклональных антител к фактору некроза опухоли (адалимубаба) при
ревматоидном артрите // Український ревматологічний журнал.- 2009- №3 (37), с. 1-
2.
http://www.rlsnet.ru/mnn_index_id_2718.htm
14.
http://spine.eurodoctor.ru/discalherniatreatment/drugdiscalhernia/
15.
И.А. Зупанец.
Современные взгляды на лечение боли в спине// Здоровье Украины.-2209-№17(222)
16.
http://www.beka.ru/php/content.php?id=350
17.
С.И. Смиян, С.Р.
Гусак, Н.В. Грималюк и др. П’ятирічний моніторинг
артралогічного статусу у хворих на остеоартроз під впливом застосування
хондропротектора структур// Український ревматологічний журнал-2008-№4 (34)
18.
Спеціалізоване
інформаційне видання «Ліки» - 2005 - № 10.
19.
Weinblatt M.E. et al., Ann Scientific Meeting,
Abstract 294 Available at: Medical Intelligence Solution 4277219.pdf, Nov. 2007
21.
Superio-Cabuslay
E, Ward MM, Lorig KR. Patient education interventions in osteoarthritis and
rheumatoid arthritis: a meta-analytic comparison with nonsteroidal
antiinflammatory drug treatment. Arthritis Care Res, 1996; 9: 292–301.
22.
Ettinger
WH, Burns R, Messier SP et al. A randomized trial comparing aerobic exercise
and resistance exercise with a health education program in older adults with
knee osteoarthritis. JAMA 1997; 277: 25–31.
23.
Hardingham
TE, Fosang AJ, Dubhia J. The structure, function and turnover of aggrecan, the
large aggregating proteoglycan from cartilage. Aur J Clin Chem Clin Biochem,
1994; 32: 249–57.
24.
http://medvestnik.ru/1/0/9768.html
25.
http://www.remissia.ru/auto/artrit.php