Комплексная оценка железодефицитных состояний
МИНИСТЕРСТВО НАУКИ И ОБРАЗОВАНИЯ
УКРАИНЫ
ЛУГАНСКИЙ НАЦИОНАЛЬНЫЙ УНИВЕРСИТЕТ
ИМЕНИ Т.Г. ШЕВЧЕНКО
КАФЕДРА АНАТОМИИ, ФИЗИОЛОГИИ ЧЕЛОВЕКА
И ЖИВОТНЫХ
КУРСОВАЯ РАБОТА
НА ТЕМУ: "КОМПЛЕКСНАЯ ОЦЕНКА
ЖЕЛЕЗОДЕФИЦИТНЫХ СОСТОЯНИЙ"
Выполнила: студентка 3 курса
факультета естественных наук
специальности "Лабораторная диагностика"
Шаповалова И.И.
Луганск, 2014
Содержание
Введение
1. Железосодержащие органические соединения в организме человека
1.1 Клеточное железо
1.2 Внеклеточное железо
2. Медико-биологические основы обеспечения организма железом
2.1 Эритропоэз
2.1.1 Эритроидный ряд клеток.
2.1.2 Регуляция эритропоэза
2.2 Синтез гемоглобина
2.3 Регенерация красной крови
2.4 Метаболизм железа
2.4.1 Обмен железа
2.4.2 Этапы обмена железа в организме
2.4.3 Потери железа
2.4.4 Регуляция метаболизма железа
3. Клинико-лабораторные характеристики красной крови и обмена
железа
4. Железодефицитные состояния
4.1 Определение
4.2 Этиология и патогенез железодефицитных состояний
4.2.1 Алиментарная недостаточность
4.2.2 Нарушение усвоения железа
4.2.3 Кровопотери
4.2.4 Перераспределение и конкурентное потребление железа
4.2.5 Нарушения транспорта железа
4.3 Клиническая картина железодефицитных состояний
4.3.1 Сидеропения (гипосидероз)
4.3.2 Анемический синдром.
4.4 Диагностика железодефицитных состояний
4.4.1 Доказательство наличия анемии
4.4.2 Доказательство наличия латентного дефицита железа
4.4.3 Доказательство гипохромности анемии
4.4.4 Доказательство дефицита железа, исключение нежелезодефицитных
причин гипохромии и микроцитоза
4.4.5 Определение причины дефицита железа
Заключение
Список использованной литературы
Введение
Для нормального роста и выполнения биологических функций
человеку и животным кроме витаминов необходим целый ряд неорганических
элементов. Эти элементы можно разделить на две класса. Один из них -
макроэлементы, а другой - микроэлементы.
Макроэлементы, к которым относятся кальций, магний, натрий,
калий, фосфор, сера и хлор, требуются организму в относительно больших
количествах (порядка нескольких граммов в сутки). Часто они выполняют более чем
одну функцию.
Более непосредственное отношение к действию ферментов имеют
независимые микроэлементы, суточная потребность в которых не превышает
нескольких миллиграммов, то есть, сопоставима с потребностью в витаминах.
Известно, что в пище животных обязательно должно содержаться
около 15 микроэлементов, большинство из которых выполняет, по меньшей мере,
какую-нибудь одну из трёх возможных функций. Во-первых, незаменимый
микроэлемент сам по себе может обладать каталитической активностью по отношению
к той или иной химической реакции, скорость которой значительно возрастает в
присутствии ферментного белка. Это особенно характерно для ионов железа и меди.
Во-вторых, ион металла может образовывать комплекс одновременно с активным
центром фермента, в результате чего происходит их сближение и переход в
активную форму. И, в-третьих, ион металла может играть роль мощного акцептора
электронов на определённой стадии.
Железо относится к тем микроэлементам, биологические функции
которых изучены наиболее полно. Значение железа для организма человека трудно
переоценить. Подтверждением этому может быть не только большая его
распространенность в природе, но и важная роль в сложных процессах,
происходящих в живом организме. Биологическая ценность железа определяется
многократностью его функций, незаменимостью другими металлами в сложных
биохимических процессах, активным участием в клеточном дыхании, обеспечивающем
нормальное функционирование тканей и организма человека.
Железо является одним из важнейших элементов в организме
человека и входит в состав многих субстратов и ферментов, отвечающих за
транспорт кислорода к клеткам, функционирование дыхательной цепи митохондрий,
окислительно-восстановительные клеточные реакции, антиоксидантную защиту,
функционирование нервной и иммунной систем и др.
1.
Железосодержащие органические соединения в организме человека
Железо, находящееся в организме человека, можно разбить на 2
большие группы: клеточное и внеклеточное. Соединения железа в клетке,
отличающиеся различным строением, обладают характерной только для них
функциональной активностью и биологической ролью для организма. В свою очередь
их можно подразделить на 4 группы:
) гемопротеины, основным структурным элементом которых
является гем (гемоглобин, миоглобин, цитохромы, каталаза и пероксидаза);
) железосодержащие ферменты негеминовой группы (сукцинат-де -
гидрогеназа, ацетил - коэнзим А - дегидрогеназа, НАДН, - цитохром С-редуктаза и
др.);
) ферритин и гемосидерин внутренних органов;
) железо, рыхло связанное с белками и другими органическими
веществами.
Ко второй группе внеклеточных соединений железа относятся
железо-связывающие белки трансферрин и лактоферрин, содержащиеся во
внеклеточных жидкостях.
.1 Клеточное
железо
Гемоглобин, содержащийся в эритроцитах, выполняет важную
для организма газотранспортную функцию - переносит экзогенный кислород и
эндогенный углекислый газ. Эритроцит по отношению к гемоглобину играет роль
буферной системы, способной регулировать общую величину газотранспортной
функции. Дыхательный пигмент крови - сложный белок, состоящий из белковой
молекулы - глобина, соединенной полипептидными цепочками с 4 комплексами гема.
Глобин состоит из 2 пар полипептидных цепочек, каждая из которых содержит
141-146 аминокислот. Гем, составляющий 4% веса молекулы гемоглобина, содержит
железо в центре порфиринового кольца. У здорового человека гемоглобин
гетерогенен. Нормальный эритроцит содержит приблизительно 30 пг. гемоглобина, в
котором находится 0,34% железа.
Миоглобин - дыхательный белок сердечной и скелетной
мускулатуры. Он состоит из единственной полипептидной цепочки, содержащей 153
аминокислоты и соединенный с гемпростетической группой. Основной функцией
миоглобина является транспортировка кислорода через клетку и регуляция его
содержания в мышце для осуществления сложных биохимических процессов, лежащих в
основе клеточного дыхания. Он содержит 0,34% железа. Миоглобин депонирует
кислород во время сокращения мышц, а при их поражении он может попадать в кровь
и выделяться с мочой.
Железосодержащие ферменты и негеминовое железо клетки
находится главным образом в митохондриях. Наиболее изученными и важными для
организма ферментами являются цитохромы, каталаза и пероксидаза.
Цитохромы делятся на 4 группы в зависимости от строения
геминовой группы:
А - цитохромы с гем - группой, соединяющей формилпорфин;
В - цитохромы с протогем - группой;
С - цитохромы с замещенной мезогем - группой;
Д - цитохромы с гем - группой, соединяющей дегидропорфин.
В организме человека содержатся следующие цитохромы:
а1, аз, в, в5, с, с1, Р450. Они представляют собой липидные
комплексы гемопротеинов и прочно связаны с мембраной митохондрии. Однако,
цитохромы в5 и Р450 находятся в эндоплазматическом ретикулюме, а микросомы
содержат НАДН - цитохром С - редуктазу. Существует мнение, что митохондриальное
дыхание необходимо для процессов дифференцировки тканей, а внемитохондриальное
играет важную роль в процессах роста и дыхания клетки. Основной биологической
ролью большинства цитохромов является участие в переносе электронов, лежащих в
основе процессов терминального окисления в тканях.
Пероксидаза содержится преимущественно в лейкоцитах и
слизистой тонкого кишечника у человека. Она также обладает защитной ролью, предохраняя
клетки от их разрушения перекисными соединениями.
Миелопероксидаза - железосодержащий
геминовый фермент, находящийся в азурофильных гранулах нейтрофильных лейкоцитов
и освобождается в фагоцитирующие вакуоли в течение лизиса гранул. Активированное
этим ферментом разрушение белка клеточной стенки бактерий является смертельным
для микроорганизма, а активированное им йодинирование частиц относится к
бактерицидной функции лейкоцитов.
К железосодержащим относятся ифлавопротеиновые ферменты, в
которых железо не включено в геминовую группу и необходимо только для реакций
переноса.
Наиболее изученной является сукцинатдегидрогеназа, которая
наиболее активна в цикле трикарбоновых кислот. Митохондриальные мембраны
свободно проницаемы для субстрата фермента.
железодефицитное состояние дефицит железо
Негеминовое железо, локализующееся главным образом в
митохондриях клетки, играет существенную роль в дыхании клетки, участвуя в
окислительном фосфолировании и транспорте электронов при терминальном
окислении, в цикле трикарбоновых кислот.
Ферритин и гемосидерин - запасные соединения
железа в клетке, находящиеся главным образом в ретикулоэндотелиальной системе
печени, селезенки и костного мозга. Приблизительно одна треть резервного железа
организма человека, преимущественно в виде ферритина, падает на долю печени.
Запасы железа могут быть при необходимости мобилизованы для нужд организма и
предохраняют его от токсичного действия свободно циркулирующего железа.
Известно, что гепатоциты и купферовские клетки печени участвуют
в создании резервного железа, причем в нормальной печени большая часть нового
железа обнаружена в гепатоцитах в виде ферритина. При парентеральном введении
железа как гепатоциты, так и купферовские клетки печени аккумулируют большое
количество дополнительного ферритина, хотя последние имеют тенденцию запасать
относительно больше из лишнего негеминового железа в виде гемосидерина.
Сферическая белковая оболочка молекулы ферритина состоит из
24 субъединиц, имеющих молекулярный вес 18500 - 19000. Общий молекулярный вес
апоферритина 445000. Электронно-микроскопические исследования показали, что
ферритин имеет полую оболочку с внутренним диаметром 70 - 80 А. Оболочка имеет
6 каналов, расширяющихся внутри (их диаметр 9-12 А).
Ядро ферритина состоит из мицелл железо-фосфатного комплекса,
имеющих кристаллическую структуру. Захват и освобождение железа осуществляется
через белковые каналы путем свободного пассажа, а его отложение и мобилизация
происходят на поверхности микрокристаллов. Стимуляция синтеза ферритина железом
является хорошо установленным фактом.
Как известно, печень является основным компонентом
ретикулоэндотелиальной системы. В конце жизнедеятельности эритроциты
фагоцитируются макрофагами этой системы, а освобождающееся железо или оседает в
печени в виде ферритина (гемосидерина), или возвращается в плазму крови и
захватывается в паренхиматозных клетках печени и мышц, а также в макрофагах
ретикулоэндотелиальной системы печени, селезенки и костного мозга.
Гемосидерин является вторым запасным соединением
железа в клетке и содержит значительно больше железа, чем ферритин. В отличие
от ферритина он нерастворим в воде. Существует достаточно аргументированное
предположение, что преобразование ферритина в гемосидерин происходит путем
постепенного перенасыщения ферритиновой молекулы железом с последующим ее
разрушением и образованием зрелого гемосидерина.
Внимание исследователей в последнее время привлекает
циркулирующий в крови ферритин. Вероятно, он происходит из клеток
ретикулоэндотелиальной системы. Имеются предположения, что сывороточный
ферритин является отражением активной секреции ферритина из печеночных клеток,
возможно из
связанных полисом. Таким образом, его присутствие в сыворотке
в небольшом количестве не является результатом разрушения клеток печени. Не
только его происхождение, но и биологическая роль в организме человека до
настоящего времени изучены недостаточно. Не вызывает сомнений точно
установленный факт концентрация сывороточного ферритина отражает состояние
запасного фонда железа в организме человека. Отметим, что хорошая зависимость
отмечена между уровнем сывороточного ферритина и мобилизуемыми запасами железа
в организме человека, изученных с помощью количественных кровопусканий, а также
между ферритином и концентрацией негеминового железа в тканях печени,
полученных с помощью биопсии у людей. Средняя концентрация его в сыворотке
крови у мужчин выше, чем у женщин, с колебаниями от 12 до 300 мкг/л.
.2
Внеклеточное железо
Во внеклеточных жидкостях железо находится в связанном
состоянии - в виде железо - белковых комплексов. Концентрация его в плазме
широко варьирует у здорового человека, составляет 10,8 - 28,8 мкмоль/л. с
достаточно большими суточными колебаниями, достигающими 7,2 мкмоль/л. Общее
содержание железа во всем объеме циркулирующей плазмы у взрослого человека
составляет 3 - 4 мг. Уровень железа в плазме крови зависит от ряда факторов:
взаимоотношения процессов разрушения и образования эритроцитов, состояния
запасного фонда железа в желудочно - кишечном тракте. Однако наиболее важной
причиной, определяющей уровень плазменного железа, является взаимодействие
процессов синтеза и распада эритроцитов.
Железо-связывающий белок трансферрин, открытый шведскими
учеными, содержится в небольшом количестве в плазме крови. Общая
железо-связывающая способность плазмы, характеризующаяся практически
концентрацией трансферрина, колеблется от 44,7 до 71,6 мкмоль/л, а свободная
железо-связывающая способность - резервная емкость трансферрина - составляет
28.8 - 50.4 мкмоль/л у здорового человека.
В плазме здорового человека трансферрин может находиться в 4
молекулярных формах:
) апотрансферрина;
) моножелезистого трансферрина А - железо занимает только А -
пространство;
) моножелезистого трансферрина В - железо занимает только
В-пространство;
) дижелезистого транферрина - заняты А и В пространства.
Молекулярный вес трансферрина 76000 - 80000, он состоит из
единственной полипептидной цепочки с расположенными на ней двумя значительно
схожими, если не идентичными, металлсвязывающими пространствами. Эти пространства
(А и В) наиболее прочно связывают железо по сравнению с ионами других металлов.
Около 6% железо-связывающего белка составляют углеводные остатки, находящиеся в
2 ответвляющихся цепочках и заканчивающихся сиаловой кислотой. Углеводы,
вероятно, не участвуют в механизме захвата железа. Синтезируется трансферрин
преимущественно в паренхиматозных клетках печени. Функции трансферрина в
организме представляют значительный интерес. Он не только переносит железо в
различные ткани и органы, но и "узнает" синтезирующие гемоглобин
ретикулоциты и, возможно другие нуждающиеся в железе клетки. Трансферрин отдает
железо им только в том случае, если клетки имеют специфические рецепторы,
связывающие железо. Таким образом, этот железо-связывающий белок функционирует как
транспортное средство для железа, обмен которого в организме человека зависит
как от общего поступления железа в плазму крови, так и от его количества,
захваченного различными тканями соответственно количеству в них специфических
рецепторов для железа. Кроме того трансферрин обладает защитной функцией -
предохраняет ткани организма от токсического действия железа.
Анализируя биологическую роль трансферрина в организме,
следует упомянуть о результатах экспериментальных исследований,
свидетельствующих о способности этого белка регулировать транспорт железа из
лабильных его запасов в эпителии клеток желудочно-кишечного тракта в плазму
крови. Из плазмы железо захватывается преимущественно костным мозгом для
синтеза гемоглобина и эритроцитов, в меньшей степени - клетками
ретикулоэндотелиальной системы и откладывается в виде запасного железа,
некоторое количество его поступает в неэритропоэтические ткани и используется
для образования миоглобина и ферментов тканевого дыхания (цитохромы, каталаза и
т.д.). Все эти процессы являются сложными и до конца не изученными.
Однако некоторые этапы наиболее важного процесса передачи
железа трансферрином клеткам костного мозга можно представить следующим
образом:
) адсорбция трансферрина рецепторными участками на
поверхности ретикулоцитов;
) образование прочного соединения между трансферрином и
клеткой, возможно проникновение белка в клетку;
) перенос железа от железо-связывающего белка к
синтезирующему гемоглобин - аппарату клетки;
) освобождение трансферрина в кровь.
Известно, что количество связывающих
трансферрин
пространств максимально в ранних
эритроидных
предшественниках и уменьшается по мере
созревания этих клеток.
Железо-связывающий белок лактоферрин обнаружен во многих
биологических жидкостях: молоке, слезах, желчи, синовиальной жидкости,
панкреатическом соке и секрете тонкого кишечника. Кроме того, он находится в
специфических вторичных гранулах нейтрофильных лейкоцитов, образуясь в клетках
миелоидного ряда со стадии промиелоцита. Подобно трансферрину, лактоферрин способен
связывать 2 атома железа специфическими пространствами. Он состоит из одной
полипептидной цепочки, молекулярный вес приблизительно равен 80000. В
физиологических условиях этот железо-связывающий белок насыщен железом до 20% в
ничтожных количествах он содержится в плазме крови, освобождаясь в нее из
нейтрофильных лейкоцитов. Несмотря на схожесть лактоферрина и трансферрина, эти
железо-связывающие белки отличаются друг от друга по антигенным свойствам,
составу аминокислот, белков и углеводов.
В настоящее время известны следующие функции этого белка:
бактериостатическая, участие в иммунных процессах и абсорбции железа в
желудочно-кишечном тракте. Свободный от железа лактоферрин - аполактоферрин
обладает бактериостатическими свойствами, которые теряются при насыщении его
железом. Аполактоферрин тормозит in vitro рост бактерий и грибов, и возможно,
играет роль во внутриклеточной гибели микроорганизмов. При низкой концентрации
лактоферрина в нейтрофильных лейкоцитах может уменьшаться их бактерицидная
активность.
Растворимые рецепторы трансферрина (sTfR) - это белки,
расположенные на поверхности клеток, которые обеспечивают перенос ионов железа
внутрь клетки с её поверхности. Часть из них растворима и находится в крови.
Рецептор состоит из двух пептидных цепей, проходящих сквозь мембрану клетки.
Молекула транферрина, несущая до двух атомов железа, присоединяется к внешнему,
экстрацеллюлярному концу рецептора, после чего поглощается клеткой путем
эндоцитоза. В сформированной везикуле происходит изменение рН, железо меняет
степень окисления (с Fe3+ на Fe2+) и, в дальнейшем,
используется для синтеза гемоглобина или сохраняется в форме депонированного
железа. Белковая часть трансферрина, освободившись от железа, вместе с
рецептором выходит на поверхность клетки, где апотрансферрин отделяется и весь
цикл повторяется. При повышенной потребности в железе цикл рецептора
трансферрина ускоряется и все больше рецепторов располагается на поверхности
клетки. При этом все чаще внешняя (внеклеточная) часть рецептора подвергается расщеплению
экстрацеллюлярными протеазами. В результате воздействия протеаз от рецептора
отделяется и попадает в кровь довольно стабильный фрагмент - пептид с
молекулярным весом 95 a, называемый растворимым рецептором трансферрина,
концентрацию которого можно определить с помощью иммуноферментного метода.
Приблизительно 80% рецепторов трансферрина находится на плазматической мембране
эритропоэтических клеток. Кроме того, наличие рецептора показано в клетках
плаценты, в лимфоцитах и даже в некоторых опухолевых клетках. Плотность
рецептора трансферрина на поверхности клеток-предшественников эритроцитов
повышается, по мере развития клеток, вплоть до ретикулоцита, однако на
поверхности зрелого эритроцита рецепторов трансферрина не обнаружено.
Мониторинг уровня sTfR позволяет определить терапевтический успех применения
эритропоэтина. Обычно при адекватной стимуляции эритропоэтической системы, sTfR
начинает повышаться. При локальном дефиците железа уровень ферритина и sTfR
изменяются разнонаправлено: ферритин снижается, sTfR повышается. При повышении
ферритина при хронических воспалениях, опухолях, эффективную потребность железа
можно оценить только при определении концентрации sTfR.
Железосерные ферменты - это еще один важный
класс железосодержащих ферментов, участвующих в переносе электронов в клетках
животных, растений и бактерий. Железосерные ферменты не содержат гемогрупп, они
характеризуются тем, что в их молекулах присутствует равное число атомов железа
и серы, которые находятся в особой лабильной форме, расщепляющейся под
действием кислот. К железо - серным ферментам относится, например, ферредоксин
хлоропластов, осуществляющий перенос электронов от возбужденного светом
хлорофилла на разнообразные акцепторы электронов.
2.
Медико-биологические основы обеспечения организма железом
2.1
Эритропоэз
Эритропоэз - один из самых мощных процессов образования
клеток в организме. За 70 лет человек производит около 3,5 тонн эритроцитов. У
взрослого человека эритропоэз протекает в костном мозге. Родоначальниками
кроветворения являются стволовые клетки, способные давать все ростки клеток
крови.
2.1.1
Эритроидный ряд клеток.
Собственно эритроидный ряд (см. табл. 2.1.1) начинается с
проэритробластов - потомков стволовых клеток, у которых появляется
чувствительность к эритропоэтину. В проэритробластах начинается синтез
гемоглобина, продолжающийся в ряду созревающих клеток. По мере накопления
гемоглобина в последующих клетках деление приостанавливается, ядро уменьшается
в размере. На последнем этапе ядро из клетки удаляется, затем исчезают остатки
РНК, еще выявляемые при специальной окраске в молодых эритроцитах -
ретикулоцитах. Наиболее известным фактором, регулирующим эритропоэз, является
гормон эритропоэтин (ЭПО), синтезируемый в почках. Уровень ЭПО повышается при
быстром развитии гипоксии - обильная кровопотеря, острый гемолиз, острая ишемия
почек, подъем в горы. При хронических анемиях уровень ЭПО, как правило,
нормален, исключая апластическую анемию, сопровождающуюся чрезвычайно высоким
уровнем гормона.
табл. 2.1.1
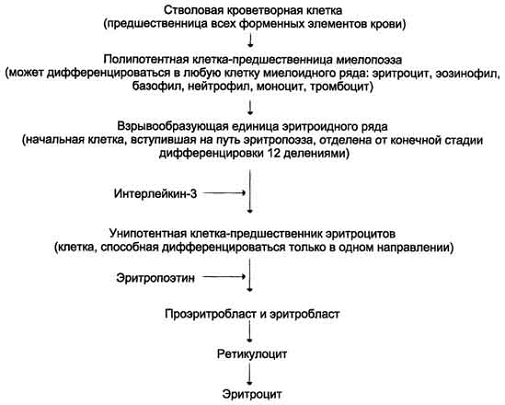
2.1.2
Регуляция эритропоэза
Наряду с ЭПО, в крови присутствуют ингибиторы эритропоэза
(ИЭПО). Это разнообразные вещества, часть которых относится к
среднемолекулярным токсинам, образующимся в нормальных и патологических процессах.
Баланс активности ЭПО и ИЭПО регулирует эритропоэз. При необходимости
экстренной регенерации индуцируется эритропоэтиновый механизм - значительное
преобладание активности ЭПО над активностью ИЭПО. При почечной недостаточности
и ряде хронических заболеваний, сопровождающихся повышенным образованием или
нарушением выведения среднемолекулярных токсинов, активность ИЭПО доминирует
над ЭПО, что ведет к угнетению эритропоэза и развитию анемии хронических
заболеваний.
2.2 Синтез
гемоглобина
Гемоглобин составляет 95% белка эритроцитов. Молекула
гемоглобина состоит из двух пар различных по структуре цепей глобинового белка,
в каждой из которых находится железосодержащая протопорфириновая группа - гем.
Синтез гемоглобина начинается с ранних этапов эритропоэза и идет путем
синхронной продукции гема и глобиновых цепей с образованием законченной
молекулы.
Образование гемоглобина регулируется ЭПО, рост концентрации
которого ускоряет синтез глобина. Активность поступления железа в клетки
костного мозга также регулирует образование гемоглобина. Уровень железа в
клетках определяет скорость образования гема. В свою очередь, свободный гем
через белки-регуляторы усиливает синтеза глобина. Эта связь систем синтеза гема
и глобина синхронизирует их работу - в норме лишь незначительное количество
свободного протопорфирина и глобина остается не связанным в гемоглобине.
2.3
Регенерация красной крови
Действие многих факторов ведет к нарушению мембран и
внутренней структуры эритроцитов. Физиологический гемолиз измененных эритроцитов
- постоянный процесс в организме. Основная масса эритроцитов разрушается в
селезенке. Здесь имеется открытый кровоток, и эритроциты плотно контактируют с
макрофагами в паренхиме органа. У здорового человека разрушается 180-270 млн.
эритроцитов в сутки. Железо этих эритроцитов накапливается в макрофагах и
обменивается через трансферрин крови с костным мозгом и другими органами и
тканями. В норме скорость регенерации красной крови соответствует уровню
физиологического гемолиза. При массивной кровопотере или повышенном
кроверазрушении активность эритропоэза за счет выброса ЭПО может возрастать в
сотни раз. Адекватный уровень эритропоэза невозможен при недостатке или
нарушениях обмена ряда незаменимых, поступающих только с пищей веществ. Витамин
В12 и фолиевая кислота, участвуя в обмене нуклеотидов, являются незаменимыми
факторами для синтеза ДНК и деления любых клеток. Недостаток в организме этих
витаминов приводит к развитию мегалобластных анемий: В12-дефицитной и
фолиеводефицитной анемии. Недостаточное поступление железа в клетки костного
мозга ограничивает возможность синтеза гема и, как следствие, - гемоглобина.
Угнетение синтеза гема наблюдается и при недостатке витамина В6, в связи с тем,
что этот процесс осуществляется ферментами, зависимыми от пиридоксина.
Недостаток в организме железа и витамина В6 сопровождается развитием
микроцитарных анемий: сидеропенической (ЖДА) и сидеробластной, соответственно.
.4 Метаболизм
железа
.4.1 Обмен
железа
В организме здорового человека содержится около 3-4 г железа
(40-50 мг Fe/кг). Выделяют три фонда железа: - функциональное железо находится
в составе гемоглобина, миоглобина и железосодержащих энзимов. - транспортная
форма представлена железом в составе трансферрина. - депонированное железо
находится в составе ферритина и гемосидерина внутренних органов. Обмен железа
является высокоорганизованным процессом, в котором все железо, выделяемое при
распаде гемоглобина и других железосодержащих белков, вновь утилизируется.
Поэтому, несмотря на то, что ежедневно абсорбируется и выводится лишь малая
часть железа (0,03-0,05%), его метаболизм очень динамичный. Кинетика железа
здорового мужчины весом 70 кг имеет следующие параметры: эритроциты - 2000-2500
мг; плазма - 4 мг; запасы - 800-1000 мг; миоглобин и ферменты - 300 мг; всасывание
- 1-2 мг/сутки; потери - 1-2 мг/сутки; высвобождение при гемолизе - 25
мг/сутки; потребление при эритропоэзе - 25 мг/сутки.
Содержание железа в сыворотке в норме приведено ниже
(Табл.2.4.1).
Табл. 2.4.1
|
Возраст
|
Содержание
железа
|
|
Мкг/дл
|
Ммоль/л
|
|
Новорожденные
|
100-200
|
17,9-44,75
|
|
Дети до 2 лет
|
40-100
|
7,16-17,9
|
|
Дети старше 2
лет
|
50-120
|
8,95-21,48
|
|
Взрослые:
|
|
|
|
Мужчины женщины
|
50-160 40-150
|
8,95-28,64
7,16-26,85
|
|
|
|
|
|
|
|
|
2.4.2 Этапы
обмена железа в организме
Процесс усвоения железа состоит из ряда последовательных
этапов:
) начальный захват железа щеточной каймой клеток слизистой
оболочки кишечника.
) внутриклеточный транспорт, образование запасов железа в
клетке.
) освобождение железа из слизистой оболочки кишечника в
кровь.
В экспериментальных исследованиях выяснилось, что клетки
эпителия слизистой оболочки кишечника чрезвычайно быстро забирают железо из его
полости. А ультразвуковые исследования показали, что первый этап обеспечивает
достаточную концентрацию железа на поверхности слизистой оболочки клеток для
последующего его усвоения организмом. При этом железо концентрируется щёточной
кайме, превращения происходят на мембране микроворсинок.
Второй этап - это поступление железа в богатую рибосомами
цитоплазму и межклеточное пространство. И, наконец, третий этап - перенос
железа в кровеносные сосуды.
Комплекс трансферрин-железо, образовавшийся в результате
захвата железа из клетки слизистой оболочкой кишечника, поступает главным
образом в костный мозг, небольшая его часть - в запасный фонд, преимущественно
в печень, и ещё меньшее количество железа забирается тканями для образования
миоглобина, некоторых ферментов тканевого дыхания и нестойких комплексов железа
с аминокислотами и белками.
Основным источником плазменного железа являются его
поступления из внутренних органов, таких как печень, селезёнка, костный мозг,
где происходит разрушение гемоглобина эритроцитов. Небольшое количество железа
поступает в плазму из запасного фонда и при взятии его из пищи в
желудочно-кишечном тракте. Преобладающим циклом в обмене железа в организме
человека является образование и разрушение гемоглобина эритроцитов, что
составляет 25 мг железа в сутки. Фермент сыворотки крови, вероятно, осуществляет
транспортировку железа к клеткам печени, однако его роль в общем обмене железа
в организме человека представляется минимальной.
Обмен железа между транспортным и тканевым его фондами изучен
недостаточно, так как пути и движения железа из тканей в плазму крови и
наоборот изучены мало. Расчётные данные, однако, свидетельствуют о том, что
величина плазменно-тканевого обмена железа составляет приблизительно 6 мг в
сутки.
2.4.3 Потери
железа
Потери железа из организма в норме происходят, главным образом,
через кишечник: часть выделяется вместе с желчью, часть - с отторгающимся
эпителием. Кроме того, железо теряется с эпителием кожи, волосами, с мочой, а у
женщин репродуктивного возраста - с менструальными кровопотерями.
2.4.4
Регуляция метаболизма железа
Усвоение железа зависит от его запасов в организме: при
дефиците - возрастает, а при избыточном накоплении - снижается. Роль основного
регулятора метаболизма железа выполняют мукозный и плазменный трансферрин.
Мукозный трансферрин (мобилферрин) синтезируется в печени и
выделяется с желчью. В просвете кишечника ионы железа связываются мобилферрином
и транспортируются в энтероциты, где железо отделяется от белка и концентрация
мобилферрина возрастает, что способствует увеличению поступления железа в слизистые
кишечника. При дефиците железа увеличивается и содержание трансферрина в плазме
крови. В результате, переход железа из слизистой в транспортную форму протекает
быстро и эффективно. Низкие же запасы железа позволяют трансферрину быстро
высвобождать железо в тканях и возвращаться в новый транспортный цикл.
Следствием таких адаптивных сдвигов при дефиците железа
являет существенное повышение его абсорбции из пищи. Избыточное накопление
железа в организме сопровождается истощением резервных возможностей ферритина,
что затрудняет высвобождение транспортного железа в тканях. Это в свою очередь
увеличивает степень насыщения трансферрина, и он теряет свои резервы в
связывании железа. Переход железа из клеток слизистой в транспортную форму
угнетается - большая часть железа, поступающего в клетки кишечника, фиксируется
в ферритине слизистых и эвакуируется из организма при отторжении эпителия.
3.
Клинико-лабораторные характеристики красной крови и обмена железа
Изучение состояния крови и обмена железа, как правило,
начинается рутинным исследованием периферической крови. Основными показателями,
отражающими состояние красной крови, являются концентрация гемоглобина (Hb) и
количество эритроцитов (Er). Снижение показателя Hb ниже уровня 120 г/л, часто
сопровождающееся понижением Er, расценивается как анемическое состояние.
Превышение же нормальных показателей может развиваться в условиях высокогорья,
при хронических заболеваниях легких и эритропролиферативных заболеваниях.
Большое значение в клинической практике имеет гематокрит (Ht)
- показатель общего объема эритроцитов в крови. Значение Ht зависит от объема
плазмы крови, численности и размеров эритроцитов. Снижение Ht наблюдается при
гемодилюции и анемиях. Следует иметь в виду, что гематологические анализаторы
оценивают Ht не путем центрифугирования, а расчетным методом, что не исключает
возможность значительной погрешности.
Для выяснения патогенеза нарушений красной крови важное
значение имеют индексы насыщения эритроцитов гемоглобином. В первую очередь,
это цветовой показатель (ЦП). Значения ЦП ниже 0,86 рассматривают как
гипохромные, в пределах нормы - как нормохромные, превышающие 1,10 - как
гиперхромные. Гипохромные состояния характерны для ЖДА, сидеробластной анемии,
талассемии, анемии при хронических заболеваниях. Гиперхромия эритроцитов
наблюдается при мегалобластной анемии. Такие индексы насыщения эритроцитов, как
среднее содержание гемоглобина в эритроците (MCH) и средняя концентрация
гемоглобина в эритроциты (MCHC), вычисляются по тем же физиологическим параметрам,
как и ЦП. Поэтому эти показатели отличаются лишь порядком числовых значений и,
имея однонаправленное клиническое значение, не вносят дополнительной
информации. Важной характеристикой красной крови является размер и форма
эритроцитов. Размеры эритроцитов варьируют в известных пределах -
физиологический анизоцитоз. Эритроциты с диаметром менее 6,7 мкм относятся к
микроцитам, с диаметром больше 7,7 мкм - к макроцитам, а с диаметром больше 9,5
мкм - к мегалоцитам. Соотношение эритроцитов различных размеров выражается
графически в виде эритроцитометрической кривой. Сдвиг вершины кривой вправо
означает преобладание макро - и даже мегалоцитов, сдвиг влево - преобладание
микроцитов. Уширение основания кривой указывает на значительную степень
анизоцитоза. Макро и мегалоцитоз характерны для мегалобластных анемий,
микроцитоз, часто в сочетании с анизоцитозом, - для ЖДА, сидеробластной анемии,
анемии при хронических заболеваниях, талассемии. Показатель среднего объема
эритроцитов (MCV) является расчетным5, значительно коррелирует со средним
размером эритроцитов.
Важные, надежные характеристики красной крови могут быть
получены при изучении морфологии эритроцитов на сухих мазках. Именно
морфологические исследования образцов крови позволяют отчетливо выявлять нарушения
размера (микро-, макро-, мегалоцитоз, анизоцитоз) и формы эритроцитов
(пойкилоцитоз), обнаруживать специфические для некоторых заболеваний
патологические формы эритроцитов.
Показателем, отражающим активность эритропоэза, является
количество ретикулоцитов (молодых эритроцитов). Пониженное число ретикулоцитов
характерно для апластических состояний, повышенное - наблюдается при активации
регенерации крови при гемолитической анемии, после острых кровопотерь, после
назначении препаратов железа при ЖДА, стимуляции эритропоэза ЭПО, фолиевой
кислотой, витамином В12. Изучение показателей обмена железа осуществляется
системой биохимических тестов. Концентрации протопорфирина в эритроцитах
отражает степень обеспеченности железом эритроидных клеток костного мозга. Количество
протопорфирина, - предшественника гема, возрастает в эритроцитах при угнетении
синтеза гема из-за дефицита железа в костном мозге. Показатель концентрации
сывороточного железа является отражением содержания в первую очередь
транспортного пула железа. Снижение этого показателя характерно для развернутых
форм железодефицитных состояний. Превышение нормальных значений может
свидетельствовать об избыточном накоплении железа.
При интерпретации уровня железа в сыворотке нужно иметь в
виду, что его концентрация подвержена суточным колебаниям - максимальная в
утренние часы. Показатель сывороточного железа непосредственно перед и во время
менструаций выше, чем после их окончания. Некоторые контрацептивы повышают
уровень сывороточного железа. Особо резко концентрация железа в сыворотке
повышается после приема железосодержащих лекарственных препаратов, но этот
подъем кратковременный - 2-4 дня после однократного приема, после чего,
возвращается к исходному уровню. Могут наблюдаться и случайные вариации уровня
сывороточного железа, например, при резком повышении мяса в рационе.
Общая железосвязывающая способность сыворотки (ОЖСС) отражает
степень "голодания" сыворотки и насыщения железом трансферрина. Суть
метода состоит в максимальном насыщении сыворотки железом и оценке количества
железа, которое может быть связано с белками в 1 литре сыворотки крови. Разница
между показателями ОЖСС и концентрацией железа в сыворотке характеризует
латентную железосвязывающую способность сыворотки (ЛЖСС). Этот показатель
отражает неиспользуемый резерв трансферриновой системы в связывании железа.
Отношение показателя сывороточного железа к ОЖСС, выраженное
в процентах называется коэффициентом насыщения трансферрина железом. Для
железодефицитных состояний характерно повышение ОЖСС, значительное повышение
ЛЖСС и снижение насыщения трансферрина. При избыточном накоплении железа
наблюдаются противоположные сдвиги - высокое насыщение трансферрина железом и
низкие значения ЛЖСС и ОЖСС. Показатели общего и свободного трансферрина в
сыворотке значительно коррелируют с показателями ОЖСС и ЛЖСС, соответственно, и
самостоятельное значение имеют лишь при диагностике редких нарушений обмена
железа обусловленных нарушением его транспорта. Наиболее специфичным и
чувствительным показателем, отражающим запасы железа, является уровень
ферритина в сыворотке. Снижение его концентрации наблюдается с самых ранних
стадий развития дефицита железа. А повышенный уровень характерен для состояний
с избыточным накоплением железа. Для избежания ошибок при интерпретации теста
сывороточного ферритина следует иметь в виду, что концентрация ферритина может
повышаться в острой фазе воспаления из-за его выхода из поврежденных клеток.
Косвенным показателем запасов железа в организме является
десфераловый тест. Десферал - комплексон, связывающий железо и выводящий его с
мочой. Тест состоит в оценке количества выделяемого с мочой железа после
введения 500 мг десферала. При дефиците запасов количество выделяемого железа
составляет 0,2 мг и ниже, а при избыточных резервах - превышает нормальный
уровень.
|
Показатель
|
Метод
|
Принцип метода
|
|
Ферритин
|
Турбидиметрический
|
Данный метод
основан на реакции образца, содержащего ферритин человека и специфических
ингибиторов с образованием нерастворимого комплекса, который может быть
измерен турбидиметрически при длине волны 700 нм. Концентрация ферритина
может быть определена путем построения стандартной кривой по поглощению
стандартов.
|
|
Железо
сыворотки
|
Колориметрический
|
Окисленный ион
железа освобождаясь в кислой среде от своего белкового носителя трансферина
полуколичественно восстанавливается в молекулярную форму. Затем
восстановленное железо образует комплексное соединение с чувствительным
индигатором железа - хромогеном, в результате чего получается голубой
хромофор, который имеет максимальную абсорбцию при 595 нм.
|
|
ОЖСС
|
Колориметрический
|
Избыток железа
добавлят в сыворотку, чтобы создать насыщенные условия для его белкового
носителя трансферина. Несвязанный ион железа осаждают карбонатом магния
(основным). После центрифугирования определяют содержание железа в
супернатанте.
|
|
Трансферрин
|
Иммунотурбидиметрический
|
Разведенные
пробы добавляют к буферу, содержащему специфические относительно
человеческого трансферрина (сайдерофилина) ингибиторы. Образующуюся мутность
раствора, которая пропорциональна концентрации трансферрина в образце,
измеряют турбидиметрически при 340 нм. После построения стандартной кривой
(абсорбция относительно разведений стандарта) определяют концентрацию
трансферрина в образце. Анализ можно выполнять вручную (при комнатной
температуре) или с помощью автоматического анализатора.
|
4.
Железодефицитные состояния
4.1
Определение
Железодефицитное состояние или недостаточность железа
определяется как дефицит общего железа, обусловленный несоответствием между его
поступлением и расходом (потери или возросшее потребление), приводящим к
отрицательному балансу.
Железодефицитная анемия (ЖДА) - синдром, характеризующийся
снижением наполнения гемоглобина железом с последующим уменьшением содержания
гемоглобина в эритроците и угнетением эритропоэза из-за дефицита железа.
4.2 Этиология
и патогенез железодефицитных состояний
Железодефицитные состояния всегда являются лишь синдромом,
осложняющим самые разные заболевания, патогенез которых прямо или косвенно
затрагивает метаболизм железа.
В развитие дефицита железа вовлечены два основных механизма:
уменьшение снабжения железом и повышенная потребность в железе. Недостаточное
обеспечение организма железом может наблюдаться из-за его недостатка в пищевом
рационе (алиментарная недостаточность) или нарушения всасывания железа.
Повышение потребности организма в железе может быть вызвано физиологически и
патологически обусловленными причинами. Естественными, физиологическими
факторами являются: рост организма детей и подростков, менструации,
беременность, лактация. К естественным причинам следует отнести также рост
мышечной массы и объема крови при физических нагрузках.
Под влиянием патологических причин рост потребности в железе
происходит либо вследствие увеличения потерь железа при хронических и 25 острых
кровопотерях, либо вследствие перераспределения железа в организме с
исключением его из основного метаболизма.
4.2.1
Алиментарная недостаточность
Недостаток железа в пище способствует развитию дефицита
железа из-за отсутствия компенсации его потерь. Различия в усвоении гемового и
негемового железа являются решающими в биодоступности железа пищи. Железо в
мясных продуктах, представленное в форме гема, усваивается на 20-30% независимо
от состава пищи. В то время, как железо из растительной пищи, представленное
неорганическими солями, усваивается лишь при определенных условиях на 1 - 7%.
Алиментарная недостаточность в большей степени имеет значение
для лиц, придерживающихся вегетарианской диеты, с низким социально -
экономическим уровнем жизни, у больных с психической анорексией. Как правило,
алиментарная недостаточность играет роль в сочетании с другими причинами
дефицита железа, чаще - в содружестве с повышенной кровопотерей.
4.2.2
Нарушение усвоения железа
Любые патологические состояния двенадцатиперстной и
проксимальных отделов тонкой кишки могут приводить к развитию дефицита железа.
Значительное нарушение всасывания железа может быть последствием гастроэктомии
с выключением части двенадцатиперстной кишки, резекции тонкой кишки или хронического
панкреатита и обусловленного им синдрома мальабсорбции. У некоторых больных,
нарушенная абсорбция железа может маскироваться общими синдромами, такими как
стеаторрея, спру, целиакия или диффузный энтерит. Атрофический гастрит и
сопутствующая ахлоргидрия также снижают всасывание железа. Недостаточность
железа часто возникает после операций на желудке и гастроэнтеростомии.
Нарушение всасывания железа может быть обусловлено избыточным
содержанием в продуктах питания ингибиторов абсорбции железа (фитины, танины,
фосфаты, оксалаты, кальций). Специфической причиной низкого усвоения железа
может являться дефицит меди в организме меди, который нередко развиваться при
длительном, несбалансированном применении препаратов цинка, блокирующих
усвоение меди. Угнетение абсорбции железа может развиваться и вследствие
длительного применение при язвенной болезни и гастродуоденитах антацидов и
препаратов с обволакивающим механизмом действия. Как самостоятельный фактор,
нарушение всасывания железа является редкой причиной развития дефицита железа,
но он приобретает большое значение при сочетании с другими факторами,
нарушающими метаболизм железа.
4.2.3
Кровопотери
Острые потери крови, снижая количество эритроцитов, ведут к
развитию острой постгеморрагической анемии. В дальнейшем, в зависимости от
степени кровопотери, компенсаторной реакции эритропоэза и наличия резервов
железа, может развиваться картина железодефицитного состояния. Но, тем не
менее, ведущее место среди причин дефицита железа занимают хронические кровопотери.
Маточные кровопотери являются основной причиной дефицита
железа у женщин репродуктивного возраста. Они могут наблюдаться при меноррагиях
различной этиологии, яичниковой дисфункции, аденоматозе, миоме матки,
эндометриозе, злокачественных опухолях матки, наличии внутриматочных
контрацептивов. Кровопотери из кишечной трубки являются наиболее частой
причиной дефицита железа у мужчин и неменструирующих женщин. Потери крови могут
возникать на всех уровнях пищеварительной системы. При воспалительных заболеваниях
десен, стоматитах, тромбоцитопатиях, ДВС-синдроме, ангиоматозах могут
наблюдаются хронические десневые кровотечения. Эрозивный эзофагит (чаще - при
недостатке кардии или грыже пищеводного отверстия диафрагмы), варикоз вен
пищевода и кардиального отдела желудка (при циррозе печени и других формах
портальной гипертензии) могут стать причинами хронических пищеводных
кровопотерь. Эрозии желудка, язвы желудка и двенадцатиперстной кишки, опухоли и
полипы желудка могут стать причиной хронических кровопотерь, связанных с
патологией желудка. Значение хронических кровопотерь из кишечника как причины
дефицита железа увеличивается с возрастом из-за роста частоты дивертикулеза
тонкого кишечника, дивертикулярной болезни, опухолей тонкого кишечника, чаще -
полипоза и опухолей толстого кишечника. Реже потери крови из кишечника
обусловлены болезнью Крона и неспецифическим язвенным колитом.
Кровоточащий геморрой является также одной из самых
распространенных причин дефицита железа. Носовые кровотечения, как и десневые,
являются причиной развития дефицита железа, главным образом, у больных с
геморрагическими диатезами (телеангиоэктазия, тромбоцитопатия,
тромбоцитопенические пурпуры, ДВС - синдром) или при ангиопатиях-ангиоматозах.
Относительно редкой причиной дефицита железа являются кровопотери в замкнутые
полости и ткани, которые могут наблюдаться при эндометриозе, изолированном
легочном сидерозе, ангиопатиях, гломических опухолях. Причиной недостаточности
железа также может являться гематурия, наблюдаемая при хроническом гематурическом
нефрите, мочекаменной болезни, поликистозе почек, геморрагическом цистите, а
также перманентном внутрисосудистом гемолизе (болезнь Маркиафавы),
пароксизмальной ночной гемоглобинурии, механическом внутрисосудистом гемолизе
(маршевая анемия).
Значительную и часто неоцениваемую адекватно роль играют
ятрогенные кровопотери. К развитию дефицита железа могут приводить частые,
повторные заборы крови для исследований.
4.2.4
Перераспределение и конкурентное потребление железа
Железо необходимо для развития практически всех
микроорганизмов. Поэтому избыточное развитие нормальной или патогенной флоры
кишечника при дисбиозах неизбежно приводит к усиленному конкурентному
потреблению микроорганизмами железа из пищи и, как следствие, к уменьшению
поступления железа в организм. Самостоятельно этот фактор имеет существенное
значение в развитии дефицита железа у детей раннего возраста, при тяжелых
дисбактериозах, и у пожилых людей, при гиперплазии кишечной флоры в
дивертикулах и мегаколон. Но чаще имеет место сочетание конкурентного
потребления железа кишечной флорой и хронических кровопотерь из ЖКТ. Нарушение
метаболизма железа наблюдается при многих хронических инфекционных заболеваниях
бактериальной природы. Здесь также развивается конкурентное потребление железа
патогенной флорой. Но более значимым для развития дефицита является в этих
случаях перераспределение железа в организме: длительная высокая активность
макрофагов сопровождается накоплением значительного количества железа в
ретикулоэндотелиальных клетках и его блокированием от участия в основном
метаболизме минерала в организме. В результате без истинного дефицита железа
развивается картина железодефицитного состояния. Подобное перераспределение
железа в организме с исключением его из основного обмена также может
наблюдаться при опухолевых процессах, когда значительное количество железа
блокируется в неопластической ткани.
4.2.5
Нарушения транспорта железа
Картина железодефицитного состояния без истинного дефицита
железа может развиваться при снижении в крови уровня трансферрина. Это может
иметь место при гипопротеинемиях различной этиологии (нефротический синдром,
нарушение белок-синтетической функции печени, синдром мальабсорбции,
алиментарная белковая недостаточность). В редких случаях концентрация трансферрина
или нарушения его строения могут быть генетически детерминированы.
4.3
Клиническая картина железодефицитных состояний
Общепринятой классификации железодефицитных состояний не
существует. По степени развития дефицита железа и выраженности клинических
проявлений выделяют несколько стадий железодефицитных состояний.
Стадия истощения запасов железа (латентный дефицит железа).
Потеря железа превышает его поступление - запасы железа уменьшаются. У пациента
отсутствуют какие-либо симптомы. Гематокрит, гемоглобин, индексы насыщения
эритроцитов, морфология эритроцитов - в пределах нормы. Сывороточное железо - в
норме, ферритин сыворотки, количество железа в костном мозге и насыщение
трансферрина - снижены, ОЖСС повышена. Всасывание железа в кишечнике компенсаторно
увеличено.
Стадия железодефицитного эритропоэза. Истощение запасов
железа начинает угнетать эритропоэз. У пациента умеренно представлена
симптоматика гипосидероза. Уровень гемоглобина на грани нормы. Гематокрит,
индексы насыщения и морфология эритроцитов - в пределах нормы. Железо запасов
отсутствует или резко снижено. Низкий уровень железа и ферритина сыворотки,
низкое насыщение трансферрина, ОЖСС и КПЭ - повышены.
Стадия железодефицитной анемии (клинически манифестированный
дефицит железа). ЖДА легкой степени. Начало развернутой стадии железодефицита.
У пациента активная симптоматика гемосидероза, анемическая симптоматика
отсутствует или умеренная. Гемоглобин снижен до 90 г/л, нередко при нормальных
индексах насыщения эритроцитов гемоглобином и их морфологии. Низкие или
отсутствующие запасы железа. Ферритин, железо сыворотки и насыщение
трансферрина - на низком уровне, ОЖСС и КПЭ - повышены. Выраженная ЖДА
(субкомпенсированная). У пациента активная сидеропеническая и анемическая
симптоматика. Гемоглобин снижен в пределах 90-70 г/л. Со стороны эритроцитов -
явная картина гипохромии и микроцитоза: Отсутствие запасов железа. Ферритин
сыворотки, железо сыворотки, насыщение трансферрина - на очень низком уровне,
показатели ОЖСС и КПЭ - резко повышены. Тяжелая ЖДА. У пациента картина
тяжелого анемического синдрома с циркуляторными нарушениями и тканевой
гипоксией. Гемоглобин резко снижен (<70 г/л). Микроцитоз, гипохромия.
Ферритин, железо сыворотки и насыщение трансферрина крайне снижены. Клиническая
картина железодефицитных состояний чрезвычайно разнообразна, и в меньшей
степени обусловлена анемическим синдромом, а в большей - сидеропенией.
4.3.1
Сидеропения (гипосидероз)
Гипосидероз связан с тканевым дефицитом железа, необходимого
для нормальной трофики органов и тканей. Уже на ранних стадиях развития
дефицита железа снижаются его запасы в тканях и наблюдаются изменения со
стороны максимально чувствительных к дефициту тканевого железа систем. К
трофическим нарушениям вследствие гипосидероза относится и вторичный
иммунодифецит, проявляющийся склонностью к хронизации воспалительных процессов
и частыми инфекционно-воспалительными заболеваниями. Симптоматика гипосидероза
зависит от глубины тканевого дефицита железа. При значительном дефиците железа,
сопровождающем анемию, ведущими проявлениями являются изменения со стороны кожи
и ее придатков, общая слабость, невозможность сосредоточиться, снижение памяти,
утомляемость, длительная астенизация после перенесенных заболеваний, появление
специфической бледности кожи, часто с алебастровым или зеленоватым оттенком.
Гипосидероз без анемического синдрома имеет большое
самостоятельное значение, так как имеются доказательства того, что клинически
не манифестированный дефицит железа играет роль в развитии умственной отсталости
детей, сердечной недостаточности, болезни Паркинсона и Альцгеймера.
4.3.2
Анемический синдром.
Анемический синдром при железодефицитных состояниях
проявляется хорошо известными и неспецифическими для анемии любого
происхождения симптомами, выраженность которых во многом зависит от скорости
снижения уровня гемоглобина. Как правило, ЖДА развивается постепенно, и больные
адаптируются к ней, часто приписывая свои недомогания переутомлению,
психическим и физическим перегрузкам. В связи с этим в клинической картине ЖДА
доминируют симптомы гемосидероза, а не малокровия.
4.4
Диагностика железодефицитных состояний
В практике спортивной медицины железодефицитные состояния,
как правило, выявляются при проведении плановых обследований состояния здоровья
спортсменов. Причем, чаще всего при этом выявляются лабораторные признаки уже
развернутых, клинически манифестированных стадий дефицита - ЖДА. Очевидно, что
в таких случаях организм спортсмена уже длительное время находился под
негативным влиянием дефицита железа клинически неявных, латентных стадий.
Поэтому, крайне актуально не только безошибочное, но и максимально раннее
выявление железодефицитных состояний у спортсменов. В этом случае следует
рассмотреть всю последовательность диагностического поиска при подозрении
наличия железодефицитного состояния, которую можно условно представить в виде
ряда последовательных этапов.
4.4.1
Доказательство наличия анемии
На второй стадии диагностического поиска производится
лабораторное исследование крови. Несмотря на рутинный характер этого
исследования, на этом этапе могут быть ошибки как ложноположительной, так и
ложноотрицательной диагностики анемии. Анемия может маскироваться наступившим
сгущением крови при патологических процессах, сопровождающихся обильной рвотой,
профузными поносами, полиурией. При подобных явлениях, лабораторный этап
диагностики нарушений обмена железа можно корректно провести лишь после
устранения патологических причин дегидратации организма. У спортсменов сгущение
крови может наблюдаться при форсированной сгонке веса, которая, по сути,
представляет собой вариант интенсивной дегидратации организма. Разжижение
крови, гемодилюция, возникает при искусственном перенасыщении крови
трансфузионными растворами, в результате задержки жидкости в сосудистом русле
или обильном притоке в кровь тканевой жидкости. При гемодилюции количество
гемоглобина и численность эритроцитов в единице объема крови будет снижено.
Подобная "анемия", вернее, псевдоанемия, носит временный характер и
проходит по мере того, как исчезает вызвавший ее "отек крови".
Проблема разделения анемии и псевдоанемии особо остро стоит в спортивной
медицине в связи с тем, что сама спортивная деятельность предрасполагает к
развитию состояния гемодилюции. Активная мышечная деятельность, усиливая
метаболизм и потоотделение, вызывает интенсивное обезвоживание организма - при
нагрузках на выносливость спортсмен может терять до 2-3 литров воды в час. В
ответ на потерю воды и электролитов системы регуляции реагируют выбросом в
кровь гормонов вазопрессина и альдостерона. Вазопрессин уменьшает диурез, а
альдостерон, задерживая натрий в плазме крови, удерживает ее объем в нормальных
пределах. Если в ходе подобных нагрузок атлет своевременно не восполняет запасы
воды и электролитов соответственно их потерям, то к моменту окончания нагрузок
содержание альдостерона в крови может быть столь высоким, что последующее за
этим активное удержание жидкости в организме спортсмена может сопровождаться
состоянием гемодилюции в течение нескольких суток. Очевидно, чтобы однозначно
разделить анемию и псевдоанемию, необходимо провести инструментальную оценку
объема циркулирующей крови. К сожалению, эти методы исследования малодоступны
для широкой практики. Поэтому, помощь в разделении гемодилюции и анемии может
оказать изучение морфологии эритроцитов (при гемодилюции не происходит
изменение степени насыщенности эритроцитов гемоглобином и их размеров) и уровня
сывороточного железа и ферритина (при гемодилюции наблюдается нормальный или
незначительно пониженный уровень).
4.4.2 Доказательство
наличия латентного дефицита железа
Дефицит железа более чем в половине случаев протекает в
скрытой, клинически неявной форме, без развития ЖДА. Поэтому при диагностике
железодефицитных состояний важно четко понимать, что на начальных стадиях
железодефицита недостаток железа в организме сопровождается истощением его
запасов в тканях. Но именно трофические нарушения, вызванные дефицитом
тканевого железа ответственны за развитие основных негативных последствий
недостаточности железа для организма человека: резкое угнетение аэробного
энергетического обмена, патологические изменения со стороны
сердечно-сосудистой, нервной, пищеварительной, иммунной систем. Развитие
клинически явной формы дефицита железа, - ЖДА, для человека, по сути, лишь
дополняет последствия дефицита тканевого железа генерализованной гемической
гипоксией. Поэтому, как при целенаправленном диагностическом поиске с наличием
у врача гипотезы о дефиците железа у пациента, так и при проведении планового
обследования состояния здоровья пациента, отсутствие в результатах
лабораторного исследования крови признаков анемии не должно отвергать
необходимость изучения состояния запасов железа в организме.
Часто используемый в клинической практике показатель
концентрации сывороточного железа не является адекватным отражением состояния
запасов железа. Снижение содержания железа в сыворотке наблюдается лишь при
полном истощении депо железа, на стадии железодефицитного эритропоэза. Кроме
того, показатель сывороточного железа при его фактически истощенных запасах
может за несколько часов увеличиться после приема препаратов железа, в том
числе, витаминно-минеральных комплексов.
Корректная оценка состояния запасов железа в организме
проводится по показателям ОЖСС и концентрации ферритина в сыворотке крови, изменение
которых отмечается с самых ранних стадий развития дефицита железа.
4.4.3
Доказательство гипохромности анемии
Под термином гипохромность понимают снижение содержания
гемоглобина в эритроците, определяемое визуально при микроскопии. Вместе с тем,
гипохромность - это и снижение индексов насыщения эритроцита гемоглобином:
цветового показателя (ЦП) и среднего содержания гемоглобина в эритроците (MCH).
МСН (СРЕДНЕЕ СОДЕРЖАНИЕ ГЕМОГЛОБИНА В ЭРИТРОЦИТЕ)
Нормальные значения
|
Возраст
|
Женщины
|
Мужчины
|
|
0-2
|
24,0 - 31,0пг
|
24,5 - 29,0пг
|
|
3-6
|
25,0 - 30,5пг
|
25,5 - 29,5пг
|
|
7-12
|
26,0 - 31,0пг
|
|
13-16
|
27,0 - 32,0пг
|
26,5 - 32,0пг
|
|
17-19
|
27,0 - 33,0пг
|
27,0 - 32,5пг
|
|
20-29
|
27,5 - 33,0пг
|
27,5 - 33,0пг
|
|
30-39
|
27,0 - 34,0пг
|
27,5 - 33,5пг
|
|
40-49
|
27,0 - 34,0пг
|
27,5 - 34,0пг
|
|
50-59
|
27,0 - 34,5пг
|
27,5 - 34,0пг
|
|
60-65
|
26,5 - 33,5пг
|
27,0 - 34,5пг
|
|
>65
|
26,0 - 34,0пг
|
26,0 - 35,0пг
|
Материал для исследования: венозная или капиллярная кровь.
Кровь берется с ЭДТА.
МСН (mean corpuscular hemoglobin) характеризует среднее содержание
гемоглобина в отдельном эритроците. Этот параметр можно вычислить из показателя
гемоглобина и количества эритроцитов.
МСН= (НВ9г/дл*10/RBC (10-12/л))
Расчет можно провести по номограмме (по Мазону). В
современных гематологических анализаторах этот показатель определяется
автоматически. МСН должен коррелировать со значениями МСV (средний объем
эритроцитов) и МСНС (средняя концентрация гемоглобина в эритроците). МСН
относительно редко используется для характеристики анемии.
Наиболее точным методом анализа содержания гемоглобина в
эритроцитах по-прежнему остается визуальная картина клеток крови. При ЖДА
выявляется отчетливая гипохромия, характеризующаяся наличием широкого
просветления в центре эритроцита, которое напоминает кольцо (анулоцит). В норме
соотношение диаметра центрального просветления и периферического
"затемнения" соотносится примерно, как 1: 1, при гипохромии - как
2-3:
. В мазке крови больных ЖДА преобладают микроциты -
эритроциты уменьшенного размера, отмечается неодинаковая величина (анизоцитоз)
и различные формы (пойкилоцитоз) эритроцитов. При ЖДА могут обнаруживаться и
мишеневидные эритроциты, но их число незначительно (0,1-1%). Количество
сидероцитов (эритроциты с гранулами железа, выявляемые при специальной окраске)
резко снижено в сравнении с нормой вплоть до полного отсутствия. Поскольку
важнейший тезис диагностики нарушений обмена железа состоит в том, что врач при
рассмотрении результатов анализа крови должен обратить внимание не только на ЦП
и MVH, но и на морфологическую картину эритроцитов, которая отражается в
анализе врачом-лаборантом (например, гипохромия, микроцитоз и т.д.). В
сомнительных случаях желательно обсудить результаты анализа периферической
крови с врачом-лаборантом и повторно просмотреть мазки крови пациента.
4.4.4
Доказательство дефицита железа, исключение нежелезодефицитных причин гипохромии
и микроцитоза
Наличие гипохромной анемии делает весьма вероятным
предположение о наличии ЖДА, однако, не исключает наличие анемии другого
происхождения.
Грубейшей ошибкой является назначение больным до выяснения
механизма и причины анемии "антианемической" терапии (препараты
железа, витамин В12, фолиевую кислоты, гемотрансфузии), что радикально меняет
картину крови, костного мозга и биохимических показателей. Показатели сывороточного
железа, после назначения препаратов железа, становятся нормальными уже через
несколько часов при низком уровне запасов железа в организме. Назначение В12
или фолиевой кислоты, в том числе и содержащих эти факторы поливитаминов, может
значительно повысить ретикулоцитоз, уводя врача в сторону гипердиагностики
гемолитического состояния. Поэтому после такого "комплексного"
лечения выявить патогенетические особенности анемии у больного, как правило, не
представляется возможным. Для предупреждения подобных ошибок врач должен
руководствоваться следующими положениями:
В случае нормальных значений биохимических показателей обмена
железа, следует признать, что наблюдаемая анемия не связана с дефицитом железа,
и дальнейший диагностический поиск должен быть сосредоточен на других видах
гипохромных анемий:
Для формирования новой диагностической гипотезы необходимо
использование дифференциально-диагностических признаков гипохромных анемий.
4.4.5
Определение причины дефицита железа
ЖДА является лишь синдромом, осложняющим самые разные
заболевания, большинство из которых курабельны (дисфункциональные кровотечения,
миома матки, язвенная болезнь, кровоточащий геморрой и др.). Поэтому поиск
причины ЖДА должен проводиться со всей тщательностью, базироваться на учете
наиболее вероятных причин в каждом конкретном случае. Для такого исследования
часто привлекаются все современные методы, включая эндоскопию, томографию, и
т.д. Причины дефицита железа у пациентов различаются по частоте в зависимости
от возраста. Экспертные оценки показывают, что для подростков характерны две
ведущие причины - менструальные кровопотери и алиментарная недостаточность.
Среди взрослых спортсменов доминируют различные варианты кровопотерь: у женщин
- маточные кровопотери, у мужчин - желудочно-кишечные. В то же время часто
имеет место сочетание нескольких причин. Причем, нередко выраженность каждой из
них в отдельности невысокая, может быть компенсирована увеличением усвоения
пищевого железа, и не должна приводить к дефициту железа. Хронические потери
крови, даже незначительные по объему, но продолжающиеся длительное время,
приводят к истощению запасов железа с последующим нарушением синтеза
эритроцитов и развитием ЖДА. Так, простая оценка показывает, что ежедневная
потеря 10 мл крови (2-3 чайных ложки), а с ней - 4 мг железа, существенно
превышает нормальные суточные потери железа и не может компенсироваться
поступлением из пищи. При поиске причины дефицита железа у женщин необходимо
уточнить объем менструальных кровопотерь. О повышенной кровопотере говорит
наличие большого числа крупных сгустков (более 3-4 мм), смена более 2-3
прокладок в день, выделения крови на протяжении 5 дней и более. Повышенные
маточные кровопотери наблюдаются при меноррагии различного генеза
(тромбоцитопатии и др.), дисфункциональных маточных кровотечениях, миоме матки,
эндометриозе, наличии внутриматочных контрацептивов, опухолевых процессах в
матке. Недооценивать значимость повышенных менструальных кровопотерь нельзя. В
среднем женщина во время менструаций теряет 50 мл крови (25 мг железа). В то же
время известно, что у женщин страдающих меноррагиями, количество теряемой крови
достигает 200 мл и выше (100 мг железа и более). В этом случае среднесуточная
потеря составит более 4 мг. Хронические кровопотери из ЖКТ часто связаны с
язвенной болезнью, эрозивными поражениями слизистых, полипозом, дивертикулезом.
Нужно помнить, что явный признак кровотечения из ЖКТ, - мелена, наблюдается при
обильных кровотечениях (свыше 100 мл одномоментно) только из пищевода и
желудка. В то же время, для спортсменов более характерны кишечные
микрокровопотери. Для диагностики таких потерь крови необходимо проведение
"реакций кала на скрытую кровь" - пробы Грегерсена и Вебера, или
исследование с радиоактивным хромом. Десневые и носовые хронические кровотечения
являются главным образом следствием геморрагических диатезов, требующих
различных подходов к лечению.
Нередкой причиной дефицита железа является гематурия, которая
может возникать и как следствие патологий (нефрит, мочекаменная болезнь,
поликистоз почек, цистит), и в связи с интенсивными физическими нагрузками. В
последнем случае после длительных нагрузок на выносливость могут иметь место
эпизоды клинически манифестированной макрогематурии (моча - красная, цвета
"мясных помоев", нередко - тяжесть, боль в пояснице). Микрогематурия
до 50-100 эритроцитов в поле зрения, даже перманентного характера, едва ли
может рассматриваться как причина дефицита железа.
Заключение
Железо (Fe) - компонент, необходимый для нормальной
деятельности различных геминовых и негеминовых субстратов: гемоглобина,
миоглобина, цитохромов, пероксидаз и каталаз. Указанные ферментные системы
участвуют в транспорте кислорода, тканевом дыхании, удалении перекисей
свободнорадикальных реакций. Адекватные количества Fe необходимы для
эффективного эритропоэза (образование гемоглобина в эритробластах). Передача Fe
вызревшим эритроцитам происходит в основном при высвобождении его из
трансферрина в области рецептора на мембране-предшественнице.
Лабораторные и инструментальные исследования проводятся с
целью:
выявления анемического синдрома;
выявления дефицита железа;
выявления причины ЖДА.
В клиническом анализе крови определяются:
снижение концентрации гемоглобина, более выраженное по
сравнению со снижением концентрации эритроцитов, что отражает низкий цветовой
показатель;
гипохромия (уменьшение среднего содержания гемоглобина в
эритроците и средней концентрации гемоглобина в эритроците);
микроцитоз и пойкилоцитоз эритроцитов (снижение среднего
объема эритроцитов).
При биохимическом исследовании крови выявляются:
снижение концентрации сывороточного железа (не следует
определять на фоне приема препаратов железа или в первые 6-7 дней перерыва в
приеме препарата);
снижение концентрации ферритина менее 30 мкг/л;
повышение общей и латентной железосвязывающей способности
сыворотки (общая железосвязывающая способность сыворотки более 60 мкмоль/л);
значительное снижение процента насыщения трансферрина железом
- менее 25 %.
С целью обнаружения источника кровопотери показано проведение
комплексного обследования, которое должно включать эндоскопические исследования
желудочно-кишечного тракта (ЭГДС, колоноскопия), рентгенографию желудка, при
необходимости - с пассажем бария по тонкой кишке, исследование объема
кровопотери из пищеварительного тракта с использованием радиоактивного хрома.
Список
использованной литературы
1. Воробьев
П.А. Анемический синдром в клинической практике. - М.: Ньюдиамед, 2001. - 168
с.
2. Дворецкий
Л.И. Железодефицитные анемии. - М.: Ньюдиамед, 1998. - 40 с.
. Идельсон
Л.И. Гипохромные анемии. М.: Медицина, 1981.192 с.
. Городецкий
В.В., Годулян О.В. Железодефицитные состояния и железодефицитная анемия:
лечение и диагностика. Методические рекомендации. М.: Медпрактика-М, 2005.
. Аркадьева
Г.В. Диагностика и лечение железодефицитных анемий. Учебно-методическое
пособие. М., 1999.58 с.
. Долгов
В.В., Луговская СЛ., Морозова В.Т. и др. Лабораторная диагностика анемий. М.,
2001.84 с.
. Косицкий
Т.И. / Физиология человека. - М.: Медицина, 1986.
. Покровский
В.М., Коротько Г.Ф. / Физиология человека. В 2-х тт. - М.: Медицина, 1997.
. Окороков
А.Н. Диагностика болезней внутренних органов. - Москва: Мед. Лит., 2001 - Т.4.
. Кассирский
И.А. Клиническая гематология. М. - 1970. - 800с.
. Павлов
Э.А., Еременко М.А. Значение комплексного гематологического обследования для
ранней диагностики дефицита железа и ЖДА // Гематол. и трансфуз. - 1991. - №6.
Современные методы лечения больных апластическими анемиями. (Методические
рекомендации). - Л. - 1991. - 28с.
. Сучков
А.В., Митирев Ю.Г. Анемия // Клин. мед. - 1997. - №7. - С.71-75.
. Тихомиров
А.Л. Железо для будущей мамы // Здоровье. - 2000. - №10.
. Тихомиров
А.Л., Сарсания С.И., Ночевкин Е.В. Современные принципы лечения
железодефицитных анемий в гинекологической практике // Рус. мед. жур. - 2000. -
№9.
. Ферро-Фольгамма
® Терапия железом, фолиевой кислотой и витамином В12. Научный обзор. WORWAY
PHARMA. - 39c.
. Харрисон
Г.Р. Внутренние болезни. М.: Медицина. - 1996. - т.7. - С.572-587.
. Шехтман
М.М., Бурдули Г.М. Болезни органов пищеварения и крови у беременных М.:
"Триада-х". - 1997. - С.183-302.