Кумарини. Лікарська рослинна сировина, що містить прості кумарини, гідрокси – та метокси – похідні кумаринів
КУРСОВА РОБОТА
Кумарини.
Лікарська рослинна сировина, що містить прості кумарини, гідрокси - та метокси
- похідні кумаринів
Вступ
Рослинний світ подарував людству величезне
багатство - лікарські рослини, які завжди були джерелами життя, їжі та
здоров'я. Багато хто з них пройшли багатовікову перевірку і складають безцінний
фонд сучасної фітотерапії. Безсумнівно, що її становлення носило емпіричний
характер. Право на життя завойовували ті лікувальні ефекти рослин, які були
очевидні. [2]
Незважаючи на досягнуті успіхи в галузі хімічного
синтезу лікарських речовин, природні біологічно активні сполуки в даний час не
тільки не втратили свого значення, але, навпаки, з кожним роком розширюються
перспективи їх використання. Актуальність фітотерапії зросла ще й тому, що
почастішали випадки терапевтичних невдач, поява алергічних реакцій на
синтетичні медикаменти.
Кожному класу хімічних речовин притаманні певні
лікувальні ефекти, вони можуть підсумовуватися і забезпечувати появу нових
видів активності. Вміст у лікарських травах комплексу цінних речовин сприяє
вирівнюванню і нормалізації життєво важливих процесів, забезпечує організм
мінеральними солями і вітамінами, підтримує на певному рівні обмін речовин.
Одним з переваг лікування лікарськими травами є їх мала токсичність та
можливість тривалого застосування без істотних побічних явищ. [9]
Окрім поодиноких рослин для досягнення більш
вираженого терапевтичного ефекту в практичній медицині застосовують збори з
кількох, іноді більше 10 видів лікарських рослин.
Фітотерапія - прадавня галузь медицини, що
вимагає спеціальних знань. Самостійно або в комплексі з іншими видами лікування
вона обов'язково повинна проводиться за призначенням і під контролем лікаря з
урахуванням особливостей течії патологічного процесу і фармакологічної
активності терапевтично активних сполук рослини. [7]
Останніми роками спостерігається розширення
діапазону наукових пошуків щодо вивчення властивостей лікарських засобів
рослинного походження та наукового обґрунтування доцільності широкого
впровадження фітотерапії в клінічну медицину. Наукові розробки виконують у
закладах освіти на рівні пошукової та ініціативної тематики кафедр та
факультетів фармацевтичного профілю. Водночас ці роботи є фрагментами наукового
супроводу ряду національних та державних програм у сфері охорони здоров’я, які
нині реалізуються. Розширюється діапазон експериментальних досліджень та
наукових клінічних розробок також у науково-дослідних установах МОЗ та АМН
України.
За експертною оцінкою спеціалістів, що була опублікована
у бюлетні ВООЗ за 1987 рік, 75% усіх хворих повинні лікуватися тільки засобами
рослинного походження, які мають меншу побічну дію. [2]
Фітопрепарати можна комбінувати із синтетичними
медикаментами для посилення терапевтичної дії і зменшення побічних ефектів
синтетичних засобів. Наприклад, широко відомий препарат барбовал застосовують у
медичній практиці понад 30 років. До його складу входить валідол, етиловий
спирт альфа-бромізовалеріанової кислоти, фенобарбітал. Барбовал вживають при
неврозах, істерії, тахікардії, стенокардичних болях, вегето-судинній дистонії,
на ранніх стадіях гіпертонічної хвороби, а також спазмах травного тракту, які
характеризуються болями в животі. Барбовал посилює дію препаратів, що
пригнічують функцію ЦНС (снодійні, седативні, анальгетики, нейролептики,
транквілізатори). Інший препарат - кратал, що містить амінокислоту таурін,
екстракт плодів глоду колючого і екстракт трави собачої крапиви, широко
застосовують для лікування вегето-судинної та нейроциркуляторної дистонії, хронічної
ішемічної хвороби серця, кардіоміопатії. [7]
Отже, докладне вивчення рослин і впровадження в
медичну практику нових фітопрепаратів дозволить не лише ефективніше лікувати
різні недуги, але й застосовувати ці медикаменти для реабілітації хворих.
. Кумарини як клас природніх сполук
Кумарини - класс природніх сполук, який міститься
у рослинах, основою хімічної будови яких є кумарин або ізокумарин. Скелет
кумарина являє собою циклізовану ортооксикоричну кислоту (9,10 - бензо-α-пірон). [12]
Кумарин - родоначальник цієї групи сполук -
вперше був виділений Фогелєм у 1820 р. із плодів південноамериканського дерева
тонко (Dipterix odorata, род. Fabaceae). Свою назву кумарин отримав від
місцівої назви цього дерева - «coumarouna».
.1 Класифікація кумаринів
Структура кумарину як лактону о-кумарової кислоти
булла визнана не одразу, але проведений синтез кумарину із саліцилового
альдегіду з малоновою кислотою вказав на його зв’язок з о-гідрокикоричною
кислотою. [24]
Природні кумарини в залежності від їх хімічної
будови поділяють на такі групи: [5]
. Власне кумарини: кумарин, ізокумарин,
дигідрокумарин, глікозиди кумарину. Ці сполуки знайдені у траві буркуну
лікарського (Melilotus officinalis, Fabaceae).
|
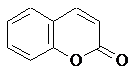 
|
|
|
Кумарин
|
Ізокумарин
|
. Окси-, метокси(алкокси) - и
метилендіоксикумарини. Замісники можуть бути у бензеновому, піроновому і
одночасно в обох кільцях. Найбільше поширені ці сполуки в рослинах родин
Apiaceae та Rutaceae.
. Фурокумарини, або кумарон-α-пірони. Сполуки утворені в результаті конденсації фуранового
кільця з кумариновим 6,7 - положенні (похідні псоралену) або в 7,8 - положенні
(похідні ангеліцину). Замісники можуть бути в усіх трьох кільцях.
. Піранокумарини або хроменопірони. Сполуки
утворені в результаті конденсації кумарину з 2,2 - диметилпіраном в положеннях
5,6; 6,7 або 7,8 та мають замісники у всіх кільцях.
|
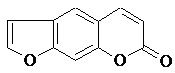  
|
|
|
|
Псорален
|
Ангеліцин (ізопсорален)
|
Піранокумарин
|
. Бензокумарини. Сполуки утворені в результаті
конденсації кумарина з бензеновим кільцем в положенні 3, 4. Зустрічаються в
рослинах родин Anacardiaceae, Rosaceae.
. Куместани (куместроли). Кумаринові сполуки, що
містять систему бензофурану, конденсовану з в 3,4 - положенні (куместрол та
інші). Виділені з різних видів конюшини Trifolium spp., Fabaceae.
|

|
|
Пеуцеданін
|
. Інші, ще більш складні конденсовані похідні
(афлатоксин та інші).
1.2 Фізико-хімічні властивості кумаринів
кумарин
хімічний біологічний каштан
Кумарини й фурокумарини - кристалічні, безбарвні
запашні речовини. При нагріванні до 1000 С сублімуються. Кумарини
добре розчиняються в органічних рочинниках: етиловому і метиловому спиртах,
петролейному й диетиловому ефірах, хлороформі, жирах та жирних оліях. У
водно-спиртових сумішах розчиняються в основному глікозиди. Розчиняються
кумарини також у водних лужних розчинах (особливо при нагріванні) за рахунок
утворення солей гідроксикоричних кислот (властивість лактонів). Більшість
кумаринів виявляють характерну флюоресценцію в УФ-світлі в нейтральних
спиртових, лужних розчинах і концетрованій сірчаній кислоті у видимій частині
спектру. Цим особливо відрізняються похідні умбеліферону, які мають інтенсивну
яскраво-блакитну флуоресценцію в УФ-світлі. [12], [25]
.3 Виявлення, виділення та кількісне визначення
кумаринів
Для виявлення кумаринів в рослинах та сировині
використовуються лактонні властивості кумаринів, їх здатність до флуоресценції
при ультрафіолетовому опроміненні та давати забарвлені розчини зі специфічними
реактивами.
Найбільш характерною є реакція з діазосполуками
(діазотований n-нітроанілін, діазотована сульфаниіловая кислота, біс -
діазотований бензидин). [6]
Цю реакцію проводять наступним чином: невелику
кількість подрібненої свіжої або висушеної сировини заливають 5-10 мл етанолу,
залишають на 4 години та нигрівають впродовж 2-3 хвилин при температурі не вище
500 С, потім розчин фільтрують та додають декілька крапель 5%
розчину лугу і нагрівають впродовж декількох хвилин на водяній бані. У випадку
присутності кумаринів розчин жовтіє. До частини лужного розчину додають
декілька крапель свіжеприготованого діазореактиву. За наявності кумаринів
розчин набуває кольору від коричнево-червоного до вишневого.
Здатність до флуоресценції мають не тільки
кумарини, а й інші природні сполуки. Сааме через це визначення кумаринів із
застосуванням флуоресценції може розглядатися як додатковий метод.
Широкі можливості для визначення у рослинах та
сировині кумаринів, при чому не тільки їх суми, а і окремих сполук, відкрилися
післявпровадження у фармакогностичну практику хроматографічного аналізу.
Застосовують в основному паперову хроматографію та хроматографію у тонкому шарі
сорбенту.
Похідні кумарину краще за все розділяються за
допомогою розподільної хроматографії не папері, просоченому етиленгліколем,
пропіленгліколем, формальдегідом або 0,1 М розчином натрію гідрофосфату.
Рухомою фазою є петролейний ефір або бутанол, насичений водою. Виявлення
проводять безпосереднім спостереженням в УФ-світлі, а також післе оприскування
хроматограм розчинами лугу, діазореактивами, рідше реактивом Драгендорфа. Різна
рухомість, а також колір флуоресценції дозволяють ідентифікувати кумарини,
фурокумарини, дигідрокумарини. Оксикумарини, як правило, залишаються на старті
у більшості систем, і тільки обробка паперу формамідом в метиловому спирті або
ацетоні дозволяє збільшити рухомість та отримати задовільні результати. [11]
Звичайно, що паперова хроматографія має свої
недоліки, котрі можна легко усунути при застосуванні методу ТШХ. Перевагою цьго
методу є не тільки швидкість, а й більша чіткість розділення (меншому
розповсюдженню плям), можливість визначення плям шляхом обробки хроматограм
агресивними проявниками при підвищених температурах.
Хроматографічні методи дуже зручні і для
препаративних цілей, тобто виділення кумаринів. З цією метою із сировини
спочатку отримують витяг. Найбільш вичерпна екстракція кумаринів, як вільних,
так і глікозидів, досягається за допомогою етанолу, хоча можливе використання
бензену, хлороформу, діетилового та петролейного ефірів. Зазвичай останні
розчинники використовують для очистки спитових екстрактів після відгонки
етанолу. [14]
Методом попередньої ідентифікації кумаринів у
рослинній сировині були відкриті гідроксилвмісні кумарини (скополетин и
умбеліферон), ацетильовані дигідропохідні 7,8 - фурано - та 7,8 -
піранокумарину (пеуценідин, атамантин, віснадин) у смовді гірській,
дніпровській та амі зубній.
Для кількісного визначення кумаринів широко
застосовують колориметричні методи. В їх основу покладено здатніть кумаринів
утворювати стійкі червоно-пурпурні розчини з діазотованими n-нітроаніліном або
сульфаніловою кислотою в лужному середовищі.калібрувальний графік будують за
однією з відомих сполук. Значно ширше використовуєються спектрофотометричні
методи кількісного визначення кумаринів. В основу цих методів покладено зміну
оптичної щільності розчинів кумаринів при довжині хвилі максимуму поглинання в
УФ області того чи іншого кумарину в залежності від концентрації. [11]
Велику специфічність мають методики визначення
оксикумаринів за забарвленими комплексними сполуками, що вони утворюють з
хлоридом алюмінію, хлорокисом цирконію (хлористим цирконілом), азотнокислим
галієм.
Кількісне визначення оксикумаринів в середовищі
неводних розчинників (ацетону, диметилформаміду, диметилсульфоксиду)
потенціометричним методом можливе з використанням у якості титрантів гідроокису
тетраетиламонію або натрію. Метод має перевагу перед оптичними в точності
визначення і не потребує наявності стандартних речовин для проведення
кількісного визначення. [6]
У наш час широке розповсюдження отримали
комбіновані методи, що включають в себе попереднє роздулення на папері, в
тонкому шарі сорбенту з подальшим визначенням речовин в елюатах з плям
хроматограм, а також безпосереднім скануванням оптичної густини або визначенням
площі плями на хроматограмі.
.4 Розповсюдженість кумаринів
Вивчаючи кумарини рослин, Г.К. Ніконов зауважив,
що у видах рослин південних широт найбільш часто зустрічаються похідні
кумарину, що містять в якості замісника ізопренові ланцюги та їх похідні. В
рослинах країн помірного клімату та північних широт спостерігається накопичення
кумаринів збагачених киснем, що містять у своїй молекулі цукрові залишки,
складноефірні, метокси-, окси - угрупування. [8]
Кумарини знайдені у рослинах різних родин.
Найбільш типові вони для рослин Apiaceae, Rutaceae, Fabaceae. У рослинах інших
родин (Asteraceae, Hippocastanaceae, Solanaceae) зустрічаються відносно рідко.
Найпоширеніші прості похідні кумарину і фуро кумарину. Основна кількість сполук
цього класу знаходиться у вільному стані, рідше - у формі глікозидів. [4]
Кумарини розподіляються в рослинах нерівномірно.
Кількість їх коливається від 0,2 до 10%. Вони накопичуються переважно в плодах,
насінні, коренях, корі, квітках і менше - в траві та листках. В родині
селерових кумаринові сполуки локалізуються в ефіроолійних канальцях. Часто
можна зустріти і 5-10 кумаринів різної хімічної структури в одній рослині.
Якісний і кількісний склад їх відмінний у різних видів навіть всередині одного
роду. Можливі ці відмінності і всередині одного виду (підвиду, хемотипу). Склад
кумаринів змінюється й в онтогенезі рослин. [3]
У винах деяких західноєвропейських країн знайдені
ескулетин і умбеліферон, в коньяках - кумарин, скополетин, ескулетин, а також
6-окси-7-метоксикумарин. [1]
1.5 Біологічна дія кумаринів
Роль кумаринів в рослинному світі ще недостатньо
вивчена. Відомо, що деякі з них є інгібіторами росту, іеші стимулюють
проростання насіння, треті виступають в якості захисних засобів при деяких
захворюваннях рослин, а також УФ-опроміненнях. [24]
Фотосенсибілізуючий ефект виявляють фурокумарини.
Його інтенсивність визначається місцем приєднання фуранового кільця до
кумаринового (6,7 - фурокумарини активніші за 7,8 - фурокумарини) метоксильними
угрупуваннями та їх положенням. Механізм фотосенсибілізуючої дії ще не
встановлено. Є припущення, що фурокумарини безпосередньо включаються у
біохімічний механізм утворення пігменту меланіну.
Деякі кумарини, наприклад ескулін, мають
Р-вітамінну активність. Кумарини з аміноалкільными замісниками стимулюють ЦНС.
Ряд кумаринів і фурокумаринів мають бактеріостатичну та антигрибковудію.
Виявлена деяка протипухлинна активність в ряду фурокуманинів. [16]
За даними літературних джерел кумарини та
фурокумарини розслаблюють непосмуговані м’язи кішківника, а також матки та
бронхів. Тривалість спазмолітичного ефекту кумаринів становить приблизно 20
хвилин. Сила спазмолітичного ефекту наближається до ефекту папаверину.
Виключно похідним оксикумарину властива
антикоагулянтна дія, що заснована на руйнуванні біосинтезу протромбіну, про
конвертину та інших факторів, котрі визначають зсідання крові. Дія непрямих
антикоагулянтів, з котрих дику марин є найбільш сильним, розвиваєть повільно
(через 12-72 години після прийому). При цьому протромбін, що міститься у крові,
поступово руйнується, а утворенню нового заважає пригнічення відповідних
біохімічних систем печінки. Разом зі зниженням протромбіну знижується кількість
про конвертину, уповільнюється рекальцифікація плазми та слабшає толерантність
до гепарину. [10]
. Характеристика ЛРС, що містить прості кумарини
та оксикумарини
.1 Трава буркуну лікарського - Herba Melliloti
Буркун лікарський або буркун жовтий (Melilotus
officinalis (L.) Pall.) - рослина роду буркунів (Melilotus), родини бобових
(Fabaceae). Дворічна трав'яниста рослина 40-130 см заввишки.
Походження назви. Назва роду утворена від
двох латинських слів, одне з яких означає «мед», а друге є римською назвою
конюшини. Видова назва у перекладі з латинської - «аптечна», «лікарська» (дана
рослині за цілющі властивості). [5]
Можливі домішки. Основними домішками до
буркуну лікарського є:
. Буркун високий - Mellilotus altissimus
. Буркун зубчастий - Mellilotus dentatus
. Буркун білий - Mellilotus albus
Морфологічна характеристика. Цілі верхівки з
листям та бокові гілочки зі стеблом двжиною до 30 см та діаметром до 3 мм.
Прилистки ланцетні або шиловидні, цільнокраї, рідше у найнижчих листочків - з
1-2 зубчиками. Нижні листки оберненояйцевидні, верхні - продовгуваті або
ланцетні, по краю з обох сторін з 10 - 13 нерівними зубчиками у буркуну
лікарського та з 8 - 20 зубчиками у буркуну високого. Квітки метеликові,
дрібні, довжиною від 5 до 7 мм. Чашечка колокольчаста, 5-зубчаста, залишається
при плоді, гола в буркуну лікарського і опушена в буркуну високого. Іноді зустрічаються
в незначній кількості дрібні недостиглі плоди-боби - від 3 до 5 мм,
неясносітчасті або поперечно-зморшкуваті, голі чи вкриті рідкими волосками.
Сім’я одне, рідше два. Колір стебла, чашечки та плодів - зелений, віночка -
жовтий. Запах ароматний, свіжого сіно (кумарин). Смак гіркуватий. Цвіте з
червня до вересня. Плід - одно, двонасінний біб, який достигає у серпні -
вересні.
Листки буркуну присмерком або перед дощем
піднімаються догори і складаються. Це сприяє зменшенню випромінювання
внутрішнього тепла рослини і, очевидно, є захистом від небажаного підвищення
вологості повітря біля продихів. [22]
Числові показники. Вологість - не більше
14%; золи загальної - не більше 10%; стебел діаметром більше 3 мм - не більше
2%; часток, що проходять крізь сито з отворами діаметром 0,5 мм - не більше 5%;
пожовклих, побурівши та почорнілих частин рослини - не більше 2%; органічних
домішок - не більше 1%; мінеральних домішок - не більше 0,5%. [6]
Поширення. По всій Україні, де місцями утворює зарості, на
Північному Кавказі і в Поволжі. Росте на перелогах, схилах, уздовж доріг, на
пустищах, засмічене місцях, толоках, у ярах, на межах, у канавах, на парових
полях. []
Заготівля. Траву збирають під час цвітіння рослини.
Зрізають верхівку і бокові пагони. Сушать під наметом. Суху траву обмолочують і
просівають крізь дротяне сито, щоб відділити товсті стебла. [12]
Хімічний склад рослини. Трава містить кумарини
(0,4 - 0,9%): дикумарол, мелілотин, мелілотозид, а також кумарову та мелілотову
кислоти; ефірну олію, похідні пурину, ліпоїди, білок, слиз, флавоноїди, сахара,
аскорбінову кислоту, азотисті сполуки.
|

|
|
|
Дикумарол
|
Мелілотова кислота
|
Господарське значення. Буркун - медоносна, ефіроолійна і
лікарська рослина. Чай з напару квіток буркуна п'ють при грудних хворобах.
Квітки буркуна в невеликих дозах входять у різні грудні суміші лікарських
рослин. На селах сухі розтерті квітки буркуна додавалися для аромату до тютюну.
На Кавказі їдять сирі варені молоді корені буркуну. Також можливе його використання
у парфумерній промисловості в якості фіксатору запаху.
Використовують траву, квітки. [8]
Застосування. Настій трави - при
стенокардії й тромбозі коронарних судин. Трава входить до складу лікувальних
сумішей при бронхіті, туберкульозі легень, болях у шлунку, набряках,
ревматизмі, наривах, пухлинах суглобів тощо. Сировина йде на виготовлення
зеленого витяжного пластиря, входить до складу кардіопротекторного засобу
«Кардіофіт»
У народній медицині використовують при кашлі,
мігрені, безсонні, гіпертонії, клімактеричних розладах, хворобах яєчників.
Зовнішньо - для компресів, примочок при фурункулах, герпесі, тріщинах заднього
проходу, для пом'якшення та розсмоктування затвердінь, абсцесів; мазь - при
простуді і порізах. Молоде листя та суміш сухого листя й суцвіття рекомендовані
для вітамінних салатів, супів, окрошок, приправ, компотів. Настій квіток на
олії прискорює, дозрівання фурункулів.
У гомеопатії використовуються свіжі верхівки
трави при тромбофлебітах, застійних явищах в легенях, яєчниках, при головному
болі, який супроводжується почервонінням обличчя та сильним нервовим
збудженням. [9]
Дія: відхаркувальна, пом'якшувальна,
седативна, знеболююча, протизапальна, вітрогінна, антикоагулянтна[21],
протисудомна, кардіотонічна, діуретична. [15]
КАРДІОФІТ (Cardiophyt) [13]
Загальна характеристика:
основні фізико-хімічні властивості: прозора
рідина темно-коричневого кольору, з ароматним запахом. Допускається наявність
осаду;
склад: 1 мл настойки складної містить біологічно
активні речовини з трави горицвіту весняного 0,0070 г.; плодів аморфи кущової
0,0070 г.; квіток глоду 0,0070 г.; квіток бузини чорної 0,0070 г.; кореневищ з
коренями валеріани 0,0105 г.; трави буркуну 0,0070 г.; насіння каштану
кінського 0,0105 г.; листя кропиви 0,0035 г.; листя та квіток конвалії 0,0070
г.; листя м’яти перцевої 0,0070 г.; коренів солодки 0,0070 г.; трави кропиви
собачої 0,0070 г.; листя омели білої свіжих 0,0055 г.; трави чебрецю 0,0070 г.;
допоміжні речовини: спирт етиловий 40%.
Форма випуску. Настойка складна.
Фармакологічні властивості. Фармакодинаміка.
При функціональних серцево-судинних розладах Кардіофіт справляє
кардіотонічну, антиаритмічну та м’яку гіпотензивну дію. При органічних
захворюваннях серцево-судинної системи в складі комбінованої терапії Кардіофіт
оптимізує дію антиангінальних, антигіпертензивних та антиаритмічних
препаратів. Препарат має м’яку седативну дію, покращує загальний стан хворих,
переносимість фізичних навантажень, сприяючи оптимальній працездатності.
Кардіофіт при застосуванні вдень не спричинює сонливості та
загальної в’ялості.
Показання до застосування. Кардіофіт застосовується
при лікуванні нейроциркулярної дистонії, неврозів серця, пароксизмальної
суправентрикулярної тахікардії, ішемічної хвороби серця (стенокардія напруження
І-ІІ клас), гіпертонічної хвороби (І-ІІ стадія).
ВАРФАРІН
Перший лікарський засіб класу антикоагулянтів був
власне дикумарол, запатентований в 1941 році і потім застосовувався як
фармакологічний засіб. Карл Лінк продовжив роботу зі створення більш сильних
кумарино-подібних антикоагулянтів для використання в якості отрути для
гризунів, в результаті чого у 1948 році був синтезований варфарін. Назва
«варфарін» (англ. warfarin) походить від абревіатури WARF (англ. Wisconsin
Alumni Research Foundation) + закінчення - arin, вказує на
зв’язок з кумарином. Варфарін спочатку був зареєстрований як отрута для
гризунів у США у 1948 році і одразу ж став популярним. [18]
Після випадку у 1951 році, коли призовник армії
США безуспішно намагався закінчити життя самогубством, прийнявши декілька доз
варфаріну у складі отрути для гризунів та повністю видужав у госпіталі, де йому
вводили вітамін К (вже тоді відомий як специфічний антидот), були розпочаті
дослідження з застосування варфаріну в якості терапевтичного антикоагулянту.
Було виявлено, що він перевершує за ефективністю дикумарол, а у 1954 році був
схвалений для медичного застосування у людей. [20]
Точний механізм дії залишався невідомим доки у
1978 році не було продемонстровано, що варфарін інгібує фермент
епоксидредуктазу, у наслідок чого порушує метаболізм вітаміну К.
Варфарін є антикоагулянтом непрямої дії. [15]
Оптимальна антикоагулянтна дія спостерігається на 3-5 день після прийому
останньої дози. Варфарін пригнічує синтез вітамін К-залежний синтез біологічно
активних форм кальцій-залежних факторов згортання крові ІІ, VII, IX та X, а
також білки С, S і Zв печінці. Також варфарін може діяти на інші білки, що не
беруть участь у згортанні крові. [17]
2.2 Насіння каштану кінського - (Semina
Hippocastani)
Листя каштану - (Folia Hippocastani)
Гіркокаштан звичайний (Кінський каштан звичайний
Aesculus hippocastanum L.) - рослина родини кінськокаштанових
(Hippocastanaceae). Дерево з гарною
густою кроною до 30 м заввишки.
Походження назви. Від aesculus -
латинської назви дерев’янистої рослини; грецьке hippos - кінь; castanum - від
латинського castanea - назва справжнього каштану. [5]
Морфологічна характеристика. Лстки
супротивні, п’яти-семипальчастоскладні, з довгими жолобовидними черешками,
близько 25 см у поперечнику, сидячі, обернено яйцевидні, коротко загострені,
злегка зубчасті, клиноподібно звужені; молоді листки в основі жилок рудо
волосяні. Старе гілля брунатно-сіре, молоді товсті пагони - світло-бурі, голі.
Бруньки до 2,5 см завдовжки, яйцевидні, темно-бурі, клейкі, покриті шкірястою
лускою. Квітки зібрані в гроно 20-30 см заввишки, чашечки квіток дзвоникуваті,
пухнасті з 5 нерівними лопатями. Віночок п'ятипелюстковий, білий з жовтуватою,
далі червонястою плямою в зіві. Плід - велика яйцевидно-овальна коробочка з гострими
колючками, що містить 1-3 насінини. Зріле насіння овальної форми, в діаметрі
3-5 см, вкрите блискучою, брунатною шкіркою з великою сіруватою плямою біля
основи. Без запаху. Гірко-в’яжучого, трохи маслянистого смаку. Цвіте в травні,
плоди дозрівають у вересні - жовтні. [6]
Числові показники. Вміст есцину,
визначеного спектрофотометричним методом, має бути не менше 7%; вологість не
більше 12%; загальної золи не більше 2,5%; інших частин рослини (плодоніжки,
стулки коробочок) не більше 1%; органічних домішок не більше 0,5%; мінеральних
домішок не більше 0,5%.
Поширення. Росте по всій території
України (походить з південно-східної Європи, Балкани). У ряді країн СНД широко
розповсюджене як декоративне дерево. [22]
Заготівля. Збирають кору молодих
гілок - навесні, квіти - в травні, шкірку насіння - восени. Насіння сушать на
відкритому повітрі або в сушарках при температурі 40-500С.
зберігають сировину в сухому місці до п’яти років в добре провітрюваному
приміщенні. Листки можна заготовляти протягом літа; сушать їх на повітрі у
затінку. [23]
Хімічний склад сировини. Насіння містить глюкозид
ескулін, що розщеплюється на ескулетин та глюкозу. Ескулетин являє собою 6,7 -
диоксикумарин. Поряд з ескулетином у насінні виявлений інший кумаринів глюкозид
- фраксин (білш типовий для видів Fraxinus), що відщеплює глюкозу та фраксетин
і явл
яє собою 6-метокси - 7,8 - диоксикумарин.
Окрім окси- і метоксикумаринів в насінні
кінського каштану містяться флавоноїди, що представленібі - та триозидами
кверцетину і кемпферолу. Також містить три терпеновий сапонін есцин, агліконом
якого є есцигенін (група β-амірину), а
сахарами - ксилоза, глюкоза і глюкуронова кислота. У насінні багато крохмалю
(до 50%), містить жирну олію (6-8%), білкові (8-10%), дубильні (приблизно 1%)
речовини. [16]
|
 
|
|
|
Ескулін
|
Фраксин
|
Використання. З насіння виробляють
водно-спиртовий екстракт ескузан (Aescusanum), що застосовується для
профілактики тромбозів, при венозному застої та розширенні вен нижніх кінцівок,
а також при геморої. Дія розрахована на ескулін та фраксин, що мають
антикоагулюючі властивості (слабші за дикумарол). З тією ж метою у гомеопатії
застосовують настоянку та мазь, що містить 10% настоянки.
За кордоном випускають багато патентованих
препаратів, до складу яких входять речовини кінського каштану. 10% настоянка з
листя каштану завдяки наявності каротиноїдів застосовується в терапії маткових
та гемороїдальних кровотеч. [2]
Фармакологічні властивості. Застосовують при
маткових і гемороїдальних кровотечах, геморагічних діатезах, при варикозному
розширенні вен, тромбофлебітах (стимулює антитромбічну активність сироватки
крові й посилює наповнення кров'ю жильної системи), при атеросклерозі (змінює
хімізм крові і особливо обмін холестерину), для профілактики апоплексії (в корі
містяться глікозиди ескулетин і фраксин, які, уповільнюють зсідання крові, і
речовини, рівноцінні хініну), при захворюваннях жовчного міхура, хронічних
захворюваннях кишок, при суглобному ревматизмі, артритах різної етіології,
малярії, нічному занімінні рук та ніг. [10]
Препарати. [13]Номенклатура
лікарських засобів кінського каштану налічує багато препаратів: Аесцин;
Венастат; Венен (Венен гель Доктора Тайсса); Венітан; Веноплант; Кінский
каштан; Концентрин; Репарил (Репарил-гель); Цикловен (Цикловен-форте); Екстракт
насіння кінського каштану (сухий, густий, рудкий); Ескузан (Ескузан 20); Есцин
та інші.
Настій кори. 1 чайна ложка подрібненої кори на 2
стакани (400 мл) охолодженної кип’яченої води, настоювати 8 годин, процідити,
приймати по 2 столові ложки 4 рази на день.
Настій кори для зовнішнього застосування. 50 г.
кори на 1 л окропу, кип’ятити 15 хвилин та настояти 8 годин, процідити. Роблять
сидячі прохолодні вани при гемороїдальних кровотечах впродовж 15 хвилин після
спорожненя кішківника.
Ескузан (Aescusanum) є водно-спиртовим екстрактом
з плодів кінського каштану. Містить сапонін - есцин і флавоноїди з додаванням
вітаміну В1. Приймають при застої та розширенні вен нижніх кінцівок,
при виразках гомілки та геморої 3 рази на день по 10-15 крапель у якості вено
тонізуючого ті антитромбічного засобу.
Анавенол (Anavenol) - комбінований препарат у
формі драже. Містить ескуліну 1,5 мг, 0,5 мг дигідроергокристину та 30 мг
рутину. Приймають по 2 драже 3 рази на день після їжі. Також випускається у
формі крапель, що містять в 1 мл ескуліну 1,5 мг, 0,5 мг дигідроергокристину та
рутину натрію сульфоналу 40 мг.
Есфлазид (Aesflazidum) - містить есцин з плодів
каштану та суму флавоноїдів з листя. Форма випуску - таблетки, що містять 0,005
г. есцину і 0,025 г. флавазиду. В перші два дні лікування всередину по 1
таблетці 1-2 рази на день, потім по 3-4 таблетки на день. Курс лікування при
тромбофлебітах, флебітах - від 2 тижнів до 2-3 місяців, а при геморої - від 1
до 4 тижнів. При рецидивах курс лікування повторюють.
Можливі побічні ефекти у вигляді нудоти, печії,
болю в області серця зникають зі зниженням дози. Препарати кінського каштану
застосовують під наглядом лікаря з контролем протромбіну крові.
Загальні висновки
Кумарини - класс природніх сполук, який міститься
у рослинах, основою хімічної будови яких є кумарин або ізокумарин. Скелет
кумарина являє собою циклізовану ортооксикоричну кислоту (9,10 - бензо-α-пірон).
Природні кумарини в залежності від їх хімічної
будови поділяють на сім груп, кожна з яких має свої особливості хімічної будови
та біологічної активності, що виявляють сполуки цієї групи.
Кумарини знайдені у рослинах різних родин.
Найбільш типові вони для рослин Apiaceae, Rutaceae, Fabaceae. У рослинах інших
родин (Asteraceae, Hippocastanaceae, Solanaceae) зустрічаються відносно рідко.
Найпоширеніші прості похідні кумарину і фуро кумарину. Основна кількість сполук
цього класу знаходиться у вільному стані, рідше - у формі глікозидів.
Клас кумаринів виявляє досить широкий спектр
різноманітної біологічної активності. Але виключно похідним оксикумарину
властива антикоагулянтна дія, що заснована на руйнуванні біосинтезу
протромбіну, про конвертину та інших факторів, котрі визначають зсідання крові.
Дія непрямих антикоагулянтів, з котрих дику марин є найбільш сильним,
розвиваєть повільно (через 12-72 години після прийому). При цьому протромбін,
що міститься у крові, поступово руйнується, а утворенню нового заважає
пригнічення відповідних біохімічних систем печінки. Разом зі зниженням
протромбіну знижується кількість про конвертину, уповільнюється рекальцифікація
плазми та слабшає толерантність до гепарину.
Основним препаратом з трави Буркуну лікарського є
кардіофіт, що виявляє кардіотонічну, антиаритмічну та м’яку гіпотензивну дію; у
складі комплексної терапії оптимізує дію антиангінальних, антигіпертензивних та
антиаритмічних препаратів. Препарат має м’яку седативну дію, покращує загальний
стан хворих, переносимість фізичних навантажень, сприяючи оптимальній працездатності.
Перший лікарський засіб класу антикоагулянтів був
власне дикумарол, запатентований в 1941 році і потім застосовувався як
фармакологічний засіб. Карл Лінк продовжив роботу зі створення більш сильних
кумарино-подібних антикоагулянтів для використання в якості отрути для
гризунів, в результаті чого у 1948 році був синтезований варфарін.
Варфарін є антикоагулянтом непрямої дії,
синтетичного походження. Оптимальна антикоагулянтна дія спостерігається на 3-5
день після прийому останньої дози. Варфарін пригнічує синтез вітамін К-залежний
синтез біологічно активних форм кальцій-залежних факторов згортання крові ІІ,
VII, IX та X, а також білки С, S і Zв печінці. Також варфарін може діяти на
інші білки, що не беруть участь у згортанні крові.
З ЛРС Гіркокаштану звичайного виготовлють більше
десяти різноманітних препаратів та лікарських форм. Але для всіх цих препаратів
притаманна спільна біологічна активність: стимуляція антитромбічної активність
сироватки крові й посилення наповнення кров'ю жильної системи, зміна хімізму
крові і особливо обміну холестерину, уповільнення зсідання крові. Саме ці
напрямки дії активних речовин і обумовлюють застосування препаратів каштану при
маткових та гемороїдальних кровотечах, геморагічних діатезах, при варикозному
розширенні вен, тромбофлебітах, атеросклерозі, для профілактики апоплексії; при
захворюваннях жовчного міхура, хронічних захворюваннях кишок, при суглобному
ревматизмі, артритах різної етіології, малярії, нічному занімінні рук та ніг.
Література
1. Валуйко Г.Г. Биохимия и технология красных вин. - Москва, 1993
. Гамерман А.Ф. Лікарські рослини: (Рослини - цілителі)./ А.Ф.
Гамерман, Г.Н. Кадаєв, А.А. Яценко-Хмелевський. - М.: Вища школа, 1990. - 544
с.
. Георгієвський В.П., Комісаренко Н.Ф., Дмитрук С.Е. Біологічно активні
речовини лікарських рослин - Новосибирськ «Наука», 1990 - с. 473.
. Лавренов В.К., Лавренова Г.В. Сучасна енциклопедія лікарських
рослин - СПб.: Видавничий Дім «Нева», 2006 - с. 587.
. Ковальов В.М., Павлій О.І., Ісакова Т.І. Фармакогнозія з основами
біохімії рослин - Х.: «Прапор», 2000 - 703 с.
. Ковальов В.М., Попова Н.В., Кисличенко В.С. та ін. Практикум з
фармакогнозії - Х: «Золоті сторінки», 2003 - 512 с.
. Ковалева Н.Г. Лікування рослинами. - М.: Медицина, 1971 - с.
246.
. Коренская И.М. Лекарственные растения и лекарственное
растительное сырье содержащие флавоноиды, кумарины, хромоны - Воронеж, 2007 -
81 с.
. Куркин В.А. Основы фитотерапии: учеб. пособие для студентов,
обучающихся по специальности Фармация/В.А. Куркин. - Самара: Офорт, 2009. - 963
с.
. Корсун В.Ф., Ситкевич А.Е., Єфімов В.В. Лікування препаратами
рослинного походження. - Мінськ, 1995. - 383 с.
. Ложкин, А.В. Природные кумарины: методы выделения и анализа /
А.В. Ложкин, Е.И. Саканян // Хим.-фармац. журн. - 2006. - Т. 40, №6. - С.
47-55.
. Муравйова Д.А. Фармакогнозія: підр. для студ. фармац. вузів/
Д.А. Муравйова, И.А. Самиліна, Г.П. Яковлев. - 4-е вид., перер. і доп. - М.:
Медицина, 2002 - 656 с.
. Машковський М.Д. Лікарські засоби, т. 1 - Москва: «Новая волна»,
2002 - с. 541.
. Семенистая Е.Н. Высокоэффективная жидкостная хроматография в
исследовании физико-химических свойств кумаринов, фурокумаринов и их комплексов
с переходными металлами, - Автореферат - 2007 - с. 47.
. Харкевич Д.А. Фармакологія./ Д.А. Харкевич - 6-е вид., перер. і
доп. - М.: ГЕОТАР МЕДИЦИНА, 1999. - 664 с.
. Фармакогнозия. Лекарственное сырье растительного и животного
происхождения: учеб. пособие для студентов фармацевт. вузов, обуч. по
специальности «Фармация» / под ред. Г.П. Яковлева. - 2-е изд., испр. и доп. -
СПб.: СпецЛит, 2010. - 863 с.
. Baglin TP, Keeling DM, Watson HG (February 2006). «Guidelines on
oral anticoagulation (warfarin): third edition-2005 update». Br. J. Haematol.
132 (3).
. Freedman MD (March 1992). «Oral anticoagulants:
pharmacodynamics, clinical indications and adverse effects». J Clin Pharmacol
32 (3): 196-209.
. P.K. Jain and Himanshu Joshi. Coumarin: Chemical and
Pharmacological Profile - Journal of Applied Pharmaceutical Science 02 (06);
2012: 236-240.
. Hirsh J, Fuster V, Ansell J, Halperin JL (2003). «American Heart
Association/American College of Cardiology Foundation guide to warfarin
therapy». J. Am. Coll. Cardiol. 41 (9): 1633-52.
. Manfred Kollroser and Caroline Schober. Determination of
Coumarin-type Anticoagulants in Human Plasma by HPLC-Electrospray Ionization
Tandem Mass Spectrometry with an Ion Trap Detector - Clinical Chemistry 48:1
84-91 (2002).
. fito.nnov.ru
. medicbook.org.ua
. www.herbs2000.com/h_menu/coumarins.htm
. www.ncbi.nlm.nih.gov