|
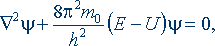
|
(4)
Предложенный вывод «классического»
аналога уравнения Шрёдингера не опирается на какие-либо гипотезы и постулаты.
Это выгодно отличает его от обоснования, данного самим Шрёдингером, которое
всегда представлялось исследователям не вполне убедительным. В особенности это
замечание касается физического смысла функции ψ. В его толковании среди
наиболее крупных физиков-теоретиков до сих пор отсутствует единодушие. В
большинстве своем они трактуют функцию ψ как величину, квадрат которой,
будучи умноженным на элемент объема dV, характеризует вероятность ψ2dV
нахождения частицы в заданной области пространства. Это понятие предполагает
индетерминизм даже на уровне элементарных процессов, т.е. утрату квантовой
механикой способности предсказывать события (определять последующие значения
параметров по предшествующим). Вместе с тем применение понятия вероятности к
отдельному атому или отдельной молекуле в известный момент времени довольно
бессмысленно, так как последние обладают вполне определенным значением
кинетической энергии, находятся в определенном месте и движутся в определенном
направлении. В изложенном же порядке идей волновая функция приобретает простой
и ясный смысл энергии электрона как функции параметров его орбитального
движения. Так решается, пожалуй, самый принципиальный из физических вопросов,
связанных с квантовой механикой. Наряду с этим устраняется одна из
принципиальных трудностей классической электродинамики, состоящая в
невозможности объяснить существование устойчивых орбит электронов из-за
кажущейся неизбежности их «падения» на ядро при излучении ими энергии. Такое
излучение с позиций классической электродинамики должно иметь место даже тогда,
когда величина скорости электрона остается неизменной (изменяется лишь
направление вектора скорости на орбите). Если же излучение порождается
исключительно процессом превращения кинетической энергии в другие формы,
направление скорости уже не играет роли.
Известно, что консервативные системы (E
= const), подчиняющиеся этому уравнению, могут обладать только вполне
определенными значениями энергии. Это же следует и из выражения (1), согласно
которому определенным длинам волн спектра излучения атомов соответствуют
определенные радиусы электронных орбит. Таким образом, идея «квантования»
энергии электронов и их орбит также естественным образом вытекает из классических
представлений.
Предложенный подход выгодно отличается
также от атомной механики Бора, которая хотя и придерживалась в основном
классических принципов, потребовала ряда дополнительных постулатов. Наиболее
уязвимым из них явилось допущение о том, что электрон излучает в момент
перехода с одной орбиты на более низкую, так что частота излучаемых волн
зависит как от начальной, так и от конечной энергии атома. Отсюда следовало,
что электрон либо каким-то непостижимым образом «знает» о будущей орбите, либо излучает
только после попадания на конечную стационарную орбиту. Ввиду неприемлемости
обоих следствий это положение всегда оставалось самым непонятным и слабым
звеном в теории Бора. С изложенных позиций электрон переходит на нижележащую
орбиту лишь после того, как атом излучает энергию. Тем самым устраняется
основная трудность теории Бора.
Представление о том, что излучают не
электроны, а атомы, объясняет также результаты опытов по «дифракции
электронов», поскольку позволяет допустить, что дифракционную картину создают
не электроны, а возбуждаемые ими атомы вокруг отверстия, через которое они
пролетают. Тем самым проливается новый свет на дуализм «волна – частица».
Однако наиболее важным результатом
предложенного подхода являются дополнительные возможности нахождения параметров
электронных орбит по данным спектроскопических наблюдений. В частности, по
известным длинам волн излучения λ или волновым числам νλ
≡ 1/λ = ν/c можно найти радиус i-й устойчивой электронной
орбиты ai атомов, излучающих на этой частоте. Исходя из равенства на
такой орбите центробежной силы fω = mev2/ai
силе взаимодействия электрона с ядром fr = e2/ai2,
после подстановки в выражение νλ = p/hc несложно найти
радиус электронной орбиты, соответствующий определенной частоте излучения:
|
ai = (e2/4π2c2meνλ2)–3
м.
|
(5)
|
После этого нетрудно найти среднюю
орбитальную скорость электронов v = 2πaiν, кинетическую
энергию электрона на i-й орбите Ek = mev2/2 и
число оборотов электрона на орбите n = ν. Однако вопрос о соответствии
такого подхода результатам экспериментов остается при этом открытым.
Список литературы
Де Бройль Л. Ann. De Phys, V. 10, 1925, p. 22. Перевод с фр.: «Введение в волновую механику». – Харьков –
Киев, 1934.
Фейнман Р. Нобелевская лекция. Пер. с
англ. М.: Наука, 1976.
Шрёдингер Э. Ann. Phys., Bd. 79, 1926, p. 361,
489; Bd. 80, 1926, p. 437; Bd. 81, 1926, p. 109. Перевод с нем.: «Четыре лекции по волновой механике». –
Харьков – Киев, 1936.
Де Гроот С., Мазур П. Неравновесная
термодинамика, М.: Мир, 1964.
Эткин В.А. Термодинамика неравновесных
процессов переноса и преобразования энергии. Саратов: Изд-во СГУ, 1991.
Похожие работы на - Классические основания квантовой механики
|