“Перфторан”: революционная комбинация
“Перфторан”: революционная комбинация
Андрей Артурович Недоспасов, д.х.н., Наталия
Владимировна Беда, м.н.с., Институт молекулярной генетики РАН
“Нет
ничего более практичного, чем хорошая теория” - фундаментальная наука неизбежно
находит выход в практику. Увы, в родном отечестве эта аксиома все чаще
оказывается теоремой, проблемой, а то и просто иллюзией. Быть может,
фундаментальные исследования, описанные в этой работе, позволят восстановить статус-кво
и минимизировать ущерб от возникшего дисбаланса.
Многие
лекарственные препараты и методы лечения, открытые задолго до “эры NO”, в
большей или меньшей степени влияют на метаболизм оксидов азота, но действие это
часто остается незамеченным, а лечебные эффекты объясняются какими-то другими
причинами. Яркий пример тому - клиническое применение искусственных
кровезаменителей на основе перфторорганических соединений (ПФС), известных в
России под названиями “Голубая кровь” и “Перфторан” [1-3].
Идея
ПФС-кровезаменителей возникла в конце 60-х годов XX в. Поскольку жидкие ПФС
прекрасно растворяют кислород, эмульсии из них могли бы выполнять
газотранспортную функцию эритроцитов крови. Исследования активно велись в
Японии, СССР и США. В 80-е годы, во время афганской войны, опытные партии
советских препаратов спасли немало жизней раненым, обреченным на неминуемую
смерть от потери крови. В настоящее время “Перфторан” допущен к клиническому
применению и свободно продается в аптеках.
Со
временем выяснилось, что применение “Перфторана”, в том числе в малых дозах,
часто дает положительные эффекты, для которых связь с его газотранспортной
функцией не просматривается. Одновременно обнаружили ряд побочных эффектов,
также не находивших объяснения. Сегодня многие из них стали понятны благодаря
представлениям о мицеллярном окислительном нитрозировании *. Этот термин,
предложенный нами для введения радикала ·NO в гетерогенной среде,
подразумевает, что в значительной степени реакции идут по радикальному
механизму: молекула NO реагирует со свободным радикалом, образовавшимся из
молекулы-мишени под действием ·NO2 - продукта окисления NO.
*
Подробнее см.: Недоспасов А.А., Беда Н.В. Биогенные оксиды азота // Природа.
2005. №7. С.33-39.
Перфторуглеводороды
(ПФУ) - экстремально гидрофобные вещества с большим коэффициентом распределения
Q для кислорода и NO в смесях с водой. Кислород растворяется в них (в
гидрофобной фазе эмульсии) гораздо лучше, чем в воде или плазме крови, из-за
чего они и нашли применение в составе кровезаменителей. Благодаря мицеллярному
катализу микрокапли эмульсии в крови действуют как губки для обоих газов,
именно в них происходит теперь основная часть окисления NO.
В
предыдущей статье мы рассматривали влияние гидрофобных фаз на процессы
окисления NO (например, при образовании холестериновых бляшек на стенке
кровеносного сосуда). При сравнении с эмульсией ПФС-кровезаменителей заметны
три существенных отличия.
Во-первых,
гораздо выше значения Q. Поскольку ускорение реакции окисления NO при введении
оптимальных количеств гидрофобной фазы пропорционально QNO в присутствии
“Перфторана” окисляется гораздо быстрее [4, 5].
При этом увеличиваются скорости нитрозирования и других процессов, зависимых от
мицеллярного катализа, - все они протекают преимущественно в искусственной
гидрофобной фазе или на границе раздела фаз. Концентрация NO в водной фазе
первоначально падает, что приводит к активации ферментов NO-синтаз, поставляющих
NO.
Во-вторых,
капли эмульсии не смачивают стенки сосудов (перфторуглеводороды вообще ничего
не смачивают из имеющихся в организме поверхностей раздела фаз). Более того, NO
из холестериновых бляшек и других “обычных” гидрофобных фаз также частично
переходит в капли эмульсии. Значит, повреждающее действие продуктов окисления
NO на стенки сосудов уменьшается.
В-третьих,
линейные размеры капель эмульсии в “Перфторане” менее 0.1 мкм (диаметр
эритроцита ~20 мкм, а холестериновой бляшки много больше); соответственно,
отношение поверхности к объему оптимально для протекания реакций нитрозирования
на границе раздела. Если в окружающем пространстве присутствуют тиолы (RSH),
капля эмульсии может действовать как миниатюрный реактор по производству
тионитритов (RSNO). В норме в плазме крови довольно высокая концентрация
восстановленного глутатиона (трипептида, содержащего остаток цистеина со
свободной HS-группой), нитрозоформа которого - прекрасный донор NO.
Таким
образом, аналогия капли перфторуглеводородной эмульсии с эритроцитом оказалась
гораздо глубже, чем полагали сначала: оба переносят и кислород, и углекислый
газ, и NO/RSNO. Понятно, что даже малые дозы кровезаменителей типа
“Перфторана”, введенные в кровяное русло, обладают эффектом, характерным для
нитроглицерина (основы динамита и одновременно популярного лекарства), т.е.
вызывают релаксацию сосудов и восстанавливают кровообращение.
В
первых опытах на крысах было наглядно продемонстрировано влияние эмульсий
перфторуглеводородов на метаболизм NO: при введении “Перфторана” наблюдались
предсказанные колебания концентраций нитрита и нитрата в плазме, изменения
частоты сердечных сокращений, обычные при действии вазодилаторов типа
нитроглицерина. Ингибирование NO-синтаз снимало эти эффекты [6].
Несколько лет спустя эту работу повторили в США [7].
Побочные
эффекты применения кровезаменителей типа “Перфторан” во многих случаях
проявлялись не сразу, а спустя значительное время после переливания крови.
Поверхностно-активные вещества, используемые для стабилизации эмульсий при
создании ПФУ-кровезаменителей, выводятся из организма гораздо быстрее, чем сами
ПФУ (характерные времена - сутки и месяц соответственно). Если в первые часы
после введения эмульсия становится основным местом окисления NO, то через сутки
процессы перемещаются главным образом в естественные липидные фазы организма, в
которых растворились ПФУ. Ясно, что в организме они (в виде отдельной фазы или
растворенные в имеющихся гидрофобных фазах) будут влиять не только на параметры
мицеллярного окисления NO из-за роста QO2 и, особенно, QNO, но и на все
последующие процессы, включая нитрование и нитрозирование липидов, белков и
нуклеиновых кислот. Таким образом, “отравления” под действием химически
инертных перфторуглеводородов, в том числе газообразных, растворяющихся в
липидах, можно объяснить потерей устойчивости системы регуляции метаболизма
оксидов азота.
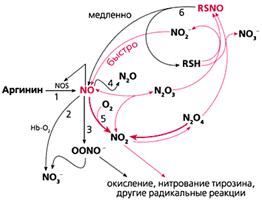
Рис.1.
Схема биосинтеза NO и основные метаболические пути оксидов азота.
Ускорение
окисления NO кислородом отражается на равновесии высших оксидов азота; при этом
их стационарные концентрации меняются. Если электрофильное нитрозилирование
(образование RSNO, рис.1) преимущественно протекает под действием NO+ (N2O3,
N2O4), а радикальные реакции (включая нитрование и окисление белков и
нуклеиновых кислот) - под действием ·NO2, то при использовании искусственных
гидрофобных фаз в качестве кровезаменителей желательно сместить равновесие в
сторону первых, во всяком случае не увеличивать стационарные концентрации NO2.
Концентрации
высших оксидов азота при окислении NO чрезвычайно низки, и измерить их обычными
методами не удается. Мы нашли простой и чувствительный способ, основанный на
определении нитрата в продуктах окисления. Нитрат восстанавливается в нитрит
соединениями ванадия, скорость этого процесса измеряют с помощью реакции Грисса
(по образованию красителя). Если из образца удалить имевшийся первоначально (до
восстановления нитрата) нитрит, весь образовавшийся краситель будет происходить
из нитрата. Поскольку в результате гидролиза N2O3 получается только нитрит
N2O3
+ H2O = 2HNO2, (1)
N2O4
+ H2O = HNO2 + HNO3, (2)
доля
нитрата в продуктах будет мерой стационарных концентраций обоих оксидов. В
целом, в малополярных гидрофобных фазах стабилизация N2O3 при сольватации
минимальна, распад на NO и NO2 усиливается, и доля NO2 должна расти:
NO2
+ NO = N2O3. (3)
Анализ
системы уравнений для стационарных концентраций оксидов азота показал, что
возможно снижение [NO2]ст независимо от изменений [NO]ст и общего пула оксидов
азота [8].
В частности, избирательно ускоряя нитрозилирование, мы снижаем не только [N2O3]ст,
но и [NO2]ст, т.е. скорости всех радикальных реакций с его участием. В этой
связи поиск катализаторов нитрозилирования/денитрозилирования становится важной
задачей биохимии.
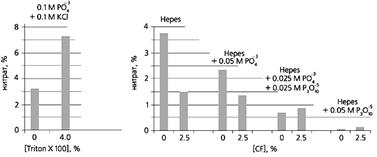
Рис.2.
Гистограмма, отражающая вклад гетерогенности среды и катализаторов
денитрозирования в баланс нитрит/нитрат при окислении NO. Слева: в гетерогенной
среде скорость окисления NO выше, чем в гомогенной. Обычно система равновесий
высших оксидов азота сдвигается в сторону NO2 и N2O4, и доля нитрата в
продуктах возрастает. Triton X 100 - детергент (аналог мыла), использованный
для получения липосом (по данным Liu et al., 1998). Справа: хотя в CF-эмульсиях
скорость окисления NO возрастает сильнее, чем в обычных липидах, сольватация и
скорости гидролиза высших оксидов азота изменены. В присутствии “Перфторана”
доля нитрата в продуктах ниже, чем в гомогенном водном растворе (левая пара
столбиков). Фосфат (PO4– 3 ), пиро- (P2O7–4 ) и триполифосфат (P3O10–5 )
ускоряют гидролиз N2O3 в нитрит. В результате стационарные концентрации NO2 и
N2O4 уменьшаются и выход нитрата падает. Видно, что полифосфат гораздо активнее,
чем фосфат. Hepes - компонент буферного раствора.
Сравним
влияние гетерогенности среды и сольватации на нитрит-нитратный баланс в
продуктах окисления NO в присутствии обычных липидов и в “Перфторане” (рис.2).
Видно, что в первом случае при добавлении гидрофобной фазы доля нитрата (а
значит, вызываемых ·NO2 радикальных реакций!) растет, во втором оказывается
ниже, чем в гомогенном водном растворе [9].
Отчасти эффект связан с каталитическим действием полиэфирного стабилизатора
эмульсии на реакцию нитрозирования. Его можно усилить с помощью других
найденных нами катализаторов. На рис.2 в качестве иллюстрации показаны
каталитические эффекты фосфата и триполифосфата. При увеличении скорости
гидролиза N2O3 (фактически - нитрозилирования воды) уменьшаются стационарные
концентрации как N2O3, так и NO2 из-за сдвига равновесия в реакции (3).
Впрочем,
и здесь не обошлось без парадоксов и неожиданностей. Перфторуглеводороды и их
гетероаналоги (вещества, содержащие помимо C и F другие атомы; например,
перфтороктилбромид - ПФБ), близкие по растворяющей способности в отношении
кислорода, считались одинаково инертными. Поэтому при создании кровезаменителей
выбор конкретных соединений был случайным и определялся в значительной степени
давлением пара и доступностью в чистом виде. (В промышленности ПФУ и их
гетероаналоги получают для далеких от медицины целей, в частности для
электротехники.) Так, основу “Перфторана” составляет смесь изомеров
перфтордекалина и перфтор-(4-циклогексил,N-метил)пиперидина (рис.3). В Японии и
США наиболее популярен перфтороктилбромид (C8F17Br, ПФБ; в кровезаменителях
“Перфлюброн”, “Оксиджент” и др.).
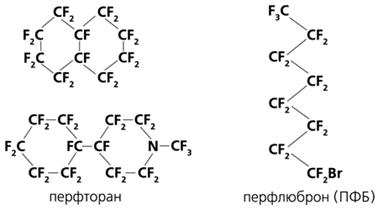
Рис.3.
Формулы перфторорганических соединений, используемых в производстве
кровезаменителей.
Интересно,
что сегодня перфтороктилбромид применяется при искусственной вентиляции легких.
В легкие пациента (чаще в одно) вводят жидкий ПФБ (~1 л) и шланг с распылителем
для подачи воздуха или кислорода. По завершении процедуры шланг удаляется, а
ПФБ остается в легких и медленно (недели-месяцы) выводится с выдыхаемым
воздухом, а часть его обнаруживается в крови.
Неоднократно
отмечалось, что физиологические свойства и кровезаменителей на основе
перфторуглеводородов, перфтороктилбромидов и чистых компонентов различны.
Причины этого оставались непонятными. Действительно, если бы эффекты этих
соединений сводились лишь к транспорту кислорода, они были бы одинаковы для
всех ПФУ и ПФБ, поскольку значения коэффициента распределения NO для
перфтороктилбромидов и не содержащих атома брома перфторсоединений, включая
перфтордекалин (основной компонент “Перфторана”), также оказались близкими.
Таким образом, объяснить различные физиологические эффекты только разной
сольватацией NO не удалось. В этой связи мы поставили под сомнение постулат об
инертности перфтороктилбромидов in vivo и начали искать природные
супернуклеофилы, способные реагировать с ним при температуре тела [10].
Для
перфторалкилгалогенидов были известны реакции перфторалкилирования при катализе
низковалентными комплексами никеля и кобальта. Наиболее известная форма
существования кобальта in vivo - кобаламин (витамин В12), который в
восстановленной форме служит кофактором ряда ферментов (рис.4). Мы показали,
что кобаламин активирует ПФБ, видимо, с образованием перфтороктильного радикала
и Co(II), который может снова восстанавливаться до Co(I). Значит, витамин В12 в
присутствии восстановителей играет роль катализатора перфторалкилирования под
действием ПФБ. Реакцию удалось “визуализировать” с использованием
флюоресцирующих мишеней. В тех же условиях связь C-F оказалась устойчивой: мы
не обнаружили перфторалкилирования под действием перфтордекалина. Судьба
гидрофобных перфторалкильных радикалов in vivo остается неизвестной. Вероятно,
они способны эффективно реагировать с NO (природным инактиватором свободных
радикалов), образуя новые токсичные продукты.
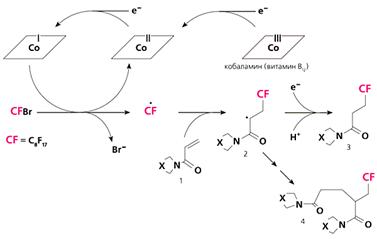
Рис.4.
Схема катализа кобаламином (витамином В12) реакций перфторалкилирования под
действием перфторалкилгалогенидов. In vivo кобаламин восстанавливается до Со+1.
Этот супернуклеофил способен “вырвать” атом брома из молекулы
перфторалкилбромида (показана как CFBr). Образующийся перфторалкильный радикал
CF· вступает в реакции с активированными двойными связями (показан замещенный
акриламид, Х - флюоресцирующая группа), ароматическими соединениями и др. Вновь
образовавшиеся радикалы (2) стабилизируются различными путями, приводя к
стабильным CF-содержащим продуктам (3, 4).
Принципиальное
отличие ПФУ и ПФБ в отношении к супернуклеофилам типа восстановленных форм
кобаламина позволяет объяснить различие свойств кровезаменителей на их основе:
ПФБ в физиологических условиях нельзя считать химически инертным. Аналогичные
объяснения применимы и к многочисленным отравлениям другими
перфторалкилгалогенидами (ПФГ): помимо механизмов, связанных с NO-катастрофами,
они могут участвовать в реакциях перфторалкилирования обычных метаболитов.
Ясно, что низкие концентрации кобаламина в тканях делают их малозаметными, но
не менее неприятными, особенно при больших “периодах полувыведения” (мера
времени жизни в организме) высших гомологов. Не исключено, что в качестве
восстановителей ПФГ, помимо B12, могут выступать и другие метаболиты. Поскольку
современный уровень знаний не позволяет оценить отдаленные последствия и
степень риска, эксперименты с использованием перфторалкилгалогенидов на людях
следовало бы предельно ограничить.
Общее
число пациентов, получивших большие дозы перфтороктилбромидов по медицинским
показаниям, и добровольцев, участников испытаний, неизвестно, но заведомо
пятизначное. Низшие газообразные перфторалкилгалогениды используются как
растворители, в том числе при химической чистке одежды, как фреоны
(бромтрифторметан), а также в огнетушителях и автоматических противопожарных
системах - от военной техники до космических кораблей многоразового
использования (“Спейс Шаттл”). Описано множество случаев отравлений, в том
числе со смертельным исходом, при вдыхании газообразных
перфторалкилгалогенидов. Очевидно, что и длительность воздействия, и
концентрации этих веществ (в частности, в наших химчистках самообслуживания)
могут меняться в широких пределах. Известны примеры, когда серьезные проблемы
со здоровьем и смерть наступали спустя значительное время после отравления ПФГ.
Открытие
перфторалкилирования при катализе известным витамином после 40 лет работ по
использованию ПФГ в медицине поднимает серьезные философские вопросы.
Корреляция между появлением озоновых дыр и попаданием фреонов в атмосферу -
факт, установленный в ходе фундаментальных научных исследований. Реакция
образования перфторалкильных радикалов при облучении фреонов ультрафиолетом
попала не только в вузовские, но и в школьные учебники. Связь алкилирования ДНК
и свободно-радикальных реакций с мутациями и раком должен уметь объяснить любой
выпускник средней школы. Аналогия между озоном и высокоактивными метаболитами,
участвующими в реакциях окисления (в том числе при биосинтезе NO), также
кажется достаточно очевидной. Тем не менее тысячам добровольцев и пациентов
вводили и продолжают вводить большие дозы ПФГ, которые остаются в организме на
месяцы. Остается загадкой, почему и у участников, и у организаторов таких
экспериментов, несмотря на все эти знания, никогда не возникал вопрос о
химической инертности ПФГ in vivo. Отрицательный ответ на этот вопрос мог и
должен был быть получен много лет назад, до начала массовых экспериментов на
людях.
Сегодня
острая необходимость в изучении биохимии ПФГ и методов детоксикации этих
соединений и их потенциальных метаболитов очевидны, поскольку, несмотря на
предупреждения экологов, их по-прежнему широко используют в технике и в быту, и
случайные контакты с ними в случае разного рода аварий и форс-мажорных
обстоятельств будут случаться и впредь даже при полном прекращении
использования перфтороктилбромидов в медицине. Не исключено, что эффективным
методом выведения труднолетучих ПФГ и продуктов их превращений окажется
кратковременное введение стабилизированных эмульсий химически инертных
перфторуглеводородов (типа “Перфторана”) с последующим удалением их
гемосорбцией вместе с “экстрагированными” перфторалкилгалогенидами.
*
* *
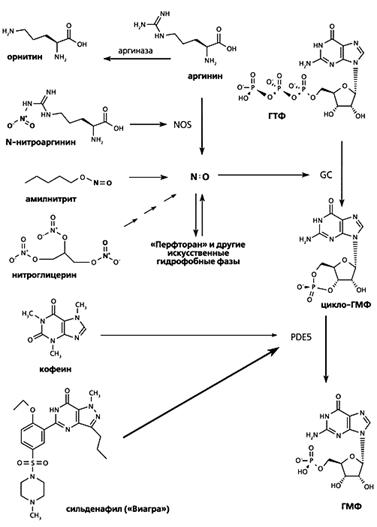
Рис.5.
Популярные фармацевтические препараты, механизм действия которых связан с
регуляцией метаболизма оксидов азота.
Развитие
септического шока связано с чрезмерной активностью NO-синтазы, индуцированной
попавшими в кровоток патогенами. Организм, пытаясь обезопасить себя от
вторжения чужеродных клеток, производит большие количества NO для их
уничтожения. Это приводит к активации гуанилатциклазы, слишком сильному
расширению сосудов, как следствие - к падению давления крови. Смерть наступает
от снижения эффективности кровообращения. Ингибиторы NO-синтазы (например,
нитроаргинин) или введение в кровь аргиназы (фермента, разрушающего аргинин -
предшественник NO) могут быть спасительными.
Уровень
цикло-ГМФ поддерживается балансом активностей гуанилатциклазы (синтез) и
специфической фосфодиэстеразы PDE5 (распад). Ингибирование последней
обеспечивает высокую концентрацию цикло-ГМФ даже при недостатке синтеза NO,
активирующего гуанилатциклазу. Кофеин - слабый и неспецифический ингибитор
фосфодиэстераз, расщепляющих цикло-ГМФ. Сильденафил (“Виагра”) - мощный и
специфический ингибитор фосфодиэстеразы PDE5 - оказался эффективным средством
при импотенции (злые языки утверждают, что именно это открытие было решающим
для членов Нобелевского комитета). Тот же эффект может быть достигнут
ингибированием аргиназы.
“Перфторан”
и другие искусственные гидрофобные фазы могут выступать и как активаторы, и как
блокаторы различных NO-зависимых процессов. Растворимость NO и O2 в эмульсии
перфторуглеводорода выше, чем в плазме крови, что первоначально обеспечивает
переток NO из плазмы в гидрофобную фазу эмульсии, где из-за мицеллярного
катализа скорость его окисления выше, чем в окружающей капли эмульсии плазме. В
целом, концентрация NO в крови падает (показано красной стрелкой), одновременно
падает необратимое окисление NO в нитрат под действием гемоглобина. Снижение
концентрации растворенного NO может активировать NOS. Продукты окисления NO
преимущественно образуются в эмульсии, и именно там выше нитрозилирующая активность.
Дальнейшая судьба продуктов окисления может регулироваться; возможен вариант,
когда эмульсия становится источником NO-доноров.
Скорости
накопления знаний, появления новых технологий к началу третьего тысячелетия
стали буквально фантастическими. В существенной степени столь бурный рост имеет
автокаталитический механизм: он обеспечивается успехами науки в предшествующие
годы и регулируется скоростью превращения фундаментальных научных открытий в
новые технологии, используемые как для “потребления”, так и для дальнейшего
развития исследований. Для биологических наук примерами первых являются
появление методов диагностики и лечения неизлечимых ранее заболеваний или
выведение высокопродуктивных сельскохозяйственных культур. Ко вторым можно
отнести все более тонкие методы анализа (веществ, клеток и целых организмов)
или синтеза сложных “биологических” молекул. В целом, предшествующие успехи в
фундаментальных исследованиях предопределяют новые достижения как в экономике,
так и в самой науке.
Работа
выполнена при поддержке Российского фонда фундаментальных исследований.
Проекты
02-04-49530 и 03-04-06492.
Список литературы
1.
Шноль С.Э. Герои и злодеи российской науки. М., 1997.
2.
Иваницкий Г.Р. // Биофизика. 2001. V.46. P.5-33.
3. Squires J.E. // Science. 2002. V.295. P.1002-1005.
4. Gordin V.A., Nedospasov A.A. // FEBS Lett. 1998. V.424.
P.239-242.
5.
Рафикова О.В. // Татьянин день. Мицеллярный катализ окисления оксида азота в
эмульсиях перфторуглеводородов и его влияние на цикл оксида азота в организме
млекопитающих. М., 2000.
6. Rafikova O., Sokolova E., Rafikov R., Nudler E. // Circulation.
2004. V.110. P.3573-3580.
7. Nedospasov A.A. // J. Biochem. Molecular. Toxicol. 2002. V.16.
P.109-120.
8.
Беда Н.В., Пименова (Сунцова) Т.П., Недоспасов А.А. // Проблемы и перспективы
молекулярной генетики / Ред. Е.Д.Свердлов. М., 2004. Т.2. C.237-301.
9.
Беда Н.В., Недоспасов А.А. // Биохимия. 2003. Т.68. С.1697-1704.
Для
подготовки данной работы были использованы материалы с сайта http://vivovoco.nns.ru