|
Марки стали
|
Содержание
углерода, %
|
Предел прочности при растяжении, МПа
|
Предел текучести, МПа
|
Относительное удлинение, %
|
|
08 кп, пс
10 кп, пс
15 кп, пс
20 кп, пс
25 –
30 –
35 –
40 –
45 –
50 –
60 –
70 –
80 –
|
0,05...0,11
0,07...0,14
0,12...0,19
0,17...0,24
0,22...0,30
0,27...0,35
0,32...0,40
0,37...0,45
0,42...0,50
0,47...0,55
0,57...0,65
0,67...0,75
0,77...0,85
|
330
340
380
420
460
500
540
580
610
640
690
730
1100*
|
200
210
230
250
280
300
320
360
380
410
430
950*
|
35
31
27
25
23
21
20
19
16
14
12
9
6*
|
* Механические свойства после закалки и отпуска.
Примечание: В таблице
приведены только некоторые марки сталей.
Инструментальные
качественные углеродистые стали предназначены для изготовления режущего,
мерительного и штамповочного инструмента небольших размеров. Марки этих сталей
обозначаются буквой У и цифрой, показывающей содержание углерода в десятых
долях процента (У7, У8, У9,..., У13). Высококачественные стали имеют низкое
содержание серы (до 0,02 %) и фосфора (до 0,03%), меньше неметаллических включений,
обладают повышенными механическими свойствами. В обозначениях марок высококачественных
сталей в отличие от качественных ставится буква А (например, У7А,У8Аит. д.).
[2, стр.320-321]
Сталь легированная.
При
введении в углеродистые стали специальных легирующих добавок (Cr, Mn, Ni, Si, W, Mo, Ti, Co, V и др.) достигается
значительное улучшение их физико-механических свойств (например, повышение
предела текучести без снижения пластичности и ударной вязкости и т.д.).
Легирующие
добавки, растворяясь
в железе, искажают и нарушают симметрию его кристаллической решетки, так как
они имеют другие атомные размеры и строение внешних электронных оболочек. Чаще
всего увеличивается карбидосодержащая фаза за счет уменьшения углерода в
перлите, что соответственно увеличивает прочность стали. Многие легирующие
элементы способствуют измельчению зерен феррита и перлита в стали, что
значительно повышает вязкость стали. Некоторые легирующие элементы расширяют
область аустенита, снижая критические точки Ас3, а другие, наоборот,
сужают эту область. Большое значение на практике имеет способность большинства
легирующих элементов повышать прокаливаемость стали на значительную толщину,
задерживая переход аустенита в другие структуры, что создает возможность закаливать
стали при умеренных скоростях охлаждения. При этом уменьшаются внутренние
напряжения и снижается опасность появления закалочных трещин.
Согласно
существующим стандартам легированные стали классифицируют по назначению, химическому
составу и микроструктуре.
По
назначению легированные стали разделяют на три класса: конструкционные
(машиноподелочные и строительные), инструментальные и стали с особыми
физико-химическими свойствами.
Для
обозначения марок сталей принята буквенно-цифровая система. Легирующие элементы
обозначаются буквами: С – кремний, Г – марганец, X – хром, Н – никель, М –
молибден, В – вольфрам, Р – бор, Т – титан, Ю – алюминий, Ф – ванадий, Ц –
цирконий, Б – ниобий, А – азот, Д – медь, К – кобальт, П – фосфор и т.д. Цифры,
стоящие перед буквами, показывают содержание углерода в конструкционных сталях
в сотых долях процента, в инструментальных - в десятых долях процента. Цифры,
стоящие за буквами, показывают содержание легирующих элементов в процентах.
Если содержание элементов не превышает 1,5 %, то цифры не ставят. Буква А,
стоящая в конце марки, означает, что сталь высококачественная. Например, сталь
марки 35ХНЗМА – высококачественная, содержащая 0,35 % С, 1 % Сг, 3 % Ni, 1 % Mo.
По
химическому составу легированные стали делят на три класса: низколегированные с общим
содержанием легирующих элементов до 2,5 %; среднелегированные – от 2,5
до 10% и высоколегированные, содержащие более 10 % таких элементов,
например нержавеющая сталь 1Х18Н9.
В
зависимости от структуры, которую получают легированные стали после нормализации,
их делят на пять классов: перлитная, мартенситная, аустенитная, феррит-ная и
карбидная (ледебуритная). Большинство конструкционных и инструментальных
сталей относится к сталям перлитного класса. Такие стали содержат
незначительное количество легирующих элементов (не более 5...6 %), хорошо
обрабатываются давлением и резанием.
После
нормализации имеют структуру перлита (сорбита, троостита). После закалки и
отпуска заметно повышают механические свойства.
Основным
преимуществом легированных сталей по, сравнению со сталью марки СтЗ является их
большая прочность при сохранении достаточно высокой пластичности и
свариваемости, что позволяет повысить допускаемые напряжения и уменьшить расход
металла на изготовление конструкций, а также повышенная стойкость к атмосферной
коррозии. [2, стр. 321-323]
СТРОЕНИЕ МЕТАЛЛОВ
Исследование
структуры металла проводят путем изучения макроструктуры с увеличением до 10
раз и без увеличения; микроструктуры с увеличением от 10 до 2000 раз на
оптических микроскопах и до 100 000 раз на электронных микроскопах, атомной
структуры – рентгенографическим анализом.
Металлы
представляют собой кристаллические тела с закономерным расположением атомов в узлах
пространственной решетки.
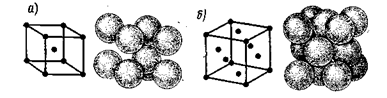
Рис. 3. Элементарный кубический кристалл: а – объемно-центрированный;
б – гранецентрированный
Решетки
состоят из ряда кристаллических плоскостей, расположенных друг от друга на
расстоянии нескольких нанометров (1 нм = 10-9 м). Для железа эти
расстояния 28,4 нм (α=Fe) и 36,3 нм (γ = Fe). Большинство металлов
имеет пространственные решетки в виде простых геометрических фигур. Отдельные
участки кристаллической решетки прочно связаны между собой в комплексы – зерна.
Взаимное расположение зерен отдельных элементов и сплавов определяет структуру
металлов и их свойства.
Атомы
металлов характеризуются малым количеством электронов (1...2) на наружной оболочке,
легко отдают их, что подтверждается высокой электропроводностью.
Черные
металлы имеют простые кубические ячейки решеток (рис. 3) двух видов: а)
центрированный или объемно-центрированный куб (9 атомов в ячейке), объем шаров
занимает 68 %; б) гранецентрированный или куб с центрированными гранями (14
атомов), объем шаров занимает 74 %. Некоторые цветные металлы и их сплавы имеют
гексагональную (шестигранную) решетку.
Железо,
олово, титан и другие металлы обладают свойствами аллотропии, т.е. способностью
одного и того же химического элемента при различной температуре иметь разную
кристаллическую структуру. Аллотропические превращения сопровождаются выделением
или поглощением теплоты. Железо имеет четыре аллотропические формы: α-Fe; β-Fe, γ-Fe, δ-Fe. Практическое значение
имеют α -Fe и γ -Fe, так как p-Fe и б-Fe отличаются от a-Fe только величиной
межатомного расстояния, а для β-Fe характерно отсутствие магнитных свойств.

Рис. 4. Кривые охлаждения и нагревания железа
Температура,
при которой происходит переход металла из одного аллотропического вида в
другой, называется критической. Величины этих температур видны на диаграмме
охлаждения и нагревания чистого железа (рис. 4) в виде участков,
свидетельствующих о том, что фазовые превращения происходят с выделением
теплоты при нагревании.
Все
металлы находятся в твердом состоянии до определенной температуры. При нагреве
металла амплитуда колебания атомов достигает некоторой критической величины,
при которой происходят разрушение кристаллической решетки и переход металлов из
твердого в жидкое состояние. Процесс кристаллизации заключается в росте
кристаллов путем отложения новых кристаллических групп вокруг возникших зародышей.
Рост кристаллических образований происходит в определенных направлениях.
Вначале образуются главные оси кристалла путем роста в трех взаимно
перпендикулярных направлениях, а затем от каждой из этих осей образуются новые
и возникает не полностью завершенный кристалл, называемый дендритом. В
дальнейшем все промежутки между осями дендрита заполняются упорядоченно
расположенными атомами.
В
условиях несвободной кристаллизации образующиеся кристаллы получают неправильные
очертания и форму и называются кристаллитами или зернами. Величина зерен
оказывает существенное влияние на механические свойства металлов: чем мельче
зерна, тем прочнее металл.
Технические
металлы и сплавы представляют собой поликристаллические тела, состоящие из большого
числа различно ориентированных кристаллических зерен (поперечные размеры зерен
– 0,001...0,1 мм). Поэтому в целом металлы и сплавы можно считать условно
изотропными телами.
Структура.
Сплавы
обладают металлическими свойствами и состоят из двух элементов и более. Элементы,
входящие в состав сплавов, называют компонентами.
Компоненты
сплавов
в процессе затвердевания и последующего охлаждения могут образовывать
химические соединения, твердые растворы на базе одного из компонентов или
нового химического соединения и механические смеси.
Химические
соединения, образующиеся на основании общих химических законов (валентности,
ионной связи), могут быть выражены химическими индексами. Обычно химические
соединения повышают твердость и хрупкость металлов и, как правило, имеют
кристаллическую решетку другого типа, чем у каждого из элементов в отдельности.
Твердые
растворы
– сплавы, у которых атомы растворимого элемента рассеяны в кристаллической
решетке растворителя; растворимый элемент может замещать часть атомов основного
металла или внедряться между ними, но без образования молекул определенного
состава. В железоуглеродистых сплавах Fe–С атомы углерода внедряются в поры решетки Fe. В отличие от химических
соединений состав твердых растворов непостоянен и зависит от температуры и
концентрации (проникания одного элемента кристаллической решетки в другой).
Кристаллическая решетка твердого раствора сохраняет тип решетки одного из компонентов,
который по этому признаку считается растворителем.
Механические
смеси (эвтектики, эвтектоиды) – микроскопически малые, тесно перемешанные и
связанные между собой компоненты сплава, состоящие из чистых металлов, твердых
растворов и химических соединений. Эвтектики образуются из жидкого сплава при
охлаждении и характеризуются самой низкой температурой затвердевания смеси,
хорошими литейными качествами и высокими механическими свойствами. Эвтектоиды
образуются при распаде твердого раствора. Эвтектические и эвтектоидные смеси
возникают при определенной концентрации отдельных составляющих и определенной
температуре. В сплавах, отличных по составу от эвтектических, при затвердевании
в первую очередь выпадает компонент, избыточный по отношению к эвтектическому.
Изменения
структуры и свойств сплавов с изменением концентрации и температуры в наглядной
форме представлены на диаграммах состояния сплавов. Эти диаграммы не содержат
фактора времени и соответствуют условию очень медленного нагрева и охлаждения.
Диаграмма состояния
железоуглеродистых сплавов (рис. 5).
Основными
структурами, составляющими железоуглеродистые сплавы, являются следующие.
Феррит – твердый раствор
углерода в α -Fe. При температуре 723° С
предельное содержание углерода 0,02 %. При отсутствии примесей не корродирует.
Цементит – карбид железа Fe3C – химическое соединение,
содержащее 6,67 % углерода. Является составной частью эвтектической смеси, а
также самостоятельной структурной составляющей. Способен образовывать твердые
растворы путем замещения атомами других металлов, неустойчив, распадается при
термической обработке. Цементит очень тверд (НВ 800) и хрупок.
Аустенит – твердый раствор
углерода в γ –Fe. Атомы углерода
внедряются в кристаллическую решетку, причем насыщение может быть различным в
зависимости от температуры и примесей. Устойчив только при высокой температуре,
а с примесями Mn, Сг – при обычных, даже низких температурах. Твердость аустенита
НВ 170...220.
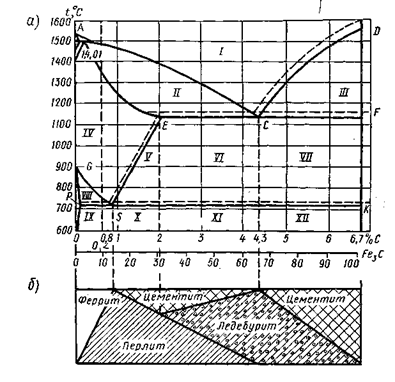
Рис. 5. Диаграмма состояния железоуглеродистых сплавов:
а – диаграмма; I – жидкий
сплав; II – жилкий сплав и кристаллы аустенита; III – жидкий
сплав и цементит; IV – аустенит; V – цементит и аустенит; VI – аустенит, цементит,
ледебурит; VII – цементит и ледебурит; VIII – феррит и аустенит; IX – феррит и
перлит; X – цементит и перлит; XI – перлит, цементит;
ледебурит; XII – цементит, ледебурит; б – ориентировочные
отношения структурные составляющих в различных областях диаграммы.
Перлит
– эвтектоидная
смесь феррита и цементита, образуется при распаде аустенита при температуре
723° С и содержании углерода 0,83 %. Примеси Si и Мn способствуют образованию
перлита и при меньшем содержании углерода. Твердость перлита НВ 160...260.
Структура перлита может быть пластинчатой и глобулярной (зернистой).
Ледебурит
– эвтектическая
смесь аустенита и цементита, образующаяся при 1130° С и содержании углерода 4,3
% Структура неустойчивая: при охлаждении аустенит, входящий в состав
ледебурита, распадается на вторичный цементит и перлит. Ледебурит очень тверд
(НВ 700) и хрупок.
Графит – мягкая и хрупкая
составляющая чугуна, состоящая из разновидностей углерода. Встречается в серых
и ковких чугунах.
На
диаграмме состояния железоуглеродистых сплавов (рис 5) на оси ординат отложена
температура, на оси абсцисс – содержание в сплавах углерода до 6,67 % т.е. до такого
количества, при котором образуется химическое соединение Fe3C – цементит. Пунктирными
линиями нанесена диаграмма состояния для системы железо – графит, так как
возможен распад цементита Fe3С.
Рассматриваемую
диаграмму правильнее считать не железоуглеродистой, а железоцементитной, так
как свободного углерода в сплавах не содержится. Но так как содержание углерода
пропорционально содержанию цементита, то практически удобнее все изменения
структуры сплавов связывать с различным содержанием углерода.
Все
линии на диаграмме соответствуют критическим точкам, т. е. тем температурам,
при которых происходят структурные изменения в сплавах. Критические точки для
стали впервые открыл русский ученый-металлург Д.К. Чернов.
Линия
ACD – линия начала
кристаллизации сплава (линия ликвидуса), линия AECF – линия конца
кристаллизации сплава (линия солидуса). Только чистые металлы и эвтектика
плавятся и затвердевают при постоянной температуре. Затвердевание всех
остальных сплавов происходит постепенно, причем из жидкого сплава сначала
выделяется избыточный по отношению к составу эвтектики компонент. Область AESG на диаграмме соответствует
аустениту. Линия GS – начало выделения феррита, а линия SE – вторичного цементита.
Линия PSK соответствует окончательному распаду аустенита и
выделению перлита. В области ниже линии PSK никаких изменений
структуры не происходит.
В
зависимости от содержания углерода железоуглеродистые сплавы получают следующие
названия:
При содержании углерода <0,83
% – доэвтектоидные стали
»
» » 0,83...2% – заэвтектоидные
стали
»
» » 2,0...4,3% – доэвтектические
чугуны
»
» » 4,3.. .6,67% – заэвтектические
чугуны
С увеличением
содержания углерода в железоуглеродистых сплавах меняется и структура, увеличивается
содержание цементита и уменьшается количество феррита. Чем больше углерода в
сплавах, тем выше твердость, прочность, но ниже их пластические свойства.
Механические свойства сплавов зависят также от формы и размера частиц
структурных составляющих. Твердость и прочность стали тем выше, чем тоньше и
мельче частицы феррита и цементита. [2, стр. 302-308]
СВОЙСТВА МЕТАЛЛОВ
Химические свойства.
В соответствии с местом, занимаемым в периодической системе
элементов, различают металлы главных и побочных подгрупп. Металлы главных
подгрупп (подгруппы а) называются также непереходными. Эти металлы
характеризуются тем, что в их атомах происходит последовательное заполнение s-и p-электронных оболочек. В
атомах металлов побочных подгрупп (подгруппы б), называемых переходными,
происходит достраивание d- и f-оболочек, в соответствии с чем их делят на d-группу и две f-группы – лантаноиды и
актиноиды. В подгруппы а входят 22 металла: Li, Na, К, Rb, Cs, Fr (I a);
Be, Mg, Ca, Sr, Ba, Ra (II a); Al, Ga, In, Tl (III a); Ge, Sn, Pb
(IV a); Sb, Bi (V a); Po (VI a). В подгруппы б входят: 1) 33 переходных металла d-группы [Сu, Ag, Аи (I б); Zn, Cd, Hg
(II б); Sc, Y, La,
Ac (III 6); Ti, Zr, Hf, Ku (IV б); V, Nb, Та, элемент с Z = 105 (V б); Сr, Mo, W (VI б); Mn, Тс, Re (VII б); Fe, Co, Ni,
Ru, Rh, Pd, Os, Ir, Pt (VIII б)]; 2) 28 металлов f-группы (14 лантаноидов и 14 актиноидов).
Электронная структура атомов некоторых d-элементов имеет ту
особенность, что один из электронов внешнего уровня переходит на d-подуровень. Это происходит
при достройке этого подуровня до 5 или 10 электронов. Поэтому электронная
структура валентных подуровней атомов d-элементов, находящихся в одной подгруппе, не
всегда одинакова. Например, Cr и Мо (подгруппа VI б) имеют внешнюю
электронную структуру соответственно 3d54s1 и 4d55s1, тогда как у W она 5d46s2. В атоме Pd (подгруппа VIII 6) два внешних
электрона «перешли» на соседний валентный подуровень, и для атома Pd наблюдается d10 вместо ожидаемого d8s2.
Металлам присущи многие общие химические свойства, обусловленные
слабой связью валентных электронов с ядром атома: образование положительно
заряженных ионов (катионов), проявление положительной валентности
(окислительного числа), образование основных окислов и гидроокисей, замещение
водорода в кислотах и т.д. Металлические свойства элементов можно сравнить,
сопоставляя их электроотрицательность [способность атомов в молекулах (в
ковалентной связи) притягивать электроны, выражена в условных единицах];
элементу присущи свойства металла тем больше, чем ниже его электроотрицательность
(чем сильнее выражен электроположительный характер).
Если расположить металлы в последовательности увеличения их нормальных
потенциалов, получим так называемый ряд напряжений или ряд активностей.
Рассмотрение этого ряда показывает, что по мере приближения к его концу – от
щелочных и щёлочноземельных металлам к Pt и Аи – электроположительный
характер членов ряда уменьшается. Металлы от Li по Na вытесняют Н2
из Н2О на холоду, а от Mg по Тl – при нагревании. Все металлы, стоящие в ряду
выше Н2, вытесняют его из разбавленных кислот (на холоду или при
нагревании). Металлы, стоящие ниже Н2, растворяются только в
кислородных кислотах (таких, как концентрирированная H2SO4 при нагревании или HNO3), a Pt, Аи – только в царской
водке (Ir нерастворим и в ней).
Металлы от Li no Na легко реагируют с О2 на холоду;
последующие члены ряда соединяются с О2 только при нагревании, a Ir, Pt, Аи в прямое
взаимодействие с О2 не вступают. Окислы металлов от Li no Al и от La no Zn трудно восстановимы; по
мере продвижения к концу ряда восстановимость окислов увеличивается, а окислы
последних его членов разлагаются на металлы и О2 уже при слабом
нагревании. О прочности соединений металлов с кислородом (и др. неметаллами)
можно судить и по разности их электроотрицательностей: чем она больше, тем
прочнее соединение [3, стр. 133-134].
Физические свойства.
Большинство металлов кристаллизуется в относительно простых
структурах – кубических и гексагональных ЛГУ, соответствующих наиболее плотной
упаковке атомов. Лишь небольшое число металлов имеет более сложные типы
кристаллических решёток. Многие металлы в зависимости от внешних условий
(температуры, давления) могут существовать в виде двух или более
кристаллических модификаций.
Электрические свойства. Удельная электропроводность металлов при
комнатной температуре σ~10-6–10-4 ом-1
см-1, тогда как у диэлектриков, например, у серы,
σ~10-17 ом-1 см-1.
Промежуточные значения σ соответствуют полупроводникам. Характерным
свойством металлов как проводников электрического тока является линейная
зависимость между плотностью тока и напряжённостью приложенного электрического
поля. Носителями тока в металлах являются электроны проводимости,
обладающие высокой подвижностью. Согласно квантово-механическим представлениям,
в идеальном кристалле электроны проводимости (при полном отсутствии
тепловых колебаний кристаллической решётки) вообще не встречают
сопротивления на своём пути. Существование у реальных металлов электросопротивления
является результатом нарушения периодичности кристаллической решётки. Эти
нарушения могут быть связаны как с тепловым движением атомов, так и с наличием
примесных атомов, вакансий, дислокаций и др. дефектов в кристаллах. На
тепловых колебаниях и дефектах (а также друг на друге) происходит рассеяние
электронов.
При нагревании металлов до высоких температур наблюдается
«испарение» электронов с поверхности металлов (термоэлектронная эмиссия).
Эмиссия электронов с поверхности металлов происходит также под действием
сильных электрических полей ~ 107 в/см в результате
туннельного просачивания электронов через сниженный полем потенциальный барьер.
В металлах наблюдаются явления фотоэлектронной эмиссии, вторичной
электронной эмиссии и ионно-электронной эмиссии. Перепад температуры
вызывает в металлах появление электрического тока или разности потенциалов
Тепловые свойства. Теплоёмкость металлов обусловлена как ионным
остовом (решёточная теплоёмкость Ср), так и электронным газом
(электронная теплоёмкость Сэ). Хотя концентрация электронов проводимости
в металлах очень велика и не зависит от температуры, электронная теплоёмкость
мала и у большинства металлов наблюдается только при температурах в несколько
градусов кельвина. Теплопроводность металлов осуществляется главным образом
электронами проводимости.
Магнитные свойства. Переходные металлы с недостроенными f- и d-электронными оболочками
являются парамагнетиками. Некоторые из них при определённых температурах
переходят в магнитоупорядоченное состояние. Магнитное упорядочение существенно
влияет на все свойства металлов, в частности на электрические свойства: в
электросопротивление вносит вклад рассеяние электронов на колебаниях магнитных
моментов. Гальваномагнитные явления при этом также приобретают специфические черты.
Магнитные свойства остальных металлов определяются электронами
проводимости, которые вносят вклад в диамагнитную и парамагнитную
восприимчивости металлов, и диамагнитной восприимчивостью ионного состава.
Магнитная восприимчивость X большинства металлов относительно мала (X ~ 10-6) и слабо
зависит от температуры.
Механические свойства. Многие металлы обладают комплексом механических
свойств, обеспечивающим их широкое применение в технике, в частности в качестве
конструкционных материалов. Это, в первую очередь, сочетание высокой пластичности
со значит, прочностью и сопротивлением деформации, причём
соотношение этих свойств может регулироваться в большом диапазоне с помощью
механических и термических обработки металлов, а также получением сплавов
различного состава.
Исходной характеристикой механических свойств металлов является модуль
упру гости G, определяющий сопротивление кристаллической решётки упругому
деформированию и непосредственно отражающий величину, сил связи в кристалле. В
монокристаллах эта величина, как и остальные механические характеристики,
анизотропна и коррелирует с температурой плавления металла (например, средний
модуль сдвига G
изменяется от 0,18-1011 эрг/см3 для легко плавкого
Na до 27•1011 эрг/см3
для тугоплавкого Re).
Сопротивление разрушению или пластической деформации идеального кристалла
примерно 10-1 G. Но в реальных кристаллах эти характеристики, как
и все механические свойства, определяются наличием дефектов, в первую очередь
дислокация. Перемещение дислокаций по плотноупакованным плоскостям приводит к
элементарному акту скольжения – основному механизму пластической деформации
металла. Важнейшая особенность металлов – малое сопротивление скольжению
дислокации в бездефектном кристалле. Это сопротивление особенно мало в
кристаллах с чисто металлической связью, которые обычно имеют плотноупакованные
структуры. В металла с ковалентной компонентой межатомной связью, имеющих
объемно-центрированную решётку, сопротивление скольжению несколько больше,
однако всё же мало по сравнению с чисто ковалентными кристаллами. Сопротивление
пластической деформации, по крайней мере в металлах с гранецентрированной
кубической и гексагональной решётками, связано с взаимодействием движущихся
дислокаций с др. дефектами в кристаллах, с др. дислокациями, примесными
атомами, внутренними поверхностями раздела. Взаимодействие дефектов
определяется искажениями решётки вблизи них и пропорционально G. Для отожжённых монокристаллов
начальное сопротивление пластической деформации (предел текучести) обычно ~
10-3–10-4 G. Для монокристаллов металлов характерно наличие
трёх стадий деформационного упрочнения. На 1-й стадии значительная часть
дислокаций выходит на поверхность и коэффициент упрочнения мал; на 2-й стадии
дислокации накапливаются в кристалле, их распределение становится существенно
неоднородным. На 3-й стадии плотность дислокации, G и коэффициент упрочнения
уменьшаются вследствие аннигиляции дислокаций, выдавливаемых из их плоскостей
скольжения. Значение этой стадии больше для металлов с объемно-центрированной
решёткой.
При Т > 0,5 Тпл в пластической
деформации начинают играть существенную роль точечные дефекты, в первую очередь
вакансии, которые, оседая на дислокациях, приводят к их выходу из плоскостей
скольжения. Если этот процесс достаточно интенсивен, то деформация не
сопровождается упрочнением: металл течёт с постоянной скоростью при неизменной
нагрузке (ползучесть). Протекание процессов релаксации напряжений и постоянная
разрядка дислокационной структуры обеспечивают высокую пластичность металлов
при их горячей обработке, что позволяет придавать изделиям из металлов
разнообразную форму. Отжиг сильно деформированных монокристаллов металлов
нередко приводит к образованию поликристаллов с малой плотностью
дислокаций внутри зёрен (рекристаллизация).
Достижимые степени деформации металлов ограничены процессом
разрушения. По мере роста плотности дислокаций при холодной деформации растёт
неравномерность их распределения, приводящая к концентрации напряжений в местах
сгущения дислокаций и зарождению здесь очагов разрушения – трещин. В реальных
кристаллах такие концентрации напряжений имеются и в исходном недеформированном
состоянии (скопление примесей, частицы др. фаз и т.п.). Но вследствие
пластичности металла деформация вблизи опасных мест снимает напряжения и
предотвращает разрушение. Однако если сопротивление движению дислокаций растёт,
то релаксационная способность материала падает, что под нагрузкой приводит к
развитию трещин (хрупкое разрушение). Это особенно проявляется в металлах с
объёмно-центрированной решёткой, в которых подвижность дислокаций резко
уменьшается при понижении температуры (из-за взаимодействия с примесями и
уменьшения числа кристаллографических возможных плоскостей скольжения). Предотвращение
хладноломкости – одна из важнейших технических проблем разработки конструкционных
металлических материалов. Другая актуальная проблема – увеличение прочности и
сопротивления деформации при высоких температурах. Зародышами разрушения в этих
условиях служат микропоры, образующиеся в результате скопления вакансий.
Эффективный способ повышения высокотемпературной прочности – уменьшение
диффузионной подвижности точечных дефектов, в частности легированием.
Применяемые в технике конструкционные металлические материалы
являются поликристаллическими. Их механические свойства практически изотропны и
могут существенно отличаться от свойств монокристаллов металлов. Межфазные
границы вносят дополнительный вклад в упрочнение. С другой стороны, они могут
быть местами предпочтительного разрушения (межзёренное разрушение) или
деформации. Изменяя число и строение межфазных границ, форму и пространственное
расположение отдельных структурных составляющих многофазных систем
(поликристаллов, гетерофазных агрегатов, возникающих вследствие фазовых
превращений, или искусственно полученных композиций), а также регулируя состав
и дефектную структуру отдельных кристаллов, можно получить огромное
разнообразие механических свойств, необходимых для практического использования
металлических материалов. [3, стр. 133-136].
ПРИМЕНЕНИЕ МЕТАЛЛОВ В СТРОИТЕЛЬСТВЕ.
Сталь.
В
строительстве сталь используют для изготовления конструкций, армирования
железобетонных конструкций, устройства кровли, подмостей, ограждений, форм
железобетонных изделий и т.д. Правильный выбор марки стали обеспечивает
экономный расход стали и успешную работу конструкции.
Для
изготовления несущих (расчетных) сварных и клепаных конструкций рекомендуют
следующие виды сталей: мартеновскую – марок ВМСтЗпс (сп, кп), низколегированную
– марок 15ГС, 14Г2, 10Г2С, 10Г2СД; природно-легированную – марок 15ХСНД,
10ХСНД; кислородно-конвертерную – марок ВКСтЗсп (пс, кп).
Стали
марок Ст4 и Ст5 рекомендуют для конструкций, не имеющих сварных соединений, и
для сварных конструкций, воспринимающих лишь статические нагрузки.
Сталь
для конструкций, работающих на динамические и вибрационные нагрузки и
предназначенных для эксплуатации в условиях низких температур, должна
дополнительно проверяться на ударную вязкость при отрицательных температурах.
К
стали для мостовых конструкций предъявляют специальные требования (ГОСТ
6713-75) по однородности и мелкозернистости, отсутствию внешних дефектов,
прочностным и деформационным свойствам.
Для
армирования железобетонных конструкций сталь применяют в виде стержней,
проволоки, сварных сеток, каркасов. Арматурная сталь может быть горячекатаная
(стержневая) и холоднотянутая (проволочная). По форме сталь чаще всего бывает
круглая, а для улучшения сцепления – периодического профиля. В отдельных
случаях для повышения механических свойств сталь обрабатывают наклепом и
применяют термическую обработку.
Стержневую
арматуру в
зависимости от механических свойств делят на классы: A-I, A-II, A-III, A-IV и др. При обозначении
класса термически упрочненной арматурной стали добавляют индекс «т» (например,
Ат-III), упрочненную вытяжкой –
«в» (например, А-Шв).
Арматурная
проволока может
быть холоднотянутой класса B-I (низкоуглеродистой) для ненапрягаемой арматуры и класса В-II (углеродистой) для
напрягаемой арматуры. Для обычного армирования преимущественно применяют
арматурную сталь классов A-III (марок 25Г2С, 35ГС и др.), А-II (марок Ст5) и
обыкновенную арматурную проволоку, а при особом обосновании также A-I (марки СтЗ) и А-IIв. Для предварительно
напряженного армирования используют высокопрочную проволоку, арматурные пряди и
арматуру класса A-IV (марок ЗОХГ2С, 20ХГСТ, 20ХГ2Ц и другие низколегированные стали),
а также упрочненную вытяжкой сталь класса А-IIIв (марок 35ГС, 25Г2С).
Сортамент
прокатного металла и металлоизделий в строительстве разнообразен: сортовая сталь,
прокатная сталь листовая, уголки, швеллеры, двутавры, трубы и другие служат
основой для изготовления металлических конструкций (балки, колонны, фермы и
т.д.). На сортаменты имеются ГОСТы наиболее рациональных типов профилей и
частоты их градаций.
Сортовая
сталь:
круглая (диаметром 10...210 мм) применяется для изготовления арматуры,
скоб, болтов; квадратная (сторона квадрата 10...100 мм); полосовая (шириной
12...20 мм) – для изготовления связей, хомутов, бугелей.
Сталь
листовая включает
листы толщиной от 4…160 мм, шириной 600...3800 мм; тонколистовая кровельная –
черная и оцинкованная толщиной до 4 мм; широкополочная толщиной 6...60 мм,
шириной 200...1500 мм, длиной 5...12 м.
Уголковые
профили (равнополочные
и неравнополочные) выпускают площадью сечения 1,0...140 см2.
Швеллеры
характеризуются
сечением швеллеров и определяются его номером, который соответствует высоте
стенки швеллера в сантиметрах.
Двутавры
– основной
балочный профиль – разнообразны по типам; обозначаются номером, соответствующим
их высоте в сантиметрах. Трубы круглые имеют диаметр 8... …1620 мм. Трубы могут
быть квадратного и прямоугольного сечения.
В
строительстве также широко применяют специальные профили и металлические
материалы: стальные канаты и проволоку, профилированные настилы и
т.д. [2, стр. 323-325]
Чугуны.
Чугунами
называют железоуглеродистые сплавы, содержащие более 2 %. углерода. Чугун
обладает более низкими механическими свойствами, чем сталь, но дешевле и хорошо
отливается в изделия сложной формы. Различают несколько видов чугуна.
Белый
чугун, в
котором весь углерод (2,0...3,8%) находится в связанном состоянии в виде Fe3C (цементита), что и
определяет его свойства: высокие твердость и хрупкость, хорошую
сопротивляемость износу, плохую обрабатываемость режущими инструментами. Белый
чугун применяют для получения серого и ковкого чугуна и стали.
Серый
чугун содержит
углерод в связанном состоянии только частично (не более 0,5%). Остальной
углерод находится в чугуне в свободном состоянии в виде графита. Графитовые
включения делают цвет излома серым. Чем излом темнее, тем чугун мягче. Образование
графита происходит в результате термической обработки белого чугуна, когда
часть цементита распадается на мягкое пластичное железо и графит. В зависимости
от преобладающей структуры различают серый чугун на перлитной, ферритной или
ферритоперлитной основе.
Свойства
серого чугуна зависят от режима охлаждения и наличия некоторых примесей.
Например, чем больше кремния, тем больше выделяется графита, а потому чугун
делается мягче. Серый чугун имеет умеренную твердость и легко обрабатывается
режущими инструментами. Серый чугун, применяемый в строительстве, должен иметь
предел прочности при растяжении не менее 120 МПа, а предел прочности при изгибе
280 МПа.
Из
серого чугуна отливают элементы конструкций, хорошо работающие на сжатие:
колонны, опорные подушки, башмаки, тюбинги, отопительные батареи, трубы водопроводные
и канализационные, плиты для полов, станины и корпусные детали станков, головки
и поршни двигателей, зубчатые колеса и другие детали.
Ковкий
чугун получают
после длительного отжига % белого чугуна при высоких температурах, когда
цементит почти полностью распадается с выделением свободного углерода на
ферритной или перлитной основе. Углеродные включения имеют округлую форму. В
отличие от серых ковкие чугуны являются более прочными и пластичными и легче
обрабатываются.
Высокопрочные
(модифицированные) чугуны значительно превосходят обычные серые по прочности и обладают
некоторыми пластическими свойствами. Их применяют для отливок ответственных
деталей.
При
испытании серого и высокопрочного чугунов определяют предел прочности при
растяжении, изгибе и сжатии, а при испытании ковкого чугуна – предел прочности
при растяжении, относительное удлинение и твердость.
При
маркировке серого и модифицированного чугуна, например СЧ12-28, первые две
цифры обозначают предел прочности при растяжении, последующие две – предел
прочности при изгибе. [2, стр. 325-326]
Цветные металлы и сплавы.
Сплавы
цветных металлов применяют для изготовления деталей, работающих в условиях
агрессивной среды, подвергающихся трению, требующих большой теплопроводности,
электропроводности и уменьшенной массы.
Медь
– металл
красноватого цвета, отличающийся высокой теплопроводностью и стойкостью против
атмосферной коррозии. Прочность невысокая: σв = 180...240 МПа
при высокой пластичности δ>50%.
Латунь
– сплав
меди с цинком (10...40 %), хорошо поддается холодной прокатке, штамповке, вытягиванию
σв=250...400 МПа, δ=35...15%. При маркировке латуней (Л96,
Л90, ..., Л62) цифры указывают на содержание меди в процентах. Кроме того,
выпускают латуни многокомпонентные, т.е. с другими элементами (Мn, Sn.Pb.Al).
Бронза
– сплав
меди с оловом (до 10%), алюминием, марганцем, свинцом и другими элементами.
Обладает хорошими литейными свойствами (вентили, краны, люстры). При маркировке
бронзы Бр.ОЦСЗ-12-5 отдельные индексы обозначают: Бр – бронза, О – олово, Ц –
цинк, С – свинец, цифры 3, 12, 5 – содержание в процентах олова цинка, свинца.
Свойства бронзы зависят от состава: σв=150...2Ю МПа,
δ=4...8%, НВ60 (в среднем).
Алюминий
– легкий
серебристый металл, обладающий низкой прочностью при растяжении – σв
=80...100 МПа, твердостью – НВ20, малой плотностью – 2700 кг/м3,
стоек к атмосферной коррозии. В чистом виде в строительстве применяют редко
(краски, газообразователи, фольга). Для повышения прочности в него вводят
легирующие добавки (Мn, Сn, Mg, Si, Fe) и используют некоторые технологические приемы. Алюминиевые
сплавы делят на литейные, применяемые для отливки изделий (силумины), и
деформируемые (дюралюмины), идущие для прокатки профилей, листов и т.п.
Силумины
– сплавы
алюминия с кремнием (до 14%), они обладают высокими литейными качествами, малой
усадкой, прочностью σв = 200 МПа, твердостью НВ50...70 при
достаточно высокой пластичности δ=5...10%. Механические свойства силуминов
можно существенно улучшить путем модифицирования. При этом увеличивается
степень дисперсности кристаллов, что повышает прочность и пластичность
силуминов.
Дюралюмины—
сложные
сплавы алюминия с медью (до 5,5 %), кремнием (менее 0,8 %), марганцем (до 0,8
%), магнием (до 0,8 %) и др. Их свойства улучшают термической обработкой
(закалкой при температуре 500...520°С с последующим старением). Старение
осуществляют на воздухе в течение 4...5 сут при нагреве на 170СС в
течение 4...5 ч.
Термообработка
алюминиевых сплавов основана на дисперсном твердении с выделением твердых
дисперсных частиц сложного химического состава. Чем мельче частицы
новообразований, тем выше эффект упрочнения сплавов. Предел прочности дюралюминов
после закалки и старения составляет 400...480 МПа и может быть повышен до
550...600 МПа в результате наклепа при обработке давлением.
В
последнее время алюминий и его сплавы все шире применяют в строительстве для
несущих и ограждающих конструкций. Особенно эффективно применение дюралюминов
для конструкций в большепролетных сооружениях, в сборно-разборных конструкциях,
при сейсмическом строительстве, в конструкциях, предназначенных для работы в
агрессивной среде. Начато изготовление трехслойных навесных панелей из листов
алюминиевых сплавов с заполнением пенопластовыми материалами. Путем введения
газообразователей можно создать высокоэффективный материал пеноалюминий со
средней плотностью 100...300 кг/м3. йг
Все
алюминиевые сплавы поддаются сварке, но она осуществляется более трудно, чем
сварка стали, из-за образования тугоплавких оксидов Аl2О3.
Особенностями
дюралюмина как конструкционного сплава являются: низкое значение модуля упругости,
примерно в 3 раза меньше, чем у стали, влияние температуры (уменьшение
прочности при повышении температуры более 400°С и увеличение прочности и
пластичности при отрицательных температурах); повышенный примерно в 2 раза по
сравнению со сталью коэффициент линейного расширения; пониженная свариваемость.
Титан
за
последнее время начал применяться в разных отраслях техники благодаря ценным
свойствам: высокой коррозионной стойкости, меньшей плотности (4500 кг/м3)
по сравнению со сталью, высоким прочностным свойствам, повышенной
теплостойкости. На основе титана создаются легкие и прочные конструкции с
уменьшенными габаритами, способные работать при повышенных температурах. [2,
стр.326-328]
ЛИТЕРАТУРА
1. Технология металлов и сварка. Под
ред. П.И. Полухина. М. Высшая школа. 1977.
2. Строительные материалы. А.Г.
Домокеев. М. Высшая школа. 1989
3. Большая советская энциклопедия. Под
ред. А.М. Прохорова. М. изд. «Советская энциклопедия». 1974.