Влияние стресса на показатели крови мышей
Оглавление
Введение. 3
Материалы и методы.. 3
1.Техника вскрытия лабораторных мышей
и взятие крови из сердца. 3
2. Методика нанесения мазка. 5
3. Подсчёт лейкоцитарной формулы. 7
4. Осмотическая резистентность
эритроцитов. 9
5.Выделение костного мозга. 10
6.Определение активности АЛТ и АСТ. 10
Результаты и обсуждения. 13
Заключение. 15
Список литературы.. 16
Цель:
Изучить влияние стресса на компоненты крови мышей.
На
основе выше поставленной целы были определены следующие задачи:
1.
Оценить средний рост и вес
экспериментальных животных;
2.
Изучить изменение параметров
лейкоцитарной формулы;
3.
Выделить клетки костного мозга из
бедерной кости;
4.
Изучить активность в плазме
мышей группы контроля и группы мышей подверженных стрессу;
5.
Изучить осмотическую
резистентность у группы контроля и у мышей подверженных стрессу.
Объектом
исследования явились 7 мышей женского пола. Материалом послужила кровь взятая из
сердца в шприцы с добавлением гепарина натрия.
Для
того чтобы произвести взятие крови из сердца мышки надо на носик мышки
поместить небольшую ёмкость с тампоном смоченным эфиром, чтобы она могла дышать
открываем ей рот. Важно, чтобы мышка оставалась жива во время взятия
крови!!! Для удобства вскрытия труп животного фиксируют. Для фиксации
используют инъекционные иглы или одностержневые булавки (портновские). Вскрытие
выполняют стерильными инструментами. Брюшную и грудную полости вскрывают при
фиксации животного в спинном положении с направленными в стороны и укрепленными
передними и задними конечностями (рис. 1).
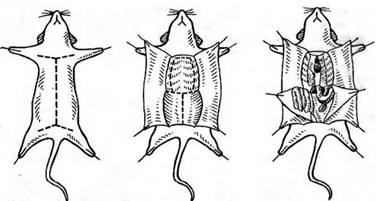
Рисунок
1 - Порядок вскрытия грудной и брюшной полостей
(по Вагнеру)
Шерсть
животного по линии разреза обрабатывают дезинфицирующим раствором. Разрез кожи
делают по белой линии от лонной кости (симфиза) до шеи. Чтобы при этом не
прорезать брюшную стенку, пинцетом, находящимся в левой руке, приподнимают кожу
и делают сначала поперечный надрез складки кожи, удерживаемой пинцетом у
симфиза, а затем, вставив одну браншу ножниц в образовавшееся отверстие,
разрезают кожу до шеи животного, после чего кожу разрезают по направлению к
каждой из четырех конечностей. Лоскуты кожи фиксируют булавками за верхние и
нижние углы. Заменив инструменты, вскрывают брюшную полость. Для этого разрез
брюшной стенки делают под линией диафрагмы и по белой линии до лонной кости.
Треугольники брюшной стенки отводят в стороны и фиксируют. В качестве вируссодержащего
материала из брюшной полости берут кусочки (или целый орган у мелких животных)
печени, селезенки, почки, брыжеечные лимфатические узлы, участок кишечника при
наличии патологоанатомических изменений или симптомов болезни, наблюдавшихся
перед смертью.
Грудную
полость вскрывают с учетом того, что она имеет твердые стенки. Для получения
доступа к находящимся в ней органам с нее надо как бы снять «крышку». Для этого
разрезают ребра поперек сзади вперед, удаляя их вместе с грудной костью.
Пункция
сердца. После выстригания шерсти и дезинфекции места укола животное
наркотизируют и фиксируют животом кверху Пальпаторно определяют место
наилучшего ощущения сердечного толчка и на 4—5 мм краниальнее от этого пункта у
левого края грудины делают прокол Пункцией сердца удается получить до 0,5 мл
крови. Путем декапитации у мыши получают примерно 0,5—0,6 мл крови.
Мазки крови делают на предметных стеклах с
помощью более узкого шлифованного предметного стекла.
Подготовка стекол.
1. С предметных стекол, бывших в
употреблении и соприкасавшихся с иммерсионным маслом, последнее удаляют сухой
тряпкой или бензином. Затем стекла кипятят без мыла и соды в течение 15—20 мин,
промывают чистой водой и погружают на 1 ч в насыщенный раствор двухромовокислого
калия в серной кислоте. Обработанные таким образом стекла промывают в течение
не менее 1 ч под струей водопроводной воды и насухо вытирают чистым
полотенцем.
2. При отсутствии двухромовокислого калия
и серной кислоты стекла, бывшие в употреблении, кладут в мыльный раствор и
выдерживают в нем 8—10 ч, а затем в том же растворе кипятят их 5—10 мин.
После кипячения стекла вынимают и
тщательно промывают под струей водопроводной воды, а затем насухо вытирают.
3. Стекла, не бывшие в употреблении,
промывают в горячей воде и насухо вытирают. Хранят стекла в стеклянной
широкогорлой банке с крышкой.
Приготовление мазков.
Взяв предметное стекло за длинные края,
прикасаются его поверхностью (отступя 0,5—1 см от узкого края) к капле крови
(но не к коже). Предметное стекло держат на столе или в левой руке за узкие
края. Правой рукой приставляют шлифованное стекло узким краем к стеклу с кровью
слева от капли под углом 45° и продвигают его вправо до соприкосновения с
кровью.
Выжидают, пока кровь расплывется по всему
ребру шлифованного стекла, и затем легким быстрым движением ведут его справа
налево до тех пор, пока не будет исчерпана вся капля. Капля крови должна быть
небольшой и соразмерена так, чтобы весь мазок помещался на стекле, не доходя
1—1,5 см до его края. Нельзя прекращать размазывание и отнимать стекло раньше,
чем капля будет исчерпана. Нельзя также сильно нажимать на стекло, так как
многие клетки могут оказаться поврежденными. Хорошо сделанный мазок тонок,
имеет желтоватый цвет и оканчивается «метелочкой».
Густо-розовые и красноватые мазки
непригодны для счета, так как они слишком толсты и клеточные элементы при этом
дифференцировать невозможно. После приготовления мазки быстро сушат на воздухе
до исчезновения влажного блеска. При медленном высыхании может изменяться
морфология клеток.
На высушенном мазке уголком предметного
стекла или карандашом (только не химическим) пишут фамилию, инициалы больного,
дату.
Краску следует готовить на воде
нейтральной реакции.
Окраска мазков. Принцип.
Все предложенные методы окраски мазков
основаны главным образом на химическом сродстве основных частей клеток к
определенным анилиновым краскам и в меньшей степени на их физических свойствах.
Цитоплазма одних клеток, будучи щелочной, имеет сродство к кислым краскам,
выявляя оксифильные элементы крови. Цитоплазма других клеток, содержащих
базофильные и нейтрофильные субстанции, поглощает и кислые, и основные краски.
Ядра, содержащие в значительном количестве нуклеиновую кислоту, связывают
главным образом основные краски.
К основным гематологическим краскам
относятся метиленовый синий и его производные— азур I (метиленазур) и азур II
(смесь равных частей азура I и метиленового синего), к кислым — водорастворимый
желтый эозин.
Азур-эозиновые смеси красок обладают
высокой чувствительностью к реакции воды и поэтому применяемая для
приготовления красителей и для смывания их дистиллированная вода должна иметь
нейтральную реакцию, т. е. рН 7,0. При кислей реакции воды клетки долго не прокрашиваются
и имеют красный оттенок. При щелочной реакции эритроциты окрашиваются в
серовато-синий цвет, а ядра и цитоплазма клеток — в очень темные цвета.
Подсчет
лейкоцитарной формулы проводят с помощью иммерсионной системы микроскопа. В
связи с тем что в мазке различные виды лейкоцитов располагаются неравномерно
(моноциты и нейтрофилы — преимущественно вдоль верхнего и нижнего продольного
края препарата, а лимфоциты — ближе к его центру), подсчет лейкоцитарной формулы
осуществляют, пользуясь следующими методическими указаниями. Под малым
увеличением микроскопа находят край мазка крови вблизи образовавшейся щеточки.
У продольного края мазка наносят каплю иммерсионного масла, после чего
фокусируют плоскость препарата Наблюдая в окуляр, отступают на 2—З поля зрения
по направлению к середине мазка. Затем продолжают продвижение препарата в том
же направлении еще на 3—5 полей зрения, в каждом из них подсчитывая имеющиеся
лейкоциты. Вслед за этим продвигают мазок на З—5 полей зрения вдоль продольного
края, меняя направление продвижения мазка под прямым углом, возвращаются к краю
мазка, продвигая при этом мазок еще на 3—5 полей зрения и так далее.
Зигзагообразную линию, по которой продвигают мазок крови, называют линией
Меандра
___ ___
|___| |___|
Подсчет продолжают до тех пор, пока не
будет сосчитано 50 % клеток. Затем подсчет продолжают на противоположной
стороне мазка. Так же, как описано выше, при продвижении мазка подсчитываюТ все
лейкоциты, обнаруживаемые в поле зрения. Подсчет заканчивают, когда сумма
ейкоцитов будет равна 100. В другом препарате обследуемого подсчитывают еще 100
лейкоцитов. регистрацию ейкоцитов при подсчеТе производят с помощью счетчика
11клавишного СЛ-1, при этом получают общую сумму и количество Каждого вида
лейкоцитов в процентах. При отсутствии счетчика регистрацию производят с
помощью записи на листе бумаги. По вертикали записывают начальные буквы
названий лейкоцитов метамиелоциты (мтмц.), палочкоядерные (п.), сегментоядерные
(с), эозинофильные (э.), базофильные гранулоциты (б.), лимфоциты (лимф.),
моноциты (мсп.), плазматические клетки (пл.).
Процентное содержание различных видов
лейкоцитов не отражает истинного количества их в 1 л крови, поэтому вычисляют
абсолютное содержание лейкоцитов в 1 л крови.для этого необходимо знать
количество лейкоцитон в 1 л крови, процентное содержание
отдельных их видов, подсчитанных в окрашенном препарате.
Таблица 1 - Лейкоцитарная
формула
|
Вид животных
|
Базофилы
|
Эозинофилы
|
Нейтрофилы
Юные
|
Палочкоядерные
|
Сегментоядерные
|
Лимфоциты
|
Моноциты
|
|
Белая мышь
|
0,0-2,0
|
.0,0-4,0
|
-
|
1,0-5,0
|
13,0-30,0
|
60,0-78,0
|
2,0-5,0
|
Таблица 2 - Показатели отлконенй
от нормы различных клеток крови
|
Показатель
|
Увеличение
|
Уменьшение
|
|
Нейтрофилы
|
Нейтрофил
|
|
Эузинофилы
|
(эозинофилия) при аллергии,
умеренно выражен при ожогах, экземе, крапивнице, паразитарных заболеваниях,
лекарственной аллергии.
|
|
|
Базофилы
|
встречается при
миелолейкозе. нервно-мышечном утомлении и голодании животных, при гемофилии,
инъекции под кожу различных сывороток, при гельминтозах
|
при некоторых инфекционных
заболеваниях
|
|
Лимфоциты
|
может возникать при поедании
корма с большим количеством жира, При вирусных инфекциях, Незначительный
лимфоцитоз бывает при заболеваниях нейтрофильно-эозинопенической группы
(пневмония, остеомиелит, сепсис и др.) и указывает на фазу выздоровления.
Увеличение количества лимфоцитов сопутствует туберкулезу, чуме свиней,
инфекционной анемии, инфлюэнце, пироплазмозу, иногда паратифу.
|
часто лимфоцитопения
наблюдается при гнойно-септических и острых, воспалительных процессах,
инфекционных болезнях, интоксикациях, то есть при всех тех состояниях, когда
в лейкоцитарной формуле увеличено число нейтрофилов
|
|
Моноциты
|
(моноцитоз) изучен
недостаточно. Появление или увеличение количества является благоприятным
симпотмом.
|
(моноцитопения) при
тяжелых септических состояниях. При резко выраженной, нейтрофилии иногда
моноциты в крови исчезают, что служит неблагоприятным признаком
|
Осмотическая
резистентность эритроцитов - метод оценки физико-химических
свойств эритроцитов, заключающийся в исследовании стойкости (резистентности) к
различным воздействиям.
Осмотическая
резистентность характеризует устойчивость эритроцитов к гемолизу при добавлении
солевых растворов со снижающейся концентрацией. Чем ниже осмотическая
резистентность эритроцитов, тем раньше происходит гемолиз.
Схема 1
|
Вода, мл
|
Физ.раствор, мл
|
Кровь, мкл
|
|
1 пробирка
|
2,5
|
-
|
10
|
|
2 пробирка
|
-
|
2,5
|
10
|
|
3 пробирка
|
1,25
|
1,25
|
10
|
Центрифугируют содержимое пробирок в
течение 10 минут при 1500 об/мин. Измерения проводят на ФЭКепри условиях: длина
волны 414 нм.
Расчёт:
Н % = 100 * Еоп/ Ек,
Где Н – степень гемолиза
Е оп - коэффициент экстинкции
Е к - оптическая плотность дистиллята
Для получения гомогената
печени выделяли орган из организма животного и помещали в гомогенизатор.
Гомогенизированную массу фильтровали через капроновый фильтр и отмывали
раствором Хенкса. Для приготовления суспензий клеток костного мозга выделяли
трубчатые кости задних конечностей.удаляли эпифизы и вымывали костный мозг
раствором Хенкса. Производили подсчет клеток в камере Горяева для приготовления
суспензии клеток в количестве 1*10-6 кл/мкл.03.04.15.
1.Аланинаминотрансфераза
(АлАТ)
АлАТ - это внутриклеточный
фермент, катализирующий обратимый перенос аминогрупп с аланина (аминокислота)
на α-кетоглутаровую кислоту (кетокислота) с образованием пирувата. Самых
больших концентраций АлАТ достигает в печени, кроме того, в меньших количествах
он содержится в скелетных мышцах, сердце, почках и поджелудочной железе.
Принцип метода: В результате переаминирования между аланином и
α-кетоглутаровой кислотой образуется глутаминовая и пировиноградная
кислоты:
аланин + a-кетоглутарат¬¾АлАТ¾®пируват + L-глутамат
Реактивы:
1. Едкий натр (NaOH):
1 н раствор
2. Субстратно-буферная смесь,
pH=7,4
- Натрий
фосфорнокислый двузамещенный (Na2HPO4): 120 мг
- Калий
фосфорнокислый однозамещенный (KH2PO4): 20 мг
-
α-кетоглутаровая кислота, динатриевая соль: 4 мг
- DL-α-аланин:
178 мг
Вещества растворяют в 1 н
растворе NaOH. Раствор NaOH добавляют осторожно,
небольшими порциями, постоянно перемешивая и измеряя pH.
Раствор доводят дистиллированной водой до объема 10 мл, перемешивают, добавляют
каплю хлороформа и хранят в холодильнике в замороженном виде. Перед
употреблением раствор должен полностью оттаять.
3. Хлорид натрия: 0,85%
раствор
4. Соляная кислота (HCl):
1 н раствор
5. Едкий натр (NaOH):
0,4 н раствор
6. Раствор 2,4-динитрофенилгидрозина:
5 мг растворяют в небольшом количестве (5-10 мл) 1 н раствора соляной кислоты
при нагревании на водяной бане. После того, как раствор остынет, доводят объем HCl
до 25 мл. На следующий день реактив фильтруется. Раствор хранят в посуде из
темного стекла в холодильнике.
7. Стандартный раствор
пировинограднокислого натрия: 11 мг вещества растворяют в небольшом количестве
воды в мерной колбе на 100 мл и доводят до метки дистиллированной водой.
Ход определения:
Определение активности АлАТ
проводят по приведенной ниже схеме 2, параллельно в опытной и контрольной
пробах.
Схема 2
|
Реактивы
|
Опытная проба (мл)
|
Контрольная проба (мл)
|
|
Субстратно-буферная смесь
|
0,5
|
0,5
|
|
Предварительно инкубируют в течение 5 мин при 370С
|
|
Сыворотка крови
|
0,1
|
-
|
|
Инкубируют точно 30 мин при 370С
|
|
Сыворотка крови (или физиологический раствор)
|
-
|
0,1
|
0,5
|
0,5
|
|
Перемешивают и выдерживают 20 мин при комнатной
температуре
|
|
0,4 н раствор NaOH
|
5,0
|
5,0
|
|
Тщательно перемешивают и выдерживают 10 мин при комнатной
температуре
|
Опытную пробу колориметрируют
против контрольной пробы при длине волны 530-540 нм (зеленый светофильтр) в
кюветах с рабочей длиной 10 мм.
2.Аспартатаминотрансфераза(АсАТ
АсАТ – фермент, содержащийся
в большом количестве в миокарде и в ткани скелетной мускулатуры. Подъем
активности чаще всего отражает поражение мышечной ткани.
Принцип метода:АсАТ катализирует реакцию переаминирования между
аспарагиновой и α-кетоглутаровой кислотой с образованием глутаминовой и
шавелевоуксусной (ЩУК) кислот:
аспартат + a-кетоглутарат¬¾АсАТ¾® ЩУК + L-глутамат
Щавелевоуксусная кислота
затем превращается в пировиноградную, которая в щелочной среде реагирует с
2,4-динитрофенилгидрозином с образованием окращенногогидразона пировиноградной
кислоты. Интенсивность окраски зависит от концентрации кислоты.
Реактивы:
1. Субстратно-буферная смесь,
pH=7,4
- Натрий
фосфорнокислый двузамещенный (Na2HPO4): 120 мг
- Калий
фосфорнокислый однозамещенный (KH2PO4): 20 мг
- α-кетоглутаровая
кислота, динатриевая соль: 3 мг
- DL-α-аспарагиновая
кислота: 266 мг
Вещества растворяют в 1 н
растворе NaOH. Раствор NaOH добавляют осторожно,
небольшими порциями, постоянно перемешивая и измеряя pH.
Раствор доводят дистиллированной водой до объема 10 мл, перемешивают, добавляют
каплю хлороформа и хранят в холодильнике в замороженном виде. Перед
употреблением раствор должен полностью оттаять.
2. Все реактивы, которые
необходимы при определении активности АлАТ
Ход определения:
Определение активности АсАТ
проводят по приведенной ниже схеме 3, параллельно в опытной и контрольной
пробах.
Схема 3
|
Реактивы
|
Опытная проба (мл)
|
Контрольная проба (мл)
|
|
Субстратно-буферная смесь
|
0,5
|
0,5
|
|
Предварительно инкубируют в течение 5 мин при 370С
|
|
Сыворотка крови
|
0,1
|
-
|
|
Инкубируют точно 60 мин при 370С
|
|
Сыворотка крови (или физиологический раствор)
|
-
|
0,1
|
|
Раствор 2,4-динитрофенилгидразина
|
0,5
|
0,5
|
|
Перемешивают и выдерживают 20 мин при комнатной
температуре
|
|
0,4 н раствор NaOH
|
5
|
5
|
|
Тщательно перемешивают и выдерживают 10 мин при
комнатной температуре
|
Опытную пробу колориметрируют
против контрольной пробы при длине волны 530-540 нм (зеленый светофильтр) в
кюветах с рабочей длиной 10 мм.
Определение количества
пирувата в пробе, образовавшегося при переаминировании с участием АсАТ,
определяют по калибровочной кривой (см. схему 2). Активность фермента выражают
в мкмоль пировиноградной кислоты, образовавшейся при инкубации 1 мл сыворотки в
течение 60 мин при 370С.
1.
Среднее значения веса и роста 35гр 9,4
см соответственно; Количество ударов сердца 520-780.
2.-3. Изменение
параметров лейкоцитарной формулы:
Таблица 3 – Параметры
лейкоцитарной формулы у мышей не подверженных стрессу
|
№
|
Лимфоциты
|
С/я
нейтрофилы
|
П/я
нейтрофилы
|
Моноциты
|
Базофилы
|
Эозинофилы
|
|
1
|
|
|
|
|
|
|
|
2
|
58
|
35
|
4
|
3
|
-
|
-
|
|
3
|
62
|
30
|
4
|
-
|
-
|
|
4
|
54
|
34
|
7
|
6
|
-
|
-
|
Таблица 4 – Параметры лейкоцитарной
формулы у мышей подверженных стрессу
|
№
|
Лимфоциты
|
С/я
нейтрофилы
|
П/я
нейтрофилы
|
Моноциты
|
Базофилы
|
Эозинофилы
|
|
1
|
64
|
17
|
13
|
4
|
1
|
1
|
|
2
|
37
|
49
|
6
|
8
|
-
|
-
|
|
3
|
50
|
37
|
6
|
7
|
-
|
-
|
По выше представленным данным в таблицах 3
и 4
4. Осмотическая резистентность у группы
контроля и у мышей подверженных стрессу.
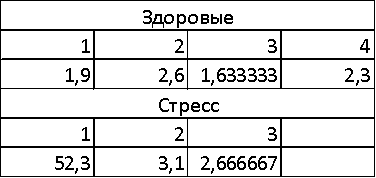
6. Определение активности АЛТ и АСТ

В результате вышеприведённых данных можем
сделать следующие выводы:
Стресс, вызванный
воздействием физических факторов: – стресс «принудительного плавания» (в
раковине длиной 50 см, шириной 30 см и глубинной 50 см с уровнем воды 15 см и
t 20°С в течение 20 минут) –
1. При сравнении
лейкоцитарной формулы контрольной и опытных групп, данные существенно
отличились друг от друга. Это связанно с тем, что во время стресса в кровь
выбрасывается гормон адреналин. Известно, что под влиянием адреналина возникает
лейкоцитоз. При истощении симпатического отдела ЦНС преобладает тормозной процесс
и наблюдается лейкопения. Это вероятно обусловлено истощением сосудистого и
костномозгового гранулоцитарных резервов. Выработка положительных условных
рефлексов уменьшает содержание гемоглобина. При стрессе происходит
перераспределения лимфоцитов между лимфоидными органами, циркулирующей кровью и
костным мозгом. При остром или несильном хроническом стрессе происходит
увеличение палочкоядерных нейтрофилов и некоторое ускорение созревания
сегментоядерных нейтрофилов. Развитие нейтрофильного лейкоцитоза связано
главным образом с увеличенным поступлением в циркуляцию костномозговых
нейтрофилов, рекрутирование которых потенцируется глюкокортикоидами и
катехоламинами.
2.Осмотическая резистентность
эритроцитов более выражена у группы опытных мышей.При остром стрессе, наряду с
эритроцитозом, снижением концентрации аскорбиновой кислоты в надпочечниках и
возрастанием концентрации оксикортикостероидов в плазме крови, наблюдается:
появление в периферическом русле популяции повышенно- и особостойких к
кислотному гемолизу эритроцитов, снижение осмотической устойчивости
эритроцитов, планоцитоз и микроцитоз, ацидемия и накопление калия и магния в
плазме крови, снижение объема плазмы, приходящейся на один эритроцит. Указанные
изменения отражают неспецифическое (стрессорное) действие изученных агентов.
3. Со стороны биохимических
показателей, характеризующих функцию печени (активность АСТ, АЛТ) существенных
изменений не обнаружено.
1. Оценили средний рост и вес экспериментальных
животных;
2. Изучили изменение параметров лейкоцитарной формулы;
3. Выделили клетки костного мозга из бедерной кости;
4. Изучили активность в плазме мышей группы
контроля и группы мышей подверженных стрессу;
5. Изучили осмотическую резистентность у группы
контроля и у мышей подверженных стрессу.
1. Микроскопическая техника: Техника вскрытия лабораторных
животных [Электронный ресурс] Точка доступа - http://labx.narod.ru/documents/technology_mortem_autopsy_lab_animals.html
(Дата обращения 07.04.2015)
2. Приготовление мазка крови для исследования [Электронный
ресурс] Точка доступа -
http://handcent.ru/patologiya/1297-prigotovlenie-mazka-krovi-dlya-issledovaniya-chast-1.html
(Дата обращения 07.04.2015)
3. Подсчет лейкоцитарной формулы крови[Электронный ресурс]
Точка доступа - http://laboratories.com.ua/20100213474/podschet-leykotsitarnoy-formuly-krovi.html
(Дата обращения 07.04.2015)
4. медицинская карта: Определение активности аминотрансфераз
(АЛТ, АСТ) [Электронный ресурс] Точка доступа - http://medkarta.com/?cat=article&id=19849(Дата
обращения 07.04.2015)