Цитопротекторы в терапии заболеваний желудка. Оптимальный подход к выбору препарата
Цитопротекторы в терапии заболеваний желудка.
Оптимальный подход к выбору препарата
Яковенко
А.В., Григорьев П.Я., Яковенко Э.П., Агафонова Н.А., Прянишникова А.С.,
Иванов
А.Н., Алдиярова М.А., Солуянова И.П., Анашкин В.А., Оприщенко И.В.
Российский
государственный медицинский университет, Москва.
Слизистая
оболочка желудка (СОЖ) постоянно подвергается воздействию экзогенных и
эндогенных агрессивных субстанций, в связи с чем она обладает целым рядом
взаимосвязанных цитопротективных механизмов, предупреждающих ее повреждение [5,
7]. Агрессивные факторы подразделяются на экзогенные и эндогенные, а также на
внутрипросветные и гематогенные. К основным внутрипросветным эндогенным
повреждающим субстанциям, с которыми СОЖ контактирует постоянно, относятся
соляная кислота, пепсин и забрасываемые в желудок желчь и панкреатические
ферменты. Экзогенные внутрипросветные факторы поступают в желудок периодически,
в различных сочетаниях и количествах. К ним относятся бактерии, в первую
очередь Helicobacter pylori (HP), вирусы, этанол, лекарственные препараты
(НПВП, кортикостероиды, цитостатики и др.), пищевые компоненты (специи), а
также термические характеристики принимаемых продуктов.
К
гематогенным эндогенным повреждающим факторам относятся провоспалительные и
вазоактивные медиаторы, продукты нарушенных метаболических процессов в
организме (мочевина, мочевая кислота и др.), а также ряд экзогенных
повреждающих субстанций: вирусы, бактерии и их токсины, лекарства, химические
субстанции, соли тяжелых металлов и др., поступающие в организм, минуя
желудочно-кишечный тракт. Под влиянием экзогенных и эндогенных ксенобиотиков в
СОЖ нарушаются метаболические процессы, что приводит к появлению новых биологических
субстратов, оказывающих тканевой деструктивный эффект.
Основными
механизмами действия повреждающих СОЖ агентов являются [1, 7]:
1)
падение трансмембранного потенциала поверхностного эпителия, способствующего
обратной диффузии водородных ионов в СОЖ;
2)
деградация пристеночной слизи и повреждение поверхностного эпителия СОЖ;
3)
индукция синтеза провоспалительных субстанций в СОЖ;
4)
блокада продукции противовоспалительных тканевых простагландинов и АТФ;
5)
активация тканевых фосфолипаз;
6)
активация перекисного окисления липидов в эпителии СОЖ;
7)
нарушение кровотока и сосудистой проницаемости в СОЖ.
При
этом механизмы повреждения СОЖ при воздействии различных факторов агрессии
нередко суммируются и в то же время имеют определенные различия (табл. 1).
Таблица
1. Факторы, повреждающие СОЖ, и ведущие механизмы их действия
|
Механизмы действия
|
Основные повреждающие факторы
|
|
H+
|
HПВП
|
желчные
кислоты
|
этанол
|
HP
|
пепсин
|
|
Падение трансмембранного потенциала, обратная диффузия H+
|
+
|
+
|
+
|
+
|
+
|
-
|
|
Прямое повреждение эпителия СОЖ
|
+
|
+
|
+
|
+
|
+
|
+
|
|
Индукция синтеза провоспалительных субстанций
|
-
|
-
|
-
|
+
|
+
|
-
|
|
Снижение синтеза тканевых простагландинов, АТФ
|
-
|
+
|
-
|
-
|
+
|
-
|
|
Активация тканевых фосфолипаз
|
-
|
-
|
-
|
+
|
+
|
-
|
|
Активация перекисного окисления липидов
|
-
|
+
|
-
|
+
|
+
|
-
|
|
Нарушение сосудистой проницаемости
|
-
|
+
|
-
|
+
|
+
|
|
Снижение кровотока СОЖ
|
-
|
+
|
-
|
-
|
+
|
-
|
|
Деградация защитной слизи
|
-
|
+
|
+
|
+
|
+
|
+
|
|
Повреждение поверхностного эпителия СОЖ
|
+
|
+
|
+
|
+
|
+
|
+
|
|
Нарушение процессов регенерации эпителия СОЖ
|
+
|
+
|
+
|
+
|
+
|
-
|
Желудочная
цитопротекция включает большой спектр внутрипросветных и тканевых механизмов,
взаимодействие которых обеспечивает целостность СОЖ и ее устойчивость к
факторам агрессии. Протективные механизмы СОЖ находятся в тесном взаимодействии
и регулируются нервными и гуморальными механизмами с участием нейропептидов и
вазоактивных медиаторов [5].
Слизистый
протективный барьер желудка имеет три линии защиты [3]. Первая линия включает
слизь, желудочную и дуоденальную секрецию бикарбонатов, гидрофобную поверхность
СОЖ и двенадцатиперстной кишки. Слизь представляет собой водонерастворимый
гель, состоящий из гликопротеиновых полимеров, тесно прилегающих к поверхности
эпителиальных клеток. В состав ее входят IgA, лизоцим, лактоферрин и другие
компоненты. Слой слизи защищает СОЖ от физических и химических воздействий, от
действия соляной кислоты и пепсина, бактерий, вирусов и их токсинов. Секреция
бикарбонатов уменьшает агрессивные свойства соляной кислоты и повышает уровень
рН защитного слоя слизи.
Вторую
линию защиты СОЖ составляет эпителиальный барьер. Апикальные поверхности
покровного желудочного эпителия и межклеточные соединения чрезвычайно устойчивы
к обратной диффузии H+ благодаря наличию на их базолатеральных поверхностях
двух транспортных систем, удаляющих водородные ионы из СОЖ. Целостность данного
барьера регулируется эндогенными факторами роста, одним из которых является
трансформирующий фактор роста - a. Данный барьер нарушается в первую очередь
при развитии воспалительного процесса в СОЖ, ассоциированного с персистенцией
HP. В состав данного барьера входят тканевые субстанции, содержащие
сульфгидрильные группы (глютатион- и тиолсодержащие протеины), которые являются
мощными естественными антиоксидантами, а также ловушками для свободных
радикалов водорода и кислорода, включая и экзогенные, поступающие со слюной и
пищей. Определенная роль в поддержании второй линии защиты принадлежит
компонентам врожденного и адаптационного иммунитета (Toll-подобные рецепторы,
антибактериальные пептиды, a- и b-дефенсины, IgA и др.), которые обеспечивают устойчивость
СОЖ к внедрению патогенных бактерий, вирусов и их токсинов [5].
Третья
линия защиты включает нормальный кровоток, который способствует удалению H+,
обеспечивает энергией метаболические процессы, поддерживает первую и вторую
линии защиты, а также репаративные процессы в СОЖ. Схема функционирования
протективных и репаративных механизмов СОЖ представлена на рис. 1.
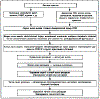
Рис.
1 Защитные и репаративные механизмы слизистой оболочки желудка
Для
восстановления защитных свойств СОЖ используются цитопротекторы. Последние
включают группы лекарственных средств с различными механизмами действия,
которые стабилизируют защитные свойства слизи за счет снижения факторов
агрессии и/или повышения факторов защиты; способствуют заживлению эрозий и язв;
восстанавливают структуру и функцию эпителия желудочно-кишечного тракта.
Основными
цитопротекторами, которые используются в клинической практике, являются
препараты висмута (висмута трикалия дицитрат - де-нол), сукральфат,
мизопростол, пентоксифиллин [4]. Кроме того, опосредованным цитопротективным
эффектом обладают также препараты, снижающие кислотную продукцию (ингибиторы
протонной помпы, блокаторы H2-рецепторов гистамина), алюминийсодержащие
антациды, донаторы сульфгидрильных групп (s-адеметионин, барбитураты, тиопентал
и др.), а также восстанавливающие тканевой кровоток.
Механизмы
действия основных цитопротекторов представлены в табл. 2 [2, 6, 7].
Таблица
2. Механизмы действия цитопротекторов СОЖ
|
Механизм действия
|
Препараты
|
|
де-нол
|
сукральфат
|
мизопростол
|
пентокси-
филлин
|
|
Повышение синтеза слизи и бикарбонатов
|
+
|
-
|
-
|
-
|
|
Повышение синтеза простагландинов
|
+
|
+
|
+
|
-
|
|
Антиоксидантный эффект
|
+
|
+
|
-
|
-
|
|
Снижение содержания провоспалительных цитокинов
|
+
|
+
|
-
|
+
|
|
Снижение активности пепсина
|
+
|
-
|
-
|
|
Связывание желчных кислот
|
±
|
+
|
-
|
-
|
|
Связывание с белками в зоне воспаления и некроза
|
+
|
+
|
-
|
-
|
|
Улучшение микроциркуляции в слизистой оболочке
|
+
|
-
|
+
|
+
|
|
Повышение содержания эпидермального фактора роста
|
+
|
-
|
-
|
-
|
|
Ингибирование NO синтетазы и адгезии бактерий
|
+
|
-
|
-
|
-
|
Анализ
представленных в табл. 2 данных показал, что препараты висмута обладают
наиболее широким спектром механизмов цитопротекции. Так, назначение де-нола
приводит к снижению продукции и активности пепсина. Препарат селективно
связывается с белками дна язвы и создает защитный слой - барьер для диффузии
H+, препятствующий повреждению области СОЖ, лишенной защитного эпителиального
покрова. Де-нол стимулирует локальный синтез простагландинов в СОЖ, увеличивает
секрецию слизи и гидрокарбонатов; усиливает кровоток в СОЖ, подавляет продукцию
цитокинов клетками воспалительного инфильтрата; обеспечивает реконструкцию
экстрацеллюлярного матрикса и полноценный ангиогенез, а также усиливает
репаративный эффект, опосредованный эпидермальным фактором роста [2, 4].
Основными
показаниями к назначению цитопротекторов являются заболевания желудка,
сопровождающиеся структурными нарушениями СОЖ (язвенная болезнь, гастриты,
мукозиты и др.). В ряде случаев данные препараты назначаются также для
профилактики повреждения СОЖ (при приеме ульцерогенных средств, стрессовых
состояниях и др.). Выбор цитопротектора и схемы его назначения зависят от
этиологии и ведущих звеньев патогенеза патологического процесса в желудке.
Ориентировочный подход к выбору препарата - цитопротектора - представлен в
табл. 3.
Таблица
3
|
Заболевания ЖКТ
|
Препарат выбора
|
|
де-нол
|
сукральфат
|
мизопростол
|
пентокси-
филлин
|
|
Язвенная болезнь, ассоциированная с НР
|
+
|
-
|
-
|
±
|
|
Хронический гастрит, ассоциированный с НР
|
+
|
-
|
-
|
±
|
|
Гастропатии, обусловленные приемом:
|
-
|
-
|
-
|
-
|
|
НПВП
|
+
|
-
|
+
|
-
|
|
алкоголя
|
+
|
+
|
-
|
+
|
|
цитостатиков
|
-
|
+
|
-
|
+
|
|
Стрессовые язвы
|
+
|
+
|
+
|
|
Рефлюкс-гастрит
|
-
|
+
|
-
|
-
|
|
Мукозиты, связанные с приемом цитостатиков
|
+
|
±
|
-
|
±
|
|
Инфекционная диарея
|
+
|
-
|
-
|
-
|
Как
следует из приведенных в табл. 3 данных, де-нол является универсальным
цитопротектором, который может быть использован практически при всех
этиопатогенетических вариантах воспалительно-деструктивных поражений слизистой
оболочки пищеварительного тракта [2].
Общепринятые
схемы терапии цитопротекторами:
1.
препараты висмута (висмута трикалия дицитрат - де-нол), 120 мг 4 раза в день,
2-4 недели;
2.
сукральфат, 1,0 г 4 раза в день, 2-4 нед;
3.
мизопростол, 200 мкг 4 раза в день, 4-8 нед;
4.
пентоксифиллин, 400 мг 3 раза в день, 4 нед.
Цитопротекторы
могут включаться в схемы лечения основного заболевания, а в ряде случаев -
назначаться в виде монотерапии. При их рациональном использовании существенно
повышается эффективность лечения заболеваний желудочно-кишечного тракта.
Список литературы
1.
Hunt, R.Н. Hellcobacter pylori. Basic
mechanisms to clinical сиге 2000 / R.Н. Hunt, G.N.J. Tytgat. - Kluwer Academic Publishers, 2000. - 689 р.
2. Lambert, J.R., Pharmacology of colloidal bismuth subcitrate
(De-Nol) and use in non - ulcer dyspepsia / JR Lambert, McLean // Hellcobacter
pylori in peptic ulceration and gastritis; eds. В.J.
Marshall, R.W. МсCallum, R.L. Guerrant. - Oxfotd,
London, Edinburgh, Melbourne: Blackwell Scientific Publications, 1991. P.
201-209.
3. Powell D.W. Physiological concepts of epithelial barriers / D.W.
Powell // Ed. А. Allen.
4. Mechanisms of mucosal protection in the upper gastrointestinal
tract. - New York: Raven Press, 1984. P. 1-6.
5. Prichard P. Drags for the GUT / P. Prichard, R. Walt, R. Chapman
// А practical guide to gastrointestinal and liver
therapy. - London, Philadelphia, Toronto, Sydney; WB Saunders company limited,
1998. - 443 р.
6. Rose, S. Gastrointestinal and Hepatobiliary patnophysiology / S.
Rose. - Madison; Fence Greek Publishing LLC, 1998. - 475 р.
7. Tarnawski F. Cellular and molecular mechanisms of ulcer healing.
Is quality of mucosal scar affected by treatment? / F. Tarnawski, К. Таnue, А.М. Santos et al // Scand. J. GastroenteroL 1995. Suppl. 210. Vol. 9.
8. Whittle, BJR. Protective mechanisms of the gastric mucosa / В.J.R. Whittle // The stomach; eds. S. Gustavsson, D. Кumar, D.Y. Graham. - Edinburgh, London, Madrid: Churchill
Livingstone, 1992. P. 81-101.
Для
подготовки данной работы были использованы материалы с сайта http://www.medlinks.ru/