Хемилюминесцентный анализ и его клиническое значение
Хемилюминесцентный
анализ и его клиническое значение
Введение
Как правило,
энергично протекающие химические реакции сопровождаются выделением энергии в
форме тепла. Существуют, однако, реакции, например, с участием перекисей, при
которых энергия выделяется в виде света: это явление носит название
хемилюминисценции. Процессы жизнедеятельности сопровождаются сверхслабым
излучением (собственная хемилюминисценция клеток и тканей), обусловленным в
основном реакциями с участием свободных радикалов. Некоторые организмы обладают
способностью излучать свет, видимый невооруженным глазом, что называется
биолюминесценцией. Она характерна для некоторых грибов, микроорганизмов,
беспозвоночных. Впервые явление хемилюминесценции было обнаружено в середине XX
века итальянскими астрономами Л. Колли и У. Фаччини в виде свечение
непигментированных тканей растений.
Весь механизм химической реакции, сопровождающейся хемилюминесценцией,
можно отразить в трех последовательных стадиях:
. Электрон отсоединяется от одного из участников реакции
(восстановителя) и присоединяется к другому (окислителю), что приводит к
запасанию в системе химической энергии, которая позже выделится в форме
лучистой.
. Перенос электрона на один из более высоких энергетических
уровней, то есть переход продукта реакции в возбужденное состояние.
. Переход продукта в основное состояние, сопровождающееся
выделением энергии в виде кванта света (происходит собственно явление
люминесценции).
Свечением также сопровождается образование свободных радикалов при
воздействии на вещество некоторых физических факторов: ионизирующего излучения
(радиохемилюминесценция), ультрафиолетового и видимого света
(фотохемилюминесценция), электрического тока (электролюминесценция),
ультразвука (сонолюминесценция), трения (триболюминесценция).
А.Г. Гурвич и его последователи (С. Родионов, Г.М. Франк, Р. Одюбер, А.
Стреллер) разработали последовательно биологический, физический газозарядный
детекторы и ФЭУ, служившие для изучения собственного слабого свечения клеток
животных и растений, названного Гурвичем митогенетическими лучами. Было
установлено, что собственное свечение тканей обуславливается реакциями активных
форм кислорода, реакциями цепного (перекисного) окисления липидов и реакциями с
участием окиси азота. Из них особое значение для лабораторных исследований в
медицине имеют реакции с участием активных форм кислорода, так как в 1971г. Р.
Элланом была открыта собственная хемилюминисценция активированных фагоцитов,
связанная с использованием ими активных форм кислорода в борьбе с антигенами.
1.Принцип метода
Низкая интенсивность собственной хемилюминесценции не позволяет напрямую
использовать ее в аналитических целях, потому используется метод активированной
хемилюминесценции.
Активаторы хемилюминесценции разделяются на физические и химические.
Химические активаторы - это соединения, вступающие в реакцию с активными
формами кислорода или свободными радикалами, выделяющимися в ходе основного
процесса, с образованием продукта в возбужденном электронном состоянии, при переходе
которого в основное происходит высвечивание фотонов. Широко используются такие
активаторы как люминол (3-аминофталевый гидразид) и люцигенин (бис-N-метилкридиний). Физические
активаторы не влияют на ход исследуемой реакции, но усиливают интенсивность хемилюминесценции
в 3-4 раза. К физическим активаторам относятся некоторые люминесцирующие
соединения, применяемые при цепном окислении липидов - хлорофилл а, родамин Ж,
хинолизин-кумарины, бактериофеофитин, Tb+ и пр. [1]
Существует новый метод проведения хемилюминесцентного анализа,
предусматривающий последовательную двухстадийную стимуляцию различными
химическими активаторами, что дополнительно повышает интенсивность свечения и
позволяет использовать меньшее количество исследуемого материала для получения
объективно регистрируемых результатов. [7]
Изучение хемилюминесценции биологических объектов показывает ее связь со
свободнорадикальным окислением в организме, протекающим без участия ферментов
за счет восстановления молекулярного кислорода до его активных форм:
супероксидного анион-радикала, гидроксильного радикала, синглентного кислорода.
Основным источником этих соединений является аутоокисление липидов, главным
образом ненасыщенных жирных кислот, при котором выделяется свободные радикалы,
взаимодействующие с кислородом с образованием пероксидов. При рекомбинации этих
пероксидов происходит выделение квантов света. Другими источниками
хемилюминесценции в свободнорадикальном окислении могут быть возбужденные
молекулы димеров кислорода, кетонов, циклических гидроперекисей, оксалатов и
альдегидов, биогенных аминов. Также эмиссия фотонов наблюдается при распаде
перекисей (промежуточных продуктов реакций с молекулярным кислородом).
Ингибируется свободнорадикальное окисление в организме за счет природных антиоксидантов,
разделяющихся на антиоксиданты гидрофобный (токоферолы, флавины, каротиноиды,
стероиды) и гидрофильной (сульфгидрильные соединения SH- группы белков, аскорбиновая кислота) фаз. Таким образом,
хемилюминесцентная активность может говорить об избыточном свободнорадикальном
окислении в организме, недостатке или низкой активности антиоксидантов, что
свидетельствует, например, о гиповитаминозных состояниях (некоторые витамины,
такие как D и C, являются сильными антиоксидантами).
Другим важным направлением клинического применения хемилюминесценции
является оценка активности иммунокомпетентных клеток.
Хемилюминесцентный анализ применяется для обнаружения катализаторов,
разлагающих пероксид водорода с образованием свободных радикалов (например,
обнаружение гемсодержащего соединения - миоглобина в моче после инфаркта,
оценка скорости заживления ран по экссудату), определения содержания
гемоглобина в крови, исследование защитных механизмов крови (обнаружение
фагоцитов и оценка их активности), диагностики небактериальной аллергии (оценка
активности эозинофилов, контролирующих воспалительные реакции).
Хемилюминесценсция клеток крови наблюдается при действии кратковременных
электрических импульсов, стимулирующих выделение активных форм кислорода и
увеличение проницаемости клеточных мембран, при добавлении к лейкоцитам
суспензии бактерий, оболочек дрожжевых клеток, кристаллов кварца и сульфата
бария и др. корпускулярных антигенов, получивших название стимулов.
Стимулированная ХЛ в присутствии активатора - показатель функционального
состояния фагоцитов крови. Активность фагоцитов возрастает при наличии в
организме очагов воспаления и снижается при длительном недостатке кислорода,
связанном с общим ослаблением организма. Повышение спонтанной и индуцированной
хемилюминесцентной активности фагоцитов наблюдается у больных с бактериальной
инфекцией, опухолями, снижение - при артритах, диабете, иммунодефицитных
состояниях, в т.ч. врожденной недостаточности системы комплемента.
Помимо фагоцитов, неиндуцированной (собственной) хемилюминесцентной
активностью обладают клетки тимуса и лимфоциты. Механизмы хемилюминесценции
лимфоцитов те же, что у фагоцитов, однако из-за более низкой активности
ферментов оксидаз и оксигеназ интенсивность их свечения значительно меньше. Для
инициирования свечения используются антииммуноглобулины и митогены, параметры
свечения различаются в зависимости от функционального состояния лимфоцитов и
потому позволяют оценивать их метаболическую активность и устойчивость к
повреждениям.
Индуцированная хемилюминесценция сыворотки крови, по мнению большинства
исследователей, является наиболее чувствительным и объективным методом изучения
процесса перекисного окисления липидов. Реакции цепного окисления отличаются
большой сложностью и включают в себя целый ряд быстропротекающих стадий.
Основные участники реакций, свободные радикалы, обычными методами химического
анализа определены быть не могут из-за своей крайне высокой реакционной
способности и неустойчивости в биохимических системах. Поэтому регистрация
интенсивности свечения в режиме реального времени представляет собой ценную
информацию для анализа механизма реакций перекисного окисления липидов. [4]
Также хемилюминесцентные реакции можно использовать в иммунологических
исследованиях для получения сигнала в модифицированном ИФА, при этом повышается
чувствительность метода и сокращается время проведения анализа. В качестве
метки в ИФА широко применяют пероксидазу хрена, для выявления которой
используются такие реакции. В прямом анализе, когда метка ставится на антиген,
при ферментативной реакции образуется перекись водорода и окисляет люминол,
катализатором этой реакции выступает пероксидаза хрена. Для усиления сигнала
используются различные соединения, например, люциферин, фенолы, в этом случае
интенсивность люминесценции усиливается в 10-100 раз, в отдельных вариантах в
500 раз (усиленный хемилюминесцентный анализ). Люминесцентный сигнал очень
стабилен, его уровень достигает максимума за 30 с (для сравнения: цветная
реакция с ОФД в качестве индикатора полностью развивается лишь за 30 мин). При
непрямом анализе люминолом или его производными метится антитело. Такая метка в
свободном состоянии способна окисляться перекисью водорода с выделением света.
Если она образовала комплекс, то теряет способность окисляться.
Хемилюминесцентный анализ используют для измерения содержания АТФ, и
АТФ-азы, креатинкиназы, аденилатциклазы, фосфодиэстеразы, миелопероксидазы,
протеолитических ферментов, ферментов монооксигеназной системы печени и др.
Материалом могут выступать клеточные элементы крови (нейтрофилы, эозинофилы,
лимфоциты, моноциты), плазма и сыворотка крови, моча больного.
Материалом для исследования являются:
) Разведенная цельная кровь (оптимальное разведение - 1:22);
) Выделенные фракции клеток.
Другими вариантами разведения крови, по разным авторам, являются 1:9,
1:21, 1:40, 1:100, 1:200, однако рост интенсивности свечения наблюдается до
разведения 1:22 в связи со снижением оптической плотности раствора, а при
дальнейшем разведении снижается за счет понижения концентрации фагоцитирующих
клеток в нем. Недостаток использования цельной крови - антиоксидазная
активность плазмы, искажающая результаты исследования.
Получение изолированной фракции клеток может производиться путем
осаждения или центрифугирования (на примере нейтрофильных гранулоцитов):
А) к 5 мл крови из локтевой вены с гепарином добавляют 1 мл полиглюкина.
Смесь инкубируют в течение 30 мин при 37°С для ускорения осаждения эритроцитов.
Полученный лейкоцитарный супернатант дважды отмывают в растворе Хенкса без
фенолового красного по 10 мин при 400 g. Супернатант сливают, оставшиеся
нейтрофильные гранулоциты разводят в 1 мл раствора Хенкса и получают взвесь.
Подсчитывают количество нейтрофильных гранулоцитов в камере Горяева.
Б) 2 мл крови из локтевой вены в центрифужные пробирки, хорошо
перемешивают с 80 ЕД гепарина и 1 мл полиглюкина, инкубируют смесь 25 минут при
37°C и 30 минут при комнатной температуре, после чего переносят лейкоцитарный
супернатант в чистые центрифужные пробирки и трижды отмывают в растворе Хенкса
без фенолового красного по 5 минут при 1500 об/мин. По окончании третьего
центрифугирования супернатант удаляют, а оставшиеся клетки разводят в 2 мл
раствора Хенкса. Подсчет лейкоцитов осуществляют в камере Горяева: к 20 мкл лейкоцитарной
взвеси добавляют 200 мкл 10% раствора уксусной кислоты с 0,25% раствором
трипанового синего. После подсчета клетки доводят раствором Хенкса до
концентрации 2*106 /мл.
Наиболее простым способом проведения исследования является регистрация
неиндуцированной, собственной хемилюминесценции клеток крови, т.е. без
использования каких-либо активаторов процесса, однако наблюдаемое при этом
свечение имеет очень слабую интенсивность, вследствие чего необходимо
нахождение большого количества исследуемых клеток в пробе.
хемилюминесцентный клинический клетка
Таблица1 . Индукторы клеточной хемилюминесценции
|
Физические
|
УФ
|
|
Лазерное излучение
|
|
Электропорация
|
|
Химические
|
Агонисты рецепторов
|
ФМЛФ
|
|
|
анти-CD36
|
|
|
Зимозан А
|
|
Ca2+ ионофор
|
|
|
Иономицин
|
|
Активаторы ПКС
|
ФМА
|
|
|
ТФА
|
|
Корпускулярные
|
Частицы латекса
|
|
Микроорганизмы
|
Escherichia coli
|
|
|
Candida albicans
|
Широко применяется использование химического активатора хемилюминесценции
- люминола.

Рис.1 - Схема выделения кванта света при воздействии люминола
Для регистрации интенсивности хемилюминесценции используется прибор
хемилюминометр. Помимо оценки функциональной активности клеток он может
применяться в следующих областях:
· Изучение процессов свободно-радикального окисления.
· Оценка состояния прооксидантных и антиоксидантных систем
человека и животных.
· Определение антиоксидантной активности фармакологических
препаратов, биологических жидкостей, косметологических средств и пищевых
добавок.
· Выявление наличия и определение следовых концентраций
различных веществ.
· Контроль микробиологической чистоты различных объектов
(продуктов питания, воды, воздуха, технологических поверхностей, помещений).
· Контроль токсичности проб воды, воздушной среды, почвы, а
также различных соединений и материалов.
В измерительные кюветы вносятся реакционные смеси, включающие в себя
суспензию исследуемых клеток, донорскую сыворотку (группа AB, резус-отрицательная), люминол (или другой
активатор хемилюминесценции) и раствор Хенкса.
ИБА = Sиндуцир. : Sспонт.
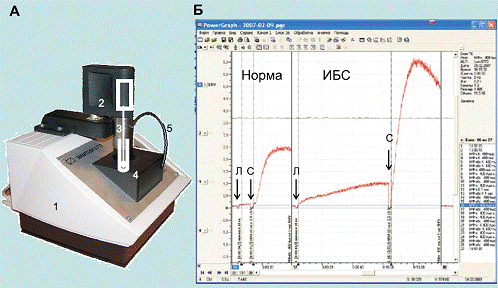
Рис.2 - прибор для ХЛ и регистрация результатов: А - хемилюминометр: 1-
корпус, 2 - электромотор, 3- мешалка, 4- кювета, 5- светоизолированная трубка
для добавления растворов по ходу измерения. Б - пример записи кривых
хемилюминесценции (слева - моноциты здорового донора, справа - моноциты
больного ишемической болезнью сердца): Л - момент добавления люминола, С -
момент стимула ФМА. [2]
.Учет и интерпритация результатов
Регистрируемые хемилюминометром данные выносятся на экран компьютера в
виде кривых хемилюминесценции. При исследовании спонтанной хемилюминесценции
(т.е. метаболической активности клеток крови) учитываются данные по одной
кривой. Полученные значения будут различаться у здоровых людей и лиц с
патологиями.
Повышение хемилюминесценции сыворотки и плазмы крови обуславливается
активацией иммунокомпетентных клеток, накоплении в крови кислородных радикалов
и гидроперекисей при усиленном окислении липидов, снижением уровня
антиоксидантов; отмечается при воспалениях, язвенной болезни, ревматизме,
гиповитаминозах, ранних стадиях атеросклероза, в стрессовых ситуациях.
Понижение хемилюминесценции крови объясняется большинством исследователей
следствием нарушения проницаемости клеточных мембран и выходом в кровь
низкомолекулярных пептидов, угнетающих хемилюминесценцию; отмечается при
ишемии, гипоксии, злокачественных новообразованиях, гипервитаминозе Е,
хронических бронхитах.
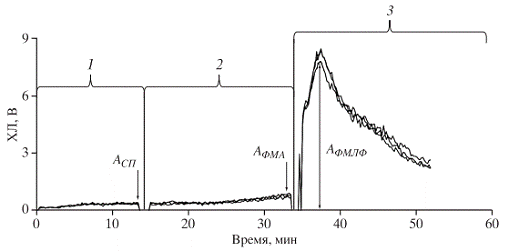
Рис.3 - Типичная хемилюминограмма крови здорового человека при
двухстадийной стимуляции: 1 - спонтанная ХЛ; 2 - предстимуляция ФМА (4β-форбол-12-миристат-13-ацетат); 3-
стимул фМЛФ (N-формил-метионил-лейцил-фенилаланин); А - амплитуды ответа
Индекс бактериальной активности повышается при воспалительных процессах:
у здоровых лиц, согласно результатам исследований, ИБА не превышает 1,47, у
больных в 92% случаев ИБА выше 1,47 и может превышать 6. [9]
Хемилюминесцентный анализ мочи больного позволяет диагностировать ранние
стадии почечной недостаточности, воспаления почек и гипоксические состояния:
повышение ХЛ отмечается при гипоксии, нефрите, пиелонефрите, гломерулонефрите;
снижение - почечной недостаточности, заболеваниях, сопровождающихся нарушением
выделительной и концентрационной функций почек.
Заключение
Хемилюминесценция со времен своего открытия превратилась в явление,
нашедшее широкое применение в клинической практике: фармакологии (исследование
биологически активных соединений, оценка эффективности действия антиоксидантов
и подбор препаратов), лабораторной диагностике (выявление скрытых патологий и
ранняя диагностика заболеваний, оценка активности патологического процесса,
оценка функционального состояния печени и почек, определение воспалительных
процессов), токсикологии и медицине катастроф (оценка тяжести состояния при
ожогах, травмах и отравлениях, контроль за лечением), реаниматологии и хирургии
(оценка тяжести состояния больных, оценка эффективности гемодиализа и
плазмофереза, изучение действия и подбор анестетиков), акушерстве и
неонатологии (ранняя диагностика токсикозов и внутриутробной инфицированности,
наблюдение за беременными, развитием плода и новорожденного), кардиологии
(выявление предрасположенности и ранняя диагностика сердечно-сосудистых
заболеваний), трансплантологии (оценка жизнеспособности трансплантатов, раннее
определение реакций отторжения трансплантатов), иммунологии и аллергологии
(оценка иммунного статуса, диагностика иммунодефицитных состояний и
аутоиммунных болезней, выявлений алллергенов), нефрологии (оценка
функционального состояния почек, эффективности гемодиализа), гематологии
(оценка функциональной активности клеток крови), судебной медицине (определение
времени смерти, выявление употребления наркотических и токсических веществ).
Список литературы
. Владимиров,
Ю.А. Активированная хемилюминесценция и биолюминесценция как инструмент в
медико-биологических исследованиях / Ю.А. Владимиров // Соровский
образовательный журнал. - 2001. - Т.7, №1 - с.16-23
. Владимиров,
Ю.А. Свободные радикалы и клеточная хемилюминесценция / Ю.А. Владимиров, Е.В. Проскурина
// Успехи биологической химии. - 2009. - Т.49 - с.341-388
. Камышников,
В.С. Справочник по клинико-биохимическим исследованиям и лабораторной
диагностике / В.С. Камышников - М.: МЕДпресс-информ, 2004.
. Клинические
аспекты применения хемилюминесцентного анализа / Ю.С. Винник, А.А. Савченко,
О.В. Теплякова и др. // Сибирский медицинский журнал. - 2004. - Т.46, №5. -
С.11-16.
. Образцов,
И.В. Хемилюминесцентный анализ клеток крови в медицине: история, теория,
практика / И.В. Образцов, М.А. Годков // Молекулярная медицина. - 2013. - №4. -
с.3-9
. Определение
активности ферментов монооксигеназной системы печени / Э.Э. Кузнецова, В.Г.
Горохова, А.Г. Горохов, А.А. Рунович // Бюллетень Восточно-Сибирского научного
центра Сибирского отделения Российской академии медицинских наук. - 2006. - №6.
- С.147-149.
8. RU 2366953 C2 Биохемилюминесцентный способ определения фагоцитарной
активности нейтрофилов / Д.Г. Дерябин, И.Ф. Каримов; ГБОУ ВПО «Оренбургский
государственный университет». - №2007139351/15; Заявл. 23.10.2007; Опубл.
10.09.2009, Бюл. №25. - 16 с.
9. RU 2431837 С2 Способ определения
антибактериальной резистентности организма человека / О.А. Коленчукова, А.А.
Савченко; НИИ медицинских проблем Севера Сибирского отд. РАМН. -
№2009124934/15; Заявл. 29.06.2009; Опубл. 10.10.2011, Бюл. №29. - 6 с.
10. RU 2445626 C1 Способ определения функциональной способности
фагоцитирующих клеток / О.В. Теплякова, Ю.С. Винник, А.А. Савченко и др.; ГБОУ
ВПО «Красноярский государственный медицинский университет имени проф. В.Ф.
Войно-Ясенецкого Минздрава РФ. - №2011107691/15; Заявл. 28.02.2011; Опубл.
20.03.2012, Бюл. №8. - 8 с.