|
Лекарственное веществоБез добавления щелочиПри добавлении щелочи
|
|
|
|
Фенол
|
Темно-зеленая
|
Вишнево-красная
|
Сине-зеленая
|
Фиолетовая
|
|
Резорцин
|
Фиолетово-черная
|
Фиолетово-черная
|
|
Кислота салициловая
|
Светло-коричневая, переходящая в фиолетовую
|
Желтая
|
|
Кислота ацетилсалициловая
|
Желтая
|
Сиреневая
|
|
Мезатон
|
Бурое
|
Желто-бурое
|
|
Пиридоксина гидрохлорид
|
Бесцветное
|
Розовато-желтое, переходящее в буро-желтое.
|
3.
Идентификация простой эфирной связи
спирт фенольный
гидроксил эфирный
3.1
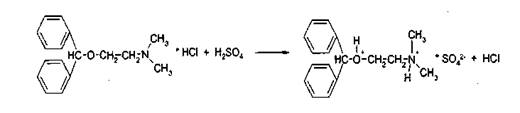
Реакции образования оксониевых солей с кислотой серной концентрированной
Методика. На
часовое стекло или фарфоровую чашку наносят 3-4 капли кислоты серной
концентрированной и прибавляют 0,05 г. димедрола, появляется желто-оранжевое
окрашивание, постепенно переходящее в кирпично-красное. При добавлении
воды окраска исчезает.
4.
Идентификация альдегидной группы
.1
Реакции окисления альдегидов
Альдегиды
превращаются в кислоты под влиянием окислителей. Они восстанавливают из
растворов солей многие металлы (например, катионы Ag, Cu, Hg и др.), особенно в
присутствии щелочи. Комплексные соединения этих металлов позволяют применять их
в щелочной среде в виде растворов, из которых при действии на них альдегидов
выделяются характерные осадки различного цвета.
Реакция
с аммиачным раствором серебра нитрата (реакция «серебряного зеркала»)
Методика. К 2 мл
раствора нитрата серебра прибавляют 10% раствор аммиака (~ 0,5 мл) до
растворения образующегося при постепенном приливании раствора аммиака осадка,
затем доливают раствор, содержащий ~ 0,01-0,005 г. вещества, при осторожном
нагревании (лучше на водяной бане при температуре 50-60°С); выделяется
металлическое серебро.

Реакция
с реактивом Фелинга
Методика. К 2 мл
раствора, содержащего около 0,01-0,005 г. вещества, приливают 5 мл раствора
Фелинга, нагревают до кипения; образуется красно-оранжевый осадок.
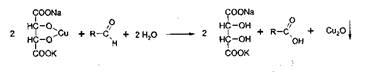
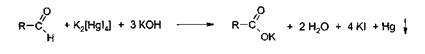
Реакция
с реактивом Несслера
Методика. К 2-3
каплям раствора альдегида прибавляют 2-3 капли реактива Несслера и нагревают.
Выделяется бурый осадок металлической ртути.
4.2
Реакция нуклеофильного присоединения-отщепления
В качестве
реагентов используются первичные амины (образуются основания Шиффа);
гидрохлорид гидроксиламина (образуются оксимы).
Методика. К 1 мл
раствора альдегида прибавляют 1 мл щелочного раствора гидроксиламина гидрохлорида.
Постепенно выпадает осадок оксима.
 .
.
.3
Реакции конденсации
Альдегиды в среде
кислоты серной конденсируются с фенолами, образуются окрашенные хиноны.
5.
Идентификация карбоксильной группы
.1
Реакция диссоциации - кислая среда
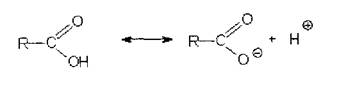
(метилоранж
окрашивается в розовый цвет, лакмусовая бумага розовеет)
.2
Реакция образования сложных эфиров (этерификация)
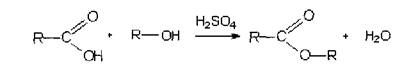
Общий вид реакции:
Например, кислота
бензойная образует сложный эфир (этилбензоат) в присутствии концентрированной
серной кислоты.

5.3
Реакция с солями тяжелых металлов
При этом
образуются: серебряные соли белого цвета; ртутные - серого цвета; соли железа
(Ш) - розовато-жёлтого цвета - и др.; соли меди (П) - голубого или синего
цвета;
кобальтовые -
сиреневого или розового цветов.
Методика: К 5 мл
теплого раствора никотиновой кислоты (1:100) приливают 1 мл раствора ацетата
меди или сульфата меди, выпадает осадок синего цвета.
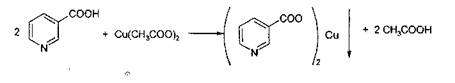
На
бензоаты: с раствором хлорида окисного железа
(III)
образуется розовато-желтый осадок.
Методика. Препарат
растворяют в щелочи, взбалтывают, разбавляют водой, фильтруют. К фильтрату
прибавляют раствор хлорида окисного железа, образуется:

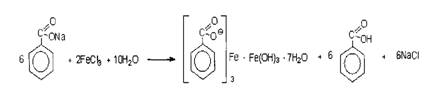
На
салицилаты: раствором хлорида
окисного железа (III) образуется фиолетовое окрашивание.
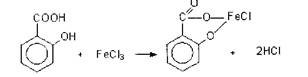
6.
Идентификация сложноэфирной группы
.1
Реакции гидролиза
Препараты,
содержащие в своей структуре сложноэфирную группу, подвергаются щелочному или
кислотному гидролизу.
Реакции
щелочного гидролиза. Под действием щелочей
образуется соль органической кислоты и спирт.
Методика. 0,05 г. анестезина
нагревают с 5 мл раствора едкого натра и приливают 0,1 н. раствор йода до
неисчезающего желтого окрашивания; появляется запах йодоформа.

Реакции
кислотного гидролиза. Под действием кислоты образуется органические кислоты
Методика. 0,2 г
кислоты ацетилсалициловой помещают в фарфоровую чашку, добавляют 0,5 мл
концентрированной кислоты серной, перемешивают и добавляют 1-2 капли воды;
ощущается запах кислоты уксусной. Затем добавляют 1-2 капли формалина;
появляется розовое окрашивание.
6.2
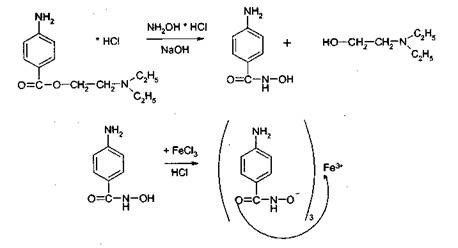
Гидроксамовая реакция
При взаимодействии
с гидроксиламином в щелочной среде образуются гидроксамовые кислоты, которые
после подкисления кислотой хлороводородной образуют окрашенные гидроксаматы с
солями железа (III) или меди (II).
Методика. 0,1 г
новокаина растворяют в 2 мл воды, прибавляют 2 мл щелочного раствора
гидроксиламина, встряхивают 5 мин, прибавляют 2 мл разведенной кислоты
хлороводородной и 0,5 мл 10% раствора железа (III) хлорида. Появляется вишневое
окрашивание.
7.
Идентификация лактонов
Лактонами
называются внутренние сложные эфиры.
Гидроксамовая
реакция
Методика: 0,02 г.
препарата (пилокарпин) растворяют в 3 мл спирта 95%, прибавляют 1 мл щелочного
раствора гидроксиламина, встряхивают, ставят на водяную баню на 5 минут. Затем
добавляют 2 мл кислоты хлористоводородной разведенной, 0,5 мл 10% раствора
железа (III) хлорида в 0,1 моль/л растворе кислоты хлористоводородной.
Появляется красное или красно-фиолетовое окрашивание.

8.
Идентификация первичной ароматической аминогруппы
.1
Реакция диазотирования с последующим азосочетанием (реакция образования
азокрасителя)
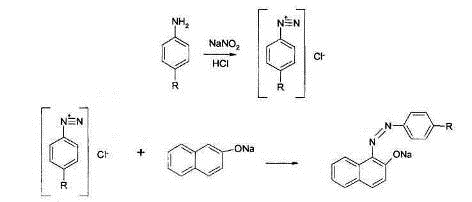
Общим свойством
первичных ароматических аминов является способность к образованию соли диазония
и азокрасителей. Реакция образования соли диазония проводится с натрия нитритом
в кислой среде. Ионы диазония, обладающие электрофильными свойствами, вступают
с ароматическими соединениями (с фенолами или ароматическими аминами) в реакцию
электрофильного замещения с образованием азокрасителя.
Реакция
диазотироеания с последующим азосочетанием включены в раздел «Общие реакции на
подлинность» ГФ XI и широко используются в внутриаптечном контроле.
Методика. 0,05 г.
препарата растворяют в 1 мл разведенной хлористоводородной кислоты, если
необходимо, нагревают, охлаждают во льду, прибавляют 2 мл 1% раствора нитрита
натрия; полученный раствор прибавляют к 1 мл щелочного раствора β-нафтола, содержащего
0,5 г ацетата натрия; образуется осадок от желто-оранжевого до оранжево-красного
цвета.
9.
Идентификация имидной группы
.1
Реакция образования солей с тяжелыми металлами
Многие
лекарственные вещества содержат в своей молекуле имидную группу, например, все
сульфаниламидные препараты, производные барбитуровой кислоты, производные
пурина (теофиллин, теобромин) и др.
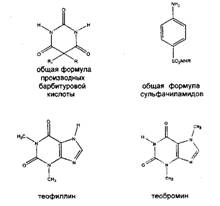
Для всех этих
соединений характерны реакции с солями тяжелых металлов с образованием
окрашенных солей.
Методика. 0,05 г.
препарата (если он нерастворим в воде, т.е. кислые формы) переводят в соли
добавлением 0,1 н. раствора щелочи до едва заметного голубоватого окрашивания
раствора (индикатор тимолфталеин) или приготавливают насыщенный раствор
препарата в 0,1 н. растворе щелочи. После встряхивания полученной смеси ее
фильтруют. Фильтрат нейтрализуют 0,1 н. раствором соляной кислоты до
слабо-голубого окрашивания (индикатор - тимолфталеин). Полученный раствор
разливают в три пробирки и в каждую прибавляют по 2-Зкапли растворов хлорида
окисного железа, хлорида кобальта и сульфата меди соответственно. Образующиеся
при этом окрашенные растворы или осадки приведены в табл. 5.
Таблица 5. Цветные
реакции сульфаниламидных препаратов с солями тяжелых металлов
|
Препарат
|
Окраска осадка или раствора от прибавления растворов
|
|
Хлорида окисного железа
|
Хлорида кобальта
|
Сульфата меди
|
|
Сульфацил
|
Красноватое окрашивание раствора
|
Розовое окрашивание раствора
|
Голубой с зеленоватым оттенком осадок
|
|
Норсульфазол
|
Светло-оранжевый осадок
|
Осадок сиреневый, быстро переходящий в сине-фиолетовый
|
Осадок грязно-фиолетового цвета, переходящий в темно-лиловый
|
|
Сульфадимезин
|
То же
|
Осадок сиреневого цвета
|
Осадок желто-зеленого цвета, переходящий в красно-бурый
|
|
Сульгин
|
Раствор желтого цвета
|
Раствор розового цвета.
|
Раствор голубого цвета.
|
|
Этазол
|
Осадок светло-оранжевого цвета
|
Осадок белого цвета при стоянии темнеющий
|
Осадок травянисто-зеленого, переходящий в темный цвет
|
|
Фталазол
|
-
|
-
|
Осадок серо-грязно-фиолетовый
|
Список
литературы
1.Беликов
В.Г. Фармацевтическая химия. В 2 ч. Ч. I. Общая фармацевтическая химия:
Учеб. для фармац. ин-тов и фак. мед. ин-тов. - М.: Высш. шк.; 1993. - 432 с.
2.Глущенко
Н.Н. Фармацевтическая химия: Учебник для студ. сред. проф. учеб. заведений /
Н.Н. Глущенко, Т.В. Плетенева, В.А. Попков; Под ред. Т.В. Плетеневой. - М.:
Издательский центр «Академия», 2004. - 384 с.
3.Государственная
фармакопея российской федерации / «Издательство «Научный центр экспертизы
средств медицинского применения», 2008. - 704 с.
4.Государственная
фармакопея СССР: Вып. I. Общие методы анализа/ МЗ СССР. -11-е изд., доп. - М: Медицина,
1987. - 336 с.
5.Органическая
химия: Учеб. Для вузов: В 2 кн. / В.Л. Белобородое, С.Э. Зурабян, А.П. Лузин,
Н.А. Тюкавкина; Под ред. Н.А. Тюкавкиной. - М.: Дрофа, 2003. - Кн. 1: Основной
курс. - 640 с.
6.Руководство
к лабораторным занятиям по фармацевтической химии: Учебное пособие / Аксенова
Э.Н., Андрианова О.П., Арзамасцев А.П. и др. / Под ред. А.П. Арзамасцева. - М.:
Медицина, 2004. - 384 с.