Химические превращения 4-оксоалкановых кислот
МИНИСТЕРСТВО
ОБРАЗОВАНИЯ И НАУКИ РФ
ФБГОУ ВПО
«СРАТОВСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
ИМЕНИ
Н.Г.ЧЕРНЫШЕВСКОГО»
Кафедра
органической и биоорганической химии
химические превращения 4-оксоалкановых кислот
КУРСОВАЯ
РАБОТА
студентки
2 курса Института химии
Пискуровой
Виктории Сергеевны
Научный
руководитель
д.х.н.,
профессор А.Ю. Егорова
Зав.
кафедрой
д.х.н.,
профессор О.В. Федотова
Саратов 2013
Введение
-Кетоноалкановые кислоты, как и многие другие
органические соединения, очень важны в жизнедеятельности человека. Они находят
широкое применение в производстве смазочных материалов, пластификаторов./1/ Их
так же используют для получения насыщенных кислот алифатического ряда, а на
основе последних - синтетические моющие средства. Несмотря на широкое
практическое применение 4-оксоалкановых кислот, стоит вопрос о разработке
наиболее выгодных способов получения. Получить их можно путем расщепления
фуранового цикла фурилкарбинолов. Данный способ был изучен М.И. Ушаковым и В.Ф.
Кучеровым /2/. Реакция протекает под действием минеральных кислот и,
соответственно, приводит к образованию 4-кетонокарбоновых кислот или их сложных
эфиров.
Литературный обзор
Получить 4-оксокарбоновые кислоты, как уже
упоминалось выше, можно из фурилкарбинолов. Механизм этой реакции нельзя
считать окончательно установленным. Наиболее вероятна схема, предложенная
Легером (1):
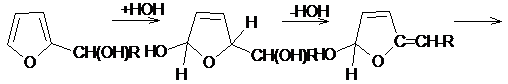
изомеризация 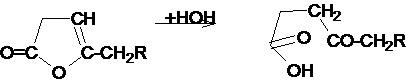
Кроме этого, ɤ-кетокарбоновые кислоты и их
эфиры способны к внутримолекулярной циклизации, которая приводит к образованию
5-алкилзамещенных 3Н-тиолен-2-онов и 3Н-фуран-2-онов. Авторами был разработан
способ получения 5-алкил-4-тиолен-2-онов (2а-г) на основе этиловых эфиров ɤ-кетокарбоновых
кислот(3) :

1а-и 2а-и
3а-и
-3 а, д R=
C₃H₇;
б R= С₄H₉;
в, ж R= iso-C₄H₉;
г, з R=C₅H₁₁;
е R=C₄H₉;
и R= iso-C₅H₁₁;
а-г R`= C₂H₅;
д-и R`=H;
а-г X=S;
д-и X=O
-оксоалкановые кислоты и их эфиры так же склонны
к реакциям аминирования. Реакции гетероциклизации 4-оксоалкановых кислот под
действием ароматических аминов приводят к образованию N-арилзамещенных
пиррол-2-онов. (4)

А
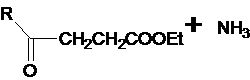
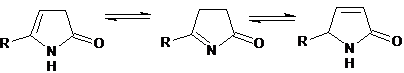
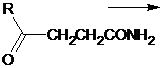
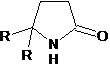
-3 a
R= C₃H₇;
b R=C₅H₁₁;
е R=C₄H₉;
c R=
i-C₅H₁₁;
d R = C₆H₁₃;
e R= C₇H₁₅;
f R= C₈H₁₇
Атака аммиаком возможна по атому углерода
оксогруппы, с образованием интермедиата А либо по атому углерода этоксикарбонильной
группы с образованием амидов 4-оксоалкановых кислот.(4)
Аммонолиз эфиров 1e,f
приводит в амидам 3e,f,
которые были выделены упариванием реакционных смесей. В этих амидах открытая и
циклическая формы довольно устойчивы и таутомерное равновесие не устанавливается.(4)
Взаимодействие 4-оксоалкановых кислот 4a-g
с ацетатом аммония авторы проводили кипячением в ксилоле или уксусном
ангидриде. Целевые N-незамещенные
пиррол-2-оны 2a-g
с выходами до 70% получены в уксусном ангидриде.(4)

4 a-g 2a-g 3e-g
2,3,4 a R=Pr ; b R=C₅H₁₁
; c R= i-C₅H₁₁;
d R= C₆H₁₃;R=
CH; f R= CH; g R= Ph
Использование ксилола позволяет получить
соединения 2e-g
с выходом до 65% с одновременным выделением амидов 3e-g
(20%). В этом случае реакция протекает, вероятно, также через стадию
образования амидов 4-оксоалкановых кислот, циклизация которых с лучшими
выходами осуществляется в уксусном ангидриде.(4)
Взаимодействие этиловых эфиров 4-оксоалкановых
кислот 5а-с с ароматическими аминами при кипячении в ксилоле протекает с
образованием целевых 1-арил-5-алкил (арил)-3Н- пирролин-2-онов 2а-с с выходами
63-75%, а также изомерных 1-арил-5-алкил-5Н-пирролин-2-онов 3а-с с выходами
10-35%.


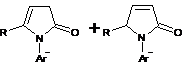
2, 3 ,5 а
R= CH, Ar= CH; b R = CH, Ar = CH; c R= i-CH, Ar = CH
При проведении реакции в мягких условиях, в
растворе этилового спирта, выходы соединений 2а-с и 3а-с в каждом случае в
сумме не более 18%, поскольку реакция проходит через стадию образования
промежуточных енаминов А и инаминов В, циклизация которых вследствие снижения
активности атома азота затруднена. (5)
На основе 4-оксоалкановых кислот возможен синтез
5-алкил(арил)-3-арилиден-3Н-фуран-2-онов. Синтез проводится при обработке
4-оксоалкановых кислот эквимолекулярным количеством альдегидов в присутствии
ацетата натрия.

,3 а R=CH, б R= CH, в R=CH₇, г с д R= CH-i; 2 а R=C₆H, Ar= CH; б R= CH, Ar= CH; в R=CH,Ar= CH; г R= CH, Ar= CH; д R=CH, Ar= CH-Cl-o; е R=CH, Ar= CH-NO-o; ж R= CH, Ar= CHN(CH); з R=CH, Ar= фурил-2; и
R= CH, Ar= фурил-2; к
R= CH-i, Ar= фурил-2; л
R= CH, Ar= α- NO-фурил-2; м R= CH, Ar=
5-йодфурил-2.
Схема образования соединений 2а-д на
основе 4-оксоалкановых кислот (3а-д) предполагает первоначальную лактонизацию
кислот в 3Н-фуран-2-оны (1а-д), вступающие в последующую реакцию конденсации с
альдегидами, без выделения промежуточных продуктов.
Следует отметить, что возможно
неоднозначное протекание процесса. Однако альтернативное направление реакции,
первой стадией которой является конденсация альдегидов по метиленовой группе β-положения
кислоты, характеризующегося большей С-Н кислотностью, чем α-метиленовое
звено, и последующая лактонизация продукта, приводящая к образованию
5-алкенил-4-арилидентетрагидрофуран-2-она (4), не реализуется.(6)

Кроме этого, были синтезированы
гетероциклические системы ряда бензопирролоимидазолов и пирролохинозолинонов
реакцией 1,4-оксоалкановых кислот с 1,2-бинуклеофилами. (7)
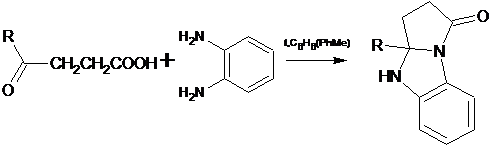
1 R=
Ph; 2 R=4-Me-C₆H₄
кетоноалкановый кислота
фурилкарбинол синтез
Цель исследования и обсуждение результатов
Ацилирование по Фриделю-Крафтсу служит удобным
методом введения ацильной группы в ароматическое ядро, что приводит к
образованию арилзамещенных кетонов. Целью настоящей работы является получение
4-(4-метоксифенил)-4-оксобутановой кислоты. В качестве ацилирующего агента
использовали ангидрид янтарной кислоты в присутствии кислоты Льюиса.

В качестве кислоты Льюиса использовали
безводный хлорид алюминия, который был взят в стехиометрическом избытке,
поскольку катализатор уходит из реакции, образуя комплекс янтарным ангидридом.
Происходит образование донорно-акцепторного комплекса. Образовавшаяся
электрофильная частица ацилирует анизол преимущественно по пара-положению,
вследствие стерических затруднений. В результате чего образовавшийся замещенный
алюминий дихлорид гидролизуется в слабокислой среде с образованием
4-(4-метоксифенил)-4-оксобутановой кислоты. Физико-химические характеристики
полученного соединения соответствуют литературным данным.
Экспериментальная часть
В ходе работы мы использовали:
|
Янтарный
ангидрид
|
ч.
|
ТУ
6-09-3611-74
|
|
Анизол
|
|
|
|
Хлорид
алюминия
|
осч.
|
ТУ
6-09-2267-72
|
|
Соляная
кислота
|
хч.
|
ГОСТ
3181-67
|
|
Ацетон
|
ГОСТ
2603-71
|
Синтез 4-(4-метоксифенил)-4-оксобутановой
кислоты.
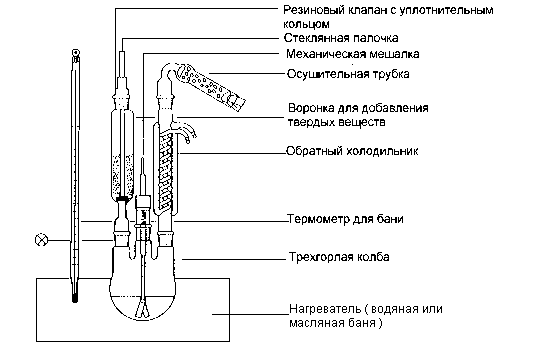
В трехгорлую колбу объемом 1л.,
снабженную механической мешалкой и обратным холодильником помещают 34г
янтарного ангидрида и 250 мл анизола. При перемешивании через третье горло,
закрытое пробкой на шлифе, порциями вносят 100 г тонкоизмельченого безводного
хлорида алюминия.
Происходит выделение HCl, смесь
разогревается. По окончании прибавления хлорида алюминия при перемешивании
смесь нагревают в течении 1 часа. Далее к охлажденному раствору приливают 150
мл холодной дистиллированной воды. Происходит разогревание. В охлажденную колбу
приливают 50 мл концентрированной HCl. Твёрдый
продукт охлаждают, промывают холодной смесью 50 мл концентрированной HCl и 150 мл
воды, а затем фильтруют и промывают водой. Образовавшиеся светло-желтые
кристаллы перекристаллизовывают из горячей воды. Раствор фильтруют, после
охлаждения фильтрата выпадают белые кристаллы кислоты.
Выход: 30г. (44,3%) Т.пл. 156-157°С
.
Инструкция по охране труда и технике
безопасности
Работа с легколетучими
растворителями
При работе с легколетучими
растворителями всегда нужно иметь под рукой листовой асбест, песок и другие
средства тушения. На рабочем столе и соседних столах не должно быть открытого
пламени. Особую осторожность следует соблюдать при работе с эфиром. При отгонке
эфира водяную баню следует наливать водой, нагреваемую в стороне от места
работы с эфиром. К приемнику присоединяют резиновую трубку, конец которой
опущен под рабочий стол.
При возникновении пожара надо
немедленно удалить легковоспламеняющиеся вещества и тушить пламя, накрывая его
влажным одеялом или засыпая песком.
На рабочем мете нужно иметь
количество растворителя, не превышающего суточную потребность. Большое
количество хранить в сейфе или специально отведенных местах.
Работа с кислотами и щелочами
Крепкие кислоты, щелочи и крепкие их
растворы при попадании на тело могут вызвать сильные ожоги. Поэтому при работе
с ними следует соблюдать следующие меры предосторожности:
а) работать в очках и резиновых
перчатках;
б) обеспечить удобное хранение
кислот и щелочей;
в) приливать кислоту в воду, а не
наоборот;
г) при переливании из склянки в
склянку пользоваться воронкой.
При ожогах кислотой обоженное место
промыть большими порциями воды и обработать 2% раствором бикарбоната натрия.
При ожогах щелочью обработать пораженное место раствором борной кислоты. При
попадании кислоты (или щелочи) в глаза промыть водой и обратиться к врачу.
Первая помощь при острых отравлениях
химическими веществами
Концентрированные кислоты
симптомы отравления: при вдыхании
паров - насморк, чихание, кашель, жжение в горле; при попадании брызг в глаза -
резкая боль, слезотечение; при попадании на кожу - ожоги.
Первая помощь: обильное промывание
водой, затем 2% раствором соды, затем опять водой, закапывание в глаза
новокаина, альбуцида.
Работа с электроприборами
Работа с электрическими и
электронагревательными приборами требует особенно внимательного и точного
соблюдения правил по технике безопасности. Это связано с тем, что при особых
условиях (большая влажность, отсутствие исправной изоляции), поражение может
быть нанесено током при напряжении 36В или даже 12В.
Первым и необходимым условием
безопасности является устройство защитного заземления. Работать разрешается
только при исправном оборудовании.
В целях безопасной работы
категорически запрещается:
1. Проверять
на ощупь наличие напряжения и нагрев токоведущих частей прибора.
2. Применять
для соединения блоков и приборов провода с поврежденной изоляцией.
3. Снимать
кожух прибора, включенного в сеть 220В.
При поражении электрическим током человека,
необходимо отключить установку с помощью выключателя, освободить пострадавшего
от действия электрического тока, оказать ему первую помощь.
Выводы
1. Обобщены литературные данные, посвящённые
синтезу и свойствам 4-кетокарбоновых кислот.
2. Поведен синтез
4-п-анизол-4-оксобутановой кислоты.
. На основании литературных данных
предложен возможный механизм реакции.
Список использованных источников
1. База
патентов СССР <http://patentdb.su/>, Способ получения кетоалкановых
кислот
http://patentdb.su/5-745891-sposob-polucheniya-ketoalkanovykh-kislot.html
. А.А.
Пономарёв, В.А. Седавкина. Синтез ɤ- кетонокарбоновых кислот и ɤ-лактонов
из фурилалкилкарбинолов. -ЖОХ , 1961. - т.31. -С. 984-985
. В.А.
Седавкина, Н.А. Морозова, А.Ю. Егорова, И.Г. Остроумов. Синтез и реакции
конденсации 5-алкил-3Н-тиолен-2-онов и 5-алкил-3Н-фуран-2-онов по метиленовой
группе гетероцикла. - ХГС,1987. - №4.-С. 451
. А.Ю.
Егорова, В.А. Седавкина, З.Ю. Тимофеева. Синтез и строение
5-алкил(арил)пиррол-2-онов. - ХГС, 2001. - №5. -С. 602-603
. А.Ю.
Егорова, В.А. Седавкина, З.Ю. Тимофеева. Гетероциклизация производных
4-оксоалкановых кислот в 1,5-дизамещённые пирролин-2-оны. - ХГС, 2001.- №6. -
С. 755,757-758.
. А.Ю.
Егорова, П.В. Решетов, Н.А. Морозова, В.А. Седавкина. 3-арилиденпроизводные
3Н-фуран-2-онов. Синтез и взаимодействие с малеиновым ангидридом. - ХГС, 1997.
- № 8. -С. 1043-1044.
. В.А.
Гринёв. Реакции электрофильного замещения в ряду бензопирролоимидазолонов и
пирролохиназолинонов. - Автореферат, 2011. -С. 6.