Введение в культуру in vitro растений Allium fistulosum
Аннотация
Данный эксперимент проводится с целью выявления
и изучения хромосомных перестроек, которые возникнут в регенерантах, полученных
из каллуса, благодаря перетасовке генов. Возникновение подобных изменений в
геноме, возможно, приведет к обнаружению новых свойств и качеств растения.
При проведении этой работы первоочередной
задачей является получение каллуса из семян и растительных эксплантов на
питательной среде с использованием фитогормонов или без. Следующей ступенью
является возникновение меристематических зон из каллуса и формирование из них
растений. И, наконец, микроскопический анализ полученных растительных образцов
для выявления изменений в геноме.
Оглавление
1.
Обзор литературы
.
Материалы и методы
.1
Растительный материал
.2
Методы исследования
.
Результаты и обсуждение
Выводы
Список
литературы
Введение
Развитие методов биотехнологии, в основе которых
лежит выращивание изолированных органов, тканей и клеток на искусственных
питательных средах с последующей регенерацией целых растений, определяет все
большее внедрение их в практику сельского хозяйства. Они способны значительно
ускорить селекционный процесс и значительно расширить границы воздействия
человека на живую природу.
Геном лука батуна остается слабо изученными по
целому ряду причин, в числе которых: большой размер, высокая частота дупликаций
и повышенная гетерозиготность. Размер генома A. fistulosum на 28% меньше генома
лука репчатого (Narayan, 1988), что делает его более удобным объектом
исследования. Семена лука батуна (Allium fistulosuml.) характеризуются
достаточно высоким спонтанным уровнем хромосомной нестабильности.
Цель работы: получение регенерантов из каллусной
ткани и изучение их свойств
Задачи: 1. Получение каллуса из семян и
эксплантов
. Получение регенерантов из каллуса
. Исследование свойств регенерантов на предмет
хромосомных перестроек.
В ходе работы мы проведем сравнительный анализ
сред, исходя из их способности образовывать каллус. Подберем оптимальные
условия для здорового роста и развития растительного материала.
1. Обзор литературы
Отдел: Цветковые
Класс: Однодольные
Порядок: Спаржецветные
Семейство: Амариллисовые
Подсемейство: Луковые
Род: Лук
Вид: Лук-батун
Сорт: Русский зимнийявляется крупнейшим и важным
представителем род семейства Alliaceae и включает в себя 450 видов, широко
распространены в северном полушарии. Лук-батун (лук татарский, лук дудчатый,
лук песчаный) (Allium fistulosum L.) - многолетнее травянистое растение
семейства Луковые, возделываемое ради рано отрастающей зелени. В открытом грунте
дает высококачественную продукцию с апреля по ноябрь. Хромосомный набор- (2n =
16).
Имеет три подвида - Японский, Китайский и
Русский (отличается высокой зимостойкостью и большой витаминозностью). Может
расти на одном месте несколько лет. Образует малозаметную цилиндрическую
луковицу, переходящую в ложный стебель с полыми дудчатыми листьями.
Зонтик шаровидный, многоцветковый; цветоножки
тонкие, в 2-3 раза длиннее околоцветника, околоцветник колокольчатый; листочки
околоцветника желтоватые, продолговатые, острые. Нити тычинок в 2-3 раза
длиннее околоцветника, цельные.
 <https://commons.wikimedia.org/wiki/File:Allium_cepa_B.jpg?uselang=ru>
<https://commons.wikimedia.org/wiki/File:Allium_cepa_B.jpg?uselang=ru> <https://commons.wikimedia.org/wiki/File:Allium_fistulosum_var._bulbifera,_Sint-jansui_bloemen.jpg?uselang=ru>
<https://commons.wikimedia.org/wiki/File:Allium_fistulosum_var._bulbifera,_Sint-jansui_bloemen.jpg?uselang=ru> <https://commons.wikimedia.org/wiki/File:Allium_fistulosum_bulbifera0.jpg?uselang=ru>
<https://commons.wikimedia.org/wiki/File:Allium_fistulosum_bulbifera0.jpg?uselang=ru> <https://commons.wikimedia.org/wiki/File:Allium_fistulosum_MHNT.BOT.2011.3.23.jpg?uselang=ru>
<https://commons.wikimedia.org/wiki/File:Allium_fistulosum_MHNT.BOT.2011.3.23.jpg?uselang=ru>
Слева направо:
Соцветие. Цветки (увеличено).
Луковички. Семена
В первый год после посева растение
образует дудчатые листья, которые осенью отмирают.
Со второго года, а затем ежегодно
батун выбрасывает стрелки, на которых формируются шарообразные соцветия.
Корни у лука-батуна сильно ветвятся
и распространяются в стороны на расстояние 60-70 см и на глубину 30-40 см. Корневая
система, которая весной начинает расти еще под снегом, к осени частично
отмирает. К осени образуются молодые корни и среди них такие, которые втягивают
ложную луковицу в почву и предохраняют ее тем самым от вымерзания.
От репчатого лука батун отличается
более вкусной зеленью, которая дольше сохраняется в стадии, пригодной для
потребления в свежем виде. Лук-батун размножается не только семенами, но и
вегетативно - делением куста. К концу первого года растение образует до 5
дочерних разветвлений, к концу второго года - до 10-15, а к осени третьего года
оно образует 20-30 отдельных растений, не связанных одно с другим. Вместе они
напоминают большой куст.
Лук-батун зимостойкое и
морозостойкое растение, переносит зимы с понижением температуры до -45°С. Семена
начинают прорастать при температуре 2-3°С, листья начинают расти уже при 1°С.
На одном месте батун может расти
много лет, но после четвертого года жизни кусты, разрастаясь, резко сбавляют
урожайность, сильно срелкуются. Поэтому чаще культуру ведут 3-4 года, потом
плантацию обновляют посевом семян.
«Русский зимний» - салатный,
среднеспелый, витаминный сорт. Период от начала отрастания листьев до
технической спелости 27-30 дней. Листья светло-зелёные, со средним восковым
налётом, длиной до 33 см. Вкус слабоострый. Товарную луковицу не формирует.
Ценность сорта: отличные вкусовые качества листьев, высокая урожайность,
зимостойкость, длительный срок отдачи зелёного товарного лука.
Химический состав, пищевые и
лечебные свойства. В зеленых листьях лука-батуна содержатся сахара, эфирное
масло, витамины С, А, В,, В2, PP. Причем витамина С в них в два раза больше,
чем в зеленом пере репчатого лука.
Лук-батун содержит соли магния,
калия и железа, имеет острый вкус, высокие вкусовые и целебные достоинства.
Последние в значительной степени обусловлены высоким содержанием в нем
фитонцидов. По действию на организм батун близок к репчатому луку.
Зеленые листья и все растение
используют в сыром виде для приготовления различных салатов, а также в
переработанном для - соусов, маринадов, приправ к мясным, рыбным и овощным
блюдам. Может использоваться вместо репчатого лука в первых блюдах и домашних
консервах.
Из лука-батуна получают препараты,
понижающие кровяное давление и повышающие эластичность кровеносных сосудов. В
народной медицине используется как болеутоляющее и тонизирующее средство.
Хороший источник витаминов в ранневесенний период.. fistulosum обладает генами
устойчивости к луковой листовой гнили (Currah, Maude, 1984), розовой корневой
гнили (Netzer et al, 1985) и антракнозу (Galvan et al, 1997), а также к луковой
мухе (de Ponti, Inggamer, 1984). Кроме того, лук батун отличается высоким
содержанием сухого вещества, более острым вкусом и морозостойкостью, более
ранним и более коротким цветением, большей привлекательностью соцветий для
насекомых-опылителей (Van der Meer, Van Bennekom, 1978).
Геномы этого и других видов луков до
сих пор слабо изученными из-за целого ряда причин, в числе которых: большой
размер генома, высокая частота дупликаций и повышенная гетерозиготность.
Семена лука батуна (Allium
fistulosuml.) характеризуются достаточно высоким спонтанным уровнем хромосомной
нестабильности. На втором году хранения семян частота аберрантных анафаз в
меристеме проростков может составить 3,5% и даже 14%, что зависит от сорта,
места вегетации и года урожая семян. На третьем году хранения частота
аберрантных анафаз в клетках корневой меристемы проростков может достигать 10%,
20% и 35% - в зависимости от загрязнения мест произрастания материнских
растений.
Накапливающиеся при хранении семян
изменения в геноме позволяют рассматривать возраст семян как своеобразный
мутаген, материальной основой которого являются метаболические процессы в
хранящихся семенах.
Выращивание Allium fistulosum in
vitro даёт возможность получить генетически однородный материал и освобождённый
от вирусов и бактерий на протяжении всего года независимо от факторов внешней
среды.
Регенерации растений in vitro из клеток,
тканей и органов культур является предпосылкой для применения биотехнологий в
размножении растений, селекции и генетического усовершенствования растений. Это
единственная технология для производства больших количеств элитного посадочного
материала, направленная на увеличение производства и производительности.
Микроразмножение выгодно по сравнению с традиционными методами, так как оно
может быть использовано для получения большого количества новых растений, таких
как те, которые были генетически модифицированы или разводятся с помощью
традиционных методов селекции растений.
Микроразмножение также используется,
чтобы обеспечить достаточное количество проростков для посадки из исходного
растения, которое размножается вегетативно. Это также приводит к быстрому
крупномасштабному распространению новых генотипов.
In vitro методы были
использованы с Allium для: (1) клонального размножения; (2) производство
незараженных клонов; (3) сохранение зародышевой плазмы; (4) получения новых
сортов через сомаклональной вариации и молекулярной генетики; и (5) вторичные
исследования метаболизма.
Данная опытно-селекционная работа
основана на использовании систем регенерации в пробирке, которые включают фазу
каллусообразования. Затем из каллуса должны быть сформированы меристемы,
заново, из тотипотентных клеток для осуществления регенерации. Это особенно
полезно при генерации сомаклональной вариации между клонами, и для изучения
трансформации.
Регенерация растения лука из
каллуса, однако, имеет определенные требования, хотя они отличаются в
зависимости от используемой технологии и исследовательской группы. Филлипс и
Luteyn (1983) показали, что образование каллуса и регенерация была улучшена с
помощью "пиклорам" как синтетического ауксина. Шахин и Канеко (1986)
получили улучшение регенерации из каллуса с использованием средств (BDSx BDS
макроэлементы и микроэлементы MS) в сочетании с дополнением of900 мг / литр
гидролизата казеина. В 1994 году Марани показал, что с помощью цитокинина
тидиазурон значительно повышает скорость пролиферации побегов чеснока из
меристемы нарастания.
Рассморим пример получения каллуса
из лука Шалота:
Два сорта А. сера, а именно Huruta
(DZSHT-91) и Minjar (DZSHT-164-1B) были получены в сельскохозяйственном
исследовательском центре, Debre-Zeit, Эфиопия. Свежие и неповрежденные луковицы
промывали в водопроводной воде с жидким мылом для очистки от почвы и некоторых
загрязняющих веществ из луковицы, затем обрабатывали стерильной водой,
содержащей две капли Твина 20 на 100 мл и 20% хлорной извести в течение 15-20
минут с продолжительным перемешиванием и, наконец, промывали 5-10 раз
дистиллированной водой.
Для того чтобы удалить фунгициды и
другие остатки, эксплантаты промывали в водопроводной воде, а затем в
дистиллированной, три раза. Тогда внешние сухие чешуи снимаются и отпаадют.
Нижние половинки луковиц, содержащих базальный диск, тщательно промывали и
погружали в 70% спирт в течение 1-2 мин, затем промывали четыре раза
дистиллированной водой, поверхность стерилизовали в 5,25% раствор гипохлорита
натрия (NaOCl) в течение 15 мин и снова ополаскивали четыре раза в
дистиллированной воде.
Эксплантаты, которые вырезали из
луковиц инокулировали в среде МС, содержащий 3% сахарозы и 0,8% агара, рН
доводили до 5,7. При индукции каллуса среду дополняли 1 мг/л 2, 4-Д, НАА, кН и
БАТ. Все среды помещались в автоклав при температуре 121°С, и давлении
1.05kg/см2 в течение 15 мин. Культуры инкубировали при комнатной температуре 25
± 2°С и при свете дневных люминесцентных ламп.
Каллусогенез
В настоящем исследовании, был
протестирована индукция каллусного потенциала двух сортов шалот с различными
гормонами и гормональными комбинациями. Каллус начал образовываться с 28 до 30
дней инкубации в Huruta и Minjar. Несмотря на длинный период индуцирования
каллуса, Minjar образовал больше каллуса, а также имел более высокий средний
вес, чем Huruta.
Из данного исследования было очевидно,
что среды MS, которые содержат 2,4-D, показали высокий каллусогенез (74,44%),
которому необходим минимум 28 дней для инициирования каллуса, а затем НАА +
БАТ, 2, 4-D + Кп и БАП, тогда как НАА и Кп показали самый низкий каллусогенез.
Наибольший сырой вес каллуса находится в средах, содержащих 2, 4-D.
2. Материалы и методы
.1 Растительный материал
В данном эксперименте в качестве растительного
материала использовались семена Allium
Fistulosum сорта
«Русский зимний» и растительные экспланты, полученные в дальнейшем из побегов,
образовавшихся при нестерильном проращивании семян.
.2 Методы исследования
Методы проращивания:
нестерильный
стерильный
При нестерильном проращивании в каждую чашку
Петри на влажную фильтровальную бумагу было выложено по 10 семян. После чего
чашки были размещены в световой комнате для дальнейшего наблюдения.
При стерильном проращивании семена были помещены
в марлевые мешочки, обработаны 5% раствором NaOCl в течение 12 минут и помещены
на питательные среды МС с содержанием фитогормонов и без, из расчета по 10 штук
в одну чашку. Расстояние между семенами ~1 см. На каждой чашке указывалась
дата, концентрация гормона и время стерилизации.
Для получения более точной оценки, семена и
экспланты подвергались различному времени стерилизации, а также были помещены
на среды с различной концентрацией 2,4-дихлорфеноксиуксусной кислоты (2,4*D)-
синтетического гормона-ауксина, способствующего образованию каллуса.
б/г
1мг/л
2мг/л
3мг/л
4мг/л
Образовавшиеся при нестерильном проращивании
побеги были поделены на экспланты, простерилизованы в NaOCl
(5%) 5 и 10 минут, а затем помещены на питательные среды с различной
гормональной концентрацией.
Различные условия проращивания позволяют
установить наиболее оптимальные условия для появления желаемых результатов,
таких как, в данном случае, образование каллуса.
Также, различное время стерилизации позволяет
найти оптимальный вариант, при котором будет минимум заростов, а семена и
экспланты сохранят жизнеспособность.
При обнаружении плесневых заростов, весь
растительный материал данной чашки Петри признавался непригодным для дальнейших
исследований и подвергался утилизации.
При бактериальных заростах здоровый материал
извлекался из зараженной чашки Петри и помещался в стерильную чашку с
аналогичной питательной средой.
каллусный гормональный регенерант
шалот
3. Результаты и обсуждение
В ходе эксперимента были получены нестерильные
проростки, часть которых послужила растительным эксплантом- была разделена на
кусочки ~0,5 см и помещена в чашки Петри на питательные среды различной
гормональной концентрации, вторая часть (10 шт) была помещена в пробирки с
безгормональной средой для дальнейшего роста.
Также, на стерильные питательные среды, с
гормонами и без, были помещены семена для получения каллуса.
Чашки Петри №1-20 были по ошибке облучены
ультрафиолетом, поэтому в дальнейшем не учитываются.
) Нестерильное проращивание семян (на 8 день
наблюдения)
Таблица 1
|
№
Чашки
|
Доля
проросших семян,%
|
|
1
|
70
|
|
2
|
90
|
|
3
|
80
|
|
4
|
80
|
|
5
|
80
|
|
Среднее
± доверит. интервал
|
{75,63
; 84,37}
|
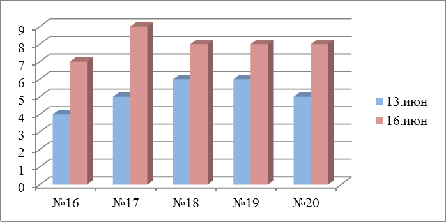
График 1
На Графике 1 показана интенсивность прорастания
семян в нестерильных условиях на влажной фильтровальной бумаге. В чашках №16 и
№19 была обнаружена плесень, поэтому в дальнейшем эксперимента они не
участвовали.
) Стерильное проращивание (на 10 день)
Таблица
2
|
Состав
среды
|
№
чашки
|
Контаминация
(+/-)
|
|
Б/г
|
1
|
_
|
|
2
|
+
|
|
3
|
+
|
|
4
|
+
|
|
5
|
_
|
|
1
мг/л
|
1
|
+
|
|
2
|
+
|
|
3
|
+
|
|
4
|
+
|
|
5
|
+
|
|
2
мг/л
|
1
|
+
|
|
2
|
+
|
|
3
|
+
|
|
4
|
+
|
+
|
|
3
мг/л
|
1
|
+
|
|
2
|
+
|
|
3
|
+
|
|
4
|
+
|
|
5
|
+
|
|
4
мг/л
|
1
|
+
|
|
2
|
+
|
|
3
|
+
|
|
4
|
+
|
|
5
|
+
|
На 10 день эксперимента проростков не
наблюдается, незараженные семена были пересажены на питательные среды с
аналогичным содержанием гормона. Выжило лишь 28% семян.
Часть нестерильно полученных проростков поделена
на экспланты и помещена на питательную среду МС с приведенными ранее
концентрациями гормона, а вторая часть - на безгормональную среду для
дальнейшего наблюдения.
Время стерилизации семян 12 минут.
Таблица
3
Результат на 24 день эксперимента (семена)
|
Состав
среды
|
№
чашки
|
Доля
проросших семян, %
|
Частота
каллусогенеза, %
|
Контаминация
|
|
1мг/л
|
1
|
20
|
10
|
+
|
|
2
|
0
|
0
|
+
|
|
2мг/л
|
1
|
0
|
0
|
_
|
|
2
|
0
|
0
|
+
|
|
3мг/л
|
1
|
0
|
0
|
+
|
|
4мг/л
|
1
|
10
|
0
|
+
|
|
2
|
0
|
0
|
+
|
|
Среднее
|
|
4,29
|
1,43
|
|
Таблица
4
Результат на 48 день эксперимента (семена)
№
чашки
|
Доля
проросших семян,%
|
Частота
каллусогенеза, %
|
Контаминация
|
|
1
мг/л
|
1
|
20
|
20
|
+
|
|
2
|
10
|
0
|
+
|
|
2
мг/л
|
1
|
0
|
0
|
_
|
|
2
|
0
|
0
|
+
|
|
3
мг/л
|
1
|
0
|
0
|
+
|
|
4
мг/л
|
1
|
10
|
0
|
+
|
|
2
|
10
|
0
|
+
|
|
Среднее
|
|
7,14
|
2,86
|
|
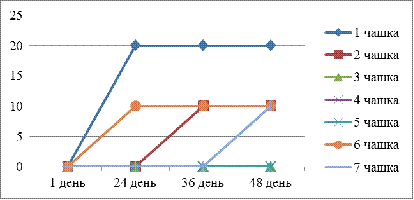
График 2
Таблица
5
Результаты на 12 день эксперимента (экспланты)
|
Состав
среды
|
№
чашки
|
Время
стерилизации
|
Доля
живых проростков, %
|
Частота
каллусогенеза, %
|
Контаминация
|
|
б/г
|
1
|
5
мин
|
100
|
0
|
+
|
|
2
|
10
мин
|
100
|
0
|
+
|
|
1
мг/л
|
1
|
5
мин
|
90
|
0
|
+
|
|
2
|
10
мин
|
70
|
0
|
|
3
|
5
мин
|
100
|
0
|
+
|
|
2
мг/л
|
1
|
5
мин
|
100
|
0
|
+
|
|
2
|
10
мин
|
100
|
0
|
+
|
|
3
мг/л
|
1
|
5
мин
|
100
|
0
|
+
|
|
2
|
10
мин
|
90
|
0
|
+
|
|
4
мг/л
|
1
|
5
мин
|
90
|
0
|
+
|
|
2
|
5
мин
|
90
|
0
|
+
|
|
3
|
10
мин
|
80
|
0
|
+
|
|
Среднее
|
|
|
92,5
|
0
|
|
Таблица
№6
Результаты на 36 день исследования (экспланты)
|
Состав
среды
|
№
чашки
|
Время
стерилизации, мин
|
Доля
живых проростков, %
|
Частота
каллусогенеза, %
|
Контаминация
|
|
б/г
|
1
|
5
|
20
|
0
|
+
|
|
2
|
10
|
30
|
0
|
+
|
|
1мг/л
|
1
|
5
|
20
|
0
|
|
2
|
10
|
0
|
0
|
+
|
|
3
|
5
|
30
|
0
|
+
|
|
2
мг/л
|
1
|
5
|
10
|
0
|
+
|
|
2
|
10
|
0
|
0
|
+
|
|
3
мг/л
|
1
|
5
|
0
|
0
|
+
|
|
2
|
10
|
0
|
0
|
+
|
|
4
мг/л
|
1
|
5
|
0
|
0
|
+
|
|
2
|
5
|
0
|
0
|
+
|
|
3
|
10
|
0
|
0
|
+
|
|
Среднее
|
|
|
9,17
|
0
|
|
Таким образом, можно отметить, что развитие
растительных образцов на питательной среде в стерильных условиях крайне низкое,
в отличие от нестерильного проращивания.
Далее рассмотрим результат помещения нестерильно
полученных проростков на безгормональную питательную среду.
) Первый день помещения на питательную
безгормональную среду (18.06)
 <#"877236.files/image008.jpg"> <#"877236.files/image009.jpg">
<#"877236.files/image010.gif">
<#"877236.files/image008.jpg"> <#"877236.files/image009.jpg">
<#"877236.files/image010.gif">
График 3
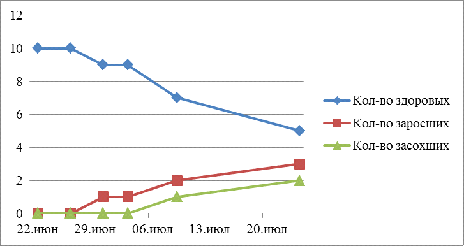
График 4
Пробирки №6 и №7 были поражены
плесенью, а №2 и №9 засохли.
Выводы
В ходе данной работы были получены данные по
интенсивности прорастания и зарастания бактериями семян и эксплантов, а также
интенсивности каллусообразования.
Можно сделать вывод, что
Показатели прорастания семян в нестерильных
условиях, как и их дальнейшее развитие в пробирках на безгормональной среде
высокие (Таблица 1, График 1, 3 и 4).
Прорастание семян на питательных средах, как и
образование каллуса из стерильных проростков и эксплантов, крайне низкое
(Таблица 3, 4, 5, 6, График 2).
Бактериальные заросты наблюдались у большей
части растительного материала.
Список использованной литературы
1. Статья
«In Vitro Plantlet Regeneration from the Bulbs of Shallot (Allium Cepa Var.
Group Aggregatum)»
2. Бутенко
Р.Г. Биология культивируемых клеток высших растений in
vitro и биотехнологии на
их основе. М.: ФБК-ПРЕСС. 1999. 160 с.
3. Научная
библиотека диссертаций и авторефератов disserCat
4. Tindal,
H.D., Vegetable in the tropics, Macmillan Education Ltd., Hong Kong, 1983, стр17
. Статья:
New Zealand Journal of Crop and Horticultural Science. Towards the
transformation of onions (Allium cepa).
7. Журавлев
Ю.Н., Омелько A.M. Морфогенез у растений in vitro II Физиология раст. 2008,
стр. 643-664
. Черемушкина
В.А. Биология луков Евразии. Новосибирск: Наука. 2004, с. 280
. Шевелуха
В С., Калашникова Е.А., Дегтярев С.В., Кочиева Е.З. и др. Сельскохозяйственная
биотехнология: учебник. 2008, с. 710
. Батыгина
Т.Б., Васильева В.Е. Размножение растений. СПб.: Изд-во С-Петербургского
университета. 2002, с. 229
. Волкова
Г.А. Биоморфологические особенности видов рода Allium L. При интродукции на
Европейский Северо-восток // 2007, с. 200
. Даева
О.В. Биологические особенности развития азиатских луков в ГБС // Экология и
интродукция растений. М. 1963, с. 110-114
. Калинин
Ф.Л., Сарнацкая В.В., Полищук В.Е. Методы культуры тканей в физиологии и
биохимии растений. Киев: Наук. Думка. 1980., с. 488
. Каменецкая
И.И., Рахимбаев И.Р. Вегетативное размножение лука каратавского в культуре
изолированных тканей // Бюллетень ГБС. 1984, с. 63