Современные аналитические подходы к выявлению фальсифицированных лекарственных препаратов группы спазмолитиков
Министерство здравоохранения
Российской Федерации
Государственное бюджетное
образовательное учреждение высшего профессионального образования
Санкт-Петербургская государственная
химико-фармацевтическая академия
Кафедра фармацевтической химии
СОВРЕМЕННЫЕ АНАЛИТИЧЕСКИЕ ПОДХОДЫ К
ВЫЯВЛЕНИЮ ФАЛЬСИФИЦИРОВАННЫХ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ ГРУППЫ СПАЗМОЛИТИКОВ
Санкт-Петербург 2015 г
Оглавление
Введение
1. Аналитические подходы к выявлению фальсифицированных
лекарственных средств
. Общая характеристика группы спазмолитических средств
. Аналитические подходы выявления фальсифицированных средств
группы спазмолитиков на примере дротаверина гидрохлорида
Заключение
Список использованной литературы
Введение
Фальсифицированные лекарственные средства являются серьезной проблемой
общественного здравоохранения. Помимо прямого вреда, наносимого больным в виде
риска для жизни и неудачного лечения, они создают также угрозу прогрессу,
достигнутому в области общественного здравоохранения, и подрывают доверие ко
всей системе здравоохранения.
По данным ВОЗ и других международных организаций, фальсифицированные
лекарственные средства обнаруживаются в большинстве государств мира. Нет ни
одной страны, в которой бы число сообщений снижалось. В большинстве стран отмечается
рост числа сообщений о выявленных случаях фальсификации [1].
Обеспечение качества лекарственных средств является одной из важнейших и
актуальнейших проблем здравоохранения России. Именно от этого показателя
зависит здоровье, а зачастую и жизнь российских граждан, что позволяет относить
проблему обеспечения надлежащего качества лекарственных средств к разряду
вопросов национальной безопасности [2].
Фальсификация лекарственных средств является одним из самых опасных
явлений современного фармацевтического рынка. Применение поддельной
фармацевтической продукции может приводить к осложнениям заболеваний, быть
причиной новых патологических процессов, а также повлечь смерть пациента.
Опасность фальсифицированных лекарств усиливается за счет возможности их приема
большим количеством людей.
Среди причин, способствующих распространению фальсифицированных
лекарственных средств в России, можно назвать большое количество дженериковых
лекарственных препаратов, зарегистрированных в Российской Федерации в настоящее
время. Каждая фирма-производитель такого препарата разрабатывает на него
собственные стандарты качества, в ряде случаев демонстрирующие между собой
существенные различия. Обилие стандартов качества лекарственных средств,
содержащих различные подходы к оценке качества одного и того же препарата
разных производителей, может существенно затруднить оценку качества
воспроизведенных лекарственных средств, что отрицательно сказывается на
эффективности выявления фальсифицированных препаратов.
Среди лекарственных средств, наиболее часто выявляющихся как
фальсифицированные на территории Российской Федерации, можно отметить
лекарственные препараты, обладающие спазмолитическим действием [3].
Как показывает практика, чаще всего фальсифицированные лекарственные
средства выявляются в процессе контроля их качества на соответствие требованиям
нормативных документов по показателю «Подлинность». Наибольшее применение для
установления подлинности имеют спектрофотометрические методы и тонкослойная
хроматография. Метод тонкослойной хроматографии является наиболее простым и
доступным с точки зрения стоимости анализа. В то же время, этот метод позволяет
проводить полуколичественный и количественный анализ, что особенно важно при
выявлении фальсифицированного лекарственного средства, содержащего активные
ингредиенты в количествах, не соответствующих указанным на этикетке [1].
Цель данной работы - обзор современных аналитических подходов к выявлению
фальсифицированных лекарственных препаратов группы спазмолитиков.
Для достижения этой цели поставлены следующие задачи:
1. Изучить литературу, посвященную выявлению фальсифицированных
лекарственных средств современными аналитическими методами.
2. Привести общую характеристику, включающую в себя классификацию по
химической структуре спазмолитических средств.
. Изучить литературу, посвященную выявлению фальсифицированных
лекарственных средств современными аналитическими методами группы
спазмолитиков.
. Изучить и охарактеризовать аналитические методики определения
фальсификатов из группы спазмолитических средств на примере дротаверина
гидрохлорида («Но-шпа»), как наиболее часто фальсифицируемым препаратом из этой
фармакотерапевтической группы.
лекарственный фальсификат хроматография
1.
Аналитические подходы к выявлению фальсифицированных лекарственных средств
Качество лекарственного средства - это совокупность свойств, которые
придают лекарственному средству (ЛС) способность удовлетворять потребителей в
соответствии со своим предназначением и соответствуют требованиям,
установленным законодательством [4].
Это определение, однако, слишком широкое, чтобы его можно было реально
применять на практике, поскольку оно пытается охватить сразу три разных уровня
качества ЛС:
-й уровень характеризует эффективность и безопасность (а также
соотношение польза/риск) самого активного фармацевтического ингредиента.
-й уровень характеризует требования к качеству спецификации на субстанцию
и готовое ЛС, а также уровень разработки, производства и контроля качества ЛС
(например, соответствие требованиям GMP), то есть - различие в качестве между
разными производителями одного и того же ЛС.
-й уровень характеризует соответствие конкретного образца препарата
требованиям собственной спецификации (являющегося частью регистрационного
досье). С точки зрения 3-го уровня качества, препарат, соответствующий
требованиям своей спецификации, является стандартным, то есть качественным. ЛС,
не соответствующее требованиям своей спецификации, является субстандартным, то
есть некачественным. В отличие от 1 и 2-го уровня, потребитель при покупке не
знает, соответствует ли препарат 3-му уровню качества, является он стандартным
или субстандартным.
Заключение о качестве 1 и 2-го уровня делают регуляторные органы на
стадии регистрации и пострегистрационных наблюдений. Заключение о качестве 3-го
уровня делает ГИ МЗ при контроле препаратов на рынке [5].
Кроме того, препарат может быть качественным (3-й уровень - с точки
зрения Фармакопеи и своих реальных характеристик качества), но
фальсифицированным. С другой стороны, препарат может быть нефальсифицированным,
но субстандартным (то есть некачественным). Такая картина в последние годы
часто наблюдалась в Российской Федерации.
ЛС можно условно поделить на две группы:
) ЛС с высоким уровнем переработки - таблетки, капсулы, инъекции, мази,
спреи и другие лекарственные формы, описанные в ГФ;
) ЛС с низким уровнем переработки (фасованное лекарственное растительное
сырье, сборы, масла и т.д.).
Методы выявления ФЛС для этих групп разные.
Для производства ЛС первой группы требуются достаточно сложное аппаратурное
обеспечение, жесткие требования к помещениям, персоналу и отработанной
технологии производства. Только в этом случае можно удовлетворить требованиям
ГФ к соответствующим лекарственным формам. К ним относятся
фармако-технологические испытания, микробиологическая чистота, стерильность,
пирогенность или ЛАЛ-тест, а также такие простые испытания, как описание,
прозрачность, цветность, рН. Эти испытания, как правило, невозможно проводить
при производстве ФЛС, для которых технология не отлажена (перечисленным
требованиям ГФ не всегда соответствуют даже нефальсифицированные ЛС).
Поэтому для выявления ФЛС на первом этапе для ЛС первой группы наиболее
эффективны такие простые фармакопейные испытания:
таблетки: однородность массы, истираемость таблеток без оболочки,
распадаемость;
капсулы: однородность массы, распадаемость;
инъекции: механические включения, рН;
суппозитории: распадаемость, устойчивость к разрушению, температура
плавления;
порошки для парентеральных ЛС: однородность массы, механические включения,
идентификация и т.д.
Кроме этих тестов, для выявления ФЛЗ ВОЗ рекомендует использовать
визуальную оценку для идентификации и полуколичественное определение
действующих веществ в ЛС методом тонкослойной хроматографии.
Если ЛС не отвечают этим требованиям, то они являются субстандартными ЛС
или ФЛС. После этого переходят к полному анализу по регистрационному досье в
уполномоченных лабораториях высокого уровня. Следует отметить, что иногда
сложно выявить разницу между субстандартными ЛС и ФЛС. Но, с точки зрения
защиты потребителя, это неважно.
Другим общим подходом для решения проблемы фальсификатов ЛС первой группы
является разработка монографий на готовые ЛС.
Для производства ЛС второй группы не требуется сложное оборудование, и
поэтому они довольно легко могут быть фальсифицированы. К этой группе относятся
такие лекарственные формы, как масла (в частности масло облепиховое и масло
тыквы), фасованное лекарственное растительное сырье, экстракты, сборы и т.д.
Появление фальсификатов на эти препараты в значительной степени связано с
отсутствием в ГФ монографий современного уровня [6].
По данным ВОЗ распространенность фальсифицированных лекарственных средств
по странам и терапевтическим группам можно представить следующим образом.
На развивающиеся страны приходится около 70% оборота всех поддельных
лекарств, на развитые - около 30%.
По терапевтическим группам:
противомикробные средства 28%,
гормональные средства 22% (включая стероиды 10%),
спазмолитические средства 18%,
противогистаминные средства 17%,
сосудорасширяющие средства 7%,
средства, применяемые при сексуальных расстройствах 5%,
противосудорожные средства 2%,
другие лекарственные средства 19%.
Чрезвычайно сложным представляется определение фальсификата лишь методом
визуальной оценки, а также простыми тестами на распадаемость или только с
помощью простых цветных реакций, которые позволяют выявить лишь грубые
подделки. В последнее время отмечается все более высокий уровень изготовления
фальсифицированных лекарств, и часто даже специалисту сложно только по внешним
признакам упаковки и самого препарата (например, внешний вид таблеток) отличить
подделку от оригинала.
В связи с этим необходима реализация схемы комбинированной оценки
препаратов, которая позволит выявлять фальсификаты с достаточно высокой
степенью достоверности при минимальных затратах времени и средств [1,7].
ВОЗ рекомендует в качестве основных методов исследование внешнего вида,
определение температуры плавления и простые качественные реакции.
В США специалистами Food and Drug Administration (FDA) было подготовлено
руководство по анализу наиболее важных и распространенных лекарственных средств
с использованием метода ТСХ.
В Германии для анализа поддельных лекарств предлагаются исследование
внешнего вида, упрощенный вариант теста на распадаемость, химические реакции и
ТСХ. Изготавливается соответствующий тест-набор - GPHF-MINILAB®.
Министерство здравоохранения и социального обеспечения Японии также
предлагает проводить исследование внешнего вида, химические реакции и ТСХ [1,
8].
На основании рекомендаций ВОЗ и опыта зарубежных специалистов коллектив
авторов кафедры фармацевтической химии ММА им. И.М. Сеченова предлагает
следующий подход.
В анализе поддельных препаратов, не содержащих действующие вещества,
указанные на этикетке, и содержащих действующие вещества, не указанные на
этикетке, основное значение должно придаваться хорошо зарекомендовавшим себя
методам установления подлинности. К ним, в первую очередь, относятся:
ТСХ: сравнение со свидетелем,
ИК спектроскопия в области 4000 - 400 см-1 (сравнение со
стандартным ИК-спектром).
Предполагается, что для осуществления данного подхода возможно создание
соответствующего тест-набора, с помощью которого как в стационарных, так и в
полевых условиях можно осуществлять скрининг подозрительных лекарственных
препаратов с применением качественных реакций и ТСХ.
Сочетание простых аналитических реакций, которые можно проводить на
фильтровальной бумаге или в выпарительной чашке, и метода ТСХ в большинстве
случаев (но не всегда) позволяет установить наличие или отсутствие в препарате
действующего вещества.
Предлагается также использовать метод ИК-спектроскопии - сравнение со
стандартным спектром. Данный метод не является экспрессным и не позволяет проводить
анализ в походных условиях, однако с его помощью можно практически однозначно
установить подлинность лекарственного средства. Причем анализировать можно не
только субстанции, как это принято в фармакопейном анализе, но и лекарственные
препараты.
Показано, что при достаточно большом содержании действующего вещества в
лекарственной форме «таблетки» (30 - 40% и более) можно получать ИК-спектр, на
котором достаточно четко видны практически все полосы поглощения активной
субстанции. Мешающее влияние вспомогательных веществ на спектре отсутствует. В
некоторых случаях вспомогательные вещества вместе с активной субстанцией
позволяют получать ИК-спектр, характерный для лекарственного препарата
конкретного производителя. Например, на рис. 1-3 представлены ИК-спектры
субстанции норфлоксацина и таблеток, содержащих данное действующее вещество.
Причем ИК-спектры препаратов разных производителей различаются (рис. 2 и 3)
между собой (набор слабых полос с частотами около 2361, 2346 и 2334 см-1
соответствует колебаниям присутствующего в атмосфере углекислого газа и не
включается в интерпретацию) [7,8,9].

Рис. 1. ИК-спектр субстанции норфлоксацина в вазелиновом масле
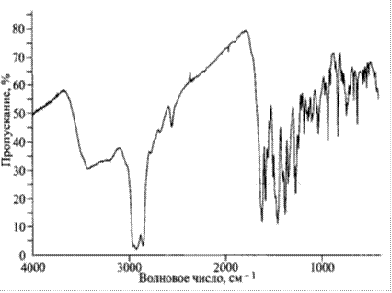
Рис. 2. ИК-спектр таблеток Нолицин 400 мг (KRKA, Словения) в вазелиновом масле
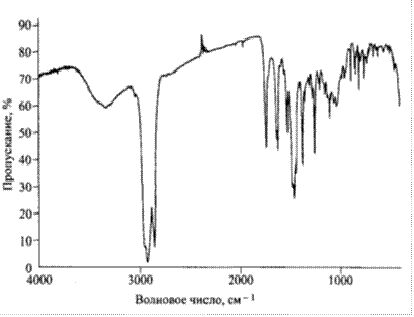
Рис. 3. ИК-спектр таблеток Норилет 200 и 400 мг (Dr. Reddy,s Ltd, Индия) в вазелиновом масле
Для анализа фальсифицированных препаратов, содержащих действующие
вещества, указанные на этикетке, но изготовленных другим производителем - не
тем, который указан на этикетке, необходимо использовать:
приоритетные методы анализа чистоты,
биофармацевтические методы - тест «растворение».
Наиболее важными методами анализа чистоты лекарственных субстанций и
препаратов в фармацевтическом анализе являются высокоэффективная жидкостная
хроматография (ВЭЖХ) и газожидкостная хроматография (ГЖХ). Поскольку при
производстве поддельных лекарств обычно используются более дешевые субстанции,
то по составу примесей (родственные соединения, остаточные органические
растворители) можно не только установить факт подделки, но и определить
происхождение фальсифицированного препарата. Более того, данные методы
позволяют устанавливать подлинность действующего вещества и проводить его
количественное определение [8].
Тест «растворение» в настоящее время активно используется в фармакопейном
анализе. Однако общая фармакопейная статья (ОФС) регламентирует анализ только
по одной точке: если другое не оговорено в документе на конкретный препарат,
требуется, чтобы через 45 мин после начала испытания в раствор перешло не менее
70% действующего вещества. Поэтому гораздо более важным является получение
кривых растворения. При этом отбор проб следует начинать уже через 5 мин после
начала испытания и строить профиль высвобождения необходимо как минимум по 6
временным точкам. На таких графиках основные различия для препаратов с
немодифицированным высвобождением обычно наблюдаются в первые 30 мин теста
[4,7].
Методы ВЭЖХ, ГЖХ, тест «растворение» так же, как и ИК-спектро-скопический
анализ, необходимо проводить в лабораторных условиях. Однако в некоторых
случаях только эти методы могут позволить выявить грамотно сделанные подделки.
Необходимо также отметить, что экспресс-анализ позволяет проводить только
первичный скрининг лекарственных препаратов. Он не заменяет фармакопейный
анализ, а дополняет его. Достаточно сложно проводить все испытания по
нормативной документации каждый раз, когда необходимо удостовериться в подлинности
препарата. Однако, если экспресс-методы вызывают сомнения в происхождении того
или иного средства, необходим полный анализ последнего по соответствующей
нормативной документации [1,8].
. Общая характеристика группы спазмолитических средств
Препараты, относящиеся к группе спазмолитиков, являются одними из самых
востребованных и назначаемых врачами различных специальностей. Дисфункция
гладкомышечных клеток внутренних органов лежит в основе как хронического, так и
острого болевого синдрома, при различных заболеваниях органов пищеварения,
мочевыводящей системы органов малого таза. Наиболее частой причиной развития
боли при патологии внутренних органов, имеющих слой гладкомышечных клеток,
является их избыточное сокращение. Симптомы спастической дисфункции органов
пищеварения встречаются в 30% случаев при отсутствии органического поражения
желудка или кишечника, что обусловливает частое самостоятельное (без врачебного
назначения) применение спазмолитических препаратов [10].
Спазмолитики могут классифицироваться по механизму действия, по
происхождению.
I. По механизму действия:
1. Нейротропные спазмолитики (М-холиноблокаторы).
А) Неселективные - атропина сульфат, платифиллин, скополамин,
гиосциламин, препараты красавки.
Б) Селективные - гиосцина бутилбромид (Бускопан).
. Миотропные спазмолитики.
А) Селективные (ингибиторы фосфодиэстеразы):
производные изохинолина (папаверин, дротаверин);
производные ксантина (теофиллин, эуфиллин);
разные (бенциклан, пинаверия бромид, адифенин, арпенал и др.).
Б) Неселективные.
Ингибиторы кальциевых каналов:
производные фениланиламина (верапамил);
производные бензотиазепина (дилтиазем);
производные дигидропиридина (нифедипин, нитрендипин).
Активаторы калиевых каналов (миноксидил, диазоксид).
Донаторы оксида азота (нитропруссид натрия, нитроглицерин и др.).
II. По происхождению:
1. Природные спазмолитики - любисток аптечный, красавка, ромашка, душица
обыкновенная, аир болотный, ортосифон (почечный чай), ландыш майский, белена
черная, пижма обыкновенная, трава чернобыльника, мята.
. Искусственные лекарственные препараты синтетического происхождения.
Нейротропные спазмолитики - воздействуют на процесс передачи нервных
импульсов в нервы, стимулирующие гладкую мускулатуру того или иного внутреннего
органа.
Миотропные спазмолитики - оказывают действие непосредственно на клетки
гладких мышц, меняя происходящие внутри них биохимические процессы.
Общепринятой систематизации спазмолитиков нет. Существует несколько
классификаций: по механизму действия; по происхождению и др. В контроле качества
таких препаратов важное значение имеет их химическая классификация.
Спазмолитическим действием обладают соединения различной химической структуры.
В таблице 1 приведена химическая классификация спазмолитических средств
[10,11].
Табл. 1. Классификация спазмолитиков по химической структуре
|
Русское и латинское название
|
Химическое название
|
Формула
|
|
Атропин Atropinum
|
8-Метил-8-азабицикло [3.2.1] окт-3-иловый эфир
эндо-(±)-альфа-(гидроксиметил) бензолуксусной кислоты
|
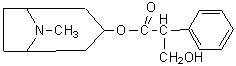
|
|
Папаверин Papaverinum
|
1-[(3,4-Диметокси-фенил)метил]-6,7-диметоксиизохинолин (в
виде гидрохлорида)
|

|
|
Платифиллин Platyphyllinum
|
3-Этилиден-6-гидрокси-5,6-диметилпергидро-1,8-диоксациклододека
[2,3,4] пирролизин-2,7-дион
|

|
|
Гиосцина бутилбромид Hyoscini butylbromidum
|
[7(S)-(1альфа,2бета,4бета, 5альфа,
7бета)]-9-Бутил-7-(3-гидрокси -1-оксо-
2-фенилпропокси)-9-метил-3-окса-9-азониятрицикло [3.3.1.02,4]нонана бромид
|

|
|
Дротаверин Drotaverinum
|
1-[3,4-Диэтоксифенил)метилен]-6,7-диэтокси-1,2,3,4-тетрагидроизохинолин
(в виде гидрохлорида)
|
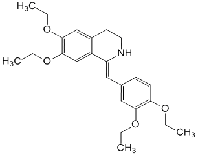
|
|
Бендазол Bendazolum
|
2-(Фенилметил)-1H-бензимидазол
|
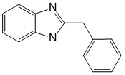
|
|
Бенциклан Bencyclanum
|
N,N-Диметил-3-[[1-(фенилметил) циклогептил]
окси]-1-пропанамин (в виде фумарата)
|
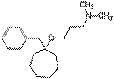
|
|
Отилония бромид Otilonii bromidum
|
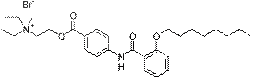
|
|
Пинаверия бромид Pinaverii bromidum
|
4-[(2-Бром-4,5-диметоксифенил)метил]-4-[2-[2-(6,6-диметилбицикло
[3.1.1]гепт-2-ил)этокси]этил] морфолиния бромид
|
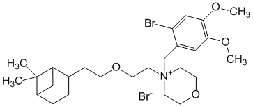
|
|
Нитроглицерин Nitroglycerinum
|
1,2,3-Пропантриола тринитрат
|
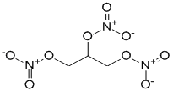
|
К лекарственным веществам изохинолинового ряда относятся такие известные
спазмолитики, как опиумный алкалоид папаверин и его синтетический аналог но-шпа.
Их назначают при стенокардии, спазмах желудка, кишечника, бронхов,
периферических сосудов и сосудов головного мозга. Папаверин был выделен в 1884
г из млечного сока незрелых плодов мака (опия), где он содержится в количестве
до 1%. К этому же химическому классу соединений принадлежит алкалоид яда кураре
тубокурарин, который в медицине нашел безопасное применение в качестве
миорелаксанта, вызывающего длительное расслабление скелетной мускулатуры при
операциях под наркозом.
Спазмолитические средства используют для лечения сердечно-сосудистых,
желудочно-кишечных, бронхолегочных, урологических и др. заболеваний как
самостоятельно, так и в комбинациях между собой и с другими препаратами [10].
3. Аналитические подходы выявления фальсифицированных средств группы
спазмолитиков на примере дротаверина гидрохлорида
На фармацевтическом рынке Центрального и Северо-Западного регионов на
сегодняшний день представлено по меньшей мере 25 торговых наименований
препаратов дротаверина гидрохлорида, выпускаемых преимущественно в форме
таблеток и растворов для инъекций [3].
Из литературных источников, посвященных данной проблеме, наибольший
интерес представляются исследования ряда авторов (Буданцев Л.А., Саканян Е.И.),
касающиеся разработки аналитических методик выявления некоторых
фальсифицированных спазмолитических средств на примере дротаверина
гидрохлорида. Эта группа исследователей предлагает применять такие методы как
ИК-спектроскопия, тонкослойная хроматография, а также высокоэффективная
жидкостная хроматография для установления подлинности субстанции и
лекарственных форм дротаверина [3, 12].
Особое внимание уделяется тому, что эти методы можно применять в
комплексе и в качестве экспресс-методов для быстрого и достоверного выявления
поддельных препаратов из группы спазмолитических средств.
При исследовании стандартов качества субстанций дротаверина гидрохлорида
показано то, что наблюдается отсутствие единых подходов к анализу лекарственных
средств даже в пределах одной лекарственной формы, что приводит к затруднениям
при выявлении их фальсификата. Установлено, что в ряде случаев используемые
методы оценки качества субстанций и препаратов дротаверина гидрохлорида
обладают недостаточной специфичностью, что показано на примере модельной смеси
дротаверина гидрохлорида и папаверина гидрохлорида, обладающего родственным
химическим строением.
В соответствии с этим, выполнены исследования по разработке комплексных
унифицированных методик оценки качества субстанции и препаратов дротаверина
гидрохлорида, позволяющих выявить их фальсификат.
В ходе идентификации субстанций установлено, что ИК-спектры, снятые в
диске калия бромида в диапазоне волновых чисел 4000-400 см-1, имеют
характерные для структуры дротаверина гидрохлорида полосы поглощения.
Разработанная методика позволяет использовать метод ИК-спектроскопии для
идентификации таблеток и растворов для инъекций независимо от их производителя
[9, 12, 13].
Проведение метода тонкослойной хроматографии (ТСХ) с использованием
системы растворителей ацетон : этанол : кислота уксусная ледяная (20:10:0,1)
позволяет провести идентификацию дротаверина гидрохлорида как в субстанции, так
и в таблетках (рис. 4). Данная методика может быть использована в качестве
экспресс-метода установления подлинности субстанции и препаратов дротаверина
гидрохлорида и их чистоты [14].
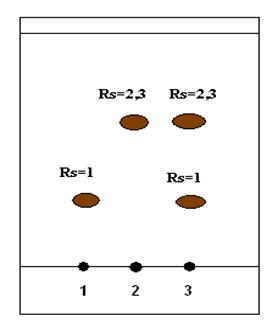
Рис. 4. Хроматограмма растворов дротаверина гидрохлорида и папаверина
гидрохлорида. Условные обозначения: 1-дротаверина гидрохлорид (Rf=0,27), 2 - папаверина гидрохлорид (Rf=0,62), 3- смесь растворов
дротаверина гидрохлорида и папаверина гидрохлорида
Помимо идентификации, данный метод также пригоден для оценки наличия
посторонних примесей в анализируемом объекте.
Разработанная методика ВЭЖХ (подвижная фаза - ацетонитрил : раствор калия
дигидрофосфата в соотношении 4 : 6 с рН 5,5; температура колонки 40°С; детектор
241 нм) позволяет надежно идентифицировать дротаверина гидрохлорид в субстанции
и лекарственных формах (рис. 5). Параметры полученных пиков, представленные в
табл. 2, могут свидетельствовать о достоверном разделении исследуемых веществ.
На основании данного метода разработана методика оценки количественного
содержания действующего компонента в исследуемых объектах. Использовались те же
условия, применяемые для идентификации субстанций и препаратов дротаверина
гидрохлорида.
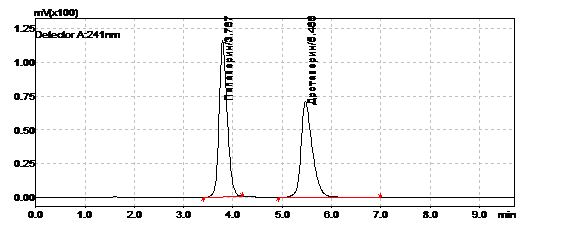
Рис. 5. ВЭЖХ-хроматограмма раствора смеси дротаверина гидрохлорида и
папаверина гидрохлорида (200 мкг/мл в ПФ)
Расчет концентрации проводится с применением внешнего стандарта и сравнением
площадей главных пиков испытуемого раствора и раствора стандартного образца.
Табл. 2. Параметры пиков дротаверина гидрохлорида и папаверина
гидрохлорида (метод ВЭЖХ)
|
Время удерживания, мин
|
Фактор асимметрии
|
Эффективность колонки, т. т.
|
Разрешение
|
Наименование
|
|
3,787
|
1,238
|
2521,976
|
4,695
|
папаверин
|
|
5,466
|
1,391
|
2789,908
|
|
дротаверин
|
Относительная погрешность методики при проведении опытов с добавками
дротаверина гидрохлорида имеет отклонения в сторону как положительных, так и
отрицательных значений, что свидетельствует об отсутствии систематической
ошибки. Результаты на примере оценки количественного содержания субстанции
дротаверина гидрохлорида представлены в табл. 3.
Табл. 3. Результаты опытов с добавками дротаверина гидрохлорида для
методики количественного определения субстанции дротаверина гидрохлорида
|
№ п/п
|
Взято субстанции, г
|
Добавлено субстанции, г
|
Должно быть, г
|
Найдено, г
|
Абсолютное отклонение
|
Относительная погрешность, %
|
|
1
|
0,01969
|
0,005507
|
0,02520
|
0,02418
|
-0,00102
|
4,05
|
|
2
|
0,02065
|
0,01240
|
0,03305
|
0,03334
|
+0,00029
|
0,88
|
|
3
|
0,02058
|
0,01541
|
0,03599
|
0,03482
|
-0,00117
|
3,25
|
0,01974
|
0,02047
|
0,04021
|
0,04215
|
+0,00194
|
4,82
|
Аналогичные результаты получены при испытании таблеток и растворов для
инъекций [3, 15].
Для идентификации изохинолиновых алкалоидов предложены различные
хроматографические методики.
Установлено, что для определения примесей в лекарственных формах,
содержащих производные изохинолина, обычно используются хроматографические
методы - ТСХ и ВЭЖХ.
Сравнительный анализ имеющихся условий определения посторонних примесей
дротаверина гидрохлорида методом ТСХ, включенных в действующие НД, показал,
что:
анализ, как правило, проводится на пластинах Kieselgel F254
(предварительно активированных или неактивированных).
оценка результатов проводится в ультрафиолетовом свете при длинах волн
254 нм (фиолетовые пятна на желтовато-зеленоватом фоне), редко - при 366 нм
(пятна голубого цвета на темном фоне), очень редко - с использованием
модифицированного реактива Драгендорфа и 0,05М раствора серной кислоты.
используется около десятка подвижных фаз, включающих в себя такие
растворители, как татрагидрофурaн, этилацетат, спирты, амины, органические
кислоты, бензол и его гомологи, хлороформ, н-гексан и др. В одном НД
предусмотрено последовательное хроматографирование в 2-х подвижных фазах.
в качестве растворителей проб используется хлороформ, метанол, буферные
растворы с различным рН
в роли вещества свидетеля, как правило, используется дротаверин, редко -
дротавералдин (основной продукт окисления)
Для выбора оптимальных условий оценки содержания примесей в дротаверина
гидрохлориде методом ТСХ нами было изучено хроматографическое поведение
дротаверина в следующих подвижных фазах:
. бензол-спирт метиловый-концентрированный раствор аммиака (40:8:0.1);
. ксилол- метилэтилкетон- спирт метиловый- диэтиламин (20:20:3:1);
. дихлорэтан- спирт метиловый-ацетон-диэтиламин (80:10:5:5);
. бензол-спирт метиловый-раствор аммиака концентрированный (20:4:0,1).
Оптимальной оказалась подвижная фаза: бензол, спирт метиловый, раствор
аммиака концентрированный - 20:4:0,1.
В качестве базового растворителя проб использован хлороформ, поскольку
дротаверина гидрохлорид в нем легко растворим, а возможность его гидролиза в
данном случае минимальна.
Изучено влияние активирования пластин на результат хроматографирования.
Экспериментально установлено, что активирование пластин в течение 1 часа при
110оС не оказывает существенного влияния на характер хроматограммы,
поскольку расположение пятен дротаверина и примесей на активированных и
неактивированных пластинах практически ничем не отличается.
Выбран способ детектирования и вещество-свидетель. В качестве вещества
свидетеля был использован непосредственно дротаверин, так как в РФ стандарты
дротавералдина, либо других известных примесей дротаверина не являются широко
доступными, а чувствительность определения как для основного, так и для
примесных веществ составляет 0,25 мкг. Для детектирования был выбран наиболее
распространенный способ - оценка в ультрафиолетовом свете при 254 нм.
Для определения посторонних примесей в комбинированном препарате «СПАЛГИН
форте» в качестве основной выбрана подвижная фаза: бензол, спирт метиловый,
раствор аммиака концентрированный - 20:4:0,1, которая, как показано выше,
пригодна для определения содержания примесей как дротаверина гидрохлорида, так
и анальгина.
В качестве растворителя использовали хлороформ (применяемый в анализе
посторонних примесей каждого индивидуального компонента препарата).
Однако в процессе исследований было отмечено, что присутствие дротаверина
гидрохлорида улучшает растворимость анальгина в хлороформе. Хроматографирование
хлороформного экстракта модельной смеси таблеток СПАЛГИН форте показало, что
дротаверина гидрохлорид частично разрушается в растворе. Этот факт, вероятно,
обусловлен влиянием анальгина.
С целью устранения описанного выше взаимного влияния компонентов
рассмотрены различные способы обработки хлороформа и получения хлороформных
растворов исследуемого препарата.
Использование безводного хлороформа не оказало существенного влияния на
результаты хроматографирования - вид хроматограмм, полученных при применении
коммерческого и безводного хлороформа одинаков; в случае использования
хлороформа, насыщенного аммиаком, либо раствором сульфита натрия, общий вид
хроматограммы также не изменяется.
При извлечении модельных смесей анальгина и дротаверина гидрохлорида в
хлороформ из водного раствора с рН 8-9 результаты были сопоставимы с
полученными при растворении непосредственно в хлороформе, но при этом
интенсивность пятна примеси с Rf 0,58 (дротавералдин) несколько снизилась.
Оптимальные результаты были получены после обработки хлороформа раствором
натрия гидроксида и натрия сульфитом.
Двумерное хроматографирование смеси анальгина и дротаверина гидрохлорида
в выбранных условиях показало, что в процессе хроматографирования не происходит
разрушения соединений. В результате первого хроматографирования отмечен рост
интенсивности пятна примеси дротаверина гидрохлорида с Rf 0,58 (дротавералдин)
по сравнению с аналогичным на хроматограмме дротаверина гидрохлорида в чистом
виде, при последующем хроматографировании в перпендикулярном направлении
образования подобного пятна не наблюдалось, то есть, качественный и
количественный состав примесей не меняется.
В качестве веществ-свидетелей выбраны дротаверин и 4-аминоантипирин, что
обусловлено результатами исследования по определению чувствительности
обнаружения соединений и, кроме того, доступностью указанных веществ, о чем
говорилось ранее.
Типичная хроматограмма, полученная в выбранных условиях представлена на
рисунке 6.

Рис. 6. Хроматографическое разделение примесей анальгина и дротаверина
гидрохлорида: 1 - препарат «СПАЛГИН форте»; 2 - дротаверина гидрохлорид,
Rf=0,48; 3 - анальгин, Rf= 0,06; 4 - 4-аминоантипирин, Rf=0,21; 5 - антипирин,
Rf=0,24; 6 - 4-метиламиноантипирин, Rf=0,26; 7- дротавералдин, Rf=0,58.
На хроматограмме обнаружено несколько пятен незначительного размера и
интенсивности между пятнами анальгина и дротаверина (исключая примеси анальгина
- до шести, которые на рисунке не представлены).
Таким образом, разработанные методики позволяют при их проведении сделать
заключение об оригинальности субстанции и препаратов дротаверина гидрохлорида
[6,15].
Заключение
Распространение фальсифицированных лекарственных средств стало глобальной
проблемой. Это представляет серьезную угрозу для жизни и здоровья человека и
негативно влияет на экономику страны. Всемирная организация здравоохранения
считает, что «фальсифицированным (контрафактным) ЛС является продукт,
преднамеренно и противоправно снабженный этикеткой, неверно указывающей
подлинность препарата и (или) изготовителя» [16].
Поэтому актуальной задачей является контроль за всеми этапами
производства лекарственного препарата от производителя к покупателю, а также
разработка унифицированных, доступных и быстрых аналитических методов выявления
фальсифицированных лекарств [2].
В настоящей работе тема, связанная с современными аналитическими
подходами по выявлению фальсифицированных лекарственных препаратов группы
спазмолитиков наиболее полно раскрыта. Основные задачи для раскрытия темы
работы выполнены, а именно:
изучены литературные источники, посвященные общим вопросам выявления
фальсифицированных лекарственных средств современными аналитическими методами,
а также более подробно рассмотрены среди них препараты из группы спазмолитиков;
приведена общая характеристика, включающую в себя классификацию по
химической структуре группы спазмолитических средств;
изучены и охарактеризовать аналитические методики определения
фальсификатов из группы спазмолитических средств на примере дротаверина
гидрохлорида.
выявлен наиболее приемлемый и современный аналитический подход для
определения фальсификатов, а именно комплексное применение тонкослойной
хроматографии, ИК-спектроскопии, а также высокоэффективной жидкостной
хроматографии для контроля качества спазмолитических средств.
Список использованной литературы
1. Арзамасцев А.П. Выявление фальсифицированных
лекарственных средств с использованием современных аналитических методов / А.П.
Арзамасцев, В.Л. Дорофеев, А.А. Коновалов // Химико-фармацевтический журнал. -
2004. - № 3. - С. 48 - 51.
2. Сафиуллин Р.С. Фальсифицированные лекарственные
средства - мировая проблема [Текст] / Р.С. Сафиуллин, К.А. Миннекеева, Д.Х.
Шакирова // Казанский медицинский журнал. - 2006. - №6. - Т.87. - С.462-466.
. Буданцев Л.А. Разработка методик анализа для
выявления фальсифицированных лекарственных средств: автореф. дисс. на соиск.
учен. степ. к. фарм. наук: 14.04.01/ Л.А. Буданцев; ВИЛАР РАСХН. М., 2011 - 24
с.
. Беликов В.Г. Фармацевтическая химия. В 2 ч. / В.Г.
Беликов. - Пятигорск, 2003. - 720 с.
5. Препьялов А.Г. Фальсифицированные лекарственные средства
на рынке Российской Федерации / А.Г. Препьялов // Ремедиум. - 2006. - №3. - С.
34-40.
6. Гризодуб
А.И. Проблемы качества и фальсификации лекарственных средств / А.И. Гризодуб //
Аптека. - 2007. - № 20. - С. 23-27.
7. Государственная фармакопея Российской Федерации XII
издание, часть 1 - М.: Издательство «Научный центр экспертизы средств медицинского
применения», 2008. - 704 с.
. Арзамасцев А.П., Дорофеев В.Л., Коновалов А.А., Кочин
В.Ю., Лебедева Н.Н., Титов И.В. Экспресс-анализ с целью выявления
фальсифицированных лекарственных средств // Пути и формы совершенствования
фарм. образования: матер. Межрегион. Научно-методич. Конф. Фармобразование -
2003. - Воронеж, 2003. - С. 20 - 23.
9. Арзамасцев А.П., Яскина Д.С. Ультрафиолетовые и
инфракрасные спектры лекарственных веществ. М.: «Медицина», 1975. - 151 с.
10. Пчелинцев М.В. Спазмолитики: от клинической фармакологии
до фармакотерапии [Текст] / М.В. Пчелинцев // Лечащий врач. - 2008. - №7.
-С.12-16.
11. Машковский М.Д. Лекарственные средства. Пособие для
врачей / М.Д. Машковский. - М.: Новая волна, 2005. - 1206 с.
. Буданцев Л.А., Воллосович Н.Е., Саканян Е.И.
Современное состояние качества лекарственных средств, представленных на
фармацевтическом рынке Санкт-Петербурга // Сборник материалов II Всероссийского съезда
фармацевтических работников, Сочи 4 - 8 июня 2005 г. - С. 57-59.
. Макаренко Т.Ф., Воронова Н.В. Использование
инфракрасной спектрофотометрии для определения но-шпы в трупном материале
//Судебно-медицинская экспертиза 1984 - 27, № 2 - С.53-54.
. Буданцев Л.А., Саканян Е.И. Разработка методик анализа
субстанции и препаратов дротаверина гидрохлорида, позволяющих выявить
фальсификат // Разработка, исследование и маркетинг новой фармацевтической
продукции: сб. науч. тр. / Пятигорская гос. фарм. акад. - Пятигорск, 2008. -
Вып. 63. - С. 220 - 221.
15. Буданцев Л.А., Саканян Е.И. Применение
УФ-спектрофотометрических методов анализа с целью выявления фальсифицированных
лекарственных средств // Достижения, проблемы и перспективы фармацевтической
науки и практики: мат. научно-практ. конф. Под ред. А.И. Лазарева / Курский
гос. мед. ун-т, Курск. - 2006. - С. 200 - 202.
16. Косенко В.В. Фальсифицированные лекарства - глобальная
проблема /В.В. Косенко, А.В. Быков, А.П. Мешковский // Вестник Росздравнадзора.
- 2009. - № 3.- С.14-26.