Растительные источники витаминов: стандартизация и медицинское применение
Министерство здравоохранения
Российской Федерации
Государственное бюджетное
образовательное учреждение высшего профессионального образования
ПЕРВЫЙ МОСКОВСКИЙ ГОСУДАРСТВЕННЫЙ
МЕДИЦИНСКИЙ УНИВЕРСИТЕТ имени
И.М.СЕЧЕНОВА
Факультет фармацевтический Кафедра фармакогнозии
Алексеева
Ирина Владимировна
Студентка 5
курса 12 группы
Растительные
источники витаминов: стандартизация и медицинское применение
КВАЛИФИКАЦИОННАЯ РАБОТА
по
специальности 060108 «Фармация»
квалификация
провизор
МОСКВА
РАБОТА ВЫПОЛНЕНА НА БАЗЕ:
КАФЕДРА ФАРМАКОГНОЗИИ ГБОУ ВПО ПЕРВЫЙ МГМУ им.
И.М.СЕЧЕНОВА
НАУЧНЫЙ РУКОВОДИТЕЛЬ ОТ КАФЕДРЫ ОРГАНИЗАЦИИ И
ЭКОНОМИКИ ФАРМАЦИИ:
Доцент, кандидат фармацевтических наук /Сергунова
Е.В./ Исполнитель /Алексеева И.В./
СОДЕРЖАНИЕ
Введение
. Ботанико-морфологическая характеристика лекарственных
растений, содержащих витамины
. Химический состав сырья
. Медицинское применение
. Анализ сырья
.1 Внешние признаки
.2 Микроскопия
.3 Качественный анализ
.4 Числовые показатели
.5 Количественное определение
Заключение
Список литературы
Введение
Витамины - органические вещества различной химической
природы, не образующиеся в достаточном количестве клетками человеческого
организма, но необходимые для его нормальной жизнедеятельности. Витамины
проявляют биологическую активность в очень малых концентрациях. Они выполняют
функции регуляторов обмена веществ. Большинство витаминов входит в состав
ферментов, являясь их коферментами. [2]
Приоритет открытия витаминов принадлежит русскому
врачу Николаю Ивановичу Лунину. В 1880 г. Н.И. Лунин писал, что в пище, кроме
«казеина, жира, молочного сахара и солей, содержатся еще другие вещества,
незаменимые для питания». Термин «витамины» был предложен польским ученым
Казимиром Функом в 1912 году от лат. «vita» - «жизнь», т.е. дословно термин означает «амины жизни».
Недостаток витаминов нарушает обмен веществ, снижает
работоспособность, вызывает быструю утомляемость, ухудшает состояние нервной
системы и вызывает другие болезненные явления.
Витамины группы К участвуют в свертывании крови,
индуцируя образование протромбина (антигеморрагический фактор). Недостаток
вызывает замедление свертывания крови и кровоизлияния. Аскорбиновая кислота
участвует в окислительно-восстановительных реакциях, в том числе в липидном и
пигментном обмене, активирует протромбин, обладает десенсибилизирующем
действием, поднимает жизненный тонус организма и повышает сопротивляемость к
экстремальным воздействиям. Недостаток витамина С вызывает цингу, или скорбут
(рыхлость десен, выпадение зубов, кровоизлияния). Витамин А (ретинол)
способствует нормализации обмена веществ, росту и развитию организма,
регенерации тканей, обеспечивает нормальную деятельность органов зрения.
Недостаток вызывает ухудшение сумеречного зрения («куриную слепоту»), сухость
роговицы, поражение слизистых.
Витамины содержатся во всех растениях, но
витаминосодержащими называют только те растения, которые избирательно
накапливают витамины в дозах, способных оказать выраженный фармакологический
эффект. Это в 500-1000 раз больше, чем в других растениях.
В настоящее время практически все витамины получают
синтетическим путем. Однако витаминосодержащие лекарственные растения не
утратили своего значения. Они широко используются, особенно в педиатрии, в
гериатрии и для лечения лиц, склонных к аллергическим заболеваниям, поскольку:
· во-первых, витамины в лекарственном
растительном сырье находятся в комплексе с полисахаридами, сапонинами,
флавоноидами, поэтому такие витамины легче усваиваются;
· во-вторых, растительные витамины реже
дают аллергические реакции, чем их синтетические аналоги;
· в-третьих, в организме человека есть
специальные системы защиты от передозировки витаминов (например, каротин в
организме человека превращается в витамин А по мере необходимости). [9]
Целью данной работы является обобщение и углубление теоретических знаний
по лекарственным растениям, содержащих витамины. В качестве лекарственного
растительного сырья будут изучены листья крапивы (витамин K), плоды шиповника (аскорбиновая
кислота), цветки ноготков (каротиноиды).
Реализация данной цели предполагает постановку следующих задач:
- рассмотрение ботанико-морфологической характеристики лекарственных
растений, содержащих витамины;
- исследование химического состава, анализ лекарственного растительного
сырья;
- медицинское применение, лекарственные препараты анализируемого сырья.
1. Ботанико-морфологическая
характеристика лекарственных растений, содержащих витамины
Крапива двудомная
Растение. Крапива двудомная - Urtica dioica L.,
семейство крапивные - Urticaceae.
Многолетнее травянистое двудомное растение, сплошь
усаженное жгучими волосками. Стебли прямостоячие, четырехгранные, неветвистые,
высотой 60-170 см. Листья черешковые, супротивные, яйцевидно-ланцетные. Цветки
мелкие, зеленые, однополые, собранные в облиственный тирс. Плод - семянка,
заключенная в остающийся околоцветник. Цветет все лето. Повсеместно
встречающееся растение. Произрастает у жилья, по оврагам и берегам рек, на
лесных вырубках, в основном как рудеральный сорняк. Часто встречается большими
зарослями на заброшенных стойбищах скота. Произрастает по всей России, кроме
Крайнего Севера.
Лекарственное сырье. Листья крапивы - folia Urticae заготавливают во время цветения (май - июль). Для
этого траву скашивают или срезают, после подвяливания обрывают листья. Листья
яйцевидно-ланцетные, шершавоволосистые, заостренные, по краям остро- и
крупнопильчатые, длинной до 20 см. ГФ XI предусматривает цельное и измельченное сырье. [14]
Недопустимыми к заготовке видами считаются крапива
жгучая и крапива коноплевая. Крапива жгучая (Urtica urens L.) - сорное и рудеральное однолетнее, однодомное растение
высотой 40-50 см. Листья эллиптические или яйцевидные длиной 4-5 см, с
округло-клиновидным основанием. Крапива коноплевая (Urtica cannabina L.) - многолетнее травянистое растение высотой 50-150 см.
Листья глубоко 3-5-рассеченные с перистозубчатыми надрезами.
Очень похожи на листья крапивы двудомной, но не имеют
жгучих волосков, листья яснотки белой, или глухой крапивы (Lamium album L.), растение из семейства губоцветных - Lamiaceae. Цветки у яснотки обоеполые, белые,
с двугубым венчиком длиной 2 см. [15]
Отличительные признаки крапивы двудомной от возможных
примесей представлены в таблице 1.
Таблица 1. Отличительные признаки крапивы двудомной от возможных
примесей.
|
Название растения
|
Опушение
|
Листья
|
Соцветия
|
|
Крапива двудомная - Urtica dioica
|
Рассеянное, из простых и
жгучих волосков
|
Яйцевидные или
продол-говато-ланцетовидные, с длинной заостренной верхушкой и сердцевидным
округлым основанием, крупнопильчатые, длиной 10-12 (17) см, шириной 5-7 см
|
Колосовидные, повислые,
пазушные, длинней или равны черешкам листьев, прижатоволосистые
|
|
Крапива жгучая - Urtica urens
|
Густое, из жгучих волосков
|
Эллиптические или
яйцевидные, с острой верхушкой и округло-клиновидным основанием, с глубоко
надрезанными тупыми, прямыми зубцами, длиной до 4-5 см, шириной 1,5-3,5 см
|
Колосовидные, не превышают
длину черешка листьев, в пазухах которых они сидят
|
|
Крапива конопляная - Urtica cannabina
|
Редкое из простых и жгучих
волосков, более обильное в узлах стеблей, по междо-узлиям иногда голое
|
Пальчато-раздельные,
черешковые, накрест супротивные (каждый сегмент, в свою очередь,
перисторассеченный с перистозубчатыми надрезами), до 16 см длиной. Первые 2-3
листа и листья пазушных побегов цельные, крупно-зубчатые
|
Соцветие ветвистое, густо
усаженное пучками цветов
|
|
Яснотка белая (крапива
глухая) - Lamium album
|
Густое, волоски не жгучие
|
Пазушные мутовки, цветки
двугубые, белые, обоеполые, длиной 2 см
|
[9, 10, 16]
Шиповник (роза), различные виды - род Rosa L.
Растения. Виды секции Cinnamomeae DC.: шиповник майский (коричный) - Rosa majalis Herrm. (r. cinnamomea L.), даурский - R. davurica Pall., Беггера - R. beggeriana Schrenk, иглистый - Rosa acicularis Lindl., морщинистый - R. rugosa Thunb., Федченко - R. fedtschencoana Regel.
Виды секции Caninae Crep.: шиповник
собачий - R. canina L., шиповник щитконосный - R. corymbifera Borkh. и некоторые другие виды шиповников;
семейство розоцветные - Rosaceae.
Все виды шиповника - кустарники, ветки - усажены
шипами и колючками. Листья очередные, непарноперистосложные с эллиптическими
или яйцевидными по краю пильчатыми листочками; прилистники , частично сросшиеся
с черешком. Цветки с ланцетными прицветниками, крупные - до 5 см в поперечнике,
одиночные или по 2-3 и более на концах ветвей. Чашелистиков - 5, они длиннее
венчика, вверху оттянуты в придатки или перистонадрезанные (секция Caninae). Лепестков 5, свободных, окрашенных
в розовый цвет; у шиповника Беггера и Федченко венчики белые. Тычинок и
пестиков много, последние находятся на внутренней стороне кувшинообразного
гипантия, завязи волосистые, столбики с рыльцами, выставляются из зева
гипантия. Плод - ягодообразный цинародий, сочный, образующийся из разросшегося
мясистого гипантия. Форма плода от шаровидной до эллиптической или яйцевидной
формы; он снаружи гладкий, голый, реже железистоопушенный, мясистый, от
красно-оранжевого до темно-красного цвета. На верхушке плодов у видов секции Cinnamomea сохраняется чашечка из 5 вверх
направленных чашелистиков, у представителей секции Canina чашелистики опадают при созревании плодов, а на
верхушке остается пятиугольная площадка. Внутри плода много мелких
плодиков-орешков, неточно называемых семенами. Орешки угловатой формы, наверху
внутренняя поверхность плода усажена многочисленными длинными щетинистыми
волосками. Плоды созревают в августе - сентябре и остаются на кустах до зимы.
Используемые в медицине виды распространены по всей
европейской части СНГ и в Балтии, на Урале, в Сибири, Центральной Азии,
Казахстане, на Кавказе, российском Дальнем Востоке.
Отдельные виды различаются между собой следующими
признаками и районами произрастания.
Шиповник майский (ш. коричный) - Rosа majalis Herrm. (R. cinnamomea L.). Ветви блестящие, красно-коричневые. Цветоносные ветви
снабжены замкнутыми книзу шипами, расположенными попарно у основания черешка, а
листоносные побеги, кроме того, усажены игловидными тонкими прямыми шипиками
неравной длины. Листья снизу густо прижатоволосистые, придатки чашелистиков
ланцетные, плоды шиповника обычно шаровидные. Произрастает почти по всей
европейской части России, особенно на севере, а также в Западной и Восточной
Сибири до Байкала.
Шиповник даурский - Rosa davurica Pall. Ветви черно-пурпуровые. Шипы изогнутые,
оттопыренные, по 2 у основания ветвей, а на молодых ветках - у основания
черешков. Листочки снизу усажены мелкими желтыми железками и слабо опушены.
Придатки чашелистиков расширенные. Плоды шаровидные, диаметром 1,5-2 см.
Произрастает в южных районах Восточной Сибири и Дальнего Востока.
Шиповник иглистый - Rosa acicularis Lindl. Ветви буроватые, густо усажены
тонкими, прямыми равномерными игольчатыми щетинками, у основания листа часто по
2 тонких шипика, листочки почти голые. Придатки чашелистиков расширенные. Плоды
эллиптические, длиной 1,5-2,5 см.. Ареал обширный - от Тихого океана до
Санкт-Петербурга, но к западу от Онежского озера изреживается; южная граница
ареала проходи через Северный Казахстан, по Волге на запад и далее к Финскому
заливу.
Шиповник морщинистый - Rosa rugosa Thunb. Ветви
усажены многочисленными прямыми щетинками. Листочки эллиптические, толстые,
сильно морщинистые, сверху голые, снизу сероопушенные. Цветки одиночные или
собраны по 3-6, красные или темно-розовые. Плоды крупные, шаровидные,
ярко-красные, увенчанные вверхстоящими простыми чашелистиками. Растет на
Дальнем Востоке, Камчатке, Сахалине на песчаных почвах и по морским берегам.
Широко культивируется в европейской части РФ в садах и парках, где плоды и
заготавливаются.
Шиповник Беггера - Rosa beggeriana
Schrenk. Ветви
сизоватые. Шипы крупные, серповидные, при основании расширенные, желтоватые,
сидят попарно при основании листьев. Цветки в многоцветковых сложных щитках или
метелках. Чашелистики цельные, заостренные, после цветения прямостоячие. Плоды
мелкие, длиной 0,5-1,4 см, шаровидные, похожи на горошину, красные, по
созревании с опадающим диском и чашелистиками. В верхней части плода образуется
широкое отверстие, в котором видны плодики и волоски. Распространен в
Центральной Азии. Растет на горных склонах, по берегам рек и ручьев, на
опушках, у дорого. Разводится как декоративный кустарник и применяется для
живых изгородей.
Шиповник Федченко - Rosa fedtschenkoana Regel. Высокий кустарник высотой до 6 м с голыми ветвями.
Шипы крупные, прямые, твердые, к основанию сильно расширенные. Листочки
кожистые, сизоватые, голые. Цветки очень крупные до 8 см в поперечнике. Плоды
крупные - до 5 см длины, покрыты железистыми щетинками.
Шиповник собачий - Rosa canina L. Кустарник с дугообразными ветвями, зеленой или красно-бурой
корой. Шипы редкие, у основания весьма широкие, серповидно-изогнутые. Цветки
одиночные или их 3-5, на длинных цветоножках, лепестки бледно-розовые или
белые. Плоды продолговато-эллиптические, ярко- или светло-красные. Чашелистики
перисто-рассеченные, после цветения отгибаются вниз и опадают задолго до
созревания, оставляя после себя пятиугольную площадку. Весьма полиморфный вид.
Широко распространен в средней полосе и южных районах европейской части России,
Крыму на Кавказе, в Центральной Азии. Растет на опушках лесов, в разреженных
лесах, по склонам, берегам рек и ручьев, на вырубках, у дорог.
Лекарственное сырье. Доброкачественное сырье
представляет собой высушенные плоды шиповника - fructus Rosae различной формы и величины, с отверстием на верхушке,
получающимся после удаления чашечки, частично с сохранившимися, вверхстоящими
цельными чашелистиками или пятиугольной площадкой. Стенки высушенных плодов
твердые, хрупкие, наружная их поверхность блестящая, реже матовая, более или
менее морщинистая. Орешки мелкие, угловатые, твердые, желтые, волоски белые.
Вкус стенки плода кисловато-сладкий, слегка вяжущий, запаха нет.
Ноготки лекарственные (календула лекарственная)
Растениe.
Ноготки лекарственные ( календула лекарственная) - Calendula officinalis L., семейство сложноцветные - Asteraceae (Compositae).
Однолетнее травянистое растение (рис. 5). Все растение
железисто-опушенное с ветвистым прямостоячим стеблем высотой около 50-70 см.
Листья очередные, продолговато-обратнояйцевидные. Золотисто-желтые и оранжевые
цветки, собранные в крупные корзинки; краевые - ложноязычковые, в центре
трубчатые. Плоды - семянки разной формы и величины развиваются из краевых
язычковых цветков, срединные трубчатые - бесплодные. Цветет растение со второй
половины лета до поздней осени. Дикорастущие формы неизвестны. Растение
встречается только в культуре.
Лекарственное сырье. Для медицинских целей используют
цветочные корзинки. Их собирают без цветоносов в период горизонтального стояния
язычковых цветков. За летне-осенний период возможно от 10 до 20 сборов по мере
распускания новых корзинок. Собранное сырье (цветки календулы - flores Calendulae) сушат на воздухе в тени или в
сушилках.
Цельные высушенные корзинки диаметром около 0,5-4 см,
цветоложе плоское. Голое, обертка состоит из одного ряда зеленых узколанцетных
заостренных листочков. Краевые язычковые цветки имеют на верхушке 2-3 зубчика и
расположены в 2-3 ряда, у махровых форм бывает до 12 рядов язычковых цветков и
их общее количество в корзинке достигает 100 язычков. Цветочных корзинок с
цветоносами допускается не более 6 %, а цветочных корзинок, полностью
осыпавшихся без язычковых цветков, - не более 20 % (ГФ XI). [14]
2. Химический состав сырья
Листья крапивы являются богатым поливитаминным сырьем, в них содержатся
значительное количество витамина К1 (0,2 %), C (до 0,6 %), до 50 мг% каротиноидов (b-каротин, ксантофиллы, виолаксантин и
др.), витамин В2, пантотеновая кислота. Листья богаты хлорофиллом (до 5 %).
Найдены гликозид уртицин, дубильные вещества, содержатся муравьиная кислота и
минеральные соли.
Плоды шиповника содержат аскорбиновую кислоту (у коричных шиповников ее
накапливается от 2 до 5,5 %, у собачьих - в среднем около 1 %), каротиноиды (до
10 мг%), витамины К1, В2 и Р, флавоноиды. В зрелых плодах много сахара ( до
18%), пектиновых веществ ( в среднем около 4 %), органических кислот ( лимонная
и яблочная) до 2 % ( у собачьих шиповников не менее 2,6 %). В семенах
содержится жирное масло, богатое каротиноидами и витамином E. Согласно ГФ XI, в плодах должно быть не менее 0,2 %
аскорбиновой кислоты; в сырье, используемом для изготовления холосаса,
каротолина и сиропов ( преимущественно виды из секции Canina), органических кислот не менее 2,6 %. Наивысшее
содержание аскорбиновой кислоты в плодах шиповника наблюдается в состоянии их
полной спелости.
Цветки ноготков содержат каротиноиды: каротин, ликопин и кислородные
производные каротина - виолаксантин, цитроксантин, рубиксантин, флавоксантин и
др. В краевых цветках сумма всех каротиноидов может достигать 3 % ( на сухую
массу). Запах цветков обусловлен наличием следов эфирного масла ( до 0,12 %). В
соцветиях ноготков присутствует аскорбиновая кислота, имеются смолы (около 3
%), кислоты (яблочная до 6 %), обнаружены сапонины, дающие при гидролизе
олеаноловую и глюкуроновую кислоты. Установлено наличие тритерпендиолов
арнидиола и фарадиола. Все растение обладает фитонцидным свойством. [3]
Основные структурные формулы витаминов
Витамины, алифатического ряда

кислота аскорбиновая
Витамины, алициклического ряда
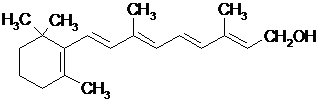
ретинол,
витамин А1
Витамины,
ароматического ряда
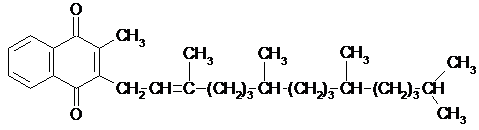
филлохинон,
витамин К1
Витамины,
гетероциклического ряда
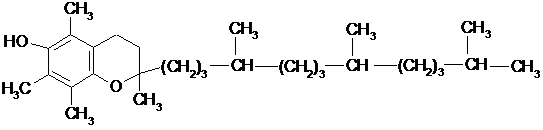
a-токоферол

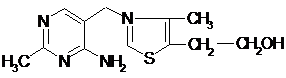
Тиамин
рутин

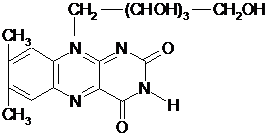
никотиновая
кислота рибофлавин
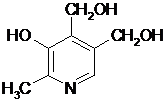

пиридоксин
кислота фолиевая
[7,
11, 13]
3. Медицинское применение
Лекарственное растительное сырье, содержащее витамины,
и лекарственные средства на его основе обладают широким спектром
фармакологического действия. Действие обусловлено витаминами и другими
биологически активными веществами: флавоноидами, дубильными веществами и др.
Действие витаминов заместительное (т.е. восполняющее
витаминную недостаточность), либо фармакологическое (т.е. влияющее на течение
ферментативных процессов, повышающее иммунные, защитные силы).
Например: введение в организм витамина С повышает
фагоцитарную активность лейкоцитов. Витамин С усиливает фармакологическое
действие лекарственных веществ и снижает их побочное токсическое действие. [9]
Применение листьев крапивы. Препараты крапивы
двудомной обладают кровоостанавливающим свойством (за счет витамина K1). Они усиливают свертывание крови,
способствуют увеличению содержания гемоглобина, повышают тонус гладкой
мускулатуры и успешно применяются в медицинской практике при различных
внутренних кровотечениях - маточных, геморроидальных, желудочных, а также наружно
для лечения хронических язв. Хлорофилл обусловливает тонизирующее действие,
усиливает основной обмен, стимулирует грануляцию и эпителизацию пораженных
тканей. Эффективны препараты листьев крапивы и при C-, гипо- и авитаминозах. Сухой экстракт входит в препарат
«Аллохол».
Применяют в форме настоя или в виде жидкого экстракта.
Листья находятся в составе желудочного и поливитаминных сборов. Из крапивы
получают хлорофилл, используемый в фармацевтической и пищевой промышленности.
Молодые побеги крапивы, богатые витаминами, употребляют в пищу. Имеются
рекомендации при выпадении волос мыть голову отваром крапивы.
Применение плодов шиповника. Цельные плоды входят в
состав поливитаминных сборов, а также могут применяться в виде настоя. Из
свежих плодов изготавливают сироп
(Sirupus fructus
Rosae), экстракт и на его основе другие
витаминные концентраты. Из плодов шиповника собачьего вырабатывают препарат
холосас (Cholosasum) - густой экстракт, применяемый при
холециститах и гепатитах. Из орешков всех видов шиповника получают жирное масло
- Oleum Rosae pinguiae, применяемое при ожогах, дерматитах
и при облучении рентгеновскими лучами. Кроме того, изготовляется богатый
каротиноидами препарат каротолин, используемый аналогично маслу.
Применение цветков ноготков. Из цветочных корзинок
ноготоков готовят настойку и мазь, рекомендуют при порезах, кнойных ранах и
язвах, фурункулезе, ожогах, а настойку, кроме того, для полоскания горла при
ангине, тонзиллите, пародонтозах. Внутрь назначают при язве желудка и как
желчегонное средство. Ноготки издавна применяют в народной медицине и
гомеопатии. Из них получают также препарат «Калефлон», применяемый как
противоязвенное средство и при хронических гастритах в фазе обострения. [14]
Пути использования сырья, содержащего витамины
Использование ЛРС, содержащего витамины разнообразно.
Сырье отпускают из аптеки без рецепта врача как лекарственные средства.
. В аптеке и в домашних условиях из сырья готовят
настои и отвары, т.е. экстемпоральные лекарственные формы. Витаминсодержащее
сырье включают в официнальные сборы: поливитаминный, желудочный, слабительный,
грудной, желчегонный, «Элекасол», сбор Здренко, «Полифитохол», «Арфазетин»,
«Гепатофит», «Полифитохол» и др. Сборы составляют на заводах по переработке
ЛРС, либо непосредственно в аптеках.
. На фармацевтических фабриках сырье используют для
получения экстракционных лекарственных форм (галеновые препараты):
- «Масло шиповника», сиропы шиповника,
шиповника с витамином С, шиповника с биоженьшенем, плодово-ягодный (шиповник,
рябина);
- «Холосас» - сироп из сгущенного
водного экстракта плодов шиповника;
- «Каротолин» - масляный экстракт каротиноидов из
плодов шиповника;
- экстракты жидкие из сырья крапивы
двудомной, календулы;
- настойка из сырья календулы;
3. На химико-фармацевтических заводах получают:
- таблетки «Аллохол», содержат сухой экстракт крапивы;
- таблетки «Калефлон», содержат сумму
полифенольных соединений цветков календулы, мазь «Календула», карофилленовая
мазь, суппозитории «Календула»;
- комбинированный препарат «Ротокан»; [6].
Таблица 2. Лекарственное растительное сырье, содержащее витамины и
препараты на его основе
|
Наименование ЛРС
|
Лекарственные формы и
препараты
|
|
Сырье, содержащее
филлохиноны
|
|
Крапивы листья - Urticae folia
|
Настой, жидкий экстракт
|
Кровоостанавливающее
средство при маточных, легочных, печеночных, почечных и других кровотечениях
|
|
В составе сборов
«Полифитохол», «Арфазетин», «Мирфазин», желудочный сбор № 3, слабительный
сбор №1
|
Витамииные, желудочные,
слабительные
|
|
Сухой экстракт в составе
препарата «Аллохол»
|
При заболеваниях печени
|
|
Сырье, содержащее
аскорбиновую кислоту
|
|
Шиповника плоды - Rosae Fructus
|
Настой, сироп, микстура
Траскова, витаминные и поливитаминные сборы
|
При авитаминозах
|
|
«Масло шиповника»,
«Каротолин»
|
Ранозаживляющее средство
|
|
«Холосас», сборы:
«Гепатофит», «Полифитохол»
|
Желчегонное средство
|
|
Сырье, содержащее каротины
и каротиноиды
|
|
Ноготков цветки - Calendulae flores
|
Настой, настойка, жидкий
экстракт, мазь «Календула», «Карофилленовая», в составе комбинированных
препаратов «Ротокан», «Алором»
|
Обладают антисептическим,
противовоспалительным, регенерирующим, раноза-живляющим и иммуно-модулирующим
действием
|
|
«Калефлон»
|
Противоязвенное средство и
при хронических гастритах в фазе обострения
|
|
В составе сборов:
«Элекасол», «Мирфазин»
|
Грудной, желчегонный
|
[6, 8]
4. Анализ сырья
.1 Внешние признаки
FOLIA URTICAE - ЛИСТЬЯ КРАПИВЫ
Собранные во время цветения и высушенные листья дикорастущего
многолетнего травянистого растения крапивы двудомной - Urtica dioica L., сем.
крапивных - Urticaceae.
Внешние признаки. Цельное сырье. Листья цельные или частично измельченные, простые,
черешковые, длиной до 20 см и шириной до 9 см (у основания), яйцевидно -
ланцетовидные и широкояйцевидные, заостренные, при основании обычно
сердцевидные, края остро- и крупнопильчатые с изогнутыми к вершине зубцами.
Поверхность листа шершавоволосистая, особенно много волосков по жилкам листа.
Черешки листьев длиной 7-8 см, округлые или полуокруглые в сечении, с бороздкой
на верхней стороне черешка, покрытые волосками. Цвет листьев темно - зеленый,
черешков - зеленый. Запах слабый. Вкус горьковатый. [1]
Измельченное сырье. Кусочки листьев различной формы,
проходящие сквозь сито с отверстиями диаметром 7 мм. Цвет темно - зеленый.
Запах слабый. Вкус горьковатый.
FRUCTUS ROSAE - ПЛОДЫ ШИПОВНИКА
Собранные в период полного созревания и высушенные плоды
кустарников различных видов шиповника (розы) - Rosa, сем. розоцветных -
Rosaceae: шиповника майского (шиповника коричного) - R. majalis Herrm.(R.
cinnamomea L.), шиповника иглистого - R. acicularis Lindl., шиповника даурского
- R. davurica Pall., шиповника Беггера - R. beggeriana Schrenk, шиповника
Федченко - R. fedtschenkoana Regel, шиповника собачьего - R. canina L.,
шиповника щитконосного - R. corymbifera Borkh., шиповника мелкоцветкового - R.
micrantha Smith, шиповника кокандского - kokanica (Regel) Regel ex Juz.,
шиповника песколюбивого - R. psammophila Chrshan., шиповника войлочного - R.
tomentosa Smith, шиповника зангезурского - R. zangezura P. Jarosch., шиповника
морщинистого - R. rugosa Thunb. и других видов розы.
Внешние признаки. Цельные, очищенные от чашелистиков и плодоножек ложные плоды разнообразной формы: от шаровидной, яйцевидной или овальной до сильно
вытянутой веретеновидной; длина плодов 0,7-3 см, диаметр -0,6-1,7 см. На
верхушке плода имеется небольшое круглое отверстие или пятиугольная площадка.
Плоды состоят из разросшегося мясистого, при созревании сочного цветоложа (гипантия) и заключенных в
его полости многочисленных плодиков - орешков. Стенки высушенных плодов твердые
хрупкие, наружная поверхность блестящая, реже матовая, более или менее
морщинистая. Внутри плоды обильно выстланы длинными, очень жесткими щетинистыми волосками.
Орешки мелкие, продолговатые, со слабо выраженными гранями. Цвет плодов от оранжево - красного до буровато
- красного, орешки светло - желтые, иногда буроватые. Запах отсутствует. Вкус
кисловато - сладкий, слегка вяжущий..
FLORES CALENDULAE -
ЦВЕТКИ НОГОТКОВ
Собранные в начале распускания трубчатых цветков и высушенные цветочные
корзинки культивируемого однолетнего травянистого растения ноготков
лекарственных (календулы лекарственной) - Calendula officinalis L., сем.
астровых - Asteraceae.
Внешние признаки. Цельные или частично осыпавшиеся корзинки диаметром до
5 см, без цветоносов или с остатками цветоносов длиной не более 3 см. Обвертка
серо - зеленая, одно - двухрядная; листочки ее линейные, заостренные,
густоопушенные. Цветоложе слегка выпуклое, голое. Краевые цветки язычковые,
длиной 15-28 мм, шириной 3-5 мм с изогнутой короткой опушенной трубкой,
трехзубчатым отгибом, вдвое превышающим обвертку, и 4-5 жилками. Цветки
расположены в 2-3 ряда у немахровых и в 10-15 рядов у махровых форм. Пестик с
изогнутой нижней одногнездной завязью, тонким столбиком и двухлопастным рыльцем.
Срединные цветки трубчатые с пятизубчатым венчиком. Цвет краевых цветков
красновато - оранжевый, оранжевый, ярко- или бледно - желтый; срединных -
оранжевый, желтовато - коричневый или желтый. Запах слабый. Вкус солоновато -
горький.[1]
4.2 Микроскопия
Микроскопия листа крапивы. При рассмотрении листа с поверхности видны клетки верхнего эпидермиса -
многоугольные или слабоизвилистые, нижнего - сильноизвилистые. Устьица окружены
3- 5 клетками эпидермиса (аномоцитный тип), встречаются в основном на нижней стороне
листа. В клетках эпидермиса часто встречаются цистолиты в виде продолговато -
округлых образований с зернистой структурой и небольшим пятном в центре -
ножкой. Волоски с обеих сторон листа,трех типов: ретортовидные, жгучие и
головчатые. Ретортовидные волоски одноклеточные, имеют расширенное основание и
вытянутую заостренную верхушку. Жгучие волоски состоят из многоклеточного
основания и крупной конечной клетки, которая оканчивается легко обламывающейся
головкой. Головчатые волоски мелкие с двух-, реже трехклеточной головкой на
одноклеточной ножке. В крупных жилках расположены клетки с мелкими друзами
оксалата кальция, образующими
характерные цепочки.
(Рис. 13). [1]
Методика приготовления микропрепаратов листьев, трав, цветков (выписка из
общей фармакопейной статьи «Техника микроскопического и микрохимического
исследования лекарственного растительного сырья», Государственная фармакопея,
XI издание)
Растительный материал, отобранный для микроскопического изучения,
помещают в пробирку и проводят его обработку для просветления:
растительный материал заливают 2-3% раствором едкого натра и кипятят в
течение 1-2 мин. После этого жидкость осторожно сливают, а материал тщательно
промывают водой и помещают в чашку Петри. Кусочки сырья вынимают из воды с
помощью скальпеля (или лопаточки) и препаровальной иглы и помещают на
предметное стекло в каплю раствора глицерина или воды. На предметном стекле его
кусочек 4 мм разделяют скальпелем или препаровальной иглой на две части; одну
из них осторожно переворачивают, чтобы получить возможность наблюдать лист под
микроскопом с верхней и нижней сторон. Стекла, используемые для приготовления
микропрепаратов, должны быть чистыми и сухими. Препарат на предметном стекле
накрывают покровным стеклом. При неосторожном накладывании покровного стекла в
препарате часто образуются пузырьки воздуха, поэтому стекло следует класть
наклонно, прикоснувшись сначала одним краем к жидкости, а затем, придерживая
стекло иглой, положить полностью. Попавшие пузырьки воздуха можно удалить
легким постукиванием по покровному стеклу тупым концом препаровальной иглы или
слегка подогреть над пламенем горелки. После охлаждения рассматривают под
микроскопом, сначала при малом, затем при большом увеличении.
Если включающая жидкость не заполняет всего пространства между предметным
и покровным стеклом или она испарилась при нагревании препарата, то ее
добавляют сбоку небольшими каплями. Если наоборот, покровное стекло свободно
плавает вследствие избыточного количества жидкости, то ее следует отсосать при
помощи полоски фильтровальной бумаги, подведенной сбоку.
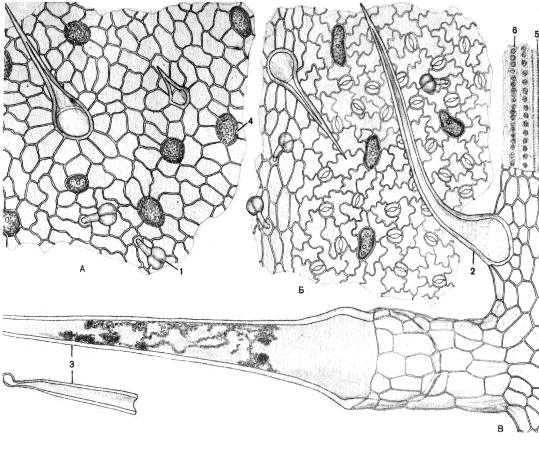
Рис. 13. Микроскопия листа крапивы с поверхности:
А - эпидермис верхней стороны листа; Б - эпидермис нижней стороны листа;
В - фрагмент крупной жилки: 1 - головчатый волосок; 2 - ретортовидный волосок;
3 - жгучий волосок; 4 - цистолиты; 5 - сосуды проводящего пучка жилки; 6 -
друзы кальция оксалата. [3]
Микроскопия плодов шиповника. При рассмотрении препарата порошка плодов видны следующие
диагностические элементы: обрывки наружного эпидермиса гипантия (плода) в виде
светло - желтых пластов, состоящих из многоугольных клеток с прямыми
неодинаково утолщенными, местами четковидно - утолщенными стенками и редкими
устьицами; обрывки мякоти
плода, состоящей из тонкостенных паренхимных
клеток, содержащих оранжево - красные
глыбки каротиноидов и многочисленные друзы оксалата кальция; фрагменты
околоплодника орешка, состоящие из групп или пластов, реже одиночных каменистых
клеток с сильно утолщенными пористыми оболочками; многочисленные крупные
одноклеточные волоски двух типов (или их обломки) - очень крупные прямые с
толстой стенкой и узкой полостью и более мелкие, слегка извилистые с широкой
полостью; обрывки проводящих пучков со спиральными сосудами. (Рис. 14). [1]
Методика приготовления микропрепаратов цельных плодов и семян (выписка из
общей фармакопейной статьи «Техника микроскопического и микрохимического
исследования лекарственного растительного сырья» Государственной фармакопеи, XI
издание)
Готовят поперечные срезы.
Срезы. Для приготовления срезов сухие плоды и семена предварительно
размягчают, поместив их на сутки во влажную камеру (влажной камерой служит
эксикатор с водой, в которую добавлено несколько капель хлороформа) или водяным
паром в течение 15-30 мин или более в зависимости от твердости объекта. Мелкие
плоды и семена запаивают в парафиновый блок размером 0,5 х 0,5 х 1,5 см.
Кончиком нагретой препаровальной иглы расплавляют парафин и в образовавшуюся
ямку быстро погружают объект. Срезы объекта делают вместе с парафином;
срезы выбирают из парафина препаровальной иглой, смоченной жидкостью, и
готовят микропрепарат в растворе глицерина.
лекарственный растение витамин медицинский

Рис.
14. Микропрепарат плодов шиповника:
элементы
порошка плодов: 1 - эпидермис плода, 2 - ткань мякоти с друзами кальция
оксалата, 3 - ткань мякоти с каротином и друзами кальция оксалата, 4 -
каменистые клетки околоплодника орешка, 5 - волоски, 6 - элементы проводящих
пучков. [15]
Микроскопия цветков ноготков. При рассмотрении язычковых цветков с
поверхности видны удлиненные клетки эпидермиса с оранжевыми округлыми
хроматопластами; на зубчиках эпидермис с сосочками, иногда с устьицами; трубка
венчика густо опушена простыми и железистыми одно - двухрядными волосками;
завязь также опушена: с выпуклой стороны железистыми, по краям вогнутой стороны
- простыми двухрядными волосками. Головка железистых волосков состоит из 2, 4
или 8 клеток. Эпидермис трубчатых цветков такой же, как у язычковых, но у
зубчиков он с более вытянутыми сосочками; нижняя часть трубки венчика и завязь
густо опушены одно - двухрядными железистыми, реже двухрядными простыми
волосками. Складчатость кутикулы, обычно маскируемая хромопластами,
просматривается только на отдельных участках. Пыльца округлая, шиповатая.
Эпидермис листочков обвертки по краю представлен удлиненными клетками с
прямыми стенками, в средней части - извилистыми стенками и устьицами; листочки
обвертки густо опушены: по краю - длинными одно - двухрядными простыми,
двухрядными железистыми и ветвистыми волосками; в средней части - только
железистыми волосками. (Рис. 15). [1]
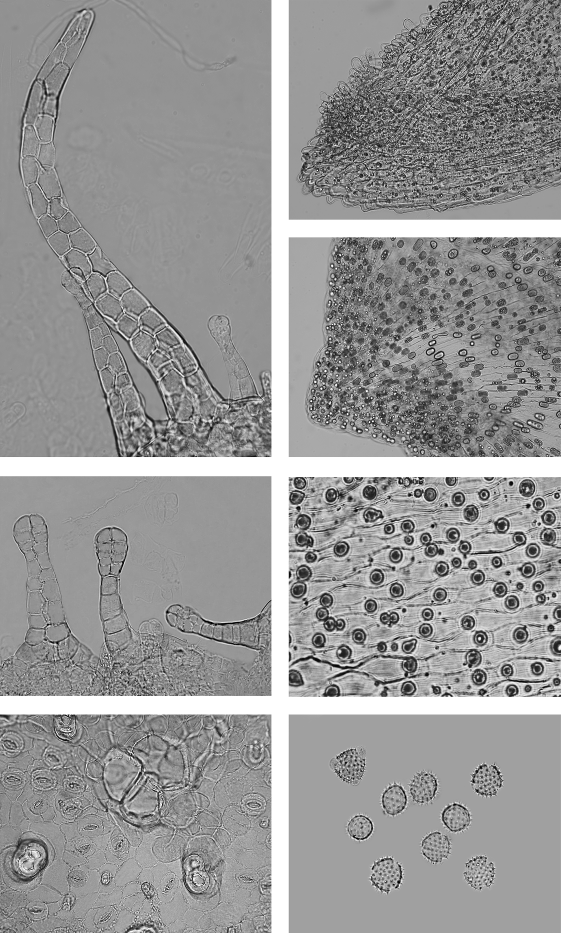
Рис. 15. Микропрепарат цветков ноготков.
- фрагмент эпидермиса завязи трубчатого цветка: а - простой
многоклеточный двухрядный волосок, b - двухрядные железистые волоски. Увел. 200×
2 - фрагмент эпидермиса завязи язычкового цветка: а - железистый
двухрядный волосок, b - железистый однорядный
волосок. Увел. 200×
- фрагмент эпидермиса листочка обвертки: а - устьица, b - 2-3-клеточные основания обломанных
волосков. Увел. 200×
4 - фрагмент зубчика венчика трубчатого цветка: а - мелкие маслянистые
капли в клетках мезофилла, b -
сосочковидные выросты клеток эпидермиса. Увел. 200×
5 - фрагмент зубчика отгиба язычкового цветка: а - маслянистые капли в
клетках мезофилла. Увел. 200×
6 - фрагмент отгиба язычкового цветка: а - маслянистые капли в клетках
мезофилла, b - складчатость кутикулы эпидермиса.
Увел. 400×
- округлые пыльцевые зерна с шиповатой экзиной и тремя порами. Увел. 200×
[17]
4.3 Качественный анализ
Качественное определение витамина К1 в листьях крапивы
Наличие витамина К1 в сырье в основном определяют
методом тонкослойной хроматографии после экстракции хлороформом или этиловым
спиртом. В УФ-свете на хроматографической пластинке витамин К1 проявляется в
виде пятна с зелено-желтой флюоресценцией.
Для обнаружения витамина К1 на хроматографических
пластинах применяют 95 % кислоту серную, 60 % кислоту хлорную и 65 % кислоту
азотную. Витамин К1 проявляется в виде бурых пятен. При обработке хроматограммы
парами йода и после смачивания ее водой витамин K1 проявляется в виде фиолетового пятна. После обработки 0,25
% раствором родамина В, витамин K1
проявляется в УФ-свете в виде пятна фиолетового цвета. [12]
Методика. Аналитическую
пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями
размером 0,25 мм; 1 г измельченного сырья помещают в колбу вместимостью 15 мл,
прибавляют 10 мл гексана и перемешивают на механическом встряхивателе в течение
3 ч. Затем фильтруют, отгоняют растворитель на ротационном испарителе при
температуре водяной бани не выше 45 ºC до объема 2-3 мл.
Микропипеткой наносят 0,1 мл извлечения полосой шириной 1,5 - 2 см на пластинку "Силуфол"
(размером 13х5 см) на расстоянии 1,5 см от края. Пластинку подсушивают на
воздухе в течение 3-5 мин и хроматографируют в системе растворителей бензол - петролейный эфир при
температуре кипения 40-70 ºС (1:1) восходящим способом.
Когда фронт растворителей пройдет 10 см, пластинку вынимают из камеры, высушивают на воздухе в
течение 2-3 мин и выдерживают в УФ - свете при длине волны 360 нм в течение 2
мин; на пластинке должно появиться пятно с желто - зеленой флюоресценцией
(витамин K1). [1]
Качественное определение аскорбиновой кислоты в плодах
шиповника
В сырье аскорбиновую кислоту в основном определяют
методом ТСХ после экстракции водой. В качестве сорбента используют силикагель G, полиамид, оксид алюминия, пластинки
«Силуфол». Подвижной фазой чаще всего является система растворителей: ледяная
уксусная кислота - ацетон - метанол - бензол (5:5:20:70) или (3:3:10:24);
хлороформ - этилацетат (1:1); этилацетат - ледяная уксусная кислота (80:20);
этанол - гексан (1:3). После хроматографирования пластинку высушивают и для
обнаружения аскорбиновой кислоты обрабатывают следующими реактивами:
- раствором 2,6-дихлорфенолиндофенолята натрия
(аскорбиновая кислота проявляется в виде белых пятен на розовом фоне);
- щелочным раствором серебра нитрата
(проявляется в виде темно-серых пятен);
- этанольным раствором кислоты
фосфорномолибденовой (проявляется в виде темно-синих пятен на желто-зеленом
фоне). [20]
Качественное обнаружение аскорбиновой кислоты основано
на ее высокой восстановительной способности.
. При действии на аскорбиновую кислоту раствором
нитрата серебра происходит восстановление серебра, при этом аскорбиновая
кислота окисляется в кетоформу:
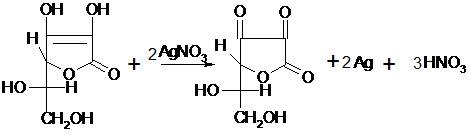
. При действии на аскорбиновую кислоту реактивом
Феллинга медь восстанавливается до гемиоксида меди красного цвета:

. При действии раствором перманганата калия раствор
обесцвечивается вследствие восстановления марганца до Mn2+:

. При взаимодействии аскорбиновой кислоты с
феррицианидом калия в присутствии разведенной соляной кислоты и с последующим
добавлением раствора трихлорида железа образуется берлинская лазурь (синяя):
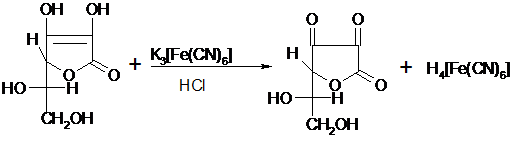
3H4[Fe(CN)6] + 4FeCl3→ 12HCl +
Fe[Fe(Fe(CN)6]3
берлинская лазурь
. Аскорбиновая кислота с солью железа (II) образует аскорбинат железа
фиолетового цвета:
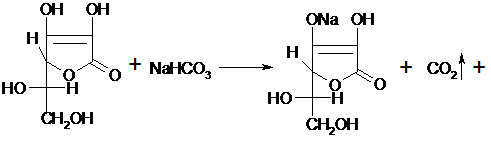
H2O
. Йод обесцвечивается от действия аскорбиновой
кислоты:

Перечисленные выше реакции можно провести с выделенной
из сырья и очищенной от сопутствующих веществ субстанцией аскорбиновой кислоты.
[19]
Идентификацию аскорбиновой кислоты можно осуществлять
спектрофотометрически: λmах = 243 нм для водного раствора в присутствии 0,1М НС1.
Спектр снимают немедленно после приготовления раствора (ЕФ). ИК-спектроскопия
также может быть использована. Полученный спектр сравнивают со спектром СО
аскорбиновой кислоты (ЕФ).
Определение основных групп биологически активных веществ в цветках
ноготков
Каротиноиды. Для качественного обнаружения
каротиноидов на хроматограмме используют их свойства образовывать с кислотами
продукты разного цвета. Для этого применяют хлористоводородную, серную,
фосфорную, азотную, муравьиную и трихлоруксусную кислоты:
- β-каротин с кислотой азотной
концентрированной окрашивается в синий цвет, переходящий в зеленый, потом в
желтый;
- β-
каротин с кислотой
серной концентрированной дает синюю окраску;
- с раствором сурьмы хлорида (III) в хлороформе (реакция Карра-Прайса)
образуются продукты синего цвета.
В сырье каротиноиды можно определить при помощи
бумажной и тонкослойной хроматографии. Для этого проводят многократную
экстракцию каротиноидов из сырья неполярными растворителями, такими как ацетон,
спирт, петролейный эфир, или смесью этанол-ацетон (1:3).
Для обработки хроматограмм часто применяют
фосфорномолибденовую кислоту. В этом случае на желтом фоне каротиноиды
проявляются в виде синих пятен при нагревании пластинки до 80 °С. [19]
1. Тонкослойная хроматография
Около 5 г измельченного сырья помещают в колбу
вместимостью 100 мл, приливают 50 мл спирта 70 %. Колбу присоединяют к
обратному холодильнику и кипятят на кипящей водяной бане в течение 30 мин.
Содержимое колбы охлаждают до комнатной температуры и фильтруют через бумажный
фильтр (раствор А).
На линию старта хроматографической пластинки со слоем
силикагеля размером 10×15 см наносят 20 мкл раствора А и 10 мкл стандартного
раствора. Пластинку с нанесенными пробами высушивают на воздухе в течение 10
мин, помещают в камеру со смесью растворителей муравьиная кислота
безводная-вода-этилацетат (10:10:80) и хроматографируют восходящим способом.
Когда фронт растворителей пройдет расстояние 10 см от линии старта, пластинку
вынимают из камеры и сушат на воздухе до удаления следов растворителей в
течение 15 мин. Затем пластинку опрыскивают последовательно 1 % раствором
дифенилборной кислоты β-этиламинового эфира и 5 % раствором полиэтиленгликоля
400, нагревают пластинку при температуре от 100 °С до 105 °С в течение 10 мин и
просматривают в УФ - свете при длине волны 365 нм.
На хроматограмме испытуемого раствора А должны быть
видны основные зоны с флуоресценцией: желтовато-коричневого, светло-голубого и
бледно-голубого цвета на уровне зон на хроматограмме стандартного раствора Rs (по рутину) около 1,00; 1,30 и 3,00
соответственно. Допускается обнаружение не менее 7 дополнительных зон с RS (по рутину) от 0,06 до 2,80,
флуоресцирующих различными цветами.
Примечания
Приготовление дифенилборной кислоты β-этиламинового эфира раствора 1%. 0,1
г дифенилборной кислоты β-этиламинового эфира растворяют в 10 мл спирта 96 %.
Раствор используют свежеприготовленным.
Приготовление полиэтиленгликоля 400 раствора 5 %. 0,5 г полиэтиленгликоля
400 растворяют в 10 мл спирта 96 %, слегка подогревая раствор на водяной бане.
Раствор используют свежеприготовленным.
Приготовление стандартного раствора. 1 мг кофейной
кислоты, 1 мг хлорогеновой кислоты и 2,5 мг рутина растворяют в 8 мл спирта 96
% в мерной колбе вместимостью 10 мл, доводят объем раствора тем же спиртом до
метки. Раствор используют свежеприготовленным.
2. Около 1 г измельченного сырья помещают в колбу
вместимостью 50 мл, приливают 10 мл хлороформа, кипятят с обратным
холодильником в течение 10 мин и охлаждают. Полученный раствор фильтруют через
бумажный фильтр и выпаривают на кипящей водяной бане до объема 1 мл (раствор
Б).
На линию старта хроматографической пластинки со слоем
силикагеля размером 10×15 см наносят 30 мкл испытуемого раствора Б и 20 мкл
раствора СО β-каротина. Пластинку с нанесенными пробами высушивают на
воздухе в течение 5 мин, помещают в хроматографическую камеру со смесью
растворителей гексан:бензол (85:15) и хроматографируют восходящим способом.
Когда фронт растворителей пройдет расстояние 10 см от линии старта, пластинку
вынимают из камеры и сушат на воздухе до удаления следов растворителей в
течение 10-15 мин.
На хроматограмме испытуемого раствора Б должна
обнаруживаться основная зона на уровне зоны на хроматограмме раствора СО β-каротина. Допускается наличие 2
дополнительных зон желто-оранжевого цвета ниже зоны β-каротина и зона на старте.
Примечание
Приготовление раствора стандартного образца β-каротина. 0,02 г β-каротина растворяют в хлороформе в
мерной колбе вместимостью 100 мл, доводят объем раствора хлороформом до метки и
перемешивают.
мл полученного раствора переносят в мерную колбу
вместимостью 100 мл и доводят объем раствора хлороформом до метки,
перемешивают.
Раствор должен быть свежеприготовленным.
. Около 5 г измельченного сырья помещают в колбу
вместимостью 100 мл, приливают 50 мл спирта 70 %. Колбу присоединяют к
обратному холодильнику и кипятят на кипящей водяной бане в течение 30 мин.
Содержимое колбы охлаждают до комнатной температуры и фильтруют через бумажный
фильтр (раствор А).
К 1 мл раствора А прибавляют 0,2 мл 3 % раствора
железа (III) хлорида, должно наблюдаться
образование окрашивания зеленовато-коричневого цвета, исчезающее при добавлении
кислоты серной разведенной (дубильные вещества).
К 2 мл раствора А приливают 1 мл воды, по стенке
осторожно приливают 1 мл раствора ванилина в кислоте серной, на границе слоев
должно наблюдаться образование окрашивания красновато-коричневого цвета в виде
кольца (тритерпеновые соединения). [18]
4.4 Числовые показатели
Числовые показатели в листьях крапивы. Цельное сырье. Влажность не более 14 %; золы общей не более 20 %; золы, нерастворимой в 10 % растворе хлористоводородной
кислоты, не более 2 %;
почерневших и побуревших листьев не более 5 %; других частей растения (стеблей,
соцветий и пр.) не более 5%; частиц, проходящих сквозь сито с отверстиями
диаметром 3 мм, не более 10%; органическо примеси не более 2 %; минеральной примеси не более 1 %.
Измельченное сырье. Влажность не более 14 %; золы общей не более 20 %; золы, нерастворимой в 10 % растворе хлористоводородной кислоты, не более 2 %; кусочков почерневших и побуревших
листьев не более 5 %; других
частей растения (кусочков стеблей, соцветий и пр.) не более 5 %; частиц, не проходящих сквозь сито
с отверстиями диаметром 7 мм, не более 10 %; частиц, проходящих сквозь сито с отверстиями размером 0,5
мм, не более 15 %; органической примеси не
более 2 %; минеральной примеси не
более 1 %.
Числовые показатели в плодах шиповника. Аскорбиновой кислоты не менее 0,2 %; влажность не более 15 %; золы общей не более 3 %; других частей шиповника (кусочки
веточек, чашелистиков и плодоножек) не более 2 %; почерневших, пригоревших,
поврежденных вредителями и болезнями плодов не более 1%; измельченных частиц
плодов, в том числе орешков, проходящих сквозь сито с отверстиями диаметром 3
мм, не более 3 %; органической примеси не более
0,5%; минеральной примеси не более 0,5 %.
Для сырья, используемого для изготовления холосаса,
каротолина и сиропов. Органических кислот не менее 2,6 %; влажность не более 15%; золы общей
не более 4 %; других частей шиповника
(кусочки веточек, чашелистиков и плодоножек) не более 2 %; почерневших, пригоревших,
поврежденных вредителями и болезнями плодов не более 3 %; измельченных частиц плодов, в том
числе орешков, проходящих сквозь сито с отверстиями диаметром 3 мм, не более
3%; недозрелых плодов (от зеленой до желтой окраски) не более 5 %; органической примеси не более
0,5%; минеральной примеси не более 0,5 %.
Числовые показатели в цветках ноготков. Экстрактивных веществ,
извлекаемых 70% спиртом, не менее 35%; влажность не более 14 %; золы общей не
более 11%; остатков цветоносов, в том числе отделенных от корзинок при анализе,
не более 6%; корзинок с полностью осыпавшимися язычковыми и трубчатыми цветками
(цветоложе с обвертками) не более 20%; побуревших корзинок не более 3%; других
частей растения (кусочков стеблей и листьев) не более 3%; органической примеси
не более 0,5%; минеральной примеси не более 0,5%. [1]
4.5 Количественное
определение
Методы количественного определения витаминов основаны
на их физико-химических свойствах, таких как окислительно-восстановительные
свойства, способность флуоресцировать в УФ-свете. Применяют различные методы
определения: титрометрические, фотоколориметрические, спектрофотометрические,
флуорометрические и др. [9]
Количественное определение витамина К
Витамин К в листьях крапивы определяют методом СФМ
(таблица 3).
Таблица 3. Количественное определение витамина K в листьях крапивы (авторский метод)
|
Этап определения
|
Сущность
|
Обоснование
|
|
Подготовительный
|
Измельчение сырья и взятие
точной навески
|
Для лучшей экстракции
|
|
Экстракция
|
Гексан
|
Витамин K
хорошо растворяется в органических растворителях
|
ТСХ (условия разделения в
качественной хорматографии)
|
Для выделения витамина K
|
|
Количественное определение
|
Обнаруженное пятно витамина
K элюируют с хроматограммы и снимают оптическую
плотность (СФМ)
|
Способность витамина K
за счет системы двойных связей поглощать свет при определенной длине волны
|
Количественное определение БАВ в плодах шиповника.
Аскорбиновую кислоту можно определять титрометрическим
методом, который основан на восстановлении 2,6-дихлорфенолиндофенола. С этим же
реактивом можно провести фотоколориметрическое определение аскорбиновой
кислоты. Для этого проводят экстракцию сырья 2 % метафосфорной кислотой,
добавляют раствор 2,6-дихлорфенолиндофенола. Через 35 сек. проводят
фотоколориметрирование. Параллельно колориметрируют контрольный раствор - 2 % метафосфорная кислота с
2,6-дихлорфенолиндофенолом. Интенсивность окраски пропорциональна количеству
аскорбиновой кислоты.
Количественное определение аскорбиновой кислоты можно
провести фотоколориметрическим методом с помощью гексацианоферрита калия. В
кислой среде аскорбиновая кислота восстанавливает гексацианоферрит калия до
гексацианоферрата калия, который в присутствии ионов железа (Ш) образует
берлинскую лазурь, с последующим ее фотоколориметрированием.
Метод количественного определения аскорбиновой кислоты
(по ГФ XI, вып. 2, стр. 294) основан на ее
способности окисляться до дегидроформы раствором 2,6-дихлорфенолиндофенолята и
восстанавливать последний до лейкоформы . Точка эквивалентности устанавливается
появлением розового окрашивания, которое свидетельствует об отсутствии
восстановителя, т. е кислоты аскорбиновой (2,6-дихлорфенолиндофенол имеет в щелочной
среде синее окрашивание, в кислой - красное, а при восстановлении
обесцвечивается): [4]


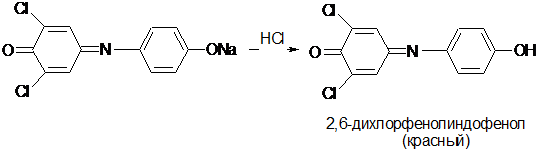
1. Определение содержания аскорбиновой кислоты. (таблица 4). Из грубо измельченной аналитической
пробы плодов берут навеску массой 20 г, помещают в фарфоровую ступку, где
тщательно растирают со стеклянным порошком (около 5 г), постепенно добавляя 300
мл воды, и настаивают 10 мин. Затем смесь размешивают и извлечение фильтруют. В
коническую колбу
вместимостью 100
мл вносят 1 мл полученного фильтрата, 1 мл 2%раствора хлористоводородной
кислоты, 13 мл воды, перемешивают и титруют из микробюретки раствором 2,6-дихлорфенолиндофенолята натрия (0,001 моль/л) до появления
розовой окраски, не исчезающей в течение 30-60 с. Титрование продолжают не более 2 мин. В случае интенсивного окрашивания фильтрата
или высокого содержания в нем аскорбиновой кислоты [расход раствора 2,6-дихлорфенолиндофенолятанатрия
(0,001 моль/л) более 2 мл], обнаруженного пробным титрованием, исходное
извлечение разбавляют водой в 2 раза или более.
Содержание аскорбиновой кислоты в пересчете на абсолютно
сухое сырье в процентах (X)
вычисляют по формуле:
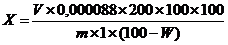
где 0,000088 - количество аскорбиновой кислоты, соответствующее 1мл
раствора 2,6-дихлорфенолиндофенолята натрия (0,001 моль/л), в граммах;
V - объем раствора 2,6-дихлорфенолиндофенолята натрия (0,001 моль/л), пошедшего
на титрование, в миллилитрах; m - масса сырья в граммах; W - потеря в массе при
высушивании сырья в процентах.
Примечания. Приготовление раствора 2,6-дихлорфенолиндофенолята натрия
(0,001 моль/л): 0,22 г 2,6-дихлорфенолиндофенолята натрия растворяют в 500 мл
свежепрокипяченной и охлажденной воды при энергичном взбалтывании (для
растворения навески раствор оставляют на ночь). Раствор фильтруют в мерную
колбу вместимостью 1 л и доводят объем раствора водой до метки. Срок годности
раствора не более 7 сут при условии хранения в холодном, темном месте.
Установка титра. Несколько кристаллов (3-5) аскорбиновой кислоты
растворяют в 50 мл 2 % раствора серной кислоты; 5 мл полученного
раствора титруют из микробюретки раствором 2,6-дихлорфенолиндофенолята натрия
до появления розового окрашивания, исчезающего в течение 1-2 нед. Другие
5 мл этого же раствора аскорбиновой кислоты титруют раствором калия йодата
(0,001 моль/л) в присутствии нескольких кристаллов (около 2 мг) калия йодида и
2-3 капель раствора крахмала до появления голубого окрашивания. Поправочный
коэффициент вычисляют по формуле:
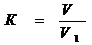
где V - объем раствора калий йодата (0,001 моль/л), пошедшего на
титрование, в миллилитрах; V1-объем раствора 2,6-дихлорфенолиндофенолята
натрия, пошедшего на титрование, в миллилитрах.
. Определение содержания свободных органических кислот. Аналитическую
пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями
диаметром 2 мм. 25 г измельченных плодов шиповника помещают в
колбу вместимостью 250 мл, заливают 200 мл воды и выдерживают в течение 2 ч на
кипящей водяной бане, затем охлаждают, количественно переносят в мерную колбу
вместимостью 250 мл, доводят объем извлечения водой до метки перемешивают. Отбирают
10 мл извлечения, помещают в колбу вместимостью 500 мл, прибавляют 200-300 мл
свеже-прокипяченной воды, 1 мл 1% спиртового раствора
фенолфталеина, 2 мл 0,1 % раствора метиленового синего и титруют
раствором натра едкого (0,1 моль/л) до появления в пене лилово- красной
окраски.
Содержание свободных органических кислот в пересчете на яблочную
кислоту в абсолютно сухом сырье в процентах (X) вычисляют по формуле:

где 0,0067-количество яблочной кислоты, соответствующее 1 мл раствора
натра едкого (0,1 моль/л), в граммах; V - объем раствора натра едкого (0,1
моль/л), пошедшего на титрование, в миллилитрах; m - масса сырья в граммах; W -
потеря в массе при высушивании сырья в процентах. [1]
Таблица
4. Количественное определение аскорбиновой кислоты в плодах шиповника
(фармакопейный метод)
|
Этап определения
|
Сущность
|
Обоснование
|
|
Подготовительный
|
Измельчение сырья и взятие
точной навески
|
Для лучшей экстракции
|
|
Экстракция
|
Водой
|
Аскорбиновая кислота
растворяется в воде
|
|
Очистка
|
Не проводится
|
Водорастворимые
органические кислоты не обладают окислительно-восстановительными свойствами и
не будут мешать определению аскорбиновой кислоты
|
|
Количественное определение
|
Титрование
2,6-дихлорфенолиндофенолятом натрия до устойчивой розовой окраски
|
Способность аскорбиновой
кислоты к окислению
|
Количественное определение химических веществ в цветках календулы.
Каротиноиды определяют в лекарственном сырье
фотоколориметрическим методом, основанном на измерении интенсивности их
природной окраски. Разработан спектрофотометрический метод определения
каротиноидов. Каротиноиды из сырья экстрагируют петролейным эфиром, затем
хроматографируют на пластинке «Силуфол» в системе петролейный
эфир-бензол-метанол (60:15:4), элюируют хлороформом и спектрофотометрируют при
длине волны 464 нм (a-каротин)
при 456 нм (β-каротин). [19]
. Около 1 г (точная навеска) измельченных цветков
ноготков, просеянных сквозь сито с отверстиями размером 1 мм, помещают в
коническую колбу вместимостью 250 мл, прибавляют 50 мл спирта 70 %, колбу
закрывают пробкой, взвешивают (с погрешностью ± 0,01 г) и оставляют на 1 ч.
Затем колбу соединяют с обратным холодильником, нагревают, поддерживая слабое
кипение в течение 2 ч. После охлаждения колбу с содержимым вновь закрывают той
же пробкой, взвешивают и потерю в массе восполняют растворителем. Содержимое
колбы тщательно взбалтывают и фильтруют через сухой бумажный фильтр, отбрасывая
первые 20 мл, в сухую колбу вместимостью 200 мл (раствор А).
мл раствора А помещают в мерную колбу вместимостью 25
мл, прибавляют 5 мл раствора алюминия хлорида, 0,1 мл кислоты уксусной и
доводят объем раствора спиртом 96 % до метки и оставляют на 40 минут (раствор
Б).
Через 40 минут измеряют оптическую плотность
испытуемого раствора Б и раствора стандартного образца Б1 на спектрофотометре в
максимуме поглощения при длине волны (408 + 2) нм в кювете с толщиной слоя 10
мм, используя растворы сравнения для испытуемого раствора и стандартного
образцов.
Содержание суммы флавоноидов в процентах (Х) в пересчете на рутин
вычисляется по формуле:
|
X =
|
А ×50×25×
ао × 1 × 100 × 100
|
=
|
А ×50×
ао × 100
|
|
Ао × а × 1 × 100×25 × (100 - W)
|
|
Ао × а × (100 - W)
|
где:
А - оптическая плотность испытуемого раствора;
Ао- оптическая плотность раствора стандартного образца рутина;
а - навеска сырья, г;
ао- навеска стандартного образца рутина, г;- влажность сырья, %;
Допускается проводить определение содержания суммы флавоноидов с
использованием удельного показателя поглощения рутина.
Примечания
Приготовление спирта 70 %. 70 мл спирта помещают в мерную колбу
вместимостью 100 мл и доводят объем раствора водой до метки и перемешивают.
Спирт 96 %. Этанол 96 %. Спирт этиловый 96% очищенный.
Приготовление алюминия хлорида раствора. 65,0 г алюминия хлорида
растворяют в воде и доводят объем раствора тем же растворителем до 100 мл.
Прибавляют 0,5 г угля активированного, перемешивают в течение 10 мин и
фильтруют. К фильтрату при непрерывном перемешивании прибавляют достаточное
количество 1 % раствора натрия гидроксида (около 60 мл) до получения рН около
1,5.
Приготовление раствора сравнения для стандартного раствора.
К 1,0 мл стандартного раствора А1 прибавляют 0,1 мл уксусной кислоты
раствора, доводят спиртом 96 % до метки в мерной колбе вместимостью 25 мл и
перемешивают (раствор сравнения готовится параллельно с раствором Б1).
Приготовление раствора сравнения для испытуемого
раствора Б. К 1 мл раствора А прибавляют 0,1 мл кислоты уксусной и доводят
спиртом 96 % до метки в мерной колбе вместимостью 25 мл и перемешивают (раствор
сравнения готовится параллельно с раствором Б).
Приготовление раствора СО рутина. Около 0,05 г (точная
навеска) рутина предварительно высушенного при 130-135 °С в течение 3 ч,
помещают в мерную колбу вместимостью 100 мл и растворяют при нагревании на
кипящей водяной бане в 85 мл спирта 96 %, охлаждают, доводят объем раствора тем
же спиртом до метки и перемешивают (раствор А1).
2. Экстрактивные вещества, извлекаемые водой. В соответствии с
требованиями ОФС «Определение содержания экстрактивных веществ в лекарственном
растительном сырье» (таблица 5). Экстрагент - вода очищенная, спирт этиловый 70%.
[18]
Таблица 5. Количественное определение суммы экстрактивных веществ в
цветках ноготков
|
Этап определения
|
Сущность
|
|
Подготовительный
|
Измельчение сырья и взятие
точной навески
|
Для лучшей экстракции
|
|
Экстракция
|
Спирт этиловый 70 %
|
Определяют содержание
веществ, растворимых в спирте, т.к. из данного сырья готовят настойку
|
|
Очистка
|
Не проводят
|
Определяют всю сумму БАВ
|
|
Количественное определение
|
Извлечение упаривают на
водяной бане. Остаток высушивают в сушильном шкафу при 100-105 °С до постоянной
массы и взвешивают
|
Метод весовой
(гравиметрический). Высушенный остаток содержит сумму веществ, извлеченных
спиртом из сырья
|
|
Этап определения
|
Сущность
|
Обоснование
|
Таблица 6.Количественное определение суммы каротиноидов в пересчете на b-каротин (нефармакопейный метод)
|
Этап определения
|
Сущность
|
Обоснование
|
|
Подготовительный
|
Измельчение сырья и взятие
точной навески
|
Для лучшей экстракции
|
|
Экстракция
|
Бензол или петролейный эфир
|
Каротиноиды хорошо
растворяются в органических растворителях
|
|
Очистка
|
Упаривание извлечения на
водяной бане
|
Для удаления пигментов и
других жирорастворимых соединений
|
|
Количественное определение
|
Снятие оптической
плотности. Раствор сравнения - калия бихромат ФЭК
|
Способность каротиноидов
поглощать свет при определенной длине волны
|
Заключение
Углубляя информационные исследования по вопросам
характеристики химического состава, анализа, медицинского применения
лекарственного растительного сырья, содержащего витамины, было рассмотрено
ботанико - морфологическое описание лекарственных растений, содержащих
витамины, былы даны методы качественного и количественного определения сырья
крапивы двудомной, видов шиповника и календулы лекарственной. Были изучены
фармакологические свойства и применение витаминов в медицине.
Лекарственное растительное сырье, содержащее витамины,
и лекарственные средства на его основе обладают широким спектром
фармакологического действия. Основная масса витаминосодержащего лекарственного
растительного сырья используется для получения суммарных препаратов, поливитаминных,
кровоостанавливающих сборов.
Препараты листьев крапивы обладают гемостатическими
свойствами, что связывают с наличием в растении витамина К и хлорофилла.
Галеновые препараты крапивы оказывают стимулирующее влияние на сократительную
активность матки. Препараты крапивы усиливают деятельность пищеварительных
желез, уменьшают метеоризм, обладают желчегонными свойствами, снижают уровень
холестерина в крови. Витамины, хлорофилл и соли железа стимулируют эритропоэз,
повышают уровень гемоглобина и основной обмен, улучшают регенерацию слизистых
оболочек, активизируют сердечно-сосудистую систему и газообмен. Крапива
оказывает общетонизирующее действие.
Препараты плодов шиповника оказывают общеукрепляющее
действие, стимулируют неспецифическую резистентность организма, усиливают
регенерацию тканей и синтез гормонов, уменьшают проницаемость сосудов,
принимают участие в углеводном и минеральном обмене, обладают
противовоспалительными свойствами. Обладают иммуностимулирующим (в отношении
гуморального и клеточного иммунитета) и желчегонным действием (обусловлено
наличием органических кислот и флавоноидов).
Препараты из календулы оказывают противовоспалительное
и ранозаживляющее действие как при наружном применении, так и при приеме
внутрь. Бактерицидные свойства по отношению к стафилококкам и стрептококкам
выражены незначительно. Сумма флавоноидов, каротиноидов и органических кислот
обеспечивает противовоспалительный и капилляроукрепляющий эффекты препаратов,
способствует повышению метаболической функции печени (улучшается состав желчи,
понижается концентрация билирубина и холестерина), повышает секреторную и
выделительную функции, стимулирует репаративные процессы желудочно-кишечного
тракта.
Список литературы
1. Государственная
фармакопея СССР. XI издание. - М.: Медицина. - Вып. 1, 1987. - 336 с. - Вып. 2,
1990. - 400 с.
2. Задорожный
А.М., Кошкин А.Г., Соколов С.Я. Справочник по лекарственным растениям.- М.:
Лесная промышленность, 1988. - 452 c.
. Карпович
В.Н., Беспалова Е.И. Фармакогнозия. - М.: Медицина, 1976. - 448 c.
. Лекарственные
растения государственной фармакопеи / Под ред. И.А. Самылиной, В.А. Северцева.
- М.: "АНМИ", 2003. - 534 с.
5. Лекарственные растения России. Иллюстрационная энциклопедия.
М.:Ээксмо, 2006. - 192 с.
6. Лекарственные
растительные средства / под ред. А.П. Арзамасцева, И.А. Самылиной. - М.:
ГЭОТАР-МЕД, 2002. - 288 с.
. Лекарственное
растительное сырье. Фармакогнозия:Учеб.пособие/ Под ред. Г.П. Яковлева и К.Ф.
Блиновой. - СПб.: СпепцЛит.,2004. - 765с.
. Лекарственные
средства растительного происхождения: справочное пособие / под ред. О.Н.
Денисенко и В.А. Челомбитько. - Пятигорск: Изд. ПятГФА, 2003. - 270 с.
. Лукашук
С.П., Орловская Т.В. Лекарственные растения и сырье, содержащие витамины:
методические указания для студентов. - Пятигорск: Изд-во ПятГФА, 2008. - 68 с.
. Мазнев
Н.И. Энциклопедия лекарственных растений. 3-е изд., исп. И доп. - М: Мартин.
2004. - 496 с.
. Машковский,
М.Д. Лекарственные средства. - 16-е изд. перераб. и доп.- М.: Новая волна,
2012. - 1216 с.
. Методы
фармакогностического анализа лекарственного растительного сырья. В 2-х ч. ч.II. Химический анализ:Учебное пособие /
Г.И.Калинкина [и др.].- Томск: СибГМУ, 2008. - 55 с.
. Минделл
Э. Справочник по витаминам и минеральным веществам. - М.: Эксмо, 2003. - 312 c.
. Муравьева
Д.А., Самылина И.А., Яковлев Г.П. Фармакогнозия: Учебник. - 4-е изд., перераб.
и доп. - М.: Медицина, 2002. - 656 с.
. Практикум
по фармакогнозии: учеб. пособие для студ. вузов / под ред. В.Н. Ковалева. -
Харьков: Изд-во НФаУ: Золотые страницы: МТК-Книга, 2004. - 512 с.
. Растения
для нас: справочное издание / К.Ф. Блинова [и др.]. - СПб.: Изд-во «Учебная
книга», 1996. - 654 с.
. Фармакогнозия.
Атлас / Под. ред. Н.И. Гринкевич, Л.Н. Сафронич. - М.: Медицина, 1983. - 512 с.
. Фармакопейная
статья «Цветки ноготков».ОФС 42-0168-06.
. Фитохимический
анализ лекарственного растительного сырья: учебное пособие / под ред. В.А.
Челомбитько. - Пятигорск: Изд. ПятГФА, 2005. - 173 с.
. Химический
анализ лекарственных растений / Под ред. Н.И. Гринкевич, Л.Н. Сафронич. - М.:
Высшая школа, 1983. - 176 с.