Окисление этилена до этиленоксида
МИНИСТЕРСТВО
ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
РОССИЙСКИЙ
ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ НЕФТИ И ГАЗА ИМ.И.М. ГУБКИНА
Кафедра
технологии химических веществ
Лабораторная
работа №1
ОКИСЛЕНИЕ
ЭТИЛЕНА ДО ЭТИЛЕНОКСИДА
Выполнила:
студентка группы ХТ-12-04
Саврасова Екатерина
Проверил:
К.х.н. Толстых Л.И.
Москва 2014
Окисление этилена с целью производства
этиленоксида является одним из крупнотоннажных производств нефтехимической
промышленности.
Оксид этилена, как правило, непосредственно не
используется, а служит сырьем для производства этиленгликоля и антифризов на
его основе, для производства этаноламинов, полиэтиленгликолей, эфиров
этиленгликоля, неионогенных поверхностно-активных веществ и других важных
продуктов.
В настоящее время практически весь этиленоксид
производят методом прямого окисления этилена на серебряном катализаторе в
газовой фазе.
Серебряный катализатор может представлять собой
сетку из металлического серебра, либо, чаще всего, серебро наносится на твердый
носитель и активируется дополнительно специальными добавками.
Основная реакция окисления:
СН2 = СН2 + О2 СН2СН2О
сопровождается реакцией полного окисления
этилена до диоксида углерода (реакция полного горения):
СН2 = СН2 + 3 О2 2 СО2 + 2 Н2О
Процесс окисления этилена является
каталитическим экзотермическим процессом. Предложены различные механизмы,
объясняющие процессы окисления этилена. Среди них механизм Туига, который
включает элементарные стадии, подразумевающие образование поверхностных
соединений AgO*, AgOO*,
способных вести цепь окисления. Элементарные стадии процесса выглядят следующим
образом:
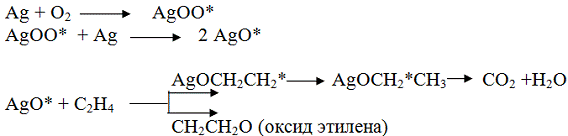
С точки зрения термодинамики нет никаких
ограничений на проведение реакции.
Кинетические уравнения, как правило,
предлагаются в форме уравнений первого порядка по этилену, например, для схемы
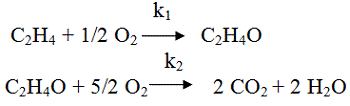
Предложены простые кинетические уравнения
Wi = ki
Cэт
k1 = 8,6 .103 exp(- 8100/ 1,98 T);=
1,85 .106 exp(- 7200/ T);
Эти уравнения справедливы для области 150 - 320
оС, содержание этилена 4%, содержании кислорода в поступающей смеси от 7 - 9 %
для циркуляционного контура до 19 - 20 % для потока без циркуляции.
Однако для относительно низких концентраций
кислорода (7 - 9%) нужно учитывать изменение его концентрации в ходе процесса,
для чего предложено изменить форму кинетических уравнений, учитывая сорбционное
торможение:
Dx/dtt
=(k1+k2) j(x,T) , dy/dt=
k2 j(x,T) ;
j(x,T)
= (1-x)/(1 +8(Cоэ./Скис)(1
- х) + k3(5Соэ + Сдоу)
х - степень превращения этилена, y
- выход (доли) этиленоксида; ci
выражены в % (Соэ=4, Скис =6,5 , Сдоу = 7.
Константа скорости k3
= 3,91.10-4 exp( - 3600 / T).
Для предложенных выше форм кинетических
уравнений и приведенных констант получено хорошее совпадение рассчитываемых и
опытных значений выходов продуктов и конверсии этилена.
При использовании в качестве катализатора
губчатого серебра при атмосферном давлении в области температур 491 - 575 оС
для расчета состава реакционной массы предложены уравнения:
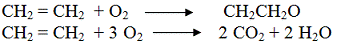
W1= k1Cэт/(Соэ
+ 0,3Cдоу)
W2= k2Cэт/(Соэ
+ 0,3Cдоу)
Для константы скорости k1
: lnko= 9.05 и E=63,8
кДж/моль ;
Для константы скорости k2
: lnko= 13,0 и E=83,0
кДж/моль ;
Особенности процесса.
Основная особенность процесса заключается в том,
что в газе, поступающем на окисление, одновременно присутствуют и этилен и
кислород, т.е. взрывоопасная смесь. Пределы взрываемости этилена в воздухе
составляют 3 - 34 % , а образующегося этиленоксида 3 - 100 % .
При снижении концентрации кислорода повышается
допустимая концентрация этилена в смеси. В промышленности окисление этилена из
соображений безопасности ведут при концентрации этилена 3 - 5 % ,т.е. ниже
нижнего предела взрываемости.
Вторая особенность - очень жесткие требования к
чистоте исходных этилена и воздуха. Для производства этиленоксида в
промышленности используется этилен концентрацией 98 - 99,9 % .
Допустимое содержание примесей в нем не должно
превышать следующих величин:
Ацетилен … 10 ppm
Сернистые соединения
( в пересчете на серу) 1 ppm
Кислород 5 - 20 ppm
Хлориды
(в пересчете на хлор) 1 ppm
Метан 1 % об.
Этан 1 % об.
Ацетилен с катализатором может привести к
образованию взрывоопасных ацетиленидов серебра, сернистые соединения являются
ядами для катализатора, кислород в этилене ограничивают для того, чтобы далее
более точно его дозировать. Это относится и к хлорсодержащим соединениям, так
как для повышения активности катализатора его обрабатывают хлорсодержащими
соединениями в строго дозированных количествах. Нежелательно присутствие в
этилене больших количеств углеводородов С3 и выше, так как они легко окисляются
до углекислоты и воды, а выделяющееся при этом тепло нарушает тепловой режим
реактора. В то же время, температуру в реакторе надо поддерживать с большой
точностью, и колебания температуры не должны превышать ± 10 оС. Это объясняется
тем, что основные показатели процесса - конверсия, селективность и активность
катализатора - очень сильно зависят от температуры.
К воздуху, поступающему на окисление,
предъявляются не менее жесткие требования.
Один из вариантов приготовления катализатора
заключается в следующем:
Готовят плавленную окись алюминия с очень низкой
удельной поверхностью 0,05 - 040 м2/г и пористостью 30 - 45 %. Гранулы
предварительно подвергают механической обработке, а затем на них наносят слой
активного серебра. Такой катализатор отличается тем, что его активность
сосредоточена главным образом на поверхности, тогда как активность в порах
зерна незначительна. Это улучшает теплоотводящие свойства катализатора и
предотвращает его спекание. Такой катализатор может работать как в
стационарном, так и в кипящем слое.
В данной лабораторной работе используется
стационарный слой катализатора.
Исходные данные
|
№
|
Температура,
оС
|
Концентр.
этилена, % об
|
Время
контакта, с
|
Интервал
отбора проб, с
|
|
4
|
235
|
4
|
1
|
0,1
|
Результаты.
|
сек
|
Этилен
|
Оксид
|
СО2
|
H2O
|
О2
|
N2
|
|
0
|
4,00
|
0
|
0
|
0
|
20,16
|
75,84
|
|
0,1
|
3,03
|
0,90
|
0,13
|
0,13
|
19,39
|
76,42
|
|
0,2
|
2,30
|
1,48
|
0,44
|
0,44
|
18,32
|
77,02
|
|
0,3
|
1,75
|
1,82
|
0,87
|
0,87
|
17,06
|
77,62
|
|
0,4
|
1,32
|
1,99
|
1,37
|
1,37
|
15,73
|
78,21
|
|
0,5
|
1,00
|
2,05
|
1,90
|
1,90
|
14,39
|
78,76
|
|
0,6
|
0,76
|
2,02
|
2,43
|
2,43
|
13,07
|
79,28
|
|
0,7
|
0,58
|
1,95
|
2,95
|
2,95
|
11,82
|
79,76
|
|
0,8
|
0,44
|
1,84
|
3,44
|
3,44
|
10,64
|
80,20
|
0,33
|
1,72
|
3,90
|
3,90
|
9,54
|
80,60
|
|
1
|
0,25
|
1,58
|
4,33
|
4,33
|
8,54
|
80,96
|
Обработка результатов.
Таблица 2. Молекулярная масса веществ,
содержащихся в контактном газе
|
Вещество
|
Молек.
Масса
|
|
Этилен
|
28
|
|
Оксид
этилена
|
44
|
|
СО2
|
44
|
|
H2O
|
18
|
|
О2
|
32
|
|
N2
|
28
|
Таблица 3. Массовый состав контактного газа
|
сек
|
Этилен
|
Оксид
|
СО2
|
H2O
|
О2
|
N2
|
|
0,0
|
112,00
|
0,00
|
0,00
|
0,00
|
645,12
|
2123,52
|
|
0,1
|
84,84
|
39,60
|
5,72
|
2,34
|
620,48
|
2139,76
|
|
0,2
|
64,40
|
65,12
|
19,36
|
7,92
|
586,24
|
2156,56
|
|
0,3
|
49,00
|
80,08
|
38,28
|
15,66
|
545,92
|
2173,36
|
|
0,4
|
36,96
|
87,56
|
60,28
|
24,66
|
2189,88
|
|
0,5
|
28,00
|
90,20
|
83,60
|
34,20
|
460,48
|
2205,28
|
|
0,6
|
21,28
|
88,88
|
106,92
|
43,74
|
418,24
|
2219,84
|
|
0,7
|
16,24
|
85,80
|
129,80
|
53,10
|
378,24
|
2233,28
|
|
0,8
|
12,32
|
80,96
|
151,36
|
61,92
|
340,48
|
2245,60
|
|
0,9
|
9,24
|
75,68
|
171,60
|
70,20
|
305,28
|
2256,80
|
|
1,0
|
7,00
|
69,52
|
190,52
|
77,94
|
273,28
|
2266,88
|
Таблица 4. Основные показатели процесса
|
Сек
|
Этилен
|
Оксид
|
Конверсия,
%
|
Выход
ОЭ , %
|
Селективность,
%
|
|
0,0
|
4,00
|
0,00
|
0,00
|
0,00
|
0,00
|
|
0,1
|
3,03
|
0,90
|
24,25
|
22,50
|
92,78
|
|
0,2
|
2,30
|
1,48
|
42,50
|
37,00
|
87,06
|
|
0,3
|
1,75
|
56,25
|
45,50
|
80,89
|
|
0,4
|
1,32
|
1,99
|
67,00
|
49,75
|
74,25
|
|
0,5
|
1,00
|
2,05
|
75,00
|
51,25
|
68,33
|
|
0,6
|
0,76
|
2,02
|
81,00
|
50,50
|
62,35
|
|
0,7
|
0,58
|
1,95
|
85,50
|
48,75
|
57,02
|
|
0,8
|
0,44
|
1,84
|
89,00
|
46,00
|
51,69
|
|
0,9
|
0,33
|
1,72
|
91,75
|
43,00
|
46,87
|
|
1,0
|
0,25
|
1,58
|
93,75
|
39,50
|
42,13
|
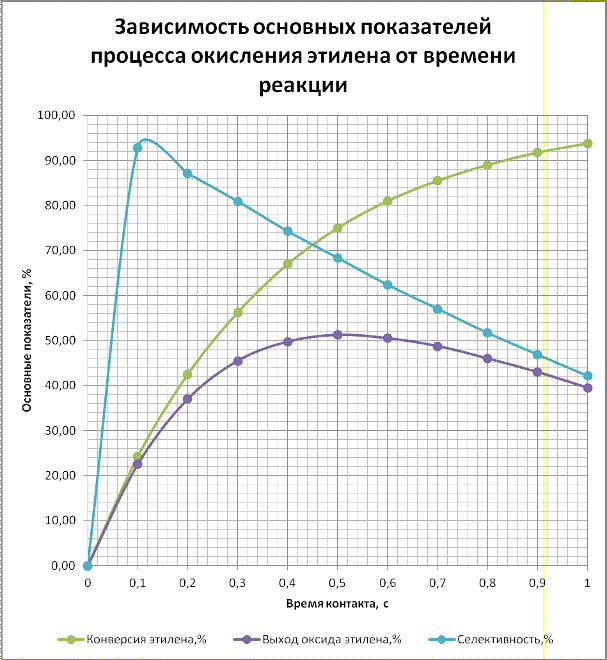
Таблица 5. Материальный баланс получения оксида
этилена окислением этилена
|
|
Масса,
г
|
%,
масс
|
|
Взято
|
|
Этилен
|
112,00
|
3,89
|
|
О2
|
645,12
|
22,40
|
|
N2
|
2123,52
|
73,72
|
|
Итого
|
2880,64
|
100,00
|
|
Получено
|
|
Этилен
|
7,00
|
0,24
|
|
Оксид
|
69,52
|
2,41
|
190,52
|
6,61
|
|
H2O
|
77,94
|
2,71
|
|
О2
|
273,28
|
9,49
|
|
N2
|
2266,88
|
78,69
|
|
Всего
|
2880,20
|
99,98
|
|
Потери
|
0,44
|
0,02
|
|
Итого
|
2880,64
|
100,00
|
Вывод
окисление
этилен этиленоксид
Проанализировав полученные результаты можно
сделать вывод, что конверсия этилена увеличивается с увеличением времени
контакта. селективность процесса максимальна при времени контакта 0,1 с и
уменьшается с увеличением конверсии процесса, что связано с протеканием реакции
окисления оксида этилена до углекислого газа и воды Выход ОЭ сначала
возрастает, но при времени контакта более 0,5 с начинает убывать, так как в
реакционной массе увеличивается концентрация оксида этилена и проходит реакция
его полного окисления.
Таким образом, при проведении эксперимента при
235°C
будут наблюдаться соответствующие закономерности. Следовательно, оптимальным
временем контакта будет 0,5 с, при котором будет достигнут максимальный выход
ОЭ.