Технологія виробництва інтерферону
НАЦІОНАЛЬНИЙ
АВІАЦІЙНИЙ УНІВЕРСИТЕТ
ІНСТИТУТ
ЗАОЧНОГО ТА ДИСТАНЦІЙНОГО НАВЧАННЯ
КАФЕДРА
БІОТЕХНОЛОГІЇ
КУРСОВА
РОБОТА
з
дисципліни «Технологія імунобілогічних препаратів»
на
тему: «Технологія виробництва інтерферону»
Виконала: студентка групи
БР-401з
Батуєва І.І.
.051401 «Біотехнологія»
Київ
- 2016
ВСТУП
Інтерферон є одним із сучасних
засобів терапії та профілактики вірусних захворювань. Процес отримання
інтерферону є не тільки дуже важливим для медицини, а й технологічно складним.
Найголовнішою характеристикою отриманого препарату, крім йому властивих, є
якість. Лікарські препарати повинні бути не тільки ефективні у використанні,
але також і безпечні для людини, тому процес виробництва інтерферону повинен
бути організований з чітким дотриманням технології..
Об’єктом дослідження даної роботи є
інтерферон - біологічно активний білок, який відносять до класу цитокінів.
Інтерферон продукується клітинами організму у відповідь на вірусну хворобу. Він
забезпечує противірусний захист організму, володіє протизапальною,
імуномоделюючою, протипухлинною, радіопротективною та антиміотичною дією.
Предметом дослідження є технології виробництва інтерферонів.
Метою є огляд найпоширеніших
технологій виробництва інтерферону, їх аналіз та порівняння, зіставлення рівнів
продуктивності методів, їх трудомісткість.
1. Природа
інтерферону
інтерферон фармакокінетичний рекомбінантний немодифікований
Інтерферони - група
низькомолекулярних білків, які володіють рядом спільних біологічних
властивостей, головною з яких є здатність при контакті з клітинами викликати в
них стійкість до вірусних інфекцій. Їх молекулярна маса становить 22*103 -
94*103 дальтон. Інтерферон
був відкритий А.Айзексом і Ж. Ліндеманом в 1957 році в клітинах курча, яке було
заражене грипом.
Інтерферони хребетних і, також,
людини розділяють на три групи: α-,
або лейкоцитарні, β-,
або фібробластні, та γ-
, або імунні (продукуються Т-лімфоцитами). Найбільш сильним є γ-інтерферон.
Ці групи інтерферонів розрізняють за структурою молекул, низкою біологічних
властивостей і типом клітин, які його продукують в організмі.
Деякі характеристики інтерферонів
людини наведено в таблиці 1.1.
Таблиця 1.1. Деякі характеристики
інтерферонів людини
|
Тип інтерферона
|
Характеристика
|
|
Клітинипродуценти
|
Індуктор
|
Число генів інтер-фе-рона
|
Локалізація в хромосомах
|
Наявність нітронів в генах
|
Стабіль-ість при рН2
|
Число амінокислот
|
Мол. маса, кДа
|
|
|
|
|
|
|
|
В первинній молекулі
|
В кінцевій молекулі
|
|
|
α
|
Лейкоцити переферичної крові
|
Вірусна дволанцюгова РНК
|
14
|
9
|
-
|
Так
|
166
|
143
|
17
|
|
β
|
Фібробласти
|
____
|
2 (або 5)
|
9, 2, 5
|
-
|
Так
|
166
|
145
|
17
|
|
γ
|
Лімфоцити
|
Мітогени та антигени
|
1
|
12
|
+
|
Ні
|
166
|
146
|
17
|
Інтерферони β
і γ є глікопротеїнами,
а інтерферон α
- протеїном.
Інтерферони - клітинні білки, і тому
вони є видоспецифічними, тобто кожному виду тварин властивий свій інтерферон.
Але в свою чергу, інтерферони не є вірусоспецифічними. Є винятки такої
специфічності: інтерферон людини захищає клітини великої рогатої худоби краще,
ніж коров’ячий інтерферон [1, 2, 3].
Слід зазначити, що у кожного виду
тварин є декілька α-інтерферонів
(зокрема, у людини знайдено 14 різних генів α-інтерферонів),
один або кілька β-інтерферонів
і завжди один γ-інтерферон.
На рис.1.1 наявна послідовність гену α-інтерферона
людини і виведена відповідна структура білка, який містить 166 амінокислотних
залишків. З послідовності нуклеотидів можна побачити, що на початковому етапі
синтезується попередник інтерферону, який містить сигнальний пептид з 23
залишків амінокислот. Сигнальний пептид відщеплюється в результаті процесингу
при секреції білку. Аналогічно β-
і γ-інтерферони
синтезуються у вигляді попередників.
α-
і β-Інтерферони є
типовими глобулярними білками (вміст α-спіральних
структур 40-75%). В α-інтерферонах
було знайдено два дисульфідні зв’язки [4].
Встановлено, що індукторами
інтерферонів можуть бути: інактивовані температурою або ультрафіолетом віруси
грипу, рео-, рота- та інші віруси; деякі поліаніонні речовини (бактеріальні
ендотоксини, полікарбонові кислоти, кополімери пірану); синтетичні дволанцюгові
полірибонуклеотиди. Відомо, що дволанцюгова РНК стимулює утворення інтерферону
[3].
Гени, що кодують IFN-α
та IFN-β
локалізовані на 9-й хромосомі каріотипу людини, ген IFN-γ
- на 12-й хромосомі [5].

Рис. 1.1 Послідовність амінокислот в
α-інтерфероні
людини та нуклеотидів, що кодують білок
Інтерферони викликають стан
несприйнятливості до широкого спектра вірусних інфекцій, що індукується у всіх
клітинах, які мають рецептори до інтерферонів. Вони індукують як локальні, так
і системні противірусні реакції в інших клітинах. Крім того, інтерферони
володіють ще двома важливими властивостями: пригнічують поліферацію клітин (і,
таким чином, потенційно є протипухлинним засобом) і модулюють імунну систему.
Інтерферони синтезуються і
секретуються одними клітинами і проявляють свій ефект, діючи на інші клітини. В
цьому відношенні вони подібні до гормонів [4].
Інтерферони становлять першу «лінію
оборони» проти вірусів, яка діє ще до того, як імунні механізми виявляються
повністю задіяні. Інтерферони не мають специфічності відносно вірусів і
пригнічують репродукцію різних вірусів, чутливість яких неоднакова.
Противірусна активність інтерферонів реалізується через гальмування попадання
вірусної частинки в клітину, інгібування синтезу мРНК і трансляції вірусних
білків, також через блокування процесів складання вірусної частинки і її виходу
з інфікованої клітини. Вважається, що гальмування синтезу вірусних білків - це
основний механізм противірусної дії інтерферонів.
У результаті зв'язування молекул
інтерферонів зі специфічними інтерфероновими рецепторами на поверхні клітин
відбувається активація групи генів, локалізованих у людини в 21-й хромосомі.
Цей процес супроводжується формуванням понад 20 нових внутрішньоклітинних білків,
що сприяють виникненню резистентності до вірусів і яких немає в клітинах, що не
піддались впливу інтерферонів [6].
Серед цих ферментів можна виділити 2’,5’-олігоаденілатсинтетази
та протеїнкінази. Обидва ферменти проявляють свою активність у присутності
дволанцюгових РНК, а саме такі РНК є продуктами реплікації багатьох вірусів або
вони наявні у віріонах. Перший фермент синтезує 2’,5’-олігоаденілати (з АТФ),
які активують клітинну рибонуклеазу-1. Другий фермент фосфорилює фактор
ініціації трансляції IF-2.
Інтерферон також активує фосфодиестеразу, що розщеплює частину тРНК і, таким
чином, попереджає подовження пептидних ланцюгів. Кінцевим результатом цих
процесів є інгібування біосинтезу білка і розмноження вірусів в інфікованій
клітині, а потім - її лізис. Механізм дії інтерферону показано на рис.2.1.
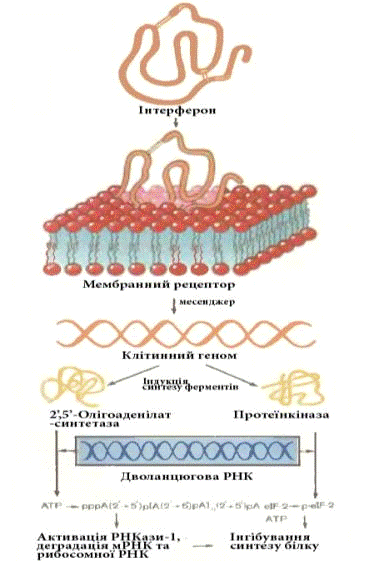
Рис. 2.1 Механізм дії інтерферону
Деякі віруси здатні протистояти дії
інтерферонів, блокуючи синтез або гальмуючи активність індукованих інтерфероном
білків. Таким чином, під впливом інтерферонів у клітині синтезується два
ферменти, один із яких гальмує синтез вірусних білків, інший - розщеплює
створені вірусні РНК. У результаті цього нові вірусні частинки або взагалі не
формуються, або їх кількість зменшується в багато десятків або сотень разів.
Ефективність дії інтерферонів
залежить під природи й функціонального стану систем, які модифікуються ними:
від наявності (або відсутності) рецепторів до інтерферону на поверхні клітини,
від рівня продукування внутрішньоклітинних молекул-посередників, які реалізують
індукований інтерфероном каскад реакцій; оптимізація терапевтичних схем,
зокрема підбір дози, шляхи введення, тривалість інтерферонотерапії та її
об’єднання з іншими лікувальними діями (лікарськими препаратами) [6].
3.
Виробництво інтерферону
.1
Виробництво лейкоцитарного інтерферону
За цією технологією можна отримати
1мкг інтерферону з 1л донорської крові, що становить одну дозу [10].
Цей метод добування інтерферону є
першим із запропонованих. Він базується на використанні донорської крові, і був
запропонований К.Кантеллом в 1977 році. При цьому лейкоцити інкубуються разом
із вірусом (наприклад, вірус Сендай або вірус хвороби Ньюкасла), а в якості
компонента поживного середовища слугує сироватка крові людини або бика (іноді -
казеїн молока). Далі суміш очищують за допомогою хроматографічних методів і
отримують достатньо концентрований препарат інтерферону
[4].
В якості клітин-продуцентів
інтерферону використовують лейкоцити людини, виділені з донорської крові,
лейкоцитарної або еритроцитної маси. Для індукції інтерферону використовується
вірус хвороби Ньюкасла, штам «Н», у вигляді неочищеної алантоїсної рідини із
вірусом [11].
Для отримання великих кількостей ІФН
використовують шестиденні одношарові культури клітин курячого ембріона або
культивовані лейкоцити крові людини, заражені певним видом вірусу. Іншими
словами, для отримання ІФН створюють певну систему вірус-клітина
[12].
Весь технологічний процес проводять
в колбах, матрацах або бутелях. Регламентом не передбачено очищення інтерферону
від баластних білків. Як показує практика роботи підприємств і товариств із
великим об’ємом випуску препарату, діючий Регламент більш прийнятний при
виготовленні інтерферону в малих кількостях.
Підприємства, які перероблюють за
день від 30 до 100 л донорської крові та таку ж кількість суспензії лейкоцитів
на інших етапах технологічного процесу, першими виявили недоліки отримання
інтерферону в матрацах, колбах або бутелях. Цими недоліками є дуже велика
трудомісткість, багатостадійність технології, великий об’єм ручної праці,
відсутність можливості автоматизації окремих технологічних процесів.
При веденні в матрацах або бутелях
стадії праймингу, індукції та біосинтезу інтерферону, враховуючи відсутність
автоматичного контролю та підтримання температурних параметрів суспензії,
призводить до отримання інтерферону з різною противірусною активністю, що в
свою чергу відбивається на собівартості та рентабельності препарату.
Іншим недоліком даної технології є
відсутність стадії очищення інтерферону від чужорідних антигенів (тобто,
вірусного індуктора, білків алантоїсної рідини, включаючи овальбумін).
Присутність чужорідних антигенів в інтерфероні для ректального використання
може викликати сенсибілізацію організму до цих антигенів, особливо до овальбуміну.
Після відкриття в 80-х роках
лімфотропних вірусів, в тому числі вірусу імунодефіциту людини (ВІЛ), що
викликає синдром набутого імунодефіциту людини (СНІД) та можливе зараження
людей через кров або препарат, виготовлений з такої крові, гостро поставило
питання про введення стадії очистки і додаткових методів інактивації можливих
вірусів-контамінантів в нативному ЧЛІ для назального використання.
Існуючі методи очистки інтерферону є
достатньо трудомісткими і мало придатні для очистки великих об’ємів
інтерферону. Так, наприклад, в технології виготовлення препарату інтерферону
для ін’єкцій використовують багатоетапну процедуру осаджування білків роданідом
калію з фракціонуванням в етанолі, контролюючи при цьому рН. Метод при
1000-кратній концентрації ЧЛІ дозволяє в 100 разів його очищувати з 60% виходом
кінцевого продукту.
Інший відомий метод очистки
інтерферону від домішок - використання імуносорбції. Інтерферон специфічно
адсорбували з суміші білків на імуносорбенті, з іммобілізованими антиінтерфероновими
імуноглобулінами, із подальшим елююванням. Був описаний метод очистки
інтерферону шляхом його осаджування сульфатом амонію із подальшим розчиненням
осаду в 2-8 М сечовині і далі гель-фільтрацією на колонці з гелем Акрилекс II-60.
Інші дослідники осаджували
інтерферон трихлороцтвою кислотою і проводили хроматографію розчиненого осаду
на колонці з Сефадексом G-100.
Однак, усі вказані методи дозволяють
отримувати високочисті препарати інтерферону з достатньо високим виходом за
противірусною активністю, але із втратами інших біологічно активних білків, які
продукуються лейкоцитами на стадії біосинтезу інтерферону.
Іншим недоліком є те, що достатньо
важко в промисловому масштабі проводити роботи з хроматографічним обладнанням
при великому об’ємі виробництва інтерферону.
Слід також зазначити, що традиційні
шляхи очищення від контамінуючих домішок, включаючи алантоїсні білки, які
видаляють на стадії готового препарату, є достатньо трудомісткими, технічно
складними, тривалими та недоречні для виробництва у великому масштабі [11] .
Даним способом виробляють такі
препарати: Інтерферон, Інтерлок. Їх призначають для лікування вірусних
захворювань, лейкозу, злоякісної меланоми, раку нирок, карциноїдного синдрому
(Інтерферон), вірусних захворювань очей, гепатитів (Інтерлок).
Інтерферон-β
виготовляють шляхом суперпродукції фібробластів людини стимулятором у
присутності інгібіторів обмінних процесів. Препарат має противірусну,
імуномодулюючу дію та протипухлинну активність. Призначається при виявленні
хронічних вірусних інфекцій в офтальмології, гінекології та урології,
дерматології, гематології, онкології.
При тривалому прийомі інтерферону в
організмі виробляються антитіла до інтерферону, що робить його нездатним до
боротьби з вірусами. Причина цих явищ криється в наявності альбуміну в
препаратах на основі інтерферону.
Альбумін отримують з крові, тому
існує ризик (хоч і мінімальний) зараження гепатитом та іншими хворобами, що
передаються через кров [12].
3.2
Виробництво рекомбінантного інтерферону
Радикальним рішенням стало вирішення
проблеми добування інтерферону використовуючи методи генної інженерії. Зокрема,
гени інтерферону вдалося еспресувати в різних клітинах, наприклад, в клітинах
бактерій, дріжджів та ссавців [4].
В наш час інтерферон отримують
переважно з використанням генно-інженерних штамів Escherichia
coli,
з 1л культури кишкової палички отримують близько
тисячі
доз продукту [10].
3.2.1
Технологія виготовлення рекомбінантного α-2
інтерферону
Субстанція інтерферону α-2
виготовляється переважно шляхом біосинтезу штаму Escherichia
coli,
у який вбудовано ген інтерферону людини. Вектором для проходження трансформації
бактеріального геному є бактеріофаг. Іноземні аналоги, як і більшість інших
генно-інженерних продуктів, виготовляють за технологією, де ампліфікатором
цільового гена слугують плазміди. Плазмідозалежні технології є
високопродуктивними, проте мають істотний недолік: цільовий продукт утворює в
клітині нерозчинні у воді кристалоподібні форми - «тільця включення».
Процес виготовлення й очищення
інтерферону в плазмідній технології складається з таких стадій: формування
клітинної біомаси, її дезінтеграція; розчинення «тілець включення» шляхом
денатурації білкових структур за допомогою сечовини або гуанідинхлориду;
ренатурація денатурованих молекул інтерферону; очищення [6].
До інтерферону α-2
людини відносять два алельні варіанти: інтерферон α-2b
та інтерферон α-2а,
які відрізняються в області коду однією нуклеотидною заміною в позиції 137 (2a:
A,
2b:
G),
що призводить до амінокислотної заміни (2a:
Lys,
2b:
Arg)
[13].
Рекомбінантна плазміда рТТКм містить
вставку повнорозмірного гена лейкоцитарного інтерферону α-2b
людини і ген Kan (аміноглікозид фосфотранстфераза). Синтез цільового гена
регулюється триптофановим промотором. Плазміда рЕТ24 виготовлена на основі
експресуючого вектора рЕТ24а ("Novagen"), транскрипція структурного
гена в якому регулюється промотором lac-оперона. Рекомбінантна плазміда рЕТ24,
містить ген Кan і послідовність,
що кодує Т7 термінатор транскрипції.
Компетентні клітини за стандартною
методикою отримують з використання CaCl2. Клітини, трансформовані відповідно
рекомбінантними плазмідами рТТКм і рЕТ24, висівають газоном на чашки Петрі з
агаризованим середовищем LB, яке містить необхідні антибіотики в кінцевій
концентрації. Ізольовані клони-трансформанти використовують для отримання
інокулята, який вирощують при температурі 30°С протягом 16-18 годин.
Штам-продуцент E.coli BLR-IFN/pET24
вирощують на поживних середовищах LB (0,5% дріжджового екстракту, Мerck, 1,5%
триптонної води, Мerck, 0,5% г NaCl, Merck), TB (10% дріжджовий екстракт,
Мerck, 10% пептон, Мerck, 5мМ гліцерин, Мerck, 72 мМ К2НРО4, Мerck, 17 мМ
КН2РО4, Мerck) №3 (10% дріжджового екстракту, Мerck, 10% гідролізат казеїну,
Мerck, 5мМ гліцерин, 1 мМ MgSO4, 90 мкМ CaCl2), амінопептид (Самсон-Мед,
Росія). Синтез гена рекомбінантного ІФН α-2b
індукують різними концентраціями ізопропіл-β-D-тіогалактопіранозіду
(ІПТГ) від 0,1мм до 1 мМ. Посівний матеріал у співвідношенні 1:50 вносять в
свіже живильне середовище LB з відповідними антибіотиками. Ріст бактерій
контролюють шляхом вимірювання оптичної щільності клітин на спектрофотометрі. В
якості хімічного індуктору механізму біосинтезу рекомбінантного білка в
культуральне середовище додають індуктор - ізопропіл-β-D-тіогалактопіранозід
(ІПТГ) до кінцевої концентрації 1 мМ.
Ферментацію проводять при
температурі 37°С. Час накопичення біомаси та цільового білка складає близько 4
годин в умовах інтенсивної аерації при перемішуванні (220 об/хв). Вивчають
динаміку зростання бактеріальної культури методом вимірювання оптичної
щільності відібраних аліквот протягом усього культивування через кожну годину.
По закінченню процесу ферментації клітинну біомасу збирають центрифугуванням
при 11000 об/хв протягом 15 хвилин.
Лізис клітин-продуцентів проводять
обробкою лізоцимом і ДНК-азою у присутності іонів Mg2+. Тільця включення
збирають центрифугуванням при 11000 об/хв протягом 25 хвилин.
Схеми очищення тілець включення
рекомбінантного ІФН α-2b
з різних продуцентів BLIFN/pTТКм і BLR-IFN/pET24 мають відмінності. Тільця
включення α2b-IFN
/ рТТКм оброблюють серією відмивочних розчинів, що мають у своєму складі:
детергенти (тритон Х-100, твін-20), сечовину і ізопропанол. Розчинення тілець
включення проводять в розчині: 6 М гуанідин, 10 мМ дитіотреітолу, 20 мМ
Тріс-НСl, рН-8,0. Для тілець включення рα2b-IFN/рЕТ24а
була розроблена схема очищення відмивочними розчинами, що містять: детергент
(дезоксихолат натрію), ЕДТА. Розчин для розчинення тілець включення містить 8 М
сечовину, 20 мМ Тріс-НСl, рН-8,0, 10 мМ ДТТ, 1 мМ ЕДТА. Рефолдинг проводили в
буфері наступного складу: 20 мМ Тріс-НСl, рН-8,0, 70 мМ NaCl, 0,1% Тритон
Х-100, 0,1% твін-20, 5 мМ ДТТ.
Ренатурацію проводять на магнітній
мішалці протягом 16-ти годин при температурі +40°С. Концентрований розчин
тілець включення рα2b-IFN/рТТКм
розводять в 50 разів буфером наступного складу: 20 мМ Тріс-НСl, рН-8,0, 70 мМ
NaCl, 0,1% Тритон Х-100, 0,1% твін-20. Розчин центрифугують. В якості робочої
фракції використовують надосадок. Для рефолдингу розчин рα2b-IFN/pET24
розбавляють в 50 разів в буфері наступного складу: 20 мМ Тріс-НСl, рН-8,0, 70
мМ NaCl, 0,1% Тритон Х-100, 0,1% твін-20, 5 мМ ДТТ.
Хроматографічну очистку ІФН зазвичай
здійснюють в три стадії. Отриманий ренатурований ІФН на першому етапі піддають
очищенню за допомогою сорбенту СМ - Тoyopearl-650M. На другій стадії
хроматографічної очистки розчин ІФН наносять на сорбент ДЕАЕ - Тoyopearl-650M.
Очистку мономерної форми ІФН від залишків полімерних форм ІФН проводять
гель-фільтрацією на смолі типу TSK-гель «Тоyopearl» HW-55.
Антивірусну активність очищеного
рекомбінантного ІФН α-2b
оцінюють за пригніченням цитопатичної дії (ЦПД) тест-вірусу - вірусу
везикулярного стоматиту (ВВС, штам Індіана, Депозитарій Інституту мікробіології
і вірусології ім. Д.К. Заболотного НАН України).
У 96-лункові планшети зі сформованим
моношаром клітин L929 вносять послідовно два рази розведені зразки і зразки
міжнародного стандарту ІФН людини. Через 24 години клітини інфікували ВВС в
дозі 100 ТЦД50, залишаючи лунки для контролю вірусу (необроблені клітини,
інфіковані ВВС) і для контролю клітин (необроблені клітини, неінфіковані ВВС).
Планшети культивують при 37°С протягом 24 год в насиченій Н2О атмосфері з
постійним рівнем СО2 (5%). Отримані результати беруть до уваги тільки за умови,
якщо в контрольних лунках цитодеструктивних змін не було, а в контролі вірусу
спостерігають повну деструкцію клітин.
Облік кількості живих клітин
проводять після їх забарвлення кристалічним фіолетовим. Для цього з лунок
видаляють надосадову рідину, а до клітин на 15 хв вносять 0,2% розчин барвника
Crystal Violet в 2% етанолі. Барвник видаляють, а пофарбований моношар клітин
промивали водою.
Титром ІФН вважають значення,
зворотне максимальному розведенню зразка, що забезпечує захист 50% клітин від
ЦПД вірусу. Титр ІФН виражали в log2(розведення)-1, кількісно біологічну
активність визначають, порівнюючи активність досліджуваного розчину і
міжнародного стандарту ІФН.
Використовують такі бактеріальні
штами Escherichia coli: BL21 (DE3) B F- dcm ompT hsdS (rB- mB-) gal λ
(DE3), і Escherichia coli BL21(DE3) CodonPlus-RIL (F- ompT hsdS (rB-mB-) dcm
gal λ (DE3) endA Hte
[argU ileY leuW Camr], Origami
B
та ін [14, 15].
З використанням плазмідної
технології також ампліфікують ген інтерферону в клітинах дріжджів Saccharomyces
cerevisiae.
Ген ІФН α-2b
людини ампліфікують в реакції ПЛР з використанням праймерів N466
(ataccatggaaaagagatgtgatctgcctcaaacccacagcctaggtagccgt)
та N467
(atctcgagtcattcttacttcttaaggattgcaagttt).
Матрицею слугує ДНК плазми. Отриманий в результаті ампліфікації фрагмент ДНК
розміром 510 послідовностей піддають елююванню з агарного гелю, оброблюють
рестриктазами NcoI та XhoI
і клонують в лабораторній плазміді. В результаті отримують нову робочу
плазміду, яку розщеплюють по сайтах NcoI
та
XhoI. Найбільший з отриманих фрагментів ДНК, що несе
векторну частину плазміди і послідовність, що кодує пре-про область α-фактора
дріжджів, злиту с послідовністю, яка кодує промоторну ділянку гена GAL1
дріжджів, яку називають фрагмент-1. Потім, використовуючи для ПЛР праймери N449
(5’-atatagatctccagtcaacactacaa)
і стандартний зворотній pUC-праймер,
який називають N169
(5’-gagcggataacaatttcacacagg),
ампліфікують фрагмент ДНК плазміди, що містить послідовність про-ділянки α-фактора
дріжджів та злитий з ним ген інтерферону. Ампліфікований фрагмент ДНК
розщеплюють за унікальними кінцевими сайтами BglII
та XhoI
і називають фрагментом-2. Потім, в результаті випалювання один на одного двох
синтетичних олігонуклеотидів N573
(5’-gatccgaattccaa)
отримують синтетичний адаптер, що називають фрагментом-3. В результаті
спільного лігування трьох отриманих фрагментів ДНК отримують плазміду pUC18x-GAL1pFF-IFN2b.
Також можна отримати ген лідерного поліпептиду, що мітить потрійну про-ділянку α-фактора
дріжджів S. cerevisiae.
Джерелом гену інтерферону α-2a
людини
слугує плазміда pUC18x-GAL1ppI-IFN2a, яка
побудована аналогічно до pUC18x-GAL1pFFF-IFN2b, тільки
замість праймера N466 використовують
N617
(agcctaggtagccgtcggtaccttgatgctcctggcacagatgcgtaagatctctctttt).
Ампліфікований фрагмент ДНК розміром 480 послідовностей піддають елююванню з
агаризованого гелю, оброблюють рестриктазами XmaJI
та XhoI
і клонують в плазміді pUC18x-GAL1ppI-IFN2b,
яка розщеплена за тими ж ділянками. В ході побудови у складі векторів експресії
pPDX3-F-2b,
pPDX3-FF-2b
або pPDX-FFF-2b
ген інтерферону α-2b
людини заміщують на ген інтерферона α-2a
людини. Для цього зі складу вектора pPDX3-F-2b,
pPDX3-FF-2b
або pPDX-FFF-2b
вищеплюють унікальний NcoI/XhoI
фрагмент ДНК, який включає ген інтерферону α-2b
людини, а векторний залишок лігують з NcoI/XhoI
фрагментом ДНК плазміди pUC18x-GAL1ppI-IFN2a,
що кодує ген інтерферону α-2a
людини. В результаті отримують вектори експресії pPDX3-F-2a
або pPDX3-FF-2a
або pPDX3-FFF-2a,
відповідно.
Отримані вектори експресії несуть у
своєму складі ген зрілого інтерферону α-2a
людини, який злитий із послідовностями лідерних поліпептидів, що містить у
своєму складі одинарну, подвоєну чи потроєну про-ділянки α-фактору
дріжджів, відповідно.
Для аналізу рівня секреції
інтерферону α-2a
людини клітини отриманих штамів SCR-F-2b,
SCR-2b-FF,
SCR-2b-FFF,
SCR-2a-F,
SCR-2a-FF
та SCR-2a-FFF
культивують на середовищі YPD
наступного складу (в мас.%): пептон-2, дріжджовий екстракт-1, глюкоза-2,
агар-2, вода-інше, протягом 44 годин при 28°С на роторній качалці зі швидкістю
250 об./хв. Накопичення інтерферону в культуральній рідині аналізують,
використовуючи метод електрофорезу в ПААГ і метод аналітичної оберненофазної
хроматографії.
Результати аналізу (рис.3.2.1.1)
показують, що штами SCR-2b-FF
і SCR-2a-FF,
секреція інтерферону α-2
в яких направляється новими лідерними поліпептидами, що містять у своєму складі
подвоєну про-ділянку α-фактора
дріжджів, а також штами SCR-2b-FFF
і SCR-2a-FFF,
секреція інтерферону α-2
в яких направляється новими лідерними поліпептидами, що несуть у своєму складі
потроєну про-ділянку α-фактора
дріжджів, перевершують за продуктивністю штами SCR-2b-F
і SCR-2a-F,
що являються аналогами штамів-прототипів, секреція інтерферону α-2
в яких направляється стандартною пре-про ділянкою α-фактора
дріжджів, в 1.3 та 1.2 рази відповідно.
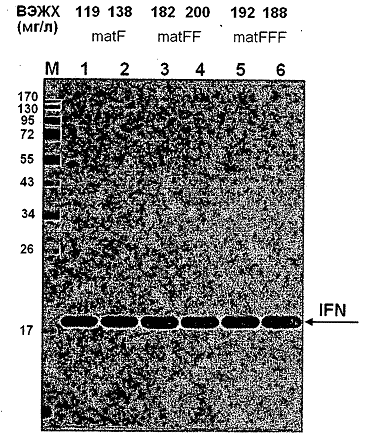
Рис.3.2.1.1 Результати аналізу рівня
секреції інтерферону α-2
людини
У процесі ренатурації молекул
інтерферону може спостерігається утворення некоректних внутрішньо- та
міжмолекулярних зв’язків. Це спричинює часткове утворення неправильних
мономерних форм рекомбінантного інтерферону, конформація яких відрізняється від
такої у природному інтерферону, а також виникнення його олігомерних структур,
яких не має у природному інтерфероні [6].кінцевим
амінокислотним залишком природного ІФН-α2
є цистеїн, який зв’язаний дисульфідним зв’язком із 98 цистеїном білка. Також у
певної частини молекул рекомбінантних ІФН-α2,
що виділяють з клітин Escherichia
coli,
на N-кінці
залишається додатковий залишок метіоніну (формілметіоніну), що робить
рекомбінантних ІФН-α2
модифікованим білком.
Надлишковий N-кінцевий
метіонін може впливати на стабільність та імуногенність білків, а також в
більшості випадків призводить до втрати їх біологічної активності. У зв’язку з
тим, що з 2005 року Європейська Фармакопея обмежила виробництво та використання
на території європейських країн препаратів, що містять модифікований ІФН-α2,
проблема видалення N-кінцевого
зі складу ІФН-α2
бактеріального походження набула великого значення.
До різновидів ферментативних
способів видалення N-кінцевого
метіоніну зі складу рекомбінантних білків відносять:
Видалення метіоніну з використанням
метіонін амінопептидази;
Способи, засновані на біосинтезі
подовженого білка, між N-кінцевим
метіоніном та зрілою частиною якого введена коротка послідовність сайту
впізнавання якої-небудь протеїнази. Наступна протеїназна обробка подовженого
білка призводить до видалення введеної послідовності разом з N-кінцевим
метіоніном.
Основний метод оснований на
біосинтезі в клітинах E.
coli
попередника безметіонінового ІФН-α2,
що містить у своєму складі послідовність зрілого інтерферону, злитого з
послідовністю дріжджового білка SUMO
(Small
Ubiquitine-like
protein
Modifier),
який відносять до родини убіквітин-подібних білків (УПБ).
Будують ген, що кодує гібридний
білок SUMO-2b
- попередник безметіонінового ІФН α-2b,
складовою частиною якого є послідовність безметіонінового інтерферону α-2b
людини, злита з послідовністю білка SUMO
дріжджів Saccharomyces cerevisiae.
Штам бактерій E.
coli
для біосинтезу виготовляють з Escherichia
coli
BL21
(DE3).
Штами культивують у відповідному поживному середовищі, що включає джерела
Карбону, Нітрогену та мінеральні солі, що зазвичай використовують для
вирощування клітин E.
coli
при температурі від 24 до 37°С. При досягненні ранньої логарифмічної стадії
фази росту культури в середовище культивування вносять індуктор ІПТГ в
концентрації від 0,1 до 2 мМ або лактозу в концентрації від 0,5 до 3%. Через
0,5-10 годин росту клітини штамів-продуцентів накопичують цільовий білок SUMO-2b
у вигляді нерозчинних тілець включення в кількості від 5 до 30% від сумарного
білка клітин. Нерозчинні тільця включення виділяють та очищують, а гібридний
білок SUMO-2b
піддають розчиненню.
Після біосинтезу білка SUMO-2b,
проводять ферментативне вищеплення цільового білку шляхом обробки протеїназою з
родини ULP
в умовах, що сприяють формуванню в інтерфероні правильно замкнутих дисульфідних
зв’язків.
Очищений безметіоніновий інтерферон α-2b
людини має наступні характеристики: чистота не нижче 96%, послідовність перших
п’яти N-кінцевих
амінокислот ідентична послідовності нативного безметіонінового ІФН-α2
людини, специфічна активність складає 2,0×108
МЕ/мг
[16].
Фармакокінетичні характеристики
рекомбінантного немодифікованого (стандартного) ІФН не дозволяє підтримувати
постійним його рівень у плазмі, що частково пояснює недостатньо високий
терапевтичний ефект.
Більшість відомих модифікацій
направлено на збільшення фізичних розмірів (гідродинамічного об’єму) або заряду
(від’ємного) молекул лікувальних білків, яке втілюють з метою уповільнення
процесу їх фільтрації з плазми крові через пори ниркових канальців.
Хімічна модифікація ІФН за допомогою
поліетиленгліколей (ПЕГ) дозволила отримати молекули ПЕГ-ІФН, для яких
характерний довший час перебування в плазмі крові і покращений
фармакокінетичний профіль.
генетична гібридизація ІФН з
довгоживучими білками крові людини, наприклад, альбумін сироватки або фрагмент
імуноглобуліну, або фрагмент антитіла, що забезпечує нековалентне зв’язування з
альбуміном сироватки крові людини безпосередньо в кровообігу (Albainterferon-alfa-2b);
генетична гібридизація ІФН зі
штучними поліпептидами, в яких наявні сайти N-глікозилування
і переважають повтори із залишків гліцину, аспарагінової кислоти і глютамінової
кислоти [18];
генетична гібридизація ІФН з
поліаніонним поліпептидом із залишків глютамінової кислоти (84 і 173 залишку) в
клітинах E. coli.
Білок не секретується і потребує довгої та трудомісткої очистки як від інших
внутрішньоклітинних білків, так і від клітинних ендотоксинів [19-21];
генетична гібридизація ІФН з
С-кінцевим пептидом (СТР) β-субодиниці
хоріонічного гонадотропіну людини, що містить 28 амінокислотних залишків, які
формують чотири сайти О-глікозилування. Одна чи кілька копій СТР, які
приєднуються до С-кінця молекули, суттєво подовжують тривалість життя
терапевтичних білків в плазмі крові. Використання СТР-технології обмежено
необхідністю отримувати модифіковані білки виключно в клітинах тварин, що
забезпечує коректне О-глікозилювання [22-28];
генетична зміна природної
послідовності ІФН з метою конструювання сайтів N-глікозилювання.
Модифікований таким чином ІФН, що продукується в культурі клітин СНО, містить
чотири або п’ять N-вуглеводневих
ланцюгів і володіє в 25 разів збільшеним часом життя в кровообігу. Для нього
характерне збільшення протипухлинної активності, але зниження специфічної
противірусної активності in vitro [29].
генетична гібридизація (кон’югація)
ІФН з високорозчинними, хімічно та імунологічно інертними неструктурованими
поліпептидами (НП), що здатні в фізіологічних умовах імітувати поведінку
молекул ПЕГ. Такі НП у водних розчинах при фізіологічно сольових, температурних
та буферних умовах стійкі до фолдингу (формування третинної структури),
агрегації, неспецифічної адсорбції і підтримують стабільне положення типу
«клубок». До таких НП відносять: XTEN-поліпептиди
(вміщують випадкові чергування 6 амінокислотних залишків аланіну, глютамінової
кислоти, гліцину, проліну, серину і треоніну), PAS-поліпептиди
(вміщують залишки проліну, аланіну і серину), HAP,
або ОЯ8-поліпептиди (мають багато залишків гліцину).
Для отримання гібридного ІФН
використовують штами E.
coli
або Saccharomyces
cerevisiae
ВКПМ Y-3927
і Saccharomyces
cerevisiae
ВКПМ Y-3928.
Для посіву в ферментері отримують
посівну культуру шляхом культивування штама-продуцента цільового гібридного
білку в середовищі наступного складу, в мас.%: пептон 1-3, дріжджовий екстракт
0,5-3, глюкоза 1-3, вода-залишок, рН середовища-природній на протязі 16-40
годин при температурі 22-32°С на орбітальній качалці 100-350 об./хв.
Посівною культурою засівають
ферментер (0,5-1000 л), який містить ферментаційне середовище наступного
складу, в мас.%: пептон 1-3, дріжджовий екстракт 0,5-3, глюкоза або
сахароза1-4, вода-залишок, рН середовища-природній. Кількість посівної
культури, яку вносять в ферментер, становить 3-15% від об’єму ферментаційного
середовища.
Ферментацію проводять при 22-32°С,
аерації 0,5-1000 л/хв і швидкості перемішування культури 100-1500 об./хв. Через
16-30 год після посіву в ферментер процес проводять без підживлення або
починають підживлювати 30-60% розчином глюкози або сахарози зі швидкістю 2-10
г/л/год і утримують рН в діапазоні 5,0-7,2. Загальна тривалість ферментації
складає 38-68 год.
Продукція цільового гібридного білку
в таких умовах складає не менше 0,12 г/л [17].
Очистка проводиться так само, як і
для не гібридного ІФН α-2b:
. Культуральну рідину, що містить
цільовий білок, відділяють від біомаси дріжджів за допомогою центрифугування
при 8500g
на протязі 10 хвилин;
. Отриманий центрифугат
культуральної рідини очищують від клітинних обломків за допомогою
мікрофільтрації на мембранному касетному модулі з поліпропілену із номінальним
відсіканням 0,2 мкм і номінальною площею фільтрації 0,1 м2 ;
. Захват ІФН із отриманого
мікрофільтрату проводять, використовуючи катіонобмінну хроматографію на носії SP-Sepharose
Fast
Flow
(GE
Healthcare).
Для цього триманий фільтрат підкислюють оцтовою кислотою до значення рН
4,4-4,5. Підкислений фільтрат пропускають через колонку з SP-Сефарозой,
збалансований 40 мМ буферним розчином ацетату амонію, рН 4,5, що містить 0,05% Tween
80 (буфер А). Після проходження фільтрату через колонку і наступної промивки
колонки розчином 0,12 M NaCl
в буфері А, ІФН піддають елююванню розчином 0,4 M
NaCl
в буфері А;
. Проводять тонку очистку ІФН з
отриманого елюату з використанням препаративної оберненофазної високоефективної
рідинної хроматографії.
Характеристики ефективності етапів
виділення і очистки інтерферону α-2b
з культуральної рідини наведено в таблиці 3.2.1.1 [30].
Характеристики ефективності
етапів виділення і очистки гібридного α-2b
з культуральної рідини наведено в таблиці 3.2.1.2 [17].
Таблиця 3.2.1.1. Результати етапів
очистки ІФН α-2b
з культуральної рідини штама-продуцента Saccharomyces
cerevisiae
ВКПМ Y-3493
[30]
|
Етап
|
Опис етапу
|
Метод очистки
|
Ефективність етапу (%)
|
Вихід ІФН α-2b
(%)
|
|
0
|
Культуральна рідина
|
-
|
-
|
-
|
|
1
|
Відділення біомаси
|
Центрифугування
|
100
|
100
|
|
2
|
Очистка від обломків клітин
|
Мікрофільтрація
|
82
|
82
|
|
3
|
Захват
|
Катіонобмінна хроматографія на SP-сефарозі
|
91
|
75
|
|
4
|
Тонка очистка
|
Хроматографія в оберненій фазі С 18
|
74
|
55
|
|
5
|
Концентрування
|
Катіонобмінна хроматографія на CM-сефарозі
|
90
|
50
|
Таблиця 3.2.1.2 Результати етапів
очистки гібридного
ІФН α-2b
з культуральної рідини штама-продуцента Saccharomyces
cerevisiae ВКПМ Y-3493
|
Етап
|
Опис етапу
|
Метод очистки
|
Ефективність етапу (%)
|
Вихід GFNa-80(%)
|
|
0
|
Культуральна рідина
|
-
|
-
|
100
|
|
1
|
Відділення біомаси
|
Центрифугування
|
90
|
90
|
Захват
|
Катіонобмінна хроматографія на SP-сефарозі
|
80
|
72
|
|
3
|
Тонка очистка
|
Хроматографія в оберненій фазі С 18
|
75
|
54
|
|
4
|
Концентрування
|
Катіонобмінна хроматографія на CM-сефарозі
|
76
|
41
|
В результаті отримують не менше
0,05г цільового гібридного білку з 1 л культуральної рідини.
Принципова технологічна схема
виготовлення рекомбінантного інтерферону наведена в Додатку А [17].
На відміну від плазмідної технології
добування інтерферону ґрунтується на використанні як ампліфікатора цільового
гену (гену інтерферону) бактеріофагу, у геном якого генно-інженерним методом
вбудований ген інтерферону. Бактеріофаг (вірус бактерій), уражаючи бактеріальну
клітину, розмножується в ній, копіюючи багаторазово свою ДНК, і вбудований в
неї ген інтерферону, синтезує свої білки, у тому числі й інтерферон. На певній
стадії розвитку бактеріофаг лізує бактеріальну клітину. Інтерферон виходить у
культуральну рідину, причому у водорозчинному стані, не утворюючи нерозчинних
форм. Синтез організований таким чином, що інтерферон нагромаджується поза
клітиною, у культуральному середовищі, тому не утворює «тілець включення», як
це відбувається за плазмідною технологією добування інтерферону. Нагромадження
інтерферону в культуральній рідині дозволяє очищати його за спрощеною схемою:
не відбувається формування біомаси, її дезінтеграція, денатурація білків для
розчинення «тілець включення» та ренатурація молекул інтерферону. Відсутність
стадії концентрування клітин (формування біомаси), а, отже, й клітинних бімсів,
дозволяє добувати високоочищений препарат інтерферону менш складним методом,
ніж той, який використовують для очищення аналогів [6].
Очищення проводять іонообмінною
хроматографією. Чистоту білка контролюють методом електрофорезу в
панакриламідному гелі, що та відповідає рекомендаціям ВООЗ: в очищеному
препараті міститься не менш як 95 % білка інтерферону [6].
Рекомбінантні інтерферони α-2
використовують для терапії вірусних та пухлинних захворювань, включаючи
лікування твердих пухлин, таких як рак сечового міхура, рак нирки,
ВІЛ-індукована саркома Капоши та ін. Інтерферон має також знеболювальну дію.
Також дані інтерферони є основними терапевтичними засобами, які використовують
для лікування хронічних форм гепатитів B
та C
[13, 16].
Відомі такі фармацевтичні препарати,
що містять в якості діючої речовини α-2
інтерферон: «Роферон» (Hoffman-La
Roche
AG,
Швейцарія), «Інтрон-А» (Schering-Plough,
США), «Реальдирон» (Biotechna,
Литва), «Реаферон» («Вектор-Медика», Росія), «Інтераль» (НДІ ОЧБ, Росія).
Препарати «Реаферон», «Інтераль» і «Інтрон-А» містять в якості стабілізатора
альбумін людини, що вимагає додаткової перевірки лікарських форм на відсутність
вірусів гепатиту В, С та ВІЛ. Препарат «Інтрон-А» додатково містить в якості
стабілізуючого агенту гліцин [31].
3.2.2 Технологія
виготовлення рекомбінантного α-1
інтерферону
Для виготовлення рекомбінантного α-1
інтерферону використовують штам дріжджів Pichia
pastoris
KM71
[31].
Для отримання штаму дріжджів Pichia
pastoris
- продуцента α-1
інтерферону людини, клітини дріжджів штаму PS99
трансформують плазмідою pHIN.
Клітини дріжджів вирощують в 100 мл
середовища YEPD при 30°С до
набуття культурою оптичної густини, відповідній 2-4 од. поглинання при довжині
хвилі 600 нм. Клітини двічі промивають стерильною водою, після чого суспендують
в 0,3 мл 100мМ розчину ацетату літію та інкубують при 30°С на протязі 30 хв. До
50 мкл отриманої суспензії клітин додають 0,1-1 мкг плазмідної ДНК, 50 мкг ДНК
сперми лосося, спершу денатурованої нагріванням (10 хв при 100°С) і 0,3 мл
розчину 100 мМ ацетату літію, що містить 40% ПЕГ 4000. Далі пробу інкубують 30
хв при 30°С і 20 хв при 42°С, занурюють на 15 с в крижану баню і центрифугують
10 с при 10000 об./хв. Клітини суспендують в 1 мл стерильної води та висівають
на тверде середовище SC. Клони
трансформантів виростають через 2-3 доби. Вирощені клони пересівають на чашки
із середовищем SC,
що містить 2% глюкозу, окремими колоніями, потім відбивають на середовище ММ (1,34%
Yeast Nitrogen Base (“Difco”, USA), 0,5% метанолу, 2%
агару (“Difco”,
USA) для відбору трансформантів,
не зростаючих на середовищі з метанолом, що свідчить про інтеграцію чужорідного
гену в локус АОХІ (фенотип Met-) [32].
По закінченню процесу культивування
видаляють клітини дріжджів за допомогою центрифугування при 6-7 тис. об./хв на
протязі 15 хвилин, при +4°С. Всі наступні дії здійснюють при температурі +4°С.
Надосадову рідину пропускають через нітроцелюлозний фільтр з діаметром пор 0,45
мкм (Millpore
Inc.).
Отриманий таким чином фільтрат
концентрують на ультрафільтраційній установці УПЛ-0,6 із використанням мембрани
АР-0,2-15ПА (НПК «Біотест»), яка відсікає сполуки із молекулярною масою менше
15 кДа, на цій стадії відбувається видалення низькомолекулярних компонентів
середовища і зменшення вихідного об’єму до 100-200 мл.
Далі проводять сольове осадження
цільового білку, доводячи насичення сульфату амонію до 60%. Осад цільового
білку збирають центрифугуванням при 12-14 тис. об./хв на протязі 20 хвиин.
Отриманий осад розчиняють в 50 мМ амоній-ацетатному буфері (рН 5,5), що містить
2 мМ ЕДТА, 0,05% Твін-20, і наносять на колонку, яка містить 1000 мл Сефакрилу HR
100, збалансованого таким самим буфером. Перші 350
мл відкидали, фракції, що містять цільовий білок, об’єднують.
Отриманий таким чином елюат титрують
10% аміаком до рН 7,0 і наносять на колонку, що містить 50 мл ДЕАЕ-целюлозу,
збалансовану 50 мМ амоній-ацетатним буфером (рН 7,0), який містить 2 мМ ЕДТА,
0,05% Твін-20. Відмивають колонку послідовно 100 мл збалансовуючим буфером і
100 мл збалансовуючим буфером, який містить 0,1 М хлориду натрію. Елюювання
проводять градієнтом концентрації хлористого натрію від 0,1 М до 1,0 М в 50 мМ
амоній-ацетатному буфері (рН 5,5), який містить 2 мМ ЕДТА, 0,05% Твін-20.
Електрофорез в редукуючих умовах
показує, що молекулярна маса отриманого білку становить приблизно 20 кДа. За
даною схемою очистки можна отримати препарат інтерферону α-1b,
з
вмістом домішок не більше 5%. Питома активність становить 0,3-1,0×108
МЕ/мг.
Активність препарату змінюється в залежності від терапевтичної форми та композиції
(табл. 3.2.2.1) Середній вихід з 1л культури становить 7-9 мг [31].
Таблиця 3.2.2.1. Вплив складу
препарату на активність α-1b
інтерферону
[31]
|
pH
|
ЕДТА, мг/мл
|
Твін-20, мг/мл
|
Вихідна активність препарату, МЕ/мл
|
Активність препарату через 6 міс. зберігання
при +4°С, МЕ/мл
|
Збереження активності, %
|
|
Рідка форма
|
|
5,5
|
0,5
|
0,5
|
(11,0±0,8)×106
|
(9,5±0,6)×106
|
86,3
|
|
5,5
|
0,5
|
2,5
|
(10,8±0,8)×106
|
(9,1±0,8)×106
|
84,2
|
|
5,5
|
0,5
|
5,0
|
(10,6±0,8)×106
|
(8,9±0,7)×106
|
84,0
|
|
5,5
|
0,8
|
0,5
|
(11,1±0,8)×106
|
(10,7±0,8)×106
|
96,4
|
|
5,5
|
0,8
|
2,5
|
(10,4±0,8)×106
|
(9,9±0,8)×106
|
95,1
|
|
5,5
|
0,8
|
5,0
|
(10,3±0,8)×106
|
95,2
|
|
5,5
|
1,5
|
0,5
|
(11,3±0,8)×106
|
(10,7±0,7)×106
|
95,1
|
|
5,5
|
1,5
|
2,5
|
(10,6±0,8)×106
|
(10,0±0,8)×106
|
94,0
|
|
5,5
|
1,5
|
5,0
|
(10,5±0,8)×106
|
(9,8±0,7)×106
|
93,6
|
|
6,7
|
0,8
|
0,5
|
(11,0±0,8)×106
|
(9,8±0,6)×105
|
89,1
|
|
7,8
|
0,8
|
0,5
|
(10,7±0,8)×106
|
(8,3±0,6)×105
|
77,5
|
|
Суха ліофілізована форма
|
|
5,5
|
0,8
|
0,5
|
(9,8±0,9)×106
|
(9,3±0,7)×106
|
95,1
|
|
6,7
|
0,8
|
0,5
|
(10,3±0,6)×106
|
(8,6±0,8)×106
|
83,6
|
|
7,8
|
0,8
|
0,5
|
(9,9±0,6)×106
|
(7,7±0,9)×106
|
77,8
|
3.2.3
Технологія виробництва рекомбінантного β-1
інтерферону
Інтерферон β
людини або фібробластний інтерферон секретується, в основному, фібробластами і
є глікопротеїном із молекулярною масою 20 кДа. Його структура позначається як
ІФН- β-1а. Пептидна
частина ІФН- β-1а
представлена 166 амінокислотними залишками. Молекула містить вільну
сульфгідрильну групу цистеїну в положенні Cys16
і один внутрішньомолекулярний дисульфідний зв'язок в положенні Cys30-Cys140.
Рекомбінантний інтерферон β,
який отримують в бактеріальній системі, являє собою неглікозильований білок, що
має заміну цистеїну в положенні 16 на серин (рис.3.2.3.1). Така заміна
позбавляє проблеми утворення димерів за рахунок неправильного замикання
дисульфідних зв’язків. Така структура фібробластного інтерферону має назву ІФН-β-1b.

Рис. 3.2.3.1 Послідовність
амінокислот в ІФН-β-1b
Створення штама-продуцента людського
інтерферону β-1b
дозволило отримувати біологічно активний білок в кількості, необхідній як для
проведення різноманітних структурно-функціональних досліджень, так і для
використання в медичній практиці [33].
Рекомбінантний ІФН-β-1b
людини отримують в нерозчинній формі у вигляді тілець включення. У порівнянні з
розчинною формою, експресія білку у вигляді тілець включення має ряд переваг -
нерозчинні агрегати білку не проявляють токсичної дії, практично не атакуються
протеазами, та з високим виходом виділяються центрифугуванням [34].
До 150 г тілець
включення рекомбінантного ІФН-β-1b
людини приливають 1000 мл розчину, який містить 0,3 % трифтороцтвої кислоти
(ТФО). Після цього тільця включення гомогенізують в блендері із швидкістю 800
об./хв на протязі 1 хвилини, переносять в стакан з магнітною мішалкою і
залишають перемішуватися протягом 1 години при температурі 4°С. Далі отриману
суспензію центрифугують при 4°С протягом 40 хвилин на швидкості 10000 об./хв.
Отриманий осад переносять в блендер, заливають 1,0 л розчину 1-пропанол:вода
(1:1) з додаванням 0,3% ТФО, гомогенізують зі швидкістю 800 об./хв протягом 1
хвилини, охолоджують розчин при -20°С протягом 20-30 хвилин і ставлять
перемішуватися при 4°С на 1-2 години.
Отриманий екстракт центрифугують при
4°С протягом 40 хвилин на швидкості 10000 об./хв. Потім отриманий супернатант
фільтрують через скловолокно і розбавляють розчином, що містить 0,3 % ТФО до
концентрації 1-пропанола 20 %.
На наступному етапі екстракт білку
наносять на обернено-фазову колонку DAU-100
(розмір колонки 10×10
см)
(YMC
Co.,
LTD,
Japan),
наповнену сорбентом GEL-Butyl
C4
(YMC
Co.,
LTD,
Japan)
і збалансовану розчином, який містить 0,1 % ТФО і 20 % 1-пропанол. Навантаження
на сорбент може досягати 40 мл сумарного білку на 1 мл носія. Після нанесення
розчину білку, колонку промивають початковим розчином ТФО і 1-пропанолу до
отримання на спектрофотометрі значень, що дорівнюють значенням базової лінії
при довжині хвилі 280 нм. Сорбовані білки піддають елююванню в градієнті
концентрації 1-пропанолу (від 20 % до 50 %) при довжині хвилі 280 нм. Фракції,
що містять цільовий білок за результатами аналізу на обернено-фазній колонці,
об’єднують. З об’єднаної фракції, зібраної з обернено-фазної колонки, осаджують
білок додаванням рівного об’єму буферного розчину, який містить 50 мМ Na2HPO4,
і доведенням рН отриманого розчину до 6,0.
Потім суспензію білку центрифугують
з використанням центрифуги за 4°С протягом 30 хвилин на швидкості 14000 об./хв.
Отриманий осад розмішують в 400 мл такому самому буферному розчині і знов
центрифугують за аналогічних умов.
Далі осад наносять на колонку BPG
200/500 (розмір колонки 20×30
см)
(JE
Healthcare,
USA),
заповнену гелем Sephadex
G-25
Fine
(JE
Healthcare,
USA)
та збалансовують розчином 10 мМ NaOH.
Елюювання проводять в ізократичному режимі при довжині хвилі 280 нм. Із
фракції, зібраної з колонки, осаджують білок шляхом внесення дигідрофосфату
натрію до сумарної концентрації реактиву в розчині 50 мМ і доведеням рН розчину
до 6,0 і проводять центрифугування суспензії білку з використанням центрифуги
при 4°С протягом 30 хвилин за швидкості 14000 об./хв.
Отриманий осад гомогенізують в
буферному розчині, який містить 100 мМ NaH2PO4,
pH
4,2 і прогрівають до 65°С, додають рівний об’єм заздалегідь нагрітого до 65°С
75% розчину фенола у воді. Проводять інкубацію на протязі 20 хвилин в
термошейкері при 65°С. Потім реакційну суміш охолоджують до 10°С, домагаючись
повного розшарування фаз, та видаляють водну фазу за допомогою водоструминного
насосу.
Отриманий розчин білку в фенолі
розводять в 6,5 разів 30 % етиловим спиртом, додають ТФО до 0,1 % і наносять на
обернено-фазну колонку DAU-50
(розмір колонки 5×20
см)
(YMC
Co.,
LTD,
Japan),
заповнену сорбентом С18 (YMC Co.,
LTD,
Japan)
та збалансовану розчином, який містить 0,1 % ТФО та 20 % 1-пропанолу.
Навантаження на сорбент може досягати 40 мг сумарного білку на 1 мл носія.
Після нанесення розчину білку, колонку промивають початковим розчином ТФО і
1-пропанолу до показання спектрофотометром значень, рівних значенням базової
лінії за довжини хвилі 280 нм. Сорбовані білки піддають елююванню в градієнті
концентрації 1-пропанолу (від 20 % до 50 %) за довжини хвилі 280 нм. Фракції,
що містять цільовий білок за результатами аналізу на обернено-фазній колонці
С18, об’єднують.
Розчин цільового білку наносять на
колонку BPG
200/500 (розмір колонки 20×30
см)
(JE
Healthcare,
USA),
заповнену гелем Sephadex
G-25
Fine
(JE
Healthcare,
USA)
та збалансовану розчином 10 мМ NaOH.
Елюювання проводять в ізократичному режимі за довжини хвилі 280 нм. В отриманій
фракції білку визначають концентрацію за допомогою обернено-фазної
хроматографії на колонці С18.
Вихід готового продукту з 1 г
цільового білку, отриманого при екстракції на першому етапі з тілець включення,
становить 0,3 цільового білку. Чистота білку не менше 98 %. Матеріальний баланс
промислового процесу очищення ІФН-β-1b
вказаний в табл. 3.2.3.1 [33].
Таблиця 3.2.3.1. Матеріальний баланс
основних стадій промислового процесу очистки ІФН-β-1b
[33]
|
Стадії очистки ІФН-β-1b
|
Вихід ІФН-β-1b,
г
|
Хроматографічна чистота ІФН-β-1b,
%
|
Вміст
|
|
|
|
|
Білків E.
coli
нг/мгбілку
|
Ендотоксинів Од./мгбілку
|
|
Екстракція білку з 150 г тілець включення
|
5
|
100
|
60-70
|
>100
|
>250
|
|
ВЕРХ на С4, YMC
|
4
|
80
|
65-75
|
90-100
|
50-250
|
|
Розчинення білку в 1% лаураті натрію
|
4
|
80
|
|
|
|
|
Ренатурація
|
2,8
|
70
|
|
|
|
|
Очистка білку фенолом
|
2,5
|
50
|
70-75
|
20-60
|
2-5
|
|
ВЕРХ на С18, YMC
|
1,4
|
28
|
96-98
|
5-10
|
≤1
|
Основним терапевтичним ефектом ІФН-β-1b
противірусна та імуномоделююча активність, зниження частоти загострення
розсіяного склерозу з ремітуючим протіканням на одну третину і зменшення
кількості нових ділянок ураження головного мозку. Крім того, знижується частота
загострень при вторинно-прогресуючому протіканні розсіяного склерозу і
зменшується вираженість атрофії головного мозку. Препарати на основі ІФН-
β-1b
відомі під назвами: Екставіа, Бетаферон, Авонекс та ін. [33-34].
ВИСНОВОК
Інтерферони - група низькомолекулярних
білків, які володіють рядом спільних біологічних властивостей, головною з яких
є здатність при контакті з клітинами викликати в них стійкість до вірусних
інфекцій. Інтерферони хребетних і, також, людини розділяють на три групи: α-,
або лейкоцитарні, β-,
або фібробластні, та γ-
, або імунні (продукуються Т-лімфоцитами).
Інтерферони викликають стан
несприйнятливості до широкого спектра вірусних інфекцій, що індукується у всіх
клітинах, які мають рецептори до інтерферонів. Вони індукують як локальні, так
і системні противірусні реакції в інших клітинах. Крім того, інтерферони
володіють ще двома важливими властивостями: пригнічують поліферацію клітин (і,
таким чином, потенційно є протипухлинним засобом) і модулюють імунну систему.
За використання лейкоцитарної
технології виготовлення інтерферону, створюють певну систему вірус-клітина
крові (лейкоцити або фібробласти). При цьому лейкоцити інкубуються разом із
вірусом (наприклад, вірус Сендай або вірус хвороби Ньюкасла), а в якості
компонента поживного середовища слугує сироватка крові людини або бика (іноді -
казеїн молока). Далі суміш очищують за допомогою хроматографічних методів і
отримують достатньо концентрований препарат інтерферон. За цією технологією
можна отримати 1мкг інтерферону з 1л донорської крові, що становить одну дозу.
Недоліком даної технології є проблема очищення інтерферону від чужорідних
антигенів (тобто, вірусного індуктора, білків алантоїсної рідини, включаючи
овальбумін).
Субстанція інтерферону α-2
виготовляється за рекомбінантною технологією переважно шляхом біосинтезу штаму Escherichia
coli,
у який вбудовано ген інтерферону людини. Вектором для проходження трансформації
бактеріального геному є бактеріофаг, або плазміда. Процес виготовлення й
очищення інтерферону в плазмідній технології складається з таких стадій:
формування клітинної біомаси, її дезінтеграція; розчинення «тілець включення»
шляхом денатурації білкових структур за допомогою сечовини або гуанідинхлориду;
ренатурація денатурованих молекул інтерферону; очищення. З 1л культури кишкової
палички отримують близько тисячі
доз продукту. З використанням плазмідної технології також ампліфікують ген
інтерферону в клітинах дріжджів Saccharomyces
cerevisiae.
N-кінцевим
амінокислотним залишком природного ІФН-α2
є цистеїн, який зв’язаний дисульфідним зв’язком із 98 цистеїном білка. Також у
певної частини молекул рекомбінантних ІФН-α2,
що виділяють з клітин Escherichia
coli,
на N-кінці
залишається додатковий залишок метіоніну (формілметіоніну), що робить
рекомбінантних ІФН-α2
модифікованим білком. Надлишковий N-кінцевий
метіонін може впливати на стабільність та імуногенність білків, а також в
більшості випадків призводить до втрати їх біологічної активності. Тому в
роботі був розглянутий спосіб видалення N-кінцевого
метіоніну. Фармакокінетичні характеристики рекомбінантного немодифікованого
(стандартного) ІФН не дозволяє підтримувати постійним його рівень у плазмі, що
частково пояснює недостатньо високий терапевтичний ефект.
З огляду на це, також було розглянуто технологію виготовлення модифікованого
рекомбінантного інтерферону α-2
людини.
Для виготовлення рекомбінантного α-1
інтерферону використовують штам дріжджів Pichia
pastoris
KM71.
Рекомбінантний інтерферон β,
який отримують в бактеріальній системі, являє собою неглікозильований білок, що
має заміну цистеїну в положенні 16 на серин. Рекомбінантний ІФН-β-1b
людини отримують в нерозчинній формі у вигляді тілець включення. У порівнянні з
розчинною формою, експресія білку у вигляді тілець включення має ряд переваг -
нерозчинні агрегати білку не проявляють токсичної дії, практично не атакуються
протеазами, та з високим виходом виділяються центрифугуванням. Вихід готового
продукту з 1 г цільового білку, отриманого при екстракції на першому етапі з
тілець включення, становить 0,3 цільового білку. Чистота білку не менше 98 %.
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
1. Биотехнология:
Учеб. пособие для вузов. В 8 кн. / под ред. Н.С. Егорова, В.Д. Самуилова. Кн. 2
Современные методы создания промышленных штаммов микроорганизмов / В.Г.
Дебабов, В.А. Лившиц. - М.: Высш. шк., 1988. - 208 с.
. Колешко,
О.И. Микробиология с основами вирусологии: учебник / О.И. Колешко, Т.В.
Завезенова - Иркутск: Изд-во Иркут. ун-та, 1999. - 452 с.
. Елинов,
Н.П. Основы биотехнологии. Для студентов институтов; аспирантов и практических
работников. / Н.П. Елинов. - СПБ: Изд-во «Наука», 1995. - 600 с.
. Овчинников,
Ю.А. Биоорганическая химия. / Ю.А. Овчинников. - М.: Просвещение, 1987. - 815
с.
5. Губський,
Ю.І. Біологічна хімія:
підручник. / Ю.І. Губський. - Київ-Тернопіль: Укрмедкнига, 2000. - 508 с.
6. Гаркава,
К.Г. Біотехнологія. Вступ до фаху: навч.посіб./
К.Г. Гаркава, Л.О. Косоголова, О.В. Карпов, Л.С. Ястремська. - К.:
НАУ, 2012. - 296 с.
7. Биотехнология.
Принципы и применение: Пер. с англ. / под ред. И. Хиггинса, Д. Беста, Дж.
Джонса. - М.: Мир, 1988. - 480 с.
8. Burmester,
Gerd-Ruediger. Color Atlas of Immunology / Gerd-Ruediger Burmester, Antonio
Pezzutto, Timo Ulrichs, Alexandra Aicher. - Stuttgart-New York: Thieme, 2003. -
322 p.
9. Wood,
P. Understanding immunology (Second edition) / Peter Wood. - Harlow: Pearson
Education Limited, 2006. - 300 p.
10. Сартакова,
О.Ю. Промышленная микробиология: учебное пособие по курсу «Основы микробиологии
и биотехнологии» / О.Ю. Сартакова, И.И. Ползунова. - Барнаул: Изд-во АлтГТУ,
2009. - 173 с.
11. Кулагин,
В.Ф. Разработка научных основ технологии крупномасштабного производства
человеческого лейкоцитарного интерферона: автореф. дисс. докт. мед. наук:
03.00.06. / Кулагин Валерий Федорович; Научно-производственное объединение
«Иммунопрепарат». - Уфа, 1995. - 75 с.
12. Способ
получения зрелого интерферона альфа-2 человека с использованием дрожжей
Saccharomyces cerevisiae и штамм-продуцент интерферона альфа-2 человека
(варианты); пат. WO 2012/128662 A1 Всемирная Организация Интеллектуальной Собственности
/ Корниенко Е.В.; заявитель и патентообладатель Козлов Дмитрий Георгиевич,
Яковенко Андрей Романович, Тезов Владимир Адольфович
13. Мельник,
А.И. Получение очищенного рекомбинантного α2b-интерферона
человека / А.И. Мельник, И.В. Орловская, Н.М. Жолобак, Н.Я. Спивак // Мікробіологічний
журнал.
- 2012. - Т. 74, №3. - С. 72-78
14. Method
for the production of high-level soluble human recombinant interferon alpha in
E. coli and vectors useful for such a production; pat. US 2009/0258394 A1
United States Patent Application Publication / inventors: Mohamad Dahmani
Fathallah, Imen Rabhi-Essafi; assignee: Institut Pasteur
15. Гибридный
белок, штамм бактерий Escherichia coli - продуцент гибридного белка и способ
получения безметионинового интерферона α-2b
человека из этого гибридного белка [Текст]; пат. RU 2 441 072 C1 Федеральная
Служба по Интеллектуальной Собственности / авторы: Козлов Д.Г., Чеперигин С.Э.,
Губайдуллин И.И., Яковенко А.Р., Казаров А.А.; патентообладатели: Федеральное
государственное унитарное предприятие «Государственный научно-исследовательский
институт генетики и селекции промышленных микроорганизмов», Общество с
ограниченной ответственностью «ФАРМАПАРК», Министерство образования и науки
Российской Федерации
16. Гибридный
белок, обладающий пролонгированным действием, на основе рекомбинантного
интерферона α-2 человека
(варианты), способ его получения и штамм Saccharomyces cerevisiae для
осуществления этого способа (варианты); пат. RU 2 515 913 C1 Федеральная Служба
по Интеллектуальной Собственности / авторы: Козлов Д.Г., Чеперигин С.Э.,
Губайдуллин И.И., Ефремов Б.Д., Котлова Е.К., Рябиченко В.В., Честухина Г.Г.,
Яроцкий С.В.; патентообладатель: Федеральное государственное унитарное
предприятие «Государственный научно-исследовательский институт генетики и
селекции промышленных микроорганизмов»
17. Conjugates
of biologically active proteins having a modified in vivo half-life; pat. US
2009/0298762 A1 United States Patent Application Publication / inventors: Marc
Besman, Stewart Chipman, David Leung, Jach Singer; assignee: Cell Therapeutics,
Inc.
18. Recombinant
production of polyanionic polymers and uses thereof; pat. US 2002/0169125 A1
United States Patent Application Publication / inventors: David W. Leung,
Philip A. Bergman, Alan Lofquist, Gregory E. Pietz, Christopher K. Tompkins,
David W. Waggoner JR.; assignee: Cell Therapeutics, Inc.
19. Recombinant
production of polyanionic polymers and uses thereof; pat. AU 2002252429 A8
Australian Patent Office / inventors: David W. Waggoner JR., Gregory E. Pietz,
Philip A. Bergman, Alan Lofquist, , Christopher K. Tompkins, David W. Leung;
applicant: David W. Leung
20. Recombinant
production of polyanionic polymers and uses thereof; pat. WO 02/077036 A2 World
Intellectual Property Organization / inventors: Philip A. Bergman, Alan
Lofquist, Gregory E. Pietz, Christopher K. Tompkins, David W. Waggoner JR.;
applicant: David W. Leung
21. Long-acting
polypeptides and methods of producing same; pat. US 2012/0015437 A1 United
States Patent Application Publication / inventors: Fuad Fares, Udi Eyal Fima
22. Long-acting
growth hormone and methods of producing same; pat. US 2012/0035101 A1 United
States Patent Application Publication / inventors: Fuad Fares, Udi Eyal Fima
23. Long-acting
veterinary polypeptides and methods of producing and administering same; pat.
US 2012/0004286 A1 United States Patent Application Publication / inventors:
Fuad Fares, Udi Eyal Fima
24. Long-acting
interferons and derivatives thereof and methods thereof; pat. US 2011/0286967
A1 United States Patent Application Publication / inventors: Fuad Fares, Udi
Eyal Fima
25. Long-acting
coagulation factors and methods of producing same; pat. US 2010/0317585 A1
United States Patent Application Publication / inventors: Fuad Fares, Udi Eyal
Fima
26. Long-acting
growth hormone and methods of producing same; pat. US 2010/ 0081614 A1 United
States Patent Application Publication / inventors: Fuad Fares, Udi Eyal Fima
28. Glycosylated
human alpha interferon muteins, method for obtaining them and use; pat. US
2012/0134960 A1 United States Patent Application Publication / inventors:
Ricardo Agustin Lopez, Natalia Analia Ceaglio, Marina Etcheverrigaray, Marcos
Rafael Oggero Eberhardt, Ricardo Kratje; assignees: Protech Pharma, S.A.,
Ricardo Agustin Lopez
29. Способ
микробиологического синтеза зрелого интерферона альфа-2 человека, штамм
Saccharomyces cerevisiae - продуцент зрелого
интерферона альфа-2 человека (варианты); пат. RU 2 427 645 C1 Федеральная
Служба по Интеллектуальной Собственности, Патентам и Товарным знакам / авторы:
Козлов Д.Г., Чеперегин С.Э., Губайдуллин И.И., Ефремов Б.Д., Казаченко К.Ю.,
Яковенко А.Р., Казаров А.А., Котлова Е.К., Рябиченко В.В., Честухина Г.Г.,
Глазунов А.В., Черноморова Н.О., Акишина Р.И.; патентообладатель: Федеральное
государственное унитарное предприятие «Государственный научно-исследовательский
институт генетики и селекции промышленных микроорганизмов»
30. Способ
получения рекомбинантного альфа 1b-интерферона человека и фармацевтическая
композиция для лечения вирусных заболеваний на основе рекомбинантного альфа
1b-интерферона человека; пат. RU 2 380 405 C2 Федеральная служба по
интеллектуальной собственности, патентам и товарным знакам / авторы: Падкина
М.В., Доброгорская М.В., Карабельский А.В., Самбук Е.В., Смирнов М.Н.;
патентообладатели: Федеральное государственное образовательное учреждение
высшего профессионального образования Санкт-Петербургский государственный
университет, Общество с ограниченной ответственностью «БИОТЕХ»
31. Штамм
дрожжей Pichia pastoris - продуцент лейкоцитарного интерферона-1b человека,
рекомбинантная плазмидная ДНК PHIN и способ ее конструирования; пат. RU 2 203
950 C1 Российское агенство по патентам и товарным знакам / авторы: Падкина
М.В., Парфенова Л.В., Самбук Е.В., Смирнов М.Н.; патентообладатель: Общество с
ограниченной ответственнотью «БИОТЕХ»
32. Промышленный
способ получения и очистки рекомбинантного интерферона β-1b
человека из телец включения; пат. RU 2 473 696 C1 Федеральная служба по
интеллектуальной собственности / авторы: Бобрускин А.И., Кононова Н.В.,
Мартьянов В.А., Шустер А.М.; патентообладатель: Закрытое акционерное общество
«ГЕНЕРИУМ»
33. Способ
очистки рекомбинантного интерферона β-1b;
пат. RU 2 392 282 C1 Федеральная служба по интеллектуальной собственности,
патентам и товарным знакам / авторы: Воробьев И.И., Пономаренко Н.А. Мирошников
А.И., Смирнов И.В.; патентообладатели: Учреждение Российской академии наук
Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова
РАН, Российская Федерация, от имени которой выступает Федеральное агентство по
науке и инновациям
Додаток
Принципова
технологічна схема виготовлення рекомбінантного інтерферону