|
s
|
|
|
|
|
|
n = 1
|
↑↓
|
|
p
|
|
|
|
n = 2
|
↑↓
|
↑↓
|
↑↓
|
↑↓
|
d
|
|
n = 3
|
↑↓
|
|
|
|
|
Последний, 12-й электрон атома магния занимает s-орбиталь, следовательно,
магний относится к s-электронному семейству.
Задача 3
Исходя из закономерностей периодической системы, дайте мотивированный
ответ на вопрос: какой из двух гидроксидов более сильное основание: NaOH или
RbOH,Ca(OH)2 ИЛИ Cu(OH)2, Zn(OH)2 или Sr(OH)2?
Решение
. RbOH - сильнее, так как сверху вниз по группе усиливаются
основные свойства гидроксидов.
. Ca(OH)2 - сильнее, это - щелочь, гидроксид s-
элемента
Cu(OH)2 -гидроксид d- элемента.
. Sr(OH)2 сильнее, это - щелочь, гидроксид s- элемента,
Zn(OH)2 - амфотерный гидроксид d- элемента.
Задача 4
Значение энтальпии растворения в воде Na2CО3= -25,1
кДж/моль, a у Na2CO3*10H2O= +66,934 кДж/моль.
Вычислить энтальпию гидратации Na2CO3.
Решение
По закону Гесса: тепловой эффект (изменение энтальпии) химической реакции
зависит только от начального и конечного coстояния участвующих в реакции
веществ и не зависит от промежуточных стадий процесса.створение Na2CO3
в воде можно изобразить следующими процессами:
Na2CO3 + 10 H2O = Na2CO3*10H2O
+ ∆ H12CO3*10H2O + (n - 10) H2O
= Na2CO3*nH2O + ∆ H2 (+66.934 кДж/моль)
Суммарная реакция:
Na2CO3 + n H2O = Na2CO3*nH2O
+ ∆ H3 (-25.1 кДж/моль)
Из закона Гессa следует:
∆H3 = ∆H1 + ∆H2.
Отсюда: ∆ H1 = - 25,1 - 66,934 = - 92,034 кДж/моль
Задача 5
При увеличении температуры на 30 градусов скорость реакции возросла в 64
раза. Вычислите температурный коэффициент реакции.
Решение
Дано:

 Т = 30 °С
Т = 30 °С
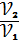
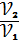 = 64
= 64

Расчёты:
Преобразуем
уравнение Вант-Гоффа 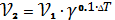
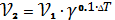 в
соответствии с условием задачи и рассчитаем значение температурного
коэффициента:
в
соответствии с условием задачи и рассчитаем значение температурного
коэффициента:
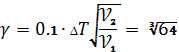
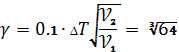 = 4
= 4
Ответ:
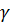
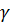 = 4.
= 4.
Задача
6
В
каком направлении произойдет смещение равновесия при понижении давления в
системах:
N2 + 3H2 ↔
2NH3
SO2 + O2 ↔
2SO3
Напишите
выражение констант равновесия данных систем.
Решение
N2+3H2=2NH3
Кр=[
NH3]2/[
H2]3[N2]
При
понижении давления химическое равновесие смещается в сторону увеличения
количеств газообразных веществ. В данной реакции из 4-х моль газообразных
веществ образуется 2 моль, поэтому при понижении давления равновесие сместится
влево, т.е. в сторону обратной реакции.
2SO2+O2=2SO3
Кр=[ SO3]2/[ SO2]2[O2]
При
понижении давления химическое равновесие смещается в сторону увеличения
количеств газообразных веществ. В данной реакции из 3-х моль газообразных
веществ образуется 2 моль, поэтому при понижении давления равновесие сместится
влево, т.е. в сторону обратной реакции.
Задача
7
Составьте
молекулярные уравнения реакций, которым соответствуют следующие
ионно-молекулярные уравнения:
S2 + 2H+ = H2S2
+ OH- = NO2- + H2O+ + Cl-
= AgCl.
Решение
К++S2-+2H++2Сl-=H2S+2К++2Сl-
К2S+2HСl=H2S+2КСl
HNO2+OH-=NO-2+H2O2+Na++OH-=Na++NO-2+H2O2+NaOH=NaNO2+H2O
Ag++NO-3+Na++Cl-=AgCl+
Na++ NO-33+NaCl=AgCl+ NaNO3
Задача 8
На
основании электронных уравнений расставьте коэффициенты в уравнения, укажите
окислитель и восстановитель.
H2O2→ H2O + O2
KMnO4 + NaSO3 + H2SO4
→ MnSO4 + K2SO4 + Na2SO4
+ H2O
Решение
Н2О-2→
Н2О-2 + О02
О-2+2е→
2О-2│1- окислитель, реакция восстановления
О-2-2е→
О20│1- восстановитель, реакция окисления
2Н2О2→ 2Н2О + О2+7O4+Na2S+4O3+H2SO4→Mn+2S+6O4+K2SO4+
Na2SO4+H2O+7+5e →Mn+2│2- окислитель, реакция восстановления
S+4-2e→S+6│5-
восстановитель, реакция окисления
2KMnO4+5Na2SO3+3H2SO4→2MnSO4+K2SO4+
5Na2SO4+3H2O
Задача
9
В
какой пробирке происходит реакция при внесении кадмиевых пластинок в растворы
хлоридов железа (II) и кобальта (II). Напишите
молекулярные и электронные уравнения реакций.
Решение
Протекание
окислительно-восстановительной реакции возможно, если потенциал окислителя
больше потенциала восстановителя Еок-ля > Евосст
В
данной реакции окислителями являются ионы железа и кобальта, а восстановителем
атомы кадмия и ионы хлора. Сравним потенциалы всех участников химической
реакции:
Е0Сd=
-0.40B
Е0Fe2+=-0.44B
Е0Сo2+=-0.28B
Е0Cl2/Cl-=1.358B
Согласно
значениям электродных потенциалов возможна реакция только в пробирке с хлоридом
кобальта:
Сd+СoCl2→CdCl2+Co
Задача
10
Почему
химически чистый цинк обнаруживает большую стойкость против коррозии, чем
технический? Напишите электронные уравнения анодного и катодного процессов,
протекающих при коррозии технического цинка в кислой среде.
Решение
Химически
чистый цинк более устойчив против коррозии, потому, что не содержит примесей.
Примеси в техническом цинке в среде электролита приводят к образованию
гальванических элементов и как следствие этого к электрохимической коррозии.
Примеси являются катодными зонами, а атомы цинка являются анодными зонами.
Составим
схему гальванического элемента:
(-)
ZnïH+ ï Zn (+)
Электродные
процессы:
газ атом химический анодный
- Анод (Zn) Zn0 - 2ē ® Zn2+окисление
Катод (Zn) H++2ē ® H2восстановление0+
2H+ = Zn2++H2
Используемая литература
1. Глинка Н.Л. Общая химия. - Л.: Химия, 1985.
. Глинка Н.Л. Задачи и упражнения по общей химии. -
М.: Высшая школа, 1985.
. Ахметов Н.С. Общая и неорганическая химия. - М.:
Высшая школа, 1988.
. Лучинский Г.П. Курс химии. - М.: Высшая школа, 1985.
. Некрасов Б.В. Учебник общей химии.- М.: Химия, 1981.
. Кудрявцев А.А. Составление химических уравнений. -
М.: Высшая школа, 1979.
. Васильева В.Г., Грановская А.А., Теперова А.А.
Лабораторные работы по общей и неорганической химии. - М.: Химия, 1979.
. Никитин Д.П. Новиков Ю.В. Окружающая среда и
человек. М.: высшая школа, 1980.
. Бокрис Д.О. Химия окружающей среды. - М.: Химия,
1982.