Синтез оптически чистого 3R-метилциклопентан-1-она из L-(-)-ментола
Федеральное агентство по образованию
Российской Федерации
Государственное образовательное
учреждение
высшего профессионального образования
«Башкирский государственный
университет»
Химический факультет
Кафедра биоорганической химии
Специализация «биоорганическая химия»
ДИПЛОМНАЯ РАБОТА
Синтез оптически чистого 3R-метилциклопентан-1-она из L-(-)-ментола
СОДЕРЖАНИЕ
ВВЕДЕНИЕ
СПИСОК СОКРАЩЕНИЙ
Глава 1.ЛИТЕРАТУРНЫЙ ОБЗОР
Глава 2.ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Глава 3.МЕТОДЫ ПОДГОТОВКИ РАСТВОРИТЕЛЕЙ И РЕАГЕТОВ
Глава 4.ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
ВЫВОДЫ
СПИСОК ИСПОЛЬЗУЕМОЙ ЛИТЕРАТУРЫ
ВВЕДЕНИЕ
Среди основных составных частей современной органической химии синтез,
пожалуй, является одной из тех, которые обладают долгой историей. Идеи
функциональности и стереохимии, например, возникли во второй половине XIX в., а концепции химической связи и
механизмов реакций в таком виде, как они известны сегодня, появились несомненно
лишь в прошлом. Синтез же был важной составной частью органической химии с
самого начала её возникновения: поэтому история его развития насчитывает многие
столетия. Тем не менее, следует отметить, что большинство ранних синтетических
работ были отрывочным и сводились в основном к выделению веществ (причём
сомнительной чистоты) из природного сырья. Действительно, систематическое
развитие органического синтеза относится к XIX в., хотя его начало было положено значительно раньше.
В последнее время органический синтез развивался вместе с развитием
органической химии в целом. По мере роста знаний в области структурной и
теоретической химии, разработки и усовершенствования методов эксперимента
химики получили возможность ставить перед собой всё более заманчивые
синтетические цели. Это в свою очередь привело к открытию новых реакций и
совершенствованию новых экспериментальных методов, а следовательно, в
дальнейшем к постановке новых синтетических целей [1].
Очень важное место в органической химии занимает синтез молекул,
содержащих кольцевые системы. Их можно использовать для изучения механизмов
реакций, когда получение такой информации в ряду ациклических соединений
затруднено. Циклические молекулы обладают стереохимическими свойствами, которые
не свойственны большинству ациклических молекул. (Примером может служить
органическое вращение вокруг простых связей в кольцевых системах). В природе
встречается огромное количество циклических молекул: фактически циклических
молекул больше, чем ациклических. К природным веществам, содержащим циклы
различного типа, относятся пенициллин, холестерин, никотин, ДНК, РНК, камфора и
каннабиол [2].
Эффективность многих биологически активных соединений в большинстве
случаев зависит от их стереохимической чистоты, поэтому важное значение имеет
правильный выбор исходного сырья и пути его трансформаций в целевую молекулу.
Один из них - это функционализация природных соединений с сохранением имеющихся
асимметрических центров.
В течение многих лет в литературе уделялось достаточное внимание
сложноэфирным производным оптически активного 3R-метилциклопентан-1-она. Они использовались в синтезе ряда
биологически активных вещест: производных каннабиноидов [3],
4-оксоциклопентабензпиранов, обладающих гипотенсивным, антидепрессантным,
обезболивающим, антиконвульсивным, успокаивающим и седативногипнотическим
действием [4]; в синтезе ипомимарона и 4-ипоминола - фураноидных метаболитов
терпеноидного происхождения, вырабатываемых в стрессовых ситуациях сладким
картофелем [5].
После декарбоксилирования в 3R-метилциклопентан-1-он сложноэфирные производные применялись в синтезе
компонента болгарского розового масла - 4R-розоксида [2-(2,2-диметилвинил)-4R-тетрагидропирана] и его 4S-эпимера [6]. 4R-розоксид
имеет очень важное значение в парфюмерной (присутствует в отдушках для губных
помад; в парфюмерных композициях для духов, дезодорантов, туалетных вод [7]) и
пищевой промышленностях (ароматизатор для колбасных изделий) [9].
Японскими учёными предложены препараты для ванн очень мягкого действия,
применяемые при солнечных ожогах, содержащие 0,1 - 80% (предпочтительно 1,0-
20%) масла из семян розы, в составе которой присутствует 4R-розоксид. Масло из семян розы
обладает заживляющим действием [8].
Из сложноэфирных производных оптически чистого 3R-метилциклопентан-1-она синтезируют:
1) α-акораден и δ-акорадиен. Эти соединения часто
встречаются в растительных маслах. (Акорановый тип получил своё название от
латинского наименования широко распространённого в средних широтах
лекарственного растения аира (Acorus calamus)) [10].
) ретигераниевую кислоту, на основе которой предложен новый
дерматологический препарат для загара, обладающий репеллентным действием.
Препарат обладает высокой эффективностью за счёт снижения раздражения. [11].
) (+) - актинидин. Он является одним из редких монотерпеноидных
алкалоидов. Выделяют его из высушенных корней лекарственного растения Valeriana officinalis, обладающего лёгким успокаивающим
действием. Актинидин является высокоактивным ингибитором активности
холинэстеразы и уменьшает активность ацетилхолинэстеразы. В естественных
условиях оказывает незначительный эффект на кроликов, а также является
аттрактантом для кошек [12]. Актинидин как основной алкалоид Valeriana officinalis находит большое применение в
фармакологии [13].
После декарбоксилирования сложноэфирные производные оптически активного 3R-метилциклопентан-1-она используются
в синтезе ювабиона, содержаржащийся в смоле бальзамической пихты Abies balsamea. Он является биологически активным
бисаболановым метаболитом, обладает активностью ювенильного гормона. Это
селективный ювеноид: оказывает гормоноподобное действие только на насекомых
семейства Pyrrocoridae (клопы). [10].
Сам же 3-метилциклопентан-1-он является искусственным ароматизатором
(вносит вклад в мясной аромат варёной говядины) [14] и используется в синтезе
компонента масла бархатцев Tagetes glandulifera -
(+)-дигидротагетона, используемого в фармакологии [15].
Таким образом, 3R-метилциклопентан-1-он
является ценным интермедиатом для синтеза ряда биологически активных
соединений, используемых в пищевой и в парфюмерной промышленностях, в бытовых
целях. Поэтому разработка эффективных путей его синтеза является актуальной
задачей.
циклизация
диизопропиловый эфир
СПИСОК СОКРАЩЕНИЙ
DMSO -
диметилсульфоксид
Et
этил
Me
метил
MCPBA
мета-хлорнадбензойная кислота
PCC
пиридиния хлорхромат
Ph
фенил
Pri
изо-пропил
THF
тетрагидрофуран
кипячение
t
нагревание
Глава 1. ЛИТЕРАТУРНЫЙ ОБЗОР
В литературном обзоре представлены именные реакции, направленные на
получение циклических соединений (малых, средний и макроциклов).
НАЗАРОВ
Циклизация аллилвинилкетонов в циклопентеноны под действием фосфорной
кислоты:
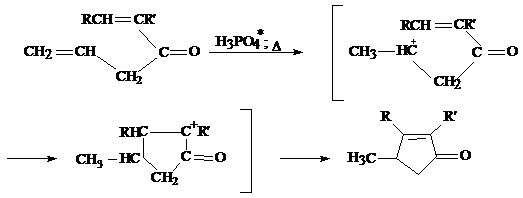
H2SO4, HCl, n-CH3C6H4SO3H, HCOOH, лед.
CH3COOH + H2SO4
Винильная
группа может содержать алифатические или ароматические заместители [16]. Как
винильная, так и аллильная группы могут быть частью циклической системы:
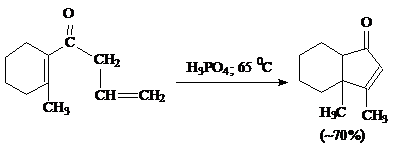

Аллилвинилкетон и все замещённые кетоны, винильная группа которых входит
в систему пятичленного цикла, гидратируются с последующей циклизацией в
тетрагидро-γ-пироны:
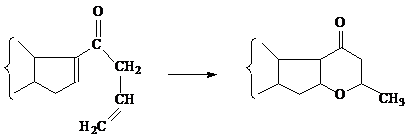
Реакция находит применение в синтезе стероидов [17].
БЕРТЛО (BERTHELOT)
Циклотримеризация ацетилена в бензол при пропускании через раскалённые
трубки:
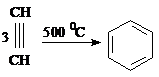
Бензол
образуется с низким выходом; побочными продуктами являются метан, нафталин и
смолы. Метод не находит практического применения; имеются другие, более
эффективные методы получения ароматических углеводородов. Реакция представляет
лишь исторический интерес, так как является первым примером превращения
алифатического соединения в ароматическое [18].
ИПАТЬЕВ
Получение
производных циклопропана циклоконденсацией 1,4-дибромолефинов с натриймалоновым
эфиром:
 * Бензол, диоксан
* Бензол, диоксан
В реакцию вступают
алифатические и алициклические дибромолефины, например:

1,1,4,4-Тетразамещённые 1,4-дибромолефины не образуют циклопропанового
кольца. Кроме натриймалонового эфира в реакции используют натриевые производные
циануксусного и бензоилуксусного эфиров, ацетилацетона и дезоксибензоина,
например:

Из
дибромолефинов и способных к енолизации циклических β-дикетонов получают производные дигидрофурана [19],
например:

ПЕЙН
- СМИТ ( PAYNE - SMITH С.W.)
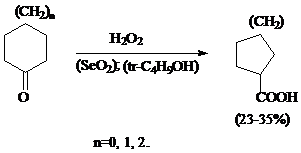
Аналогично окисляются пергидроинданоны и декалоны, давая смесь карбоновых
кислот с цис- и транс-конфигурацией [20].
СИММОНС
- СМИТ (SIMMONS - SMITH R.D.)
Получение циклопропанов из олефинов действием йодистого метилена и
цинк-медной пары:
Из СH2I2 и цинк-медной пары образуется йодистый йодметилцинк
(реагент Симмонса - Смита), который и присоединяется к олефину. Другие
метиленгалогениды в реакцию не вступают [21].
В реакцию вступают также олефины, содержащие функциональные группы,
жирноароматические и непредельные гетероциклические соединения и циклоолефины
(С6-С12), например:


В случае диенов образуется смесь продуктов, например:
 Наличие
гидроксильной группы в молекуле олефина приводит к более высоким выходам
соответствующих продуктов:
Наличие
гидроксильной группы в молекуле олефина приводит к более высоким выходам
соответствующих продуктов:

Замена
цинк-медной пары цинк-серебряной парой приводит обычно к существенному
увеличению выхода продуктов. Так, например, в случае метилакрилата при замене
цинк-медной пары цинк-серебряной парой выход эфира циклопропанкарбоновой
кислоты возрастает с 9 до 80% [21].
НОРРИШ
(NORRISH)
Фотохимическое
расщепление карбонильных соединений с последующим превращением образовавшихся
свободных радикалов по типу I или II [22].
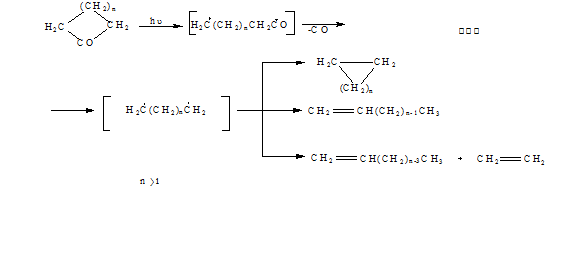 Тип I*
(для циклоалканонов в газовой фазе) - декарбонилирование ацилбирадикала и
образование циклоалкана или алкенов (см. выше).
Тип I*
(для циклоалканонов в газовой фазе) - декарбонилирование ацилбирадикала и
образование циклоалкана или алкенов (см. выше).
Тип
II* (в жидкой фазе) - переход γ-водородного атома к кислороду с образованием
1,4-бирадикала и «фотоэлиминирование», приводящее к олефину и енолу, или
циклизация бирадикала в производное циклобутана:
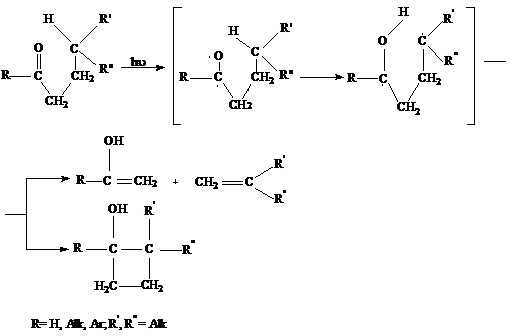
В
некоторых случаях, например при фотолизе изовалерианового альдегида (в парах),
наблюдаются одновременно оба типа превращения [22]:
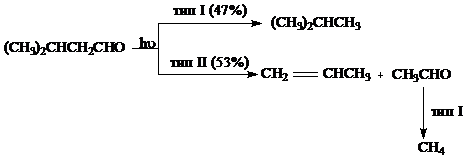
ВИДЕКВИСТ
(WIDEQVIST)
Межмолекулярная конденсация кетонов или альдегидов с динитрилом
броммалоновой кислоты под действием иодистого калия и последующая
циклизация в тетрацианоциклопропаны [23]:
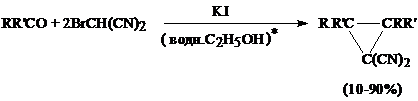
R, R’= H, Alk, Ar H2O, тетрагидрофуран
В реакцию вступают также циклические кетоны (C5-C10). Из
ароматических альдегидов и этилового эфира бромциануксусной кислоты аналогично
получают замещённые циклопропаны:

Ar = C6H4, C6H4Cl, C6H4OCH3, C6H4NO2
В качестве побочных продуктов при этом образуются (с выходом 10-30 %) RC6H4CH=C(CN)COOC2H5. [23].
БЛАН (BLANC)
Циклизация 1,4- и 1,5-дикарбоновых кислот в кетоны под действием
уксусного ангидрида:
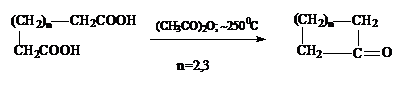
Разветвление
углеродной цепи, особенно наличие геминальных CH3-групп,
способствует циклизации. При n=4 реакция проходит с малыми выходами, при n>4
образуются межмолекулярные ангидриды [24] .

Кислоты с n=0,1, а также
соединения типа R2C(COOH)2 в указанных условиях превращаются в ангидриды (в
соответствии с правилом Блана):
Правило Блана: под действием уксусного ангидрида 1,4- и 1,5-дикарбоновые
кислоты превращаются в кетоны, а 1,2- и 1,3-дикарбоновые кислоты - в ангидриды,
например [24]:

Правило Блана часто используют при установлении строения терпенов и
стероидов.
БЛЭЗ (BLAISE)
Циклизация 2,6-дикетонов с образованием циклогексенонов под действием
хлористого водорода [25]:
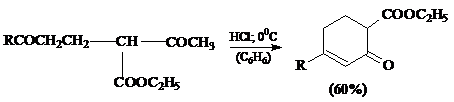 R= CH3, C2H5
R= CH3, C2H5
,7-Дикетоны в этих условиях циклизуются с образованием семичленного
цикла, а 2,5-дикетоны образуют производные фурана [25], например:
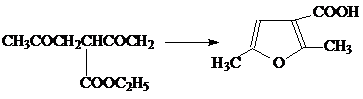
КОУП (COPE)
Термическая изомеризация 1,5-диенов, сопровождающаяся миграцией аллильной
группы от С-3 к С-1 и сдвигом двойных связей [26]:
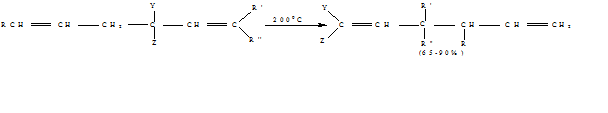 Перегруппировка является внутримолекулярной реакцией,
протекающей через циклическое переходное состояние с инверсией аллильной
группы. Скорость реакции зависит от природы заместителей (Y и Z) и
уменьшается в ряду:
Перегруппировка является внутримолекулярной реакцией,
протекающей через циклическое переходное состояние с инверсией аллильной
группы. Скорость реакции зависит от природы заместителей (Y и Z) и
уменьшается в ряду:
CN > CN + COOC2H5 >2COOC2H5
,5-Диены, не содержащие
электроноакцепторных заместителей, реагируют, как правило, в более жёстких условиях
(~3000С). Дивинилциклопропан и дивинилциклобутан перегруппировываются с
расширением цикла [26], например:

В случае соединений типа ArC(YZ)CH2CH=CH2 перегруппировка не происходит.
Синтез кетонов термической изомеризацией 3-окси-1,5-диенов называют
окси-перегруппировкой Коупа (oxy-Cope) [26]:
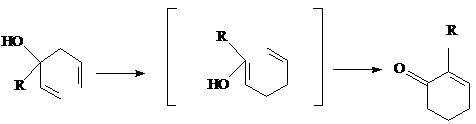
ПЕРКИН
(PERKIN)
Получение алициклических соединений алкилированием β-дикарбонильных соединений
дигалогеналканами в присутствии алкоголята [27]:

В реакцию вступают различные дигалоген- и дикарбонильные соединения, а
также β-кетонитрилы, например [27]:

ДИКМАН (DIECKMANN)
Внутримолекулярная конденсация сложных эфиров двухосновных карбоновых
кислот в присутствии оснований с образованием циклических β-кетоэфиров [28].
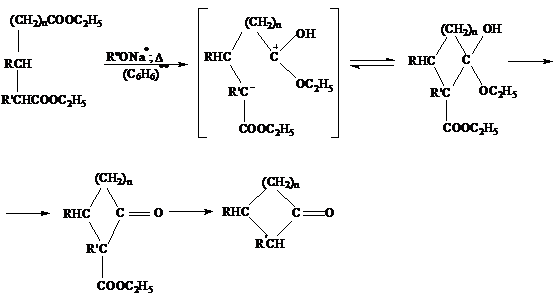
* Na, K, ROK, NaH, KH, KNH2, NaNH2, ** абс.
C2H5OH,
эфир
Лёгкость замыкания цикла цикла зависит от природы α-заместителя и уменьшается в ряду H > CH3 > C2H5 (дальнейшее удлинение цепи не
оказывает заметное влияние на скорость реакции). Как правило, образуются
пятичленные циклы, но возможно получение макроциклов. На направление циклизации
(размер цикла) влияют заместители в β-положении (например, метильная группа
блокирует соседнюю CH2-группу, а COOC2H5 - активирует [28].
Эфиры, содержащие гетероатом (N, S, O), претерпевают аналогичную конденсацию:
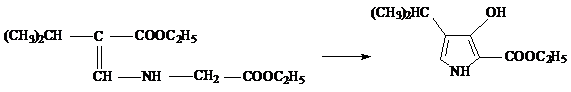
Побочные продукты те же, что и в реакции Кляйзена. Следует отметить также
возможность образования ацилоинов, особенно при использовании Na и NaH.
Реакция широко применяется для получения полициклических систем. Метод Хауза-Бабада
(House-Babad) - получение циклических кетонов циклизацией солей
фосфония (реакция, родственная конденсации Дикмана) [28]:
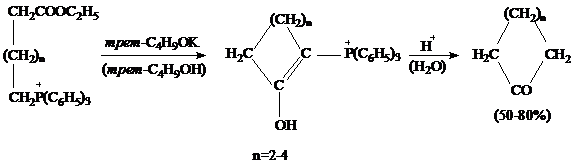
Синтез
Дикмана - Компа (Komppa) - конденсация щавелевого эфира с эфирами глутаровой
кислоты или её аналогов и последующая циклизация с образованием α-дикетонов [28]:

ДИЛЬС
- АЛЬДЕР (DIELS - ALDER)
1,4-Присоединение соединений с активированной кратной связью (диенофилов)
к сопряжённым диенам с образованием циклических структур (диеновый синтез)
[30].
В реакцию вступают циклические, ациклические и гетероциклические
1,3-диены и соединения с фрагментами
В качестве диенофилов кроме олефинов могут быть использованы соединения,
содержащие группировки и др.
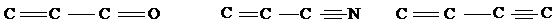
Реакция
проходит, как правило, с высокими выходами.

Наличие электроноакцепторных заместителей в диенофиле и электронодонорных
в диене облегчает процесс присоединения. Скорость реакции уменьшается с
увеличением числа и объёма заместителей в исходных веществах.
Диеновый синтез протекает по схеме цис-присоединения; компоненты
ориентируются в соответствии с правилом «накопления насыщенности», что приводит
к образованию эндо-изомеров:

Кислоты Льюиса не только ускоряют реакцию, но и вызывают изомеризацию
продуктов. Так, при реакции 2-метилбутадиена-1,3 с метилвинилкетоном в обычных
условиях образуется смесь 1,4- и 1,5-дизамещённых циклогексенов в соответствии
71:29; в присутствии SnCl4
повышается доля 1,4-изомера (93:7).
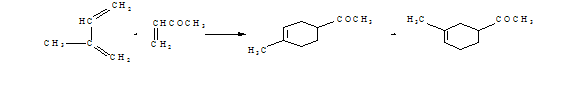
Реакция
Дильса - Альдера обратима. При нагревании аддукты обычно распадаются на
исходные компоненты или дают новые диен- и диенофил («ретро-реакция» Дильса -
Альдера или «ретро-диеновое» разложение), например [31]:
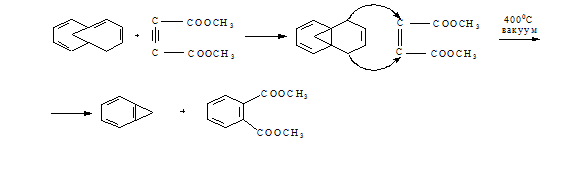
Взаимодействие
несопряжённого диена с диенофилом, в результате которого три π-связи превращаются в три σ-связи с образованием двух новых циклов, называют
«гомо-реакцией» Дильса - Альдера, например:

Диеновый синтез широко применяется во всех областях органической химии.
ВИХТЕРЛЕ (WICHTERLE)
Получение бициклических кетонов конденсацией циклических кетонов с
1,3-дихлор-цис-бутеном-2 и последующей циклизацией под действием серной кислоты
[32]:
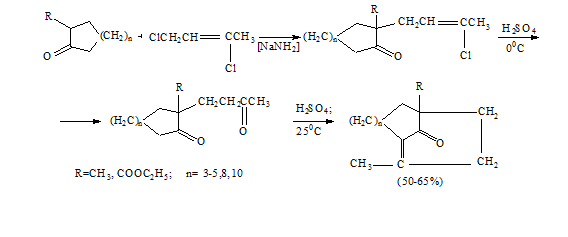
При
R=H и n=1,2 циклизация проходит с участием метильной группы
боковой цепи:
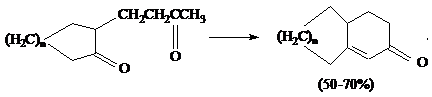
Аналогично циклизуются непредельные алифатические кетоны:
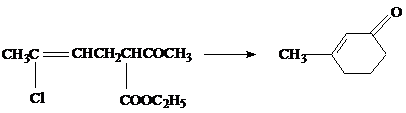
БЛОМКВИСТ (BLOMQUIST)
Синтез макроциклических кетонов внутримолекулярной конденсацией
алифатических дикетенов, полученных дегидрохлорированием хлорангидридов
дикарбоновых кислот [33]:
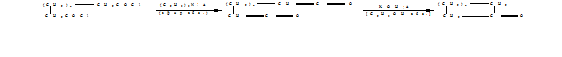 В реакцию
вступают также хлорангидриды непредельных кислот:
В реакцию
вступают также хлорангидриды непредельных кислот:
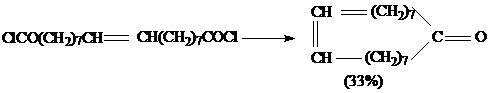
Побочные продукты: линейные полимеры типа: HOOC(CH2)n[CO(CH2)n]xCOOH и дикетоны (в результате межмолекулярной
конденсации). Последняя реакция подавляется при проведении процесса в условиях
сильного разбавления [33].
РУЖИЧКА (RUZICKA)
Получение циклических кетонов пиролизом солей дикарбоновых кислот в
вакууме [35]:
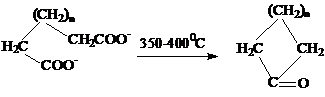 n =
до 31
n =
до 31
В реакции могут быть использованы соли Ca, Th, Ce, V, Zr, Pb и Ba. Выходы кетонов зависят от размера кольца: С5-С6 - ~ 80 % ,
С7-С8 - 10-20%, С9-С13 - 0,5 %, затем выходы несколько повышаются (для С17 ~
8%) и далее снова падают до ~2 %. Побочная реакция - образование макроциклических
дикетонов (до С34) [35].
Промышленные варианты процесса - нагревание смеси кислот с оксидами
указанных металлов при пропускании паров кислоты над оксидом металла.
ХЭНСЛИ - ПРЕЛОГ - ШТОЛЛЬ (HANSLEY
- PRELOG - STOLL)
Получение макроциклических ацилоинов циклизацией эфиров дикарбоновых
кислот под действием металлического натрия*:

=7,
8 и т. д.
Ацилоины
получают лишь при большом избытке Na (4 экв), в противном случае
происходит циклизация по Дикману. Выходы продуктов при n=7-11
составляют ~40% и повышаются с увеличением размера цикла, например при n =19
выход ацилоина 96% [36].
Метод
позволяет получать гетероциклические, а также макроциклические ацилоины с n=фениленовыми
звеньями, например:

m>10; R=Alk, Ar
Ацилоины
легко превращаются в кетоны восстановлением цинком в кислоте или дегидратацией
с последующим гидрированием α,β-непредельного
кетона [36].
РОБИНСОН - МАННИХ (ROBINSON R. - MANNICH)
Получение
бициклических непредельных кетонов алкилированием циклических кетонов
четвертичными солями β-аминокетонов (оснований Манниха) под действием
оснований с последующей циклизацией в результате внутримолекулярной альдольной
конденсации [37]:
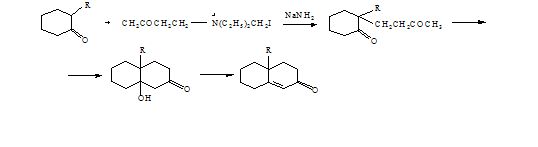
Аналогично
реагируют и другие циклоалканоны (С7-С15). Проведение реакции облегчается, если
предварительно кетон превращают в α-оксиметиленкетон конденсацией с HCOOC2H5:

При
использовании бис-оснований Манниха получают производные мостиковых
углеводородов:
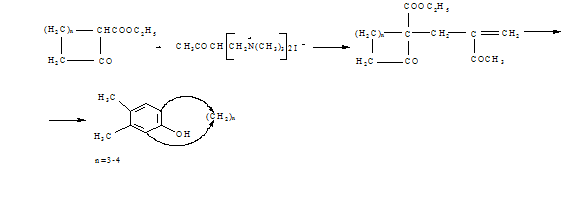
Бициклические
непредельные кетоны могут быть получены также присоединением по Михаэлю
циклических β-дикетонов к α,β-непредельным кетонам с последующей циклизацией под
действием основания*, например [37]:
*
Называют также аннелированием по Робинсону.
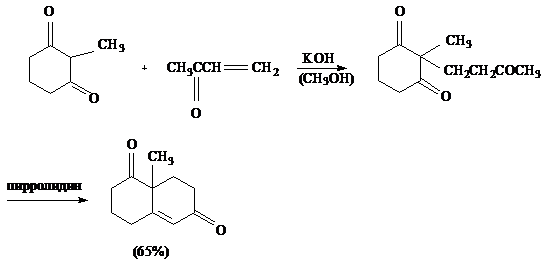
БЮХНЕР (BUCHNER)
Присоединение алифатических диазосоединений к олефинам (или ацетиленам) с
образованием замещённых пиразолинов (или пиразолов) с последующим превращением
в производные циклопропана [38]:
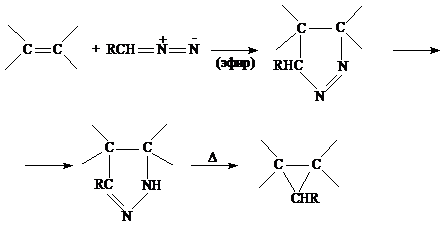
Аналогично реагируют α,β-непредельные кетоны, эфиры
непредельных кислот, арилзамещённые олефины, например [38]:
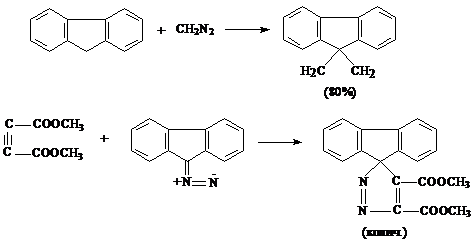
Аналогично
олефинам реагирует бензол:

В
случае α,β-непредельных кетонов или эфиров R’’CH-группа
присоединяется к β-углеродному атому. Сопряжённые диены присоединяют
диазосоединения в положение 1,2.
КИЖНЕР
Замыкание кольца циклопропана при термическом разложении пиразолинов,
образующихся при взаимодействии α,β-непредельных альдегидов или кетонов и
гидразина [39]:


Выходы
на стадии разложения пиразолинов достигают 90%, а общие выходы замещённых
циклопропанов 50-70 %. В реакцию вступают карбонильные соединения с
алифатическими, алициклическими, ароматическими и гетероциклическими
заместителями [39]
МАЙО (MAYO)
Фотохимическое присоединение ацетилацетона к циклоолефинам с образованием
дикетонов [40]:
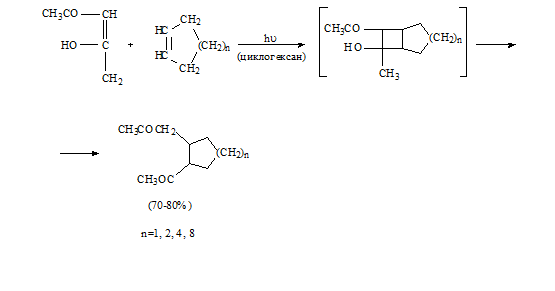
Использование
2-ацетилциклоалканонов позволяет получать полициклические кетоны, например
[40]:

РЕППЕ (REPPE)
Циклополимеризация ацетилена или его производных в арены и
циклополиолефины в присутствии никелевых катализаторов [41]:
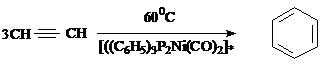
Реакция
позволяет с выходами, близкими к количественным, получать бензол и его
производные [41], а также циклооктатетраен:

Получение
циклооктатетраена открывает путь для синтеза пробковой кислоты и полиамидов на
её основе.
ЦИГЛЕР
(ZIEGLER)
Получение
макроциклических кетонов циклизацией динитрилов под действием N-алкиланилидов
натрия с последующими гидролизом и декарбоксилированием* [42]:
* LiN(C2H5)C6H5, LiN(C2H5)2; ** (n-C3H7)2O, (i-C3H7)2O
* Называют также реакцией Циглера-Торпа (Тhorpe).

Необходимость
большого разбавления (вследствие возможной полимеризации) достигается путём
очень медленного добавления раствора динитрила к раствору конденсирующего
средства. Выходы кетонов зависят от размера кольца [42]:
Выход, % Выход, %
C5-C7 ………..колич. C12 ………………. 8
C8
……………88 C13 ……………… 15
C9-C11……….1- 2 C14-C25
…………. 60
C26-C32 ………….~80
Метод позволяет получать также кислородсодержащие макрогетероциклические
соединения:

ШОЛЛЬ (Scholl)
Дегидроциклизация полициклических диарилкетонов с образованием
конденсированных циклических систем при нагревании с AlCl3 [43].

* AlCl3 + NaCl
В реакцию вступают моно- и поликетоны, имеющие свободное пери- положение
по отношению к карбонильной группе. Присутствие органических оснований или
следов йода облегчает реакцию.
Если пери-положение занято или в пара-положении к СО-группе находятся
группы ОН или OR, образуется пятичленное кольцо:
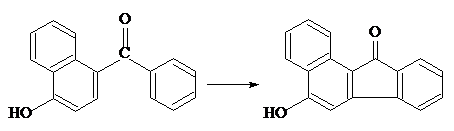
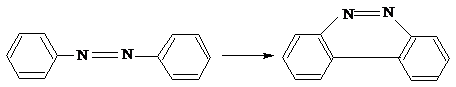
Аналогично циклизуются полициклические нитрилы, имиды и азосоединения,
например [43]:
ВЮРЦ
- ФИТТИГ (WURTZ - FITTIG)
Получение жирноароматических углеводородов конденсацией арилгалогенидов с
алкилгалогенидами под действием металлического натрия [44]:
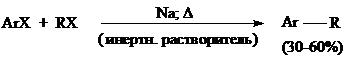
Обычно применяют алкилбромиды, реже иодиды и очень редко хлориды. Легче
всего реагируют первичные алкилгалогениды, труднее - вторичные, а третичные
[кроме (С6Н5)3СХ] не вступают в реакцию. Вместо RX могут быть использованы R2SO4, например:
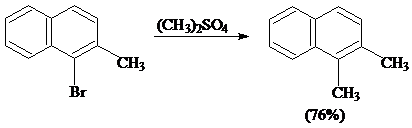
Побочные процессы: образование Ar - Ar, R - R, RH и олефинов.
Метод
может быть использован для синтеза элементоорганических соединений, например: 
Модификация
Виттига - Витта (Wittig - Witt) - использование фениллития вместо натрия при
конденсации галогенпроизводных жирноароматических углеводородов [44]. Метод
даёт возможность получать макроциклы:
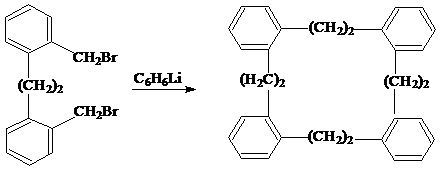
РЭПСОН
(RAPSON)

R, R’=H, CH3, OCH3 * SnCl4, HF, Al2O3, ThO2; ** [Pd\C]
Получение трифениленов взаимодействием циклогексенилциклогексанона и
арилмагнийбромидов с последующей циклизацией в октагидротрифенилены и
дегидрированием последних [45].
Наилучший результат (выход ~30%) получен при применении в качестве
катализатора на стадии циклизации смеси CaO + Al2O3 + ThO2. При R=R’=CH3 реакция идёт с низким выходом (~2-3%) [45].
ФУДЗИМОТО - БЕЛЛО (FUJIMOTO - BELLEAU)
Получение циклических α,β-непредельных кетонов из δ-еноллактонов и реактива Гриньяра с
последующим гидролизом под действием едкого кали в метаноле [46]:
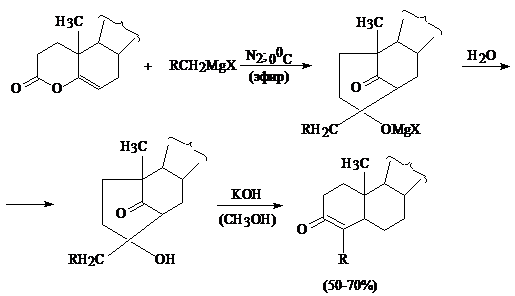
R = Alk, C6H5
Аналогично реагируют δ-енаминлактамы:

Вместо
реактива Гриньяра можно использовать алкилиденфосфораны или фосфонат-анионы.
Реакция широко применяется в химии стероидов.
ХУНСДИККЕР
(HUNSDIECKER)
Получение
макроциклических кетонов циклизацией ω-галоген-алгилацетоуксусных эфиров в результате внутримолекулярного
алкилирования под действием поташа с последующим гидролизом и
декарбоксилированием:
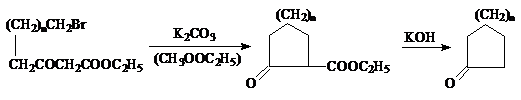
Реакцию проводят при большом разбавлении во избежание межмолекулярной
конденсации. Метод позволяет получать кетоны с хорошими выходами [47].
Таким образом, из литературного обзора видно, что методы циклизации
достаточно многочисленны и широко используются в органическом синтезе.
Глава 2. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Ранее эфиры 4R-метил-2-оксоциклопентан-1-карбоновой
кислоты получали циклизацией диметиловых и диэтиловых эфиров 3R-метил-1,6-гександикарбоновой кислоты
[4, 5, 48], а 3R-метилциклопентан-1-он
(9) - их декарбоксилированием [15]. Известен также синтез [49] исходя из
дорогого и малодоступного R-пулегона,
используя на ключевой стадии циклизацию 3R-метил-1,6-гександикарбоновой кислоты.
Нами предлагается новый подход к синтезу оптически чистого 3R-метилциклопентан-1-она (9) на основе
доступного монотерпеноида - L-(-)-ментола
(1), доступный [6] из мятного масла - эфирное масло перечной мяты Mentha piperita в стадии цветения. Так как данный
экстракт в своем составе имеет наряду с ментолом также его сложные эфиры,
ментон и ряд других соединений, для отделения спирта (1) была проведена следующая
цепь превращений. Щелочная обработка привела к гидролизу эфиров, а этерификация
борной кислотой дала труднолетучий борат ментола. Примеси же были удалены
вакуумированием. Омылением остатка был регенерирован ментол, отогнанный с
водяным паром. Экстракция его из воды и осушка дали »60% ментола (1),
[α]D25 -47.7° (с 2.4; EtOH), ср. -48.5o (с 5.0; EtOH)
[6].
Для осуществления синтеза соединения (9) нами использована следующая цепь
селективно протекающих трансформаций. Окислением спирта (1) по Джонсу бихроматом
калия был получен (-)-ментон (2). Его окисление по Байеру-Виллигеру кислотой
Каро протекало региоспецифично с образованием 3R,7-диметилоктан-6S-олида (ментолактона) (3).Переведением его в ментолактон (3), согласно
[50], и переэтерификацией с помощью изопропанола в присутствии H2SO4 был получен изопропил-3R,7-диметил-6S-гидроксиоктаноат
(4). Последовательное окисление по Кори, а затем по Байеру-Виллигеру кислотой
Каро, протекающее региоспецифично, привело к диизопропиловому эфиру 3R-метилгексан-1,6-диовой кислоты (6).
Циклизация последнего по Дикману проведена несколькими способами. При
использовании изопропилата натрия как основания получена смесь (3.5:1) по
данным ГЖХ и спектра ПМР: из соотношения интегральных интенсивностей дублета в
области 1.15 м.д. для группы СН3-4 и дублета при 1.19 м.д. для СН3-5,
принадлежащих изопропиловым эфирам 4R-метил-2-оксо- (7) и 5R-метил-2-оксо-
(8) циклопентан-1-карбоновых кислот соответственно, неделимым колоночной
хроматографией. Декарбоксилирование полученной смеси эфиров (7) и (8)
нагреванием в DMSO в присутствии NaCl по методике [51] приводит к
единственному продукту - 3R-метилциклопентан-1-ону
(9). Попытка повысить региоселективность реакции циклизации диэфира (6),
используя амид натрия как основание, ранее использованный в [52] для
диметилового эфира 3-метилгексан-1,6-диовой кислоты, оказалась неудачной:
вернулось исходное соединение. Циклизация соединения (6) в присутствии натрия,
также применяемого для циклизации диэфиров [53], протекает с
декарбоксилированием и образованием единственного продукта - циклопентанона
(9).


Глава 3.
МЕТОДЫ ПОДГОТОВКИ РАСТВОРИТЕЛЕЙ И РЕАГЕНТОВ
Ацетон
перегоняют над CaCl2, т. кип.
56оС [3].
Диэтиловый эфир выдерживали над КОН, последовательно перегоняли над
металлическим Na и LiAlH4, т.кип. 34.5оС [3].
Толуол (пара-) сульфохлорид. 10 г неочищенного TsCl растворяли в минимальном количестве хлороформа и
быстро охлаждали. Выпавшую п-толуолсульфокислоту отфильтровывали, маточный
раствор оставляли на два дня на созревание при комнатной температуре.
Охлаждали, после фильтрации получали 7 г мелких белых кристаллов очищенного TsCl, т. пл. 145-146оС.
Пиридин выдерживали в течение длительного времени над гранулами КОН, затем
перегоняли над ВаО, т. кип. 115.3оС. [3]
Хлорхромат пиридиния Py×CrO3-HCl (РСС) [21]. К 184 мл 6 н. HCl (1,1 моль) быстро при перемешивании
прибавляли 100 г (1 моль) CrO3.
После 5 мин гомогенный раствор охлаждают до 0оС и 79.1 г (1 моль) Py осторожно прибавляют в течение 10
мин. При 0оС выпадает желто-оранжевая соль, которую отфильтровывают, выход
180,8 г (84%). Перед употреблением вакуумируют.
Тетрагидрофуран выдерживали над КОН, последовательно перегоняли над
металлическим Na и LiAlH4, т.кип. 65.оС [3].
Хлорид меди (I) промывали в
аппарате Сокслетта абс. ТHF,
сушили под вакуумом.
Хлористый метилен перегоняли над Р2О5, т. кип. 40оС [3].
Хлороформ перегоняли над Р2О5, т. кип. 61.2оС [3].
Глава 4. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
ИК-спектры записывали на приборе UR-20 в тонком слое. Спектры ЯМР
регистрировали на спектрометре «Bruker
АМ-300» (рабочая частота 300.13 МГц для ПМР и 75.47 МГц для ЯМР 13С) в CDCl3.
За внутренний стандарт приняли значение сигналов в ПМР - примеси протонов в
дейтерированном растворителе d 7.27 м.д. для CDCl3,
а в ЯМР 13С - средний сигнал CDCl3 d 77.00 м.д. ГЖХ выполняли на приборах
«Chrom-5» [длина колонки 1.2 м, неподвижная
фаза - силикон SE-30 (5%) на Chromaton N-AW-DMCS (0.16-0.20 мм), рабочая температура
50-3000С] и «Chrom-41» [длина колонки 2.4 м,
неподвижная фаза - PEG-6000, рабочая
температура 50-2000С]; газ-носитель - гелий. Колоночную хроматографию
осуществляли на силикагеле L
(ЧССР) с зернением 40-100 мкм. Анализ ТСХ проводили на пластинках “Silufol UV-254” (ЧССР). Оптическое вращение измерено на поляриметре “Perkin-Elmer-241-MC”.
Данные элементного анализа всех соединений отвечали вычисленным. анализа всех
соединений отвечали вычисленным.
L-(-)-Ментол
(1). 10 г «мятного масла» растворяют в 50 мл этанола, добавив 2 г КОН, смесь
кипятят 30 мин. Затем почти полностью отгоняют спирт, к остатку добавляют 25 мл
Н2О и 25 мл Еt2O. Все это переносят в делительную воронку. Эфирный слой
промывают небольшими порциями воды до pH=7, отделяют и сушат Na2SO4.
После отгонки растворителя масло переносят в колбу Кляйзена, соединенную
с приемником через короткий воздушный холодильник; добавляют 1 г борной кислоты
и включают вакуумный насос. Когда разряжение достигнет 10 - 15 мм рт. ст.,
нагревают колбочку на водяной бане; вода образующаяся при этерификации
отгоняется. Затем водяную баню заменяют масляной и медленно поднимают
температуру до 200оС. Разряжение доводят до 3 мм рт. ст, при этом отгоняются
все спутники ментола, а трудно летучий ментиловый эфир борной кислоты остается
в перегонной колбе.
Остаток переносят в круглодонную колбу емкостью 100 мл вместе с небольшим
количеством спирта, используемого для смывания стенок; добавляют 2 мл
насыщенного раствора NaHCO3
и начинают отгонку с водяным паром. Борный эфир омыляется, а ментол переходит в
дистиллят. При помощи делительной воронки еще не застывшее масло отделяют от
Н2О, переносят в коническую колбочку и охлаждают. Затвердевший ментол
перекристаллизовывают из петролейного эфира. Выход 50% от эфирного масла; т.
пл. 42-43оС, [α]20D- 49о (с 20, EtOH) [54]
3R,7-Диметилоктан-6S-олид (3). К перемешиваемой при t<10o смеси 24 мл конц. H2SO4 и 8 мл воды присыпали 16.8 г (60
ммоль) K2S2O8, а затем
последовательно прикапывали 26 мл воды и 5 г (32.5 ммоль) ментона (2).
Перемешивали при комнатной температуре 24 ч, далее осторожно вылили в 20 мл
холодной воды, экстрагировали CH2Cl2 (3х50 мл), последовательно
промывали насыщенными растворами Na2S2O3, NaCl.
Сушили MgSO4, упаривали и получили 4.31 г (78%)
сложного эфира (4), [α]D26 -8.5° (c 4.0;
CHCl3). ИК-спектр (ν,
см-1): 1380, 1390 (CH3), 1730 (C=O). Спектр ПМР
(300 Мгц, CDCl3): 0.94 и 0.96 (д, 6Н, J 6.84 Гц, CH3-7, H-8),
1,02 (д, 3Н, J 6.64 Гц, СН3-3), 1.16-1.34 (м, 2Н,
Н-4), 1.55-1.60 (м, 2Н, Н-5), 1.79-1.94 (м, 2Н, Н-3, Н-7), 2.42-2.57 (м, 2Н,
Н-2), 3.99-4.05 (м, 1Н, Н-6). Спектр ЯМР 13С (СDCl3): 17.09 и 18.40 (СН3-7, С-8), 23.96 (к, СН3-3),
30.42 (д, С-3), 30.93 (т, С-4), 33.33 (д, С-7), 37.43 (т, С-5), 42.55 (т, С-2),
84.83 (д, С-6), 175.26 (с, С-1)
Изопропиловый эфир 3R,7-диметил-6S-гидроксиоктановой кислоты (4). Раствор 2.5 г (14.7 ммоль)
ментолактона (3), полученный из L-(-)-ментола
(1) согласно [55], в 19 мл сухого изопропанола, подкисленный двумя каплями
конц. Н2SO4, перемешивали на магнитной мешалке
72 ч. Изопропанол упаривали, остаток разбавляли этилацетатом, последовательно
промывали насыщенными растворами NaCl, NaHCO3, NaCl, сушили над MgSO4 и упаривали. Получили 2.87 г (85%) оксиэфира (4),
[α]D20 -13.30 (с 0.90, CHCl3). ПМР спектр (CDCl3,
δ, м.д., J / Гц): 0.82 (д, J=6.8, Н-8, СН3-7, 6Н), 0.84 (д, J=6.8, СН3-3, 3Н), 1.19 (д, J=6.8, (СН3)2СН, 6Н), 1.93 (м, Н-2¸Н-5, Н-7, 8Н), 3.25 (м, Н-6, 1Н),
3.97 (уш.с., ОН, 1Н). Спектр ЯМР 13С (СDCl3): 18.73 (к, С-8, СН3-7), 19.64 (к, СН3-3), 21.68 (к,
СН(СН3)2), 30.42 (д, С-3), 31.24 (т, С-4), 32.86 (т, С-5), 33.22 (д, С-7),
41.83 (т, С-2), 67.19 (д, СН(СН3)2), 76.63 (д, С-6), 172.67 (с, С-1).
Изопропиловый эфир 3R,7-диметил-6S-оксооктан-1-овой кислоты (5). К суспензии 4.18 г (19.4
ммоль) РСС в 75 мл сухого СН2Сl2
прикапывали раствор 2.87 г (12.4 ммоль) оксиэфира (4) в 5 мл сухого СН2Сl2. Перемешивали 3 часа, разбавляли Et2O (80 мл), отфильтровывали через слой Al2O3 и упаривали.
Получили 2.50 г (83%) кетоэфира (5), [α]D20 +2.8 (с 2.82, CHCl3). ПМР спектр (CDCl3,
δ,м.д., J/Гц): 0.91 (д, J=6.1, СН3-3, 3Н), 1.07 (д, J=6.8, СН3-7, Н-8, 6Н), 1.19 (д, J=6.1, (СН3)2СН, 6Н), 1.50 (м, Н-3,
Н-4, 3Н), 2.22 (м, Н-2, Н-5, Н-7, 5Н), 4.97 (септет, J=6.1, (СН3)2СН, 1Н). Спектр ЯМР 13С (СDCl3): 18.21 (к, С-8, СН3-7), 19.41 (к,
СН3-3), 23.86 (к, (СН3)2СН), 30.01 (д, С-3), 30.26 (т, С-4), 37.74 (т, С-5),
40.76 (д, С-7), 41.86 (т, С-2), 67.38 (д, (СН3)2СН), 172.35 (с, С-1), 214.38
(д, С-6).
Диизопропиловый эфир 6R-метилгексан-1,6-диовой
кислоты (6). К суспензии 3.10 г (8.9 ммоль) МCPBA в 30 мл сухого CHCl3 при комнатной температуре прикапывали раствор 1.40 г
(6.2 ммоль) кетона (5) в 10 мл сухого CHCl3. Перемешивали 48 ч, разбавляли 100 мл СН2Cl2, последовательно промывали насыщенными растворами NaHCO3, Na2S2O3, NaCl, сушили MgSO4 и упаривали. Получили 1.25 г (83%) диэфира (6),
[α]D20 +3.1 (с 3.20, CHCl3). ПМР спектр (CDCl3,
δ, м.д., J/Гц): 0.93 (д, J=6.1, СН3-3, 3Н), 1.19 (д, J=6.1, (СН3)2СН, 12Н), 4.97 (септет, J=6.1, (СН3)2СН, 2Н), 2.06 (м, Н-2¸Н-5). Спектр ЯМР 13С (СDCl3): 19.18 (к, СН3-3), 21.72 (к,
(СН3)2СН), 30.32 (д, С-3), 30.64 (т, С-4), 41.92, 42.47 (оба т, С-2, С-5),
67.39, 67.44 (оба д, (СН3)2СН), 172.26 (с, С-6), 173.02 (с, С-1).
Изопропиловые эфиры 4R-метил-2-оксо-
(7) и 5R-метил-2-оксо- (8)
циклопентан-1-карбоновых кислот. К раствору изопропилата натрия, полученного из
0.05 г (2.05 мг-ат.) Na и
0.13 г (2.1 ммоль) изопропанола в 3 мл сухого толуола, прикапывали (Ar) раствор 0.50 г (2.1 ммоль) диэфира
(6) в 2 мл сухого толуола. Смесь кипятили в течение 8 ч. Охлаждали до комнатной
температуры, выливали в 25 мл холодной воды, содержащей 8.5 мл СН3СООН. Водный
слой экстрагировали эфиром (3 х 40 мл), последовательно промывали насыщенными
растворами NaHCO3 и NaCl, сушили Na2SO4 и упаривали. Получили 0.30 г (79%)
смеси (3.5:1) эфиров (7) и (8) по данным ГЖХ.
Изопропиловый эфир 4R-метил-2-оксоциклопентан-1-карбоновой
кислоты (7). ПМР спектр (CDCl3, δ, м.д., J/Гц): 1.15 (д, J=6,
СН3, 3Н), 1.19 (д, J=6, СН(СН3)2,
6Н), 2.22 (м, СН2, СНСН3, 5Н), 3.26 (т, J= 6.4, СНСО2, 1Н), 5.35 (септет, J= 6.1, СН(СН3)2, 1Н).
Изопропиловый эфир 5R-метил-2-оксоциклопентан-1-карбоновой
кислоты (8). ПМР спектр (CDCl3, δ, м.д., J/Гц): 1.19 (д, J=6,
СН3, 3Н), 1.19 (д, J=6, СН(СН3)2,
6Н), 1.46 и 2.15 (оба м, СН2, 4Н), 2.75 (м, СНСН3, 1Н), 3.15 (д, J= 9.1, СНСО2, 1Н), 5.35 (септет, J= 6.1, СН(СН3)2, 1Н).
R-метилциклопентан
(9). а. К нагретой до 900С суспензии 0.04 г (1.9 мг-ат.) Na в 3 мл сухого толуола (Ar) прикапывали раствор 0.47 г (1.9
ммоль) диэфира (6) в 4 мл сухого толуола и кипятили 1 ч. Реакционную массу
разбавляли гексаном и отфильтровывали через слой Al2O3 (2 см).
Получили 0.15 г (81%) метилциклопентанона (9), [α]D20 +152.50 (с 1.20, CHCl3), см. [α]D20 +1540 (с 0.6, МеОН) [56].
Параметры ИК, ПМР и ЯМР 13С идентичны полученным ранее [57].
б. К раствору 0.50 г (2.5 ммоль) смеси диэфиров (7) и (8) в 21 мл DMSO и 3 мл H2O добавляли 0.70 г
(12 ммоль) NaCl и выдерживали при 1650С в течение 2
ч, затем охлаждали, водный слой экстрагировали петролейным эфиром, сушили Na2SO4 и упаривали. Получили 0.16 г (65%) циклопентанона (9),
идентичного полученному в опыте а.
ВЫВОДЫ
Таким образом, исходя из доступного монотерпеноида L-(-)-ментола разработана схема
синтеза ценного интермедиата для синтеза ряда биологически активных веществ -3R-метилциклопентан-1-она с общим
выходом 30% в расчете на исходное соединение (ментол). Циклизация по Дикману
была проведена несколькими способами. Увеличили региоселективность при
циклизации использованием диизопропилового эфира 3R-метилгексан-1,6-диовой кислоты до соотношения продуктов
3,5:1 (при использовании соответствующего диметилового эфира образовывалась
смесь продуктов 2,5:1).
СПИСОК ИСПОЛЬЗУЕМОЙ ЛИТЕРАТУРЫ
1. А. Терней. Современная органическая химия // М.: Мир
-1981. - 1.- С. 679.
2. Р. Маки, Д. Смит. Путеводитель по органическому синтезу //
М.: Мир.- 1985 - С. 352.
3. R. K. Razdan, G. R. Handrick, H. C. Danzell, J. F.
Howes, M. Winn, N. P. Plotnikoff, P. W. Dodge, A. T. Dren // J. Med. Chem.
-1976. - №19.- С. 552
. H. R. R. Kumar, D. H. Cloyce, K. J. Ruth // Pat. USA N 4007207- Реф. в РЖХим.- 22О98П -1977.
. L. T. Burka, R. M. Bowen, B. J. Wilson // J. Org.
Chem.- № 39.-P. 3241.- 1974.
. S. Takano, K. Masuda, K. Ogasavara. //
Heterocycles.-№ 16.-P.1509.- 1981.
7 Rosen Komposition. Schweisheimer. // Seifen - Ồle -
Fette - Wachse. - 1959.- 85.- № 26.- С. 821 - 822.
Препарат для ванн: Заявка 1319414, Япония, МКИ4 А 61 К 7/50/ Саймо Ясухико, Марамацу Цукаса; К.к. Цумура. - № 63 - 151579; Заявл. 20.06.88; Опубл. 25.12.89. // Кокай токё кохо. Сер.
3(2). - 1989. - 103 - С. 83-87. - Яп.
. Способ получения ароматизатора для колбасных изделий: Пат.
1833144 СССР, МКИ5 А 22 С. 11/ 100/ Солнцева Г.Л., Андреенков В.А., Белоусова
Е.Е, Романова Н.В., Афанасьева И.И.// Всес.н.-и. и конструкт. ин-т мяс.
пром-ти. - № 4948516/134.
10 Семёнов. Химия природных соединений // Новосибирск:
Сибирская
изд-ая фирма РАН, Наука. - 2000.- С. 664.
11 Nouvelles compositions dermstologiques bronzantes
insectifuges // Заявка 2622103 Франция; МКИ4 А 61 К 7/42/ Thorel Jean - Noёl. - № 8714590; Заявл. 22.10.87. Опубл. 28.04.89.
Vinilketenes. Synthesis of (+)-Actinidine. // J. Org.
Chem.- Vol. 42.- № 12.- p. 2111.- 1977.
Isolation, Structure and Synthesis of Alkaloids from
Valeriana officinalis L. // Acta Chem. Scand.- 21.- 1967.- № 1.- p. 53.
14 L. G. Mac, J. M. Ames. // J. Food Sci. -№ 52.-P.
42.- 1987.
B. Lefebvre, J.-P. Le Roux, J. Kossanyi, J.-J.
Basselier // C. r. Acad. sci..- C. 277.- 1049.- 1973.
Назаров И.Н. О механизме гидратации и циклизации диенов.
Новый м метод синтеза циклопентенонов // Успехи химии. - 1951.- Т. 20.- С. 71.
Назаров И.Н. Успехи органического синтеза на основе ацетилена
//Успехихи химии.- 1951.- Т. 20.- С. 309.
1. 18 Raphael R. A. Acetylenic Compounds in
Organic Synthesis // London.- Buttenworths scientific publ.- 1955.- P 65.
19 Ипатьев В.П., ЖРФХО.- 1901.- Т. 33.- С. 540.
Payne G. P., Smith C.W. Reaction of Hydrogen Peroxide
II. A Novel Use of Selenium Dioxide as Catalyst for the Ring Contraction of
Cycloalkanones to Cycloalkanecarboxylic Acids. // J. Org. Chem..- 1957.- V.
22.- P. 1680.
. 21 Simmons H.E., Smith R.D. A new synthesis
of cyclopropanes from olefins // J. Am. Chem. Soc.- 1958.- V. 80.- P. 5323.-
1959.- V. 81.- P. 4256.
Lewis F.D., Hillard T.A. Photochemistry of
Methyl-Substituted Butyrophenones.// J. Am. Chem. Soc.- 1972.- V. 94.- № 11.- P. 3852-3858
Журина Ф.Г., Вульфсон Н.С.Взаимодействие бромциануксусного
эфира с ароматическими альдегидами в условиях реакции Реформатского и
Видеквиста.II // Журнал органической химии.- 1967.-Т. 3.- С. 504
24 Bachmann E., Deno N.C.Preparation of the Isomeric
2-( Naphthylmethyl) cyclopentanones \\ J. Am. Chem. Soc.- 1949.- V. 71.- P.
3540.
25 Jäger
H., Keymer R.- Arch. Pharm.- 1960.- V. 293.- P. 896.
26 Baldwin J.E., Kaplan M.S. A Mechanistic Alternative
for the Thermal Antara-Antara Cope Rearrangements of Bicyclo[3.2.0]
hepta-2,6-dienes and Bicyclo[4.2.0] octa-2,7-dienes. // J. Am. Chem. Soc.-
1971.- V. 93.- P. 3969.
27 Rice L. M., Grogan C.H. Spiranes.II.Spiro[3.3]
heptane Derivatives.// J. Org. Chem.- 1961.- V. 26.- P. 54.
28 House H. O., Babad H. A new Synthesis of Cyclic
ketones. // J. Org. Chem.-
1963.- V. 28.- P. 90.
29 Хаузер Ч.Р. Хадсон Б.Е. Конденсация сложных эфиров и
сложные реакции. // Органические реакции под реакцией Берлина А.Я.- Т. 1.- С.
345.
Онищенко А. С., Диеновый синтез.// М., Изд. АН СССР.- 1963.-
С. 649
Вассерман А., Реакция Дильса - Альдера. // Пер. с англ. Под
ред. Л. М. Когана и О.Н. Темкина. М., «Мир».-
1968.- С. 133
James A., Marshall J. A., Schaeffer D. J. Synthesis of
Bicyclo [4.4.0] decanones and Bicyclo [3.3.1] nonanones via the Wichterle
Reaction. // J. Org. Chem.-
1965.- V. 30.- P. 3642.
Физер Л., Физер М., Органическая химия. // Изд. 2-е. Т. 2.
Пер. с англ. Под ред. Н.С. Вульфсона. М., «Химия».- 1970.- С. 82.
Синтез органических препаратов. // Под ред. акад. Казанского
Б.А.,М.-1949.- Т. 1.- С. 518.
Синтез органических препаратов. // Под ред. акад. Платэ А.Ф.,
М.-1949.- Т. 8.- С. 48.
Синтез органических препаратов. // Под ред. акад. Платэ А.Ф.,
М.-1949.- Т.
8.- С. 48.
Spencer T. A., Schmiegel K.K., Williamson K.L.
Synthesis of 1,9-cis-Diacetoxy--octalone-6;
Stereochemical Course of the Robinson Annelation Reaction. // J. Am. Chem. Soc.- 1963.- V. 85.- P. 3785.
38 ОR.- V. 18.- P. 217.
39 Мещеряков А. П., Глуховцев В. Г., Петрова Д. Синтез
1-метил-1,2-дицикло-пропилциклопропана. // ДАН СССР.- 1960.- Т. 130.- С. 779.
Mayo P., Takeshita H. Photochemical synthesis.6. the
formation of heptandiones from acetylacetone and alkenes. // Can. J. Chem.-
1963.- V. 41.- P. 440.
Meriwether L. S.,Leto M.F., ColthupE.C., Kennerly G.W.
The polymerization of Acetylenes by Nickel-Carbonyl-Phosphine Complexes.IV.
Kinetics and Polymerization Mechanisms. // J. Org. Chem.- 1962.- V. 27.- P.
3930.
Houben-Weyl. // Bd. 4.- S. 758.- OR.- V. 15.- P. 28.
Olah G. A., Schilling P., Gross I. M. // Am. Chem. Soc. - 1974.- V. 96.- P. 876.
Касухин Л. Ф., Грагеров И. П. // Ж. орг. хим.- 1971.- Т. 7.- С. 2009.
45 Buess C. M., Lawson D. D. The preparation,
reactions, and properties of triphenylenes. // Chem. Rev.- 1960.- V. 60.- P.
315.
46 Belleau B. // J. Am. Chem. Soc. - 1951.- V. 73.- P.
5441.
47 Herzig K.,
Rüchardt C., Zum Mechanismus der Hunsdiecker-Reaktion. // Chem. Ber.-
1972.- Bd. 105.- S. 363.
48 Sandoz Patents Ltd. // Pat. Britain № 1,004,661.-
1965. - Сhem. Abstr.- 64, 2058h.- 1966.
W. C. M. Kokke, F. Varkevisser.// J. Org. Chem.-№ 39.-
P. 1535.- 1974.
D. F. Taber, S. A. Saleh, R. W. Korsmeyer // J. Org.
Chem.- № 45.- P. 4699.- 1980.
В. Н. Одиноков, Г. Ю. Ишмуратов, М. П. Яковлева, Р. Л.
Сафиуллин, А. Н. Волгарев, В. Д. Комиссаров, Г. А. Толстиков // Докл. АН.- №
326.- С. 842.- 1992.
Н. С. Вульфсон, В. И. Зарецкий. Реакция Дикмана. Реакции и
методы исследования органических соединений // М.: Гос. научно-техн. изд-во
хим. лит-ры. № 12.-С. 7.- 1963.
В. Н. Одиноков, Р. И. Галеева, Г. А. Толстиков. // Ж. орган.
Химии.- 12.-
1442.- 1976.
54 James A., Marshall J. A., Schaeffer D. J. Synthesis
of Bicyclo [4.4.0] decanones and Bicyclo [3.3.1] nonanones via the Wichterle
Reaction. // J. Org. Chem.- 1965.- V. 30.- P. 3642.
55 Taber D. F., Saleh S. A., Korsmeyer R. W. // J. Org. Chem.- № 45.- P. 4699.-
1980.
Kokke W. C. M., Varkevisser F., Photochemistry of
Methyl-Substituted Butyrophenones. // J. Org. Chem..- № 39.-P. 1535.- 1974.
57 Salaün
J., Ollivier J. // Nouv. j. chim.- № 5.- P. 587.- 1981.