Свойства элементов подгруппы меди
Содержание
Введение
. Атомные свойства
. Нахождение в природе
. Получение
. Физические свойства
. Химические свойства
простых веществ
. Свойства соединений
меди, серебра и золота
. Токсичные свойства
меди, серебра, золота и их соединений
. Применение меди,
серебра, золота и их соединений
Заключение
Список литературы
Введение
Побочную подгруппу I
группы периодической системы элементов Д.И. Менделеева образуют медь, серебро и
золото (подгруппа меди).
Медь - происхождение русского названия не установлено. Лат. Cuprum (Cu) - от греч. купрос (название о. Кипр); по месту добычи
медных руд.
Медь известна человечеству с древнейших времен (5000-3500 лет до н.э.).
Подробно описаны ее свойства Агриколой (1550-1556 г.г.), Василием Валентином
(1599-1602 г.г.). Сплавы меди сыграли заметную роль в развитии цивилизации.
Серебро - возможно, от ассир. сарпу (светлый); по цвету металла. Лат. Argentum (Ag) от греч. аргос (белый, восходит к санскр. арганта -
светлый).
Серебро было известно уже с 5000 - 4000 г.г., вновь открыто В. Бирингуччо
(1560 г.), Агриколой (1550 - 1556).
Золото - одного корня с русск. желтый; по цвету металла. Лат. Aurum (Au) - от аурора (утренняя звезда); по блеску металла.
Золото добывалось и обрабатывалось задолго до н.э. (5000 лет до н.э.),
большой вклад в его изучение внесли В. Бирингуччо (1540 г.), П.Р. Багратион
(1843 г.).
По распространенности в природе элементы этой подгруппы стоят далеко
позади соответствующих щелочных металлов. Если содержание самой меди в земной
коре оценивается еще довольно большой величиной - 0,003%, то доля серебра
составляет уже только 2×10-6 %, а золота - 5×10-8
%.
Природная медь слагается из изотопов 63Сu (69,1 %) и 65Сu (30,9 %),
серебро - из изотопов 107Аg (51,35 %) и 109Аg (48,65 %), тогда как золото
является “чистым” элементом (197Аu).
В основном состоянии элементы подгруппы меди имеют строение внешних
электронных оболочек 3d104s1 (Сu), 4d105s1 (Аg), 5d106s1 (Аu) и одновалентны.
Возбуждение ближайших потенциально трехвалентных состояний Сu (3d94s14р1), Аg
(4d95s15р1) и Аu (5d96s16р1) требует затраты соответственно 464, 673 и 502
кДж/моль.
Медь принадлежит к интересным в биологическом отношении элементам. Она
является катализатором внутриклеточных окислительных процессов.
Установлено, что небольшие количества меди необходимы для нормального
развития растений и удобрение почв (особенно - болотистых и песчаных) ее
соединениями часто сопровождается резким повышением урожайности. По отношению к
избыточному содержанию меди устойчивость растительных организмов очень
различна.
Из животных организмов больше всего содержат меди некоторые моллюски
(осьминоги, устрицы). У высших животных она накапливается главным образом в
печени и клеточных ядрах других тканей. Недостаточное поступление Сu в организм (ежедневная норма для
человека составляет около 5 мг) ведет к уменьшению новообразования гемоглобина
и развитию анемии, которая может быть излечена введением соединений меди в
пищу. Из отдельных видов последней наиболее богаты медью молоко и дрожжи.
Следы серебра (порядка 0,02 мг Аg на 100 г сухого вещества) содержатся в
организмах всех млекопитающих, но его биологическая роль не ясна. У человека
повешенным содержанием Аg (0,03 мг на 100 г свежей ткани, или 0,002 вес.% в
золе) характеризуется головной мозг. Интересно, что в изолированных ядрах его
нервных клеток - нейронов (число которых у человека составляет около 15 млрд.)
- серебра гораздо больше (0,08 вес.% в золе). С пищевым рационом человек
получает в среднем около 3,1 мг Ag за сутки. Относительно много его содержит
яичный желток (0,2 мг в 100 г). Выводится серебро из организма главным образом
с калом.
Относительно содержания в организмах и биологической роли золота пока
ничего определённого не известно. Отмечалось наличие его в зернах, листьях и
стеблях кукурузы. Воды океана содержат переменные количества золота, (от
ничтожных следов до 65 мг/т).
1. Атомные
свойства
медь серебро золото
элемент
Элементы подгруппы меди являются предпоследними d-элементами (каждый в своем периоде). В атомах элементов
должны находиться по 9 d-электронов.
Однако, поскольку d-подуровень
близок к завершению, энергетически оказывается более выгодным переход одного s-электрона в d-состояние (таблица 1.1). Поэтому энергетическое состояние
валентных электронов выражается общей формулой (n - 1)d10ns1 («провал» электрона).
Таблица 1.1. Атомные свойства элементов подгруппы меди и их соединений
|
Элементы
|
Символ
|
Валентные электроны
|
Радиус атома, нм
|
ОЭО
|
|
Медь
|
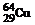 3d104s10,1231,75 3d104s10,1231,75
|
|
|
|
|
Серебро
|
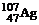 4d105s10,1441,42 4d105s10,1441,42
|
|
|
|
|
Золото
|
 5d106s10,1441,42 5d106s10,1441,42
|
|
|
|
У элементов подгруппы меди в образовании химической связи могут
участвовать s-электрон внешнего энергетического уровня и 1 или 2 d-электрона
предвнешнего энергетического уровня. Поэтому возможные степени окисления +1,
+2, +3. Причем для меди характерно состояние окисления +2, для серебра +1, для
золота +3.
Сродство к электрону у Cu, Ag, Au значительно больше, чем у s-эле-ментов I
группы, а у Au даже выше, чем у кислорода и серы.
Этот факт объясняется эффектом проникновения s-электронов внешнего уровня к ядру.
В соединениях с низшими степенями окисления элементы подгруппы меди
проявляют основные свойства, а в соединениях с высшими степенями окисления -
амфотерные.
2. Нахождение
в природе
Среди элементов данной подгруппы наиболее распространенной является медь,
а серебро и золото - редкие элементы. Медь, серебро и золото встречаются в
природе, как в самородном состоянии, так и в виде соединений (таблица 1.2).
По минеральному составу медные руды делятся на три группы: сульфидные,
окисленные и самородные.
Чистое серебро сопутствует золоту. Золото в природе чаще встречается в
самородном состоянии. Из химических соединений золота, имеющих промышленное
значение, известны минералы - теллуриды.
В морской воде содержится около 0,05 мг/т.
Таблица 1. 2. Содержание элементов подгруппы меди в земной коре
|
Элемент
|
Содержание в земной коре, %
мол. доли
|
Минералы
|
|
Медь Cu
|
3,6 × 10-3
|
Cu2O - куприт; Cu2S -халькозин; CuCO3×Cu(OH)2
- малахит; 2CuCO3×Cu(OH)2 - азурит; Cu3FeS4
- борнит
|
|
Серебро Ag
|
1,6 × 10-4
|
Ag2S - серебряный блеск, аргентит; AgCl
- роговое серебро, хлораргирит; AgBr - бромаргирит; Ag3SbS3
- пираргирит; Ag3AsS3 - пираргирит
|
|
Золото Au
|
5 × 10--8
|
AuTe2 - калаверит; AuAgTe4 -
сильванит
|
3. Получение
Для получения меди используют пиро- и гидрометаллургические процессы.
Выплавка меди из ее сульфидных руд - сложный процесс. Большинство
металлов подгруппы меди получают обжигом сульфидов и дальнейшим их
восстановлением:
Cu2O + C = 2Cu + CO
Cu2O + Cu2S = SO2 + 6Cu
Процесс извлечения меди из халькопирита можно выразить суммарной
реакцией:
2CuFeS2 + 5O2 + 2SiO2 = 2Cu + 2FeSiO3 + 4SO2
В результате таких процессов получают черную медь. Для получения чистой
(рафинированной) меди (99,9-99,99% Cu) ее очищают электролизом.
Гидрометаллургические методы получения меди основаны на растворении
минералов, содержащих медь, в разбавленных растворах H2SO4 или NH3. Из полученных растворов медь
вытесняют железом или выделяют электролизом.
Наиболее чистые металлы получают электролизом солей.
Ag2S + 4KCN = 2K[Ag(CN)2] + K2S+ 2KCN = K[Ag(CN)2] + KCl
Аналогично получают золото из золотоносного песка:
4Au + 8NaCN + 2H2O + O2 = 4Na[Au(CN)2] + 4NaOH
Na[Au(CN)2] + Zn = Na2[Zn(CN)4] + 2Au
4. Физические
свойства
Медь, серебро и золото - блестящие металлы красного, белого и желтого
цветов. Они отличаются высокой плотностью, тепло- и электропроводностью.
Металлы подгруппы меди обладают высокими температурами кипения и плавления
(таблица 1.3), а также высокой (особенно золото) пластичностью. Из них могут
быть получены тончайшие проволока и фольга. Они превосходят другие металлы по
тепло- и электропроводности, а именно, серебро и медь занимают по этим
показателям I и II места среди металлов.
На воздухе
медь окисляется, покрываясь зелено-серой пленкой CuCO3 × Cu(OH)2, серебро и золото устойчивы к
окислению кислородом:
2Cu + O2 + CO2 + H2O = (CuOH)2CO3
При наличии в воздухе сероводорода серебро покрывается черным Ag2S.
Таблица 1.3. Физические свойства элементов подгруппы меди и их соединений
|
Вещество
|
d, г/см3
|
tпл, 0С
|
tкип, 0С
|
Электропроводность
|
Твердость
|
|
Cu медь
|
8,9
|
1085
|
2540
|
57
|
3,0
|
|
Ag серебро
|
10,5
|
961
|
2170
|
59
|
2,7
|
|
Au золото
|
19,3
|
1064
|
2880
|
40
|
2,5
|
5. Химические свойства простых
веществ
Металлы подгруппы меди малоактивны, причем химическая активность
понижается в подгруппе сверху вниз.
Об уменьшении химической активности в ряду Cu-Ag-Au свидетельствуют значения стандартных
электродных потенциалов, которые составляют соответственно +0,34; +0,80; +1,45
В.
Наиболее характерная степень окисления золота +3; известны соединения
золота со степенями окисления +1 и +2.
Золото Д малоактивный в химическом отношении металл, нормальный
электродный потенциал реакции Au3++3 e=Аu при 298 К Фо= 1,498 В. Для
одновалентного золота Аu++е=Аu, при нормальных условиях этот потенциал
составляет 1,962 В. В ряду напряжений, металлов золото располагается правее
водорода, причем дальше всех остальных металлов. Поэтому в растворе соляной,
серной и других кислот при отсутствии окислителей золото не растворяется.
Хорошо растворяет золото смесь кислот, состоящая из 1 объема азотной кислоты и
3Д4 объемов соляной («царская водка»). На воздухе золото не изменяет своего
цвета и не взаимодействует с кислородом даже при иагревании до 400 °С. При обычных
условиях поверхность золота покрыта тончайшим адсорбированным слоем кислорода,
однако непосредственно, даже при нагреве, золото не соединяется не только с
кислородом, но и с серой, и селеном. Оксид Аu2О и оксид Аu2О3 могут быть
получены только косвенным путем. С водородом золото не реагирует даже при
высоких температурах. Однако летучие гидриды типа АuН образуются в небольших
количествах при обдувке золота струей водорода при температурах выше 1425 °С.
Воздействуя на золото атомарным водородом, удается получить бесцветный твердый
гидрид, который очень неустойчив. Водород крайне незначительно растворяется в
твердом золоте. Максимальная растворимость при 900°Ссоставляет ~8*10-4%. При
воздействии аммиака на водную суспензию Аu2О образуется соединение Au3N*NH3,
которое после промывки разбавленной азотной кислотой переходит в Au3N*H2О. В
сухом состоянии оба соединения взрывоопасны. Золото не реагирует с углеродом
даже при высоких температурах. Соединение золота с этим элементом может быть
получено косвенным путем Д воздействием ацетилена на раствор тиосульфатного
комплекса золота, при этом образуется желтый карбид Аu2С2, точнее ацетилид
золота, который крайне взрывоопасен. Золото реагирует с хлором, бромом и иодом.
Реакция с бромом протекает при комнатной температуре с образоваинем бромида
AuBr3. С сухим хлором и иодом золото вступает в реакцию только при нагревании,
при этом образуется хлорное золото AuCl3. Теплоты образования АиС13 и AuBr3
соответственно равны 117,08 и 54,15 кДж/моль. В водном растворе хлора (хлорной
воде) золото легко растворяется. Еще более активно, чем ионы хлора, действуют
на золото ноны CN-. В их присутствии золото окисляется даже кислородом воздуха.
Этот процесс лежит в основе получения золота цианидным выщелачиванием из
золотоносной руды. Со своими ближайшими аналогами Д серебром и медью Д золото
образует непрерывные твердые растворы, аналогичный характер взаимодействия
наблюдается при сплавленнн золота с некоторыми элементами VIII группы Д
платиной и палладием. В системах золото Д медь и золото Д платина непрерывные
твердые растворы существуют лишь при высоких температурах, при понижении
температуры наблюдается их распад с образованием упорядоченных металлических
соединений, так называемых фаз Курнакова. Золото образует ряд металлических
соединений (ауридов) с электроположительными и переходными металлами ПА, IIIA,
IVA, VIIA и VIIIA подгрупп. Ограниченные твердые растворы и металлические
соединения золото образует со многими элементами, более электроотрицательными
по сравнению с ним. Так, золото образует широкие области ограниченных твердых
растворов с металлами ПА подгруппы (цинком, кадмием, ртутью), IIIA подгруппы
(алюминием, галлием, индием), IVA подгруппы (германием, оловом, свинцом) и VA
подгруппы (мышьяком, сурьмой). За пределами растворимости в этих системах
образуются соединения, имеющие во многих случаях переменные составы.
Характерная черта золота Д большое разнообразие во взаимодействии с другими
элементами Периодической системы, связанное с образованием твердых растворов н
большого числа металлических соединений различного состава, с различной
кристаллической структурой и различной природой химической связи. Все это
обусловливает возможность создания на основе золота большого числа сплавов
различного назначения.
Серебро проявляет химические свойства, характерные для элементов Iб
подгруппы периодической системы Менделеева. В соединениях обычно одновалентно.
Серебро находится в конце электрохимического ряда напряжений, его
нормальный электродный потенциал Ag = Ag+ + e- равен 0,7978 в.
При обычной температуре Ag не взаимодействует с О2, N2 и Н2. При действии
свободных галогенов и серы на поверхности Серебра образуется защитная пленка
малорастворимых галогенидов и сульфида Ag2S (кристаллы серо-черного цвета). Под
влиянием сероводорода H2S, находящегося в атмосфере, на поверхности серебряных
изделий образуется Ag2S в виде тонкой пленки, чем объясняется потемнение этих
изделий. Сульфид можно получить действием сероводорода на растворимые соли
Серебра или на водные суспензии его солей. Растворимость Ag2S в воде 2,48·10-3
моль/л (25 °С). Известны аналогичные соединения - селенид Ag2Se и теллурид
Ag2Te.
Из оксидов Серебра устойчивыми являются оксид (I) Ag2O и оксид (II) AgO.
Оксид (I) образуется на поверхности Серебра в виде тонкой пленки в результате
адсорбции кислорода, которая увеличивается с повышением температуры и
давления.O получают действием КОН на раствор AgNO3. Растворимость Ag2O в воде -
0,0174 г/л. Суспензия Ag2O обладает антисептическими свойствами. При 200 °С
оксид Серебра (I) разлагается. Водород, оксид углерода (II), многие металлы
восстанавливают Ag2O до металлического Ag. Озон окисляет Ag2O с образованием
AgO. При 100 °С AgO разлагается на элементы со взрывом. Серебро растворяется в
азотной кислоте при комнатной температуре с образованием AgNO3. Горячая
концентрированная серная кислота растворяет Серебро с образованием сульфата
Ag2SO4 (растворимость сульфата в воде 0,79% по массе при 20 °С). В царской
водке Серебро не растворяется из-за образования защитной пленки AgCl. В
отсутствие окислителей при обычной температуре НCl, HBr, HI не взаимодействуют
с Серебром благодаря образованию на поверхности металла защитной пленки
малорастворимых галогенидов. Большинство солей Серебра, кроме AgNO3, AgF,
AgClO4, обладают малой растворимостью. Серебро образует комплексные соединения,
большей частью растворимые в воде. Многие из них имеют практическое значение в
химические технологии и аналитической химии, например комплексные ионы
[Ag(CN)2]-, [Ag(NH3)2]+, [Ag(SCN)2]-.
Отношение к
простым веществам
С водородом эти элементы гидридов не образуют.
С галогенами образуют галиды с соответствующими степенями окисления: медь
окисляется до +1, +2 (при обычной температуре), остальные при нагревании: Ag до +1 (лучше всего взаимодействует с
фтором), Au до +1, +3 (лучше всего
взаимодействует с хлором).
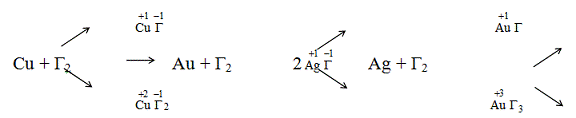
Кислородом медь окисляется до степеней окисления +1, +2. Оксиды Ag2O, Au2O, Au2O3 получаются
косвенным путем.
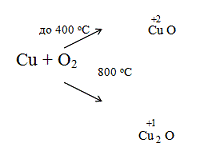
Оксид серебра (I) Ag2O образуется при окислении серебра озоном.
С серой образуют сульфиды все элементы, кроме золота.
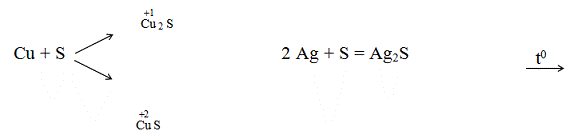
С некоторыми малоактивными неметаллами (например, фосфором и углеродом)
взаимодействуют только медь и серебро (образуются фосфиды и карбиды).
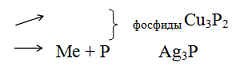
С металлами образуют сплавы, в том числе и между собой.
Известны сплавы меди: бронза, томпак, манганин, мельхиор, латунь,
константан.
Медь, серебро и золото образуют сплавы друг с другом.
Все элементы подгруппы меди растворяются в ртути, образуя амальгамы.
Отношение к
сложным веществам
Так как в ряду стандартных электродных потенциалов металлы подгруппы меди
расположены правее водорода, то они взаимодействуют только с разбавленными
кислотами в присутствии окислителя, например кислорода:
Cu + 4HCl + O2 = 2CuCl2
+ 2H2O
С водой не взаимодействуют.
С кислотами - окислителями (разбавленная и концентрированная HNO3,
концентрированная H2SO4) реагируют все металлы, кроме золота.
При этом кислоты могут окислять их только за счет аниона:

Золото растворяется лишь в горячей концентрированной селеновой кислоте,
«царской водке» (HNO3(конц.) + 3HCl(конц.)) и в насыщенном хлором
растворе HCl:
Au + HNO3 + 3HCl = AuCl3 + NO + 2H2O+ HNO3 + 4HCl = H[AuCl4] + NO + 2H2O
Au + 6H2SeO4(конц.)
= Au2(SeO4)3 + 3SeO2 + 6H2O+ 3Cl + 3HCl = H[AuCl4]
Все металлы устойчивы к щелочам.
Однако медь в присутствии кислорода растворяется в водных растворах
аммиака:
4Cu + 8NH3 + O2 + 2H2O = 4[Cu(NH3)2]OH
6. Свойства
соединений меди, серебра и золота
Медь,
серебро и золото образуют оксиды состава 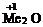 , где они
проявляют низшую степень окисления +1, которым соответствуют гидроксиды
, где они
проявляют низшую степень окисления +1, которым соответствуют гидроксиды  - основания средней силы.
- основания средней силы.
Cu2O -
красного цвета
Ag2O -
темно-бурого цвета нерастворимы в воде
Cu2O и Ag2O
взаимодействуют с азотной кислотой и с концентрированными растворами щелочей,
т.е. обладают амфотерными свойствами. Растворению малорастворимых соединений
этих элементов способствует образование комплексов:
Ag2O + 2HNO3 = 2AgNO3
+ H2O
Cu2O + 2NaOH + H2O = 2Na[Cu(OH)2]O(Сu2O) + 4NH3 + H2O ® 2[Ag(NH3)2]OH+ KCl =
K[AgCl2]+ 2KCN = K[Ag(CN)2] + KCl+ 2Na2S2O3 = Na3[Ag(S2O3)2] + NaBr
Гидроксид CuOH образуется
при действии щелочи на соли Cu+.
AgOH
существует в растворе в очень малых концентрациях, т.к. разлагается в момент
образования:
AgOH =
Ag2O + H2O
Поэтому при действии щелочей на растворы солей серебра (I) образуется оксид Ag2O, а не AgOH:
2AgNO3 +
2NaOH = Ag2O + 2NaNO3 + H2O
Соединения серебра (I) - сильные окислители. В реакциях с пероксидом
водорода, арсином, альдегидами, иодидом калия и соединениями марганца (II) в
растворе аммиака восстанавливается серебро.
Характерным взаимодействием соединений серебра (I) в аммиачных растворах с альдегидами (например, глюкозой) является
реакция «серебряного зеркала» (окисление альдегидов до соответствующих кислот
или их солей):
2[Ag(NH3)2]OH + R-CHO = 2Ag ¯+ R-CHONH4 + 3NH3 + H2O
Гидроксид золота (I)
разлагается с выделением соответствующего оксида:
AuOH =
Au2O + H2O
Соединения Cu (I) и Au (I) легко
окисляются, даже кислородом воздуха, например
4CuCl + O2 + 4HCl = 4CuCl2+ 2H2O
Соединения CuГ и AuГ (Г - галоген) диспропорционируют:
3AuГ = 2Au + AuГ3
CuI = Cu + CuI2
Соединения
элементов со степенью окисления +2 представлены следующими веществами: 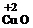 - оксид меди (II) черного
цвета; AgF2 и AgO, Ag3(PO4)2, известны комплексы Ag (II).
- оксид меди (II) черного
цвета; AgF2 и AgO, Ag3(PO4)2, известны комплексы Ag (II).
Наиболее
распространены соединения меди (II), которые являются сильными окислителями. На
окислительных свойствах сульфата меди (II) основан
процесс дегазации белого фосфора и фосфина:
5CuSO4 + 2P + 8H2O = 5Cu + 2H3PO4 + 5H2SO4
CuSO4 + PH3 + 4H2O = 4Cu + H3PО4 +
4H2SO4
Качественная
реакция на соединения меди (II) протекает с альдегидами, например глюкозой, при нагревании
с образованием сначала желто-оранжевого осадка гидроксида меди (I), а
затем красного осадка Cu2O.
Из
соединений с кислородом со степенью окисления +2 устойчивы соединения меди.
Оксид CuO нерастворим в воде, но растворим в кислотах.
Гидроксид
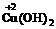 - осадок голубого цвета, образуется при действии
щелочей на соли меди (II):
- осадок голубого цвета, образуется при действии
щелочей на соли меди (II):
CuSO4 + 2KOH = Cu(OH)2 + K2SO4
Гидроксид
меди (II) - неустойчивое соединение, разлагается при
нагревании:
Cu(OH)2
= CuO + H2O
Гидроксид
меди (II) обладает амфотерными свойствами. Растворим в
растворах кислот и щелочей.
В
щелочной среде происходит получение гидроксокомплексов:
Cu(OH)2 + 2NaOH = Na2[Cu(OH)4]
С
водным раствором аммиака гидроксид меди и оксид меди (II) образуют
аммиакат меди (II) сине-фиолетового цвета:
Cu(OH)2 + 4NH3 = [Cu(NH3)4](OH)2 + 4NH3 + Н2О = [Cu(NH3)4](OН)2
CuSO4 + 4NH3 =
[Cu(NH3)4]SO4
В
растворах разбавленных кислот гидроксид меди и оксид меди (II)
образуют аквакомплексы:
Cu(OH)2 + 2HCl + H2O = [Cu(H2O)4]Cl2
Соли
элементов побочной подгруппы I группы и сильных кислот легко гидролизуются:
Cu(NO3)2 + H2O 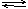 CuOHNO3
+ HNO3.
CuOHNO3
+ HNO3.
Из соединений со степенью окисления +3 известны соединения меди и золота.
При окислении гидроксида меди (II) в щелочной среде гипохлоритом образуется купрат - производное меди (III):
2Cu(OH)2 + NaClO + 2NaOH = 2NaCuO2 + NaCl + 3H2O
Купраты неустойчивы и разлагаются с выделением кислорода в водной среде
или при подкислении:
4NaCuO2 + 6H2O = O2 + 4Cu(OH)2 + 4NaOH
NaCuO2 + 12HCl = 4NaCl + 4CuCl2 + O2 + 6H2O
Оксид
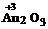 - темно-коричневого цвета порошок, нерастворим в
воде, получают косвенным путем. Соответствующий ему гидроксид Au(OH)3 получают
при действии концентрированных растворов щелочей на хлорид золота (III) AuCl3:
- темно-коричневого цвета порошок, нерастворим в
воде, получают косвенным путем. Соответствующий ему гидроксид Au(OH)3 получают
при действии концентрированных растворов щелочей на хлорид золота (III) AuCl3:
AuCl3 + 3NaOH = Au(OH)3 + 3NaCl
Гидроксид
золота (III) обладает амфотерными свойствами с преобладанием
кислотных свойств. При растворении его в щелочах образуются аураты (соли
метазолотой кислоты HAuO2):
Au(OH)3 + KOH = K[Au(OH)4]
При
взаимодействии с HCl образуется анионный комплекс:
Au(OH)3 + 4HCl = H[AuCl4] + 3H2O
Гидроксид
Au(OH)3 - вещество красно-бурого цвета, при просушивании
переходит в желто-красный порошок HAuO2 × H[AuCl4] × 4H2O -
золотохлористоводородную кислоту. Образуется при упаривании раствора золота в
насыщенной хлором хлороводородной кислоте:
2Au + 3Cl2 + 2HCl = 2H[AuCl4]
Соль
этой кислоты Na[AuCl4] × 2H2O
называется «золотой» солью.
Ионы
золота (III) - сильные окислители:
2AuCl3 + 3SnCl2 + 6HCl = 2Au¯ + 3H2[SnCl6]
AuCl3 + 3H2O2 + 6KOH = 2Au¯ + 3O2 + 6KCl +
6H2O.
7. Токсичные
свойства меди, серебра, золота и их соединений
Все соли меди ядовиты, раздражают слизитые, поражают желудочно-кишечный
тракт, вызывают тошноту, рвоту, заболевание печени. При вдыхании пыли меди
развивается хроническое отравлении. Предельно-допустимые концентрации (ПДК) для
аэрозолей 1 мг/м3, питьевой воды 1 мг/л, для рыбных водоемов 0,01 мг/л, в
сточных водах до биологической очистки 0,5 мг/л.
Медеплавильное производство является источником канцерогенов.
ПДК серебра в воздухе 0,1-0,5 мг/м3. При попадании растворимых соединений
серебра на кожу и слизистые оболочки происходит восстановление серебра до
серо-черного коллоидного металла. Это окрашивание исчезает в результате
растворения и истирания коллоидного серебра.
При отравлении соединениями серебра следует дать большое количество
10%-ного раствора хлорида натрия (поваренной соли).
Некоторые препараты Au (I) токсичны, накапливаются в почках, в
меньшей степени - в печени, селезенке и гипоталамусе; накопление в почках может
привести к их заболеванию, а также дерматитам, стоматитам, тромбоцитопении.
Все растворимые производные меди, серебра и золота ядовиты!
8. Применение меди, серебра, золота и их соединений
Медь, серебро и золото находят применение как в индивидуальном состоянии,
так и в виде сплавов:
латунь (40 - 50% Zn,
остальное - Cu) - гильзы боеприпасов;
бронза (сплавы меди с оловом, алюминием, кремнием, висмутом, бериллием,
фосфором);
нейзильбер (65% Cu,
20% Zn, 15% Ni);
томпак (90% Cu, 10% Zn).
Линии высоковольтных передач изготавливают из сплавов Cu - Zn - Cd,
отличающихся значительной прочностью и твердостью.
Свыше 50% меди используется в электрохимической промышленности. Сплавы
меди с другими металлами широко применяются в машиностроительной
промышленности, в судостроении, в электротехнике (в качестве полупроводниковых
материалов - Cu2O и CuO),
энергетической промышленности, стекольной промышленности для окраски стекол в
красный цвет. Все медные сплавы обладают высокой стойкостью против атмосферной
коррозии. Соли меди - минеральные краски различных цветов.
Медь относится к числу микроэлементов, необходимых живым организмам.
Серебро используется при изготовлении мощных циклотронов (серебряные
провода), при изготовлении аккумуляторов (в газоанализаторах), для дезинфекции
воды.
Аммиачный раствор оксида серебра в присутствии глюкозы восстанавливают до
серебра (получение зеркал).
Ион Ag+ обладает сильно выраженными
бактерицидными свойствами. Поэтому в медицине используют «серебряные марли» и
«вату».
AgNO3
- исходное вещество для получения всех производных серебра, применяется в
аналитической химии и в медицине под названием «ляпис». Галогениды серебра
применяются в фотографии.
Золото используют для покрытия металлов, в медицине, в ювелирном деле.
Соединения золота применяют для золочения и окраски стекол и фарфора, в
фотографии используются AuCl3
и H[AuCl4].
Элементы подгруппы меди находят и другое разнообразное применение,
включая окислительно-восстановительные каталитические процессы.
Заключение
Медь Си - необходимый микроэлемент живых организмов. Серебро Ag и золото
Au - примесные микроэлементы. Их соединения применяют в медицине.
Медь - биогенный элемент, содержится в тканях животных и растений. Общая
масса меди в организме взрослого человека примерно 100 мг, что составляет около
0,0001%. Примерно 30% этого количества содержится в мышцах. Печень и мозг также
богаты медью. Металлическая медь и ее соединения токсичны. Наиболее важными с
физиологической точки зрения являются медьсодержащие белки - цитохромоксидаза и
супероксиддисмутаза.
Цитохромоксидаза - один из компонентов дыхательной цепи, локализованной в
мембранах митохондрий. Обеспечивает клеточное дыхание, восстанавливая кис-лород
до воды на конечном участке дыхательной цепи.
Ежедневно организму требуется 2,5-5,0 мг меди. При недостатке в организме
меди может развиваться болезнь - медьдефицитная анемия. Медь необходима для
усвоения железа, в частности, при синтезе цитохромоксидазы, которая содержит и
железо, и медь. При дефиците меди нарушается нормальное развитие соединительных
тканей и кровеносных сосудов.
Отравления обычно связаны со случайной передо-зировкой инсектицидов,
вдыханием порошка металла, заглатыванием растворов солей меди. Большую
опасность представляют напитки, хранящиеся в медных сосудах без защитного покрытия
стенок.
В качестве наружного средства применяют 0,25%-ный водный раствор сульфата
меди CuSO4 при воспалении слизистых оболочек и конъюнктивитах. Малые дозы этого
препарата могут применяться во время приема пищи для усиления эритропоэза при
малокровии.
В организме взрослого человека обнаруживается около 1 мг серебра, т. е.
примерно 10% (1 часть на миллион), и до 10 мг золота, т. е. примерно 10% (10
частей на миллион).
Антисептические свойства растворимых солей серебра известны с древних
времен. Священнослужители давно знали, что вода («святая») при хранении в
серебряных сосудах долго не портится, т. е. не подвергается микроб-ному
загрязнению. В настоящее время это свойство «серебряной» воды используется
моряками в дальних плаваниях. Сильные токсические проявления у взрослого
человека наблюдаются при приеме внутрь 7 г AgNO3.
В медицине издавна используются такие препараты, как кристаллический
нитрат серебра AgN03 (ляпис) и его водные растворы. Давно известны также
препараты коллоидного металлического серебра протаргол (8% Ag) и колларгол (70%
Ag), которые представляют собой мелкодисперсные порошки с металлическим
блеском. Каждая частица таких порошков представляет собой кристаллик
восстановленного металлического серебра размером менее 1 мкм с белковой оболочкой
из альбумина (протаргол) или коллагена (колларгол). Белковая оболочка защищает
кристаллики серебра от слипания и обеспечивает их переход в водную среду
(солюбилизирует).
Препараты серебра применяют как противовоспалительные, антисептические и
вяжущие средства.
В качестве эффективных противовоспалительных средств применяют также
препараты золота. Наиболее известны кризанол с 30%-ным содержанием благородного
металла, и коллоидное золото.
Металлы, особенно серебро, имеют необычные свойства, которые придают им
важное значение для промышленного применения, помимо их значения в качестве
денежной и декоративной ценности. Они являются отличными проводниками
электричества, самыми лучшими среди всех металлов. Серебро также является самым
лучшим теплопроводящим элементом и самым лучшим отражателем света, а также
имеет такое необычное свойство, как чернение, образование на его поверхности
тёмного слоя, при этом электроводность его не ухудшается.
Медь широко используется для электрических соединений в схемотехниеке.
Иногда в особо точном оборудовании электрические контакты изготавливают из
золота ввиду его высокой коррозийной стойкости. Серебро также широко
используется в критически важных случаях для изготовления электрических
контактов. Также оно используется в фотографии (потому что под действием света
из нитрата серебра происходит выпадение серебра), сельском хозяйстве, медицине,
аудиофилии и в научных приложениях.
Золото, серебро и медь являются довольно мягкими металлами, поэтому при
ежедневном использовании в качестве монет происходит быстрый выход их из строя,
драгоценные металлы легко истираются в процессе применения. Для нумизматических
функций эти металлы должны быть легированы другими металлами, чтобы повысить их
износостойкость.
Золотые монеты: золотые монеты, как правило, производятся из сплава с 90
% золота (например, монеты США до 1933 г.), или чистотой 22 карат (92 % золота,
как например, современные коллекционные монеты и крюгерранд), остальное медь и
серебро. Весовые золотые монеты содержат до 99,999 % золота (например, в
канадских монетах серии «Кленовый лист»).
Серебряные монеты: серебряные монеты содержат, как правило, 90 % серебра
(как, например, чеканились монеты США до 1965 г., которые были распространены
во многих странах), или, как в стерлинге, 92,5 % серебра, как в монетах
Британского Содружества до 1967 г. и других чеканках из серебра, остальное
составляет медь.
Медные монеты: медные монеты часто имеют весьма высокую чистоту, около 97
%, и, как правило, легированы небольшим количеством цинка и олова.
Инфляция привела к снижению номинальной стоимости монет, они уже не
являются той твёрдой валютой, которой были исторически. Это привело к тому, что
современные монеты стали делать из цветных металлов: мельхиор (медь и никель в
пропорции 80:20, черного цвета), никель-латунь (медь, никель и цинк в пропорции
75:5:20, золотистого цвета), марганец-латунь (медь, цинк, марганец и никель),
бронза, а также просто сталь с гальванопокрытием.
Список
литературы
1.Аналитическая химия. Физические и физико-химические методы
анализа./ Под ред. О.М.Петрухина. М.; 2006.
.Артеменко А.И. Органическая химия. М.; 2006.
.Ахметов Н.С. Общая и неорганическая химия. М.; 2008.
.Биологическая химия./Под ред. Ю.Б.Филипповича,
Н.И.Ковалевская, Г.А.Севастьяновой. М.; 2009.
.Биохимия / Под редакцией В.Г.Щербакова. СПб.; 2008.
.Вольхин В.В. Общая химия. Избранные главы. СПб, М,
Краснодар.; 2008.
.Вольхин В.В. Общая химия. Основной курс. СПб, М, Краснодар.;
2008.
.Гельфман М.И., Юстратов В.П. Химия. СПб, М, Краснодар.;
2008.
.Глинка Н.Л. Общая химия. М.; 2007.
.Говарикер В.Р., Васванатхан Н.В., Шридхар Дж.М. Полимеры М.;
2009.
.Гранберг И.И. Органическая химия. М.; 2007.
.Дорохова Е.Н., Прохорова К.В. Аналитическая химия.
Физико-химические методы. М.; 2006.
.Семчиков Ю.Д. Высокомолекулярные соединения. М.; 2009.
.Зимон А.Д., Лещенко Н.Ф. Коллоидная химия. М.; 2008.
.Зимон А.Д. Физическая химия. М.; 2008.
.Ипполитов Е.Г., Артемов А.В., Батраков В.В. Физическая
химия. М.; 2007.
.Ким А.М. Органическая химия. Новосибирск; 2009.
.Коржуков Н.Г. Общая и неорганическая химия. М.; 2008.
.Коровин И.В. Общая химия. М.;2009.
.Кругляков П.М.,Лещенко Н.Ф. Физическая и коллоидная химия.
М.; 2007.
.Нейланд О.Я. Органическая химия. М.; 2006.
.Никольский А.Б.,Суворов А.В. Химия. СПб.; 2007.
.Петров А.А., Бальян Х.В., Трощенко А.Т. Органическая химия.
СПб.;2008.
.Семенов И.Н., Перфилова Н.Л. Химия. СПб.; 2006.