|
Физико-химические свойства
|
Обозначение
|
Единица измерения
|
Значение
|
|
Молекулярная масса
|
М
|
-
|
53,06
|
|
Температура затвердевания
|
Тзатв
|
°С
|
-83,55
|
|
Температура кипения
|
Ткип
|
°С
|
77,3
|
|
Температура воспламенения
|
Тв
|
°С
|
2
|
|
Температура самовоспламенения
|
Тсв
|
°С
|
370
|
|
Концентрационный предел взрываемости в смеси с воздухом
|
КПВ
|
%
|
3-17
|
|
Предельно-допустимая концентрация в воздухе
|
ПДК
|
|
0,5
|
|
Плотность при 20°С
|
d204
|
г/см3
|
0,8064
|
|
Вязкость при 20°С
|
η
|
мПа-с
|
0,40
|
|
Вязкость при 60°С
|
η
|
мПа-с
|
0,25
|
|
Давление пара при 20°С
|
Рп
|
кПа
|
11,3
|
Рп
|
кПа
|
26,67
|
|
Давление пара при 80°С
|
Рп
|
кПа
|
108,7
|
|
Дипольный момент (пар)
|
μ
|
Кл∙м
|
1,29-10-29
|
|
Потенциал ионизации
|
-
|
эВ
|
10,75
|
|
Критическое давление
|
Ркрит
|
МПа
|
3,54
|
|
Критическая температура
|
Ткрит
|
°С
|
246
|
|
Теплоемкость
|
С0р
|
кДж/(кг∙К)
|
2,09±0,12
|
|
Энтальпия образования (газ)
|
ΔН0 обр
|
кДж/моль
|
-190
|
|
Энтальпия образования (жидк.)
|
ΔН0 обр
|
кДж/моль
|
-152
|
|
Энтальпия испарения (0-80°С)
|
ΔН0 исп
|
кДж/моль
|
32,6
|
|
Энтальпия сгорания
|
ΔН0сгор
|
кДж/моль
|
1,76
|
|
Энтропия (пар)
|
ΔS0
|
Дж/(моль∙К)
|
274,1
|
|
Растворимость в воде при 20°С
|
Р(Н2О)
|
%
|
7,3
|
Акрилонитрил смешивается с
большинством органических растворителей в любом соотношении, частично растворим
в воде. Образует азеотропные смеси с водой (87,5% акрилонитрила; температура
кипения 70,5°С), бензолом (47%; 73,3°С), метанолом (38,7%; 61,4°С),
четыреххлористым углеродом (21%; 66°С) и др.
Пары акрилонитрила тяжелее воздуха,
легко воспламеняются от искр и пламени и образуют с воздухом в широком
диапазоне концентраций взрывоопасную смесь. Ликвидация пожара осуществляется
спиртоустойчивой пеной, разбрызгиванием воды, двуокисью углерода.
Акрилонитрил обладает раздражающим
действием, легко всасывается через неповрежденную кожу. Токсическое действие
подобно цианидам (вызвано образованием цианида в организме). При горении
образуются ядовитые газы. Воздействие акрилонитрила вызывает у человека
раздражение глаз, покраснение и жжение кожи, головную боль, тошноту, слабость,
одышку, потливость, сердцебиение, понижение температуры тела, ослабление
пульса, судороги, потерю сознания, Тяжелое отравление может привести к асфиксии
и смерти.
Для акрилонитрила, как химического
соединения, наиболее характерны реакции по связи С=С, в том числе полимеризация
с образованием полиакрилонитрила и сополимеризация с бутадиеном, стиролом,
винилхлоридом и др. Под действием концентрированной серной кислоты акрилонитрил
превращается в акриламид (CH2=CHC(O)NH2) и акриловую кислоту (СН2=СНСООН).
Учитывая вышесказанное, хранить
акрилонитрил следует защищенным от огня, в темноте, отдельно от сильных
окислителей, оснований, пищевых продуктов и кормов, только в стабилизированном
состоянии.
1.1 Области
применения акрилонитрила
Акрилонитрил используют при
производстве карбоцепных синтетических волокон, причем основным
волокнообразующим полимером является не полиакрилонитрил, а его сополимеры,
содержащие небольшие количества (5-10%) второго мономера или двух других
мономеров. В промышленности волокно из чистого полиакрилонитрила почти не
вырабатывают ввиду его низкой эластичности, плохой окрашиваемости и
недостаточной устойчивости к истиранию.
Сополимеризацией акрилонитрила с
бутадиеном получают бутадиен-нитрильные каучуки, обладающие многими ценными
свойствами, в особенности маслостойкостью. Из полимеров акрилонитрила
вырабатывают синтетическое волокно (нитрон), а из сополимеров
акрилонитрила с хлористым винилом получают волокна, известные под названиями
виньон и дайнел. Полнакрилонитрильные волокна по объему выработки
занимают сейчас второе место после полиамидных волокон.
Кроме этого, акрилонитрил используют
в производстве акрилонитрил бутадиен стирола (АВС-пластиков), стирола
акрилонитрила (САН-пластика), бутадиен-нитрильного каучука, цианэтилцеллюлозы,
акриламида, метилакрилата, глутаминовой кислоты и адиподинитрила.
Несмотря на то, что акрилонитрил
запрещен для использования при производстве продуктов питания, его продолжают
применять в качестве ядохимиката при выращивании зерновых, фруктов, табака; в
качестве "точечного инсектицида" на мельницах и в хлебопекарнях для
уничтожения насекомых в муке.
Акрилонитрил применяется для
обработки хлопкового волокна придавая ему прочность и стойкость против гниения.
Он используется для производства пластических масс, пластификаторов, клеев.
Сополимеризацией стирола и акрилонитрила получают ударопрочный полистирол.
При омылении акрилонитрила водным
раствором серной кислоты образуется соль акриламида.
Поскольку акрилонитрил является
одним из важнейших мономеров, используемых в химической промышленности, то он
производится в больших объемах.
1.2 Основные виды
сырья для получения акрилонитрила
Поскольку в промышленности для
получения акрилонитрила используется метод окислительного аммонолиза пропилена,
то основными видами сырья соответственно являются пропилен и аммиак.
Пропилен (пропен) CH2=CHCH3 - бесцветный газ со
слабым запахом. Основным источником пропилена является пиролиз (процесс
глубокого расщепления углеводородного сырья под действием высоких температур).
Готовый продукт должен соответствовать ГОСТу 25043-87, согласно которому
объемная доля пропилена должна составлять не менее 99,8% в продукте высшего
сорта и 99,0% - первого сорта. Кроме того, ГОСТ предусматривает отсутствие в
продукте свободной воды.
Пропилен транспортируется по
трубопроводу и в предназначенных для сжиженных газов железнодорожных и
автомобильных цистернах. Баллоны с пропиленом перевозят железнодорожным и
автомобильным транспортом в крытых транспортных средствах. Транспортировку
производят в соответствии с правилами перевозки опасных грузов, действующими на
данном виде транспорта.
Для синтеза акрилонитрила методом
окислительного аммонолиза пропилена применяется 90-92%-ный пропилен, который не
должен содержать сернистых соединений, отравляющих катализатор, а также метан и
непредельные углеводороды (поскольку метан способствует образованию синильной
кислоты, олефины образуют другие нитрилы).
Аммиак по химическому составу
отвечает формуле NH3. В обычных условиях
представляет собой бесцветный газ с резким запахом.
Транспортировка аммиака производится
аналогично транспортировке пропилена.
Исходная смесь для получения
акрилонитрила содержит 5-8% C3H6, 5-9% NH3, 0-30% водяного пара (остальное - воздух).
2. Технологическая часть
.1 Физико-химические
основы процесса производства нитрила акриловой кислоты
Катализаторы окислительного
аммонолиза пропилена подобны применяемым при окислении пропилена в акролеин.
Первоначальные разработки основывались на молибдате висмута (Вi2О3:
МоО3 = 1: 2), к которому затем добавили промотор - P2O5
(висмут-фосфор-молибденовые катализаторы). Хорошие результаты дают также
ванадий-молибдаты висмута, оксидный уран-сурьмяный катализатор и др. Имеются и
более многокомпонентные катализаторы с добавками оксидов Со, Ni, Fe, As, W, Те
и других металлов и редкоземельных элементов. Эти катализаторы используют в
чистом виде или нанесенными на SiO2, Аl2О3 и
кизельгур.
Все эти катализаторы работают по
окислительно-восстановительному механизму, и скорость реакции зависит только от
парциального давления пропилена, что свидетельствует о лимитирующей стадии
взаимодействия пропилена с окисленным активным центром катализатора, где
образуется хемосорбированный алкильный радикал. В свою очередь, на другом
активном центре сорбируется аммиак, вероятно, в виде аминного радикала:NH.
Взаимодействие их друг с другом с участием кислорода решетки и дает
акрилонитрил.
Побочными продуктами окислительного
аммонолиза пропилена являются HCN, СН3СN, небольшие количества НСНО
и СН3СНО (образуются за счет окислительной деструкции пропилена), а
также СО2 (в основном образуется за счет окисления пропилена).
Доказано, что альдегиды и нитрилы получаются главным образом параллельно.
Метод получения акрилонитрила
совместным окислением пропилена и аммиака кислородом воздуха разработан фирмой
«Sohio» и реализован в 1960 г. в США. По технологии этой фирмы работают заводы
в Японии, Германии, Англии, Франции, Италии и других странах. Некоторые фирмы -
«Bayer», «SNAM Progetti», «Distillers», «Ugine» - разработали собственную
технологию в присутствии новых модификаций стационарных катализаторов.
Процесс окислительного аммонолиза
пропилена вначале проводили в трубчатых реакторах со стационарным слоем
катализатора, но теперь используют аппараты с псевдоожиженным слоем. Это
позволило лучше регулировать температуру, сняло ограничения по взрывоопасности
исходной смеси и исключило необходимость разбавления ее водяным паром.
Окисление ведут воздухом, поддерживая объемное отношение С3Н6:
NH3: О2 в пределах 1: (0,9-1,1): (1,8-2,4). Важно, чтобы
в отходящей из реактора смеси находился непревращенный аммиак, т.к. в противном
случае растет выход альдегидов и СО2. Необходим и некоторый избыток
кислорода, который вместе с пропиленом и аммиаком обеспечивает
окислительно-восстановительные свойства среды, благоприятные для повышения
активности и селективности катализатора.
На разных установках и катализаторах
процесс окислительного аммонолиза пропилена осуществляют при 370-500°С и
0,2-1,4 МПа, большей частью при 420-470°С и давлении 0,2 МПа. Время контакта 6
с обеспечивает степень конверсии пропилена до 80% (в одном из новых процессов
даже 95%). При этом пропиленовая фракция может содержать 5-40% пропана, что
снижает ее стоимость. Селективность процесса по акрилонитрилу при описанных
условиях составляет 80-85%, причем побочно образующиеся синильная кислота и
ацетонитрил выпускают как товарные продукты, что снижает себестоимость
акрилонитрила. На разных установках выход HCN и ацетонитрила составляет
соответственно 50-200 и 25-100 кг на 1 т акрилонитрила; на 1 т акрилонитрила
расходуется 0,96 т пропилена.
В новейших схемах производства
акрилонитрила реализована эффективная система утилизации тепла с получением
пара (высокого и среднего давления), обеспечивающего все потребности самой
установки (привод компрессора для воздуха, разделение смесей и др.).
2.2 Технологическая
схема получения акрилонитрила
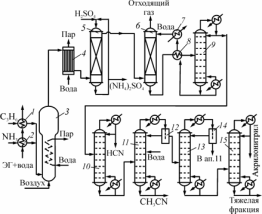
1, 2 - испарители; 3 - реактор; 4 - котел-утилизатор;
5, 6 - абсорберы;
7 - холодильник; 8 - теплообменник; 9 - отпарная
колонна;
10, 15 - ректификационные колонны; 11 - колонна
экстрактивной дистилляции; 12, 14 - сепараторы; 13 -
колонна азеотропной сушки
Рисунок 1 - Технологическая схема
получения акрилонитрила
Жидкие аммиак и пропиленовую фракцию
испаряют в аппаратах 1 и 2 при помощи смеси этиленгликоля (ЭГ) с
водой; смесь при этом охлаждается до низких температур, а ее холод
утилизируется (в том числе для конденсации синильной кислоты). Газообразные
аммиак, пропиленовая фракция и воздух в ранее рассмотренных соотношениях
поступают в реактор 3 с псевдоожиженным слоем катализатора. Реактор
охлаждается кипящим водным конденсатом. За счет реакционного тепла генерируется
пар высокого давления, который служит для привода воздушного турбокомпрессора,
а выходящий из компрессора «мятый» пар используется на стадии разделения
продуктов. Горячие газы по выходе из реактора проходят котел-утилизатор 4,
где генерируется пар среднего давления. Частично охлажденные реакционные газы
прежде всего очищают от аммиака в абсорбере 5 с помощью циркулирующего
раствора сульфата аммония, содержащего серную кислоту. Отработанный в абсорбере
раствор сульфата аммония выпаривают и кристаллизуют, получая 400 кг (NH4)2SO4
на 1 т акрилонитрила. Далее из газа в абсорбере 6 водой поглощают
акрилонитрил, синильную кислоту и ацетонитрил, а отходящий газ, в зависимости
от состава, сбрасывают в атмосферу или дожигают в печи с получением пара.
Водный раствор продуктов с низа
абсорбера 6 подогревают в теплообменнике 8 оборотной водой и
подают в отпарную колонну 9 с кипятильником и дефлегматором, где от воды
отгоняют синильную кислоту, акрилонитрил и ацетонитрил. Воду через
теплообменник 8 и холодильник 7 возвращают в абсорбер 6, а
смесь продуктов направляют на разделение.
Обычно из смеси в первую очередь
отгоняют наиболее летучую синильную кислоту в ректификационной колонне 10 с
кипятильником и дефлегматором при небольшом вакууме (чтобы избежать попадания
высокотоксичной HCN в атмосферу). Из кубовой жидкости в колонне 11 с
водой в качестве третьего компонента отгоняют более летучую азеотропную смесь
акрилонитрила, оставляя в кубе водный раствор ацетонитрила с примесью менее
летучих соединений (циангидрины формальдегида и ацетальдегида, образовавшиеся
из этих альдегидов и HCN). Из раствора затем выделяют ацетонитрил (на схеме не показано).
Дистиллят разделяют в сепараторе 12 на водный и органический слои,
возвращая воду в колонну 11.
Водный акрилонитрил подвергают
азеотропной осушке в колонне 13, снабженной кипятильником, дефлегматором
и сепаратором 14, где разделяются водный и акрилонитрильный слои. Первый
возвращают в колонну 11, т.к. он содержит растворенный акрилонитрил, а
второй служит орошением колонны 13. Сухой акрилонитрил собирают в кубе
колонны 13 и после окончательной ректификации в колонне 15 получают
в виде дистиллята нужной чистоты. На стадии разделения продуктов во избежание
полимеризации акрилонитрила к смеси добавляют ингибиторы.
В стационарном слое катализатора
процесс ведут в реакторах трубчатого типа, в которых катализатор находится в
трубах, а межтрубное пространство заполнено высокотемпературным теплоносителем
- нитрит-нитратной смесью. Стационарный слой катализатора должен быть очень
прочным и термостойким, способным проработать несколько тысяч часов без
заметного пыления, чтобы предотвратить рост сопротивления потоку газа в
трубках.
При синтезе акрилонитрила выделяется
большое количество тепла. Поэтому, во избежание сильных перегревов, диаметр
трубки реактора не должен превышать 32 мм. В связи с этим при использовании
реактора трубчатого типа достичь большой мощности единичного аппарата не
удается.
В реакторах с псевдоожиженным слоем
катализатора этот недостаток устраняется. Выделяющееся в процессе синтеза тепло
отводится за счет испарения воды в змеевиках, расположенных в зоне реакции.
Основным недостатком реакторов этого типа является истирание катализатора и
унос мелких частиц его потоком газа, что приводит к потере дорогостоящих
молибденовых и висмутовых солей и ухудшению экономических показателей процесса.
Широкое применение получили реакторы
с кипящим слоем катализатора, в которых можно обеспечить изотермичность
процесса и наиболее рациональный отвод теплоты.
Наряду с основной, сильно
экзотермичной реакцией (ΔН = -515 кДж/моль), происходит образование HCN, ацетонитрила (CH3CN), CO и CО2. Для уменьшения образования
таких побочных продуктов, как акролеин, ацетальдегид и ацетон, затрудняющих
очистку акрилонитрила, аммиак обычно подают в небольшом избытке.
Выход акрилонитрила составляет
75-80% по пропилену.
2.3 Расчет материального
баланса
В процессе протекают следующие
реакции:
основная
СН3-СН=СН2 + NH3 + 1,5О2 "СН2=СН-CN + 3H2O, (1)
побочные
СН3-СН=СН2 + NH3 + 2,5О2 "СН3CN + СО2 + 3H2О, (2)
СН3-СН=СН2 + NH3 + 2О2 "НCN + СО2 + СН4 + 3H2O. (3)
Часовая производительность по
акрилонитрилу с учетом потерь составляет:
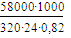 =
9209,86 кг/ч.
=
9209,86 кг/ч.
Расход пропилена
по реакции (1) 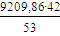 = 7298,38 кг/ч;
= 7298,38 кг/ч;
по реакции (2)  = 1317,76 кг/ч;
= 1317,76 кг/ч;
по реакции (3) 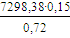 =1520,50 кг/ч;
=1520,50 кг/ч;
Суммарный расход пропилена по
реакциям
,38+1317,76+1520,50 = 10136,64 кг/ч;
Расход технического пропилена с
учетом степени конверсии
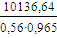 =
18757,66 кг/ч,
=
18757,66 кг/ч,
В том числе
пропилена  кг/ч,
кг/ч,
пропана 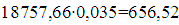 кг/ч;
кг/ч;
Расход аммиака на все реакции
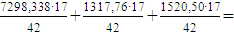 4102,93
кг/ч;
4102,93
кг/ч;
Расход технического аммиака
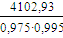 =
4229,28 кг/ч,
=
4229,28 кг/ч,
в том числе:
аммиака 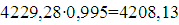 кг/ч,
кг/ч,
примесей 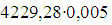 = 21,15 кг/ч;
= 21,15 кг/ч;
Расход кислорода на все реакции
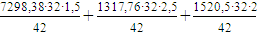 =
13167,98 кг/ч,
=
13167,98 кг/ч,
Или 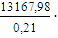 22,4 = 9217,59 м3/ч;
22,4 = 9217,59 м3/ч;
Расход воздуха
 =
73893,29 м3/ч,
=
73893,29 м3/ч,
или
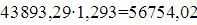 кг/ч;
кг/ч;
в том числе
азота 43586,04 кг/ч,
кислорода 13167,98 кг/ч;
Рассчитывают массовое количество
образовавшихся продуктов:
Вода по реакции (1) 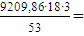 9383,63 кг/ч,
9383,63 кг/ч,
Ацетонитрил по реакции (2)  1286,38 кг/ч,
1286,38 кг/ч,
Диоксид углерода по реакции (2)  1380,51 кг/ч,
1380,51 кг/ч,
Вода по реакции (2) 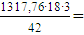 1694,26 кг/ч,
1694,26 кг/ч,
Синильная кислота по реакции (3) 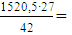 977,46 кг/ч,
977,46 кг/ч,
Вода по реакции (3) 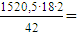 1303,29 кг/ч,
1303,29 кг/ч,
Метан по реакции (3) 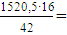 579,24 кг/ч.
579,24 кг/ч.
Материальный баланс производства
нитрила акриловой кислоты окислительным аммонолизом пропилена приведен в
таблице 2.
Таблица 2 - Материальный баланс
производства нитрила акриловой кислоты
|
Подается
|
кг/ч
|
Образуется
|
кг/ч
|
|
Пропиленовая фракция: пропан пропилен
|
18757,66 656,52
18101,14
|
Нитрил акриловой кислоты
|
9209,86
|
|
|
Ацетонитрил
|
1286,38
|
|
|
Синильная кислота
|
977,46
|
|
Аммиак технический: аммиак примеси
|
4229,28 4208,13
21,15
|
Вода
|
12381,18
|
|
|
Пропилен
|
7964,5
|
|
|
Пропан
|
656,52
|
|
Воздух: кислород азот
|
56754,02 13167,98
43586,04
|
Аммиак
|
105,20
|
|
|
Примеси в аммиаке
|
21,15
|
|
|
Азот
|
43586,04
|
|
|
Метан
|
579,24
|
|
|
Диоксид углерода
|
2973,41
|
|
Всего
|
79740,96
|
Всего
|
79740,96
|
2.4 Расчет теплового
баланса
Уравнение теплового баланса
Ф0+Ф1+Ф2+Ф3=Ф4+Ф5+Ф6+Ф7+Ф8+Фпот+Фотв,
где Ф0 -теплота реакций,
Ф1 - пропан-пропиленовая
фракция,
Ф2 - аммиак,
Ф3 - кислород,
Ф4 - остаток фракции,
Ф5 - не прореагировавший
аммиак,
Ф6 - акрилонитрил,
Ф7 - ацетонитрил,
Ф8 - синильная кислота,
Фпот - теплопотери,
Фотв - отводимая теплота.
Здесь Ф0, Ф1,
Ф2, Ф3 - входящие тепловые потоки (Фприх); Ф4,
Ф5,Ф6, Ф7, Ф8, Фпот, Фотв
- отводимые тепловые потоки.
Температура процесса 723 К.
Уравнение теплового потока
Ф = 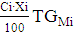 ,
,
где Ci - удельная
теплоемкость, Дж/(моль▪К);
Xi - содержание компонента, масс.д.,%;
GMi - молярный расход, кмоль/с:
G =  ,
,
где Р - расход, кг/ч;
М - молекулярная масса.
Удельные теплоемкости:
Спропилен = 63,89
Дж/(моль∙К);
Спропан = 73,51 Дж/(моль∙К);
Саммиак = 35,65 Дж/(моль∙К);
Скислород = 29,37
Дж/(моль∙К);
Сакрилонитрил = 72,398
Дж/(моль∙К);
СHCN = 35,864 Дж/(моль∙К);
Приход теплоты:
- приход теплоты с
пропилен-пропановой фракцией:
Мфр= Σ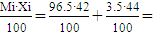 42.07
42.07
Gфр = 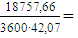 0,124 кмоль/с
0,124 кмоль/с
Ф1=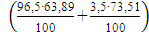 ∙723∙0,124 = 5757,71 кВт
∙723∙0,124 = 5757,71 кВт
- приход теплоты с
аммиаком
G =  0,0688
кмоль/с
0,0688
кмоль/с
Ф2 = 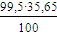 ∙723∙0,0688 = 1764,46 кВт
∙723∙0,0688 = 1764,46 кВт
- приход теплоты с
кислородом
G = 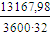 =
0,1143 кмоль/с
=
0,1143 кмоль/с
Ф3 = 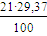 ∙723∙0,1143 = 509,7 кВт
∙723∙0,1143 = 509,7 кВт
- приход теплоты
вместе с химическими реакциями
ΔН0298
= ΣΔН0298(прод)-ΣΔН0298(исх)
По реакции (1)
ΔН0298
= (184,9-725,475)-(20,414-46,19)= -514,799 кДж/моль
По реакции (2)
ΔН0298
= (87,9-393,511-725,475)-(20,414-46,19)= -1005,31 кДж/моль
По реакции(3)
ΔН0298
= (1134,7-393,511-743847-483,65)-(20,414-46,19) =
= -791,532 кДж/моль
Ф0 = 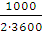 = (5143799∙173,77+1005,31∙31,375+791,535∙36,2) =
= (5143799∙173,77+1005,31∙31,375+791,535∙36,2) =
=20785,23 кВт
- общий приход
теплоты
Фприх = Ф0+Ф1+Ф2+Ф3=20785,23+5620,93+1764,46+509,7=28680,32
кВт
Отводимая теплота
- потри теплоты в
окружающую среду
Фпот = 0,05Фприх=
0,05∙28680,32 = 1434,02 кВт
- теплота отводимая с
остатком фракции
G’фр = 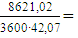 0,057
кмоль/с
0,057
кмоль/с
Ф4 = 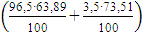 ∙723∙0,057 = 2646,57 кВт
∙723∙0,057 = 2646,57 кВт
- теплота отводимая с
остатком аммиака
G = 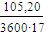 =
0,0017 кмоль/с
=
0,0017 кмоль/с
Ф5 = 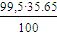 ∙723∙0,0017 = 43,60 кВт
∙723∙0,0017 = 43,60 кВт
- теплота, отводимая
с целевым продуктом - акрилонитрилом
G = 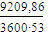 = 0,048
кмоль/с
= 0,048
кмоль/с
Ф5 =  ∙723∙0,048 = 2016,78 кВт
∙723∙0,048 = 2016,78 кВт
- теплота отводимая с
побочным продуктом - ацетонитрилом
G = 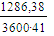 =
0,0087 кмоль/с
=
0,0087 кмоль/с
Ф5 = 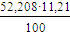 ∙723∙0,0087 = 36,81 кВт
∙723∙0,0087 = 36,81 кВт
- теплота отводимая с
побочным продуктом - синильной кислотой
G = 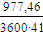 = 0,01
кмоль/с
= 0,01
кмоль/с
Ф5 =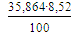 ∙723∙0,01 = 22,09 кВт.
∙723∙0,01 = 22,09 кВт.
Тепловой баланс представлен в
таблице 3.
Таблица 3 - Тепловой баланс
производства нитрила акриловой кислоты
|
Приход
|
кВт
|
%
|
Отвод
|
кВт
|
%
|
|
Ф0-теплота реакций;
|
20785,23
|
72,13
|
Ф4 - остаток фракции
|
2646,57
|
9,18
|
|
Ф1-пропан-пропиленовая фракция
|
5757,71
|
19,98
|
Ф5 - не прореагировавший аммиак
|
43,60
|
0,15
|
|
Ф2 - аммиак
|
1764,46
|
6,12
|
Ф6 - акрилонитрил
|
2016,78
|
7,00
|
509,7
|
1,77
|
Ф7 - ацетонитрил
|
36,81
|
0,13
|
|
|
|
Ф8 - синильная кислота
|
22,09
|
0,08
|
|
|
|
Фпот - теплопотери
|
1434,02
|
4,98
|
|
|
|
Фотв - отводимая теплота
|
22587,12
|
78,48
|
|
Всего
|
28817,10
|
100
|
Всего
|
28817,10
|
100
|
2.5 Расчет реактора
Насыпная плотность катализатора ρнас = 2500 кг/м3, плотность частиц ρ=4700 кг/м3,
Эквивалентный диаметр частиц dэ=1 мм. Температура воздуха
450 0С. Число псевдоожижения Кω=1.6. Производительность
катализатора 10500 т/ч, при среднем времени пребывания его в реакторе τ0=480 мин. Расход воздуха в рабочих условиях 73893,29 м3/ч.
Живое сечение решетки 0,015, диаметр отверстий 0,8 мм, толщина решетки 2 мм.
Динамический коэффициент вязкости
воздуха при 450 0С: μ=0,034∙10-3 Па∙с.
Плотность воздуха
ρ =
1,293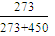 = 0,488 кг/м3;
= 0,488 кг/м3;
следовательно,
Ar = 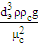 =
=  = 1,946∙
= 1,946∙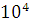 ;
;
Значению Ar=1,946∙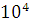 соответствует Lyкр=4∙
соответствует Lyкр=4∙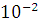 . Отсюда
. Отсюда
ωкр =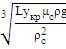 =
=  =
0,505 м/с;
=
0,505 м/с;
Определяем рабочую скорость воздуха:
ω = Кω∙ωкр=1,6∙0,505=0,808 м/с;
Найдем порозность взвешенного слоя.
При Кω=1,6
Ly = 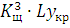 =1,63∙0,04=0,16;
=1,63∙0,04=0,16;
По приложению при Ly=1,6∙10-1
и Ar=1,946∙104
имеем ε=0,47.
Действительная скорость воздуха в
свободном сечении слоя:
ωд =  =
= 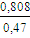 =
1,719 м/с;
=
1,719 м/с;
Секундный расход воздуха:
V =  =
20,526 м3/с;
=
20,526 м3/с;
Площадь сечения аппарата:
S =  =
=  = 25,403 м2;
= 25,403 м2;
Диаметр реактора:
D =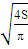 =
=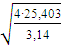 = 5,689 м;
= 5,689 м;
Определяем высоту слоя в реакторе.
Масса катализатора в реакторе:
М=L∙τ0=10500∙480/60=84000 кг;
Объем неподвижного слоя
катализатора:
Vk = M/ρнас = 84000/2500 = 32,6 м2;
Высота неподвижного слоя:
h0 = Vk/S = 32,6/25,403 = 1,323 м;
Порозность неподвижного слоя:
ε0 = 1- 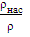 = 1-
= 1-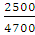 =
0,47;
=
0,47;
Высота взвешенного слоя при Кω=1,6:
h = 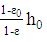 =
=  1,323 = 1.323 м;
1,323 = 1.323 м;
Общая высота реактора:
Н = 5h = 5∙1.323=6,615 м;
Рассчитаем гидравлическое сопротивление
реактора. Сопротивление слоя:
Δрсл
= ρ(1-ε0)gh0 = 4700(1-0,47)9,81∙1,323
= 32400 Па;
Скорость воздуха в отверстиях
решетки при живом сечении φ=0,015:
ω0 = ω/φ = 0,808/0,015 = 53,87 м/с;
Диаметр отверстий решетки d0= 0,0008 м, толщина решетки δ=0,002 м. При d0/δ=0.4 по приложению находим С=0,63.
Сопротивление решетки:
Δрреш
= 0,503ω02ρс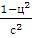 = 0,503∙53,872∙0,488∙
= 0,503∙53,872∙0,488∙ 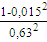 = 1800 Па;
= 1800 Па;
Сопротивление реактора:
Δр=Δрсл+Δрреш=32400+1800=34200
Па.
3. Экологическая часть
.1 Источники поступления
Природных источников акрилонитрила не
существует. Акрилонитрил используется в производстве искусственных волокон,
полимеров и резины, а также в промышленности органического синтеза. Может
поступать в окружающую среду при производстве, переработке, использовании,
хранении, транспортировке и захоронении отходов. Кроме непосредственных эмиссий
в атмосферу при производстве и промышленном использовании, возможны потери
вследствие аварий, сбоях в работе оборудования и несоблюдении технологии и
правил работы.
Атмосфера. Распределение
акрилонитрила в атмосфере тесно связано с розой ветров; самые высокие
концентрации обнаруживаются в непосредственной близости от заводов (до
нескольких сотен мг/м3), особенно с подветренной стороны, и быстро
убывают с расстоянием (менее 10 мкг/м3 на расстоянии 1 км). Процессы
разложения акрилонитрила в атмосфере преимущественно химические; время
полуразложения в атмосфере 9-32 ч. По оценкам, среднее содержание в воздухе
Нидерландов около 0,01 мкг/м3, что ниже предела обнаружения для
существующих методов определения акрилонитрила (0,3 мкг/м3). В
других странах эта концентрация еще более низкая.
Вода. Поступление с осадками
незначительно. Время полуразложения в воде 5-7 дней, однако аварийное
поступление акрилонитрила в грунтовые воды может повлечь за собой многолетнее
их загрязнение, несмотря на принимаемые меры по очистке.
Почва. Разлагается преимущественно
микроорганизмами.
3.2 Обезвреживание
отходящих газов в производстве акрилонитрила
реактор акрилонитрил
высокополимерный кислота
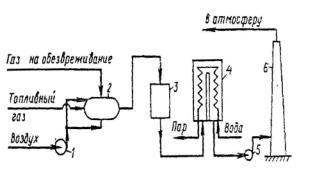
- воздуходувка; 2 -
топка-подогреватель; 3 - реактор;
- котел-утилизатор; 5 - дымосос; 6 -
труба
Рисунок 2 - Схема установки
каталитического обезвреживания отходящих газов производства акрилонитрила
При синтезе акрилонитрила на основе
аммиака и пропилена технологические газы отмываются от нее водой. Поступающие
со стадии адсорбции отходящие газы содержат (об.%): СО - 2,3; пропилена - 0,5;
пропан - 0,04; О2 - до 3; инертные газы - остальное.
Для очистки их подают в
топку-подогреватель 2 где нагревается до температуры 200 - 250 0С в
зависимости от типа используемого катализатора. Путем сжигания вводимого в
топку топливного газа в воздухе нагнетаемом воздуходувкой 1. Расход воздуха
рассчитывается не только на сжигание топливного газа, но и на последующее
каталитическое окисление находящихся в газах оксида углерода и углеводородов.
Смесь топочных и отходящих газов с воздухом направляется в работающий в
адиабатических условиях реактор 3. Используемый шариковый катализатор (ШПК - 2)
содержит 0,2% платины нанесенной на оксид алюминия. Степень очистки достигает
98 - 99%. Происходящие на катализаторе окислительные реакции экзотермичны, что
приводит к сильному разогреву продуктов катализа. Конвертированные газы при
температуре 400 0С передаются в котел - утилизатор 4, обеспечивающий
производство перегретого пара до 380 0С водяного пара под давлением
4 МПа. Выходящие из котла-утилизатора 4 обезвреженные газы при 200 0С
дымососом 5 через дымовую трубу 6 выбрасываются в атмосферу.
При обезвреживании 60 тыс. м3/ч
отходящих газов расход электроэнергии составляет 500 кВ и производительность
пара 26,5 т/ч.
Пути поступления в организм.
Основное значение поступление акрилонитрила с воздухом имеет на производстве,
при этом дополнительная доза, получаемая при проживании в непосредственной
близости от соответствующих предприятий является несущественной. В
непроизводственных условиях значительным источником поступления акрилонитрила
является курение. Данных по содержанию акрилонитрила в питьевой воде нет, но,
поскольку основным источником его поступления в воду являются аварии, питьевая
вода вряд ли может рассматриваться как серьезный источник поступления
акрилонитрила в организм. В пищевые продукты (особенно масло, маргарин)
акрилонитрил может поступать из полимерных контейнеров и упаковочных
материалов, состоящих из сополимеров акрилонитрила. Легко всасывается через
неповрежденную кожу.
Острое отравление. Запах
акрилонитрила ощущается при 0,008-0,04 мг/дм3, но к нему быстро
наступает привыкание. Вдыхание 0,3-0,5 мг/дм3 в течение 5-10 мин
вызывает жжение слизистых верхних дыхательных путей и слезотечение. При
концентрациях 0,035-0,22 мг/дм3 в течение 20-45 мин - тупая головная
боль, стеснение в груди, возбуждение и чувство страха, кожный зуд.
Превращения в организме и выделение.
Абсорбция в дыхательных путях человека независимо от экспозиции составила
48%. Гидролиз с отщеплением CN- протекает в печени под
влиянием фермента роданезы с образованием роданидов. Частично акрилонитрил
выделяется с выдыхаемым воздухом в неизмененном виде.
Предельно допустимая концентрация
0,5 мг/м3.
Заключение
Был рассмотрен процесс получения
акрилонитрила окислительным аммонолизом пропилена. Другие методы получения
акрилонитрила в значительной степени утратили свое былое значение, т.к. при их
использовании не достигается нужный выход акрилонитрила, следовательно они
экономически менее целесообразны.
Поскольку в промышленности для
получения акрилонитрила используется метод окислительного аммонолиза пропилена,
то основными видами сырья соответственно являются пропилен и аммиак.
Были рассчитаны материальный баланс,
который показал высокую степень конверсии исходных продуктов; тепловой баланс,
который показал, что процесс протекает с большим выделением тепла, которое
обеспечивает все потребности самой установки (привод компрессора для воздуха,
разделение смесей и др.). Были рассчитаны основные показатели реактора получения
акрилонитрила.
Список использованных
источников
1. Филимонова, О.Н. Технологические расчеты производственных
процессов [Текст]: учеб. пособие / О.Н. Филимонова, М.В. Енютина. - Воронеж.
гос. технол. акад., - Воронеж, 2005. - 120 с.
2. Родионов, А.И. Техника защиты окружающей среды [Текст]:
учебник для вузов / А.И. Родионов, В.Н. Клушин, Н.С. Торочешников. - 2-е изд.,
перераб. и доп. - М.: Химия, 1989. - 512 с.
. Павлов, К.Ф., Романков, П.Г., Носков А.А. Примеры и
задачи по курсу процессов и аппаратов химической технологии [Текст]: учебное
пособие для вузов; под ред. Чл.-корр. АН СССР П.Г. Романкова. - 10-е изд.,
перераб. и доп. - Л.: Химия, 1987. - 576 с., ил.
. Расчеты аппаратов кипящего слоя: Справочник [Текст]; под
ред. И.П. Мухленова, Б.С. Сажина, В.Ф. Фролова. - Л.: Химия, 1986. - 352 с.
. Справочник нефтехимика. В 2 т. Т. 2; под ред. С.К.
Огородникова. - Л.: Химия, 1978. - 592 с., ил.
. Справочник химика Т.1; под ред. Б.Н. Никольский. - Л.:
Химия, 1966. - 1072 с.
. Справочник химика Т.2; под ред. Б.Н. Никольский. - Л.:
Химия, 1971. - 1168 с.
. Вредные вещества в промышленности. Справочник для
химиков, инженеров и врачей. [Текст]: под ред. засл. деят. науки проф. Н.В.
Лазарева и док. мед. наук Э.Н. Левиной.изд. - 7-е, пер. и доп. В трех томах. Т.2;
- Л.: Химия, 1979. - 624 с.