Определение молярной массы эквивалента металла методом вытеснения водорода
МИНОБРНАУКИ
РОССИИ
Федеральное
государственное бюджетное образовательное учреждение
высшего
профессионального образования
«Ижевский
государственный технический университет имени М.Т. Калашникова»
Кафедра
«Химия и химическая технология»
Факультет
«РиД»
Лабораторная
работа №1
Тема:
«Определение молярной массы эквивалента металла методом вытеснения водорода »
Выполнил:
студент гр. Б01-131-1 Федорова
С.Н.
Проверил:
к.т.н., доцент Кибенко
В.Д.
Ижевск,
2014
Цель работы
Экспериментальным путем по реакции металла с
кислотой определить малярную массу эквивалента металла оценить погрешность
опыта
Теоретическая часть
. Эквивалент - условная или реальная частица
вещества, которая может присоединять, замещать или быть каким-либо другим образом
равнозначной одному атому или иону водорода в кислотно-основных или
ионно-обменных реакциях или одному электрону в окислительно-восстановительных
реакциях.
. Молярная масса эквивалента вещества - масса
одного моля эквивалента вещества.
М( )=
)=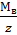 =f*
=f*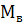 [г/моль]
[г/моль]
где z-число эквивалентности, а 1/z-фактор
эквивалентности (число, обозначающее какая доля от реальной частицы
эквивалентна одному атому водорода).

Экспериментальная часть
Реакция, на которой
основан эксперимент
Al+6HCl=2AlCl3+3H2
Схема установки:
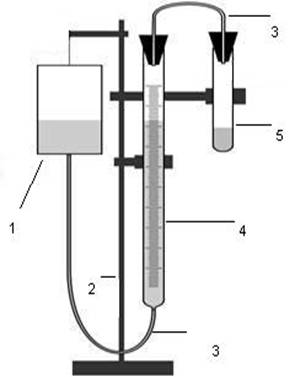
-сосуд с водой; 2-штатив; 3-соединительные
трубки; 4-бюретка на 50 мл; 5-пробирка
Порядок выполнения
опыта
реакция погрешность опыт металл
1. Проверил установку на герметичность;
. Установили уровень воды в бюретке на 0
отрезке;
. Залили в пробирку HCl;
. Всыпали в кислоту порошок метала;
. Закрыть пробирку пробкой с газоотводной
трубкой;
. По окончанию записали объем
выделившегося водорода по показаниям газоизмерительной бюретке.
Экспериментальные
данные
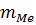 =0,0189 г
=0,0189 г
V(H2)=20,0
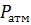 =
=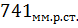 =
=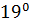 C=
C=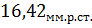
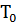 =273°K
=273°K
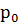 =760 мм рт. Ст
=760 мм рт. Ст
р=724.53 мм рт. ст.
V(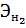 )=11200
мл/моль
)=11200
мл/моль
Вычисления
. Приводим объем выделившегося водорода к
нормальным условиям, используя уравнение состояния газа:

.По закону эквивалентов:
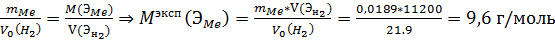
Вычисление ошибки
. ∆абс=|M(Э(Ме))тер
- М(Э(He)экв|= 0,66
M(Э(Me)тер
= 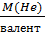 =
=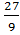 = 9 г\моль
= 9 г\моль
. ∆отр =  •
100% = 7,3%
•
100% = 7,3%
Вывод
Проводя опыт, я экспериментальным путем по
реакции металла с кислотой определила малярную массу эквивалента металла и
оценила погрешность опыта.
.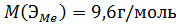
.