Марганец и хром. Биологическая роль, нормы потребления. Пищевые источники микроэлементов
Педиатрический факультет
Кафедра общей и биоорганической химии
- теоретическая
Реферат на тему:
«Марганец и хром. Биологическая роль,
нормы потребления. Пищевые источники микроэлементов»
Содержание
Глава 1. Общая характеристика марганца и хрома
.1 История открытия марганца, общие сведения
.2 Получение марганца
.3 Химические свойства марганца и его соединений
.4 История открытия хрома, общие сведения
.5 Получение хрома
.6 Химические свойства хрома и его соединений
Глава 2. Биологическая роль марганца и хрома
Глава 3. Нормы потребления марганца и хрома
.1 Нормы потребления марганца, недостаток и переизбыток
микроэлемента
.2 Нормы потребления хрома, недостаток и переизбыток
микроэлемента
Глава 4. Пищевые источники микроэлементов
.1 Пищевые источники марганца
.2 Пищевые источники хрома
Список литературы
Глава 1. Общая характеристика марганца и хрома
.1 История открытия марганца, общие сведения
Один
из основных минералов марганца - пиролюзит
<https://ru.wikipedia.org/wiki/%D0%9F%D0%B8%D1%80%D0%BE%D0%BB%D1%8E%D0%B7%D0%B8%D1%82>
- был известен в древности как чёрная магнезия и использовался при варке стекла
для его осветления. Его считали разновидностью магнитного железняка
<https://ru.wikipedia.org/wiki/%D0%9C%D0%B0%D0%B3%D0%BD%D0%B5%D1%82%D0%B8%D1%82>,
а тот факт, что он не притягивается магнитом
<https://ru.wikipedia.org/wiki/%D0%9C%D0%B0%D0%B3%D0%BD%D0%B8%D1%82>,
Плиний Старший
<https://ru.wikipedia.org/wiki/%D0%9F%D0%BB%D0%B8%D0%BD%D0%B8%D0%B9_%D0%A1%D1%82%D0%B0%D1%80%D1%88%D0%B8%D0%B9>
объяснил женским полом чёрной магнезии, к которому магнит «равнодушен». В 1774
г. шведский химик К. Шееле
<https://ru.wikipedia.org/wiki/%D0%A8%D0%B5%D0%B5%D0%BB%D0%B5,_%D0%9A%D0%B0%D1%80%D0%BB_%D0%92%D0%B8%D0%BB%D1%8C%D0%B3%D0%B5%D0%BB%D1%8C%D0%BC>
показал, что в руде содержится неизвестный металл. Он послал образцы руды
своему другу химику Ю. Гану
<https://ru.wikipedia.org/wiki/%D0%93%D0%B0%D0%BD,_%D0%AE%D1%85%D0%B0%D0%BD_%D0%93%D0%BE%D1%82%D0%BB%D0%B8%D0%B1>,
который, нагревая в печке пиролюзит с углем, получил металлический марганец. В
начале XIX века для него было принято название «манганум» (от немецкого
Manganerz - марганцевая руда).
Ма́рганец - элемент
<https://ru.wikipedia.org/wiki/%D0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9_%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82>
побочной подгруппы седьмой группы четвёртого периодапериодической системы
химических элементов <https://ru.wikipedia.org/wiki/%D0%9F%D0%B5%D1%80%D0%B8%D0%BE%D0%B4%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%81%D0%B8%D1%81%D1%82%D0%B5%D0%BC%D0%B0_%D1%85%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D1%85_%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82%D0%BE%D0%B2>
Д. И. Менделеева
<https://ru.wikipedia.org/wiki/%D0%9C%D0%B5%D0%BD%D0%B4%D0%B5%D0%BB%D0%B5%D0%B5%D0%B2,_%D0%94%D0%BC%D0%B8%D1%82%D1%80%D0%B8%D0%B9_%D0%98%D0%B2%D0%B0%D0%BD%D0%BE%D0%B2%D0%B8%D1%87>
с атомным номером <https://ru.wikipedia.org/wiki/%D0%90%D1%82%D0%BE%D0%BC%D0%BD%D1%8B%D0%B9_%D0%BD%D0%BE%D0%BC%D0%B5%D1%80>
25. Обозначается символом Mn (лат.
<https://ru.wikipedia.org/wiki/%D0%9B%D0%B0%D1%82%D0%B8%D0%BD%D1%81%D0%BA%D0%B8%D0%B9_%D1%8F%D0%B7%D1%8B%D0%BA>
Manganum, ма́нганум,
в составе формул по-русски читается как марганец, например, KMnO4 - калий
марганец о четыре). Простое вещество
<https://ru.wikipedia.org/wiki/%D0%9F%D1%80%D0%BE%D1%81%D1%82%D0%BE%D0%B5_%D0%B2%D0%B5%D1%89%D0%B5%D1%81%D1%82%D0%B2%D0%BE>марганец
- металл <https://ru.wikipedia.org/wiki/%D0%9C%D0%B5%D1%82%D0%B0%D0%BB%D0%BB>
серебристо-белого цвета
<https://ru.wikipedia.org/wiki/%D0%A6%D0%B2%D0%B5%D1%82>. Наряду с
железом
<https://ru.wikipedia.org/wiki/%D0%96%D0%B5%D0%BB%D0%B5%D0%B7%D0%BE> и
его сплавами относится к чёрным металлам <https://ru.wikipedia.org/wiki/%D0%A7%D1%91%D1%80%D0%BD%D1%8B%D0%B5_%D0%BC%D0%B5%D1%82%D0%B0%D0%BB%D0%BB%D1%8B>.
Известны пять аллотропных модификаций марганца - четыре с кубической и одна с
тетрагональной кристаллической решёткой.Конфигурация валентных электронов Mn 4s23d54p0.
Для марганца характерны степени окисления: +2 ( например, MnO, Mn(OH)2),
+3, +4(MnO2, Mn(OH)4, H4MnO4, H2MnO3), +6 (MnO3, H2MnO4, K2MnO4), +7 (Mn2O7, HMnO4, KMnO4).
1.2 Получение марганца
· Алюминотермическим
<https://ru.wikipedia.org/wiki/%D0%90%D0%BB%D1%8E%D0%BC%D0%B8%D0%BD%D0%BE%D1%82%D0%B5%D1%80%D0%BC%D0%B8%D1%8F>
методом, восстанавливая оксид Mn2O3, образующийся при прокаливании пиролюзита:

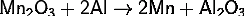
· Восстановлением
железосодержащих оксидных руд марганца коксом
<https://ru.wikipedia.org/wiki/%D0%9A%D0%B0%D0%BC%D0%B5%D0%BD%D0%BD%D0%BE%D1%83%D0%B3%D0%BE%D0%BB%D1%8C%D0%BD%D1%8B%D0%B9_%D0%BA%D0%BE%D0%BA%D1%81>.
Этим способом в металлургии обычно получают ферромарганец (~80 % Mn).
· Чистый
металлический марганец получают электролизом.
1.3 Химические свойства марганца и его соединений
Порошкообразный
марганец сгорает в кислороде (Mn + O2 → MnO2). Марганец при нагревании
разлагает воду, вытесняя водород
<https://ru.wikipedia.org/wiki/%D0%92%D0%BE%D0%B4%D0%BE%D1%80%D0%BE%D0%B4>
(Mn + 2H2O →(t) Mn(OH)2 + H2↑), образующийся гидроксид марганца
замедляет реакцию.
Марганец
поглощает водород, с повышением температуры его растворимость в марганце
увеличивается. При температуре выше 1200 °C взаимодействует с азотом
<https://ru.wikipedia.org/wiki/%D0%90%D0%B7%D0%BE%D1%82>, образуя
различные по составу нитриды <https://ru.wikipedia.org/wiki/%D0%9D%D0%B8%D1%82%D1%80%D0%B8%D0%B4%D1%8B>.
Углерод
<https://ru.wikipedia.org/wiki/%D0%A3%D0%B3%D0%BB%D0%B5%D1%80%D0%BE%D0%B4>
реагирует с расплавленным марганцем, образуя карбиды
<https://ru.wikipedia.org/wiki/%D0%9A%D0%B0%D1%80%D0%B1%D0%B8%D0%B4%D1%8B>
Mn3C и другие. Образует также силициды
<https://ru.wikipedia.org/wiki/%D0%A1%D0%B8%D0%BB%D0%B8%D1%86%D0%B8%D0%B4%D1%8B>,
бориды
<https://ru.wikipedia.org/wiki/%D0%91%D0%BE%D1%80%D0%B8%D0%B4%D1%8B>,
фосфиды <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%81%D1%84%D0%B8%D0%B4%D1%8B>.соляной
<https://ru.wikipedia.org/wiki/%D0%A1%D0%BE%D0%BB%D1%8F%D0%BD%D0%B0%D1%8F_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0>
и серной
<https://ru.wikipedia.org/wiki/%D0%A1%D0%B5%D1%80%D0%BD%D0%B0%D1%8F_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0>
кислотами реагирует по уравнению:
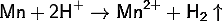
С
концентрированной серной кислотой реакция идёт по уравнению:
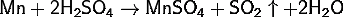
С
разбавленной азотной кислотой
<https://ru.wikipedia.org/wiki/%D0%90%D0%B7%D0%BE%D1%82%D0%BD%D0%B0%D1%8F_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0>
реакция идёт по уравнению:
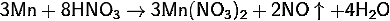
В
щелочном растворе марганец устойчив.
Устойчивые степени окисления марганца +2, +4, +7 в соединениях
кислородного и солевого характера. В медицинской практике используются
соединения марганца (II) и
марганца (VII).
Марганец (II) оксид MnOвстречается в природе в виде мелких
зеленых кристаллов, плохо растворимых в воде. При нагревании на воздухе
превращается в оксид:
MnO +3O2→6MnO2
Марганец (II) оксид
растворяется в кислотах:
+ 2H+ + 5H2O→[Mn(H2O)6]2+
Марганец (II) гидроксид
обладает слабоосновными свойствами, окисляется кислородом воздуха и другими
окислителями до марганцеватистой кислоты или ее солей манганитов:
(OH)2 + H2O2→H2MnO3↓ + H2O
В щелочной среде Mn2+
окисляется до MnO42-, а в кислой до МnO4-:
+ 2KNO3 + 4KOH→K2MnO4 + 2KNO2 + K2SO4 + 2H2O
Образуются соли марганцовистой H2MnO4 и марганцовой HMnO4 кислот.
Марганец (IV) оксид MnO2 является устойчивым природным
соединением марганца, которое встречается в четырех модификациях. Все
модификации имеют амфотерный характер и обладают окислительно-восстановительной
двойственностью.
Соединения Mn(VI) - неустойчивы. В растворах могут
превращаться в соединения Mn(II), Mn(IV), Mn(VII): оксид марганца (VI) MnO3 -
темно-красная масса, вызывающая кашель. Гидратная форма MnO3 - слабая марганцовистая кислота H2MnO4, которая существует только в водном растворе. Ее
соли (манганаты) легко разрушаются в результате гидролиза и при нагревании. При
50̊ С MnO3 разлагается:
MnO3→2MnO2 +O2
и гидролизуется при растворении в воде:
MnO3 +
H2O→ MnO2
+2HMnO4
Производные Mn(VII) - это марганец (VII) оксид Mn2O7 и его гидратная
форма кислота HMnO4, известная только в растворе. Mn2O7 устойчив до 10̊ С, разлагается со взрывом:
2O7 → 2 MnO2 +O3
При растворении в холодной воде образуется кислота:
2O7 + H2O →2HMnO4
.4 История открытия хрома, общие сведения
В
1766 году <https://ru.wikipedia.org/wiki/1766_%D0%B3%D0%BE%D0%B4> в
окрестностях Екатеринбурга
<https://ru.wikipedia.org/wiki/%D0%95%D0%BA%D0%B0%D1%82%D0%B5%D1%80%D0%B8%D0%BD%D0%B1%D1%83%D1%80%D0%B3>
был обнаружен минерал, который получил название «сибирский красный свинец»,
PbCrO4. Современное название - крокоит
<https://ru.wikipedia.org/wiki/%D0%9A%D1%80%D0%BE%D0%BA%D0%BE%D0%B8%D1%82>.
В 1797 <https://ru.wikipedia.org/wiki/1797> французский химик Л. Н.
Воклен <https://ru.wikipedia.org/wiki/%D0%92%D0%BE%D0%BA%D0%BB%D0%B5%D0%BD,_%D0%9B%D1%83%D0%B8_%D0%9D%D0%B8%D0%BA%D0%BE%D0%BB%D0%B0>
выделил из него новый тугоплавкий металл
<https://ru.wikipedia.org/wiki/%D0%9C%D0%B5%D1%82%D0%B0%D0%BB%D0%BB>
(скорее всего Воклен получил карбид хрома <https://ru.wikipedia.org/w/index.php?title=%D0%9A%D0%B0%D1%80%D0%B1%D0%B8%D0%B4_%D1%85%D1%80%D0%BE%D0%BC%D0%B0&action=edit&redlink=1>).
Название
элемент
<https://ru.wikipedia.org/wiki/%D0%AD%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82_(%D1%85%D0%B8%D0%BC%D0%B8%D1%8F)>
получил от греч.
<https://ru.wikipedia.org/wiki/%D0%93%D1%80%D0%B5%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9_%D1%8F%D0%B7%D1%8B%D0%BA>
χρῶμα - цвет
<https://ru.wikipedia.org/wiki/%D0%A6%D0%B2%D0%B5%D1%82>, краска - из-за
разнообразия окраски своих соединений.
Хром
- элемент
<https://ru.wikipedia.org/wiki/%D0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9_%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82>
побочной подгруппы 6-ой группы 4-го периода периодической системы химических
элементов <https://ru.wikipedia.org/wiki/%D0%9F%D0%B5%D1%80%D0%B8%D0%BE%D0%B4%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%81%D0%B8%D1%81%D1%82%D0%B5%D0%BC%D0%B0_%D1%85%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D1%85_%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82%D0%BE%D0%B2>
Д. И. Менделеева
<https://ru.wikipedia.org/wiki/%D0%9C%D0%B5%D0%BD%D0%B4%D0%B5%D0%BB%D0%B5%D0%B5%D0%B2,_%D0%94%D0%BC%D0%B8%D1%82%D1%80%D0%B8%D0%B9_%D0%98%D0%B2%D0%B0%D0%BD%D0%BE%D0%B2%D0%B8%D1%87>
с атомным номером <https://ru.wikipedia.org/wiki/%D0%90%D1%82%D0%BE%D0%BC%D0%BD%D1%8B%D0%B9_%D0%BD%D0%BE%D0%BC%D0%B5%D1%80>
24. Обозначается символом Cr(лат.
<https://ru.wikipedia.org/wiki/%D0%9B%D0%B0%D1%82%D0%B8%D0%BD%D1%81%D0%BA%D0%B8%D0%B9_%D1%8F%D0%B7%D1%8B%D0%BA>
Chromium). Простое вещество <https://ru.wikipedia.org/wiki/%D0%9F%D1%80%D0%BE%D1%81%D1%82%D0%BE%D0%B5_%D0%B2%D0%B5%D1%89%D0%B5%D1%81%D1%82%D0%B2%D0%BE>
хром - твёрдый металл
<https://ru.wikipedia.org/wiki/%D0%9C%D0%B5%D1%82%D0%B0%D0%BB%D0%BB>
голубовато-белого цвета <https://ru.wikipedia.org/wiki/%D0%A6%D0%B2%D0%B5%D1%82>.
Хром иногда относят к чёрным металлам
<https://ru.wikipedia.org/wiki/%D0%A7%D1%91%D1%80%D0%BD%D1%8B%D0%B5_%D0%BC%D0%B5%D1%82%D0%B0%D0%BB%D0%BB%D1%8B>.
Конфигурация валентных электронов Cr 4s13d54p0.
Для хрома характерны степени окисления: +2 (CrO, Cr(OH)2-
основные, восстановительные свойства), +3 (Cr2O3, Cr(OH)3
- амфотерные свойства), +6.
Хром
является довольно распространённым элементом (0,02 масс. долей, %). Основные
соединения хрома - хромистый железняк (хромит <https://ru.wikipedia.org/wiki/%D0%A5%D1%80%D0%BE%D0%BC%D0%B8%D1%82>)
FeO·Cr2O3. Вторым по значимости минералом является крокоит
<https://ru.wikipedia.org/wiki/%D0%9A%D1%80%D0%BE%D0%BA%D0%BE%D0%B8%D1%82>PbCrO4.
Самые
большие месторождения хрома находятся в ЮАР <https://ru.wikipedia.org/wiki/%D0%AE%D0%90%D0%A0>
(1 место в мире), Казахстане
<https://ru.wikipedia.org/wiki/%D0%9A%D0%B0%D0%B7%D0%B0%D1%85%D1%81%D1%82%D0%B0%D0%BD>,
России
<https://ru.wikipedia.org/wiki/%D0%A0%D0%BE%D1%81%D1%81%D0%B8%D1%8F>,
Зимбабве <https://ru.wikipedia.org/wiki/%D0%97%D0%B8%D0%BC%D0%B1%D0%B0%D0%B1%D0%B2%D0%B5>,Мадагаскаре
<https://ru.wikipedia.org/wiki/%D0%9C%D0%B0%D0%B4%D0%B0%D0%B3%D0%B0%D1%81%D0%BA%D0%B0%D1%80>.
Также есть месторождения на территории Турции <https://ru.wikipedia.org/wiki/%D0%A2%D1%83%D1%80%D1%86%D0%B8%D1%8F>,
Индии <https://ru.wikipedia.org/wiki/%D0%98%D0%BD%D0%B4%D0%B8%D1%8F>,
Армении
<https://ru.wikipedia.org/wiki/%D0%90%D1%80%D0%BC%D0%B5%D0%BD%D0%B8%D1%8F>,
Бразилии <https://ru.wikipedia.org/wiki/%D0%91%D1%80%D0%B0%D0%B7%D0%B8%D0%BB%D0%B8%D1%8F>,
наФилиппинах
<https://ru.wikipedia.org/wiki/%D0%A4%D0%B8%D0%BB%D0%B8%D0%BF%D0%BF%D0%B8%D0%BD%D1%8B>.
Главные
месторождения хромовых руд в РФ известны на Урале
<https://ru.wikipedia.org/wiki/%D0%A3%D1%80%D0%B0%D0%BB> (Донские и
Сарановское).
Разведанные
запасы в Казахстане составляют свыше 350 миллионов тонн (2 место в мире).
.5 Получение хрома
Хром
встречается в природе в основном в виде хромистого железняка Fe(CrO2)2 (хромит
железа). Из него получают феррохром <https://ru.wikipedia.org/wiki/%D0%A4%D0%B5%D1%80%D1%80%D0%BE%D1%85%D1%80%D0%BE%D0%BC>
восстановлением в электропечахкоксом
<https://ru.wikipedia.org/wiki/%D0%9A%D0%B0%D0%BC%D0%B5%D0%BD%D0%BD%D0%BE%D1%83%D0%B3%D0%BE%D0%BB%D1%8C%D0%BD%D1%8B%D0%B9_%D0%BA%D0%BE%D0%BA%D1%81>
(углеродом):

Феррохром
<https://ru.wikipedia.org/wiki/%D0%A4%D0%B5%D1%80%D1%80%D0%BE%D1%85%D1%80%D0%BE%D0%BC>
применяют для производства легированных сталей.
)
сплавляют хромит железа с карбонатом натрия (кальцинированная сода) на воздухе:
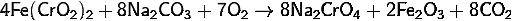
)
растворяют хромат натрия и отделяют его от оксида железа;
)
переводят хромат в дихромат, подкисляя раствор и выкристаллизовывая дихромат;
)
получают чистый оксид хрома восстановлением дихромата натрия углём:

)
с помощью алюминотермии
<https://ru.wikipedia.org/wiki/%D0%90%D0%BB%D1%8E%D0%BC%D0%B8%D0%BD%D0%BE%D1%82%D0%B5%D1%80%D0%BC%D0%B8%D1%8F>
получают металлический хром:
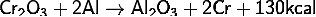
)
с помощью электролиза
<https://ru.wikipedia.org/wiki/%D0%AD%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BB%D0%B8%D0%B7>
получают электролитический хром из раствора хромового ангидрида
<https://ru.wikipedia.org/wiki/%D0%A5%D1%80%D0%BE%D0%BC%D0%BE%D0%B2%D1%8B%D0%B9_%D0%B0%D0%BD%D0%B3%D0%B8%D0%B4%D1%80%D0%B8%D0%B4>
в воде, содержащего добавку серной кислоты
<https://ru.wikipedia.org/wiki/%D0%A1%D0%B5%D1%80%D0%BD%D0%B0%D1%8F_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0>.
При этом на катодах совершаются в основном 3 процесса:
· восстановление шестивалентного хрома
до трехвалентного с переходом его в раствор;
· разряд ионов водорода с выделением
газообразного водорода;
· разряд
ионов, содержащих шестивалентный хром
<https://ru.wikipedia.org/wiki/%D0%A8%D0%B5%D1%81%D1%82%D0%B8%D0%B2%D0%B0%D0%BB%D0%B5%D0%BD%D1%82%D0%BD%D1%8B%D0%B9_%D1%85%D1%80%D0%BE%D0%BC>,
с осаждением металлического хрома;
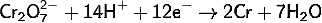
.6 Химические свойства хрома и его соединений
марганец хром микроэлемент организм
Хром
устойчив на воздухе
<https://ru.wikipedia.org/wiki/%D0%92%D0%BE%D0%B7%D0%B4%D1%83%D1%85> за
счёт пассивирования
<https://ru.wikipedia.org/wiki/%D0%9F%D0%B0%D1%81%D1%81%D0%B8%D0%B2%D0%B8%D1%80%D0%BE%D0%B2%D0%B0%D0%BD%D0%B8%D0%B5>.
По этой же причине не реагирует с серной и азотной кислотами. При 2000 °C
сгорает с образованием зелёного оксида хрома(III) Cr2O3, обладающего
амфотерными свойствами
<https://ru.wikipedia.org/wiki/%D0%90%D0%BC%D1%84%D0%BE%D1%82%D0%B5%D1%80%D0%BD%D0%BE%D1%81%D1%82%D1%8C>.
Синтезированы
соединения хрома с бором
<https://ru.wikipedia.org/wiki/%D0%91%D0%BE%D1%80_(%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82)>
(бориды
<https://ru.wikipedia.org/wiki/%D0%91%D0%BE%D1%80%D0%B8%D0%B4%D1%8B>
Cr2B, CrB, Cr3B4, CrB2, CrB4 и Cr5B3), с углеродом
<https://ru.wikipedia.org/wiki/%D0%A3%D0%B3%D0%BB%D0%B5%D1%80%D0%BE%D0%B4>
(карбиды
<https://ru.wikipedia.org/wiki/%D0%9A%D0%B0%D1%80%D0%B1%D0%B8%D0%B4>
Cr23C6, Cr7C3 и Cr3C2), c кремнием <https://ru.wikipedia.org/wiki/%D0%9A%D1%80%D0%B5%D0%BC%D0%BD%D0%B8%D0%B9>
(силициды
<https://ru.wikipedia.org/wiki/%D0%A1%D0%B8%D0%BB%D0%B8%D1%86%D0%B8%D0%B4%D1%8B>
Cr3Si, Cr5Si3 и CrSi) и азотом
<https://ru.wikipedia.org/wiki/%D0%90%D0%B7%D0%BE%D1%82> (нитриды
<https://ru.wikipedia.org/wiki/%D0%9D%D0%B8%D1%82%D1%80%D0%B8%D0%B4%D1%8B>
CrN и Cr2N).
Большинство
соединений хрома имеет яркую окраску самых разных цветов.
Соединения
трехвалентного хрома химически инертны.
В
природе хром находится в трех- (шпинель - двойной оксид MgCrO4
- магнохромит) и шестивалентном состоянии (PbCrO4 -
крокоит). Образует оксиды основного, амфотерного и кислотного характера.
Хром
(II) оксид CrO - кристаллы красного (красно-коричневого) цвета или
черный пирофорный порошок, нерастворимый в воде. Соответствует гидроксиду Cr(OH)2.
Гидроксид желтого ( влажный) или коричневого цвета. При прокаливании на воздухе
превращается в Cr2O3 (зеленого цвета):
2Cr(OH)2 + 0,5O2= Cr2O3 + 2 H2O
Катион
Cr2+ - бесцветен, его безводные соли белого, а водные
-синего цвета. Соли двухвалентного хрома являются энергичными восстановителями.
Водный раствор хром (II) хлорида используется в газовом анализе для
количественного поглощения кислорода:
CrCl2 + 2 HgO +
3H2O + 0,5O2 = 2HgCl2 + 2 Cr(OH)3↓
(грязно-зеленый
осадок)
Хром
(III) гидроксид обладает амфотерными свойствами. Легко
переходит в коллоидное состояние. Растворяясь в кислотах и щелочах, образует
аква- или гидроксокомплексы:
(OH)3
+ 3H3O+ = [Cr(H2O)6]3+ (сине-фиолетовый раствор)
Cr(OH)3
+ 3OH- = [Cr(OH)6]3- (изумрудно-зеленый раствор)
Соединения
трехвалентного хрома, как и двухвалентного, проявляют восстановительные
свойства:
(SO4)3 + KClO3 + 10 KOH = 2K2CrO4 + 3 K2SO4 + KCl +
5H2O
Соединения
хрома(VI), как правило, кислородосодержащие комплексы хрома
оксид шестивалентного хрома соответствует хромовым кислотам.
Хромовые
кислоты образуются при растворении в воде CrO3. Это сильно
токсичные растворы желтого, оранжевого и красного цвета, обладающие
окислительными свойствами. CrO3 образует полихромовые кислоты, например, H2CrO4,
H2Cr2O7, H2Cr3O10, H2Cr4O13. Цвета растворов меняются от желтого до красного.
Глава 2. Биологическая роль марганца и хрома
Марганец- биогенный элемент, один из десяти металлов жизни, необходимых
для нормального протекания процессов в живых организмах.
Марганец
содержится в организмах всех растений и животных, хотя его содержание обычно
очень мало, порядка тысячных долей процента, он оказывает значительное влияние
на жизнедеятельность, то есть является микроэлементом
<https://ru.wikipedia.org/wiki/%D0%9C%D0%B8%D0%BA%D1%80%D0%BE%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82%D1%8B>.
В теле взрослого человека содержится 12 мг (1,6 * 10-5%). Марганец
концентрируется в костях (43%), остальное - в мягких тканях, в том числе и
мозге.
В
организме марганец образует металлокомплексы с белками, нуклеиновыми кислотами,
АТФ, АДФ, отдельными аминокислотами. Содержащие марганец металлоферменты
аргиназа, холинэстераза, фосфоглюкомутаза, пирувакарбоксилаза.
Марганец
участвует в синтезе витамина С и В12.
Атомный
радиус марганца 128 пм. Это объясняет то обстоятельство, что марганец может
замещать магний ( атомный радиус 160 пм) в его соединении с АТФ, существенно
влияя на перенос энергии в организме.
Почти
одинаковое значение атомного радиуса марганца (128 пм) и железа (126 пм) объясняет
способность марганца замещать железо в порфириновом комплексе эритроцита. По
той же причине марганец может замещать и цинк ( атомный радиус 127 пм) в
цинкзависимых ферментах, изменяя при этом их каталитические свойства.
Для
организма перманганаты являются ядами, их обезвреживание может происходить
следующим образом:
KMnO4+5H2O2+6CH3COOH=2Mn(CH3COO)2+2CH3COOK+8H2O+5O2
Для
лечения острых отравлений перманганатом используется 3%-ный водный раствор H2O2 ,
подкисленный уксусной кислотой.
Калий
перманганат KMnO4 - наиболее известное соединение марганца,
применяемое в медицине. Используют водные растворы с содержанием KMnO4
от 0,01 до 5%. В качестве кровоостанавливающего средства применяют 5%-ный
раствор. Растворы калия перманганата обладают антисептическими свойствами,
которые определяются его высокой окислительной способностью. MnSO4
применяют при лечении малокровия.
Избыточное
накопление марганца в организме сказывается, в первую очередь, на
функционировании центральной нервной системы. Это проявляется в утомляемости,
сонливости, ухудшении функций памяти. Марганец является политропным ядом,
поражающим также легкие, сердечно-сосудистую и гепатобиллиарную системы,
вызывает аллергический и мутагенный эффект.
Хром
- один из биогенных элементов <https://ru.wikipedia.org/w/index.php?title=%D0%91%D0%B8%D0%BE%D0%B3%D0%B5%D0%BD%D0%BD%D1%8B%D0%B9_%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82&action=edit&redlink=1>,
постоянно входит в состав тканей растений и животных. В организме взрослого
человека содержится примерно 6 г Cr (0,1%) У животных хром участвует в обмене липидов
<https://ru.wikipedia.org/wiki/%D0%9B%D0%B8%D0%BF%D0%B8%D0%B4%D1%8B>,
белков <https://ru.wikipedia.org/wiki/%D0%91%D0%B5%D0%BB%D0%BA%D0%B8>
(входит в составфермента <https://ru.wikipedia.org/wiki/%D0%A4%D0%B5%D1%80%D0%BC%D0%B5%D0%BD%D1%82>
трипсина
<https://ru.wikipedia.org/wiki/%D0%A2%D1%80%D0%B8%D0%BF%D1%81%D0%B8%D0%BD>),
углеводов
<https://ru.wikipedia.org/wiki/%D0%A3%D0%B3%D0%BB%D0%B5%D0%B2%D0%BE%D0%B4%D1%8B>.
В
чистом виде хром довольно токсичен, металлическая пыль
<https://ru.wikipedia.org/wiki/%D0%9F%D1%8B%D0%BB%D1%8C> хрома раздражает
ткани лёгких
<https://ru.wikipedia.org/wiki/%D0%9B%D1%91%D0%B3%D0%BA%D0%B8%D0%B5>.
Металлический хром нетоксичен, а соединения Cr (III)
и Cr(VI) опасны для здоровья. Они вызывают раздражение кожи,
что приводи к дерматитам. Соединения хрома(VI) приводят к разным заболеваниям
человека, в том числе и онкологическим. Есть предположение, что производные
хрома (VI) обладают канцерогенными свойствами. 0,25-0,3г
дихромата калия вызывают летальный исход. Соединения хрома (VI)
применяют как фунгициды (протравливающие вещества). Соединения хрома (III)
благоприятно влияют на рост растений.
Сr+3-
влияет на углеводный обмен, обеспечивает чувствительность ткани к инсулину.
CrO3 обладает
прижигающим действием, это свойство используют в медицине.
Смертельная
доза K2Cr2O7 для взрослого человека составляет 0,3г.
Снижение
содержания хрома в пище и крови приводит к уменьшению скорости роста,
увеличению холестерина <https://ru.wikipedia.org/wiki/%D0%A5%D0%BE%D0%BB%D0%B5%D1%81%D1%82%D0%B5%D1%80%D0%B8%D0%BD>
в крови.
Глава 3. Нормы потребления марганца и хрома
.1 Нормы потребления марганца, недостаток и переизбыток микроэлемента
Марганец (Mn) необходим для правильного развития клеток. Его присутствие
в организме - обязательное условие для полноценного усвоения витамина В1
(тиамина), меди и железа, необходимых для осуществления кроветворной функции.
Без тиамина невозможен процесс строительства клеток, в частности нервных. При
дефиците этого витамина возникают запоры, полиневриты, склонность к развитию
анемии и остеопороза.
Суточная потребность марганца для взрослого организма составляет 0,2-0,3
мг на 1 кг массы тела.
Для детей и подростков норма рассчитывается так: 5-7 лет - 0,07-0,1 мг/кг,
для подростков - 0,09 мг/кг веса.
В пересчёте на организм взрослого человека норма потребления марганца
составляет от 2,5 до 5 мг в сутки.
Детский же организм требует, естественно, меньшее количество - около 1-2
мг в день.
Интенсивность физической нагрузки оказывает влияние на потребность в
микроэлементе, поэтому норма потребления марганца для спортсменов несколько
больше, чем среднестатистическая потребность взрослого организма и составляет
от 7 до 8,5 мг в день.
При длительном недостатке марганца в организме могут возникнуть
патологические состояния, плохо поддающиеся коррекции. Например, если будущая
мать испытывает дефицит Mn, то плод развивается неправильно: ребёнок может
получить патологию развития конечностей, родиться со сращиванием подвижных суставов,
с деформацией черепа.
Дефицит марганца приводит к различным формам анемии, нарушениям функций
воспроизводства у обоих полов, задержке роста детей, проявлениям дефицита массы
тела и др.
Недостаток марганца может наблюдаться у людей со следующими клиническими
симптомами и заболеваниями:
хроническая усталость, слабость, раздражительность;
аллергический насморк, склонность к бронхоспазмам;
остеопороз и артроз, в группе риска - женщины и пожилые люди;
избыточный вес, в сочетании с повышенном уровнем липидов в
крови;
склонность к судорогам у детей, задержка их психомоторного
развития.
Опасно
не только недостаточное содержание марганца в организме, но и его избыток.
Повышенное содержание марганца в тканях организма вызывает следующие нарушения:
ухудшается всасывание железа и возникает риск развития анемии
<http://fitfan.ru/health/bolezni/2305-anemiya.html>, ухудшается состояние
нервной системы, возникает нарушение всасывания кальция, что приводит к
нарушению функционирования костно-мышечной системы.
Основными
клиническими симптомами интоксикации марганцем являются:
потеря аппетита;
прогрессирующие галлюцинации;
значительное ухудшение памяти;
болезненная сонливость;
мышечные боли, судороги.
Определенные
категории людей наиболее подвержены к возникновению избытка марганца в
организме. Им необходимо снижать концентрацию данного микроэлемента в
организме, исключая из рациона продукты богатые Mn. В эту категорию входят люди
страдающие болезнью Паркинсона, а также работающие на вредном производстве:
нефтеперерабатывающих и сталеплавильных заводах, электротехнических станциях.
Если же говорить о профессиях, то это преимущественно электросварщики, шахтёры
и т.д.
Также
избыток марганца приводит к патологиям, идентичным рахиту. Заболевание названо
марганцевым рахитом. К полному выздоровлению от данного недуга приводит лечение
витамином D при полноценном питании.
Если
предстоит назначение приёма марганецсодержащих препаратов, следует непременно
проверить в крови его уровень, так как неконтролируемый приём витаминных и
минеральных препаратов часто приводит к нарушению баланса микроэлемента в
организме.
.2
Нормы потребления хрома, недостаток и переизбыток микроэлемента
Хром
- критически важный микроэлемент. В природе он встречается в трех различных
формах, причем в нашем рационе преобладает одна из них (хром III).
Суточная
потребность взрослого человека в хроме составляет 0,20-0,25 мг.
Дефицит
хрома в организме может развиваться при длительном питании преимущественно
продуктами, бедными хромом, использовании больших количеств сахара, который
способствует выведению хрома с мочой. К числу таких продуктов относятся хлеб из
муки высших сортов, кондитерские изделия.
Дефицит
хрома в организме ведет к снижению чувствительности тканей к инсулину,
ухудшению усвоения ими глюкозы, увеличению ее содержания в крови.
Опыты
показали, что, если в организме крыс мало хрома, уровень холестерина и сахара в
крови повышается, а жировые вещества оседают на стыках аорты. Когда крыс
докармливают этим элементом, уровень холестерина и сахара в крови снижается.
У
здоровых людей содержание хрома несколько выше нормы. Это является признаком
полноценного усвоения глюкозы. Если усвоение сахаров нарушено, содержание этого
элемента снижается.
Хром
очень нужен больным диабетом, он "сотрудничает" с инсулином, помогая
регулировать уровень сахара или глюкозы в крови. Несмотря на то что получен
синтетический GTF, все-таки лучше предпочесть натуральный хром, содержащийся в
дрожжах - самом богатом его источнике, как более эффективный. Кроме того,
биологически активный хром находится в телячьей печени и проросших зернах
пшеницы.
Там,
где люди работают в контакте с хромом и вынуждены вдыхать хромовую пыль, они, к
сожалению, в 29 раз чаще, чем другие жители тех же мест, и в 11 раз чаще, чем
рабочие других отраслей промышленности, заболевают раком легких или бронхов.
Слишком
много хрома обычно около фабрик и вообще в промышленных районах, где из-за
отсутствия хорошей системы пылеулавливания этот металл в больших количествах
уносится в воздух.
Глава
4. Пищевые источники микроэлементов
.1
Пищевые источники марганца
Для
поддержания оптимального количества микроэлемента в организме необходимо знать,
как восполнить его недостаток в организме и как не допустить его избыточного
накопления. Для ответа на эти вопросы необходимо знать, с какими продуктами
питания Mn в организм попадает и в каких количествах. Очень много марганца
содержится в таких напитках, как чай и кофе. Клюква, съедобные каштаны, перец также
им богаты. Ниже приведены данные по продуктам и количеству Mn (в миллиграммах)
на 1 килограмм продукта.
Продукт
Содержание марганца, мг/кг продукта
Молоко
0,04
Мясо
(всех видов, кроме свинины, птица и яйца) 0 - 50
Свинина,
почки, сыр 2-10
Рыба
(крабы и раки) 0,5-2
Масло
оливковое 0,5-2
Мёд
светлый 0,5 - 2
Лимон
0,5
Сельдерей
0,5 - 2
Капуста
белокочанная, цветная, ревень, редька, оливки, морковь, огурцы, грибы,
картофель, спаржа, репа, помидоры, ржаная мука, сливы, финики, виноград 2
- 10
Печень,
свекла, фасоль, хлеб пшеничный и ржаной, лук, зеленый горошек, брусника,
бананы, петрушка, смородина, черника, чернослив, тёмный мёд, устрица, инжир,
дрожжи 2 - 10
Мука
пшеничная 10 - 70
Шпинат,
салат, малина, шоколад, сухой в зёрнах горох и фасоль, рис, орех кокосовый,
ячмень, желатин 30
Какао
35
Мука
и хлопья овсяные 36
Перец
65
Соевая
мука, съедобный каштан 40
Клюква
40 - 200
Чай
(все сорта) 150 - 900
Употребляя
вышеперечисленные продукты можно достаточно легко удовлетворить потребность
организма в марганце. При дефиците микроэлемента следует больше употреблять
продуктов натуральных, нерафинированных, без тепловой обработки. Для
предотвращения избыточного накопления марганца необходимо избегать употребления
продуктов, с большим содержанием данного микроэлемента, или подвергать их
тщательной термической обработке.
.2
Пищевые источники хрома
Хром
является эссенциальным (жизненно необходимым) элементом.
Организм
взрослого человека содержит 5-6 мг хрома.
Наибольшие
концентрации хрома наблюдают в печени и почках (0,6 мкг/кг), а также в хрящевой
и костной ткани, кишечнике, щитовидной железе.
Наиболее
важными источниками хрома являются субпродукты (печень), мясо
<http://eat-info.ru/references/encyclopedia/>, продукты из цельного
зерна, сыр, бобовые и специи, яйца, морепродукты, рыба, бананы, апельсины,
яблоки, кукуруза, зеленый лук, капуста, морковь, томаты, сладкий перец,
картофель, грибы, черника, рябина, голубика, клюква, облепиха, пивные дрожжи,
молочные продукты и молоко.
Список
литературы
1. Учеб.
для вузов/ Ю.А.Ершов, В.А.Попков, А.С. Берлянд и др.; Под ред. Ю.А. Ершова. -
3-е изд., стер. - М.: Высш. шк., 2002. - 263-276с.: ил.
. А.Я
Губергриц "Лечебное питание"
3. http://sovetik.ucoz.ru/publ/pishhevye_dobavki/khrom_naznachenie_istochniki_dozirovanie_issledovanija/5-1-0-181
. <http://fitfan.ru/nutrition/vitamins/3239-marganec.html>