Изучение химической сборки макромолекул в гидролизе органоалкоксисиланов
Содержание
Введение
1. Литературный обзор
1.1 Гидролитическая поликонденсация органоалкоксисиланов
1.1.1 Исходные реагенты
1.1.2 Гидролиз
.1.2.1 Влияние катализатора
.1.2.2 Стерические и индукционные эффекты
.1.2.3 Отношение H2O/Si
.1.2.4 Влияние растворителя
.1.2.5 Механизм гидролиза
.1.2.5.1 Гидролиз в присутствии кислоты, как катализатора
.1.2.5.2 Гидролиз в присутствии щелочи, как катализатора
.1.2.6 Обратимость реакции гидролиза
.1.3 Реакции конденсации продуктов гидролиза
.1.3.1 Механизм реакций конденсации
.1.3.1.1 Конденсация в основных условиях
.1.3.1.2 Конденсация в присутствии кислоты, как катализатора
1.1.3.2 Порядок реакции по реагентам
.1.3.3 Влияние катализатора
.1.3.4 Стерические и индуктивные эффекты
.1.3.5 Влияние растворителя
.1.3.6 Влияние обратных реакций
1.2 Способы оценки формирования цепи олигоорганосилоксанов
2. Обсуждение результатов
.1 Методология эксперимента
.2 Частичный гидролиз органотриалкоксисиланов
. Экспериментальная часть
.1 Техника эксперимента
.2 Контроль состава продуктов ГПК органоалкоксисиланов
3.3 Частичный гидролиз фенилтриметоксисилана и
метилтриэтоксисилана
3.4 Получение диметилтетраэтоксидисилоксана
.5 Частичный гидролиз диметилтетраэтоксидисилоксана
Выводы
Список литературы
органоалкоксисилан гидролиз кислота щелочь катализатор
Введение
Гидролиз органоалкоксисиланов является исторически первым процессом,
используемым для синтеза полиорганосилоксанов [1]. Тем не менее, на сегодняшний
день полиорганосилоксаны получают в промышленности путем гидролиза не
алкоксисиланов, а органохлорсиланов. Это обусловлено тем, что органохлорсиланы
являются основными промышленными мономерами. Методы прямого синтеза
алкоксисиланов находятся на стадии своего развития и возможно появятся
предпосылки, что в ближайшем будущем именно эти соединения станут основными
промышленными мономерами для получения кремнийорганических полимеров.
Оба класса веществ (органохлорсиланы и алкоксиды Si) являются важными исходными реагентами для получения
полиорганосилоксанов различного строения и материалов, получаемых на основе
золь-гель технологий. В силу более раннего становления промышленного
производства органохлорсиланов
За последние 25 лет развито новое направление исследований в области ГПК
органохлорсиланов - это изучение роли фазового квазиравновесия реакционной
системы на механизм формирования (химическую сборку) полимерных цепей
силоксанов. Установлено, что вследствие гетерофазного характера процесса
полиорганосилоксаны образуются в органической фазе по ГТФК продуктов частичного
гидролиза. Разработан метод формирования блочной, позвенной, полимеризационной
и циклической сборки макромолекул.
Что касается изучения ГПК органоалкоксисиланов, то при наличии сложного
механизма, кинетики гидролиза и конденсации исследование влияния гетерофазности
процесса на химическую сборку макромолекул не проводились. В связи с тем, что
реакционная способность алкоксисиланов меньше, а растворимость выше, чем у
хлорсиланов, роль фазового равновесия и сборки цепи может проходить по другому.
В этой связи цель нашей работы - изучение химической сборки в процессе
гидролитической поликонденсации органотриалкоксисиланов.
1. Литературный обзор
1.1 Гидролитическая поликонденсация органоалкоксисиланов
Гидролитическая поликонденсация кремнийорганических мономеров на
сегодняшний день остается основным способом получения полиорганосилоксанов
различного строения. Ввиду того, что требования к качеству и экологичности
производства таких полимеров постоянно возрастают, назрела необходимость
перехода при получении полиорганосилоксанов из органохлорсиланов на
органоалкокси-производные.
В настоящее время алкоксисиланы играют важную роль в получении
кремнийорганических материалов. Тетраалкоксисиланы используются при получении SiO2 и гибридных полимеров в золь-гель
процессах. Замещенные алкил- или арилалкоксисиланы - исходные соединения для
получения силиконовых смол. В сочетании с тетраалкоксисиланами или другими
соединениями они способны образовывать трехмерные структуры, которые
применяются для получения гетерополисилоксанов. Диорганодиалкоксисиланы -
мономеры для получения линейных и циклических олигомеров и полимеров.
В результате гидролитической поликонденсации органоалкоксисиланов
образуется полисилоксан и побочный продукт - спирт [1]. Склонность
первоначально образующихся гидроксильных производных кремния к межмолекулярной
конденсации с образованием сложных молекул с силоксановыми связями лежит в
основе образования полисилоксанов [1]. Алкоксисиланы вступают в реакцию
гидролиза, а затем продукты гидролиза могут участвовать в реакциях гомофункциональной
конденсации с выделением воды и гетерофункциональной конденсации с выделением
спирта (уравнения 1-3). Зачастую эти реакции реализуются одновременно и их
соотношения зависят от многих факторов.
Гидролиз (1)
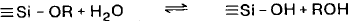
Этерификация
ГТФК (2)
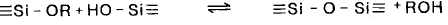
ГМФК (3)

Поскольку вода и алкоксисиланы не смешиваются, используют взаимный
растворитель. Необходимо отметить, что полисилоксаны можно получить и без
добавления растворителя [2], ведь в результате гидролиза образуется спирт,
который служит гомогенизирующим агентом в данной системе. Так же спирт может
выступать не только в качестве растворителя, но и способствовать протеканию
обратных реакций (уравнения 1-2).
В зависимости от состава и структуры желаемого конечного продукта
варьируется отношение H2O/Si m = 1-50 и концентрации кислот или оснований от 0,01 до 7 М,
используемых в качестве катализатора [3;4].
Для проведения полного гидролиза тетраалкоксисилана теоретически
достаточным является отношение H2O/Si = 2.
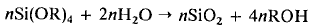 (4)
(4)
Однако даже при избытке воды (m >2) реакция не проходит до конца. Вместо этого образуется ряд
интермедиатов ([SiOx(OH)y(OR)z]n.
На рис. 2 показана последовательность ЯМР Si29 спектров и образования продуктов с
течением времени при гидролизе тетраэтоксисилана в кислых условиях с значением m = 2 [5]. Наблюдается, что реакция
образования безводного полисилоксана не идет к завершению, о чем
свидетельствует комплексы распределения видов Qn (n= 0-4 OH
групп) даже по прошествии времени.
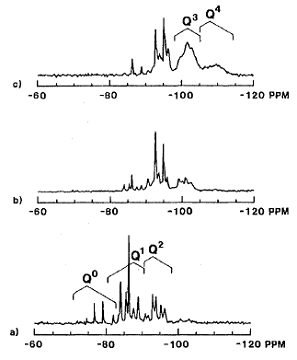
Рис. 1. ЯМР Si29 спектры при гидролизе
тетраэтоксисилана (m=2) в присутствии
кислоты, как катализатора, через а) 3 часа, b) 3 дня, е) 14 дней.[5]
На практике реакции гидролиза и конденсации проходят одновременно.
 (5)
(5)
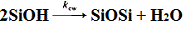 (6)
(6)
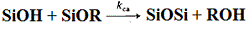 , (7)
, (7)
где kh - константа скорости гидролиза, cw - константа скорости ГМФК, ca - константа скорости ГТФК.
Kay и Assink [63.95-97] представили 15 видов
возможных соединений общей формулы Si(OR)x(OH)y(OSi)z
в матричной форме, как показано на рис. 22, где упорядоченный триплет (x, y, z) соответствует
числу -OR, -OH, -OSi на
центральном атоме кремния (x+y+z=4=координация Si).
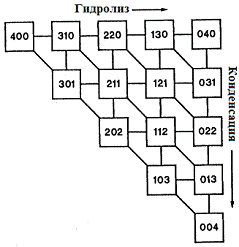
Рис. 2. Матричная форма соединений вида Si(OR)x(OH)y(OSi)z. [38,55,74].
Kay и Assink [38, 55, 74, 75] используя ЯМР H1 и 29Si определили значения kh, kcw, kca начальных стадий во времени при
кислотно-катализируемом гидролизе тетраметоксисилана и рассмотрели несколько
кинетических моделей. ЯМР H1 использовался с целью измерения
относительного количества метокси- групп и метилового спирта. По полученным
данным выделили 2 существующие лимитирующие стадии: 1) если скорость гидролиза
гораздо больше скоростей конденсаций, тогда количество метокси- групп будет
уменьшатся, до значения соответствующего гидролизу без конденсации (дальнейшее
уменьшение количества метокси- групп происходит с низкой скоростью соизмеримой
с общей скоростью конденсации); 2) если скорость гидролиза намного меньше общей
скорости конденсаций, тогда гидролиз будет следовать за быстрой конденсацией (в
этом случае, уменьшение количества метокси- групп происходит со скоростью
пропорциональной скорости гидролиза). С помощью ЯМР 29Si определяли скорость образования Si-O-Si связей. Две лимитирующие стадии
могут быть рассмотрены на основе уравнения:
d[(SiO)Si]/dt = kcw[SiOH]2 + Kca[SiOH][SiOR]
(8)
Если kcw гораздо больше чем kca, скорость конденсации будет пропорциональна
[SiOH]2. Если kcw намного меньше чем kca, скорость конденсации будет
пропорциональная [SiOH][SiOR]. В случае, когда начальная общая
скорость конденсации является незначительной в сравнении с начальной скоростью
гидролиза, а также начальные реакции гидролиза является завершенными, то
уравнение 8 можно записать как:
d[(SiO)Si]/(<[SiOH]>*dt) = (kcw - kca)<[SiOH]>
+ kca[SiOMe]o (9)
Это выражение имеет силу при малых значениях времени, когда концентрация Si-O-Si мала по
сравнению с концентрацией начальных метокси- групп.
Многочисленные исследования показали, что изменение условий синтеза
(таких как, значения m,
типа катализатора и его концентрации, типа растворителя, температуры и т.д.)
влияют на структуру и свойства образующегося полисилоксана [5].
1.1.1 Исходные реагенты
Наиболее распространенными тетраалкоксисиланами используемыми в золь-гель
технологии являются тетраэтоксисилан и тетраметоксисилан. Традиционным методом
получения тетраалкоксисиланов или органоалкоксисиланов является реакция этерификации
тетрахлорсилана или органохлорсиланов, соответственно [6].
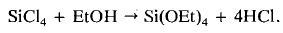 (10)
(10)
В таблицах 1 и 2 приведены химические формулы и свойства некоторых
тетраалкоксисиланов и органоалкоксисиланов использующихся в золь-гель технологиях.
Таблица 1. Физические свойства некоторых тетраалкоксисиланов [7].
|
Название
|
ММ
|
Ткип, 0С
|
nD (200С)
|
d (200С)
|
η
|
µ
|
|
Тетраметоксисилан 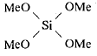 152,21211,36881,025,461,71 152,21211,36881,025,461,71
|
|
|
|
|
|
|
|
Тетраэтоксисилан 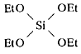 208,31691,38380,93-1,63 208,31691,38380,93-1,63
|
|
|
|
|
|
|
|
Тетра-н-пропоксисилан 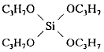 264,42241,4010,9161,661,48 264,42241,4010,9161,661,48
|
|
|
|
|
|
|
|
Тетра-н-бутоксисилан 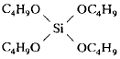 320,51151,41260,8992,001,61 320,51151,41260,8992,001,61
|
|
|
|
|
|
|
|
Тетра(2-метоксиэтокси)силан
 328,41791,42191,0794,9- 328,41791,42191,0794,9-
|
|
|
|
|
|
|
Таблица 2. Физические свойства некоторых органоалкоксисиланов [7].
|
Название
|
ММ
|
Ткип, 0С
|
d
|
µ
|
nD
|
|
Метилтриэтоксисилан MeSi(OEt)3
|
178.3
|
141
|
0,895
|
1,72
|
1,3832
|
|
Метилтриметоксисила MeSi(OMe)3
|
136,22
|
102
|
0,955
|
1,6
|
1,3696
|
|
Метилтри-н-пропоксисилан MeSi(n-OPr)3
|
220,4
|
83
|
0,88
|
-
|
-
|
|
Фенилтриметоксисилан PhSi(OEt)3
|
240,37
|
112
|
0,996
|
1,85
|
1,4718
|
|
Винилтриэтоксисилан 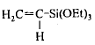 190,311600,9031,691,396 190,311600,9031,691,396
|
|
|
|
|
|
В качестве исходных реагентов для получения полиорганосилоксанов также
используют олигомеры. Klempeper и его сотрудники использовали такие олигомеры, как «молекулярные
строительные блоки» для получения молекул с точно контролируемой структурой
цепи [8;9]. В их исследованиях использовались такие соединения, как
гексаметоксидисилоксан (а), октаметокситрисилоксан (б) и кубический октамер.
а)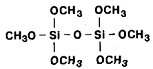 б)
б)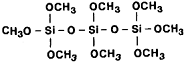
в)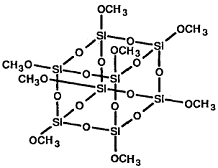
Октамер получали пользуясь реакциями в следующей последовательности [10]:
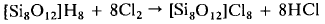 (11)
(11)
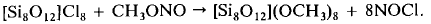 (12)
(12)
При выборе исходных мономеров, рассматривают стерические и индуктивные
характеристики алкокси- групп или органических заместителей, связанных с атомом
кремния, которые во многом определяют кинетику гидролиза и конденсации [6].
Олигомеры являются более подходящими в качестве исходных реагентов, когда
необходимо увеличить содержание кремнийорганики в растворе (например,
огнеупорных связующих) или когда требуется индивидуальная основа. Это является
перспективным при разработке неорганических силикатов с новыми свойствами.
1.1.2 Гидролиз
Реакция гидролиза проходит в результате нуклеофильной атаки атома
кислорода воды, на атом кремния о чем свидетельствуют «меченные» изотопы воды с
тетраэтоксисиланом, который образует только «непомеченный» этанол в щелочных и
кислых системах [11].
Si-OR + H18OH SI-OH18 + ROH (13)
Такое же поведение наблюдается в органоалкоксисиланах RxSi(OR)4-x, где х от 1 до 3 [12].
Тетраалкоксисиланы, органотриалкоксисиланы и диорганодиалкоксисиланы
гидролизуются под действием водяных паров [12]. Гидролиз облегчается в
присутствии гомогонизирующих растворителей (ацетона, этанола, ТГФ, диоксана и
др.). Следует подчеркнуть, что добавление спирта, как растворителя, может
способствовать реакциям этерификации (2) или деполимеризации (3).
1.1.2.1 Влияние катализатора
Гидролиз проходит наиболее быстро, когда используют катализаторы.
Минеральные кислоты и аммиак более широко используются в золь-гель технологии,
а также другие известные катализаторы уксусная кислота, KOH, KF, HF, амины и
оксиды. Многие авторы сообщают, что минеральные кислоты являются более
эффективными катализаторами, чем эквивалентные им концентрации оснований [12].
Однако, раньше не учитывались ни повышение кислотности силанольных групп
со степенью гидролиза и конденсации (кислые силанолов может нейтрализовать
основных катализаторов [13]), ни обратимость реакций (образование
негидролизованных мономеров).
McNeil
[10], Pohl и Osterholtz [14] изучали гидролиз
алкилтриалкоксисиланов в буферных водных растворах. В этих исследованиях не
рассматривались сложности связанные с pH, полимеризацией или системами вода - органический растворитель.
Полученные константы скорости указаны на графике зависимости от pH (Рис. 1). Гидролиз представляется
как специфический кислотный или специфический основный катализ.
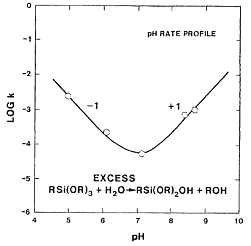
Рис. 3. Зависимость константы скорости гидролиза от pH среды [14].
Aclion
исследовал гидролиз тетраэтоксисилана в кислых и основных условиях в среде
различных растворителей: метанол, этанол, диоксан. Степень гидролиза
определялась путем отгонки этилового спирта относительно полисилоксана. Aelion и его сотрудники заметили, что
на скорость и степень реакции гидролиза наибольшее влияние оказывают сильные и
концентрированные кислоты и основания. Такие факторы, как температура и
растворитель имеют вторичное значение. Они обнаружили, что все сильные кислоты
ведут себя аналогично, в то время как слабым кислотам для достижения той же
степени прохождения реакции необходимо длительное время. С помощью графика
зависимости log константы скорости гидролиза от log [HCl], они пришли к выводу, что реакция характеризуется
первым порядком в присутствии концентрированной кислоты. Хотя общий кислотный
катализ не может быть полностью исключен, в механизмах реакции гидролиза с
участием ионов водорода подразумевается специфический кислотный катализ.
Как и в кислых условиях, гидролиз тетраэтоксисилана в основных является
функцией от концентрации катализатора [15]. Порядок реакции был определен
сравнением времени необходимым для завершения конкретной степени гидролиза. В
очень разбавленных растворах, был определен первый порядок гидролиза по NaOH. Однако когда концентрация
тетраэтоксисилана была увеличена, реакция больше не соответствовала простому
порядку, поскольку осложнялась вторичными реакциями. Слабые основания,
гидроксид аммония и пиридин оказывают заметное влияние на скорость реакции,
только если присутствуют в больших концентрациях. В основных условиях кинетика
гидролиза еще более сильно зависит от природы растворителя, чем в
кислотно-катализируемых.
Результаты влияния различных катализаторов на общие скорости гидролиза и
конденсации обобщены Pope и
Mackenzie для гидролиза тетраэтоксисилана в этаноле
(m = 4) [16]. Их результаты
перечисленные в таблице 5, не только показывают влияние ионов гидроксония и
гидроксильных ионов на время гель образования, но и результаты влияния
оснований, прежде всего F- (примерно такое же как OH-) и возможность увеличения координации кремния выше
четырех, например в R3SiF2- [17]. Многие закономерности HF катализа указывают на основной
катализ, что свидетельствует о роли OH-
и F-. Андрианов предполагает, что каталитическое влияние
предполагает протекание реакции через бимолекулярный нуклеофильный механизм (SN2 - Si), в котором происходит смешение OR-, атака нуклеофила F- на атом Si и последующий гидролиз Si-F связи [18]. Однако Curriu показывает, что первым шагом является обратимое образование
пятивалентного интермедиата, что ослабляет окружающие Si-OR связи [19].
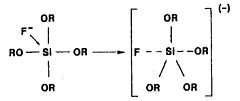
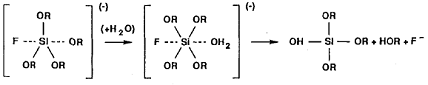 (14)
(14)
Как показывает Coltrain, уменьшение времени гелеобразования происходит в том случае, когда
используется уксусная кислота как катализатор в отличие от HCl, HNO3, H2SO4 и не является связанным с каталитическим действием
ацетат иона, но связана с понижением кислотности уксусной кислоты в этиловом
спирте [20]. На рис. 4а и 4б приводится зависимость времени гелеобразования от pH водных растворов используемых для
гидролиза и pH реагирующих золей (pH*). Когда сравнивают основные pH*, кривые совпадают и указывают на
отсутствие противоионов.
Таблица 3. Время гелеобразования и pH растворов ТЭОС с различными катализаторами [16].
|
Катализатор
|
Концентрация ТЭОС (моль)
|
pH среды
|
Время гелеобразования, ч
|
|
HF
|
0,05
|
1,90
|
12
|
|
HCl
|
0,05
|
0,05
|
92
|
|
HNO3
|
0,05
|
0,05
|
100
|
|
H2SO4
|
0,05
|
0,05
|
106
|
|
HOAc
|
0,05
|
3,70
|
72
|
|
NH4OH
|
0,05
|
9,95
|
107
|
|
Без катализатора
|
-
|
5,00
|
1000
|
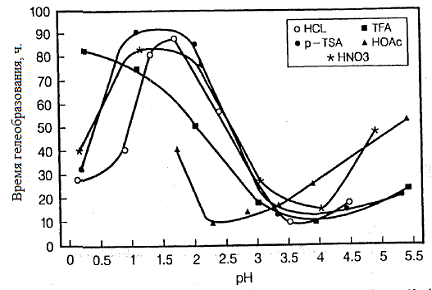
Рис. 4а. Зависимость времени гелеобразования от pH среды в гидролизе тетраэтоксисилана (m=4). p-TSA: пара-толуолсульфокислота, HOAc: уксусная кислота, TFA: трифторуксусная кислота [20].
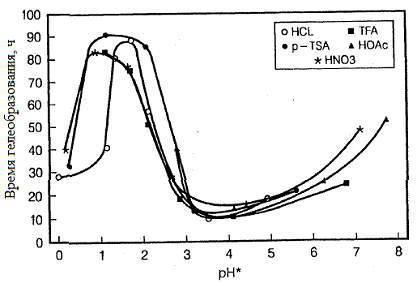
Рис. 4б. Зависимость времени гелеобразования от pH в гидролизе тетраэтоксисилана (m=4).. p-TSA: пара-толуолсульфокислота, HOAc: уксусная кислота, TFA: трифторуксусная кислота [20].
.1.2.2 Стерические и индукционные эффекты
Стерические факторы оказывают сильнейшее влияние на гидролитическую
стабильность органоалкоксисиланов [20]. Различные осложнения влияют на алкокси
группу и замедляет гидролиз, причем скорость гидролиза больше всего уменьшают
разветвленые алкокси группы. Aelion
наблюдал влияние алкильной цепи с различной длиной цепи и степенью разветвления
на гидролиз тетраалкоксисилана в присутствии кислоты. Результаты данных
иследований приведены в таблицах 4 и 5 [15].
Таблица 4. Константы скорости гидролиза тетраалкоксисиланов (RO)4Si в кислых условиях при 20 0С [15].
|
R
|
k*102 (моль-1с-1[H+]-1)
|
|
C2H5
|
5,1
|
|
C4H9
|
1,9
|
|
C6H13
|
0,83
|
|
(CH3)2CH(CH2)3CH(CH3)CH2
|
0,3
|
Таблица 5. Константы скорости k*102 (моль-1с-1[H+]-1) гидролиза алкоксиэтоксисиланов (RO)4-nSi(OC2H5)n при 20 0С [15].
|
n
|
R
|
|
C6H13
|
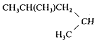 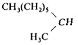 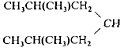
|
|
|
|
0
|
0,8
|
-
|
-
|
0,03
|
|
1
|
1,1
|
-
|
-
|
-
|
|
2
|
5,0
|
0,15
|
0,095
|
0,038
|
|
3
|
5,0
|
-
|
-
|
-
|
На рис. 5 сравниваются гидролиз тетраэтоксисилана и тетраметоксисилана в
кислых и щелочных условиях. Как видно из графика, замедляющие действие этокси
группы заметно проявляется.
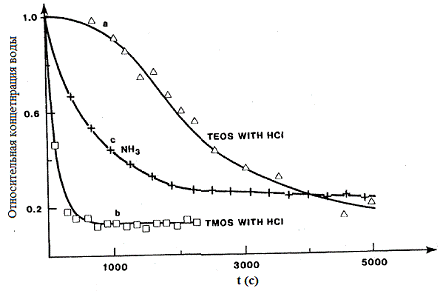
Рис. 5. Зависимость относительной концентрации воды от времени реакции
гидролиза [21].
В соответствии с Воронковым [12], в случае органоалкоксисиланов вида (RO)x(R’O)4-xSi, где R’O большая по
размеру алкокси группа, чем RO, и
если R’O линейной структуры, то замедление скорости гидролиза
проявляется только при х=0 или 1. Если R’O разветвленной
структуры, то его замедляющее действие проявляется даже при х=2.
С помощью ГЖХ проводили исследования гидролиза тетраэтоксисилана в
н-пропаноле, используя двух - основный кислотный и щелочной катализатор [22].
Данные исследования показали влияние замены этокси- группы на н-пропокси уже на
первом шаге гидролиза (в кислых условиях). Гидролиз н-пропокси групп протекал
намного медленнее, чем гидролиз этокси- групп и при щелочных и при кислых
условиях во втором шаге гидролиза. Данные результаты говорят о то что
замедляющие действие больших, линейных алкокси групп проявляется независимо от
степени замещения. Замена алкокси группы на алкильную группу увеличивает
электронную плотность на атоме кремния. Гидролиз (замена OR на OH) и конденсация (замена OR или OH на OSi) наоборот уменьшает электронную
плотность на атоме кремния. Замена алкокси группы на алкильную в первом случае,
гидрокси или OSi во втором, увеличивает стабильность
положительных или отрицательных зарядов в переходном состоянии, соответственно.
Индукционный эффект очень важен, поскольку улучшает кинетические характеристики
реакций с участием положительных и отрицательных зарядов в переходных
состояниях.
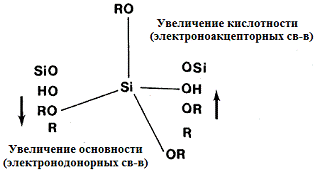
Рис. 6. Индуктивный эффект заместителей на атоме кремния (R, OR, OH, -OSi) [23].
Индуктивный эффект видно из исследований гидролиза метилэтоксисилана (CH3)x(C2H5O)4-xSi, где x = 0 до 3 [24]. На рис. 6 показано, что в кислых условиях (HCl) скорость гидролиза увеличивается с
увеличением х (электроно-донорных алкильных групп), в то время как в основных
условиях (NH3) четко прослеживается обратная тенденция. На рис. 7
показан эффект более быстрого замещения метокси группы, сравнивая гидролиз
тетраметоксисилана и тетраэтоксисилана. Ускорение или замедление гидролиза с
увеличением х в кислых или основных условиях, соответственно, предполагает что
механизм гидролиза чувствителен к индуктивному эффекту и видимо не зависит от
степени замещения алкильной группой. Так как увеличение стабильности
переходного состояния увеличивает скорость реакции, индуктивный эффект
свидетельствует о положительном и отрицательном зарядах переходного состояния в
кислых или основных условиях.
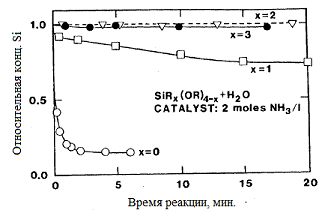
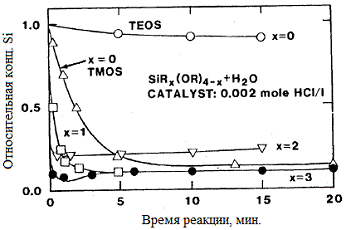
Рис. 7. Зависимость относительной конц. Si от времени реакции гидролиза различных алкоксисиланов в
этаноле (объемное отношение алкоксилана/этанол = 1:1) ● - (CH3)3SiOC2H5, ۷-
(CH3)2Si(OC2H5)2, □ - (CH3)Si(OC2H5)3, ○ - Si(OC2H5)4, ∆ - Si(OCH3)4[24].
Эти рассуждения приводят к гипотизе, что в кислых условиях скорость
гидролиза уменьшается с каждой последующей стадией гидролиза
(электроноакцепторной), в то время как в щелочных условиях увеличиваются
электроноакцепторные возможности OH, а
также (OSi) и ускоряется каждая последующая
стадия гидролиза.
Рассматривая с точки зрения органической химии, индуктивный эффект
органоалкоксисиланов RxSi(OR)4-x показывает, что использование
кислоты в качестве катализатора предпочтительнее, поскольку она является более
эффективной в случаях х > 0 [24].
1.1.2.3 Отношение H2О/Si (m)
Как говорилось ранее, гидролиз осуществляли при значениях m в диапазоне 1-25 в зависимости от
получения желаемых продуктов, например волокон, геля или коллоидных частиц. Из
уравнения 1 следует, что увеличение m способствует протеканию реакции гидролиза. Aelion и сотрудники определили для кислотно-катализируемого
гидролиза тетраэтоксисилана первый порядок реакции по Н2О и нулевой
порядок по воде в основных условиях. Это вероятно связано с образованием
силоксановой связи в результате гидролиза мономера и реакции перераспределения
(как изложено в пункте 1.3.5.). Pouxviel
и сотрудники [26] использовали ЯМР Si29 исследуя гидролиз тетраэтоксисилана в присутствии кислоты, как
катализатора, для трех систем в которых m m = 0.3 (недостаток воды), m =4 (стехиометрическое кол-во воды), m = 10 (избыток воды). На рис. 8 показаны изменение
концентрации мономера Q0 во времени при стехиометрическом
количестве и избытке воды. При увеличении значения r наиболее очевидным является ускорение реакции гидролиза. В
системе при m = 4, непрореагировавший мономер Q0 (0,4) остается даже после четырех часов с начала
гидролиза, но в случае когда m =
10, не остается непрореагированного мономера уже по прошествии одного часа.
Этот результат противоречит ранее полученным результатам в которых говорилось о
затормаживающем эффекте при увеличении отношения H2O/Si на скорость гидролиза в кислых
условиях [21].
Это так же видно сравнивая концентрации уже полностью прореагировавших
мономеров Q (4,0), что большее значение r обуславливает более полный гидролиз
мономера, перед его значительной конденсацией. В соответствии с уравнениями 2 и
3, различная степень гидролиза мономера влияет на относительные скорости ГМФК и
ГТФК. При m < 2 предпочтительнее продукты
реакции получаются по механизму ГТФК, а при m равном или больше 2 по ГМФК.


Рис 8. Графики изменения концентрации Q0 (x,y) - Si(OH)x(OEt)y
от времени гидролиза в присутствии кислоты: а) H2O/Si = 3.8, b) H2O/Si = 10 [26].
Хотя увеличение значения r в
целом способствует гидролизу, когда r увеличивается при постоянном соотношении растворитель/алкоксисилан, концентрация
алкоксисилана в смеси уменьшается. Это в свою очередь снижает скорость
гидролиза и конденсации, что собственно вызывает увеличение времени
гелеобразования. Данный эффект виден на рис. 8, где показано время
гелеобразования для тетраэтоксисилана в кислых условиях, как функция от
значения r и исходным молярным отношением
этанола к тетраэтоксисилану [27].
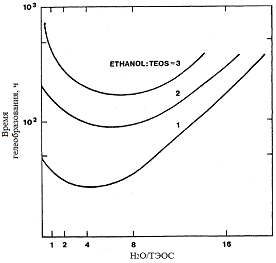
Рис 9. График зависимости времени гелеобразования от m (H2O/ТЭОС),
для трех систем с различным отношением этилового спирта к ТЭОС [27].
На рис. 9 показана диаграмма фазового равновесия тройной системы
тетраэтоксисилан - этанол - вода. Из нее видно, что большие значения r в системе жидкость-жидкость приводит
к несмешиваемости; однако как только образуется этанол, в качестве побочного
продукта реакций гидролиза и частичного гидролиза тетраэтоксисилана, это
приводит к гомогенности смеси. Вода является побочным продуктом реакции
конденсации (уравнение 3), большие значения r также может соответствовать гидролизу по силоксановой связи
(обратная уравнению 3).
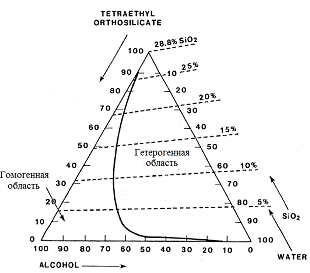
Рис.10. Трехфазовая диаграмма для системы
тетраэтоксисилан-вода-растворитель.
1.1.2.4 Âëèÿíèå ðàñòâîðèòåëÿ
Ðàñòâîðèòåëü
îáû÷íî äîáàâëÿþò
äëÿ ïðåäîòâðàùåíèÿ
ðàçäåëåíèÿ ñèñòåìû
íà ôàçû æèäêîñòü-æèäêîñòü
íà íà÷àëüíûõ
ýòàïàõ ðåàêöèè
ãèäðîëèçà è êîíòðîëÿ
çà êîíöåíòðàöèÿìè
àëêîêñèñèëàíà
è âîäû, ÷òî âëèÿåò
íà êèíåòèêó ãåëåîáðàçîâàíèÿ.
 ïîñëåäíåå âðåìÿ,
âëèÿíèå ðàñòâîðèòåëÿ
èçó÷àëîñü â ñâÿçè
«êîíòðîëÿ ñóøêè
õèìè÷åñêèõ äîáàâîê»
(DCAA), â êîòîðîé
èñïîëüçîâàëè
ýòàíîë è äðóãîé
ðàñòâîðèòåëü
äëÿ îáåñïå÷åíèÿ
âûñûõàíèÿ ìîíîëèòíîãî
ãåëÿ áåç òðåùèí
[28].
Ðàñòâîðèòåëè
ìîæíî êëàññèôèöèðîâàòü
êàê ïîëÿðíûå èëè
íå ïîëÿðíûå è ïðîòîííûå
è íå ïðîòîííûå.
Ïîëÿðíîñòü âî
ìíîãîì îïðåäåëÿåò
ñîëüâàòèðóþùèå
ñïîñîáíîñòè
ïîëÿðíûõ è íå ïîëÿðíûõ
ðàñòâîðèòåëåé.
Áîëåå ïîëÿðíûå
ðàñòâîðèòåëè
(âîäà, ýòàíîë, ôîðìàìèä
è ò.ä.) èñïîëüçóþò
äëÿ ðàñòâîðåíèÿ
ïîëÿðíûõ òåòðààëêîêñèñèëàíîâ,
êîòîðûå èñïîëüçóþòñÿ
â çîëü-ãåëü òåõíîëîãèè.
Ìåíåå ïîëÿðíûå
ðàñòâîðèòåëè
òàêèå êàê äèîêñàí
èëè òåòðàãèäðîôóðàí
èñïîëüçóþòñÿ
äëÿ îðãàíîàëêîêñèñèëàíîâ
èëè ñèëàíîëîâ.
Ïðîñòûå ýôèðû
ñïèðòîâ, òàêèå
êàê ìåòîêñèýòàíîë
è ýòîêñèýòàíîë
ïðîÿëâÿþò êàê
ïîëÿðíûå òàê è
íå ïîëÿðíûå õàðàêòåðèñòèêè
è ïðèìåíÿþòñÿ
â ñëó÷àÿõ ñ ïîëÿðíûìè
è íå ïîëÿðíûìè
ðåàãåíòàìè ïðèñóòñòâóþùèõ
â ðàñòâîðàõ. Äèïîëüíûé
ìîìåíò ðàñòâîðèòåëÿ
îïðåäåëÿåò ðàññòîÿíèå,
íà êîòîðîì çàðÿä
îäíîãî âèäà ìîæåò
«îùóùàòüñÿ» îêðóæàþùèìè
âèäàìè. ×åì ìåíüøå
äèïîëüíûé ìîìåíò,
òåì áîëüøå ýòà
äëèíà ñòàíîâèòüñÿ.
Ýòî âàæíî â ýëåêòðîñòàòè÷åñêîé
ñòàáèëüíîñòè
ñèñòåì (ýëåêòðîñòàòè÷åñêàÿ
ñòàáèëüíîñòü
áîëåå ýôôåêòèâíà
â ñèñòåìàõ ñ
ìàëåíüêèì äèïîëüíûì
ìîìåíòîì) è êîãäà
ó÷èòûâàåòñÿ
ðàññòîÿíèå íà
êîòîðîì íàõîäÿòñÿ
çàðÿæåííûå êàòàëèòè÷åñêèå
÷àñòèöû, íàïðèìåð
OH- íóêëåîôèë
è H3O+ ýëåêòðîôèë,
ïðèòÿãèâàþùèåñÿ
èëè îòòàëêèâàþùèåñÿ
îò ïîòåíöèàëüíûõ
ðåàêöèîííûõ
öåíòðîâ â çàâèñèìîñòè
îò èõ çàðÿäà
[29].
Íàëè÷èå ëàáèëüíûõ
ôîòîíîâ îïðåäåëÿåò
áóäóò ëè àíèîíû
èëè êàòèîíû ñîëüâàòèðîâàòüñÿ
ñèëüíåå áëàãîäàðÿ
âîäîðîäíûì ñâÿçÿì.
Ãèäðîëèç ÿâëÿåòñÿ
êàòàëèçèðóåìûì
ïðîöåññîì ëþáûì
ãèäðîêñèëüíûì
èîíîì (pH>7) èëè èîíîì
ãèäðîêñîíèÿ
(pH<7). Ìîëåêóëû
ðàñòâîðèòåëÿ
ó êîòîðûõ èìåþòñÿ
âîäîðîäíûå ñâÿçè
ãèäðîêñèëüíîãî
èîíà èëè èîíà
ãèäðîêñîíèÿ ñíèæàþò
êàòàëèòè÷åñêóþ
àêòèâíîñòü â
ùåëî÷íûõ èëè
êèñëûõ óñëîâèÿõ,
ñîîòâåòñòâåííî.
Òàêèì îáðàçîì,
àïðîòîííûå ðàñòâîðèòåëè
ó êîòîðûõ íå îáðàçóþò
âîäîðîäíûõ ñâÿçåé
ñ ãèäðîêñèë èîíîì
ñïîñîáñòâóþò
ñîçäàíèþ ãèäðîêñèë
èîíà áîëåå íóêëåîôèëüíîãî,
â òî âðåìÿ êàê
ïðîòîííûé ðàñòâîðèòåëü
ñîçäàåò èîí ãèäðîêñîíèÿ
áîëåå ýëåêòðîôèëüíûé.
Âîäîðîäíàÿ ñâÿçü
òàê æå ìîæåò âëèÿòü
íà ìåõàíèçì
ñàìîãî ãèäðîëèçà.
Íàïðèìåð, âîäîðîäíûå
ñâÿçè ñïîñîáíû
àêòèâèðîâàòü
ñëàáûå óõîäÿùèå
ãðóïïû îñóùåñòâëÿÿ
áèìîëåêóëÿðíûé,
íóêëåîôèëüíûé
(SN2-Si) ìåõàíèçì
ðåàêöèè.
Íàëè÷èå íåóñòîé÷èâûõ
ïðîòîíîâ òàêæå
âëèÿåò íà ñòåïåíü
îáðàòíûõ ðåàêöèé
(óðàâíåíèÿ 1-3). Àïðîòîííûå
ðàñòâîðèòåëè
íå ó÷àñòâóþò
â îáðàòíûõ ðåàêöèÿõ
òàêèõ êàê ýòåðèôèêàöèÿ
(óðàâíåíèå 1) èëè
ãèäðîëèç (óðàâíåíèå
3), ïîñêîëüêó îòñóòñòâóþò
ýëåêòðîôèëüíûå
ïðîòîíû è íå ïðîèñõîäèò
äåïðîòîíèðîâàíèå
äëÿ ôîðìèðîâàíèÿ
äîñòàòî÷íî ñèëüíûõ
íóêëåîôèëîâ
(íàïðèìåð OH- è OR-)
íåîáõîäèìûõ
äëÿ òàêèõ ðåàêöèé
êàê:
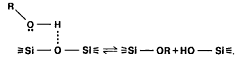 (15)
(15)
Ïîýòîìó ñðàâíèâàÿ
ñ ýòàíîëîì èëè
âîäîé, àïðîòîííûå
ðàñòâîðèòåëè
òàêèå êàê äèîêñàí,
ÒÃÔ ÿâëÿþòñÿ çíà÷èòåëüíî
áîëåå èíåðòíûìè
(ò.å. îíè íå ïðèíèìàþò
ó÷àñòèå â ðåàêöèÿõ
çîëü-ãåëü îáðàçîâàíèÿ),
õîòÿ êàê ãîâîðèëîñü
ðàíåå, îíè ñïîñîáíû
âëèÿòü íà êèíåòèêó
ðåàêöèé, óâåëè÷èâàÿ
ñèëó íóêëåîôèëîâ
èëè ñíèæàÿ ñèëó
ýëåêòðîôèëîâ.
1.2.5.Ìåõàíèçì
ãèäðîëèçà
 ïðåäûäóùèõ
ðàçäåëàõ áûëî
ðàññìîòðåí ãèäðîëèç
òåòðààëêîêñè-
è îðãàíîàëêîêñèñèëàíîâ,
âëèÿíèå ñòåðè÷åñêèõ
è èíäóêòèâíõ
ýôôåêòîâ, à òàêæå
âëèÿíèå êàòàëèòè÷åñêèõ
êèñëîò (H3O+) è îñíîâàíèé
(OH-). Ïîðÿäîê ðåàêöèè
ïî îòíîøåíèþ
ê âîäå è ìîíîìåðó
íàáëþäàåòñÿ
2 è 1, â èòîãå òðåòèì
è âòîðûì ïîðÿäêîì
îáùåé êèíåòèêè,
ñîîòâåòñòâåííî.
Îñíîâûâàÿñü
íà ýòèõ ôàêòîðàõ,
ýòî â öåëîì äîêàçûâàåò,
÷òî ãèäðîëèç
ïðîòåêàåò ïî ðåàêöèè
áèìîëåêóëÿðíîãî
íóêëåîôèëüíîãî
çàìåùåíèÿ (SN2-Si) ñ ó÷àñòèåì
ïÿòèêîðäèíàöèîííîãî
èíòåðìåäèàòà
èëè ïåðåõîäíîãî
ñîñòîÿíèÿ, õîòÿ
ïî àíàëîãèè ñ
îðãàíè÷åñêîé
õèìèåé èîíû Si(OR)3+ áûëè ïðåäëîæåíû
â êà÷åñòâå âîçìîæíûõ
èíòåðìåäèàòîâ
[24].
1.2.5.1 Ãèäðîëèç
â ïðèñóòñòâèè
êèñëîòû, êàê êàòàëèçàòîðà
 êèñëûõ óñëîâèÿõ,
âïîëíå âåðîÿòíî,
÷òî àëêîêñè ãðóïïà
ïðîòîíèðóåòñÿ
íà ïåðâîé ñòàäèè
(ïðîòåêàåò áûñòðî).
Ýëåêòðîííàÿ ïëîòíîñòü
ïîëó÷àåòñÿ ñíÿòîé
ñ àòîìà êðåìíèÿ,
äåëàÿ åãî áîëåå
ýëåêòðîôèëüíûì
è ñëåäîâàòåëüíî
áîëåå âîñïðèèì÷èâûì
ê àòàêå âîäîé.
Pohl è Osterholtz îòäàâàëè ïðåäïî÷òåíèå
ïåðåõîäíûì ñîñòîÿíèÿì
ñî çíà÷èòåëüíûìè
õàðàêòåðèñòèêàìè
SN2 òèïîâ
[14]. Ìîëåêóëà âîäû
àòàêóÿ ñ òûëà
àòîì êðåìíèÿ,
ïðèîáðåòàåò ÷àñòè÷íûé
ïîëîæèòåëüíûé
çàðÿä. Ýòîò çàðÿä
ïðîòîíèðóÿ àëêîêñèä
ñîîòâåòñòâåííî
óìåíüøàåòñÿ,
îáðàçóåòñÿ ñïèðò
êàê áîëåå õîðîøàÿ
óõîäÿùàÿ ãðóïïà.
Ïðè ðàçðóøåíèè
ïåðåõîäíîãî ñîñòîÿíèÿ
âûäåëÿåòñÿ ñïèðò
è ïðîèñõîäèò
ïåðåñòðîéêà òåòðàýäðà:
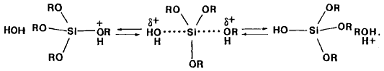 (16)
(16)
 ñîîòâåòñòâèè
ñ ýòèì ìåõàíèçìîì,
ñêîðîñòü ãèäðîëèçà
óâåëè÷èâàþò
çàìåñòèòåëè
ñ ìåíüøèìè ñòåðè÷åñêèìè
çàòðóäíåíèÿìè
íà àòîìå êðåìíèÿ.
Ýëåêòðîíîäîíîðíûå
çàìåñòèòåëè
(ò.å. àëêèëüíûå
ãðóïïû), ÷òî ïîìîãàþò
ñòàáèëèçàöèè
ïîëîæèòåëüíîãî
çàðÿäà, ñïîñîáñòâóþ
óâåëè÷åíèþ ñêîðîñòè
ãèäðîëèçà (ðèñ.
7), íî â ìåíüøåé
ñòåïåíè, ïîòîìó
÷òî àòîì êðåìíèÿ
ïðèîáðåòàåò ìàëåíüêèé
çàðÿä â ïåðåõîäíîì
ñîñòîÿíèè.
Èñïîëüçóÿ îïòè÷åñêè
àêòèâíûå ìîíîìåðû
RxSi(OR)4-x,Sommer è åãî ñîòðóäíèêè
äîêàçàëè ÷òî
îáðàùåíèå êîíôèãóðàöèè
ïðîèñõîäèò âî
âðåìÿ ãèäðîëèçà
íåñêîëüêèõ ìîíîìåðîâ
â òîì ÷èñëå R3Si(OCH3). Êàê ïðàâèëî,
îáðàùåíèå êîíôèãóðàöèè
âñòðå÷àåòñÿ
â îáùèõ ðåàêöèÿõ
çàìåùåíèÿ ñ õîðîøî
óõîäÿùèìè ãðóïïàìè
òàêèìè êàê Cl- è OCOR-,
÷üè ñîïðÿæåííûå
êèñëîòû (ñîîòâåòñòâóþò
ïðîòîíèðîâàíûì
àíèîíàì) èìåþò
pKa<6 íåçàâèñèìî
îò ïðèðîäû ðàñòâîðèòåëÿ
ïðè óñëîâèè, ÷òî
àòàêóÿ ðåàãåíò
ââîäèò ãðóïïó
áîëåå îñíîâíóþ,
÷åì óõîäÿùàÿ
ãðóïïà [32]. Äëÿ «áåäíûõ»
óõîäÿùèõ ãðóïï
òàêèõ êàê H èëè OR, ñîïðÿæåííûå
êèñëîòû êîòîðûõ
èìåþò pKa>6, ñîõðàíåíèå
èëè ïåðåñòðîéêà
òåòðàýäðà ìîæåò
ïðîèñõîäèòü â
çàâèñèìîñòè
îò ïðèðîäû êàòàëèòè÷åñêîãî
êàòèîíà è ïîëÿðíîãî
ðàñòâîðèòåëÿ.
Íàïðèìåð, âîäîðîäíàÿ
ñâÿçü ðàñòâîðèòåëÿ
ìîæåò ñïîñîáñòâîâàòü
ïåðåñòðîéêå ïóòåì
àêòèâàöèè «áåäíûõ»
óõîäÿùèõ ãðóïï
[12].
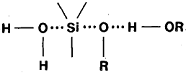 (17)
(17)
Klemperer è
ñîòðóäíèêè, ïîêàçàëè
÷òî â íåéòðàëüíûõ
óñëîâèÿõ îëèãîìåðû
(êóáè÷åñêîãî
îêòàìåðà) ãèäðîëèçóþòñÿ
áåç ïåðåñòðîéêè
[8]. Ýòî ïðåäïîëàãàåò,
÷òî ñîõðàíåíèå
èëè ïåðåñòðîéêà
òåòðàýäðà äàëüøå
âëèÿåò íà ñïåöèôè÷åñêèå
êîíôèãóðàöèîííûå
ñâÿçè.
Íåêîòîðûå èññëåäîâàòåëè
ïðåäïîëîæèëè
ìåõàíèçì ãèäðîëèçà
ñ ó÷àñòèåì àòàêè
ñáîêó íà àòîì
êðåìíèÿ áåç ïåðåñòðîéêè
òåòðàýäðà [13;32]. Âîçìîæíûé
ìåõàíèçì êàòàëèçà
â êèñëûõ óñëîâèÿõ
ÿâëÿåòñÿ ñëåäóþùèì:
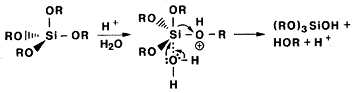 (18)
(18)
Ýòîò ìåõàíèçì
ÿâëÿåòñÿ ñâÿçüþ
ñòåðè÷åñêîãî
è èíäóêòèâíîãî
ýôôåêòà. Ñðàâíèâàÿ
SN2 ìåõàíèçìû
îïèñàííûå âûøå,
ýëåêòðîíîäîíîðíûå
çàìåñòèòåëè
äîëæíû îêàçûâàòü
áîëüøåå âëèÿíèå,
ïîòîìó ÷òî àòîì
êðåìíèÿ ïðèîáðåòàåò
áîëüøèé çàðÿä
â ïåðåõîäíîì ñîñòîÿíèè.
Òèììñ ïðåäëîæèë
ìåõàíèçì êèñëîòíî-êàòàëèçèðóåìîãî
ãèäðîëèçà ñ ó÷àñòèåì
èîíà êðåìíèÿ
(Si+) [34]. Çà áûñòðûì
ïðîòîíèðîâàíèåì
àëêîêñè ãðóïïû,
ñëåäóåò ìåäëåííàÿ
ñòàäèÿ, â êîòîðîé
èîí êðåìíèÿ ôîðìèðóåò
óõîäÿùèé ñïèðò:
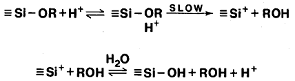 (19)
(19)
Âîäà ðåàãèðóåò
ñ èîíîì êðåìíèÿ,
îáðàçóÿ ñèëàíîë
è ôîòîí ðåãåíåðèðóåòñÿ.
Ýòà ðåàêöèÿ õàðàêòåðèçóåòñÿ
òðåòèì ïîðÿäêîì
è óñêîðÿåò àòàêó
ýëåêòðîíîäîíîðíîãî
çàìåñòèòåëÿ
íà àòîì êðåìíèÿ
(ðèñ. 7).
1.2.5.2 Ãèäðîëèç
â ïðèñóòñòâèè
ùåëî÷è, êàê êàòàëèçàòîðà
 îñíîâíûõ óñëîâèÿõ,
âåðîÿòíî, ÷òî
âîäà áûñòðî äèññîöèèðóåò
íà íóêëåîôèëüíûå
ãèäðîêñèëüíûå
àíèîíû óæå íà
ïåðâîé ñòàäèè.
Ïîñëå ÷åãî ãèäðîêñèëüíûé
àíèîí àòàêóåò
àòîì êðåìíèÿ.
Her [33] è Keefer [13] ïðåäëîæèëè
SN2-Si ìåõàíèçì
â êîòîðîì OH- âûòåñíÿåò
OR- ñ ó÷àñòèåì
òåòðàýäðà êðåìíèÿ.
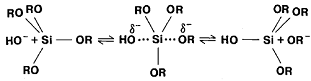 (20)
(20)
Êàê ãîâîðèëîñü
ðàíåå íà ìåõàíèçì
ãèäðîëèçà â ïðèñóòñòâèè
êèñëîòû âëèÿþò
ñòåðè÷åñêèå
è èíäóêòèâíûå
ôàêòîðû, îäíàêî
ñòåðè÷åñêèå
ôàêòîðû èãðàþò
áîëåå âàæíóþ
ðîëü, ïîñêîëüêó
àòîì êðåìíèÿ
ïðèîáðåòàåò ìàëåíüêèé
çàðÿä â ïåðåõîäíîì
ñîñòîÿíèè. Pohl è Osterholtz ðàññìàòðèâàëè,
êàê SN2**-Si òàê è SN2*-Si ìåõàíèçìû
ñ ó÷àñòèåì ñòàáèëüíîãî
ïÿòè-êîîðäèíàöèîííîãî
èíòåðìåäèàòà
[14]. Èíòðåìåäèàò
ðàñïàäàåòñÿ,
ïðîéäÿ âòîðîå
ïåðåõîäíîå ñîñòîÿíèå
â êîòîðîì ëþáîé
îêðóæàþùèé ëèãàíä
ìîæåò ïîëó÷èòü
÷àñòè÷íûé îòðèöàòåëüíûé
çàðÿä:
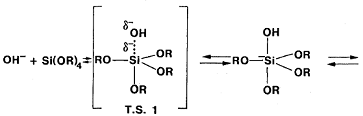
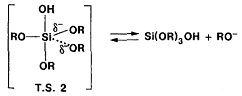 (21)
(21)
Ãèäðîëèç ïðîèñõîäèò
òîëüêî âûòåñíåíèåì
àëêîêñè àíèîíà,
êîòîðîìó îêàçûâàþò
ïîìîùü âîäîðîäíûå
ñâÿçè àëêîêñè
àíèîíà íà ðàñòâîðèòåëå
(óðàâíåíèå 17).
Àòîì êðåìíèÿ
ïðèîáðåòàåò îòðèöàòåëüíûé
çàðÿä â ïåðåõîäíîì
ñîñòîÿíèè, SN2**-Si èëè SN2*-Si ìåõàíèçìû
îðèåíòèðóåò
÷óâñòâèòåëüíîñòü
ê èíäóêòèâíîìó
è ñòåðè÷åñêîìó
ýôôåêòàì. Ýëåêòðîíîàêöåïòîðíûå
çàìåñòèòåëè
òàêèå êàê -OH èëè -OSi ïîìîãàþò ñòàáèëèçàöèè
îòðèöàòåëüíîãî
çàðÿäà íà àòîìå
êðåìíèÿ, ÷òî âûçûâàåò
óâåëè÷åíèå ñêîðîñòè
ãèäðîëèçà ñî
ñòåïåíüþ OH çàìåí, â òî
âðåìÿ êàê ýëåêòðîíîäîíîðíûå
çàìåñòèòåëè
óìåíüøàþò ñêîðîñòü
ãèäðîëèçà (ðèñ.
9). Òàê êàê îáðàùåíèå
êîíôèãóðàöèè
ÿâëÿåòñÿ íå ïîëíîé
(óðàâíåíèå 21), ñêîðîñòü
ãèäðîëèçà ìîæåò
óâåëè÷èâàòüñÿ
ñî ñòåïåíüþ êîíäåíñàöèè.
Êèíåòèêà ãèäðîëèçà
ïðåäïîëàãàåòñÿ
èìååò ïåðâûé
ïîðÿäîê ïî [OH-] è âòîðîé ïîðÿäîê
ïî âîäå è ïîëèñèëèêàòó
(òðåòèé ïîðÿäîê
îáùåé êèíåòèêè)
äëÿ âñåõ òðåõ ìåõàíèçìîâ,
SN2*-Si, SN2**-Si è SN2*-Si. Ïîýòîìó,
â öåëîì íå ïðåäñòàâëÿåòñÿ
âîçìîæíûì ïðîâåñòè
ðàçëè÷èå ìåæäó
ýòèìè ìåõàíèçìàìè
ïî ïîðÿäêó ðåàêöèè.
.1.2.6 Îáðàòèìîñòü
ðåàêöèè ãèäðîëèçà
Ðåàêöèÿ ãèäðîëèçà
(óðàâíåíèå 1) ìîæåò
ïðîòåêàòü â îáðàòíîì
íàïðàâëåíèè,
â êîòîðîé ñïèðò
ìîæåò âûòåñíÿòü
ãèäðîêñèëüíóþ
ãðóïïó îáðàçóÿ
àëêîêñèñèëàí
è âîäó. Ýòîò îáðàòíûé
ïðîöåññ (ýòåðèôèêàöèÿ)
ïðåäïîëîæèòåëüíî
ïðîèñõîäèò ÷åðåç
ìåõàíèçì àíàëîãè÷íûé
ïðÿìûì ðåàêöèÿì,
ò.å. ðåàêöèþ áèìîëåêóëÿðíîãî
íóêëåîôèëüíîãî
çàìåùåíèÿ: SN2-Si, SN2**-Si èëè SN2*-Si, SN2**-Si. Ïî óðàâíåíèþ
22 ïîêàçàí ìåõàíèçì
ðåàêöèè ýòåðèôèêàöèè
â êèñëûõ óñëîâèÿõ:
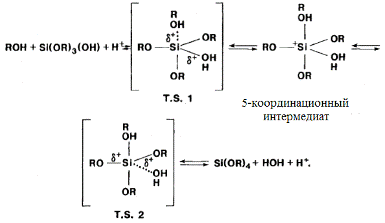 (22)
(22)
Âîðîíêîâ, îäíàêî,
ïðåäïîëàãàåò
ôîðìèðîâàíèå
àêòèâíîãî øåñòè÷ëåííîãî
ïåðåõîäíîãî êîìïëåêñà,
êîòîðûé ñîäåðæèò
äâå ìîëåêóëû ñïèðòà
[12].
Íàáëþäåíèÿ çà
ðåàêöèåé ýòåðèôèêàöèè
ïîêàçûâàþò, ÷òî
îíà ïðîõîäèò
áîëåå ãëóáîêî
â êèñëûõ óñëîâèÿõ
[3;22]. Ýòî ïðèâåëî Keefer’à ê ñëåäóþùåìó
çàêëþ÷åíèþ, ÷òî
îñíîâíî-êàòàëèòè÷åñêèé
ìåõàíèçì âêëþ÷àåò
â ñåáÿ ïåðåñòðîéêó
êîíôèãóðàöèè,
êîòîðàÿ ïðè êèñëîòíîì
êàòàëèçå íå ïðîèñõîäèò
[13]. Âåðîÿòíî, ÷òî
ðåàêöèÿ ýòåðèôèêàöèè
õàðàêòåðèçóåòñÿ
ïåðâûì ïîðÿäêîì
ïðè êèñëûõ óñëîâèÿõ,
ñ ó÷àñòèåì ïðîòîíèðîâàíûõ
ñèëàíîëüíûõ
ãðóïï; â òî âðåìÿ
êàê ïðè îñíîâíûõ
óñëîâèÿõ, õàðàêòåðèçóåòñÿ
ïåðâûì ïîðÿäêîì
ñ ó÷àñòèåì äåïðîòîíèðîâàíîãî
ñïèðòà è îáðàçîâàíèåì
íóêëåîôèëà OR-. Ïîýòîìó
ñêëîííîñòü ê
ýòåðèôèêàöèè
íàèáîëåå íàáëþäàåòñÿ
â êèñëûõ óñëîâèÿõ,
÷òî òàê æå ìîæåò
áûòü âûçâàíî
ëåãêîñòüþ ïðîòîíèðîâàíèÿ
ñèëàíîëüíîé
ãðóïïû (ïðè pH 1-3).
Keefer ðàññ÷èòàë
êîëè÷åñòâî ñèëàíîëà,
âñòóïèâøåãî
â ðåàêöèþ ýòåðèôèêàöèè
äëÿ íåñêîëüêèõ
ãåëü-îáðàçóþùèõ
óñëîâèé è ñòåïåíè
êîíäåíñàöèè
[13]. Â ñîîòâåòñòâèè
ñ ýòèìè ðàñ÷åòàìè,
ãèäðîëèç ìîã
ëåãêî èäòè ê çàâåðøåíèþ
ñ íåáîëüøèì èçáûòêîì
âîäû â êèñëûõ
óñëîâèÿõ, íî âûñóøåííûé
ãåëü áûë ñóùåñòâåííî
ýòåðèôèöèðîâàí
[3;22].
Ðåàêöèÿ ïåðåýòåðèôèêàöèè
- ýòî ðåàêöèÿ, â
êîòîðîé ñïèðò
âûòåñíÿåò àëêîêñè
ãðóïïó è îáðàçóåòñÿ
íîâûé ñïèðò:
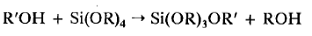 (23)
(23)
Ýòà ðåàêöèÿ øèðîêî
èçó÷àëàñü, ïîñêîëüêó
ÿâëÿåòñÿ îáùèì
ìåòîäîì ïîëó÷åíèÿ
ðàçëè÷íûõ ïîëèàëêîêñèñèëàíîâ
[36].
 çîëü-ãåëü òåõíîëîãèè
ïåðåýòåðèôèêàöèÿ
ïðîèñõîäèò ïðè
ãèäðîëèçå àëêîêñèñèëàíîâ
â ñïèðòîâûõ ñðåäàõ
ñ ðàçëè÷íûìè
àëêîêñè ãðóïïàìè.
Íàïðèìåð, Brinker íàáëþäàë
ñóùåñòâåííûé
îáìåí àëêîêñè
ãðóïï âî âðåìÿ
êèñëîòíî-êàòàëèçèðóåìîãî
ãèäðîëèçà òåòðàýòîêñèñèëàíà
â í-ïðîïàíîëå
[22]. Ïåðåýòåðèôèêàöèÿ
òàê æå èãðàåò
âàæíóþ ðîëü â ìíîãîêîìïîíåíòíûõ
ñèñòåìàõ, â êîòîðûõ
èñïîëüçóåòñÿ
íåñêîëüêî àëêîêñèñèëàíîâ
ñ ðàçëè÷íûìè
àëêîêñè ãðóïïàìè.
Ïîñëå ïðîõîæäåíèÿ
ðåàêöèé ïåðåýòåðèôèêàöèè
ïðîèñõîäèò ïîñëåäóþùèé
ãèäðîëèç, êèíåòèêà
êîòîðîãî çàâèñèò
îò ñòåðè÷åñêèõ
è èíäóêöèîííûõ
õàðàêòåðèñòèê
ïðèøåäøåé àëêîêñè
ãðóïïû. Ýòî ãîâîðèò
î òîì, ÷òî ïåðåýòåðèôèêàöèÿ
ïðîòåêàåò ïî ðåàêöèè
íóêëåîôèëüíîãî
çàìåùåíèÿ àíàëîãè÷íî
ýòåðèôèêàöèè.
Èç òàáëèöû 8 âèäíî,
÷òî ñòåïåíü ðåàêöèè
ïåðåýòåðèôèêàöèè
ðåçêî ñíèçèëàñü,
êîãäà èñïîëüçîâàëèñü
ãðîìîçäêèå âòîðè÷íûå
è òðåòè÷íûå ñïèðòû.
Èç èññëåäîâàíèé
îïòè÷åñêè àêòèâíûõ
êðåìíèéîðãàíè÷åñêèõ
ñîåäèíåíèé áûëî
óñòàíîâëåíî,
÷òî ïåðåýòåðèôèêàöèÿ
ìîæåò ïðîòåêàòü
ñ ñîõðàíåíèåì
èëè èçìåíåíèåì
êîíôèãóðàöèè
â çàâèñèìîñòè
îò ïðèðîäû óõîäÿùèõ
ãðóïï, ðàñòâîðèòåëÿ
è êàòàëèçàòîðà.
Ïîñêîëüêó àëêîêñè
çàìåñòèòåëè
ÿâëÿþòñÿ ïëîõèìè
óõîäÿùèìè ãðóïïàìè,
Âîðîíêîâ ïðåäëîæèë,
÷òî òîëüêî â î÷åíü
ïîëÿðíûõ ðàñòâîðèòåëÿõ
ìîæåò ïðîèñõîäèòü
äîñòàòî÷íîå
ðàçäåëåíèå çàðÿäà
â ïåðåõîäíîì ñîñòîÿíèè
ðåàëèçóþùèéñÿ
ïî SN2-Si ìåõàíèçìó,
êîòîðûé ïðîòåêàåò
ñ èçìåíåíèåì
êîíôèãóðàöèè.
 ìåíåå ïîëÿðíûõ
ðàñòâîðèòåëÿõ,
êàê ïðàâèëî, íàáëþäàåòñÿ
ñîõðàíåíèå êîíôèãóðàöèè.
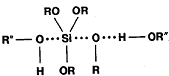 (24)
(24)
Òàáëèöà 8. Ñòåïåíü
ðåàêöèé ãèäðîëèçà
è ýòåðèôèêàöèè
â êèñëûõ óñëîâèÿõ,
ïðè ãèäðîëèçå
òåòðàýòîêñèñèëàíà
â ðàçëè÷íûõ ðàñòâîðèòåëÿõ.
|
Ðàñòâîðèòåëü
|
Ãèäðîëèç
(%)
|
Ýòåðèôèêàöèÿ
(%)
|
|
Ìåòèëîâûé
ñïèðò
|
76
|
44,7
|
|
Èçîïðîïèëîâûé
ñïèðò
|
63
|
35,2
|
|
Òðåò-áóòèëîâûé
ñïèðò
|
67
|
0
|
.1.3. Ðåàêöèè êîíäåíñàöèè
ïðîäóêòîâ ãèäðîëèçà.Êàê
ðàññìàòðèâàëîñü
ðàíüøå, îáðàçîâàíèå
ñèëîêñàíîâîé
ñâÿçè ïðîèñõîäèò
ñ ïîìîùüþ ðåàêöèè
ÃÒÔÊ (2) èëè ÃÌÔÊ
(3). Engelhardt è åãî ñîòðóäíèêè
[37] èñïîëüçîâàëè
ßÌÐ Si29 â èññëåäîâàíèÿõ
êîíäåíñàöèè
ñèëîêñàíîëîâ
ïðè âûñîêèõ çíà÷åíèÿõ
pH. Èõ ðåçóëüòàòû
ïîêàçûâàþò, ÷òî
òèïè÷íîé ïîñëåäîâàòåëüíîñòüþ
ïðîäóêòîâ ÿâëÿåòñÿ
ìîíîìåð, äèìåð,
ëèíåéíûé è öèêëè÷åñêèé
òðèììåð, öèêëè÷åñêèé
òåòðàìåð è âûñøèå
öèêëû.
.1.3.1 Ìåõàíèçì ðåàêöèé
êîíäåíñàöèè
Íàèáîëåå îáøèðíîå
èçó÷åíèå ÃÌÔÊ
R2Si(OH)2 â âîäíî-îðãàíè÷åñêèõ
ñðåäàõ ïðîâåäåíî
íà íàøåé êàôåäðå
[77], à òàê æå ïîëüñêèìè
ó÷åíûìè [38]. Îòìå÷àåòñÿ,
÷òî ïðîöåññ ïîëèêîíäåíñàöèè
äèîðãàíîñèëàíäèîëîâ
ÿâëÿåòñÿ êèíåòè÷åñêè
ñëîæíûì ïðîöåññîì
èç-çà áîëüøèõ
ðàçëè÷èé â ðåàêöèîííîé
ñïîñîáíîñòè
ìîíîìåðà è îáðàçóþùèõñÿ
îëèãîìåðîâ, èç-çà
ïðîòåêàíèÿ ïîáî÷íûõ
ïðîöåññîâ èõ öèêëèçàöèè.
 ñëó÷àå ÃÌÔÊ
â ñðåäå îðãàíè÷åñêèõ
ñïèðòîâ ïðîöåññ
îñëîæíÿåòñÿ ðåàêöèÿìè
ýòåðèôèêàöèè
R2Si(OH)2 è àëêîãîëèçà
îëèãîñèëîêñàíîâ.
Êðîìå òîãî, â õîäå
êîíäåíñàöèè
èçìåíÿþòñÿ ñâîéñòâà
ñðåäû âñëåäñòâèå
óìåíüøåíèÿ êîíöåíòðàöèè
ïîëÿðíûõ ìîëåêóë
ìîíîìåðà è óâåëè÷åíèÿ
êîíöåíòðàöèè
ïîëÿðíûõ ìîëåêóë
âîäû [39]. Âûøå óêàçàííûå
ïîáî÷íûå ïðîöåññû
òàêæå ÿâèëèñü
ïðè÷èíîé òîãî,
÷òî îñíîâíûå
êèíåòè÷åñêèå
ïàðàìåòðû ÃÌÔÊ
îïðåäåëÿëèñü ïî
êèíåòè÷åñêèì
êðèâûì äî 15-25% êîíâåðñèè
ìîíîìåðà.
.1.3.1.1 Êîíäåíñàöèÿ
â îñíîâíûõ óñëîâèÿõ
Íàèáîëåå øèðîêî
ðàñïðîñòðàíåííûé
ìåõàíèçì ðåàêöèè
êîíäåíñàöèè
ïðåäëîæèë Her [35]. Îí âêëþ÷àåò
â ñåáÿ àòàêó íóêëåîôèëüíûì
äåïðîòîíèðîâàííûì
ñèëàíîëîì íà
íåéòðàëüíî-çàðÿæåííûé
ñèëàíîë.
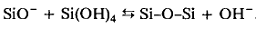 (25)
(25)
Ýòà ðåàêöèÿ ðàñïîëîæåíà
âûøå èçîýëåêòðè÷åñêîé
òî÷êè (pH>2-4,5; â çàâèñèìîñòè
îò ñòåïåíè êîíäåíñàöèè
ïîëèñèëîêñàíà),
ãäå ïîâåðõíîñòü
ñèëàíîëîâ ìîæåò
áûòü äåïðîòîíèðîâàíà
â çàâèñèìîñòè
îò èõ êèñëîòíîñòè.
Íà êèñëîòíîñòü
ñèëàíîëîâ ñèëüíîå
âëèÿíèå îêàçûâàþò
çàìåñòèòåëè
ó èõ àòîìîâ êðåìíèÿ.
Êîãäà OR èëè
OH çàìåùàåòñÿ
íà -OSi, ñíèæàåòñÿ
ýëåêòðîííàÿ ïëîòíîñòü
íà àòîìå Si, òåì ñàìûì
óâåëè÷èâàÿ êèñëîòíîñòü
ïðîòîíîâ íà äðóãèõ
ñèëàíîëàõ [66]. Ñêîðîñòü
êîíäåíñàöèè
äîñòèãàåò ìàêñèìàëüíîãî
çíà÷åíèÿ â çîíå
íåéòðàëüíîé
pH-ñðåäû, ãäå
ñóùåñòâåííî
âûñîêè êîíöåíòðàöèè
êàê ïðîòîíèðîâàíûõ
òàê è äåïðîòîíèðîâàííûõ
ñèëàíîëîâ. Ìèíèìàëüíàÿ
ñêîðîñòü êîíäåíñàöèè
íàáëþäàåòñÿ
âáëèçè èçîýëåêòðè÷åñêîé
òî÷êè (ðèñ.).
Pohl è
Osterholtz [14], à òàêæå
Âîðîíêîâ [12] ïðåäëîæèëè
ïîõîæèå ìåõàíèçìû
äëÿ ãèäðîêñèëüíîãî
àíèîíà è îñíîâíî-êàòàëèçèðóåìûõ
ðåàêöèé êîíäåíñàöèè
àëêèëñèëàíòðèîëà
è àëêèëñèëàíäèîëà:
 (26)
(26)
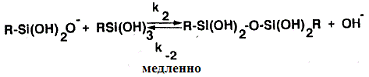
d[ñèëàíòðèîë]/dt = k1k2/k-1
[RSi(OH)3]2[OH-]
 ýòîì ìåõàíèçìå
ãèäðîêñèëüíûé
àíèîí ðåàãèðóåò
ñ àëêèëñèëàíòðèîëîì
(ðåàêöèÿ ÿâëÿåòñÿ
îáðàòèìîé), ÷òî
âåäåò ê óñòàíîâëåíèþ
êîíöåíòðàöèîííîãî
ðàâíîâåñèÿ ñ
àíèîíîì Si(OH)2O-. Â ðåçóëüòàòå
âçàèìîäåéñòâèÿ
ýòîãî àíèîíà
ñ àëêèëñèëàíòðèîëîì
(ëèìèòèðóþùàÿ
ñòàäèèÿ) îáðàçóåòñÿ
äèàëêèëòåòðàãèäðîêñèäèñèëîêñàí
è ãèäðîêñèëüíûé
àíèîí. Ñîîòâåòñòâåííî
ñêîðîñòü êîíäåíñàöèè
(äëÿ ýòîãî ìåõàíèçìà)
ïî ãèäðîêñèëüíîìó
àíèîíó õàðàêòåðèçóåòñÿ
ïåðâûì ïîðÿäêîì,
è âòîðûì ïî àëêèëñèëàíòðèîëó.
Äàëåå êîíäåíñàöèÿ
äèñèëîêñàíà
ñëîæíî ïðîñëåæèâàåòñÿ
èç-çà ìàëåíüêîãî
âðåìåíè ðåàêöèè,
ïðåäïîëîæèòåëüíî
ïî ïðè÷èíå ñòåðè÷åñêèõ
ýôôåêòîâ.
Ñ÷èòàåòñÿ, ÷òî
ìåõàíèçì îñíîâíî-êàòàëèçèðóåìîé
êîíäåíñàöèè
âêëþ÷àåò â ñåáÿ
ïÿòè- èëè øåñòèêîîðäèíàöèîíûé
èíòåðìåäèàò
èëè ïåðåõîäíîå
ñîñòîÿíèå [40-44]. Okkerse ïðåäëîæèë
áèìîëåêóëÿðíûé
èíòåðìåäèàò,
âêëþ÷àþùèé øåñòèêîîðäèíàöèîííûé
àòîì êðåìíèÿ
[42]:
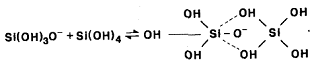 (27)
(27)
Íà îñíîâàíèè
ðåçóëüòàòîâ èññëåäîâàíèÿ
ÃÌÔÊ ñèëàíîëîâ
Â. Ãðàáá [45], Ç. Ëÿñîöêèé
[39, 46] è Â. Ðóòö [47] ïðåäëàãàþò
ñëåäóþùóþ ñõåìó
ìåõàíèçìà ÃÌÔÊ,
êàòàëèçèðóåìîé
îñíîâàíèÿìè
(ñõåìà 1):

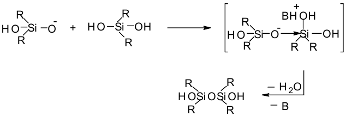
Swain ïðåäëîæèë,
÷òî àòîì êðåìíèÿ
îáðàçóåò ñòàáèëüíûé
ïÿòèêîîðäèíàöèîííûé
èíòåðìåäèàò:
SN2**-Si èëè SN2*-Si ìåõàíèçìû
[40].
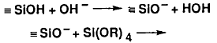
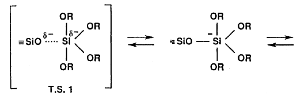
 (28)
(28)
Ìåõàíèçì àññîöèàòèâíîé
êîíäåíñàöèè
ñ ó÷àñòèåì ïÿòè-
èëè øåñòèêîîðäèíàöèîííîãî
èíòåðìåäèàòà
òàêæå ñîîòâåòñòâóåò
ðàñøèðåííîé
êèíåòèêå êîíäåíñàöèè
ïðè âûñîêèõ äàâëåíèÿõ,
êîòîðóþ íàáëþäàë
Arteki è åãî ñîòðóäíèêè
[41] (Ðèñ. 11). Îí àíàëèçèðîâàë
àêòèâèðîâàííûå
îáúåìû â îñíîâíî-êàòàëèçèðóåìîì
ìåõàíèçìå êîíäåíñàöèè
ñ ó÷àñòèåì ïÿòèêîðäèíàöèîííîãî
èíòåðìåäèàòà
(óðàâíåíèå 27). Îíè
ïðèøëè ê âûâîäó,
÷òî èç-çà ïåðåñòàíîâêè
ìîëåêóë ðàñòâîðèòåëÿ
îêîëî àíèîííîãî
íóêëåîôèëà SiO-, è ñðàâíèìî
ìåíüøèõ êîëè÷åñòâàõ
ïåðåõîäíûõ ñîñòîÿíèé
ñ êîëè÷åñòâîì
ðåàãåíòîâ, äèññîöèàöèè
ñèëàíîëüíûõ
âèäîâ è îáðàçîâàíèÿ
ïåðåõîäíûõ ñîñòîÿíèé
ñïîñîáñòâóþò
óìåíüøåíèþ àêòèâèðîâàííûõ
îáúåìîâ. Òàêèì
îáðàçîì, äàííûå
ðåàêöèè óñêîðÿþòñÿ
ïðè äàâëåíèè.
Òàêèå æå ðàññóæäåíèÿ
ïðèìåíèìû ê ìåõàíèçìó
ñ ó÷àñòèåì ïÿòè
- êîîðäèíàöèîííîãî
èíòåðìåäèàòà.
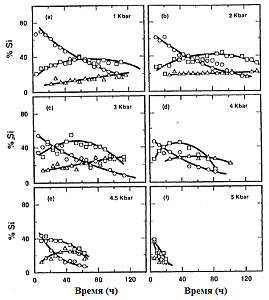
Ðèñ. 11. Âðåìåííàÿ
çàâèñèìîñòü
âñåõ íàáëþäàåìûõ
êîíäåíñèðîâàííûõ
âèäîâ âî âðåìÿ
ãèäðîëèçà òåòðàìåòîêñèñèëàíà
â êèñëûõ óñëîâèÿõ:
à) 1 áàð, b) 2 êáàð, c) 3 êáàð, d) 4 êáàð, e) 4,5 êáàð, f) 5 êáàð, (m=10).  - Q0;
- Q0; - (Q1)2, (Q1)3;
- (Q1)2, (Q1)3;
 - Q1Q2Q1, (Q2)4 [41]
- Q1Q2Q1, (Q2)4 [41]
Èñïîëüçóÿ ìåòîä
ïîëóýìïèðè÷åñêèõ
ìîëåêóëÿðíûõ
îðáèòàëåé, Davis è Durggraf [44] èññëåäîâàëè
îñíîâíî-êàòàëèçèðóåìóþ
ïîëèìåðèçàöèþ
ñèëàíîëîâ. Èõ
ðàñ÷åòû ïîêàçàëè,
÷òî âîäà áîëåå
ëåãêî ðàñõîäóåòñÿ
â òîì ñëó÷àå êîãäà
àòîì êðåìíèÿ
ìîæåò ñìåíèòü
ñâîþ âàëåíòíîñòü
ñ øåñòè äî ïÿòè
ðàíüøå ÷åì ñ ïÿòè
äî ÷åòûðåõ. Ýòè
ðåçóëüòàòû ñâèäåòåëüñòâóþò
â ïîëüçó ìåõàíèçìà
êîíäåíñàöèè
ñ ó÷àñòèåì ïÿòè-êîîðäèíàöèîííîãî
èíòåðìåäèàòà.
Òå æå ñàìûå ðàññóæäåíèÿ
ïðèìåíÿþòñÿ â
îñíîâíî-êàòàëèçèðóåìîì
ãèäðîëèçå, ãäå
ëåã÷å âûòåñíèòü
ñïèðò èç äèìåðà
÷åðåç ïÿòèêîîðäèíàöèîííûé
èíòåðìåäèàò,
÷åì èç ìîíîìåðà,
ïîäðàçóìåâàÿ
ñîãëàñîâàíèå
ãèäðîëèçà è îáðàçîâàíèå
äèìåðà.
1.3.1.2 Ìåõàíèçì êîíäåíñàöèè
â ïðèñóòñòâèè
êèñëîòû, êàê êàòàëèçàòîðà
Ïîñêîëüêó â âîäíûõ
ñèñòåìàõ âðåìÿ
ãåëåîáðàçîâàíèÿ
íàõîäèòñÿ íèæå
èçîýëåêòðè÷åñêîé
òî÷êè, ïðèíÿòî
ñ÷èòàòü, ÷òî
ìåõàíèçì êîíäåíñàöèè
â ïðèñóòñòâèè
êèñëîòû âêëþ÷àåò
â ñåáÿ ïðîòîíèðîâàíèå
ñèëàíîëîâ. Ïðîòîíèðîâàíèå
ïðèâîäèò ê òîìó,
÷òî àòîì êðåìíèÿ
ñòàíîâèòñÿ áîëåå
ýëåêòðîôèëüíûì
è òàêèì îáðàçîì
áîëåå âîñïðèèì÷èâûì
ê íóêëåîôèëüíîé
àòàêå. Íàèáîëåå
îñíîâíûå ñèëàíîëû
(ìîíîìåð èëè ñëàáî
ðàçâåòâëåííûå
îëèãîìåðû) ëåã÷å
ïðîòîíèðóþòñÿ.
Ïîýòîìó ðåàêöèÿ
êîíäåíñàöèè
ïðåäïî÷òèòåëüíåå
ïðîèñõîäèò ìåæäó
íåéòðàëüíûìè
è ïðîòîíèðîâàíûìè
ñèëàíîëàìè.
Pohl è
Osterholtz ïðåäëîæèëè
[14], ÷òî ïðè pD íèæå 4.5 óâåëè÷åâàåòñÿ
ñêîðîñòü êîíäåíñàöèè
àëêèëñèëàíòðèîëà
(ðèñ. 12à) è â ýòîì
ó÷àñòâóåò ïðîòîíèðîâàííûé
ñèëàíîë:
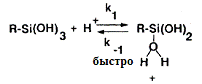
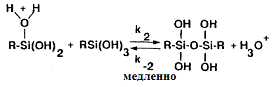 (29)
(29)
d[ñèëàíòðèîë]/dt = k1k2/k-1 [RSi(OH)3]2[H+]
 ñîîòâåòñòâèè
ñ ýòèì ìåõàíèçìîì,
ñêîðîñòü êîíäåíñàöèè
õàðàêòåðèçîâàëàñü
ïî èîíó äåéòåðèÿ
ïåðâûì ïîðÿäêîì
è âòîðûì ïî ñèëàíòðèîëó.
Èç ýòèõ ðåçóëüòàòîâ
áûëè íå ÿñíû ðàçëè÷èÿ
ìåæäó ìåõàíèçìàìè
SN2-Si, SN2**-Si èëè SN2*-Si.
Ïîýòîìó áûë
ïðåäëîæåí ìåõàíèçì
ðåàêöèè äëÿ îñíîâíî-
è êèñëîòíî-êàòàëèçèðóåìîé
êîíäåíñàöèè
ñ ó÷àñòèåì ïÿòè-
èëè øåñòèêîîðäèíàöèîíîãî
èíòåðìåäèàòà,
ãäå êèíåòèêà
ðåàêöèé êîíäåíñàöèè
çàâèñèò îò ñòåðè÷åñêèõ
è èíäóêöèîííûõ
ôàêòîðîâ. Çàìåñòèòåëü
ó àòîìà êðåìíèÿ,
êîòîðûé óìåíüøàåò
ñòåðè÷åñêèå
çàòðóäíåíèÿ
â ïåðåõîäíîì ñîñòîÿíèè,
ïîâûøàåò êèíåòè÷åñêèå
õàðàêòåðèñòèêè
êîíäåíñàöèè.
Îáúåìíûå ãðóïïû
ó àòîìà êðåìíèÿ
çàìåäëÿþò ïðîöåññ
êîíäåíñàöèè.
Çàìåíà áîëåå
ýëåêòðîíîäîíîðíîé
OR ãðóïïû
íà áîëåå ýëåêòðîäîíîðíóþ
OH èëè OSi ñòàáèëèçèðóåò
îòðèöàòåëüíûé
çàðÿä íà íóêëåîôèëå
è òàêèì îáðàçîì
ïîâûøàåò êèíåòè÷åñêèå
õàðàêòåðèñòèêè
â îñíîâíî-êàòàëèçèðóåìîé
êîíäåíñàöèè.
Àíàëîãè÷íûå
ðàçìûøëåíèÿ
ïðèâåëè ê ïðåäïîëîæåíèþ,
÷òî îáøèðíûé
ãèäðîëèç è êîíäåíñàöèÿ
äåñòàáèëèçèðóåò
ïîëîæèòåëüíî
çàðÿæåííûé èíòåðìåäèàò
è òàêèì îáðàçîì
ïîíèæàþò êèíåòè÷åñêèå
õàðàêòåðèñòèêè
â êèñëîòíî-êàòàëèçèðóåìîé
êîíäåíñàöèè.
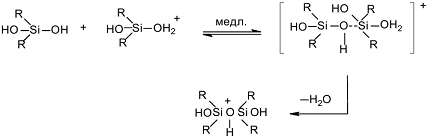
Íà îñíîâàíèè
ðåçóëüòàòîâ èññëåäîâàíèÿ
ÃÌÔÊ ñèëàíîëîâ
Â. Ãðàáá [45], Ç. Ëÿñîöêèé
[39, 46] è Â. Ðóòö [47] ïðåäëàãàþò
ñëåäóþùóþ ñõåìó
ìåõàíèçìà ÃÌÔÊ,
êàòàëèçèðóåìîé
êèñëîòàìè (ñõåìà
2):
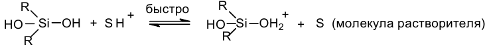

.1.3.2 Ïîðÿäîê ðåàêöèè
ïî ðåàãåíòàì
Îïðåäåëåíèå
ïîðÿäêà ðåàêöèè
ïî ñèëàíîëó ïîêàçàëî,
÷òî â ñëó÷àå êèñëîòíîãî
êàòàëèçà êàê
äëÿ äèîðãàíîñèëàíäèîëîâ,
òàê è äëÿ òðèîðãàíîñèëàíîëîâ
îí ðàâåí äâóì
íåçàâèñèìî îò
çàìåñòèòåëåé
ó àòîìà êðåìíèÿ.
Òàê, âòîðîé ïîðÿäîê
ïî ìîíîìåðó îáíàðóæåí
äëÿ ÃÌÔÊ Me2Si(OH)2
â ñðåäå äèîêñàíà
[39] è ìåòàíîëà
[48], äëÿ R2Si(OH)2 ñ ëèíåéíûìè
[49] è ðàçâåòâëåííûìè
àëêèëüíûìè çàìåñòèòåëÿìè
[50].  ñëó÷àå XCH2MeSi(OH)2
[51] ñ ãàëîèäîì â
ìåòèëüíîì ðàäèêàëå
ïîðÿäîê ïî ñèëàíîëó
íåìíîãî ïðåâûøàë
âòîðîé, ÷òî ñâÿçûâàþò
ñ èçìåíåíèåì
ñâîéñòâ ñðåäû.
Ïîðÿäîê ðåàêöèè
îïðåäåëÿëè ïî çàâèñèìîñòè
íà÷àëüíîé ñêîðîñòè
ðåàêöèè îò íà÷àëüíîé
êîíöåíòðàöèè
ñèëàíîëà â èíòåðâàëå
0.05 - 0.6Ì. Ëèíåéíàÿ
çàâèñèìîñòü
â êîîðäèíàòàõ
ðåàêöèè âòîðîãî
ïîðÿäêà 1/[SiOH] = f(t) ñîáëþäàëàñü
äî êîíâåðñèè
ìîíîìåðà 25 - 50 % äëÿ
Me2Si(OH)2, 15 - 20 % äëÿ XCH2MeSi(OH)2
è äðóãèõ ñèëàíäèîëîâ.
Ðåçêîå óìåíüøåíèå
ñêîðîñòè âûäåëåíèÿ
âîäû ïîñëå äîñòèæåíèÿ
óêàçàííûõ ñòåïåíåé
êîíâåðñèè àâòîðû
îáúÿñíÿþò çíà÷èòåëüíî
ìåíüøåé ðåàêöèîííîé
ñïîñîáíîñòüþ
ãèäðîêñèëüíûõ
ãðóïï îáðàçóþùèõñÿ
îëèãîìåðîâ. Â
÷àñòíîñòè, óñòàíîâëåíî,
÷òî òåòðàìåòèëäèñèëîêñàíäèîë
êîíäåíñèðóåòñÿ
â 35 ðàç ìåäëåííåå,
÷åì Me2Si(OH)2 â ñðåäå
äèîêñàíà è â
10 ðàç ìåäëåííåå
- â ñðåäå ìåòàíîëà.
Ïðåäïîëàãàåòñÿ,
÷òî ïîíèæåíèå
ðåàêöèîííîé
ñïîñîáíîñòè
äèìåðà îáóñëîâëåíî
ìåíüøèì èíäóêöèîííûì
ýôôåêòîì HOSiMe2O-
ãðóïïû â òåòðàìåòèëäèñèëîêñàíäèîëå
â ñðàâíåíèè ñ
ãðóïïîé OH- â Me2Si(OH)2.
Ç. Ëÿñîöêèé ñîîáùàåò
òàêæå, ÷òî ïîñëå
çàìåäëåíèÿ ðåàêöèè,
íà áîëåå ãëóáîêèõ
ñòàäèÿõ ïðîöåññà
îáíàðóæèâàåòñÿ
óñêîðåíèå ðåàêöèè
[39]. Ýòîò ôàêò íèêîãäà
íå îáñóæäàëñÿ
äðóãèìè èññëåäîâàòåëÿìè.
Ç. Ëÿñîöêèé ïðåäïîëàãàåò,
÷òî óñêîðåíèå
ðåàêöèè îáóñëîâëåíî
òåì, ÷òî âûäåëÿþùàÿñÿ
â ðåàêöèè âîäà
óâåëè÷èâàëà
êàòàëèòè÷åñêóþ
àêòèâíîñòü
HCl. Ïðîâåðêà ýòîãî
ïðåäïîëîæåíèÿ
ïóòåì äîáàâëåíèÿ
âîäû â ðåàêöèîííóþ
ñèñòåìó ïîêàçàëà,
÷òî äåéñòâèòåëüíî
ñ óâåëè÷åíèåì
êîíöåíòðàöèè
âîäû îò 0.15 äî 0.35Ì óâåëè÷èâàåòñÿ
ñêîðîñòü êîíäåíñàöèè.
Îäíàêî íåîáõîäèìî
îòìåòèòü, ÷òî
â òàêîì ñëó÷àå
àâòîêàòàëèç
êîíäåíñàöèè
äîëæåí áûë íàáëþäàòüñÿ
ñ ïåðâûõ àêòîâ
íà÷àëà ðåàêöèè,
à íå òîëüêî íà
ãëóáîêèõ ñòàäèÿõ
ïðîöåññà. Â ïîñëåäóþùåé
ïóáëèêàöèè ïðèâîäÿòñÿ
êèíåòè÷åñêèå
êðèâûå ñ èíäóêöèîííûì
ïåðèîäîì â íà÷àëå
ðåàêöèè [52].
Èññëåäîâàíèÿ
íåìåöêèõ ó÷åíûõ
òàêæå ïîêàçàëè,
÷òî êèñëîòíî-êàòàëèçèðóåìàÿ
êîíäåíñàöèÿ
òðèîðãàíîñèëàíîëîâ
â ñðåäå äèîêñàí
- âîäà ïîä÷èíÿåòñÿ
óðàâíåíèþ ñêîðîñòè
âòîðîãî ïîðÿäêà
ïî ìîíîìåðó. Çäåñü
òàêæå íåîáõîäèìî
îòìåòèòü îäíî
îáñòîÿòåëüñòâî.
Òàê Â. Ðóòö ñ ñîàâòîðàìè
ñîîáùàåò, ÷òî
íàáëþäàëàñü
ëèíåéíàÿ çàâèñèìîñòü
1/[SiOH] = f(t) òîëüêî äî 50% êîíâåðñèè
òðèìåòèëñèëàíîëà
[47]. Êàê èçìåíÿëñÿ
õîä êèíåòè÷åñêèõ
çàâèñèìîñòåé
ïðè êîíâåðñèè
âûøå 50% íå ñîîáùàåòñÿ.
Î÷åâèäíî, îáû÷íûå
çàêîíîìåðíîñòè
ðåàêöèè âòîðîãî
ïîðÿäêà íàðóøàëèñü.
Îäíàêî ÃÌÔÊ
Me3SiOH íå îñëîæíåíà
ïîñëåäîâàòåëüíûìè
ñòàäèÿìè îáðàçîâàíèÿ
îëèãîìåðîâ, êàê
â ñëó÷àå êîíäåíñàöèè
äèîðãàíîñèëàíäèîëîâ.
Ñëåäîâàòåëüíî
èìåëèñü ïðè÷èíû
äðóãîãî ïîðÿäêà,
ïðèâîäÿùèå ê íàáëþäàåìûì
îñëîæíåíèÿì.
 ñëó÷àå îñíîâíîãî
êàòàëèçà ïîðÿäîê
ïî ìîíîìåðó ìîæåò
áûòü êàê ïåðâûé,
òàê è âòîðîé. Ïåðâûé
ïîðÿäîê ïî ñèëàíîëó
îáíàðóæåí Ç. Ëÿñîöêèì
ñ ñîàâòîðàìè
äëÿ êîíäåíñàöèè
Me2Si(OH)2 è àðèëìåòèëñèëàíäèîëîâ
â ìåòàíîëå â ïðèñóòñòâèè
NaOH è KOH. Ïîëó÷åíû ëèíåéíûå
çàâèñèìîñòè
íà÷àëüíîé ñêîðîñòè
ðåàêöèè îò íà÷àëüíîé
êîíöåíòðàöèè
ñèëàíîëà è ëèíåéíûå
çàâèñèìîñòè
lnC = f(t). Êðîìå òîãî, íàêëîí
ôóíêöèé lnC = f(t) ïðè
ðàçëè÷íûõ íà÷àëüíûõ
êîíöåíòðàöèÿõ
ñèëàíîëà îêàçàëñÿ
îäèíàêîâûì, ÷òî
óêàçûâàåò íà
îòñóòñòâèå âëèÿíèÿ
ïðîäóêòîâ ðåàêöèè
íà åå ñêîðîñòü.
Ïåðâûé ïîðÿäîê
ïî ñèëàíîëó îáúÿñíÿåòñÿ
ñ ïîçèöèé ïîâûøåííîé
êèñëîòíîñòè
äèîðãàíîñèëàíäèîëîâ,
îáóñëàâëèâàþùåé
ñìåùåíèå ðàâíîâåñèÿ
äåïðîòîíèðîâàíèÿ
ãèäðîêñèëüíîé
ãðóïïû (4) â ñòîðîíó
îáðàçîâàíèÿ
ñèëàíîëÿò àíèîíà.
Ïîñêîëüêó â ýêñïåðèìåíòàõ
êîíöåíòðàöèÿ
ñèëàíîëà áûëà
çíà÷èòåëüíî
âûøå êîí-öåíòðàöèè
êàòàëèçàòîðà,
òî êîíöåíòðàöèþ
îáðàçóþùåãîñÿ
ñèëàíîëÿò àíèîíà
àâòîðû ïðèðàâíèâàþò
ê êîíöåíòðàöèè
êàòàëèçàòîðà.
Ïîýòîìó èíòåãðàëüíîå
óðàâíåíèå ñêîðîñòè
ïðèíèìàåò âèä:
 (30)
(30)
 òîæå âðåìÿ êèíåòèêà
ÃÌÔÊ R3SiOH â âîäíîì
äèîêñàíå õàðàêòåðèçóåòñÿ
ïåðâûì ïîðÿäêîì
ïî ñèëàíîëó äàæå
äëÿ ñîåäèíåíèé
ñ ýëåêòðîíîäîíîðíûìè
çàìåñòèòåëÿìè.
 ñëó÷àå R2Si(OH)2
ñ ýëåêòðîíîäîíîðíûìè
çàìåñòèòåëÿìè
(R = Et, n-Pr è n-Bu) è, ñëåäîâàòåëüíî,
îáëàäàþùèå ìåíåå
âûðàæåííûìè
êèñëîòíûìè ñâîéñòâàìè,
ïîðÿäîê ïî ñèëàíîëó
- âòîðîé [53]. Âòîðîé
ïîðÿäîê ïî ñèëàíîëó
óñòàíîâëåí òàêæå
äëÿ ÃÌÔÊ, êàòàëèçèðóåìîé
îðãàíè÷åñêèìè
îñíîâàíèÿìè
[46]. È òîëüêî â ñëó÷àå
ïèïåðèäèíà, êàê
êàòàëèçàòîðà,
íå óäàëîñü íàäåæíî
óñòàíîâèòü ïîðÿäîê
ðåàêöèè. È â ýòîì
ñëó÷àå Ç. Ëÿñîöêèé
ñ ñîàâòîðàìè
ïðåäïîëàãàåò
îñëîæíÿþùåå âëèÿíèå
ýôôåêòîâ cðåäû.
Âòîðîé ïîðÿäîê
óñòàíîâëåí äëÿ
êîíäåíñàöèè
òåòðàìåòèëäèñèëîêñàíäèîëà
è 1,4-áèñ-äèìåòèëãèäðîêñèñèëèëáåíçîëà
(äî êîíâåðñèè
15 % [54]). Â ïîñëåäíåì
ñëó÷àå íåîáõîäèìî
îòìåòèòü, ÷òî
ïðè íà÷àëüíîé
êîíöåíòðàöèè
ñèëàíîëüíûõ
ãðóïï áîëåå 0.4 Ì
êîíñòàíòà ñêîðîñòè
ðåàêöèè âòîðîãî
ïîðÿäêà óìåíüøàëàñü,
÷òî àâòîðû òàêæå
îáúÿñíÿþò ïîíèæåíèåì
ðåàêöèîííîé
ñïîñîáíîñòè
ãèäðîêñèëüíûõ
ãðóïï îáðàçóþùèõñÿ
îëèãîìåðîâ. Îäíàêî
ïðåäïîëàãàåòñÿ,
÷òî ïðè÷èíîé
ýòîãî ÿâëÿþòñÿ
ïðîöåññû àññîöèàöèè
ìîëåêóë â êîíöåíòðèðîâàííûõ
ðàñòâîðàõ. Òàêèì
îáðàçîì, ïîðÿäîê
ïî ñèëàíîëó â
ñëó÷àå îñíîâíîãî
êàòàëèçà çàâèñèò
îò ñâîéñòâ ìîíîìåðà
è ñâîéñòâ ðåàêöèîííîé
ñðåäû.
.1.3.3 Âëèÿíèå êàòàëèçàòîðà
Êîíäåíñàöèÿ
ñèëàíîëîâ ìîæåò
ïðîõîäèòü ïîä
äåéñòâèåì òåìïåðàòóðû
áåç êàòàëèçàòîðà,
íî èñïîëüçîâàíèå
êàòàëèçàòîðà
÷àñòî áûâàåò
ïîëåçíûì.  êà÷åñòâå
êàòàëèçàòîðîâ
èñïîëüçóþò: ñîåäèíåíèÿ,
äåìîíñòðèðóþùèå
êèñëîòíûå è îñíîâíûå
õàðàêòåðèñòèêè,
íåéòðàëüíûå ñîëè,
àëêîêñèäû ïåðåõîäíûõ
ìåòàëëîâ. Êàê
îïèñûâàëîñü ðàíåå
â ðàçäåëå ãèäðîëèçà,
âëèÿíèÿ êàòàëèçàòîðà
÷àñòî îñëîæíÿåòñÿ
óâåëè÷èâàþùåéñÿ
êèñëîòíîñòüþ
ñèëàíîëüíîé
ãðóïïû ñî ñòåïåíÿìè
ãèäðîëèçà, ïîëèìåðèçàöèè
è âëèÿíèåì îáðàòíûõ
ðåàêöèé, êîòîðûå
ñòàíîâÿòñÿ âñå
áîëåå âàæíûìè
ñ áîëüøèìè êîíöåíòðàöèÿìè
âîäû.
Pohl è
Osterholtz èñïîëüçîâàëè
ßÌÐ 13Ñ è Si29 äëÿ èññëåäîâàíèé
êîíäåíñàöèè
àëêèëñèëàíòðèîëà
â áóôåðíîì ðàñòâîðå,
êàê ôóíêöèþ îò
pD (-log [D3O+]) [55]. Êîíñòàíòû
ñêîðîñòè õàðàêòåðèçóþòñÿ
âòîðûì ïîðÿäêîì
ïî àëêèëñèëàíòðèîëó.
Ó÷àñòêè ñêëîíîâ
âûøå è íèæå ìèíèìóìà
ñêîðîñòè ïðè pD 4,5 +1 è -1, ñîîòâåòñòâåííî,
óêàçûâàþò, ÷òî
êîíäåíñàöèÿ
ÿâëÿåòñÿ ñïåöèôè÷åñêè
êèñëîòíî- èëè
îñíîâíî-êàòàëèçèðóåìîé.
ßâëÿþòñÿ èíòåðåñíûìè
ñðàâíåíèÿ ðåçóëüòàòîâ
ïîêàçàíûõ íà
ðèñ.9à ñ pH-çàâèñèìîñòüþ
îò âðåìåíè ãåëåîáðàçîâàíèÿ
(ðèñ. 12b), â
êîòîðûõ ÷àñòî
èñïîëüçóåòñÿ
â êà÷åñòâå çíà÷åíèÿ
îáùàÿ êèíåòèêà
êîíäåíñàöèè
äëÿ çîëü-ãåëü ñèñòåì.
 ñîîòâåòñòâèè
ñ ðèñ. 12b îáùàÿ
ñêîðîñòü êîíäåíñàöèè
ìèíèìàëüíà ïðè
pH 1,5. Ñòàáèëüíûå
ñèñòåìû (íå îáðàçóþùèå
ãåëÿ) áûëè ïîëó÷åíû
ïðè áîëåå îñíîâíûõ
óñëîâèÿõ. Ìèíèìóì
ïðè pH 2 ñîîòâåòñòâóåò
èçîýëåêòðè÷åñêîé
òî÷êå: ïîâåðõíîñòü
ñèëàíîëüíûõ
ãðóïï ïðîòîíèðóåòñÿ
è äåïðîòîíèðóåòñÿ
ïðè íèçêèõ è âûñîêèõ
çíà÷åíèÿõ pH.
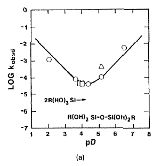
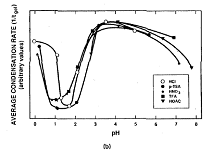
Ðèñ. 12. a) Çàâèñèìîñòü
pD - Ñêîðîñòü
êîíäåíñàöèè
äëÿ àëêèëñèëàíòðèîëîâ
â áóôåðíîì âîäíîì
ðàñòâîðå. b) óñðåäíåííàÿ
ñêîðîñòü êîíäåíñàöèè
(1/âðåìÿ ãåëüîáðàçîâàíèÿ)
äëÿ ãèäðîëèçà
òåòðàýòîêñèñèëàíà
ñ ðàçëè÷íûìè
êèñëîòàìè.
×òî êàñàåòñÿ
ïîðÿäêà ðåàêöèè
ïî êàòàëèçàòîðó,
òî è â ýòîì âîïðîñå
ìíîãî íåÿñíîñòåé.
Òàê ïîëüñêèìè
ó÷åíûìè óñòàíîâëåí
ïåðâûé ïîðÿäîê
ïî HCl â ÃÌÔÊ Me2Si(OH)2
[39], XCH2MeSi(OH)2 [51], è ñèëàíäèîëîâ
ñ ðàçâåòâëåííûìè
àëêèëüíûìè çàìåñòèòåëÿìè
[50]. Â. Ðóòö [56] è Ñ. Áèëäà
[57] ïîëó÷èëè òàêæå
ïåðâûé ïîðÿäîê
ïî HCl â ÃÌÔÊ R3SiOH.
 òîæå âðåìÿ Â.
Ãðàáá äàåò ïîðÿäîê
ïî HCl íåìíîãî áîëüøèé
åäèíèöû äëÿ ÃÌÔÊ
Me3SiOH [45]. Ïðè èçó÷åíèè
ÃÌÔÊ R2Si(OH)2 ñ àëêèëüíûìè
çàìåñòèòåëÿìè
ëèíåéíîãî ñòðîåíèÿ
îáíàðóæåíî, ÷òî
â îáëàñòè ìàëûõ
êîíöåíòðàöèé
HCl ïîðÿäîê ïî êàòàëèçàòîðó
òàêæå ≈ 1, à äàëüíåéøåå
óâåëè÷åíèå êîíöåíòðàöèè
HCl â 10 ðàç ïðèâîäèò
ê çíà÷èòåëüíî
ìåíüøåìó óâåëè÷åíèþ
ñêîðîñòè ðåàêöèè,
òî åñòü ïîðÿäîê
ïî HCl ìåíüøå åäèíèöû
[49]. Â ðàáîòå ïîêàçàíî
òàêæå, ÷òî êîíñòàíòà
ñêîðîñòè ÃÌÔÊ
Et2Si(OH)2 ìîæåò êàê
óâåëè÷èâàòüñÿ,
òàê è óìåíüøàòüñÿ
ïðè óâåëè÷åíèè
êîíöåíòðàöèè
HCl â çàâèñèìîñòè
îò êîíöåíòðàöèè
âîäû â ðåàêöèîííîé
ñèñòåìå. Áîëåå
òîãî, çàâèñèìîñòü
êîíñòàíòû ñêîðîñòè
Et2Si(OH)2 îò êîíöåíòðàöèè
âîäû â ñèñòåìå
èìååò ýêñòðåìàëüíûé
õàðàêòåð; ìàêñèìóì
ñêîðîñòè íàáëþäàåòñÿ
ïðè [H2O] = 0.75M. Ýòîò æå
ýôôåêò îáíàðóæåí
â ïðèñóòñòâèè
ñåðíîé êèñëîòû
[58]. Ëÿñîöêèé çàìå÷àåò,
÷òî ýòîò ôàêò
òðåáóåò îñîáîãî
âíèìàíèÿ ïðè
ñðàâíåíèè ðåçóëüòàòîâ,
ïîëó÷åííûõ â
ðàçíûõ óñëîâèÿõ
ýêñïåðèìåíòà.
 ïðèñóòñòâèè
HClO4 è HBr ñêîðîñòü
ðåàêöèè ïðè äîáàâëåíèè
âîäû óìåíüøàåòñÿ
ñ ñàìîãî íà÷àëà
ðåàêöèè [52, 58]. Óêàçàííûå
êèñëîòû çíà÷èòåëüíî
àêòèâíåå ñîëÿíîé
êèñëîòû.
Àíàëîãè÷íîå
ñëîæíîå âëèÿíèå
âîäû îáíàðóæåíî
íåäàâíî â ÃÌÔÊ
RMe2SiOH â ïðèñóòñòâèè
HCl â äèîêñàíå [47,
57]. Óñòàíîâëåíî,
÷òî ïðè êîíöåíòðàöèè
âîäû ìåíüøå 0,1Ì
íàáëþäàåòñÿ
èíäóêöèîííûé
ïåðèîä [57]; ìàêñèìóì
ñêîðîñòè ïðèõîäèòñÿ
íà êîíöåíòðàöèþ
âîäû 1.0Ì è ïðè [H2O]
> 2M çíà÷åíèÿ êîíñòàíò
ñêîðîñòåé óæå
íå îòëè÷àþòñÿ
îò èõ çíà÷åíèé
äëÿ ðåàêöèè â ÷èñòîé
âîäå [47]. ßâëåíèå
óñêîðåíèÿ ÃÌÔÊ
ñèëàíîëîâ âûäåëÿþùåéñÿ
âîäîé íå íàáëþäàåòñÿ
â ñëó÷àå îñíîâíîãî
êàòàëèçà êàê
äëÿ äèîðãàíîñèëàíäèîëîâ,
òàê è äëÿ òðèîðãàíîñèëàíîëîâ.
.1.3.4 Ñòåðè÷åñêèå
è èíäóêòèâíûå
ýôôåêòû
Ïðîöåññ êîíäåíñàöèè
ïðîòåêàåò ïî ðåàêöèÿì
ÃÌÔÊ (2) è ÃÒÔÊ (3),
êîòîðûå ìîãóò
ïðîèñõîäèòü î÷åíü
ñëîæíî ìåæäó
ìîíîìåðàìè è
îëèãîìåðàìè.
Ïî ýòîé ïðè÷èíå
âëèÿíèå ñòåðè÷åñêèõ
è èíäóêöèîííûõ
ôàêòîðîâ, äëÿ êîíäåíñàöèè
òåòðààëêîêñèñèëàíîâ,
ïëîõî èçó÷åíû.
 ñîîòâåòñòâèè
ñ Âîðîíêîâûì
ñêîðîñòü êîíäåíñàöèè
òðèîðãàíîñèëàíîëîâ
óìåíüøàåòñÿ
ñ óâåëè÷åíèåì
äëèíû è ñòåïåíè
ðàçâåòâëåíèÿ
öåïè àëêèëüíîãî
çàìåñòèòåëÿ
èëè óâåëè÷åíèåì
ðàçìåðîâ àðèëüíîãî
çàìåñòèòåëÿ.
 òåòðàôóíêöèîíàëüíûé
àëêîêñèñèëàíàõ
çàìåñòèòåëü
óâåëè÷èâàåò
ñòåðè÷åñêèå
çàòðóäíåíèÿ
â ïåðåõîäíîì ñîñòîÿíèè
çàìåäëÿþùèå
êîíäåíñàöèþ.
Òàê æå Âîðîíêîâ
ïðåäëîæèë, ÷òî
ñêîðîñòü êîíäåíñàöèè
óâåëè÷èâàåòñÿ
ñ ÷èñëîì ñèëàíîëüíûõ
ãðóïï (óâåëè÷åíèå
êèñëîòíîñòè)
[12].
 ïðåäûäóùåì
ðàçäåëå óêàçûâàëîñü,
÷òî ìåõàíèçì
êîíäåíñàöèè
â êèñëûõ èëè ùåëî÷íûõ
óñëîâèÿõ âêëþ÷àþò
ïðîòîíèðîâàíèå
è äåïðîòîíèðîâàíèå
ñèëàíîëîâ. Îðãàíè÷åñêèå
çàìåñòèòåëè
òàê æå âëèÿþò
íà êèñëîòíîñòü
ñèëàíîëüíûõ
ãðóïï, ó÷àñòâóþùèõ
â êîíäåíñàöèè.
Ýëåêòðîíîäîíîðíûå
àëêèëüíûå çàìåñòèòåëè
óìåíüøàþò êèñëîòíîñòü
ñèëàíîëîâ. Ýòîò
ñäâèã èçîýëåêòðè÷åñêîé
òî÷êè â ñòîðîíó
áîëåå âûñîêèõ
çíà÷åíèé pH ïîêàçàí íà
ðèñ. 9, ñóùåñòâåííî
âëèÿÿ íà pH çàâèñèìîñòü
ìåõàíèçìà êîíäåíñàöèè.
Ýëåêòðîíîàêöåïòîðíûå
ãðóïïû (-OH è -OSi) íàîáîðîò
óâåëè÷èâàþò
êèñëîòíîñòü
ñèëàíîëîâ è ñêîðîñòü
êîíäåíñàöèè
ìèíèìàëüíà äëÿ
îëèãîìåðîâ.
Òàêèì îáðàçîì,
ñòåïåíü ãèäðîëèçà
è êîíäåíñàöèè
â îðãàíîàëêîêñèñèëàíàõ
ôîðìóëû RxSi(OR)4-x è
çíà÷åíèå õ îïðåäåëÿþò
ìåõàíèçì ðåàêöèè
è óñòàíàâëèâàþò,
çíà÷åíèå êèñëîòíî-
èëè îñíîâíî-êàòàëèçèðóåìîé
êîíäåíñàöèè.
Õîòÿ âëèÿíèå
èíäóêòèâíûõ
ýôôåêòîâ âàæíî,
Âîðîíêîâ ãîâîðèò
î òîì, ÷òî ïðè êîíäåíñàöèè
äèàëêèëñèëàíäèîëà
ñòåðè÷åñêèå
ýôôåêòû ïðåîáëàäàþò
íàä èíäóêòèâíûìè
[12].
Êàê ìîæíî óâèäåòü
èç ñõåìû 1 è ñõåìû
2, îðãàíîñèëàíîëû
â ðåàêöèè êîíäåíñàöèè
ó÷àñòâóþò êàê
â ðîëè íóêëåîôèëà,
òàê è â ðîëè ñóáñòðàòà.
Î÷åâèäíî, ÷òî
òàêàÿ äâîéñòâåííàÿ
ðîëü ìîëåêóë ñèëàíîëà
äîëæíà îáóñëàâëèâàòü
ñëîæíûé ìåõàíèçì
èíäóêöèîííîãî
âëèÿíèÿ çàìåñòèòåëåé.
Óâåëè÷åíèþ ñêîðîñòè
êîíäåíñàöèè
ñèëàíîëîâ áóäåò
ñïîñîáñòâîâàòü
ðÿä ôàêòîðîâ: 1) âûñîêàÿ
êîíöåíòðàöèÿ
ïðîòîíèðîâàííîé
ôîðìû ñóáñòðàòà
(Ñõåìà 1) èëè ñèëàíîëÿò
àíèîíà (Ñõåìà
2); 2) óâåëè÷åíèå
íóêëåîôèëüíîñòè
ìîëåêóëû ñèëàíîëà
èëè ñèëàíîëÿò
àíèîíà, ñîîòâåòñòâåííî;
3) ñòàáèëèçàöèÿ
ïåðåõîäíîãî ñîñòîÿíèÿ;
4) óâåëè÷åíèå ýëåêòðîôèëüíîñòè
ïðîòîíèðîâàííîãî
è íåéòðàëüíîãî
ñóáñòðàòà.
 ñëó÷àå êèñëîòíîãî
êàòàëèçà (Ñõåìà
1) ýëåêòðîíîäîíîðíûå
çàìåñòèòåëè
ñïîñîáñòâóþò
ðåàëèçàöèè ïåðâîãî,
âòîðîãî è òðåòüåãî
óñëîâèÿ, íî ñóùåñòâåííî
ñíèæàþò ýëåêòðîôèëüíîñòü
ïðîòîíèðîâàííîé
ìîëåêóëû ñèëàíîëà.
Ïîëó÷åííîå Ç.
Ëÿñîöêèì [51] íåîæèäàííî
áîëüøîå è ïîëîæèòåëüíîå
çíà÷åíèå ðåàêöèîííîé
ïîñòîÿííîé ρ*
= +5.3 ñâèäåòåëüñòâóåò
îá îòðèöàòåëüíî
çàðÿæåííîì ïåðåõîäíîì
ñîñòîÿíèè, ÷òî
ïðîòèâîðå÷èò
ïðåäëîæåííîìó
ìåõàíèçìó (Ñõåìà
1). Ç. Ëÿñîöêèé îòìå÷àåò,
÷òî ïðè÷èíîé
ýòîãî ÿâëÿåòñÿ
çíà÷èòåëüíûé
âêëàä ñòåðè÷åñêîãî
ôàêòîðà â íàáëþäàåìóþ
âåëè÷èíó. Îáðàáîòêà
äàííûõ Ç. Ëÿñîöêîãî
[50], ïðîâåäåííàÿ
Â.Ï. Ìèëåøêåâè÷åì
[60] ñ ó÷åòîì ñòåðè÷åñêîãî
âëèÿíèÿ çàìåñòèòåëåé
ïîêàçàëà, ÷òî
ÃÌÔÊ îðãàíîñèëàíîëîâ
â êèñëîé ñðåäå
õàðàêòåðèçóåòñÿ
ñëàáûì èíäóêöèîííûì
è çíà÷èòåëüíûì
ñòåðè÷åñêèì
âëèÿíèåì:
 (31)
(31)
Îòðèöàòåëüíîå
çíà÷åíèå èíäóêöèîííîé
ïîñòîÿííîé ñåðèè
- ρ*
ïîëó÷åíî
íåìåöêèìè èññëåäîâàòåëÿìè
[57] è äëÿ ÃÌÔÊ R3SiOH:
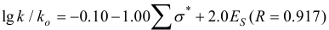 (32)
(32)
Íå âûñîêèå çíà÷åíèÿ
ρ*
äëÿ ïðîöåññà
ñ ó÷àñòèåì çàðÿæåííûõ
÷àñòèö ñâèäåòåëüñòâóþò
î êîìïåíñàöèè
ïðîòèâîïîëîæíî
íàïðàâëåííîãî
èíäóêöèîííîãî
âëèÿíèÿ çàìåñòèòåëåé
â íóêëåîôèëå
è ïðîòîíèðîâàííîì
ñóáñòðàòå. Òàêèì
îáðàçîì, ïîëó÷åííûå
äàííûå ïîäòâåðæäàþò
ïðåäëîæåííûé
ìåõàíèçì êèñëîòíî-êàòàëèçèðóåìîé
ÃÌÔÊ îðãàíîñèëàíîëîâ,
õàðàêòåðèçóþùèéñÿ
ïîëîæèòåëüíî
çàðÿæåííûì ïåðåõîäíûì
ñîñòîÿíèåì è
ïðîòèâîïîëîæíî
íàïðàâëåííûì
èíäóêöèîííûì
äåéñòâèåì çàìåñòèòåëåé.
 ñëó÷àå îñíîâíîãî
êàòàëèçà â ïðîöåññå
ÃÌÔÊ (Ñõåìà 2) ýëåêòðîíîàêöåïòîðíûå
çàìåñòèòåëè
áóäóò ñïîñîáñòâîâàòü
ðåàëèçàöèè ïåðâîãî,
òðåòüåãî è ÷åòâåðòîãî
óñëîâèé óñêîðåíèÿ
ðåàêöèè. Äåéñòâèòåëüíî,
êàê ïîêàçàëè
Ä. Õîéíîâñêè è
Ñ. Õùîíîâè÷ [61], ëîãàðèôì
îòíîøåíèÿ êîíñòàíò
ñêîðîñòåé îñíîâíîãî
(òðèýòèëàìèí)
è êèñëîòíîãî
êàòàëèçà (HCl) - lg(kB/kA)
â ñðåäå äèîêñàíà
ÿâëÿåòñÿ ëèíåéíîé
ôóíêöèåé ñóììû
èíäóêòèâíûõ
êîíñòàíò Òàôòà
ñ òàíãåíñîì
óãëà íàêëîíà
ρ*
= +4.7, ïðè÷åì
ëîãàðèôì ýòîãî
îòíîøåíèÿ ìåíÿåòñÿ
â èíòåðâàëå îò
-6 äî +4. Èç ýòîé çàâèñèìîñòè
íåñêîëüêî âûïàäàþò
äàííûå äëÿ MePhSi(OH)2
è Ph2Si(OH)2. Àâòîðû
óêàçûâàþò, ÷òî
ñàì ôàêò ëèíåéíîé
çàâèñèìîñòè
îçíà÷àåò, ÷òî
â êèñëîé è ùåëî÷íîé
ñðåäå ñòåðè÷åñêèå
ïðåïÿòñòâèÿ ñîèçìåðèìû.
ÃÌÔÊ çàìåùåííûõ
àðèëñèëàíäèîëîâ
XC6H4CH3Si(OH)2 [17] õàðàêòåðèçóåòñÿ
âåëè÷èíîé ρ*
= 1.16, ÷òî
íåñêîëüêî íèæå,
÷åì äëÿ äðóãèõ
èçâåñòíûõ ðåàêöèé
íóêëåîôèëüíîãî
çàìåùåíèÿ ó àòîìà
êðåìíèÿ [62]. Ïîëàãàþò,
÷òî íèçêîå çíà÷åíèå
ρ*
ÿâëÿåòñÿ
ñëåäñòâèåì êîìïåíñàöèè
ïðîòèâîïîëîæíî
íàïðàâëåííîãî
èíäóêöèîííîãî
âëèÿíèÿ çàìåñòèòåëåé
â ñèëàíîëÿò àíèîíå
è íåéòðàëüíîé
ìîëåêóëå ñóáñòðàòà.
Ïî äàííûì Ñ. Áèëäà
[63] èíäóêöèîííîå
âëèÿíèå çàìåñòèòåëåé
â ÃÌÔÊ R3SiOH ïîä äåéñòâèåì
îñíîâàíèé õàðàêòåðèçóåòñÿ
ðåàêöèîííîé
ïîñòîÿííîé ñåðèè
ρ*
= 1.95 (r = 0.991) äëÿ
çàìåùåííûõ òðèàëêèëñèëàíîëîâ;
ñ ó÷åòîì àðèëäèìåòèëñèëàíîëîâ
êîððåëÿöèÿ ñòàíîâèòñÿ
õóæå ρ* =1.90 (r = 0.901). Ñ. Áèëäà
ñ ñîàâòîðàìè
îòìå÷àþò, ÷òî
ïîíèæåíèå íóêëåîôèëüíîñòè
ñèëàíîëÿò-àíèîíà
ýëåêòðîíîàêöåïòîðíûìè
çàìåñòèòåëÿìè
åäâà ëè ïðèíöèïèàëüíî
ïîíèçèò åãî âûñîêóþ
íóêëåîôèëüíîñòü.
Ïîýòîìó íàáëþäàåìîå
ïîâûøåíèå ñêîðîñòè
ÃÌÔÊ îáóñëîâëåíî
äîìèíèðóþùèì
óâåëè÷åíèåì
ýëåêòðîôèëüíîñòè
àòîìà êðåìíèÿ
â ìîëåêóëå ñóáñòðàòà.
Êàê ïîêàçûâàþò
ðåçóëüòàòû ïðîâåäåííûõ
èññëåäîâàíèé
ðàçëè÷íûìè àâòîðàìè,
îñíîâíîå âëèÿíèå
íà ñêîðîñòü ÃÌÔÊ
îêàçûâàþò ñòåðè÷åñêèå
õàðàêòåðèñòèêè
çàìåñòèòåëåé,
÷òî ñîãëàñóåòñÿ
ñ áèìîëåêóëÿðíûì
íóêëåîôèëüíûì
çàìåùåíèåì SN2-Si.
 ñëó÷àå êèñëîòíî
êàòàëèçèðóåìîé
ÃÌÔÊ äèàëêèëñèëàíäèîëîâ
ñ ëèíåéíûìè àëêèëüíûìè
çàìåñòèòåëÿìè
óñòàíîâëåíî,
÷òî ðåçêîå èçìåíåíèå
ñêîðîñòè ïðîèñõîäèò
ïðè ïåðåõîäå îò
R = Me ê R = Et. Äàëüíåéøåå
óâåëè÷åíèå äëèíû
àëêèëüíîãî ðàäèêàëà
ïðèâîäèò ê íåçíà÷èòåëüíîìó
óâåëè÷åíèþ ñêîðîñòè
[49]. Àâòîðû îòìå÷àþò,
÷òî ïîñëåäîâàòåëüíîå
çàìåùåíèå ìåòèëüíîé
ãðóïïû â Me2Si(OH)2
íà âûñøóþ àëêèëüíóþ
ãðóïïó ñíèæàåò
ñêîðîñòü ðåàêöèè
ïðèáëèçèòåëüíî
íà ïîñòîÿííóþ
âåëè÷èíó, â 3-4 ðàçà.
Çàìå÷åíî òàêæå,
÷òî ìåòèëáóòèëñèëàíäèîë
êîíäåíñèðóåòñÿ
íåìíîãî áûñòðåå,
÷åì ìåòèëïðîïèëñèëàíäèîë,
íåñìîòðÿ íà áîëüøèå
ñòåðè÷åñêèå
ïðåïÿòñòâèÿ. Çàìåíà
àëêèëüíîé ãðóïïû
íà àíàëîãè÷íóþ,
íî èçîñòðîåíèÿ,
çàìåòíî ñíèæàåò
ñêîðîñòü ðåàêöèè,
íî â åùå áîëüøåé
ñòåïåíè ýòî ïðîèñõîäèò
ïðè ââåäåíèè âòîðîé
èçîàëêèëüíîé
ãðóïïû.  ñëó÷àå
èçîàëêèëñèëàíäèîëîâ
óæå íå íàáëþäàåòñÿ
àääèòèâíîãî
âêëàäà â ñêîðîñòü
ðåàêöèè ïðè ïîñëåäîâàòåëüíîé
çàìåíå ìåòèëüíûõ
ãðóïï íà èçîàëêèëüíóþ
ãðóïïó [50].
Ñêîðîñòü êîíäåíñàöèè
äèìåòèëñèëàíäèîëà
â ìåòàíîëå ñ ÊÎÍ
â 30 ðàç áîëüøå, ÷åì
ñêîðîñòü êîíäåíñàöèè
Et2Si(OH)2 [50]. Êàê îòìå÷àþò
Á. Äåÿê è Ç. Ëÿñîöêèé,
ýòî îáóñëîâëåíî
êàê íèçêîé êîíöåíòðàöèåé
äèýòèëñèëàíîëÿò-àíèîíà,
òàê è áîëüøèì
ñòåðè÷åñêèì
ýôôåêòîì ýòèëüíîãî
ðàäèêàëà. Ïîñêîëüêó
ñîîòíîøåíèå
ñêîðîñòåé ýòèõ
äâóõ ìîíîìåðîâ
â äèîêñàíå ñ
HCl (ãäå ïîëÿðíûé
ýôôåêò ìàë) ñîñòàâëÿåò
ëèøü 10, òî äåëàåòñÿ
âûâîä, ÷òî âêëàä
èíäóêöèîííîãî
ýôôåêòà R = Et â çàìåäëåíèå
êîíäåíñàöèè
Et2Si(OH)2 â ìåòàíîëå
ðàâåí 3.
Òàêèì îáðàçîì,
ñòåðè÷åñêèé
ýôôåêò çàìåñòèòåëåé
îêàçûâàåò áîëüøåå
âëèÿíèå íà ñêîðîñòü
ÃÌÔÊ ñèëàíîëîâ
êàê â êèñëîòíîì,
òàê è â ùåëî÷íîì
êàòàëèçå. Îäíàêî
â ïîñëåäíåì ñëó÷àå
èíäóêöèîííûé
ýôôåêò ïðîÿâëÿåòñÿ
ñèëüíåå, ÷åì â
êèñëîòíî êàòàëèçèðóåìîé
ÃÌÔÊ. Ýòî âèäíî,
íàïðèìåð, èç ñðàâíåíèÿ
ñêîðîñòåé êîíäåíñàöèè
äèìåòèëñèëàíäèîëà,
ìåòèëôåíèëñèëàíäèîëà
è äèôåíèëñèëàíäèîëà
â ïðèñóòñòâèè
òðèýòèëàìèíà:
íåñìîòðÿ íà áîëüøèå
ðàçìåðû ôåíèëüíîãî
çàìåñòèòåëÿ,
MePhSi(OH)2 è Ph2Si(OH)2 êîíäåíñèðóþòñÿ
áûñòðåå äèìåòèëñèëàíäèîëà
â 4 è 8 ðàç, ñîîòâåòñòâåííî
[61]. Â òî æå âðåìÿ â
ïðèñóòñòâèè
HCl ñêîðîñòü èõ êîíäåíñàöèè
ìåíüøå ÷åì Me2Si(OH)2
â 23 è 2200 ðàç, ñîîòâåòñòâåííî.
Ïðåäïîëàãàåòñÿ,
÷òî ïðîÿâëåíèå
ñòåðè÷åñêèõ
ïðåïÿòñòâèé êîíäåíñàöèè
ñèëàíîëîâ ÿâëÿåòñÿ
ñîâîêóïíîñòüþ
ñòåðè÷åñêèõ
ýôôåêòîâ çàìåñòèòåëåé
â íóêëåîôèëå
è ñóáñòðàòå
[46].
Kay è
Assink [63.95-97] èñïîëüçóÿ
ßÌÐ H1 è 29Si îïðåäåëèëè
çíà÷åíèÿ kh, kcw, kca âî âðåìåíè
íà÷àëüíûõ ñòàäèé
ïðè êèñëîòíî-êàòàëèçèðóåìîì
ãèäðîëèçå òåòðàìåòîêñèñèëàíà
è ðàññìîòðåëè
íåñêîëüêî êèíåòè÷åñêèõ
ìîäåëåé. Âàæíî
îòìåòèòü, ÷òî
êîíñòàíòû ñêîðîñòè
ãèäðîëèçà è êîíäåíñàöèè
îïðåäåëåíûå äëÿ
òåòðàìåòîêñèñèëàíà
çíà÷èòåëüíî
áîëüøå ÷åì ñîîòâåòñòâóþùèå
çíà÷åíèÿ äëÿ
òåòðàýòîêñèñèëàíà,
óêàçàííûå Pouxviel [62]. Ïîýòîìó
ñ óâåëè÷åíèåì
ýëåêòðîíî - äîíîðíûõ
ñâîéñòâ àëêîêñè-
ãðóïï ìîæíî áûëî
áû îæèäàòü óâåëè÷åíèÿ
çíà÷åíèé êîíñòàíò
ñêîðîñòåé ãèäðîëèçà
è êîíäåíñàöèè
(êèñëîòíî-êàòàëèçèðóåìûõ)
åñëè èíäóêöèîííûé
ýôôåêò èãðàåò
âàæíóþ ðîëü, íî
ýòîò ïðîòèâîïîëîæåííûé
ýôôåêò ïðåäïîëàãàåò,
÷òî äëÿ òåòðàôóíêöèîíàëüíûõ
àëêîêñèñèëàíîâ,
ñòåðè÷åñêèé,
à íå èíäóêöèîííûé
ýôôåêò ÿâëÿåòñÿ
áîëåå çíà÷èìûì
â îïðåäåëåíèè
çîëü-ãåëü êèíåòèêè.

Ðèñ. 13. Çàâèñèìîñòü
äîëè ðåàêöèé ÃÒÔÊ
è ÃÌÔÊ îò ñîîòíîøåíèÿ
âîäà/òåòðàìåòîêñèñèëàí
[38].
Çíà÷åíèÿ êðèâûõ
ïîêàçàííûõ íà
ðèñ. 13, ïîëó÷åíû
ñ ïîìîùüþ óðàâíåíèé
8,9. Î÷åâèäíî, ÷òî
ïðè ìàëåíüêèõ
çíà÷åíèÿõ m ïðåîáëàäàåò
äîëÿ ðåàêöèé ÃÒÔÊ,
ïðè m áîëüøèõ
0,6 ðåàêöèè ÃÌÔÊ
èãðàþò áîëåå
âàæíóþ ðîëü. Â
ñëó÷àå, êîãäà
êàæäàÿ êîíñòàíòà
ñêîðîñòè ãèäðîëèçà
è êîíäåíñàöèè
íàìíîãî áîëüøå
÷åì êîíñòàíòà
ñêîðîñòè ïðåäøåñòâóþùåé
ðåàêöèè, òîãäà
ìîãó ñóùåñòâîâàòü
òîëüêî 2 ìàòðè÷íûõ
âèäà (004) è (400). Îñíîâûâàÿñü
íà âëèÿíèè ñòåðè÷åñêîãî
è èíäóêöèîííîãî
ýôôåêòîâ îæèäàåìî,
÷òî íóêëåîôèëüíàÿ
àòàêà OH- (ãèäðîëèç) è
≡SiO- (êîíäåíñàöèÿ)
íà àòîì êðåìíèÿ
ìîæåò ïðîèçîéòè
â ñëó÷àå îñíîâíî-êàòàëèçèðóåìîé
ñèñòåìû. Íàîáîðîò,
êîãäà êîíñòàíòà
ñêîðîñòè êàæäîé
ïîñëåäóþùåé ñòàäèè
çíà÷èòåëüíî
ìåíüøå ïðåäøåñòâóþùåé,
ðåàêöèÿ ïðîõîäèò
âíèç ïî äèàãîíàëè
(ðèñ. 2) [38,55]. Îñíîâûâàÿñü
íà âàæíîñòè èíäóêöèîííîãî
ýôôåêòà, ìîæíî
ïðåäïîëîæèòü,
÷òî ýòîò ñëó÷àé
ñîîòâåòñòâóåò
êèñëîòíî-êàòàëèçèðóåìîé
ñèñòåìå, õîòÿ
èç ñòåðè÷åñêèõ
ðàññóæäåíèé,
îñîáåííî äëÿ
ãðîìîçäêèõ àëêîêñè-
ãðóïï, còåðè÷åñêèé
ýôôåêò ìîæåò
ïåðåâåøèâàòü
ëþáîé èíäóêòèâíûé
[23].
.1.3.5 Âëèÿíèå ðàñòâîðèòåëÿ
Èçâåñòíî, ÷òî
ðàñòâîðèòåëè
ñ âûñîêîé äèýëåêòðè÷åñêîé
ïðîíèöàåìîñòüþ
(íèòðîáåíçîë)
óñêîðÿþò êîíäåíñàöèþ
ñèëàíîëîâ [58]. Ñóùåñòâåííîå
âëèÿíèå íà ñêîðîñòü
âçàèìîäåéñòâèÿ
ñèëàíîëîâ ñ íóêëåîôèëàìè
îêàçûâàåò ñîëüâàòèðóþùàÿ
ñïîñîáíîñòü
ðàñòâîðèòåëÿ
[64] - ÷åì ïðî÷íåå
êîìïëåêñ ñèëàíîëà
ñ ðàñòâîðèòåëåì,
òåì òðóäíåå ïðîèñõîäèò
çàìåùåíèå ðàñòâîðèòåëÿ
íà íóêëåîôèëüíûé
ðåàãåíò. Ñîëüâàòèðóþùàÿ
ñïîñîáíîñòü
ðàñòâîðèòåëÿ
óáûâàåò â ðÿäó:
ïèðèäèí > äèìåòèëôîðìàìèä
> ìåòèëýòèëêåòîí
> àöåòîíèòðèë
> íèòðîìåòàí
[64]. Ðàñòâîðèòåëü
ñóùåñòâåííî
âëèÿåò íà ìåõàíèçì
ÃÌÔÊ, ÷òî ïîäòâåðæäàåòñÿ
äàííûìè ïî êîíäåíñàöèè
ñèëàíîëîâ ïîä
äåéñòâèåì 2-ýòèëãåêñîàòà-äè(í-ãåêñèë)àììîíèÿ
â ñðåäå ðàçëè÷íûõ
ðàñòâîðèòåëåé.
Òàê â àöåòîíå
ïîðÿäîê ïî ñèëàíîëó
- ïåðâûé, â äèîêñàíå
è ÄÌÔÀ - ≈ 3, â àöåòîíèòðèëå
- âòîðîé [38].
Artaki èññëåäîâàë
âëèÿíèå ïðîòîííûõ
è àïðîòîííûõ
ðàñòâîðèòåëåé
íà ñêîðîñòü ðîñòà
ïîëèñèëîêñàíîâ,
ïîëó÷åííûõ ïðè
ãèäðîëèçå òåòðàìåòîêèñèëàíà
(m=10) â íåéòðàëüíûõ
óñëîâèÿõ [65]. Ïîëó÷åííàÿ
êà÷åñòâåííàÿ
èíôîðìàöèÿ ïðåäñòàâëåíà
â òàáëèöå 9 è ñâÿçûâàåò
ðàçëè÷íûå ðàçìåðû
ïîëèñèêîêñàíîâ.
Òàáëèöà 9. Âðåìÿ
ãåëåîáðàçîâàíèÿ,
I[O] ïðè t/tgel=2, K (îòíîñèòåëüíàÿ
êîíñòàíòà ñêîðîñòè
ìîëèáäåíîâîé
êèñëîòû) äëÿ ãèäðîëèçà
òåòðàìåòîêñèñèëàíà
â ðàçëè÷íûõ ðàñòâîðèòåëÿõ.
|
Ðàñòâîðèòåëü
|
I[O]
|
K-1
|
Âðåìÿ
ãåëåîáðàçîâàíèÿ
(÷)
|
|
Ìåòàíîë
|
1
|
1
|
8
|
|
Ôîðìàìèä
|
1,3
|
1,3
|
6
|
|
Äèìåòèëôîðìàìèä
|
1,4
|
1,3
|
28
|
|
Àöåòîíèòðèë
|
1,7
|
1,9
|
23
|
|
Äèîêñàí
|
2,1
|
1,9
|
41
|
Èçó÷åíà ÃÌÔÊ
RMe2SiOH [47] è HO(SiMe2O)nH (n = 1 - 4) [66] â ãåòåðîãåííûõ
ñèñòåìàõ âîäà
- òîëóîë è âîäà
- ãåêñàìåòèëäèñèëîêñàí.
Ðàñïðåäåëåíèå
ñèëàíîëîâ è ïðîäóêòîâ
èõ êîíäåíñàöèè
õàðàêòåðèçóåòñÿ
«÷àñòíûìè» êîýôôèöèåíòàìè
ðàñïðåäåëåíèÿ
ìåæäó îðãàíè÷åñêîé
è âîäíîé ôàçàìè.
Óñòàíîâëåíî,
÷òî â ýòîé ñèñòåìå
ÃÌÔÊ ñèëàíîëîâ
ïðîòåêàåò íåðàâíîâåñíî
èç-çà íèçêîé
ðàñòâîðèìîñòè
ïðîäóêòîâ êîíäåíñàöèè
è, êàê ñëåäñòâèå,
íåïðåðûâíîé èõ
ýêñòðàêöèè â
îðãàíè÷åñêóþ
ôàçó. Àâòîðû ñ÷èòàþò,
÷òî âñëåäñòâèå
íèçêîé ðàñòâîðèìîñòè
âîäû è õëîðèñòîãî
âîäîðîäà â òîëóîëå,
êîíäåíñàöèè
ñèëàíîëîâ â îðãàíè÷åñêîé
ôàçå ïðàêòè÷åñêè
íå ïðîèñõîäèò,
ïîýòîìó ðåàêöèîííîé
ôàçîé ÿâëÿåòñÿ
âîäíàÿ ôàçà. Àâòîðû
îòìå÷àþò, ÷òî
ïåðåõîä ïðîäóêòîâ
êîíäåíñàöèè
â òîëóîëüíóþ
ôàçó îáëåã÷àåò
êîíòðîëü çà ñêîðîñòüþ
êîíäåíñàöèè
â âîäíîé ôàçå
ìåòîäàìè ÃÆÕ
è ÈÊ-ñïåêòðîñêîïèè.
ÃÌÔÊ Me3SiOH â ãåòåðîãåííîé
ñèñòåìå õàðàêòåðèçóåòñÿ
ôîðìàëüíî ïåðâûì
ïîðÿäêîì ïî ñèëàíîëó
è çíà÷åíèÿìè
ýíåðãèè àêòèâàöèè
35,0 è 35,8 êÄæ∙ìîëü-1
â ñèñòåìå òîëóîë-âîäà
è ãåêñàìåòèëäèñèëîêñàí-âîäà,
ñîîòâåòñòâåííî.
Ðàáîòû íåìåöêèõ
ó÷åíûõ óáåäèòåëüíî
ïîêàçûâàþò, ÷òî
ó÷åò ôàçîâîãî
êâàçèðàâíîâåñèÿ
âàæåí â ïðîöåññå
ÃÌÔÊ ñèëàíîëîâ
[66]. Ðàçëè÷èå â ðàñòâîðèìîñòè
ñèëîêñàíîëîâ
ÿâèëîñü ïðè÷èíîé
ñïåöèôè÷åñêîãî
ïðîòåêàíèÿ êîíäåíñàöèè
òåòðàìåòèëäèñèëîêñàí-1,3-äèîëà
è ãåêñàìåòèëòðèñèëîêñàí-1,5-äèîëà.
Óñòàíîâëåíî,
÷òî îòíîñèòåëüíî
õîðîøî ðàñòâîðèìûé
â âîäå òåòðàìåòèëäèñèëîêñàí-1,3-äèîë
ïðåâðàùàåòñÿ
ñî 100% ñåëåêòèâíîñòüþ
â îêòàìåòèëòåòðàñèëîêñàí-1,7-äèîë
áëàãîäàðÿ îòíîñèòåëüíî
âûñîêîé êîíöåíòðàöèè
â âîäíîé ôàçå
ïåðâîãî è áûñòðîé
ýêñòðàêöèè ïîñëåäíåãî
â îðãàíè÷åñêóþ
ôàçó. È íàîáîðîò,
ïëîõî ðàñòâîðèìûé
ãåêñàìåòèëòðèñèëîêñàí-1,5-äèîë,
âñëåäñòâèå åãî
íèçêîé êîíöåíòðàöèè
â âîäíîé ôàçå,
ïðåâðàùàåòñÿ
â ãåêñàìåòèëöèêëîòðèñèëîêñàí
[66].
Âòîðîé è âàæíåéøèé
ýôôåêò ðàñòâîðèòåëÿ,
êîòîðûé äîëãîå
âðåìÿ èãíîðèðîâàëñÿ
ýòî ñïîñîáíîñòü
ñïîñîáñòâîâàòü
îáðàòèìûì ðåàêöèÿì.
Her ïðåäëîæèë
[35], ÷òî ïðè óñëîâèÿõ
â êîòîðûõ ïîäàâëÿþòñÿ
îáðàòíûå ðåàêöèè,
êîíäåíñàöèÿ
ìîæåò ïðèâåñòè
ê ìîëåêóëÿðíûì
ñåòêàì, â ïðîòèâîïîëîæåííûõ
óñëîâèÿõ æå ïðèâîäèò
ê âûñîêî - ñæàòûì
êîëîèäíûì ÷àñòèöàì.
.1.3.6 Âëèÿíèå îáðàòíûõ
ðåàêöèé
Àëêîãîëèç è
ãèäðîëèç ñèëîêñàíîâîé
ñâÿçè (óðàâíåíèÿ
2 è 3) ñïîñîáñòâóåò
ðàçðûâó ñâÿçè
è ïðåîáðàçîâàíèþ,
ïîçâîëÿþùèìó
îñóùåñòâëÿòü
ïîñòîÿííóþ ïåðåñòðîéêó
ðàñòóùåãî ïîëèìåðà.
Ñêîðîñòü ãèäðîëèçà
ñèëîêñàíîâîé
ñâÿçè îáëàäàåò
ñèëüíîé pH-çàâèñèìîñòüþ,
êàê ìîæíî âèäåòü
íà ðèñ. 12. Ïðèìåðíî
ìåæäó pH 3 è 8 ñêîðîñòü ðàçðóøåíèÿ
ñèëîêñàíîâîé
ñâÿçè óâåëè÷èâàåòñÿ
áîëåå ÷åì íà 3 ïîðÿäêà
â âîäíûõ ðàñòâîðàõ.
×àñòè÷íîå ðàçáàâëåíèå
ñèñòåìû âîäîé
(äî pH=9,5) óìåíüøàåò
çíà÷åíèå ðàñòâîðèìîñòè
íà 20, êàê ïîêàçàíî
â òàáëèöå 10.
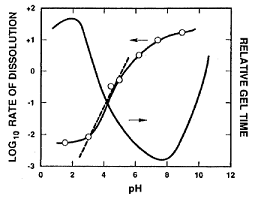
Ðèñ. 14. pH-çàâèñèìîñòü
îò ñêîðîñòè ðàñòâîðåíèÿ
è âðåìåíè ãåëåîáðàçîâàíèÿ.
Klemperer è
ñîòðóäíèêè [67] ïðèâåëè
ìåõàíèçì ïðè
êîòîðîì àëêîãîëèç
ïðîèñõîäèò â
ùåëî÷íîé ñðåäå,
ïîñðåäñòâîì ïåðåðàñïðåäåëåíèÿ
ñèëîêñàíîâîé
ñâÿçè.
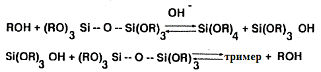 (33)
(33)
Ïåðåðàñïðåäåëåíèå
 (34)
(34)
 ýòèõ ðåàêöèÿõ
ïðè îñíîâíûõ
óñëîâèÿõ íåïðîðåàãèðîâàâùèé
ìîíîìåð îñòàåòñÿ
äàæå ïðè äîáàâëåíèè
êîëè÷åñòâà âîäû
âûøå ñòåõèîìåòðè÷åñêîãî.
Îñíîâûâàÿñü
íà ðåçóëüòàòàõ
ÃÆÕ è ßÌÐ Si29 ïîêàçàëè, ÷òî
ñëåäñòâèåì ðåàêöèè
ïåðåðàñïðåäåëåíèÿ
â «ïåðåâåðíóòîì»
ìîëåêóëÿðíî-ìàññîâîì
ðàñïðåäåëåíèè
áîëüøèå è ìàëåíüêèå
ìîëåêóëÿðíî-ìàññîâûå
âèäû ÿâëÿþòñÿ
ìàêñèìàëüíûìè
ïî îòíîøåíèþ
ê ìîëåêóëÿðíî-ìàññîâûì
èíòåðìåäèàòàì
[67;68].
 ñîîòâåòñòâèè
ñ Her [35] ðàñòâîðåíèå
àìîðôíûõ ìîëåêóë
ïðè pH âûøå 2 êàòàëèçèðóåòñÿ
èîíàìè OH-, êîòîðûå âîçìîæíî
óâåëè÷èâàþò
êîîðäèíàöèþ êðåìíèÿ
âûøå 4, îñëàáëÿÿ
îêðóæàþùèå ñèëîêñàíîâûå
ñâÿçè. Ýòîò îáùèé
íóêëåîôèëüíûé
ìåõàíèçì ïðåäïîëîæèòåëüíî
ìîæåò ïðîèñõîäèòü
÷åðåç SN2-Si, SN2**-Si èëè SN2*-Si ïåðåõîäíûå
ñîñòîÿíèÿ èëè
èíòåðìåäèàòû
è ìîæåò â ðàâíîé
ñòåïåíè îáúÿñíÿòü
äåïîëèìåðèçàöèîííûå
ìåõàíèçìû àëêîêñè
èîíîâ è èîíîâ
ôòîðà.
Òàáëèöà 10. Ðàñòâîðèìîñòü
ñèëîêñàíà â âîäíî
- ìåòàíîëüíîì
ðàñòâîðå [35].
|
Ìåòèëîâûé
ñïèðò (Ìàññ. %)
|
Ðàñòâîðèìîñòü
ïðè 25 0Ñ
|
|
0
|
140
|
|
25
|
75
|
|
50
|
40
|
|
75
|
15
|
|
100
|
5
|
Â. Ãðàáá è Ç. Ëÿñîöêèé
ñ ñîàâòîðàìè
óñòàíîâèëè, ÷òî
ÃÌÔÊ R2Si(OH)2 â ñðåäå ìåòàíîëà
ÿâëÿåòñÿ ðàâíîâåñíûì
ïðîöåññîì [39, 45, 52], ñêîðîñòü
êîòîðîãî îïèñûâàåòñÿ
óðàâíåíèåì:
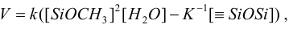
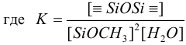 (35)
(35)
Îäíàêî ýòî óðàâíåíèå
ñïðàâåäëèâî òîëüêî
äî 50% êîíâåðñèè
ìîíîìåðà, òàê
êàê äàëåå ñêîðîñòü
ïðîöåññà ðåçêî
ïàäàåò èç-çà óìåíüøåíèÿ
ðåàêöèîííîé
ñïîñîáíîñòè
îëèãîñèëîêñàíäèîëîâ.
Äëÿ êèñëîòíî-êàòàëèçèðóåìîé
ÃÌÔÊ Me2Si(OH)2 Ê = 17,5 (25 îÑ)
[39].  ñëó÷àå îñíîâíîãî
êàòàëèçà äëÿ
çàìåùåííûõ ìåòèëôåíèëñèëàíäèîëîâ
çíà÷åíèå êîíñòàíòû
ðàâíîâåñèÿ íàõîäèòñÿ
â èíòåðâàëå 40 -
54 (25 îÑ) è î÷åíü
ìàëî çàâèñèò
îò ïðèðîäû çàìåñòèòåëåé
[52]. Ïîêàçàíî, ÷òî
êîíñòàíòà ðàâíîâåñèÿ
íå çàâèñèò îò
íà÷àëüíûõ êîíöåíòðàöèé
êîìïîíåíòîâ
ðåàêöèîííîé
ñèñòåìû [52].
ÃÌÔÊ òðèîðãàíîñèëàíîëîâ
â âîäíî - äèîêñàíîâîì
ðàñòâîðå, êàòàëèçèðóåìàÿ
HCl, ÿâëÿåòñÿ ðàâíîâåñíûì
ïðîöåññîì. Òàê
êîíñòàíòà ðàâíîâåñèÿ
Me3SiOH â ïðèñóòñòâèè
HCl ðàâíà 130 ± 10 íåçàâèñèìî
îò ñïîñîáà äîñòèæåíèÿ
ðàâíîâåñíîãî
ñîñòîÿíèÿ [69]. Â
îòëè÷èå îò ÃÌÔÊ
R2Si(OH)2 â ñðåäå ìåòàíîëà
(ñ ÊÎÍ) çíà÷åíèÿ
êîíñòàíò ðàâíîâåñèÿ
äëÿ îðãàíîäèìåòèëñèëàíîëîâ
ñèëüíî çàâèñÿò
îò ïðèðîäû çàìåñòèòåëåé
ó àòîìà êðåìíèÿ
[57, 63]. Äëÿ àðèëñèëàíîëîâ
õàðàêòåðíû íèçêèå
çíà÷åíèÿ Ê (2 - 7), äëÿ
ãàëîèäçàìåùåííûõ
ñèëàíîëîâ ïðîÿâëÿåòñÿ
ñèëüíîå âëèÿíèå
ãàëîèäà íà Ê
(ClCH2 - 24, BrCH2 - 86). Íà îñíîâå
çíà÷åíèé êîíñòàíò
ðàâíîâåñèÿ è
êîíñòàíò ñêîðîñòè
ïðÿìûõ ðåàêöèè
áûëè ðàññ÷èòàíû
êîíñòàíòû îáðàòíûõ
ðåàêöèé (ðàñùåïëåíèÿ
≡SiOSi≡), êîòîðûå ïðîâåðåíû
äëÿ ðÿäà ñîåäèíåíèé
ýêñïåðèìåíòàëüíî.
Ðàñ÷åò êîíñòàíò
ðàñùåïëåíèÿ ñèëîêñàíîâ
ïðîâåäåí â ïðåäïîëîæåíèè,
÷òî ñêîðîñòü
ðàñùåïëåíèÿ îðãàíîñèëîêñàíà
çàâèñèò îò êîíöåíòðàöèè
âîäû â ïåðâîé ñòåïåíè,
õîòÿ ýòî è íå äîêàçàíî:
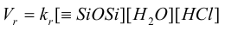 (36)
(36)
Îêàçàëîñü, ÷òî
êîððåëÿöèÿ êîíñòàíò
ðàñùåïëåíèÿ ñèëîêñàíîâ
(kr) ñ èíäóêöèîííûìè
è ñòåðè÷åñêèì
õàðàêòåðèñòèêàìè
çàìåñòèòåëåé
ïðàêòè÷åñêè
íå ñîáëþäàåòñÿ
íè â êèñëîòíîì,
íè â îñíîâíîì
êàòàëèçå [57, 63]. Íå
íàáëþäàåòñÿ
êîððåëÿöèÿ è ñ
äàííûìè ïî îñíîâíîñòè
ãåêñàîðãàíîäèñèëîêñàíîâ.
Àâòîðû îòìå÷àþò,
÷òî âñå æå ïðîñìàòðèâàåòñÿ
òåíäåíöèÿ óìåíüøåíèÿ
kr ñ óâåëè÷åíèåì
ýëåêòðîíîàêöåïòîðíûõ
è ñòåðè÷åñêèõ
ñâîéñòâ çàìåñòèòåëåé.
Ïðåäïîëàãàåòñÿ,
÷òî îòíîñèòåëüíûé
ñóììàðíûé âêëàä
èíäóêöèîííîãî
è ñòåðè÷åñêîãî
âëèÿíèÿ çàìåñòèòåëåé
ðàçëè÷åí â ïðÿìîé
è îáðàòíîé ðåàêöèÿõ.
 ðàáîòå [48] îòìå÷àåòñÿ
òàêæå, ÷òî ñòàäèÿ
äåïðîòîíèðîâàíèÿ
(3) ÿâëÿåòñÿ áûñòðîé,
âåðîÿòíî âñëåäñòâèå
íèçêîé îñíîâíîñòè
ñåðåäèííîãî
àòîìà êèñëîðîäà.
Íåîáõîäèìî
îòìåòèòü, ÷òî
ïî äàííûì Ì.Ã. Âîðîíêîâà
è Ë.À. Æàãàòû êèñëîòíûé
ãèäðîëèç ãåêñàîðãàíîäèñèëîêñàíîâ
ÿâëÿåòñÿ ðåàêöèåé
âòîðîãî ïîðÿäêà
ïî âîäå [70]. Íà îñíîâàíèè
ýòîãî àâòîðû
ïðåäïîëàãàþò,
÷òî ãèäðîëèòè÷åñêîå
ðàñùåïëåíèå ñâÿçè
≡SiOSi≡ ïðîòåêàåò
÷åðåç ïðîìåæóòî÷íûé
øåñòè÷ëåííûé
àêòèâíûé êîìïëåêñ,
ñîäåðæàùèé äâå
ìîëåêóëû âîäû,
îäíà èç êîòîðûõ
ïðîòîíèðîâàíà:
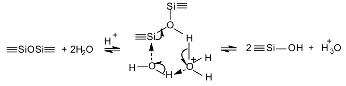 (37)
(37)
Âðåìÿ óñòàíîâëåíèÿ
ðàâíîâåñèÿ ñîêðàùàåòñÿ
ñ óâåëè÷åíèåì
êîíöåíòðàöèè
êàòàëèçàòîðà.
Àíàëîãè÷íûé
ìåõàíèçì ïðåäëàãàåòñÿ
è äëÿ ðàñùåïëåíèÿ
ñèëîêñàíîâ ïðîòîííûìè
êèñëîòàìè [70].
Îòñóòñòâèå
êîððåëÿöèè êîíñòàíòû
ðàñùåïëåíèÿ ãåêñàîðãàíîäèñèëîêñàíîâ
kr â èññëåäîâàíèÿõ
íåìåöêèõ ó÷åíûõ
îáóñëîâëåíî,
òåì, ÷òî íà ñàìîì
äåëå ðàñùåïëåíèå
ñâÿçè ≡SiOSi≡ íå ÿâëÿåòñÿ
îáðàòíîé ðåàêöèåé
îáðàçîâàíèþ
ýòîé ñâÿçè ïî
ìåõàíèçìó ÃÌÔÊ
è ïðîòåêàåò ïî
ìåõàíèçìó, ïðåäëîæåííîìó
â ðàáîòàõ [63, 70, 71]. Ïðàâäà
è â ýòîì ñëó÷àå
(6) âëèÿíèå çàìåñòèòåëåé
ó äâóõ àòîìîâ
êðåìíèÿ íà ñòàáèëüíîñòü
òàêîãî êîìïëåêñà
áóäåò íåîäèíàêîâûì.
Îäíàêî ýòîò âîïðîñ
äåòàëüíî íå èññëåäîâàí.
Èçâåñòíî, ÷òî
ëåã÷å âñåãî ãèäðîëèçóåòñÿ
ãåêñàôåíèëäèñèëîêñàí,
à íàèáîëåå óñòîé÷èâûì
ê ãèäðîëèçó ÿâëÿåòñÿ
Ph3SiOSi(o-Tol)3 [72]. Èìåþòñÿ
è ïðÿìî ïðîòèâîïîëîæíûå
äàííûå î òîì, ÷òî
ïðè ðàñùåïëåíèè
ñèëîêñàíîâ â
î÷åíü êèñëîé
ñðåäå (FSO3H - SbF5 - SO2)
íåñèììåòðè÷íûé
òðèìåòèëòðèôåíèëäèñèëîêñàí
ðàñùåïëÿåòñÿ
ëåã÷å, ÷åì ãåêñàìåòèëäèñèëîêñàí
[73].
.2 Ñïîñîáû îöåíêè
ôîðìèðîâàíèÿ
öåïè îëèãîîðãàíîñèëîêñàíîâ
 ðàáîòå Ñîêîëîâà
Ë.Á. âïåðâûå áûëî
ïðåäëîæåíî ðàçëè÷àòü
ïîëèêîíäåíñàöèþ
îò ïîëèìåðèçàöèè
ñðàâíåíèåì çàâèñèìîñòåé
êîíâåðñèè ìîíîìåðà
(ÕÌ) îò êîíâåðñèè
ôóíêöèîíàëüíûõ
ãðóïï (Xf). Â ïðåäåëüíûõ
âàðèàíòàõ ïîëèêîíäåíñàöèÿ
- ýòî ñáîðêà óäâîåíèåì,
â êîòîðîé ïîëíàÿ
êîíâåðñèÿ ìîíîìåðà
â äèìåð ñîïðîâîæäàåòñÿ
äâîéíîé êîíâåðñèåé
ôóíêöèîíàëüíûõ
ãðóïï. Ïîëèìåðèçàöèîííûé
ïðîöåññ ÿâëÿåòñÿ
ïðîöåññîì ïîçâåííîé
ñáîðêè, ïðè êîòîðîì
ïîëíîé êîíâåðñèè
ìîíîìåðà ñîîòâåòñòâóåò
ïîëíàÿ êîíâåðñèÿ
ôóíêöèîíàëüíûõ
ãðóïï.
Àâòîðû ðàáîòû
[64] îòìå÷àþò, ÷òî
óðàâíåíèå Êàðîçåðñà
îòðàæàåò áëî÷íûé
ñïîñîá ôîðìèðîâàíèÿ
ïîëèìåðà, íî îíî
èíâàðèàíòíî
ê óñëîâèÿ ïðîâåäåíèÿ
ïîëèêîíäåíñàöèîííîãî
ïðîöåññà è ïîýòîìó
íåèíôîðìàòèâíî.
Ïî ýòîé ïðè÷èíå
óðàâíåíèå Êàðîçåðñà
â ïðàêòèêå ýêñïåðèìåíòàëüíîé
è òåîðåòè÷åñêîé
ðàáîòû (â îòëè÷èå
îò óðàâíåíèÿ
Ôëîðè) íå èñïîëüçóåòñÿ.
 òî æå âðåìÿ, â
ïîñëåäíèå äåñÿòèëåòèÿ
ïîñòîÿííî âîçðàñòàåò
èíòåðåñ ê èçó÷åíèþ
íà÷àëüíûõ ñòàäèé
ïîëèêîíäåíñàöèè,
ó÷åòó ýôôåêòîâ
áëèæíåãî è äàëüíåãî
ïîðÿäêîâ â õèìè÷åñêîé
ñáîðêå ïîëèìåðîâ,
õèìèè îëèãîìåðîâ
âîîáùå. Òàê, íàïðèìåð,
äëÿ ó÷åòà ýôôåêòîâ
áëèæíåãî ïîðÿäêà
(èëè çàìåùåíèÿ
â áëèæíåé ñôåðå)
ïðåäëàãàåòñÿ
ìîäèôèöèðîâàííîå
óðàâíåíèå Êàðîçåðñà
[65]:
n=1/(1-λx),
Ãäå λ = ki/k1. Ïðè λ = 1 ýòî óðàâíåíèå
ôîðìàëüíî ïåðåõîäèò
â óðàâíåíèå Êðîçåðñà:
n=1/(1-1*x),
íî ïî ñóùåñòâó
åìó íå ñîîòâåòñòâóåò,
òàê êàê ïîñëåäíåå
óðàâíåíèå ñîîòâåòñòâóåò
ïðåäåëüíî áëî÷íîé
ñáîðêå, òî åñòü
êîãäà k1 ˃˃
ki, êîãäà
ìîíîìåð â ñèñòåìå
îòñóòñòâóåò
óæå ïîñëå ïåðâîãî
àêòà êîíäåíñàöèè.
Òàê ÷òî ââåäåíèå
λ â
ôîðìóëó Êàðîçåðñà
îøèáî÷íî. Èíâàðèàíòíîñòü
óðàâíåíèÿ Êàðîçåðñà
îáóñëîâëåíà,
î÷åâèäíî, òåì,
÷òî âåëè÷èíà
n - ýòî ñðåäíåå
çíà÷åíèå ñòåïåíè
ïîëèìåðèçàöèè
âñåé ïîëèìåðíîé
ñèñòåìû, òî åñòü
ñîäåðæàùåé ìîíîìåð.
Òàêîé ïîêàçàòåëü
íå õàðàêòåðèçóåò
ñàì îáðàçóþùèéñÿ
ïîëèìåð è âëèÿíèå
óñëîâèé ïðîöåññà
íà åãî ìîëåêóëÿðíóþ
ìàññó.
 ýòîé ñâÿçè
â ðàáîòå [64] ðàññìîòðåíà
ñòåïåíü ïîëèìåðèçàöèè
ïîëèìåðà np êàê:
np=(M0-Mt)/Pt
ãäå M0, Mt - êîëè÷åñòâî
ìîëåêóë ìîíîìåðà
â íà÷àëå è êîíöå
ïðîöåññà,
Pt - êîëè÷åñòâî
ìîëåêóë ïîëèìåðà.
Ðåøåíèå ýòîãî
óðàâíåíèÿ ïîçâîëÿåò
íàì íàéòè âçàèìîñâÿçü
np ñ êîíâåðñèåé
ôóíêöèîíàëüíûõ
ãðóïï - Xf è ìîíîìåðà XM â âèäå:
np=1/(1-XM/Xf) (1)
Äëÿ ãåòåðîñîïîëèêîíäåíñàöè
ñîìîíîìåðîâ
À è Â (ìîíîìåð Â
â èçáûòêå, q=A/B) èçâåñòíîå
óðàâíåíèå Ïèííåðà
èëè ïðàâèëî íåýêâèìîëüíîñòè
(1+q)/(1+q-2qx)
Çàïèøåòñÿ â
âèäå:
np=1/2[(1-XfA/XMA+1/(1-XfB/XMB)] (2)
np=(XMA+qXMB)/((XMA+qXMB-2XfB) (2a)
Ïðè XM=1 óðàâíåíèå (1)
è XM(A,B)=1, q=1 óðàâíåíèå
(2) ïåðåõîäÿò â óðàâíåíèå
Êàðîçåðñà.  îòëè÷àå
îò ïîñëåäíåãî
óðàâíåíèÿ (1) è
(2) ÿâëÿþòñÿ îáùèìè
äëÿ âñåãî ïîëèêîíäåíñàöèîííîãî
ïðîöåññà: îò íà÷àëüíûõ
ñòàäèé (òî åñòü
ïðè XM≤1)
äî êîíöà (Xf→1). Âàæíî îòìåòèòü
÷òî óðàâíåíèÿ
(1) èëè(2) ñîäåðæàò
â ñåáå èíôîðìàöèþ
î âëèÿíèè óñëîâèé
ïðîâåäåíèÿ ïðîöåññà
íà ìîëåêóëÿðíóþ
ìàññó ïîëèìåðà.
Ýòà èíôîðìàöèÿ
îïîñðåäîâàííî
çàêëþ÷àåòñÿ
â ñîîòíîøåíèè
Xf/XM, â êîòîðîì
çíàìåíàòåëü
ìîæåò áûòü êàê
ôóíêöèÿ îò Xf, íàïðèìåð,
XM=aXf-bXfc. Òàê ïðè
ñòàòèñòè÷åñêîé
ñáîðêè ìàêðîìîëåêóëû
èç ìîíîìåðîâ
ñ íåçàâèñèìûìè
ôóíêöèîíàëüíûìè
ãðóïïàìè (λ = ki/k1=1) çàâèñèìîñòü
XM=f(Xf) ëåãêî
ïîëó÷èòü èç óðàâíåíèÿ
Ni=(1-x)x(n-1) Ôëîðè: XM=2Xf-Xf2. Êîìáèíàöèÿ
ïîëó÷åííîãî
âûðàæåíèÿ ñ óðàâíåíèåì
(1) äàåò èñêîìóþ
çàâèñèìîñòü
â âèäå 1/np=(1-Xf)/(2-Xf). Òàê êàê
ýêñïåðèìåíòàëüíî
íå âñåãäà âîçìîæíî
îöåíèòü âåëè÷èíó
XM, òî ïîñëåäíåå
âûðàæåíèå ïîìîæåò
ïî äàííûì ÃÏÕ
èëè âèñêîçèìåòðèè
êîñâåííî îöåíèòü
np è â èòîãå
õàðàêòåð ôîðìèðîâàíèÿ
ìàêðîìîëåêóëû.
Åñëè XM=2Xf, òî ïðè
Xf=0,5 XM =1 è ìû èìååì
áëî÷íóþ ñáîðêó
â ÷èñòîì âèäå
(ëèíèÿ ÎÀÑ). Åñëè
XM≈ Xf, òî ìû èìååì
äåëî ñ ïîçâåííîé
(ïîëèìåðèçàöèîííîé)
ñáîðêîé èëè ñ
èíòåíñèâíûì
ïðîöåññîì öèêëîîáðàçîâàíèÿ
(ÎÂÑ).
2. Îáñóæäåíèå
ðåçóëüòàòîâ
Êàê ïîêàçàíî
â ëèòåðàòóðíîì
îáçîðå, àâòîðû
ðàáîòû ëîãè÷íî
ïðåäïîëàãàþò,
÷òî â ÷àñòè÷íîì
ãèäðîëèçå îðãàíîàëêîêñèñèëàíîâ
ôîðìèðîâàíèå
îëèãîìåðíîé
öåïè ìîæåò ïðîõîäèòü
ïî ìåõàíèçìàì
ãîìîôóíêöèîíàëüíîé
è ãåòåðîôóíêöèîíàëüíîé
êîíäåíñàöèè
ïðîäóêòîâ ãèäðîëèçà.
Îäíàêî ýêñïåðèìåí
Ýêñïåðèìåíòàëüíî
óñòàíîâëåíî
[80], ÷òî ðîñò öåïè
ïî ìåõàíèçìó
ÃÒÔÊ â ÷àñòè÷íîì
ãèäðîëèçå R2SiCl2 õàðàêòåðèçóåòñÿ
çíà÷èòåëüíîé
äîëåé ïîçâåííîé
ñáîðêè, ò.å. àêòàìè
ïðèñîåäèíåíèÿ
ê ðàñòóùåé öåïè
ìîëåêóë ìîíîìåðà.
Àíàëèç ëèòåðàòóðíûõ
äàííûõ ïîêàçàë
[80; 81; 82], ÷òî óïðàâëÿÿ
èíòåíñèâíîñòüþ
ïðîòåêàíèÿ ÃÒÔÊ
ìîæíî íàïðàâëÿòü
ïðîöåññ ïîëèêîíäåíñàöèè
â ñòîðîíó ëèíåéíûõ
èëè öèêëè÷åñêèõ
ñîåäèíåíèé.
 ñâÿçè ñ òåì,
÷òî óæå ìíîãèå
ãîäû âíèìàíèå
èññëåäîâàòåëåé
íàïðàâëåíî íà
ñèíòåç âûñîêîôóíêöèîíàëüíûõ
öèêëîâ, ëåñòíè÷íûõ
îëèãîìåðîâ è
ïîëèìåðîâ, ïîëèýäðè÷åñêèõ
ñèëñåñêâèîêñàíîâ
(POSS) è íà òàêóþ
îáøèðíóþ îáëàñòü,
êàê îáëàñòü çîëü-ãåëü
òåõíîëîãèè, ïðåäñòàâëÿëî
èíòåðåñ èññëåäîâàòü
ÃÏÊ îðãàíîòðèàëêîêñèñèëàíîâ
ñ ïîçèöèè ôîðìèðîâàíèÿ
öåïè è óñòàíîâèòü
êàêîé âàðèàíò
ñáîðêè èç âîçìîæíûõ
ÿâëÿåòñÿ ïðèîðèòåòíûì.
 ýòîé ñâÿçè
öåëüþ íàøåé ðàáîòû
ÿâëÿåòñÿ èçó÷åíèå
õèìè÷åñêîé ñáîðêè
â ïðîöåññå ãèäðîëèòè÷åñêîé
ïîëèêîíäåíñàöèè
îðãàíîòðèàëêîêñèñèëàíîâ.
2.1 Ìåòîäîëîãèÿ
ýêñïåðèìåíòà
Ãëàâíûì èíñòðóìåíòîì
àíàëèçà è êðèòåðèåì
ôîðìèðîâàíèÿ
îëèãîìåðíîé
öåïè â íàøåé ðàáîòå
ÿâëÿåòñÿ çàâèñèìîñòü
êîíâåðñèè ìîíîìåðà
(XM) îò êîíâåðñèè
ôóíêöèîíàëüíûõ
ãðóïï (Xf), ïðåäëîæåííûé
âïåðâûå â ðàáîòå
[79] êðèòåðèé XM=f(Xf) ó÷èòûâàë
òîëüêî êèíåòè÷åñêèé
àñïåêò, à êîëè÷åñòâåííûé
àñïåêò â âèäå
ìîäèôèöèðîâàííîãî
óðàâíåíèÿ Êàðîçåðñà
ñîäåðæàë îøèáêó.
Êîîðäèíàòíîå
ïðîñòðàíñòâî
XM - Xf ñëóæèò íàì
èíñòðóìåíòîì
äëÿ îöåíêè, êàê
êèíåòè÷åñêèõ,
òàê è òåðìîäèíàìè÷åñêèõ
è ñòðóêòóðíûõ
ôàêòîðîâ. Ýêñïåðèìåíòàëüíûå
äàííûå, ïîìåùåííûå
â ýòè êîîðäèíàòû
ìîãóò îòðàæàòü:
1. Ñîîòíîøåíèå
áëî÷íîé ñáîðêè
è ïîçâåííîé ñáîðêè
îáóñëîâëåííîå:
o êèíåòè÷åñêèìè
ôàêòîðàìè (èçìåíåíèå
ðåàêöèîííîé
ñïîñîáíîñòè
îëèãîìåðà)
o ìàêðîêèíåòè÷åñêèìè
ôàêòîðàìè (ãåòåðîôàçíîñòü
ïðîöåññà)
2. Ïðîöåññû öèêëèçàöèè
. Ïðîöåññû ïîëèìåðèçàöèè
4. Îáðàòèìîñòü
ïðîöåññà è ðåàêöèè
ìåæöåïíîãî îáìåíà.
Äëÿ ïîëó÷åíèÿ
çàâèñèìîñòåé
XM=f(Xf) ìû
ïðîâîäèëè àíàëèç
ñîñòàâà îëèãîìåðîâ
îáðàçóþùèõñÿ
â ÃÏÊ RSi(OR’)3. Ñîåäèíåíèÿ
èäåíòèôèöèðîâàëèñü
ñ ïîìîùüþ ýòàëîííûõ
îáðàçöîâ MeSi(OEt)3 è PhSi(OMe)3,
ñòðóêòóðà êîòîðûõ
áûëà ïîäòâåðæäåíà
ìåòîäîì ßÌÐ. Èäåíòèôèêàöèÿ
îëèãîìåðîâ ïðîâîäèëàñü
ñ ïîìîùüþ ãðàôèêà
çàâèñèìîñòè
âðåìåí óäåðæèâàíèÿ
îò íîìåðà ÷ëåíà
ãîìîëîãè÷åñêîãî
ðÿäà. Ðàñ÷åò õðîìàòîãðàìì
îñóùåñòâëÿëñÿ
ïî ïëîùàäÿì ïèêîâ
ìåòîäîì íîðìèðîâêè
ñ ïîïðàâî÷íûìè
êîýôôèöèåíòàìè.
Ïî äàííûì ÃÆÕ
îïðåäåëÿëè îòíîñèòåëüíûé
ìîëüíûé ñîñòàâ
(S, ìîë. ä.) ïðîäóêòîâ
èçó÷àåìûõ ðåàêöèé
ïî ôîðìóëå:
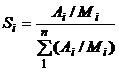 ,
,
ãäå
À - ïîêàçàíèÿ ïðèáîðà
(ïëîùàäü èëè èíòåíñèâíîñòü
ïèêà, èñïðàâëåííàÿ
ñ ó÷åòîì ïîïðàâî÷íîãî
êîýôôèöèåíòà).
Òåêóùèå
êîíöåíòðàöèè
ïðîäóêòîâ êîíäåíñàöèè
(Ñi, ìîëü/ë) ðàññ÷èòûâàëè
èñõîäÿ èç íà÷àëüíîé
êîíöåíòðàöèè
ìîíîìåðà Ñ0,
ñîîòíîøåíèé
ìàòåðèàëüíîãî
áàëàíñà è óñëîâèÿ
íîðìèðîâêè (ñì.
ýêñïåðèìåíòàëüíóþ
÷àñòü):
Ñ0-Ñ1=2Ñ2+3Ñ3+...+nCn;
S(Cn/ SCn) =
1
Ñòåïåíü
ïðåâðàùåíèÿ ìîíîìåðà
- Xm è
ñòåïåíü ïðåâðàùåíèÿ
ôóíêöèîíàëüíûõ
ãðóïï (OR èëè Ñl) - Xf ðàññ÷èòûâàëè
ïî èçâåñòíûì
ôîðìóëàì:



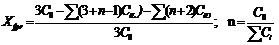 ,
,
ãäå
n - ñòåïåíü ïîëèìåðèçàöèè;
Xfpr
- "ïðèâåäåííàÿ"
ñòåïåíü ïðåâðàùåíèÿ
ôóíêöèîíàëüíûõ
ãðóïï (f = OR èëè Ñl), òî
åñòü áåç ó÷åòà
ðàñõîäîâàíèÿ
ôóíêöèîíàëüíûõ
ãðóïï â àêòå öèêëèçàöèè
ëèíåéíîé ìîëåêóëû;
Ñ0
è Ñi, - íà÷àëüíàÿ
è êîíå÷íàÿ êîíöåíòðàöèè
ìîíîìåðà;
ÑiL è CiD - êîíöåíòðàöèè
ëèíåéíûõ è öèêëè÷åñêèõ
ïðîäóêòîâ ê ìîìåíòó
çàâåðøåíèÿ ðåàêöèè.
Íà
îñíîâàíèè ýòèõ
äàííûõ ñ ïîìîùüþ
ïðîãðàììû «Ñîñòàâ
ïîëèìåðà» [àâòîðû
ïðîãðàììû: ïðîô.
Èâàíîâ Ï.Â., äîö.
Îäèíöîâ Ê.Þ. Ìîñêâà,
ÌÈÒÕÒ. 2000] ïî óêàçàííûì
âûøå ôîðìóëàì
ðàññ÷èòûâàëè
êîíâåðñèþ ïî ìîíîìåðó
è êîíâåðñèþ ïî
ôóíêöèîíàëüíûì
ãðóïïàì. Àíàëèç
çàâèñèìîñòè
XM=f(Xf) (ðèñ. 2.1) îöåíèâàþò
ñëåäóþùèì îáðàçîì:
ëèíèÿ ÎÀ îòâå÷àåò
ëèíèè ïðåäåëüíîé
áëî÷íîé ñáîðêè
â ïîëèêîíäåíñàöèè;
ñ òî÷êè çðåíèÿ
êèíåòèêè ýòî
îçíà÷àåò, ÷òî
êîíñòàíòà ñêîðîñòè
âçàèìîäåéñòâèÿ
ìîíîìåð + ìîíîìåð
çíà÷èòåëüíî
áîëüøå ÷åì êîíñòàíòà
ñêîðîñòè âçàèìîäåéñòâèÿ
ìîíîìåð + îëèãîìåð,
ñëåäîâàòåëüíî,
ìîíîìåð ðàñõîäóåòñÿ
ïî÷òè ìãíîâåííî.
Ýòîò ïîñòóëàò
è ëåæèò â îñíîâå
óðàâíåíèÿ Êàðîçåðñà.
Ïî ìåðå óâåëè÷åíèÿ
ðåàêöèîííîé
ñïîñîáíîñòè
îëèãîìåðîâ, ìû
áóäåì ïîëó÷àòü
â êîîðäèíàòàõ
XM - Xf ëèíèè
ïîñòåïåííî ïðèáëèæàþùèåñÿ
ê ëèíèè ÎÂ, êîòîðàÿ
õàðàêòåðèçóåò
äðóãîé ïðåäåëüíûé
âàðèàíò - ïîçâåííóþ
ñáîðêó ìàêðîìîëåêóëû
- îáû÷íî íàçûâàåìûé
ïîëèìåðèçàöèåé.
Â
ÃÏÊ îðãàíîàëêîêñèñèëàíîâ
íå èñêëþ÷åí ïðîöåññ
îáðàçîâàíèÿ
îðãàíîñèëàíîíà
è åãî äàëüíåéøàÿ
ïîëèìåðèçàöèÿ.
Äðóãîé
ïðè÷èíîé ñìåùåíèÿ
ýêñïåðèìåíòàëüíûõ
ëèíèé â ñòîðîíó
ëèíèè ÎÂ ÿâëÿåòñÿ
äîïîëíèòåëüíàÿ
êîíâåðñèÿ ôóíêöèîíàëüíûõ
ãðóïï â ðåàêöèè
öèêëèçàöèè.
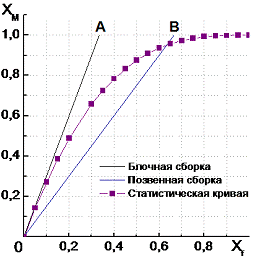
Ðèñ.
2.1 Ãðàôèê çàâèñèìîñòè
êîíâåðñèè ìîíîìåðà(XM) îò êîíâåðñèè
ôóíêöèîíàëüíûõ
ãðóïï (Xf).
È,
íàêîíåö, ïðè÷èíîé
ïîçâåííîé ñáîðêè
ìîëåêóëû îëèãîìåðà
ìîãóò áûòü ìàêðîêèíåòè÷åñêèå
óñëîâèÿ ðåàêöèè
è, â ÷àñòíîñòè,
ãåòåðîôàçíîñòü
ïðîöåññà, îáóñëàâëèâàþùàÿ
íåäîñòàòîê ãèäðîëèçóþùåãî
àãåíòà â çîíå
ðåàêöèè è åãî
ìåäëåííóþ äèôôóçèþ.
2.2 ×àñòè÷íûé
ãèäðîëèç îðãàíîòðèàëêîêñèñèëàíîâ
 êà÷åñòâå îáúåêòîâ
èññëåäîâàíèÿ
íàìè âûáðàíû
ôåíèëòðèìåòîêñèñèëàí
è ìåòèèëòðèýòîêñèñèëàí.
 êà÷åñòâå îáúåêòîâ
ñðàâíåíèÿ çàêîíîìåðíîñòåé
ñáîðêè îëèãîìåðíîé
öåïè íàìè âûáðàí
÷àñòè÷íûé ãèäðîëèç
ôåíèëòðèõëîðñèëàíà
è ãîìîôóíêöèîíàëüíàÿ
êîíäåíñàöèÿ
ôåíèëñèëàíòðèîëà,
èçó÷åííûå ðàíåå
íà íàøåé êàôåäðå.
×àñòè÷íûé ãèäðîëèç
ïðîâîäèëè â ìèêðîðåàêòîðå
èäåàëüíîãî ñìåøåíèÿ
ïåðèîäè÷åñêîãî
äåéñòâèÿ, ñíàáæåííîãî
îòðàæàòåëüíûìè
ðåáðàìè è ìåøàëêîé
â ñðåäå îñóøåííîãî
ðàñòâîðèòåëÿ,
ñîäåðæàùåãî õëîðèñòûé
âîäîðîä. Îòëè÷èòåëüíîé
îñîáåííîñòüþ
äàííîé ðàáîòû
îò ðàáîò äðóãèõ
èññëåäîâàòåëåé
ÿâëÿåòñÿ òîò ôàêò,
÷òî ñîîòíîøåíèå
âîäà/îðãàíîàëêîêñèñèëàí
â ðåàêöèîííîé
ñèñòåìå ñîîòâåòñòâóåò
çàäàííîìó. Ýòî
ñîîòâåòñòâèå
äîñòèãàåòñÿ
ïóòåì ìãíîâåííîãî
ââîäà ðåàãåíòîâ.
Àíàëèç ïðîâîäèëè
ìåòîäîì ÃÆÕ ñ
ó÷åòîì ïîïðàâî÷íîãî
êîýôôèöèåíòà
íà ÷óâñòâèòåëüíîñòü
äåòåêòîðà.
×àñòè÷íûé ãèäðîëèç
ìåòèëòðèýòîêñèñèëàíà
è ôåíèëòðèìåòîêñèñèëàíà
ïðîâîäèëè â ñðåäå
ðàçëè÷íûõ îðãàíè÷åñêèõ
ðàñòâîðèòåëåé,
ñìåøèâàþùèõñÿ
è íåñìåøèâàþùèõñÿ
ñ âîäîé. Ïðîöåññ
îñóùåñòâëÿëè
ïðè m - ñîîòíîøåíèè
âîäû è ìîíîìåðà
- â èíòåðâàëå îò
0 äî 1.
Íà ðèñóíêàõ
2.2 ïðåäñòàâëåíà
çàâèñèìîñòü
ñîñòàâà ïðîäóêòîâ
ãèäðîëèçà MeSi(OEt)3, PhSi(OMe)3
îò Xf (äàëåå
äèàãðàììà ÃÏÊ).
Èç ðèñóíêà âèäíî
íàëè÷èå áîëüøîãî
÷èñëà ïðîäóêòîâ
ãèäðîëèçà - ëèíåéíûå
îëèãîìåðû îáùåé
ôîðìóëû:
Ln ≡
RO−[R’(RO)SiO]n−R,
ãäå n = 2
- 6
è öèêëè÷åñêèå
îðãàíîàëêîêñèñèëîêñàíû
îáùåé ôîðìóëû:
Dn ≡ [R’(RO)SiO]n,
ãäå n = 3 - 4
à)
b)
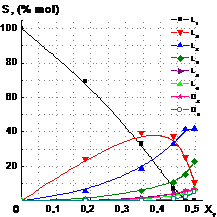
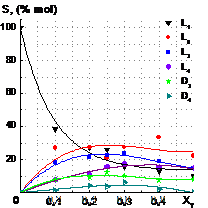
Ðèñ.
2.2. a) Äèàãðàììà
ÃÏÊ MeSi(OEt)3; b) Äèàãðàììà
ÃÏÊ PhSi(OMe)3.
Íåîáõîäèìî
îòìåòèòü, ÷òî
ïðè äàííûõ óñëîâèÿõ
ãèäðîëèçà (Ò=20 ºÑ, t=30 ìèí.) ëèíåéíîãî
è öèêëè÷åñêîãî
òåòðàìåðà â ïðîäóêòàõ
ãèäðîëèçà î÷åíü
ìàëî.
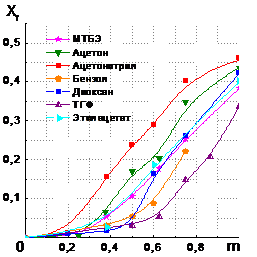
Ðèñ.
2.3. Çàâèñèìîñòü
êîíâåðñèè ôóíêöèîíàëüíûõ
ãðóïï (Xf) îò ñîîòíîøåíèÿ
m = âîäà/àëêîêñèñèëàí
â ÃÏÊ ìåòèëòðèýòîêñèñèëàíà
â ðàçíûõ ðàñòâîðèòåëÿõ.
Îáðàùàåò
íà ñåáÿ âíèìàíèå
òîò ôàêò (ðèñ.
2.2), ÷òî ìàêñèìàëüíîå
çíà÷åíèÿ êîíâåðñèè
ôóíêöèîíàëüíûõ
ãðóïï Xf ñîñòàâëÿþò
0,5-0,6, ò.å. îíè ìåíüøå
çàäàííîãî çíà÷åíèÿ
m.
Ñîïîñòàâëåíèå
êîíâåðñèè ôóíêöèîíàëüíûõ
ãðóïï Xf è m ïîêàçûâàåò
(ðèñ. 2.3): m > Xf -
ýòî ãîâîðèò î
ãåòåðîôàçíîñòè
ãèäðîëèçà, ïîñêîëüêó
÷àñòü âîäû íå
ó÷àñòâóåò â ðåàêöèè,
à íàõîäèòñÿ â
âîäíîé âàçå. Ïîëíîòà
ãèäðîëèçà è ïðèáëèæåíèå
êîíâåðñèè ôóíêöèîíàëüíûõ
ãðóïï Xf ê çàäàííîìó
çíà÷åíèþ m ïðîõîäèò
ìåäëåííî. Íà ðèñ.
2.4. ïîêàçàí îòíîñèòåëüíûé
ìîëüíûé ñîñòàâ
ïðîäóêòîâ ÃÏÊ
MeSi(OEt)3 âî âðåìåíè.
Áîëüøîå âðåìÿ
ÃÏÊ îðãàíîòðèàëêîêñèñèëàíîâ
ÿâëÿåòñÿ áîëüøèì
íåäîñòàòêîì
äëÿ çîëü-ãåëü ñîçðåâàíèÿ.
Ïîýòîìó òàêèì
îáðàçîì èçó÷àòü
ïðîöåññ òðóäíî
è ìû îãðàíè÷èëèñü
òîëüêî íà÷àëüíûìè
ñòàäèÿìè t =
30 ìèí.
Î÷åâèäíî, ÷òî
êîëè÷åñòâî âîäû
â îðãàíè÷åñêîé
ôàçå äîëæíî çàâèñåòü
îò ïðèðîäû ðàñòâîðèòåëÿ,
÷òî ïîäòâåðæäàåòñÿ
(ðèñ. 2.3). Â îäèíàêîâûõ
óñëîâèÿõ íàèáîëüøàÿ
êîíâåðñèÿ ôóíêöèîíàëüíûõ
ãðóïï äîñòèãàåòñÿ
â ðàñòâîðèòåëÿõ
ñ âûñîêîé äèýëåêòðè÷åñêîé
ïðîíèöàåìîñòüþ
è îäíîâðåìåííî
õîðîøî ñìåøèâàþùèõñÿ
ñ âîäîé.
Âûñîêîé êîíâåðñèè
ôóíêöèîíàëüíûõ
ãðóïï â «ãîìîãåíèçèðóþùèõ»
ðàñòâîðèòåëÿõ
ñ âûñîêîé äèýëåêòðè÷åñêîé
ïðîíèöàåìîñòüþ
ñîîòâåòñòâóåò
è âûñîêàÿ êîíâåðñèÿ
ìîíîìåðà è áûñòðîå
îáðàçîâàíèå
äèìåðà è òðèìåðà.
Ïî óìåíüøåíèþ
êîíâåðñèè ôóíêöèîíàëüíûõ
ãðóïï è ìîíîìåðà
ðàñòâîðèòåëè
ìîæíî ðàñïîëîæèòü
â ñëåäóþùåì ðÿäó:
àöåòîíèòðèë
˃ àöåòîí ˃ äèîêñàí,
ÌÒÁÝ, ýòèëàöåòàò,
áåíçîë ˃ ÒÃÔ. Ýòîò
ðÿä ðàñòâîðèòåëåé
ñîîòâåòñòâóåò
è «óìåíüøåíèþ
âûõîäà» äèìåðà
è òðèììåðà (ðèñ.
2.5). Ýòî îçíà÷àåò,
÷òî â ýòîì ðÿäó
ðàñòâîðèòåëåé
êîëè÷åñòâî âîäû
â îðãàíè÷åñêîé
ôàçå óìåíüøàåòñÿ.
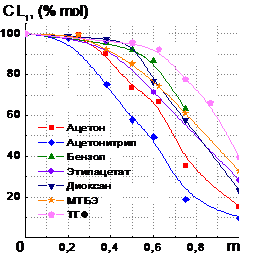
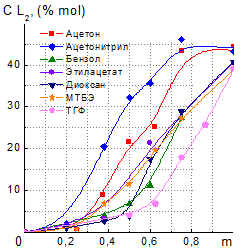 )
)
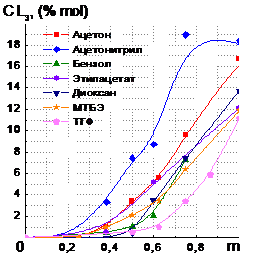
Ðèñóíîê
2.4. Èçìåíåíèå êîíöåíòðàöèè
ïðîäóêòîâ ãèäðîëèçà
MeSi(OEt)3 â çàâèñèìîñòè
îò ñîîòíîøåíèÿ
âîäà/àëêîêñèñèëàí
â ðàçëè÷íûõ ðàñòâîðèòåëÿõ;
à) - èçìåíåíèå
êîíöåíòðàöèè
ìîíîìåðà, b) - èçìåíåíèå
êîíöåíòðàöèè
äèìåðà, c) - èçìåíåíèå
êîíöåíòðàöèè
òðèììåðà.
Ñëåäîâàòåëüíî
ñêîðîñòü ðåàêöèé
ãèäðîëèçà è êîíäåíñàöèè
â ðàñòâîðèòåëÿõ
ñ âûñîêîé äèýëåêòðè÷åñêîé
ïðîíèöàåìîñòüþ
è îäíîâðåìåííî
õîðîøî ñìåøèâàþùèõñÿ
ñ âîäîé ñóùåñòâåííî
âûøå, ÷åì â äðóãèõ
ðàñòâîðèòåëÿõ.
Àíàëèç
íàøèõ ðåçóëüòàòîâ
ýêñïåðèìåíòîâ
â êîîðäèíàòàõ
Xm-Xf ïîêàçûâàåò,
÷òî ÃÏÊ ÌÒÝÑ âî
âñåõ ñåìè ðàñòâîðèòåëÿõ
èäåò îäèíàêîâî
è îáúåäèíÿåòñÿ
ïðàêòè÷åñêè
â îäíó çàâèñèìîñòü
â ïðåäåëàõ ïîãðåøíîñòè
ýêñïåðèìåíòà
(ðèñ. 2.5).
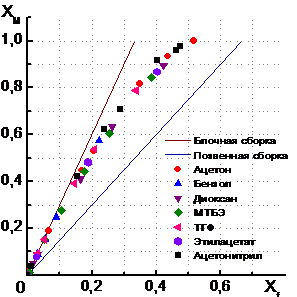
Ðèñóíîê
2.5. Çàâèñèìîñòü
êîíâåðñèè ìîíîìåðà
(XM) îò êîíâåðñèè
ôóíêöèîíàëüíûõ
ãðóïï (Xf) äëÿ
ÃÏÊ MeSi(OEt)3 â ðàçëè÷íûõ
ðàñòâîðèòåëÿõ.
Äëÿ
ñðàâíåíèÿ íà
ðèñóíêå 2.6. ïðèâåäåíû
äàííûå ãîìîêîíäåíñàöèè
ôåíèëñèëàíòðèîëà
è ÷àñòè÷íîãî
ãèäðîëèçà ôåíèëòðèõëîðñèëàíà
[78]. Òàêèì îáðàçîì,
ñðàâíèâàþòñÿ
÷åòûðå ñèñòåìû:
1. ÃÌÔÊ PhSi(OH)3
- íåò ñòàäèè ãèäðîëèçà
2. ×à MeSi(OEt)3 - åñòü
ñòàäèÿ ãèäðîëèçà
. ×à PhSi(OMe)3 - åñòü
ñòàäèÿ ãèäðîëèçà
. ×à PhSiCl3 - åñòü
ñòàäèÿ ãèäðîëèçà
Èç çàâèñèìîñòè
Xm îò Xf (ðèñ.2.6) äëÿ
ÃÏÊ MeSi(OEt)3 PhSi(OMe)3 âèäíî,
÷òî ïðèðîäà çàìåñòèòåëÿ
ó àòîìà êðåìíèÿ
ìàëî âëèÿåò íà
õàðàêòåð õèìè÷åñêîé
ñáîðêè ìîëåêóë
ïîëèñèëîêñàíà.
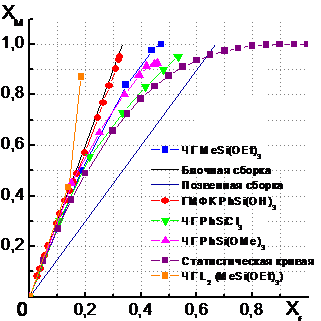
Ðèñóíîê
2.6. Çàâèñèìîñòü
êîíâåðñèè ìîíîìåðà
(Xm) îò êîíâåðñèè
ôóíêöèîíàëüíûõ
ãðóïï (Xf) äëÿ
ÃÏÊ MeSi(OEt)3, Me(OEt)2SiOSi(OEt)2Me, PhSi(OMe)3,
PhSiCl3 è
ÃÌÔÊ PhSi(OH)3.
Èíòåðåñíîå
ïîâåäåíèå ïðîÿâëÿåò
ãèäðîëèç äèìåòèëòåòðàýòîêñèäèñèëîêñàíà,
êîòîðûé îêàçûâàåòñÿ
ñëåâà îò ëèíèè
áëî÷íîé ñáîðêè,
÷òî óêàçûâàåò
íà ðàñïàä äèìåðà,
à ñëåäîâàòåëüíî
óâåëè÷åíèå ôóíêöèîíàëüíûõ
ãðóïï. Òàêàÿ çàâèñèìîñòü
õàðàêòåðèçóåò
îáðàòèìîñòü
ïðîöåññà è ìåæöåïíîé
îáìåí.
Â
÷åòâåðòîé ñèñòåìå,
î÷åâèäíî, kH >> kC èç-çà
áîëüøåé àêòèâíîñòè
ÔÒÕÑ â ñðàâíåíèè
ñ ÌÒÝÑ. Âî âòîðîé
è òðåòüåé ñèñòåìàõ
ãèäðîëèç è ïîëèêîíäåíñàöèÿ,
âåðîÿòíî, ïðîòåêàþò
ñ ñîïîñòàâèìûìè
ñêîðîñòÿìè, ò.å.
îäíîâðåìåííî.
Íà ðèñóíêå 2.6 ìîæíî
âèäåòü, ÷òî â ÃÏÊ
îðãàíîàëêîêñèñèëàíîâ
äîëÿ ïîçâåííîé
ñáîðêè ìåíüøå,
÷åì â ÃÏÊ îðãàíîõëîðñèëàíîâ.
Òåì íå ìåíåå, åå
âêëàä â îáðàçîâàíèå
ïîëèîðãàíîñèëîêñàíà
çàìåòíûé. Ïðè÷èíîé
ÿâëÿåòñÿ ãåòåðîôàçíûé
õàðàêòåð ïðîöåññà,
îáóñëàâëèâàåìûé
íåäîñòàòîê ãèäðîëèçóþùåãî
àãåíòà â çîíå
ðåàêöèè.
Ìàòåìàòè÷åñêîå
ìîäåëèðîâàíèå,
ñ èñïîëüçîâàíèåì
ïðîãðàììû «Ïîëèêîíäåíñàöèÿ»,
ïîêàçûâàåò, ÷òî
óâåëè÷åíèå kH
ïî ñðàâíåíèþ
ñ kC ïî÷òè íå ñêàçûâàåòñÿ
íà çàâèñèìîñòÿõ
XM - Xf. Óñòàíîâëåíî,
÷òî èçìåíåíèå
â ñîîòíîøåíèè
ñêîðîñòåé ãîìî-
è ãåòåðîêîíäåíñàöèè
ÿâëÿåòñÿ âàæíûì
ôàêòîðîì õèìè÷åñêîé
ñáîðêè. Óâåëè÷åíèè
âêëàäà ðåàêöèè
ÃÒÔÊ â îáùèé ïðîöåññ
êîíäåíñàöèè
ïðèâîäèò ê óâåëè÷åíèþ
äîëè ïîçâåííîé
ñáîðêè è ðàçâåòâëåíèþ.
Ïðè÷èíîé ïîçâåííîé
ñáîðêè ÿâëÿþòñÿ
íå êèíåòè÷åñêèå,
à ìàêðîêèíåòè÷åñêèå
ôàêòîðû, à èìåííî
íåäîñòàòîê ãèäðîëèçóþùåãî
àãåíòà â ðåàêöèîííîé
ôàçå. Çíàíèå
ôàêòîðîâ õèìè÷åñêîé
ñáîðêè è ñïîñîáîâ
óïðàâëåíèÿ åþ
ïîçâîëèò íàïðàâëÿòü
ïðîöåññ ÃÏÊ îðãàíîòðèàëêîêñèñèëàíîâ
ëèáî â ñòîðîíó
ïîëèìåðîâ óïîðÿäî÷åííîé
ñòðóêòóðû (ëåñòíè÷íîé)
ëèáî â ñòîðîíó
âûñîêîðàçâåòâëåíûõ
ïðîäóêòîâ.
3. Ýêñïåðèìåíòàëüíàÿ
÷àñòü
.1 Òåõíèêà ýêñïåðèìåíòà
Îñíîâíûìè îáúåêòàìè
ýêñïåðèìåíòà
ÿâëÿþòñÿ: PhSi(OMe)3, MeSi(OEt)3
è ïðîäóêòû èõ
÷àñòè÷íîãî ãèäðîëèçà:
EtO(MeSi(OEt)O)nEt èëè MeO(PhSi(OMe)O)n-1Ph, îáîçíà÷àåìûå
äàëåå êàê Ln, à òàêæå
îðãàíîöèêëîñèëîêñàíû
- Dn ≡ [Me(OEt)Si]n èëè [Ph(OMe)Si]n.
 ðàáîòå èñïîëüçîâàëèñü
ïåðåãíàííûå
ìåòèëòðèýòîêñèñèëàí
è ôåíèëòðèìåòîêñèñèëàí.
×èñòîòà áûëà
îïðåäåëåíà ïðè
ïîìîùè õðîìàòîãðàôè÷åñêîãî
àíàëèçà è ñîñòàâëÿëà
98% è 96% ñîîòâåòñòâåííî.
Òàáëèöà 3.1. Ôèçè÷åñêèå
ñâîéñòâà èñõîäíûõ
ðåàãåíòîâ.
|
Íàèìåíîâàíèå
|
Ôîðìóëà
|
ÌÌ
|
Òê, ºÑ
|
d420
ã/ìë
|
|
Ôåíèëòðèìåòîêñèñèëàí
|
PhSi(OMe)3
|
198.29
|
187
|
1.0641
|
|
Ìåòèëòðèýòîêñèñèëàí
|
MeSi(OEt)3
|
178.30
|
143
|
0,895
|
 ðàáîòå áûëè
èñïîëüçîâàíû
ñëåäóþùèå ðàñòâîðèòåëè:
àöåòîí, àöåòîíèòðèë,
äèîêñàí, òåòðàãèäðîôóðàí
(ÒÃÔ), áåíçîë, ìåòèëòðåòáóòèëîâûé
ýôèð (ÌÒÁÝ), ýòèëàöåòàò.
Òàáëèöà 3.2. Ôèçè÷åñêèå
ñâîéñòâà ðàñòâîðèòåëåé.
|
Íàèìåíîâàíèå
|
ôîðìóëà
|
MÌ
|
Òê, ºÑ
|
d420,
ã/ìë
|
nd20
|
|
Àöåòîí
|
CH3C(O)CH3
|
58.08
|
56.1
|
0.7899
|
1.3588
|
|
Àöåòîíèòðèë
|
H3C-C≡N
|
41.05
|
82
|
0.786
|
1.3441
|
|
Äèîêñàí
|
 88.111011.0331.4224 88.111011.0331.4224
|
|
|
|
|
|
ÒÃÔ
|
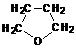 72.11660.88921,4050 72.11660.88921,4050
|
|
|
|
|
|
Áåíçîë
|
C6H6
|
78.11
|
80.1
|
0.8786
|
1,5011
|
|
ÌÒÁÝ
|
(CH3)3COCH3
|
88.15
|
55.2
|
0.7578
|
1.3756
|
|
Ýòèëàöåòàò
|
ÑÍ3-ÑÎÎ-C2H5
|
88,11
|
77
|
0,902
|
1,3720
|
×èñòîòà ðàñòâîðèòåëåé
êîíòðîëèðîâàëàñü
ïðè ïîìîùè õðîìàòîãðàôè÷åñêîãî
àíàëèçà.
 ðàáîòå èñïîëüçîâàëàñü
äèñòèëëèðîâàííàÿ
âîäà pH =
6.5-6.7
3.2 Êîíòðîëü
ñîñòàâà ïðîäóêòîâ
ÃÏÊ îðãàíîàëêîêñèñèëàíîâ
Îäíîé èç òðóäíîñòåé
èçó÷åíèÿ íà÷àëüíûõ
ñòàäèé ÃÏÊ îðãàíîàëêîêñèñèëàíîâ,
êàê è íà÷àëüíûõ
ñòàäèé ëþáîãî
ïðîöåññà îáðàçîâàíèÿ
ïîëèìåðîâ, ÿâëÿåòñÿ
àíàëèç ñîñòàâà
ïðîäóêòîâ. Äëÿ
àíàëèçà ïðîäóêòîâ
ÃÏÊ îðãàíîàëêîêñèñèëàíîâ
èñïîëüçîâàëàñü
ãàçîæèäêîñòíàÿ
õðîìàòîãðàôèÿ
- ÃÆÕ.
Õðîìàòîãðàôè÷åñêèé
àíàëèç ïðîâîäèëè
íà ïðèáîðå «Êðèñòàëë
2000Ì», ñíàáæåííûì
äåòåêòîðîì ïî
òåïëîïðîâîäíîñòè,
íà êàïèëëÿðíîé
êîëîíêå äëèííîé
10 ì, ãàç-íîñèòåëü
- àçîò.
Ñîåäèíåíèÿ
èäåíòèôèöèðîâàëèñü
ñ ïîìîùüþ ýòàëîííûõ
îáðàçöîâ PhSi(OMe)3 è MeSi(OEt)3
Èäåíòèôèêàöèÿ
ïðîäóêòîâ êîíäåíñàöèè
ïðîâîäèëàñü ñ
ïîìîùüþ ãðàôèêà
çàâèñèìîñòè
âðåìåí óäåðæèâàíèÿ
îò íîìåðà ÷ëåíà
ãîìîëîãè÷åñêîãî
ðÿäà (ðèñ.). Ðàñ÷åò
õðîìàòîãðàìì
îñóùåñòâëÿëñÿ
ïî ïëîùàäÿì ïèêîâ
ìåòîäîì íîðìèðîâêè
ñ ïîïðàâî÷íûìè
êîýôôèöèåíòàìè.
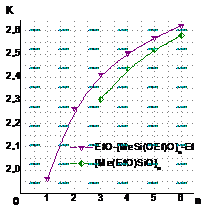
Ðèñ.
Ãðàôèê çàâèñèìîñòè
âðåìåí óäåðæèâàíèÿ
îò íîìåðà ÷ëåíà
ãîìîëîãè÷åñêîãî
ðÿäà.
Ïî
äàííûì ÃÆÕ îïðåäåëÿëè
îòíîñèòåëüíûé
ìîëüíûé ñîñòàâ
(S, ìîë. ä.) ïðîäóêòîâ
èçó÷àåìûõ ðåàêöèé
ïî îáû÷íîé ôîðìóëå:
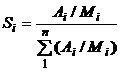 ,
,
ãäå
À - ïîêàçàíèÿ ïðèáîðà
(ïëîùàäü èëè èíòåíñèâíîñòü
ïèêà, èñïðàâëåííàÿ
ñ ó÷åòîì ïîïðàâî÷íîãî
êîýôôèöèåíòà).
Òåêóùèå
êîíöåíòðàöèè
ïðîäóêòîâ êîíäåíñàöèè
(Ñi, ìîëü/ë) ðàññ÷èòûâàëè
èñõîäÿ èç íà÷àëüíîé
êîíöåíòðàöèè
ìîíîìåðà Ñ0,
ñîîòíîøåíèé
ìàòåðèàëüíîãî
áàëàíñà è óñëîâèÿ
íîðìèðîâêè (ñì.
ýêñïåðèìåíòàëüíóþ
÷àñòü):
Ñ0
- Ñ1=2Ñ2+3Ñ3+...+nCn;
S(Cn/ SCn) =
1
Ñòåïåíü
ïðåâðàùåíèÿ ìîíîìåðà
- Xm, ñòåïåíü ïîëèìåðèçàöèè
- n è ñòåïåíü
ïðåâðàùåíèÿ ôóíêöèîíàëüíûõ
ãðóïï (OR) ðàññ÷èòûâàëè
ïî èçâåñòíûì
ôîðìóëàì:
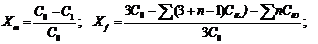

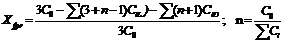 ,
,
ãäå
Xm - ñòåïåíü ïðåâðàùåíèÿ
ìîíîìåðà;
Xf - ñòåïåíü
ïðåâðàùåíèÿ ôóíêöèîíàëüíûõ
ãðóïï (OR);
Xfpr
"ïðèâåäåííàÿ"
ñòåïåíü ïðåâðàùåíèÿ
ôóíêöèîíàëüíûõ
ãðóïï (f = OR èëè Ñl), òî
åñòü áåç ó÷åòà
ðàñõîäîâàíèÿ
ôóíêöèîíàëüíûõ
ãðóïï â àêòå öèêëèçàöèè
ëèíåéíîé ìîëåêóëû;
Ñ0
è Ñ1, - íà÷àëüíàÿ
è êîíå÷íàÿ êîíöåíòðàöèè
ìîíîìåðà;
ÑiL è CiD - êîíöåíòðàöèè
ëèíåéíûõ è öèêëè÷åñêèõ
ïðîäóêòîâ ê ìîìåíòó
çàâåðøåíèÿ ðåàêöèè.
.3 ×àñòè÷íûé
ãèäðîëèç PhSi(OMe)3 è
MeSi(OEt)3
×àñòè÷íûé ãèäðîëèç
PhSi(OMe)3 è MeSi(OEt) ïðîâîäèëè
â ïåðèîäè÷åñêîì
ìèêðîðåàêòîðå
ñìåøåíèÿ (ÏÐÑ,
îáúåì 10 ìë.) ñ îòðàæàòåëüíûìè
ðåáðàìè è ñíàáæåííîãî
ìåøàëêîé, ïîêàçàííîì
íà ðèñóíêå 3.1.
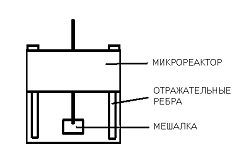
Ðèñ.
3.1. Ìèêðîðåàêòîð
äëÿ ïðîâåäåíèÿ
÷àñòè÷íîãî ãèäðîëèçà.
Â
ìèêðîðåàêòîð
çàãðóæàëè ðàñ÷åòíîå
êîëè÷åñòâî àëêîêñèñèëàíà
è ðàñòâîðèòåëÿ.
Âêëþ÷àëè ìåøàëêó
è ïåðåìåøèâàëè
â òå÷åíèå 1 ìèíóòû.
Çàòåì øïðèöîì
ìãíîâåííî ââîäèëè
ðàñ÷åòíîå êîëè÷åñòâî
êèñëîé âîäû (0.1 í
HCl), ïåðåìåøèâàëè
â òå÷åíèè 30 ìèíóò.
Ìãíîâåííûé ââîä
îáåñïå÷èâàë
çàäàííîå ñîîòíîøåíèå
âîäà/RSi(OR’)3. Ðåàêöèîííóþ
ìàññó àíàëèçèðîâàëè
ìåòîäîì ÃÆÕ äëÿ
îïðåäåëåíèÿ îòíîñèòåëüíîãî
ñîñòàâà ïðîäóêòîâ
ãèäðîëèçà.
Òàáëèöà 3.3. Äàííûå
çàãðóçîê ×à MeSi(OEt)3
|
Âåùåñòâî
|
m=n[H2O]/n[MeSi(OEt)3]
|
|
0,25
|
0,375
|
0,5
|
0,625
|
0,75
|
0,825
|
1
|
|
MeSi(OEt)3
|
|
|
|
|
|
|
|
|
Êîë. â-âà,
ìîëü
|
0,028
|
0,028
|
0,028
|
0,028
|
0,028
|
0,028
|
0,028
|
|
Ìàññà,
ã.
|
5
|
5
|
5
|
5
|
5
|
5
|
5
|
|
Îáúåì,
ìë
|
4,474
|
4,474
|
4,474
|
4,474
|
4,474
|
4,474
|
4,474
|
|
Âîäà
|
|
|
|
|
|
|
|
|
Êîë. â-âà,
ìîëü
|
0,007
|
0,0105
|
0,014
|
0,0175
|
0,021
|
0,0231
|
0,028
|
|
Ìàññà,
ã.
|
0,13
|
0,19
|
0,25
|
0,32
|
0,38
|
0,42
|
0,45
|
|
Îáúåì,
ìë
|
0,13
|
0,19
|
0,25
|
0,32
|
0,38
|
0,42
|
0,45
|
Òàáëèöà 3.5. Äàííûå
çàãðóçîê ×à PhSi(OMe)3
|
Âåùåñòâî
|
m= n[H2O]/n[PhSi(OMe)3]
|
|
0,2
|
0,4
|
0,5
|
0,6
|
0,8
|
1
|
|
PhSi(OMe)3
|
|
|
|
|
|
|
|
Êîë. â-âà,
ìîëü
|
0,0277
|
0,0277
|
0,0277
|
0,0277
|
0,0277
|
0,0277
|
|
Ìàññà,
ã.
|
3
|
3
|
3
|
3
|
3
|
3
|
|
Îáúåì,
ìë
|
3,192
|
3,192
|
3,192
|
3,192
|
3,192
|
|
Âîäà
|
|
|
|
|
|
|
|
Êîë. â-âà,
ìîëü
|
0,0055
|
0,0111
|
0,0139
|
0,0166
|
0,0222
|
0,0277
|
|
Ìàññà,
ã.
|
0,1
|
0,2
|
0,25
|
0,3
|
0,4
|
0,5
|
|
Îáúåì,
ìë
|
0,0998
|
0,1996
|
0,2496
|
0,2995
|
0,3993
|
0,4991
|
3.4 Ïîëó÷åíèå EtO[MeSi(OEt)O]2Et
Ïðîöåññ ïðîâîäèëè
â äâóãîðëîé êîëáå
îñíàùåííîé ìåøàëêîé.
 íåå çàãðóæàëè
ðàñ÷åòíîå êîëè÷åñòâî
MeSi(OEt)3 è àöåòîíèòðèëà.
Âêëþ÷àëè ìåøàëêó
è ïåðåìåøèâàëè
â òå÷åíèå 1 ìèíóòû.
Çàòåì øïðèöîì
ìãíîâåííî ââîäèëè
ðàñ÷åòíîå êîëè÷åñòâî
êèñëîé âîäû (0.1 í
HCl), ïåðåìåøèâàëè
â òå÷åíèè 30 ìèíóò.
Ìãíîâåííûé ââîä
îáåñïå÷èâàë
çàäàííîå ñîîòíîøåíèå
H2O/MeSi(OEt)3 ðàâíîå
0,6. Ïî îêîí÷àíèþ
âðåìåíè ñèíòåçà,
äîáàâëÿëè ðàññ÷èòàííîå
êîëè÷åñòâî ýïèõëîðãèäðèíà
â êà÷åñòâå àêöåïòîðà
ñîëÿíîé êèñëîòû
è ïåðåìåøèâàëè
ñìåñü â òå÷åíèè
10 ìèí. Ïîëó÷åííóþ
ðåàêöèîííóþ
ìàññó àíàëèçèðîâàëè
ìåòîäîì ÃÆÕ äëÿ
îïðåäåëåíèÿ îòíîñèòåëüíîãî
ñîñòàâà ïðîäóêòîâ
ãèäðîëèçà. Äàëåå
îòãîíÿëè ðàñòâîðèòåëü
ñ ïîìîùüþ ðîòîðíîãî
èñïàðèòåëÿ. Îñòàâøèéñÿ
ãèäðîëèçàò ïåðåãîíÿëè
íà ïåðåãîííîé
óñòàíîâêå. Íå
ïðîðåàãèðîâàâøèé
MeSi(OEt)3 ïåðåãîíÿëè
ïðè 70 0Ñ, à äèìåòèëòåòðàýòîêñèäèñèëîêñàí
ïðè 120 0Ñ. ×èñòîòà
EtO[MeSi(OEt)O]2Et áûëà îïðåäåëåíà
ïðè ïîìîùè õðîìàòîãðàôè÷åñêîãî
àíàëèçà è ñîñòàâëÿëà
90%.
.5 ×àñòè÷íûé
ãèäðîëèç EtO[MeSi(OEt)O]2Et
×àñòè÷íûé ãèäðîëèç
EtO[MeSi(OEt)O]2Et ïðîâîäèëè â
ïåðèîäè÷åñêîì
ìèêðîðåàêòîðå
ñìåøåíèÿ (ÏÐÑ,
îáúåì 10 ìë.) ñ îòðàæàòåëüíûìè
ðåáðàìè è ñíàáæåííîãî
ìåøàëêîé, ïîêàçàííîì
íà ðèñóíêå 3.1.
 ìèêðîðåàêòîð
çàãðóæàëè ðàñ÷åòíîå
êîëè÷åñòâî äèìåòèëòåòðàýòîêñèäèñèëîêñàíà
è ðàñòâîðèòåëÿ.
Âêëþ÷àëè ìåøàëêó
è ïåðåìåøèâàëè
â òå÷åíèå 1 ìèíóòû.
Çàòåì øïðèöîì
ìãíîâåííî ââîäèëè
ðàñ÷åòíîå êîëè÷åñòâî
êèñëîé âîäû (0.1 í
HCl), ïåðåìåøèâàëè
â òå÷åíèè 30 ìèíóò.
Ðåàêöèîííóþ
ìàññó àíàëèçèðîâàëè
ìåòîäîì ÃÆÕ äëÿ
îïðåäåëåíèÿ îòíîñèòåëüíîãî
ñîñòàâà ïðîäóêòîâ
ãèäðîëèçà.
Òàáëèöà 3.4. Äàííûå
çàãðóçîê ×à (EtO)2MeSiOSiMe(OEt)2
|
Âåùåñòâî
|
m= n[H2O]/n[(EtO)2MeSiOSiMe(OEt)2]
|
|
0,5
|
0,75
|
1
|
|
(EtO)2MeSiOSiMe(OEt)2
|
|
|
|
|
Êîë. â-âà,
ìîëü
|
0,0073
|
0,0073
|
0,0073
|
|
Ìàññà,
ã.
|
2,06
|
2,06
|
2,06
|
|
Âîäà
|
|
|
|
|
Êîë. â-âà,
ìîëü
|
0,00365
|
0,00547
|
0,0073
|
|
Ìàññà,
ã.
|
0,06
|
0,09
|
0,12
|
|
Îáúåì,
ìë
|
0,0599
|
0,0899
|
0,1198
|
Âûâîäû
1. Èçó÷åíà õèìè÷åñêàÿ
ñáîðêà îëèãîîðãàíîñèëîêñàíîâ
â ïðîöåññå ãèäðîëèòè÷åñêîé
ïîëèêîíäåíñàöèè
îðãàíîòðèàëêîêñèñèëàíîâ.
2. Îïðåäåëåí ñîñòàâ
îëèãîìåðîâ íà÷àëüíûõ
ñòàäèé ãèäðîëèòè÷åñêîé
ïîëèêîíäåíñàöèè
R’Si(OR)3 â
ðàçëè÷íûõ ðàñòâîðèòåëÿõ.
. Óñòàíîâëåí
ðÿä ãîìîãåíèçèðóþùåé
ñïîñîáíîñòè
ðàñòâîðèòåëåé
â ãåòåðîôàçíîì
ïðîöåññå ÃÏÊ ìåòèëòðèýòîêñèñèëàíà.
Óñòàíîâëåíî,
÷òî ñáîðêà ïîëèìåðíîé
öåïè â îáëàñòè
èñïîëüçóåìûõ
êîíöåíòðàöèé
íå çàâèñèò îò
ïðèðîäû ðàñòâîðèòåëÿ.
. Ïðîâåäåíî ñîïîñòàâëåíèå
÷åòûðåõ ïîëèêîíäåíñàöèîííûõ
ñèñòåì: ÃÌÔÊ
ôåíèëñèëàíòðèîëà,
ÃÏÊ ìåòèëòðèýòîêñèñèëàíà,
ÃÏÊ ôåíèëòðèõëîðñèëàíà,
ÃÏÊ ôåíèëòðèìåòîêñèñèëàíà.
Ïîêàçàíî, ÷òî
ïðèðîäà ìîíîìåðà
îêàçûâàåò âëèÿíèå
íà ñáîðêó ïîëèìåðíîé
öåïè, îáóñëàâëèâàÿ
ðàçëè÷íûé íåäîñòàòîê
âîäû â çîíå ðåàêöèè.
. Óñòàíîâëåíî,
÷òî â ÃÏÊ àëêîêñèñèëàíîâ
âêëàä ÃÒÔÊ â îáðàçîâàíèå
îðãàíîñèëîêñàíîâ
ÿâëÿåòñÿ ñóùåñòâåííûì,
íî ìåíüøèì, ÷åì
â ÃÏÊ îðãàíîõëîðñèëàíîâ.
Ñïèñîê ëèòåðàòóðû
1. Àíäðèàíîâ
Ê.À. Ìåòîäû ýëåìåíòîîðãàíè÷åñêîé
õèìèè // Ì., «Íàóêà».
1968, 699 ñ.
2. Cogan H.D., Setterstrom C.A. Liquid Phase
Miscibility in the Water-Ethanol-TEOS System // Chem. and Eng. News. 1946, 24,
p. 2499
. Avnir D., Kaufman V.R. Alcohol is an
unnesessary additive in the silicon alkoxide sol-gel process // J. Non -
Crystalline Solids. 1987, 192, pp. 180-182
. Brinker C.J., Keefer K.D., Schaefer D.W.,
Ashley C.S. Sol-Gel Transition in Simple Silicates // J. Non-Crystalline
Solids. 1982, 48, pp. 47-64
. Stober W., Fink A., Bohn E. J. Controlled
growth of monodisperse silica spheres in the micron size range // Colloid and
Interface Sci. 1968, 26, pp. 62-69.
. Assink R.A., Kay B.D. Spinnability of silica
sols // J. Non-Crystalline Solids, 1988, 99, p. 359
7. Àíäðèàíîâ
Ê.À. Êðåìíèéîðãàíè÷åñêèå
ñîåäèíåíèÿ // Ì.,
«ÕèìËèò», 1955, 166 ñ.
8. Anderson R., Arkles B., Larson C.L. Petrarch
systems silanes and silicones // Anal. Chem. 1987. V. 59. P. 2707-2209.
. Klemperer W.G., Mainz V.V., Miliar D.M.
Better Ceramics Through Chemistry II // Mat. Res. Soc., Pittsburgh. 1986, p.3
. Klemperer W.G., Mainz V.V., Miliar D.M.
Better Ceramics Through Chemistry II // Mat. Res. Soc., Pittsburgh. 1986, p.15
. McNeill K.J., DiCaprio J.A., Walsh D.A.,
Pratt. R.F. Kinetics and Mechanism of Hydrolysis of a Silicate Triester,
Tris(2- methoxyethoxy)phenylsilane // J.Am. Chem. Soc. 1980, 102, p.1859
12. Õàñêèí Ë.Ã.
// Äîêë. ÀÍ ÑÑÑÐ.
1952, 85, c.129.
. Âîðîíêîâ
Ì.Ã., Ìèëåøêåâè÷
Â.Ï., Þæåëåâñêèé
Þ.À. Ñèëîêñàíîâàÿ
ñâÿçü // Íîâîñèáèðñê:
Íàóêà, 1976.
. Keefer K.D. Silicon Based Polymer Science: A
Comprehensive Resource // Better Ceramics Through Chemistry II., 1984, pp.15 -
24.
15. Pohl E.R., Osterhpltz F.D. Molecular
Characterization of Composite Interfaces // Plenum, New York. 1985, p.157
. Aelion R., Loebel A., Eirich F. Hydrolysis of
ethyl silicate // J. Am. Chem. Soc. 1950, 72, pp. 5705-5712
. Pope E.J.A., Mackenzie J.D. Sol-gel processing
of silica. II. The role of the catalyst // J. Non-Crystalline Solids. 1986, 87,
p. 185
18. Corriu R.J.P., Young J.C. The Chemistry of Organic
Silicon Compounds // Wiley, New York. 1989, pp. 1241-1288
. Àíäðèàíîâ
Ê.À. Ìåòàëëîðãàíè÷åñêèå
ïîëèìåðû // Æóðí.
îáù. õèìèè 1938. Ò.8.
Ñ.1255.
20. Corriu R.J.P., LeClercq D., Vioux A., Pauthe
M., Phalippou J. Ultrastructure Processing of Advanced Ceramics // Wiley, New
York. 1988, pp. 113-126
. Coltrain B.K., Melpolder S.M., Salva J.M.
Ultrastructure Processing of Ceramics, Glasses, and Composites // Wiley, New
York. 1989
. Schmidt H., Kaiser A., Rudolph M., Lentz A.
Science of Ceramic Chemical Processing // Wiley, New York. 1986, pp. 87-93
. Brinker C.J., Keefer K.D., Schaefer D.W.,
Assink R.A., Kay B.D., Ashley C.S. Sol-gel transition in simple silicates II //
J. Non-Crystalline Solids. 1984, 63, pp. 45-59
. Brinker C.J. Hydrolysis and Condensation of
Silicates: Effects on Structure // J. Non-Crystalline Solids. 1988, 100, pp.
30-51
. Schmidt H., Scholze H., Kaiser A. Principles
of Hydrolysis and Condensation Reaction of Alkoxysilanes // J. Non- Crystalline
Solids. 1984, 63, pp. 1-11
. Aelion R., Loebel A., Eirich F. Hydrolysis of
Ethyl Silicate// Recueil Travaux Chimigues. 1950, 69, pp. 61-75
. Pouxviel J.C., Boilet J.P., Beloeil J.C.,
Lallemand J.Y. NMR study of the sol-gel polymerization // J. Non- Crystalline
Solids. 1987, 89, p. 345
. Klein L.C. Sol-gel optics: processing and
applications// Ann. Rev. Mater. Sci. 1985, 15, pp. 227 - 248.
. Hench L.L., Orcel G., Nogues J.L. Transparent
silica gel monoliths // Better Ceramics Through Chemistry II. 1986, p. 35
. Morrison R.T., Boyd R.N. Organic Chemistry //
Allyn and Bacon, Boston. 1966
. Sommer L.H., Frye G.F. Stereochemistry of
Substitution at Silicon. Reactions of the Silicon-Oxygen Bond with Inversion
and Retention of Configuration // J. Am. Chem. Soc. 1960, 82, p. 3796
. Sommer L.H., Frye G.F., Musiof M.C., Parker
G.A., Rodewald P.G., Michael K.W., Okaya Y., Pepinski P. Stereochemistry of
Substitution to Asymmetric Silicon // J. Am. Chem. Soc. 1961, 8, p. 2210
. Sommer L.H., Parker G.A., Lloyd N.C., Frye
C.L., Michael K.W. Stereochemistry of Substitution to Asymmetric Silicon // J.
Am. Chem. Soc. 1967, 89, pp. 857-860
. Uhimann D.R., Zelinski B.J., Wnek G.E. Better
Ceramics Through Chemistry II // North-Holland, New York. 1984, pp. 59-70
. Timms R.E. Kinetics of the Sol-Gel
Transition// J. Chem. Soc. 1971, A, pp. 1969-1964
. Iler R.K. The Chemistry of Silica:
Solubility, Polymerization, Colloid and Surface Properties and Biochemistry of
Silica. 1979
. Bradley D.C. Metal alkoxides// Academic
Press,1978, p. 441.
. Engelhardt V.G., Altenburg W., Hoebbel D.,
Wieker W.Z. // Anorg. Alig. Chem. 1977, 418, p. 43
. Assink R.A., Kay B.D. Sol-gel kinetics I.
Functional group kinetics // J. Non-Crystalline Solids. 1988,
99, p.359.
. Lasocki Z., Chrzczonowicz S. Rate of
polycondensation of dimethylsilandiol // Bull. Acad. Polon. Ser. Sci. Chem.
1961. V. 9. ¹ 9. P. 589-590
. Swain C.G., Esteve R.M., Jones R.H. The
copolymerization of cyclic siloxanes // J. Am. Chem. Soc. 1949, 11, p. 965.
. Artaki I., Sinha S., Irwin A.D., Jones J. NMR
and Raman study of the hydrolysis reaction in sol-gel processes // J. of
Non-Crystalline Solids. 1985, 72, pp. 391-402.
. Okkerse C. Physical and Chemical Aspects of
Adsorbents and Catalysts // Academic Press. 1970.
. Grubbs W.T. A Rate Study of the Silanol
Condensation Reaction at 25° in Alcoholic Solvents // J. Am. Chem.
Soc. 1954, 76, p. 3408.
. Davis L.P., Burggraf L.W. Ultrastructure
Processing of Advanced Ceramics // Wiley, New York. 1988, pp. 367-378.
. Grubb W.T., Osthoff R. A Rate Study of
Silanol Condensation Reaction at 25o in Alcoholic Solvents // J. Am. Chem. Soc.
1953. V. 76. P. 3408-3414.; Sommer L.H., Pietrusza E.W., Whitmore F.C.J.
Properties of Silicon-Hydroxyl Bond in Trialkylsilanols // J. Am. Chem. Soc.
1946. V. 68. P. 2282-2284.
. Lasocki Z. Substitution at silicon atom in
organosilicon compounds III. Steric and polar effects of alkyl groups in the
condensation of silandiols // Bull. Acad. Polon. 1964. V. 12. ¹ 4. P.
227-233.
. Rutz W., Lange D., Kelling H. Kondensation
von Trimethylsilanol // Z. Annorg. Allg. Chem. 1985. ¹ 528. P. 98-106.
. Chrzczonowicz S., Lasocki Z. Equlibria and
rates of polycondensation of dimethylsilandiol in methanol // Bull. Acad.
Polon. 1961. V. 9. ¹ 9. P. 591-593.
. Lasocki Z. Substitution at silicon atom in
organosilicon compounds. I. Rates of condensation of straight-chain alkyl
substituted silandiols // Bull. Acad. Polon. Sci. Ser. Sci. Chim. 1963. V. 11. ¹
11. P. 637-643.
. Lasocki Z. Substitution at silicon atom in
organosilicon compounds. II. Rates of condensation of branched-chain alkyl
substituted silandiols // Bull. Acad. Polon. 1964. V. 12. ¹ 4. P.
223-226..
. Chrzczonowicz S., Lasocki Z. Kinetics of
Condensation of (halogenomethyl) methylsilandiols in Dioxane, in acidic Media // Bull. Acad. Polon. 1962.
V. 10. ¹ 4. P. 161-163.
. Lasocki Z., Michalska Z. Substitution at a
silicon atom in organosilicon compounds. V. Medium effects in HCl-catalyzed
condensation of diethylsilane-diol in dioxane // Bull. Acad. Polon. 1965. V.
13. ¹ 4. P. 261-266.
. Dejak B., Lasocki Z., Mogilnici W. Rates of
condensation of some diorganosilandiols in methanol with potassium hydroxide as
catalist // Bull. Acad. Polon. Sci. Ser. Chim. 1969. V. 17. ¹ 1. P. 7-12.
55. Ìàðòÿêîâà
Í.È., Äîëãîïëîñê
Ñ.Á., Êàãàí Å.Ã., Ìèëåøêåâè÷
Â.Ï. Êèíåòèêà êîíäåíñàöèè
ñèëàíîëîâ â òîëóîëüíîì
ðàñòâîðå // Âûñîêîìîëåêóëÿðí.
ñîåäèíåíèÿ. Ñåð.
Á. 1971. Ò. 13. Ñ. 579-583.
56. Kay B.D., Assink R.A. Sol-Gel Science: The
Physics and Chemistry of Sol-Gel Processing // J. Non-Crystalline Solids. 1988,
104, p.112.
57. Äîëãîïëîñê
Ñ.Á., Êàãàí Å.Ã., Àõàíîâà
Ë.Ä., Êëåáàíñêèé
À.Ë., Ìàðòÿêîâà
Í.È., Ïàïåð Å.Ø. Êîíäåíñàöèÿ
ñèëàí- è ñèëîêñàíäèîëîâ
ïîä âëèÿíèåì íåóðàâíîâåøèâàþùèõ
êàòàëèçàòîðîâ
// Âûñîêîìîëåê.
ñîåä. 1970. Ò. 12À. Ñ. 2238-2241.
58. Bilda S., Lange D., Popowski E., Kelling H. Der
sauer katalysierte Kondensation von Organodimethylsilanolen in Dioxan/Wasser //
Z. Annorg. Allg. Chem. 1987. ¹ 550. P. 186-191.
. Lasocki Z. Substitution at a silicon atom in
organosilicon compounds. Condensation of diethylsilanediol in dioxane // Bull.
Acad. Polon. 1967. V. 14. ¹ 4. P. 819-823.
60. Äîëãîïëîñê
Ñ.Á., Ìàðòÿêîâà
Í.È., Êàãàí Å.Ã., Êîñòèíÿí
Ò.Ñ., Ïåòðóõíî Ë.À.
Êîíäåíñàöèÿ
ñèëîêñàíäèîëîâ
ïîä âëèÿíèåì îðãàíè÷åñêèõ
ñîëåé äâóõ- è ÷åòûðåõâàëåíòíîãî
îëîâà // Æóðí. îáù.
õèìèè. 1974. Ò. 44. Ñ. 298-303.
. Ìèëåøêåâè÷
Â.Ï., Íîâèêîâà Í.Ô.
Èíäóêöèîííûå
è ñòåðè÷åñêèå
ýôôåêòû çàìåñòèòåëåé
â õèìèè êðåìíèéîðãàíè÷åñêèõ
ñîåäèíåíèé // Óñïåõè
õèìèè. 1981. Ò. 50. Ñ. 95-110.
62. Chojnowski J., Chrzczonowicsh S. Polar effects
of substitution in base-catalysed polycondensation of silandiols // Bull. Acad.
Polon. 1966. V. 14. ¹ 1. P. 17-22.
63. Ñîììåð Ë. Ñòåðåîõèìèÿ
è ìåõàíèçìû
ðåàêöèé êðåìíèéîðãàíè÷åñêèõ
ñîåäèíåíèé. - Ì.: Ìèð,
1966. 96 ñ.
. Bilda S., Rohr G., Lange D., Popowski E.,
Kelling H. Der basenkatalysierte Kondensation von Organodimethylsilanolen in
Dioxan/Wasser // Z. Annorg. Allg. Chem. 1988. ¹ 564. P. 155
65. Äðîçäîâ Â.À.,
Êðåøêîâ À.Ï., Êíÿçåâ
Â.Í. Èçó÷åíèå
îòíîñèòåëüíîé
êèñëîòíîñòè
íåêîòîðûõ êëàññîâ
êðåìíèéîðãàíè÷åñêèõ
ñîåäèíåíèé â
íåâîäíûõ ñðåäàõ
// Æóðí. îáù. õèìèè.
1971. Ò. 41. Ñ. 881-887.
66. Artaki I., Zerda T.W., Jonas J. Study of
polimerization processes in acid and base catalyzed silica sol-gels // J.
Non-Crystalline Solids. 1986, 81, p.381.
. Rutz W., Lange D., Kelling H., Popowski E.
Der sauer katalysierte Kondensation von Dimethylsilandiol und Siloxandiolen in
Toluen/Wasser // Z. Annorg. Allg. Chem. 1986. ¹ 536. P. 197-208.
. Klempeper W.G., Ramamurthi S.D. Better
Ceramics Through Chemistry III // Mat. Res. Soc., Pittsburgh. 1988, pp. 1-14.
. Klempeper W.G., Mainz V.V., Ramamurthi S.D.,
Rosenberg F.S. Caracterization of the effect of formamide additive on the
silica sol-gel-glass forming process by 'H NMR // Better Ceramics Through
Chemistry III. 1988, pp. 15-24.
. Greber R., Resse E., Toole S. Preparation of
triorganosilanole // J. Makromol. Chem. 1962. V. 52. P. 87-90.
71. Âîðîíêîâ
Ì.Ã., Æàãàòà Ë.À.
Ãèäðîëèç ëèíåéíûõ
è öèêëè÷åñêèõ
ïîëèìåòèëñèëîêñàíîâ
// Æóðí. îáù. õèìèè.
1968. Ò. 38. Ñ. 2327-2330.
. Âîðîíêîâ
Ì.Ã. Ãåòåðîëèòè÷åñêèå
ðåàêöèè ðàñùåïëåíèÿ
ñèëîêñàíîâûõ
ñâÿçåé. - Ë.: Èçä-âî
ÀÍ ÑÑÑÐ, 1961. 48 ñ.
73. Gilman H., Benedict H.N., Hartzfeld H. J. The
hydrolysis of organosiloxanes // J. Org. Chem. 1954. V. 19. P. 419-422.
. Alah A.G., O’Brien H.D., Lui G.Y. The hydrolysis
of hexaorganosiloxanes // J. Am. Chem Soc. 1969. V. 91. P. 701-705.
. Assink R.A., Kay B.D. Sol-gel kinetics: Si
NMR and a statistical reaction model // J. Non-Crystalline Solids. 1988, 107,
pp. 35-40.
. Assink R.A., Kay B.D. Better Ceramics Through
Chemistry // North-Holland, New York. 1984, 107, p. 35-40.
77. Èâàíîâ Ï.Â.
Îñîáåííîñòè
ïîëèêîíäåíñàöèè
îðãàíîñèëàíîëîâ
// Âåñòíèê ÌÈÒÕÒ.
2011, Ò. 6, ¹3
78. Èâàíîâ Ï.Â.
Äèñ. äîê. õèì. íàóê,
Àêàäåìèÿ òîíêîé
õèìè÷åñêîé òåõíîëîãèè.
Ìîñêâà, 1998, 317 ñ.
79. Ñîêîëîâ
Ë.Á., Îñíîâû ñèíòåçà
ïîëèìåðîâ ìåòîäîì
ïîëèêîíäåíñàöèè
// Ì.: Õèìèÿ, 1979. 264 ñ.
80. Ï.Â. Èâàíîâ,
Â.À. Ïîãîäèí. 10 Âñåðîñ.
êîíô. «Êðåìíèéîðãàíè÷åñêèå
ñîåäèíåíèÿ: ñèíòåç,
ñâîéñòâà, ïðèìåíåíèÿ»,
ÈÍÝÎÑ ÐÀÍ-ÌÈÒÕÒ.
2005, 2Ñ21.
Ðàçìåùåíî
íà Allbest.ru