Выбор и обоснование энергоресурсов для производства метанола
Введение
Метанол (метиловый спирт) - одно из первых
продукций произведенных на губахинском химическом заводе. Его
производительность - 750 тыс. тонн метанола в год. Технологический процесс
производства метанола разработан английской фирмой ICI. Проект во всех частях
выполнен английской фирмой "DavyMcKee".
Качество метанола-ректификата должно
соответствовать требованиям ГОСТа 2222-95.
Управление основными стадиями процесса
централизовано и осуществляется из центрального пункта управления (ЦПУ).
Метанол, один из основных продуктов
многотоннажной химии, широко используется для получения множества ценных
химических веществ: формальдегида, сложных эфиров, аминов, растворителей,
уксусной кислоты. Мировое производство метанола превышает 20 млн т в год, и
спрос на него постоянно растет, что связано с наметившейся тенденцией
использовать метанол в новых областях, например для получения высокооктановых
бензинов, топлива для электростанций, как сырья для синтеза белка и т.д.
Метанол по объему производства и многообразию
областей применения относится к основным продуктам органического синтеза.
Областями потребления, определяющими спрос на
метанол в России, являются производства формальдегида, идущего на производство
синтетических смол и пластмасс; диметилтетрафталата, применяемого в
производстве полиэфирных волокон; синтетического каучука; растворителей;
уксусной кислоты и др.
В данной курсовой работе был проведен выбор и
обоснование энергоресурсов, географической точки строительства и мощности
производства.
Проведен термодинамический и кинетический анализ
и обоснован оптимальный технический режим.
Представлен расчет материального, теплового
баланса, расчет основного аппарата.
Также приведены технологическая схема и чертеж
основного аппарата.
1. Выбор и обоснование источников
сырья, энергоресурсов, географической точки строительства
.1 Обоснование сырья
энергоресурс использование синтез
метанол
Сырьём для производства метанола является синтез
- газ, получаемый конверсией природного газа. Снабжение предприятия природным газом
осуществляется от магистрального газопровода Чусовой - Березники - Соликамск,
который проходит рядом с предприятием.
1.2 Обоснование наличия
энергоресурсов
К энергоресурсам относятся электрическая,
тепловая энергии и вода.
Силовая энергия (380В) расходуется на работу
компрессорных машин и насосов. Световая энергия (320В) идет на бытовые нужды
завода. Источником этих видов энергии является ГРЭС им. Кирова в г. Губаха.
Энергия проходит заводскую подстанцию и
направляется в цеха.
Источником водных ресурсов служит река Косьва и
Широковское водохранилище, из которого ведется водозабор.
Вода в производстве метанола используется как
хладоагент в теплообменной аппаратуре, поэтому к ее качеству предъявляются
определенные требования по содержанию солей Ca и Mg. Поэтому на производство
вода поступает только из цеха химической водоподготовки.
Согласно калькуляции себестоимости 1т
метанола-ректификата для агрегата М-750 расход электроэнергии составляет
45кВт*ч, воды оборотной 3,5м3.
1.3 Обоснование географической точки
строительства
Для обоснования географической точки
строительства необходимо наличие следующих факторов:
близость источников сырья;
наличие потребителей;
наличие квалифицированных кадров;
благоприятные климатические условия;
наличие водных ресурсов;
наличие энергетических ресурсов;
наличие транспортных путей.
2. Выбор и обоснование способа
производства
Метанол (метиловый спирт) СН3ОН - прозрачная
жидкость со слабым специфическим запахом, напоминающим запах этилового спирта.
Температура кипения метанола 64,7°С;
температура плавления - 97,8°С; критическая
температура 240°С; плотность
0,796г/см3; теплота испарения 263 ккал/кг.
Впервые обнаруженный Боулем в 1661 г. в
продуктах сухой перегонки древесины, метанол в чистом виде был выделен лишь два
столетия спустя в 1834 г., Дугласом и Пелиготом. В тоже время была установлена
и его химическая формула.
Известно несколько способов получения метанола:
сухая перегонка древесины; термическое разложение муравьиной кислоты; синтез из
метана через метил хлорид с последующим омылением, и, наконец, неполное
окисление метана на катализаторах под давлением.
Из перечисленных методов промышленностью было
освоено получение метанола сухой перегонкой древесины. Но этот способ имеет
свои недостатки:
малая мощность;
использование дорогостоящего и дефицитного сырья
(из 1м3 березовых дров можно получить лишь 5-6 кг метанола);
большое количество примесей;
повышенный расход энергии;
высокая себестоимость конечного продукта;
В настоящее время, этот метод, бывший
единственным освоенным промышленностью процессом потерял своё значение и
вытеснен синтезом метанола из оксида углерода и водорода на катализаторах.
Последние агрегаты метанола достигают большой
единичной мощности - 750000 т/год.
Ректификация метанола - сырца происходит в ректификационной
колонне с клапанными тарелками. Питание подается в виде жидкости нагретой до
температуры кипения.
Приведем краткую характеристику метода
производства на губахинском М-750, разработанного фирмой ICI (Англия)/8/.
Исходным сырьем для производства метанола
является природный газ.
Процесс получения синтез газа, необходимого для
синтеза метанола, основан на каталитической конверсии углеводородов природного
газа с водяным паром в трубчатой печи в присутствии никелевого катализатора при
давлении Р=18 кг/см2 и t=8600С (на выходе из реакционных труб).
Синтез метанола предусматривается под давлением
80 атмосфер и температуре 210-2700С в присутствии медьсодержащего катализатора.
Отгонка примесей, содержащихся в метаноле-сырце,
предусмотрена в последовательных колоннах предварительной и основной
ректификации без давления.
Описанный метод получения метанола помимо
указанных основных стадий включает в себя ряд вспомогательных и в целом состоит
из следующих стадий:
компримирование природного газа центробежным компрессором
с Р=30 кг/см2;
двухступенчатая очистка природного газа от
сернистых соединений (гидрирование и поглощение);
каталитическая конверсия углеводородов с водяным
паром в трубчатой печи при Р= 18 кг/см2 и T= 8600С;
компримирование полученного синтез газа с Р=14,6
кг/см2 до Р=81 кг/см2 центробежным компрессором с подачей его на всас
циркуляционного компрессора цикла синтеза метанола;
синтез метанола при давлении примерно Р=80
кг/см2.
двух стадийная ректификация метанола-сырца.
Производство метанола состоит из следующих
блоков:
блока сероочистки и конверсии в составе одного
агрегата сероочистки и двух агрегатов конверсии природного газа;
блока компрессии в составе одного компрессора
природного газа, одного компрессора синтез газа и одного циркуляционного
компрессора;
блока синтеза метанола в составе двух агрегатов
синтеза;
блока ректификации метанола-сырца в составе
одного агрегата предварительной ректификации и 2-х агрегатов основной
ректификации.
В состав производства метанола также входят:
вспомогательный котел;
установка деминерализации речной воды;
оборотный цикл;
факельная установка;
склад метанола с насосной и наливной эстакадой.
Основное оборудование (реакторы, колонны,
компрессоры) установлено без резерва и рассчитано на годовой цикл работы с остановкой
для проведения ремонтов.
3. Обоснование оптимальных
параметров технологического процесса
Рассмотрим диаграмму t-x-y для системы
метанол-вода при атмосферном давлении.
Рис. 3.1 - Зависимости температуры кипения и
конденсации от состава жидкости и пара
На диаграмме t-x-y по оси абсцисс отложены
составы жидкости (метанола) и пара, а по оси ординат - температуры t для
условий постоянного давления. Верхняя кривая называется линией конденсации,
нижняя - линией кипения. Из построенной диаграммы видно, что пар конденсируется
при температуре, которая выше температуры кипения метанола. Кроме того,
температура кипения смеси ниже температуры кипения чистого ВК и выше
температуры кипения чистого. По мере увеличения содержания в смеси НК
температура кипения понижается.
Каждому определённому значению концентрации х в
жидкой фазе в состоянии равновесия соответствует вполне определённое значение
концентрации у* в паровой фазе (знаком * отмечают величину, относящуюся к
равновесному состоянию). Математически это выражается формулой:
y*=f(x) (3.2.1)
Графически взаимодействие между фазами в
ректификационной колонне можно представить на диаграмме у-х (рис.3.2).
Рис. 3.2 - Диаграмма равновесия
Рабочая линия показывает, что поступающая в
колонну жидкость концентрации х1 по мере движения вниз освобождается от НК, на
выходе из колонны концентрация х2 минимальная. По мере движения пара вверх
концентрация НК в нём возрастает.
Скорость перехода вещества пропорциональна
разности равновесной и рабочей концентраций вещества в одной из фаз. Эта
разность называется движущей силой процесса массопередачи.
Интенсификацию процесса массопередачи можно
осуществить путём увеличения поверхности контакта Fф между взаимодействующими
фазами. Практически это достигается барботажем пара через жидкость, развитием
смоченной поверхности насадки. Повышения коэффициента массопередачи К можно
достичь путём турбулизации (интенсивного перемешивания) взаимодействующих фаз,
что обеспечивается соответствующим конструктивным оформлением проточной части
аппарата. Возрастание движущей силы процесса ∆ также способствует
интенсификации массопередачи и достигается за счёт увеличения подачи флегмы в
колонну.
Влияние физических факторов.
Рассмотрим влияние температуры, давления и
ускорения силы тяжести. Поскольку объём газовой фазы с изменением температуры и
давления изменяется, исследования этих факторов на массопередачу целесообразно
проводить при постоянной массовой скорости (Wr=const).
Влияние температуры.
Влияние температуры на коэффициент массопередачи
КУ определяется температурной зависимостью m/βх.
С повышением температуры увеличиваются m и βх;
при этом отношение m/βх в
зависимости от соотношения температурных коэффициентов для m и βхможет
возрастать или уменьшаться. В соответствие с этим при при повышении температуры
КУ будет уменьшаться или увеличиваться, принимая в некоторых случаях
экстремальные значения.
Влияние давления.
Поскольку константа фазового равновесия не
зависит от давления, а константа mУХ обратно пропорциональна Р, с увеличением
давления КУ увеличивается (вследствие уменьшения mУХ).
4. Синтез и анализ ХТС (химическая,
структурная, операторная и технологическая схемы)
Отделение ректификации метанола включает в себя
следующие участки:
отгонка легких фракций от метанола-сырца;
основная ректификация;
4.1 Отгонка от метанола-сырца легких
фракций
Метанол-сырец из склада метанола насосами поз.
3254/1,2 подается в колонну отгонки легких фракций поз.1141. Стабилизация
расхода метанола-сырца, подаваемого в колонну, производится с коррекцией по
уровню в кубе колонны и расходам в колонны поз.1143/1,2.
В линию метанола-сырца перед подачей в колонну
дозируется 1%¸2% раствор NaOH для нейтрализации
избыточной кислотности, что предотвращает коррозию оборудования и трубопроводов
ректификации. Количество добавляемого раствора щелочи определяется по рН среды
кубовой жидкости колонны поз.1141 и регулируется по шкале дозировочного насоса
поз.1741.
Перед поступлением в колонну поз.1141
метанол-сырец подогревается в теплообменнике поз.1542 кубовым остатком,
поступающим из колонн основной ректификации поз.1143/1,2. Предусмотрена
сигнализация снижения температуры метанола сырца перед теплообменником поз.
1542 ниже 100С. Имеется байпасная линия теплообменника поз. 1542 с запорной
арматурой, а также линии подачи метанола-сырца в ребойлер поз. 1548 и сбросом в
дренажную систему отделения.
Метанол-сырец подается на одну из тарелок 36 или
40. Предусмотрена возможность подачи метанола-сырца по дополнительным вводам в
колонну на тарелки 28, 32.
В колонне поз. 1141 установлено 48 тарелок
ситчатого типа, двухсливных из углеродистой стали.
Температура и давление в колонне зависит от
нагрузки колонны и состава метанола-сырца.
Режим работы колонны следующий:
|
Температура,
0С
|
Давление,
кг/см2
|
|
Вверху
колонны
|
н/б
78
|
н/б
0,8
|
|
Внизу
колонны
|
80¸88
|
до
1,2
|
Нагрев кубовой жидкости колонны поз. 1141
производится в трех ребойлерах поз. 1543/1 и 2, 1548. Теплоносителем в ребойлерах
поз. 1543/1 и 2 является конвертированный газ, а в ребойлере поз. 1548 - пар
низкого давления, подаваемый в межтрубное пространство.
Пары, выходящие с верха колонны конденсируются в
2-х последовательно установленных конденсаторах. Основное количество метанола
конденсируется в аппарате воздушного охлаждения (АВО) поз. 1641.
Несконденсировавшиеся пары конденсируются в кожухотрубном теплообменнике
поз.1549 с водяным охлаждением. Распределение потоков паров флегмы на воздушный
конденсатор поз.1641 и водяной конденсатор поз.1549 производится изменением
угла наклона жалюзи АВО.
Для предотвращения накопления легколетучих
компонентов, плохо отделяемых в процессе ректификации в колонне поз. 1141,
производится отбор части конденсата (вторичного метанола) после теплообменника
поз. 1549, который самотеком поступает на склад метанола в емкость сивушных
масел поз. 1257 в количестве до 660 кг/час. Несконденсированные газы после
вторичного конденсатора поз. 1549 поступают в сепаратор поз. 1162 (в этот же
сепаратор поступают газы мгновенного испарения из расширительного сосуда
метанола-сырца поз. 1152 отделения синтеза метанола). Жидкость, отделившаяся в
сепараторе поз. 1162, стекает в линию конденсата после вторичного конденсатора
поз. 1549 и далее поступает в сборник флегмы поз. 1142.
Флегма из конденсаторов поз.1641 и 1549
поступает в сборник поз.1142. Флегма из сборника поз.1142 насосами поз.3242/1,2
подается в колонну поз. 1141 на 48 тарелку. Общая тепловая нагрузка колонны
поз.1141 поддерживается за счет подвода тепла конвертированного газа к
испарителям поз.1543/1,2, а также за счет работы дополнительного парового
подогревателя поз.1548.
Из куба колонны поз.1141 метанол подается
насосами поз.3243/1,2 в колонны основной ректификации поз.1143/1,2. Для более
полного отделения низкокипящих веществ из метанола-сырца за счет увеличения
парциального давления основного компонента - метанола, предусмотрена подача
азота через клапан HV-5010 в колонну поз. 1141.
4.2 Получение метанола-ректификата
Метанол из куба колонны отгонки мелких фракций
поз. 1141 насосами поз. 3243/1 или 2 (один в работе, другой в резерве,
предусмотрено авторезервирование насосов) подается в ректификационные колонны
поз. 1143/1 и 2. Подача метанола осуществляется на одну из питающих тарелок №№
17, 20, 24, 26, 33.
Регулирование подачи метанола в колонну основной
ректификации поз.1143/1(2) производится с учетом нагрузки соответствующей печи
реформинга, ввиду зависимости тепловой нагрузки, а следовательно и расхода
флегмы от этого показателя.
Ректификационная колонна поз. 1143/1(2)
представляет собой вертикальный цилиндрический аппарат, в котором смонтировано
83 ситчатых тарелки. Шесть верхних тарелок изготовлены из нержавеющей стали,
остальные из углеродистой.
Температура в колонне зависит от давления и состава
метанола, подаваемого после колонны поз. 1141 и нагрузки на колонну.
Режим работы колонны основной ректификации:
|
Температура,
0С
|
Давление
кг/см2
|
|
Вверху
колонны
|
н/б
78
|
н/б
0,75
|
|
Внизу
колонны
|
115¸128
|
н/б
1,7
|
Для испарения кубовой жидкости в качестве
основного тепла (75% от общего тепла) в испарителях поз.1544/1(2) используется
физическое тепло конвертированного газа при его охлаждении от 2900С до 1400С и
тепло конденсации водяных паров, содержащихся в конвертированном газе, при
температуре 1550С. Пары из верха колонны направляются в аппараты воздушного
охлаждения поз.1643/1(2), где происходит их конденсация. Давление верха колонны
поз.1143/1(2) до 0,75 кг/см2 поддерживается посредством изменения угла наклона
жалюзи АВО поз.1643/1(2), а также количеством включенных вентиляторов.
Рабочее флегмовое число (отношение расходов
флегмы к расходу ректификата) для колонн данной конструкции равняется 3-ем.
Минимальный расход флегмы, ниже которого качество метанола-ректификата не
гарантируется - 95 т/час.
Конденсат с температурой 70¸720С
стекает в сборник флегмы поз. 1144/1(2). Снижение температуры конденсата после
АВО поз. 1643/1(2) при неизменном рабочем давлении в ректификационной колонне
поз. 1143/1(2) свидетельствует о накоплении легких компонентов и инертов.
Предусмотрено автоматическое регулирование
содержания инертов по разности температур верха колонны TI-5100-13 (5200-13) и
выхода из конденсатора поз.1643/1(2) TR-5109 (5209). Необходимо следить чтобы
эта разность была в пределах 10ОС для предотвращения гидроударов в трубчатке
воздушного конденсатора поз. 1643/1(2) в зимнее время. Инерты из системы
удаляются через клапан HV-5102 (5202), установленный на линии сброса инертов из
сборника флегмы поз. 1144/1(2). Сброс производится через продувочный сепаратор SM/12-2
в факельный коллектор.
Сконденсированный метанол поступает в сборник
поз.1144/1(2). Уровень в сборнике поз.1144/1(2) поддерживается постоянным
отводом насосами поз. 3244/1,2(3,4) в колонну на 83 тарелку.
Метанол-ректификат отбирается с одной из тарелок
81,79 и охлаждается в холодильнике поз. 1541/1(2) до температуры 35·400С.
Метанол-ректификат в количестве 26000¸60000 кг/час
направляется на склад в анализную емкость поз.1255.Фракция метанол-масло-вода
подается в резервуар поз. 1257 склада метанола.
Кубовый остаток колонн основной ректификации
-вода с содержанием до 0,02% вес. метанола после охлаждения в теплообменнике
метанола-сырца поз.1542 направляется на биологическую очистку или в емкость
сточных вод поз.6942 откуда насосами поз.3249/1,2 периодически откачиваются на
биологическую очистку.
5. Выбор и обоснование конструкции
основного аппарата
Все расчёты проводились на компьютере с
использованием программы «DESIGNII»/Был проведен расчет колонны основной
ректификации где использовался модуль -Distill- 4 характерный для расчёта
полной колонны дистилляции с боковым отводом.
Исходные данные для расчета:
состав исходной смеси: СН3ОН - 83,344%мас.; Н2О
- 16,525%мас.;BuOH - 0,131%мас.
температуру на входе в колонну: 50°C
температуру верхней и нижней части колонны: 88°C
и 125°C соответственно;
давление в верхней и нижней части
соответственно: 0,4 кг/см2 и 1,1 кг/см2;
номер тарелки питания 20
номер тарелки отвода 18
Модель колонны основной ректификации.
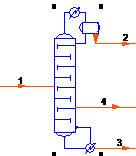
Рис. 5.1
Основные данные потоков получившиеся при
моделировании приведены в таблице 5.1.
Таблица 5.1 - Результаты математического
моделирования
|
|
1.Метанол
сырец
|
2.Метанол
ректификат
|
3.Вода
|
4.Изобутиловый
спир
|
|
Температура
|
C
|
50
|
73,03044
|
121,70089
|
104,36581
|
|
Давление
|
kg/cm2g
|
1
|
0,4000015
|
1,1
|
0,9397627
|
|
Энтальпия
|
kJ/hr
|
-85450699,8
|
-56099525,3
|
-20420168,9
|
-1714795,23
|
|
Энтропия
|
kJ/K/s
|
-65,05353
|
-45,67157
|
-14,91675
|
-1,234051
|
|
Плотность
жидкости
|
kg/m3
|
682,07032
|
632,33105
|
941,74507
|
714,8554
|
|
Удельный
вес жидкости
|
60F@STP
|
0,8267072
|
0,7993227
|
1,00008
|
0,8992441
|
|
Ср
жидкости
|
kJ/kg/K
|
3,85027
|
3,7266
|
4,25202
|
4,3856
|
|
Вязкость
жидкости
|
ns/m2
|
0,0005152
|
0,0003296
|
0,0002287
|
0,0004245
|
|
Теплопроводность
жидкости
|
W/m/K
|
0,7151839
|
0,5341914
|
0,6834024
|
0,8305499
|
|
Расход
|
m3l(NTP)/hr
|
76,30262
|
65,09584
|
9,94791
|
1,24551
|
|
Молекулярный
вес
|
32,042
|
18,0154
|
22,8801
|
|
Молярный
расход
|
kgmol/hr
|
2252,8815
|
1651,4585
|
552,0663
|
49,3567
|
|
Массовый
расход
|
kg
|
64000,08294
|
52916,03326
|
9945,695221
|
1129,286232
|
Результаты расчётов показали полную сходимость с
практическими данными, что говорит о правильности решения.
Полученные данные расчета колонны основной
ректификации приведены в таблице 5.2.
Таблица 5.2 - Данные расчета колонны основной
ректификации
|
Температура
верха
|
C
|
73,03
|
|
Температура
низа
|
C
|
121,7
|
|
Флегмовое
число
|
|
2,8
|
|
Тепловая
нагрузка на дефлегматор
|
kJ/hr
|
2,32E+08
|
|
Тепловая
нагрузка на куб
|
kJ/hr
|
2,4E+08
|
|
Максимальный
диаметр
|
m
|
5,168
|
|
CalculatedTrayMaximumFlood
|
%
|
80
|
|
Продукты
|
kgmol/hr
|
1651,458
|
Составив математическую модель основной
ректификации можно предложить следующие оптимальные параметры ведения процесса:
. температура исходной смеси Ти= 64,40С.
. давление исходной смеси Ри=1 кгс/см2
. расход исходной смеси Gи=126690 кг/ч.
. количество тарелок N=83
. флегмовое число R=2,8
. температура верха Тв=780С.
. температура низа Тн=1250С.
. давление верха Рв=0,4 кгс/см2
. давление низа Рн=1 кгс/см2
. питание подается на 20 тарелку.
. отбор сивушных масел производится с 18
тарелки.
. количество получаемого дистиллята
Gд=104219кг/ч.
6. Материальный и энергетический
баланс отделения на часовую производительность
.1 Материальный баланс
Ректификация метанола-сырца идет в две стадии.
Первая стадия - отгонка легких фракций.
Поток метанола-сырца поступает в ректификационную
колонну отгонки легких фракций.
Расход потока - 127500 кг/ч.
Состав потока:
СН3ОН - 83,3134%; Н2О - 16,4201%; СО - 0,0002%;
СО2 - 0,0688%;
СН4- 0,0136%; I-BuOH - 0,1305%; N2 - 0,0002%
В качестве флегмы подается стопроцентный
метанол.
Расход потока - 67548 кг/ч.
Состав кубового остатка:OH - 83,344%; H2O -
16,525%; i-BuOH - 0,131%;
Состав дистиллята:
СН3ОН
- 99,7759%; CO - 0,0005%; CO2 - 0,0935%; H2 - 0,0106%;
СН4 - 0,0507%; N2 -
0,0003%
Расчет ведем на 1000кг метанола.
+ 67548 = GК.О.*0,83344 + GД*0,997759Д = (195048
- GК.О.)*0,997759
= GК.О.*0,83344 + (195048 - GК.О.)*0,997759К.О.
= 126690 кг/ч.Д = 68358 кг/ч.
Таблица 6.1 - Материальный баланс
ректификационной колонны отгонки легких фракций
|
Приход
|
кг/ч
|
Расход
|
кг/ч
|
|
метанол-сырец
флегма
|
127500
67548
|
кубовый
остаток дистиллят
|
126690
68358
|
|
Итого:
|
195048
|
Итого:
|
195048
|
Вторая стадия - основная ректификация.
Кубовый остаток из колонны отгонки легких
фракций направляется в колонны основной ректификации.
В качестве флегмы используют стопроцентный
метанол.
Расход флегмы - 156176 кг/ч.
Флегма является дистиллятом.
Состав метанола - ректификата:
OH - 99,95%; H2O - 0,05%.
Из колонны основной ректификации отбирается
фракция метанол-масло-вода состава:
OH - 62,822%;H2O - 29,813%; i-BuOH - 7,365%.
Расчет ведем на 1000 кг метанола.
Из низа колонны выходит кубовый остаток.
Состав кубового остатка:
O - 99,98%; CH3OH - 0,02%.
Так как в качестве флегмы используется дистиллят
основной колонны, то ее можно сократить.
Расход сивушных масел 1127кг/ч. Т.к. колонны
две, то 2254 кг/ч.
*0,83344 = (1127*0,62822)*2 + GК.О.*0,0002 +
GРЕКТ.*0,9995
= GК.О. + GРЕКТ.РЕКТ. = 124436 - GК.О.
,5 = GК.О.*0,0002 + (124436 - GК.О.)*0,9995К.О.
= 20216 кг/ч.РЕКТ. = 124436 - 20216 =104219 кг/ч.
Таблица 6.2 - Материальный баланс основной
ректификации
|
Приход
|
кг/ч
|
Расход
|
кг/ч
|
|
кубовый
остаток
|
126690
|
метанол-ректификат
сивушное масло кубовый остаток
|
104219
2254 20216
|
|
Итого:
|
126690
|
Итого:
|
126690
|
6.2 Энергетический баланс
Исходные данные для расчета теплового баланса.
-стадия (предварительная ректификация)
Исходная смесь, состав:
CH3OH - 83,31%; H2O - 16,42%; G =
127500кг/ч.
Кубовый остаток, состав:
CH3OH - 83,34%; H2O - 16,525%; G =
126690кг/ч.
Дистиллят, состав:
CH3OH - 99,77%; H2O -0,2%; G = 68358кг/ч.
Флегма, состав:
CH3OH - 99,77%; H2O -0,2%; G = 68358кг/ч.
2-стадия(основная ректификация)
Исходная смесь, состав:
CH3OH - 83,34%; H2O - 16,525%; G =
126690кг/ч.
Кубовый остаток, состав:
CH3OH - 0,02%; H2O - 99,98%; G =
10108кг/ч.
Дистиллят, состав:
CH3OH - 99,95%; H2O - 0,05%; G =
104129кг/ч.
Флегма, состав:
CH3OH - 99,95%; H2O - 0,05%; G =
156176кг/ч.
Боковой отвод:
CH3OH - 62,822%;H2O - 29,813%;
i-BuOH - 7,365%; G = 2254кг/ч.
Расчет энергетического баланса.
-стадия (предварительная ректификация)
QПРИХОДА = QРАСХОДА (6.2.1)ПРИХОДА =QF + QС
(6.2.2)
где QF - тепло смеси.С - тепло поступающее со
стороны.
РАСХОДА = QW + QД + QФ + QП (6.2.3)
где QW - тепло кубового остатка.Д - тепло
дистиллята.Ф - тепло необходимое для образования флегмы.П - тепловые
потери(3%).
Расчет тепла приходящего с исходной смесью.
= GF*aF*Tf (6.2.4)=450C,
GF = 127500кг/ч.
где aF - удельная
теплоемкость исходной смеси (Дж/кг*К),- массовый расход исходной смеси(кг/ч).-
температура(К).
aF = XМ*aМ + (1 - XМ)*aB
(6.2.5)
где XМ - содержание метанола в смеси
(масс.доля).XМ = 0,83
aМ - уд. теплоемкость CH3OH(Дж/кг*К);aМ
=2690Дж/кг*К
aВ - уд. теплоемкость H2O(Дж/кг*К);aВ
= 4190Дж/кг*К
aF = 2945Дж/кг*К= 33168063 Вт
Расчет теплоты кубового остатка.
= GW*aW*tW (6.2.6)
где tW = 860C; GW = 126690кг/ч.
aW = XМ*aМ + (1-XМ)* aВ
(6.2.7)
aW = 3147 Дж/кг*К= 39758595 Вт
Расчет теплоты необходимой для образования
флегмы.
Ф = GФ*(1+R)*rф (6.2.8)
где GФ - расход флегмы (кг/ч). GФ = 68358кг/ч.-
флегмовое число. R = 2,664ф - удельная теплота конденсации.
ф= XМ*rМ + (1-XМ)*rВ (6.2.9)
Ф = 1076600
Ф = 45996989 Вт
Расчет теплоты дистиллята.
Д = GД*aД*tД (6.2.10)
где GД = 68358кг/ч; tД =750С.
aД = XМ*aМ + (1-XМ)* aМ
(6.2.11)
aД = 2767,9Дж/кг*КД = 18290117 Вт
Расчет тепла поступающего со стороны.
С = 1,03*(QД + QW + QФ -QF) = 73003349 Вт
Таблица 6.3 - Тепловой баланс предварительной
ректификации
|
Приход
|
Вт
|
Расход
|
Вт
|
|
1,QF
2,QС
|
33168063
73003349
|
1,QД
QW 3,QФ
|
18290117
41884306 45996989
|
|
Итого:
|
106171412
|
Итого:
|
106171412
|
-стадия(основная ректификация)
Уравнение теплового баланса:
ПРИХОДА = QРАСХОДАПРИХОДА =QF + QС
где QF - тепло смеси.С - тепло поступающее со
стороны.
РАСХОДА = QW + QД + QФ + QОТВ +QП
где QW - тепло кубового остатка.Д - тепло
дистиллята.Ф - тепло необходимое для образования флегмы.ОТВ - тепло фракции
метанол-масло-вода.П - тепловые потери(3%).
= GF*aF*tF
где tF =860C, GF = 126690кг/ч.
aF = XМ*aМ + (1 - XМ)*aB
где XМ = 0,834
aF = 3146Дж/кг*К= 37350552 Вт
Расчет теплоты кубового остатка.
= GW*aW*Tw
где tW = 1240C; GW = 10108кг/ч.
aW = XМ*aМ + (1-XМ)* aВ
aW = 4189 Дж/кг*К=6476149 Вт
Расчет теплоты дистиллята.
Д = GД*aД*tД
где GД = 104129кг/ч; tД =760С.
aД = XМ*aМ + (1-XМ)* aМ
aД = 2808Дж/кг*К
Д = 28345996 Вт
Расчет теплоты необходимой для образования
флегмы.
Ф = GФ*(1+R)*rф
где GФ = 156176кг/ч.- флегмовое число. R = 2,664
ф= XМ*rМ + (1-XМ)*rВ
где rФ = 1071800Ф = 82299806 Вт
Расчет теплоты бокового отвода.
ОТВ = GОТВ*aОТВ*tОТВ
aОТВ = 3121Дж/кг*КОТВ = 2474316 Вт
Расчет тепла поступающего со стороны.
С = 1,03*(QД + QW + QФ + QОТВ -QF) = 82245815 Вт
По / 15 / 25% тепла поступающего со стороны
является пар = 20561453 Вт. 75% -контактные газы.
Расход пара = QК / rг.п.*h
=20561453 / 2171000*0,95 »»10кг/с = 36000кг/ч.
Таблица 6.4 - Тепловой баланс основной
ректификации
|
Приход
|
Вт
|
Расход
|
Вт
|
|
1,QF
2,QС
|
37350552
82245715
|
1,QД
QW QФ 4,QОТВ
|
28345996
6476149 82299806 2474316
|
|
Итого:
|
119596267
|
Итого:
|
119596267
|
Мощность выбирается исходя из следующих положений:
Потребность в данном производстве.
Наличие сырья.
Техническая возможность оборудования.
В настоящее время потребность в метаноле очень
велика, запасы сырья достаточны. Поэтому выбор мощности будет ограничиваться
технической возможностью оборудования, максимальная единичная мощность агрегата
750000 т/год, что и принято в проекте.
Для расчёта мощности используем формулу:
ц = g * TЭФ * n,
где g - часовая производительность одной колонны
ректификации;- количества ректификационных колонн;
ТЭФ - эффективное время работы агрегата, час
ТЭФ находим по формуле:
ТЭФ = ТКАЛ - ТППР = 8760 - 1560= 7200 час.
где ТКАЛ - календарное время, час
ТППР - время планово - предупредительных
ремонтов, час.
Мощность агрегата составляет 750000 т в год
Часовая производительность = 52,08 т в час
=N/(g*Tэф)=750000/52,08*7200=2
Таким образом, для обеспечения мощности 750000
т/г потребуется установка двух колонн основной ректификации.
7. Экологическая оценка
производства, отходы производства, их утилизация, ПДК
В связи с быстрым развитием промышленности,
которое сопровождается возрастающим загрязнением воздушного бассейна и
водоемов, проблема охраны внешней среды во многих странах приобрела важное
значение. Загрязнение водоемов и атмосферы создает реальную опасность здоровью
населения и причиняет огромный ущерб рыбному хозяйству.
При производстве 1 т метанола ректификата
образуются следующие отходы:
7.1 Твёрдые отходы
К ним относятся отработанный катализатор синтеза
метанола, состава
(% вес):
Cu - 44 ±
3; ZnO - 28 ± 2; Al2O3 - 6 ±
1; Cu2O3 - 13± 1;O3 - 0,1; Na2O - 0,06; графит
- 1,5±
0,5
Предусматривается его использование в качестве
вторичного сырья предприятиями цветной металлургии.
.2 Газообразные отходы
Продувочные газы синтеза метанола, состава, (%
вес):
CO - 0,45-2,36; CO2 - 0,77-2,09; N2
- 1,8-1,59; CH3OH - 0,58-0,5;- 12,55-12,1; (CH3)2O - 0,01-0,03; H2O -
0,06-0,05; H2 - 83,78-81,28
Эти газы будут использоваться в качестве
водородсодержащего сырья для гидрирования сернистых соединений, а также в качестве
топлива в трубчатых печах.
Танковые газы, состава (% вес):
СО - 0,4-2,22; СО2 - 4,09- 11,63; H2 -
65,81-58,31; N2 - 1,24-0,96;- 19,9-18,1; (CH3)2O- 0,18-0,39; H2O - 0,8-0,83;
CH3OH- 7,55-7,56
Эти газы будут направляться в горелки печи
риформинга в качестве топлива.
7.3 Жидкие отходы
К жидким отходам можно отнести кубовый остаток
после основной ректификации следующего состава (% вес):H2O - 99,98%; CH3OH -
0,02%.
Жидкие отходы направляются на биологическую
очистку.
Из вышесказанного можно сделать вывод: что за
счёт утилизации отходов, производство метанола можно считать экологически
безопасным при условии выбора эффективного способа очистки дымовых газов от
окислов азота.
Заключение
В данной курсовой работе были рассмотрены
теоретические основы процесса ректификации метанола, проведен анализ способа
производства, представлен выбор и обоснование сырья, энергоресурсов,
географической точки строительства, дан анализ экологической безопасности. На
основе теоретического анализа выбраны оптимальные условия протекания процесса
ректификации метанола. Приведен расчет ректификационной колонны.
Приведена технологическая схема процесса
ректификации, основного аппарата.
Список использованной литературы
1. А.М.
Кутёпов, Т.И. Бондарёва, М.Г. Беренгартен Общая химическая технология, Москва
"Высшая школа", 1990г.
2. Караваев,
М.М. Технология синтетического метанола. М.М. Караваев. Исп. - М.:Химия,1984.
-144с.
. Технологический
регламент производства метанола. Ложкин, А.Ф. Оборудование крупнотоннажных
агрегатов метанола. Учебное пособие. Пермь: ППИ,1984.-86с.
. Примеры
и задачи курсу процессов и аппаратов химической технологии. К.Ф. Павлов, П.Г.
Романков, А.А. Носков: Химия, Ленинград, 1987.
. Краткий
справочник физико-химических величин.1974.-158с
. Макаров
Г.В. и др. Охрана труда в химической промышленности. М: Химия,1989.-496с.
. Виноградов
А.С., Даут В.А. Современное состояние производства метанола. Москва. 2001.
149с.
. И.А.
Александров. Массопередача при ректификации и абсорбции многокомпонентных
смесей. Л.: Химия, 1975.