3,5-динитро-4-гидрокси-пиридиноксид. Получение и свойства
3,5-динитро-4-гидрокси-пиридиноксид.
Получение и свойства
Содержание
1. Методика синтеза 3,5-динитро-4-гидрокси-пиридиноксида
.1 Получение 4-оксипиридона из γ-пирона
.2 Получение 4-гидроксипиридиноксида из 4-гидроксипиридина
.3 Получение 3,5-динитро-4-гидроксипиридиноксида
. Химические свойства 3,5-динитро-4-гидроксипиридиноксида
Список использованной литературы
1. Методика
синтеза 3,5-динитро-4-гидрокси-пиридиноксида
На основе анализа литературных источников можно сделать вывод, сто наиболее
рациональный метод получения 3,5-динитро-4-гидрокси-пиридиноксида
осуществляется с помощью достаточно сложного многостадийного синтеза. Можно
выделить три ключевые стадии синтеза. На первой происходит образование
4-оксипиридона, который, посредством таутомеризации в неполярных растворителях
образует 4-гидроксипиридин. Электронодонорный гидроксильный заместитель в
положении 4 активирует ароматическую -систему 4-гидроксипиридина, вследствие
чего упрощается электрофильное замещение [1]. Второй стадией синтеза является
нитрование 4-гидроксипиридина по положениям 3- и 5-. На третьей,
заключительной, стадии происходит образование
3,5-динитро-4-гидрокси-пиридиноксида при взаимодействии
3,5-динитро-4-гидрокси-пиридина с надкислотами. Рассмотрим перечисленные стадии
более подробно [2, c.140].
.1 Получение
4-оксипиридона из γ-пирона
Как известно из литературных данных, получение 4-оксипиридонов возможно
только из ациклических соединений, в отличие от 2-алкилоксипиридонов, которые
возможно получать гидроксилироваться под воздействием K3[Fe(CN)6]. [3, с.586]
Следовательно, первой стадией синтеза
3,5-динитро-4-гидрокси-пиридиноксида является получение 4-оксипиридона.
Получение 4-оксипиридона можно проводить несколькими способами.
Первый способ заключается в получении 4-оксипиридона из γ-пирона. Пирон, относящийся к
шестичленным кислородосодержащим гетероциклам, получают конденсацией щавелевой
кислоты и ацетона в присутствии HCl и
последующей декарбонизации над медной проволокой по реакции (1) [4, c.296]:

γ-пирон
пиридиноксид синтез водород нуклеофильный
Далее
проводится аминолиз γ-пирона и образование 4-оксипиридона. Следует отметить,
что пироны состоят в близком родстве с пиридинами, и при реакции с аммиаком
легко замещают свой кольцевой атом азота на иминогруппу, образуя
соответствующие пиридоны, в неполярных растворителях таутомеризующиеся в
4-гидроксипиридины [4, c.365]:
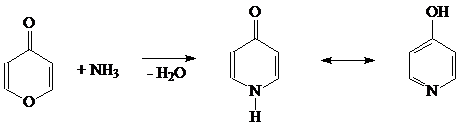
-оксопиридон
4-гидроксипиридин
С
учетом потерь веществ, возникающих на первой стадии данного синтеза, выход
4-гидроксипиридина составляет 40-50%.
Следует
отметить, что получение 4-гидроксипиридина конденсацией диальденидов чревато
образованием множества побочных продуктов и малым выходом целевого соединения.
[5, c. 95]. Наиболее рациональным способом получения
4-оксипиридина является гидролиз хлористого 4-пиридилпиридиния при кипячении
его водного раствора в течение 60 минут:
Учитывая,
что исходный хлоргидрат хлористого 4-пиридилпиридиния получается с выходом 60%,
то общий выход 4-оксипиридина из пиридина по реакции (3) составляет 35-40%. [4,
c.412]
Таким
образом, в рассмотренных методиках синтеза первого промежуточного продукта
используются доступные для практически любой лаборатории реактивы, а реакции
протекают с приемлимыми выходами конечного продукта.
.2 Получение
4-гидроксипиридиноксида из 4-гидроксипиридина
Следующей стадией приведенной цепочки реакций является получение
4-гидроксипиридиноксида из 4-гидроксипиридина. Пиридин N-оксиды получают окислением пиридинов надкислотами. В
качестве окислителя обычно используется перуксусная кислота, но во многих
случаях используются пербензойная и пероксифталевая кислоты, позволяющие
получать пиридин N-оксиды в
неполярных растворителях и в более мягких условиях. Реакция проводится в
слабокислой среде, так как в сильнокислой среде реакция не идет из-за
протонирования азагруппы (и разложения перекисного соединения), а в щелочной
среде перкислота депротонируется и превращается в малоактивный анион. [2, c.140]
Достаточно распространена методика синтеза пиридин N-оксидов при помощи смеси перекиси
водорода и уксусной кислоты. [6] 3,5-динитро-4-гидроксипиридиноксид получали
взаимодействием 3,5-динитро-4-гидроксипиридина с 30% переоксидом водорода в
среде уксусной кислоты. Выход реакции (6) составил 80% [7]
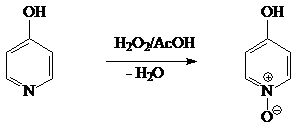
.3 Получение
3,5-динитро-4-гидроксипиридиноксида
Заключительной стадией синтеза конечного продукта:
3,5-динитро-4-гидроксипиридиноксида из 4-оксипиридиноксида. Указанную стадию
необходимо проводить после получения замещенного пиридиноксида, так как
кислородный атом в пиридиноксиде облегчает электрофильное замещение в
ароматическом кольце. [1]
В литературе приводятся аналогии между распределением электронной плотности
в N-оксиде пиридина и фенолят ионе: [9,
с.33]

Тем не менее, для оксидов пиридинов, электрофильное замещение протекает в
достаточно жестких условиях. При протонировании N-оксида по кислороду электрофильное замещение приемущественно
протекает по положению 3 (за счет вклада предельных структур D и Е, приведенных на схеме (5). [9,
с.33]
Наличие электродонорных заместителей (в данном случае - гидроксигруппы в
положении 4-) также облегчает протекание процесса электрофильного замещения в
ароматическом кольце за счет повышения электронной плотности в π-системе. Гидрокси-группа не только
существенно облегчает электрофильное замещение, но и ориентирует его в орто- и
пара- положения по отношению к этим заместителям. [9, с.32] Получение
3,5-динитро-4-гидроксипиридин-N-оксида
из 4-оксипиридин-N-оксида
осуществляется посредством нитрования 4-гидроксипиридин-N-оксида смесью 100%-серной и дымящей
азотной кислот. Промежуточным продуктом реакции является
3-динитро-4-гидроксипиридин-N-оксид
с выходом 60%, а при дальнейшем нитровании превращающийся в
3,5-динитро-4-гидроксипиридин-N-оксид
с выходом 40%. [4, c.421]
На первой стадии нитрования образуется сопряженная кислота пиридона,
которая, являясь производным фенола, достаточно легко вступает в реакцию
электрофильного замещения. [10, c.268]

При дальнейшем нитровании образуется динитрозамещенное производное:

,5-динитро-4-гидроксипиридин
Полученное
вещество представляет собой желтые кристаллы с температурой плавления около
100-110 оС. [7] Таким образом, согласно изложенной выше методике возможно
получать 3,5-динитро-4-гидроксипиридиноксид с выходом (по всем сталиям),
порядка 0,4*0,4*0,8 = 0,128 (т.е. 10 - 15%).
2. Химические
свойства 3,5-динитро-4-гидроксипиридиноксида
На основе литературных данных, а также знаний из курса органической
химии, опишем химические свойства 3,5-динитро-4-гидроксипиридиноксида, исходя
из структуры данного соединения.
1) Таутомерия
,5-динитро-4-гидроксипиридиноксид, как и все оксипиридины склонен к
таутомерным превращениям (8). Причем в полярных растворителях (воде, спиртах)
преобладает 3,5-динитро-4-оксопиридон-N-оксид, а в неполярных - 3,5-динитро-4-гидроксипиридин-N-оксид. Кроме того, достаточно
высокие температуры плавления, свойственные всем оксипиридинам являются
следствием их амфотерного характера. Как видно из представленной ниже структуры
(9) биполярного иона, между различными молекулами
3,5-динитро-4-гидроксипиридиноксид возможно образование водородны связей типа
О-H-O: [4, c.409]

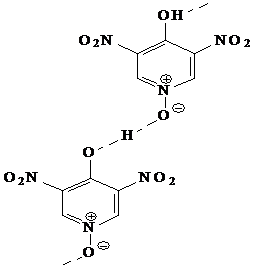
)
Кислотно-основные свойства
Как
уже было сказано в данной работе, 3,5-динитро-4-гидроксипиридиноксид является
амфотерным соединением.
Две
нитрогруппы, расположенные в положениях 3- и 5- являются акцепторными
заместителями, и смещают в свою сторону электронную плотность ароматического
кольца. Как известно из курса органической химии, при наличии в ароматическом
соединении одновременно нитро- и гидрокси групп, под воздействием нитрогруппы
возникает дефицит электронной плотности в ароматическом кольце, который
компенсируется за счет смещения электронной плотности с донорного атома
кислорода гидрокси-группы. Вследствие чего связь О-Н ослабевает и протон
становится более подвижным - усиливаются кислотные свойства соединения.
Основные
свойства 3,5-динитро-4-гидроксипиридиноксид проявляются за счет притяжения
протона атомом килорода, непосредственно связанным с пиридиновым азотом. На
схеме (10) указаны формы соединения в кислой и щелочной средах.
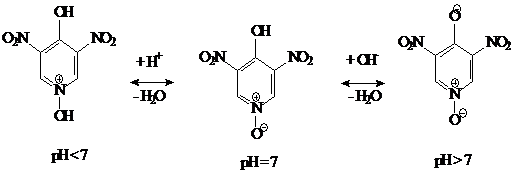
)
Реакции нуклеофильного замещения
Соединение
не вступает в реакции электрофильного замещения, так как является
электронодефицитным, однако реагирует с сильными нуклеофилами, находясь в
пиридоновой форме. К примеру, в результате реакции
3,5-динитро-4-гидроксипиридиноксида с оксохлоридом фосфора образуется
3,5-динитро-4-хлорпиридиноксид. [10, c.269] При дальнейшем протекании
реакции в избытке POCl3 возможно восстановление пиридинового атома азота за
счет внедрения атома галогена в ароматическую систему с образованием
3,5-динитро-4-хлорпиридиний хлорида. [5, c.25]

В
некоторых случаях, например при реакции с избытком хлористого сульфурила (SOCl2)
происходит также замещение нитрогрупп на атомы хлора с образованием
2,3,4,5-тетрахлорпиридинийхлорида. [5, c.25]

Возможно
протекание реакций гидроксиденитрования 3,5-динитро-4-гидроксипиридиноксида в
кислой среде (13), а в щелочной среде процесс сопровождается побочной реакцией
образования азосоединения (14). [5, c.25]


)
Окислительно-восстановительные свойства
,5-динитро-4-гидроксипиридиноксид
не проявляет ярко-выраженных окислительных и восстановительных свойств, однако
под воздействием сильных восстановителей 3,5-динитро-4-гидроксипиридиноксид
восстанавливается до 3,5-динитро-4-гидроксипиридина, а в избытке восстановителя
и в соответствующих условиях нитрогруппы восстанавливаются до аминогрупп (15).
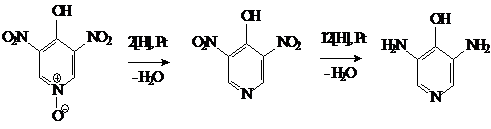
,5-динитро-4-гидроксипиридин
3,5-диамино-4-гидроксипиридин
В
заключение отметим, что на основе анализа данных литературных источников в
данной работе нами была составлена наиболее рациональная схема синтеза
3,5-динитро-4-гидроксипиридиноксида, а также рассмотрены важнейшие химические
свойства данного соединения. Таким образом, задачи, поставленные перед данной
работой, можно считать выполненными.
Список
использованной литературы
1. Аксельрод
Ж.И., Березовский В.М. Электрофильное замещение в ряду шестичленных азотсодержащих
гетероароматических соединений и их N-окисей. // Успехи химии, т. 39, №7, М.,
1970. - С. 1337 - 1353.
. Гауптман
З., Грефе Ю., Ремане Х. Органическая химия, М.: "Химия", 1979. -
832с.
. Эльдерфилд
Р. (ред.) Гетероциклические соединения. Т.1. Перевод с англ. под ред. Ю. К.
Юрьева. М.: Изд-во иностранной литературы, 1953. - 556 с.
. Бартон
Д., Оллис У.Д. Общая органическая химия. Том 8. Азотсодержащие гетероциклы. М.:
Химия, 1985. - 752 с.
6. Shaker
Y. Recent trends in the chemistry of pyridine N-oxide // ARKIVOC Volume part I,
2001. P. 242 - 268.
. Albini,
A, Pietra, S. Heterocyclic N-oxides // CRC Press: Boca Ration. 1991. - P. 263.
. Katritzky
A.R., Lam J.N. Heterocyclic N-oxides and N-imides. Heterocyclicles, 33, 1992. -
P. 1011 - 1023.
9. Юровская
М.А., Куркин А.В., Лукашёв Н.В. Химия ароматических гетероциклических
соединений. М.: Издательство МГУ им. Ломоносова, 2007. - 50 стр.
. Иванский
В.И. Химия гетероциклических соединений. М.: Высшая школа, 1978. - 559 с.