Инфекционный процесс
ВСТУПЛЕНИЕ
Проникновение микроорганизмов во внутреннюю
среду организма человека приводит к нарушению гомеостаза организма, которое
может проявиться комплексом физиологических (адаптационных) и патологических
реакций, известных как инфекционный процесс, или инфекция. Спектр этих реакций
достаточно широк, его крайние полюсы - клинически выраженные поражения и
бессимптомная циркуляция.
Термин «инфекция» (от лат. inficio - вносить
что-либо вредное и позднелат. infectio - заражение) может определять и сам
инфекционный агент, и факт его попадания в организм, но более правильно
использовать этот термин для обозначения всей совокупности реакций между
возбудителем и хозяином.
По выражению И.И. Мечникова, «...инфекция есть
борьба между двумя организмами». Вирусолог В.Д. Соловьёв рассматривал
инфекционный процесс как «особого рода экологический взрыв с резким усилением
межвидовой борьбы между организмом-хозяином и внедрившимися в него патогенными
бактериями». Известные инфекционисты А.Ф. Билибин и Т.П. Руднев (1962) определяли
его как сложный комплекс «физиологических защитных и патологических реакций,
возникающих в определённых условиях внешней среды в ответ на воздействие
патогенных микробов».
Современное научное определение инфекционного
процесса дано В.И. Покровским: «Инфекционный процесс - это комплекс взаимных
приспособительных реакций в ответ на внедрение и размножение патогенного
микроорганизма в макроорганизме, направленных на восстановление нарушенного
гомеостаза и биологического равновесия с окружающей средой».
Таким образом, участники инфекционного процесса
- микроорганизм-возбудитель заболевания, организм хозяина (человека или
животного) и определённые, в том числе социальные, условия внешней среды.
Микроорганизм представляет непосредственную
причину инфекционного заболевания, определяет специфичность его клинических
проявлений, влияет на течение и исход болезни. Его основные специфические
качества - патогенность, вирулентность, токсигенность, адгезивность и
инвазивность.
1. ПАТОГЕННОСТЬ МИКРООРГАНИЗМОВ
Человек контактирует с множеством
микроорганизмов, но лишь немногие из них способны вызывать инфекционные
болезни.
Патогенность - способность возбудителя проникать
в организм человека или животного, жить и размножаться в нём, вызывая
морфологические и функциональные нарушения в органах и тканях макроорганизма,
проявляющиеся как инфекционное заболевание. [1] Патогенность или отсутствие
таковой - видовой, генетически детерминированный признак микроорганизма.
Патогенный потенциал многих возбудителей зависит как от свойств, присущих
конкретному микроорганизму, так и от состояния факторов защиты организма -
хозяина. В зависимости от характера данных взаимоотношений все микроорганизмы
разделяют на патогенные, условно-патогенные и непатогенные.[2]
В соответствии с 9-м изданием «Определителя
бактерий» Берджи, патогенные и условно-патогенные для человека бактерии
относятся к эубактериям трех категорий:- грамотрицательные;-
грамположительные;- лишенные клеточной стенки (микоплазмы).
Эти бактерии входят в 14 из 35 известных групп
бактерий.[3] (табл 1)
Подразделение микроорганизмов на непатогенные и
условно патогенные виды имеет нечеткие границы. Более правильная оценка
паразитических свойств микроорганизма, так как в основе любого инфекционного
процесса лежит феномен паразитизма.[4]
Таблица 1. Патогенные и условно-патогенные для
человека бактерии
|
Группа
|
Категория
|
Группа
(категория) бактерий
|
Таксоны
|
|
1
2 4 5
|
I I I I
|
Спирохеты
Аэробные и микроаэро- фильные подвижные спиральные и изогнутые грамотрицательные
бактерии Грамотрицательные аэробные и микроаэро- фильные палочки и кокки
Факультативно-анаэробные грамотрицательные палочки: 1) семейства
энтеробактерий 2) вибрионов 3) пастерелл 4) не отнесенные к ним роды
|
Роды
Trеpоnema,
Borrelia, Leptospira Роды Сampylobacter,
Helicobacter, Spirillum, Wolinella Роды
Achromobacter, Acinetobacter,Agobacterium, Afipia, Alcaligenes, Bacteroides(виды
B.gracilis и
B. urealyticus) Bordetella, Brucella*, Burkhoderia*, Flaviomonas,
Flavobacterium, Francisella*,Kingella, Legionella*, Moraxella, Morococcus,
Neisseria, Pseudomonas, Stenotrophomonas 1) роды Cedecea, Citrobacter,
Edwardsiella, Enterobacter, Escherichia, Ewingella, Hafnia, Klebsiella,
Kluyvera, Leclercia, Morganella, Pantoae, Proteus, Providencia, Salmonella,
Serratia, Shigella, Tatumella, Yersinia*; 2) роды Aeromonas, Plesiomonas,
Vibrio* 3) роды Actinobacillus, Haemophilus, Pasteurella 4) роды
Calymmobacterium, Capnocytophaga, Cardiobacterium, Chromobacterium,
Eikenella, Gardnerella, Streptobacillus
|
|
6
8 9 17 18 19 20
|
I I I I II II II
|
Грамотрицательные
анаэробные прямые, изогнутые и спиральные бактерии Анаэробные
грамотрицательные кокки Риккетсии и хламидии: 1) семейства риккетсий 2)
бартонелл 3) хламидий Грамположительные Кокки Спорообразующие
грамположительные палочки и кокки Не образующие спор грамположительные
палочки правильной формы Не образующие спор грамположительные палочки
неправильной формы
|
Роды
Anaerobiospirrilum, Anaerorhabdus, Bacteroides, Bilophila, Eusobacterium, Porphyromonas, Prevotella Род Veillonella 1) роды Coxiella*, Ehrlichia, Rickettsia* 2) род Bartonlla 3) род Chlamydia, Chlamydophila
Роды
Alloiococcus, Enterococcus, Gemella, Leuconostoc, Peptococcus,
Peptostreptococcus, Planococcus, Staphylococcus, Stomatococcus, Streptococcus
Роды
Bacillus*, Clostridium Роды
Erysipelothrix, Listeria Роды
Actinomyces, Arcanobacterium, Bifidobacterium, Corynebacterium, Eubacterium,
Gardnerella, Lactobacillus, Mobiluncus, Propionibacterium, Rothia
|
|
21
22,
25, 26 30
|
II III III
|
Микобактерии
Актиномицеты
Микоплазмы
|
Род
Mycobacterium Роды Actinomadura, Gordona, Nocardia, Oerskovia, Rhodococcus,
Streptomyces, Tsukamurella Роды Mycoplasma, Ureaplasma
|
Примечание. Подчеркнуты роды, содержащие один
или несколько безусловно - патогенных видов (вариантов); * отмечены роды, в
состав которых входит один или несколько возбудителей особо опасных инфекций.
Микроорганизмы, населяющие человека или
животное, находятся с ним в различных симбиотических отношениях - от взаимовыгодных
(мутуализм) до антагонистических (паразитизм). Е.Н. Павловский определил
паразитизм как форму отношений между организмами разных видов, из которых один
(паразит) использует другого (хозяина) в качестве источника пищи и постоянного
или временного места обитания. В жизненном цикле паразитов обязательны две
фазы: пребывание (размножение) в организме хозяина и смена хозяина. Без второй
фазы невозможно существование паразитов, как биологических видов, поскольку
жизнь индивидуального хозяина всегда ограничена. Паразиты обладают генетической
информацией и соответствующими системами питания и защиты, позволяющими им
использовать организмы других видов (хозяев) и уклоняться от их защитных
механизмов. Паразитический образ жизни характерен для патогенных вирусов,
микроорганизмов, простейших, гельминтов, грибов, членистоногих.
Организм хозяина тоже содержит генетическую
информацию, дающую ему возможность регулировать свои отношения с
паразитирующими видами микроорганизмов.
По типу паразитизма возбудителей инфекционных
болезней можно разделить на три группы.
• Облигатные паразиты. Единственной средой их
обитания всегда служит определённый хозяин. Поэтому, независимо от путей
передачи, такие возбудители отличаются наиболее выраженной зависимостью от
хозяев.
• Факультативные паразиты, помимо организма
хозяина, могут циркулировать и во внешней среде.
• Случайные паразиты - возбудители типичных
сапронозов. Для них внешняя среда (почва, вода, растительные и другие
органические субстраты) служит нормальной и наиболее обычной средой
обитания.[2]
1.1
Патогенность
и вирулентность
Термин «патогенность» означает способность
микроорганизмов вызывать заболевания. Он состоит из двух греческих слов: раthos
- страдание, болезнь, и genos -рождающий. [3] Патогенными, т. е. болезнетворными,
являются далеко не все бактерии. Поэтому закономерным является вопрос, как они
возникли или чем определяется их патогенность. Однозначного ответа на него дать
невозможно, так как патогенность разных бактерий определяется их особыми
свойствами. Одним из объяснений происхождения патогенных бактерий служит
допущение того факта, что их появление связано с приспособлением к
паразитическому существованию и приобретением в связи с этим таких
биологических свойств, которые обеспечивают им способность противостоять
защитным механизмам макроорганизма. [6] Как уже отмечалось ранее, между микро-
и макроорганизмом существуют различные формы симбиоза: мутуализм, комменсализм
и паразитизм. Переход от комменсализма к паразитизму вполне логичен. Это
положение подтверждает наличие в природе так называемых микробов-двойников.
Например, есть микобактерии, патогенные для человека и теплокровных животных,
патогенные для холоднокровных и растений, и микобактерии непатогенные
(например, Мусоbacterium smegmatis - представитель микрофлоры слизистой
оболочки мочеполовых путей человека). [7]Вероятнее всего предположение, что
патогенные микобактерии обособились в разные группы в результате адаптации к
паразитизму за счет соответствующих организмов. Вместе с тем возбудители таких
заболеваний, как ботулизм и столбняк, постоянно существуют во внешней среде:
естественной средой обитания для них служит почва. Их патогенность для человека
и теплокровных животных связана со способностью вырабатывать сильнейшие
токсины. Однако не ясно, какую роль токсинообразование играет в жизни и
экологии этих бактерий. [8]
Другой механизм превращения непатогенных
бактерий в патогенные связан с получением первыми дополнительных генов от
бактериофагов либо плазмид.[9] Например, дифтерию у человека вызывают только
патогенные Corinebacterium diphtheriae, а способность синтезировать дифтерийный
экзотоксин они приобретают в результате лизогенной конверсии. Иначе говоря,
болезнетворность этих бактерий зависит от передачи им генов токсигенности от
особых токсигенных коринефагов. Интегрируясь в хромосому непатогенных
коринебактерий, такие фаги привносят в них свои гены, которые и превращают
непатогенные коринебактерий в возбудители дифтерии.[8]
В свою очередь, многие варианты диареегенных
кишечных палочек возникли в результате приобретения ими плазмид, в составе
которых имеются гены, превращающие непатогенную Е. Coli в патогенную, способную
вызывать различные формы эшерихиозов.[2]
Наконец, в природе существуют различные виды
бактерий, способных с помощью сенсорно-регуляторных систем перестраивать свой
метаболизм в зависимости от того, в каких условиях они существуют - во внешней
среде или в организме теплокровных животных. Эти бактерии (легионеллы, иерсинии
и др.) получили название сапронозных, так как естественной средой их обитания
являются почва и растительные организмы. Однако, попадая в организм человека
или животных, они изменяют свой метаболизм в сторону, способствующую их
размножению и в этих условиях, т. е. при более высокой температуре в живом
организме с его механизмами самозащиты.[10]
Патогенность, или способность вызывать
заболевание, не является абсолютной. Ее обусловленность находит свое выражение
в следующих фактах:
. Патогенность микробов проявляется
всегда по отношению к определенному виду (видам) животных. Есть бактерии,
патогенные только для человека, есть патогенные только для животных, но есть
патогенные и для человека, и для животных (возбудители чумы, бруцеллеза,
туляремии и др.).
. Непатогенный в одних условиях
(естественных) для макроорганизма возбудитель может стать патогенным в других,
измененных условиях. Например, в естественных условиях куры не болеют сибирской
язвой, но если температуру их тела искусственно понизить, они ею заболевают.
. Микроорганизмы, являющиеся
непатогенными или условно-патогенными для физиологически здоровых организмов,
могут стать патогенными при ослаблении их естественной резистентности, особенно
под влиянием радиационного облучения. [11]
Патогенность - способность вызывать заболевание
- видовое свойство бактерий, присущее виду в целом, но она может проявляться в
разной степени у разных представителей данного вида. Поэтому для оценки степени
патогенности используют термин вирулентность. [9]
Патогенность и вирулентность (лат. virulentus -
ядовитый) означают одно и то же - способность вызывать заболевание, но под
вирулентностью понимают количественную оценку, т. е. меру, степень
патогенности. [3] Вирулентность может быть как усилена (повышена), так и
ослаблена (понижена), как in
vitro, так и in
vivo. [4] При
максимальном снижении вирулентности патогенные микроорганизмы могут стать
авирулентными, т. е. невирулентными, но вирулентные микроорганизмы - всегда
патогенны. [12] Это
достигается разными способами воздействия на соответствующего возбудителя. Но
так как все признаки патогенности контролируются генами, то фактически
получение авирулентных или высоковирулентных штаммов возбудителей сводится к
селекции таких вариантов, всегда имеющихся в каждой популяции, т. е. к созданию
благоприятных для их отбора условий. Со времен Пастера искусственное снижение
вирулентности - аттенуация - положено в основу производства ряда вакцин.
Таким образом, патогенность - качественный
признак патогенного микроба, а вирулентность - количественное проявление
патогенности.
1.2
Определение вирулентности микроорганизмов
При изучении свойств микроорганизмов в ряде
случаев определяют их вирулентность (степень патогенности). Это необходимо для
характеристики возбудителей инфекций, выделенных от больных, микробоносителей и
из внешней среды, установления остаточной вирулентности живых вакцин, выявления
напряженности иммунитета у животных и т.д. [11]
Вирулентность выражают количественно: в величине
летальной или инфицирующей дозы, индексах адгезии, инвазии, цитотоксичности и
других показателях степени болезнетворности изучаемого штамма. Например, Dlm
(dosis letalis minima, минимальная летальная доза) - минимальное количество
микроорганизмов, вызывающее гибель 95 % животных определенного вида в группе, LD50
(половинная летальная доза) - количество микроорганизмов, вызывающее гибель 50
% зараженных животных в группе. LD50 является более достоверным показателем
вирулентности, так как в меньшей степени зависит от индивидуальной
чувствительности животных. [13]
При определении LD50 вид, пол, вес животных,
условия содержания, кормления должны быть строго стандартизованными. Из
культуры бактерий, вирусов или токсина делают 10-кратные разведения, каждое из
которых вводят не менее чем 4-6 животным. Через определенный срок отмечают
количество погибших животных в каждой группе и вычисляют LD50 .Для вычисления
LD50 существует несколько методов: Рида и Менча, Блисса (метод пробитов),
Кербера в модификации И. П. Ашмарина и др. [12]
В настоящее время для определения вирулентности
стараются не использовать лабораторных животных (в связи с высокой стоимостью
исследования и по этическим соображениям). С этой целью широко применяются
другие методы определения вирулентности: заражение культур тканей, куриных
эмбрионов, культур простейших, а также выявление отдельных факторов патогенности
или их генетических детерминант. [14]
Для выявления таких важных свойств возбудителя,
как адгезивность, инвазивность, цитотоксичность, испытуемой культурой
микроорганизма в строго определенном количественном соотношении заражают
монослой стандартной культуры ткани (HeLa, Нер-2, Vero и др.). Через
определенные периоды (2, 5, 24 ч) контакта при оптимальных условиях для роста
культуры ткани культуральную жидкость выливают, монослой отмывают от
несвязавшихся с ним микробных частиц, фиксируют, окрашивают и микроскопируют.
При этом просматривают 200 - 300 клеток монослоя и отмечают их состояние
(выявляют признаки цитопатического действия), подсчитывают количество внутри-
и/или внеклеточно расположенных (адгезированных) микроорганизмов и вычисляют
соответствующие индексы: индекс адгезии - среднее количество микробных клеток,
прилипших к одной эукариотической клетке, индекс цитотоксичности - доля (%)
клеток монослоя с признаками цитопатического действия и т.д. (рис.1.2).

Рисунок 1.2 - Определение вирулентности на
культуре ткани:в цитоплазме эукариотических клеток видны клетки инвазивных
Yersinia enterocolitica
В ряде случаев для определения вирулентности
достаточно обнаружить фенотипические признаки (маркеры вирулентности) у
выделенной культуры. Так, у энтеропатогенных иерсиний (возбудителей иерсиниоза
и псевдотуберкулеза) определяют кальций- зависимость роста при 37 °С (на
кальцийдефицитной среде), у возбудителей кишечных и мочевых эшерихиозов -
соответствующие адгезины (в реакции агглютинации) и т.д.
иммунный вирулентность микроорганизм патогенность
2. ФАКТОРЫ ПАТОГЕННОСТИ
Патогенность как биологический признак бактерий
реализуется через ряд последовательных процессов взаимодействия микробных
клеток с клетками и тканями макроорганизма. Это адгезия - способность
прикрепляться к клеткам; колонизация - способность размножаться на поверхности;
инвазия - способность проникать в клетки и подлежащие ткани; и образование
биологически активных продуктов, в том числе токсинов. [16]
2.1 Способность к
колонизации
Адгезия микроорганизмов к рецепторам
чувствительных клеток макроорганизма - это важнейший элемент их взаимодействия.
Бактерии могут размножаться либо в клетках, либо на поверхности клеток
слизистой (на их мембранах) либо проходить через них и далее распространяться
по организму. Поэтому ни один возбудитель, в том числе и вирусы, не может
реализовать свою патогенность, если он не способен прикрепиться к клетке
(адсорбироваться на ней). Если не произошло адгезии микроорганизмов, то обычно
они и не размножаются, а выводятся из организма. Поэтому адгезия и колонизация
- начальные, пусковые механизмы развития болезни. [17] Прикрепление к
поверхности клеток (например к эпителию слизистых оболочек) обеспечивает
адгезины, или факторы колонизации - различные микробные продукты - молекулы
адгезии (белки, ЛПС, липотейхоевые кислоты). Молекулы адгезии могут
располагаться непосредственно на поверхности бактериальной клетки либо входить
в состав микроворсинок или капсул.[18] Взаимодействие инфекционного агента с
эпителиальными клетками происходит в результате нескольких типов связей,
различных по природе и специфичности. Выделяют связи, основанные на
взаимодействии электростатических сил, обусловленные гидрофобными свойствами
поверхности, лиганд-рецепторные взаимодействия. [4]
Заряд. Бактериальные и эукариотические клетки
заряжены отрицательно, но поверхностные микроворсинки грамотрицательных
бактерий снижают заряд бактерий и уменьшают електростатические силы
отталкивания. [19]
Гидрофобность. Бескапсульные бактерии обладают
высокой гидрофобностью, усиливающей адгезивность; гидрофобные участки обладают
сродством к лигандам на поверхности эукариотческих клеток, что и приводит к
прочности связи. [7]
Специфические взаимодействия. На поверхности бактерий
имеются молекулы, способные к стереоспецифическому связыванию с
комплементарными молекулами на мембранах эукариотических клеток (например,
гемагглютинины или тейхоевые кислоты). [4]
Другие механизмы колонизации. Некоторые бактерии
способны «заранее подготавливать» место для дальнейшего размножения; например,
нейраминидаза облегчает проникновение холерного вибриона через слой слизи и
контакт с сиалосодержащими рецепторами эпителия кишечника. Микроорганизмы также
способны сорбироваться на бактериях, уже колонизировавших поверхность слизистых
оболочек, либо связывать белки, рецепторы к которому имеются на многих клетках
макроорганизма. У капсулированных бактерий в прикреплении активно участвуют
полисахариды капсулы. [20]
Для успешной колонизации очага первичного
инфицирования бактерии должны выдержать действие многочисленных и разнообразных
микробицидных факторов хозяина. Для защиты от них микроорганизмы активно
используют ряд структур (например, капсулы) и синтезируемых веществ (например
ферменты). [21]
Капсула (или слизистый слой) ингибирует
начальные этапы защитных реакций - распознавание и поглощение.
· Капсулы «экранируют» бактериальные структуры,
активирующие систему комплемента, с также структуры, распознаваемые
иммунокомпетентными клетками. Например, слой капсульного вещества защищает
тейхоевые кислоты стафилококков от связывания опсонинами.
· Гидрофильность капсул затрудняет их
поглощение фагоцитами, а само капсульное вещество защищает бактерию от действия
лизосомальных ферментов и токсичных оксидантов, выделяемых фагоцитирующими
клетками.
· Большое значение имеет лёгкая
отделяемость капсул или слизистого слоя от поверхности бактерий. В частности,
при поглощении капсулированных бактерий (например, синегнойной палочки),
последние легко «снимают с себя» капсулы и избегают прямого контакта с
фагоцитом.
Ингибирующие ферменты микробов как фактор
патогенности.
Микроорганизмы синтезируют различные ферменты,
обезвреживающие многие гуморальные защитные факторы. Например, многие
возбудители, особенно паразитирующие на слизистых оболочках, выделяют протеазы,
расщепляющие в том числе и молекулы IgA (иммуноглобулины А). В инактивировании
токсических кислородных продуктов фагоцитов задействованы каталаза и
супероксиддисмутаза. [9]
Бактериальные ферменты также способны изменять
рН окружающей среды, делая её пригодной для размножения. Например, Helicobacter
pylori выделяет уреазу, нейтрализующую кислую среду в желудке. [23]
.2 Инвазивность
Под инвазивностью понимают способность
возбудителей преодолевать защитные механизмы организма, размножаться, проникать
в его клетки и распространяться в нем. [17] Факторы инвазии у грамотрицательных
бактерий обычно представлены белками наружной мембраны.[1] Это свойство также
связано с наличием у патогенных микроорганизмов большой группы факторов
патогенности, которые наделяют их способностью к внедрению в клетки и
размножению в них; факторов, подавляющих фагоцитоз и препятствующих ему;
большой группы ферментов «агрессии и защиты». [2]
Факторы, препятствующие фагоцитозу, т. е. защищающие
от фагоцитоза. Они также связаны с компонентами клеточной стенки и либо
маскируют бактерии от фагоцитов, либо подавляют их активность. Такие факторы
есть у многих бактерий. Они представлены либо капсулой из гиалуроновой кислоты,
которая не распознается фагоцитами как чужеродная, так как химически не
отличается от таковой организма, либо капсулами другой химической природы (у В.
аnthracis, Y. pestis и т. д.); различными белками, тормозящими фагоцитоз, -
белок А (у стафилококков), М-белок (у стрептококков), антиген FraI у
возбудителя чумы; пленка из фибрина, образующаяся у стафилококков, имеющих
плазмокоагулазу; к их числу относятся также пептидогликан, тейхоевые кислоты и
другие компоненты клеточной стенки.[24]
Факторы, подавляющие фагоцитоз, например V-W-антигены
у Y. pestis. Наличие таких факторов обусловливает незавершенный характер
фагоцитоза. Чаще всего он связан с образованием бактериями веществ, которые
подавляют «окислительный взрыв» фагоцитов. Незавершенный фагоцитоз - одна из
важных причин хронизации течения болезни (хрониосепсис). [25]
Ферменты «защиты и агрессии» бактерий. Для
осуществления колонизаиии и инвазии многие бактерии выделяют ферменты агрессии
и защиты:
• нуклеазы;
• протеазы, действие которых в первую очередь
направлено на разрушение антител;
• лецитовителлаза - лецитиназа, разрушает
клеточные мембраны;
• плазмокоагулаза - способствует образованию
фибриновых барьеров;
• антифагин - липополисахарид, оказывающий
токсическое действие на фагоциты;
• фибринолизин - протеолитический фермент,
который растворяет сгустки фибрина;
• гиалуронидаза - фермент, гидролизующий
гиалуроновую кислоту - основной компонент соединительной ткани;
• нейраминидаза - отщепляет от различных
гликопротеидов, гликолипидов, полисахаридов сиаловую (нейраминовую) кислоту,
повышая проницаемость различных тканей. [17]
Три последних фермента облегчают распространение
микроорганизмов в тканях организма. С помощью таких ферментов, как
фибринолизин, лецитиназа, гиалуронидаза, протеазы и т. п., бактерии реализуют
(наряду с факторами, подавляющими фагоцитоз и защищающими от него) свои
агрессивные свойства. Эти ферменты способствуют их распространению в тканях
организма. Одним из главных ферментов защиты (например, у стафилококков)
является плазмокоагулаза. Превращая фибриноген в фибрин, этот фермент образует
своеобразную белковую пленку вокруг клеток, которая и защищает их от
фагоцитоза. [26]
Так, одним из важнейших механизмов сохранения
возбудителя в организме хозяина является микробная персистенция, заключающаяся
в образовании атипичных бесстеночных форм микроорганизма - L-форм, или
фильтрующихся форм. При этом наблюдается резкая перестройка обменных процессов,
выражающаяся в замедлении или полной потере ферментативных функций,
неспособности расти на элективных питательных средах для исходных клеточных
структур, утрате чувствительности к антибиотикам.[1]
2.3 Токсигенность
Кроме ферментов агрессии и защиты,
микроорганизмы, размножаясь, могут вырабатывать биологически активные вещества,
повреждающие клетки и ткани макроорганизма - токсины. Токсины (от греч. toxikon,
яд) - важнейшие факторы патогенности, вырабатываемые микроорганизмами и
реализующие основные механизмы инфекционного процесса. Роль микробных токсинов
впервые доказали Э. Ру и А. Иерсен(1888), отделившие «ядовитое начало»
возбудителя дифтерии от бактериальных клеток и сумевшие воспроизвести с его
помощью клиническую картину болезни морских свинок. [1]
Токсины облегчают первичную колонизацию и
вызывают системные поражения, характеризующие специфические проявления той или
иной инфекционной болезни.[28] Некоторые токсины не ведут к развитию
клинической картины, но вносят вклад в патогенез заболевания (так называемые
парциальные токсины). Спектр активности токсинов необычайно широк: от веществ,
облегчающих распространение по тканям, до метаболитов, селективно повреждающих
активность определённых клеток. [29] Бактериальные токсины традиционно
подразделяют на эндотоксины и экзотоксины, хотя подобная классификация не
совсем корректна. Эндотоксины имеются только у грамотрицательных бактерий.
Особенность эндотоксинов в том, что они термостабильны и высвобождаются из
бактериальных клеток после их разрушения. Эндотоксины, в отличие от
экзотоксинов, не обладают специфичностью действия. [16]
Бактериальные эндотоксины - структурные компоненты
внешней мембраны практически всех грамотрицательных микроорганизмов,
биохимически представляющие собой липополисахаридный комплекс (ЛПС-комплекс).
[2] Структурно-функциональный анализ молекулы ЛПС-комплекса показал, что
биологически активным сайтом (участком), определяющим все основные свойства
нативного препарата ЛПС-комплекса, служит липид А. Ему присуща выраженная
гетерогенность, что позволяет защитным силам организма его распознать. Действие
эндотоксинов малоспецифично, что проявляется сходными клиническими признаками
болезни. Их токсичность и пирогенность обусловлены липидом А, входящим в состав
ЛПС и имеющим сходную структуру у разных грамотрицательных бактерий. [24]
Эндотоксины являются воспалительными агентами:
они увеличивают проницаемость капилляров и оказывают разрушающее действие на
клетки. Многообразие проявлений отравления эндотоксином обусловлено не только
самим ЛПС, но и высвобождением многочисленных биологически активных соединений,
синтез которых он индуцирует в организме человека и животных (гистамин,
серотонин, простагландины, лейкотриены и др., всего более 20). Эти вещества и
обусловливают нарушения в различных органах и тканях. [1]
Все три компонента ЛПС - липид А, ядро
полисахарида и его боковая цепочка из повторяющихся сахаров - обладают
выраженными антигенными свойствами. ЛПС стимулирует синтез интерферонов,
активизирует систему комплемента по классическому пути, оказывает митогенное
действие на лимфоциты, а также аллергенное действие. Его токсические свойства,
в отличие от экзотоксинов, не снимаются при обработке формалином, и ЛПС не
превращается в анатоксин. [2]
Экзотоксины. Их продуцируют как
грамположительные, так и грамотрицательные бактерии. У грамположительных
бактерий экзотоксины активно секретируются через ЦМ и клеточную стенку в
окружающую среду с использованием специальных секретирующих систем. У
грамотрицательных бактерий (холерный вибрион, токсигенные кишечные палочки,
сальмонеллы) некоторые экзотоксины (энтеротоксины) синтезируются только при
определенных условиях непосредственно в инфицированном организме и нередко
сохраняются в цитоплазме, освобождаясь из клетки только после ее разрушения.
[19]
Основные свойства экзотоксинов.
Все известные бактериальные экзотоксины - белки,
среди них есть термолабильные и термостабильные. С белковой природой
экзотоксинов связаны их основные свойства: они обладают высокой силой действия
(самые сильные токсины в природе - микробного происхождения), высокой
избирательностью и связанной с ней специфичностью действия (картина столбняка у
лабораторных животных одинакова, как при заражении их возбудителем, так и его
экзотоксином), которое они проявляют после некоторого латентного периода.[4]
Экзотоксины являются сильными антигенами, а некоторые - даже суперантигенами.
Они индуцируют образование в организме антител, т. е. антитоксинов, которые
нейтрализуют их действие.[9] При обработке формалином экзотоксины
обезвреживаются и превращаются в анатоксины. Анатоксины лишены токсических
свойств, но сохраняют свою способность индуцировать синтез антитоксинов,
поэтому широко используются для создания искусственного иммунитета против
дифтерии, столбняка, ботулизма и других заболеваний.[12]
Организация и механизм действия токсической
молекулы.
Большинство токсинов представляют собой А-В
структуру. Эта структура предполагает наличие двух компонентов - В-субъединицы,
которая участвует в связывании токсина с рецептором на поверхности клетки
хозяина и способствует транспортировке токсина в клетку хозяина; и
А-субъединицы - проявляющей энзиматическую (токсическую) активность в клетке
хозяина. Структура В-доменов зависит от структуры рецепторов-мишеней, с
которыми взаимодействует токсин. А-субъединицы более консервативны чем В,
особенно в участках, критических для их ферментативной активности [30].
По механизму действия подразделяют все токсины
на 5 типов (табл.2).
Таблица 2.3 Характеристика бактериальных
токсинов
|
Микроорганизм
Токсин
|
Механизм
действия
|
Мишень
|
Болезнь
|
Участие
токсина в болезни
|
LD50
на кг
|
|
Повреждающие
мембраны
|
|
Aeromonas
hydrophila / Аэролизин
|
Пороформи-рующий
|
Гликопротеин
|
Диарея
|
(да)
|
~7мкг
(м)
|
|
Clostridium
perfringens / Перфринголизин O
|
То
же
|
Xолестерин
|
Газовая
гангрена
|
?
|
|
|
Escherichia
coli / Гемолизинd
|
То
же
|
Плазматичес-кая
мембрана
|
Инфекция
уринарного тракта
|
(да)
|
-
|
|
Listeria
monocytogenes /Листериолизин О
|
то
же
|
Xолестерин
|
Ситемные
пищевые инфекции, менингиты
|
(да)
|
3…12
мкг (м)
|
|
Staphylococcus
aureus / альфа-токсин
|
То
же
|
Плазматичес-кая
мембрана
|
Абсцессыс
|
(да)
|
40…60
нг (м)
|
|
Staphylococcus
pneumoniae Пневмолизин
|
То
же
|
Xолестерин
|
Пневмонияс
|
(да)
|
~1.5
мкг (к)
|
|
Streptococcus
pyogenes Стрептолизин О
|
То
же
|
Xолестерин
|
Стрептококовая
ангина, скарлатинас
|
?
|
8
мкг (м) 1…2 мкг (к)
|
|
Ингибиторы
Белкового синтеза
|
|
orynebacterium
diphtheriae / Дифтерийный токсин
|
АDФ-рибозил-трансфереза
|
Фактор
элонгации-2
|
Дифтерия
|
Да
|
~1.6
мкг (м) £100 нг (ч)
|
|
E.
coli / Shigella dysenteriae /Шига-токсин
|
N-гликозидаза
|
28SpPHK
|
Геморрагический
колит, гемолитический уремический синдром
|
Да
|
-
|
|
Pseudomonas
aeruginosa Экзотоксин А
|
ADФ-рибозилтранс-фераза
|
Фактор
элонгации-2
|
Пневмо-нияe
|
(Да)
|
~3
мкг (м)
|
|
Активация
путей вторичных мессенджеров
|
|
E.
coli: Цитотоксический никротизирующий фактор
|
Деамидаза
|
Rho-G-белок
|
Инфекция
уринарного тракта
|
?
|
-
|
|
Термолабильный
токсин
|
АДФ-рибозилтранс-фераза
|
G-белки
|
Диарея
|
Да
|
-
|
|
Температурно
стабильный токсин d
|
Стимуляция
гуанилатциклазы
|
Гуанилатциклазный
рецептор
|
Тоже
|
Да
|
-
|
|
Цитолетальный
растягивающий токсин d
|
Блокирование
G2
|
Неизвестна
|
Тоже
|
(Да)
|
-
|
|
EAST
|
Стимуляция
гуанилатциклазы
|
Неизвестна
|
Тоже
|
?
|
-
|
|
Bacillus
nthracis/ Отечный фактор
|
Аденилатцик-лаза
|
АТФ
|
Сибирская
язва
|
Да
|
-
|
|
Bordetella
pertussis / rоклюшный токсин
|
АДФ-рибозилтрансфераза
|
G-белки
|
Коклюш
|
Да
|
21
мкг (м)
|
|
Дермонекротический
токсин
|
Деамидаза
|
Rho
G-белки
|
Риниты
|
(Да)
|
-
|
|
Clostridium
botulinum C2-токсин
|
АДФ-рибозилтрансфераза
|
Мономер-ный
G-актин
|
Ботулизм
|
?
|
-
|
|
C.botulinim
/ C3 токсин
|
Тоже
|
RhoG-белок
|
Ботулизм
|
?
|
-
|
|
Clostridium
difficile Токсин А
|
Гликозилтранс-фераза
|
RhoG-белок
(и)
|
Диарея
/ PC
|
(Да)
|
-
|
|
Токсин
В
|
Тоже
|
Тоже
|
Тоже
|
?
|
-
|
|
Vibrio
cholerae Холерный токсин
|
АДФ-рибозилтрансфераза
|
G-белок
(и)
|
Холера
|
Да
|
~250
мкг (м)
|
|
Активаторы
иммунного ответа
|
|
S.aureus/
Энтеротоксины
|
Суперантиген
|
TCR
и MHC II
|
Пищевое
отравление с
|
Да
|
20…50
мкг (о)
|
|
Эксфолиативный
токсин
|
Суперантиген
(и сериновая протеаза)
|
То
же
|
Синдром
шелушения кожи
|
Да
|
-
|
|
S.pyogenes/
Пирогенный экзотоксин
|
Тоже
|
То
же
|
Скарлатина
синдром токсического шокаc
|
Да
|
3…6
мг (м)
|
|
Токсин
синдрома токсического шока
|
Суперантиген
|
То
же
|
Синдром
токсического шокаe
|
Да
|
-
|
|
Протеазы
|
|
B.anthracis
/ Летальный фактор
|
Металлопротеа-за
|
MAPKK1/MAPKK2
|
Сибирская
язва
|
Да
|
<114
мкг (м)
|
|
C.botulinum
Нейротоксины А-С
|
Цинк-металлопротеазы
|
VAMP
синаптобревин, SNAP-25, синтаксин
|
Ботулизм
|
Да
|
0.5…1.2
нг (м)
|
|
Clostridium
tetani Столбнячный токсин
|
Тоже
|
VAMP
синаптобревин
|
Столбняк
|
Да
|
~1
нг (м)
|
|
|
|
|
|
|
|
|
СОКРАЩЕНИЯ: EAST - энтероаггрегативный
температуростабильный токсин E.coli; TCR - рецептор Т-клеток; МНС II - главный
комплекс гистосовместимости, класс 2; МАРКК - митоген активированная протеин
киназа киназа; VAMP - везикуло-ассоциированный мембранный белок; SNAP-25 -
синаптосомал-ассоциированный белок; PC - антибиотикоассоциированные
псевдомембранозные колиты; Да - строго доказанная связь между токсином и
болезнью; (Да) - роль в патогенезе была показана на животных моделях или
клеточных культурах; ? - неизвестно; с - другие болезни также ассоциированы с этим
организмом; d - токсин также продуцируется другими семействами бактерий; (м) -
мышь; (к) - кролик; (ч) - человек; (о) - обезьяны
Порообразующие токсины. К ним относят
бактериальные токсины, функционирующие посредством вставки в плазматическую
мембрану хозяина и формирующие в ней трансмембранные поры, приводящие клетку к
лизису. Такие токсины еще называют RTX-семейством
из-за наличия в их молекулах большого количества повторов. [30] Механизм их
действия хорошо прослеживается на примере альфа-токсина S.aureus,
рассматриваемого как прототип олигомеризующегося пороформирующегося
цитотоксина. [31] Альфа-токсин является цитолитическим в отношении различных
типов клеток. У человека он способен лизировать моноциты, клетки, но точная его
роль в стафилококковом заболевании людей, неизвестна [32].
Токсины, ингибирующие синтез белка. Субстратами
для этих токсинов служат факторы элонгации и рибосомальная РНК. [9] Дифтерийный
токсин и экзотоксин А псевдомонад являются дифтамид специфическими
АДФ-рибозилтрансферазами, которые рибозилируют фактор элонгации 2 и, таким
образом, инактивируя его, подавляют синтез белка в клетках. Шига-токсин (Stx-токсин),
так же называемый веротоксином, продуцируется S.
disenteriae первого серотипа и
недавно появившимися Stx-продуцирующими
штаммами E. coli
(STEC). [27]
Токсины, генерирующие образование вторичных
мессенджеров (посредников). Бактериальные токсины могут влиять на функцию
отдельных белков эукариотической клетки, не приводя ее к гибели. Для этого они
активируют так называемых вторичных посредников, которые способны в большой
степени усиливать и искажать клеточную реакцию на внеклеточные сигналы. [31]
Протеолитические токсины. Ботулинический и
столбнячный (оба цинк-металлоэндопротеазы), в опытах на животных обнаруживают
наименьшую из известных LD50.
Эти токсины дают различную клиническую картину поражений, несмотря на столь
значительное сходство в структуре, энзиматической активности и мишенях среди
клеток нервной системы, но при различающихся путях проникновения в
макроорганизм.[33] Например, ботулинический токсин проникает в организм
энтерально и вызывает вялые параличи периферических нервов. Столбнячный же
токсин, образуясь на поверхностях ран, колонизированных C.
tetani, приводит к
спастическим параличам через поражение ЦНС.[34]
Активаторы иммунного ответа. Отдельные
бактериальные токсины могут действовать непосредственно на Т-клетки и
антигенпрезентирующие клетки иммунной системы. Самое большое семейство токсинов
данного типа называют токсинами-суперантигенами (PTSAg).
Как правило, иммуностимулирующий потенциал таких
токсинов является следствием их способности связывать различные участки белков
главного комплекса гистосовместимости II
типа, экспрессированных на поверхности антигенпрезентирующих клеток и Vбета-элементы
на Т-клеточном рецепторе.[31] Токсины данного типа характерны для случайных и
факультативных паразитов.
Трехсоставные токсины. К ним мы относим
структуры типа A1-B-A2,
где В - это субъединица, участвующая в связывании токсина с рецептором, А1 - и
А2 - субъединицы, проявляющие различную энзиматическую (токсическую) активность
в клетке хозяина. Наиболее изученным токсином данного типа является
сибиреязвенный. [35]
Происхождение токсинов. С момента открытия Roux
и Yersin в 1888г. дифтерийного токсина, этот вопрос вызывает много споров. В
последние годы появилась возможность проведения тонких молекулярных сравнений
между структурами отдельных токсинов. Результаты этих сравнений оказались
неожиданными для ученых.[30] Токсины микроорганизмов из отдаленных семейств и
даже родов, занимающих различные экологические ниши и вызывающие совершенно не
похожие инфекционные болезни, оказались весьма сходными по механизму действия и
по критическим для проявления токсичности структурам (например, шигатоксин,
коклюшный и холерный токсины). Было обнаружено сходство между токсинами и
ферментами эукариотических клеток (например, отечный фактор B. anthracis и
аденилатциклаза человека). [29] По этим данным создается впечатление широкого
эволюционного родства токсинов между собой. Но, как заметил Ю. Вертиев , у
некоторых исследователей даже возникает мысль, что токсины возникли путем
захвата из эукариотической клетки генетического материала, кодирующего токсин.
Ю. Вертиев считает, что бактериальные токсины,
интерфероны, бактериоцины и гормоны обнаруживают сходство в отношении целого
ряда важных свойств. Эти вещества синтезируются одним типом клеток, в то время
как воздействуют на другие типы клеток: они действуют на клетки в чрезвычайно
низкой концентрации (10-11-10-14 м); обладают сходной молекулярной организацией
состоят как минимум из двух функционально и структурно различных белков:
энзиматического и рецепторного; имеют сходные звенья молекулярного механизма
действия (связывание с рецепторами, активация, транслокация внутрь клетки и
модификация клеточных мишеней); обладают сходной кинетикой биологического
эффекта одноударный эффект; и, наконец, все эти вещества токсичны. [27]
2.4 Генетический контроль синтеза факторов патогенности бактерий
У бактерий обнаружено два типа генов,
контролирующих синтез факторов патогенности: гены собственной хромосомы клетки
и гены, привнесенные в хромосому так называемыми мобильными генетическими
элементами. Эта вторая группа включает в себя умеренные конвертирующие фаги,
фаги-транспозоны, плазмиды и транспозоны. Мобильными их называют потому, что
они содержат собственные генетические компоненты, кодирующие транспозазу,
интегразу, а также сайт-специфические участки, которые взаимодействуют со
специфическими сайтами хромосомы клетки и обеспечивают интеграцию в нее.[20]
Включение генома (или части генома) профага
приводит к образованию в составе хромосомы бактерий островов патогенности
(англ. Pathogenicity
islands), которые содержат
ген или кассету генов, контролирующих продукцию основных факторов патогенности.
[2] Например, в
хромосоме холерного вибриона есть два острова патогенности. В одном из них
расположены гены умеренного профага СТХφ,
а в другом - фага VPIφ.
Как правило, гены патогенности, содержащиеся в островах патогенности,
регулируются координированно, т. е. функционируют как самостоятельный геном
патогенности в составе хромосомы клетки. В результате рекомбинации умеренных
фагов с хромосомой бактерий возникли многие патогенные бактерии (Vibrio
cholerae, Corinebacterium
diphtheriae, Clostridium
botulinum, ЕНЕС и др.), а в
результате переноса генов патогенности плазмидами - Bacillus
anthracis, Yersinia
pestis, ЕТЕС, ЕIЕС,
ЕРЕС и др. [6] Во всяком случае, острова патогенности в форме мобильных
генетических элементов обнаружены у многих видов патогенных бактерий, но их нет
у близкородственных непатогенных бактерий.[8]
3. ИНФЕКЦИОННЫЙ ПРОЦЕСС
Проникновение микроба в организм приводит к
развитию комплекса физиологических (адаптационных) и патологических реакций,
направленных на восстановление гомеостаза, известных как инфекционный процесс,
или инфекция.[36] Термин «инфекция» (от лат. infictio, вносить что-либо
вредное, позднелатинское infectio, заражение) может определять и сам
инфекционный агент, и факт его попадания в организм, но более правильно его
применять для обозначения всей совокупности реакций между возбудителем и
хозяином. Основное и наиболее важное проявление инфекционного процесса -
инфекционная болезнь - клинически проявляющиеся нарушения нормальной
жизнедеятельности человека вследствие морфологических и функциональных
повреждений, вызванных проникновением и размножением в его организме
возбудителя заболевания.[28]
3.1 Происхождение
инфекционных болезней
Эволюция возбудителей инфекционных поражений
человека проходила тремя основными путями.
• Представители 1-й группы «достались в
наследство» от обезьяноподобных предков.
• Микроорганизмы 2-й группы произошли от
непатогенных предшественников.
• Микроорганизмы 3-й группы были первичными
патогенами синантропных и диких животных, но эволюционно адаптировались к
обитанию в организме человека. [6]
Тем не менее, принято считать, что предки
большинства возбудителей заразных болезней человека - свободно живущие
сапрофитные виды. Доказательством этому служит тот факт, что большинство
патогенных микроорганизмов (исключая облигатных паразитов) частично сохранило
способность некоторое время жить и размножаться вне организма-хозяина.
3.2 Классификация
инфекционных болезней
Попытки создать рациональную классификацию
инфекционных болезней предпринимали давно, при этом широко использовали самые
разные подходы и классификационные признаки.
Впервые последовательно выдержанную
классификацию инфекционных болезней, основанную на едином признаке (локализации
возбудителя в организме), предложил Л.В. Громашевский. Он считал, что рациональная
классификация инфекционных болезней служит не только высшим обобщением
достижений науки, но и теоретическим ключом для планирования системы
эпидемиологического надзора за инфекционными болезнями вплоть до их
искоренения. В соответствии с основной локализацией в организме, определяющей
механизм передачи инфекции, все инфекционные болезни Л.В. Громашевский разделил
на четыре группы:
• кишечные инфекции;
• инфекции дыхательных путей;
• кровяные инфекции;
• инфекции наружных покровов. [32]
Вместе с тем для практических нужд
первоочередное значение имеют и такие не менее важные показатели, как
характеристика основных резервуаров возбудителей инфекции (человек, животное и
абиотическая среда) и закономерности передачи возбудителей людям от этих резервуаров.
На современном этапе развития эпидемиологической
науки наиболее рациональна классификация, предложенная Б.Л. Черкасским (1994).
Она отражает не только специфику резервуара возбудителей, но и особенности
передачи патогенных микроорганизмов человеку из этих резервуаров. Только
сочетание экологических и эпидемиологических признаков способно отразить
эпидемиологическую специфику каждой инфекционной (паразитарной) болезни.
3.3 Условия развития
инфекции
Патогенность - видовой признак. Таким образом,
всегда возможны внутривидовые вариации. Вероятность развития инфекционной
болезни в значительной степени определяют видовые свойства возбудителя,
количество возбудителя, пути и место проникновения в организм, скорость
размножения. [36]
Инфицирующая доза
При попадании в организм незначительного числа
патогенных микроорганизмов (что бывает наиболее часто) их обычно эффективно
элиминируют защитные факторы организма. Для развития заболевания необходимо,
чтобы патоген обладал достаточной вирулентностью, а его количество
(инфицирующая доза) превышало некоторый порог, определяемый в каждом конкретном
случае вирулентностью возбудителя и состоянием резистентности организма.[40] В
контексте патогенных свойств инфицирующую дозу можно рассматривать как
определённое количество микроорганизмов, обеспечивающее возможность адгезии,
колонизации и инвазии в ткани. [28]
Скорость размножения
На вероятность развития инфекционного процесса и
его тяжесть существенно влияет скорость размножения возбудителя. [17] Например,
чумная палочка настолько быстро размножается в организме, что иммунная система
практически не успевает ответить на её проникновение формированием защитных
реакций. [41]
Входные ворота инфекции
Место внедрения патогенного возбудителя в
организм человека называют входными воротами инфекции, от их локализации
нередко зависит клиническая картина заболевания.[18] Свойства микроорганизма и
пути его передачи обусловливают разнообразие входных ворот. Ими могут быть
кожные покровы (например, для возбудителей сыпного тифа, чумы, сибирской язвы,
малярии), слизистые оболочки дыхательных путей (в частности, для вируса гриппа
и менингококка), ЖКТ (например, для возбудителей брюшного тифа, дизентерии),
половых органов (для возбудителей сифилиса, ВИЧ-инфекции, гонореи). При
различных инфекционных болезнях могут быть одни (холера, грипп) или несколько
(бруцеллёз, туляремия, чума) входных ворот. [7]
3.4 Динамика
инфекционного процесса
При развитии инфекционного процесса можно
выделить несколько стадий.
• Проникновение инфекционного агента; его
адаптация к условиям внутренней среды организма и колонизация тканей, к которым
тропен микроорганизм.
• Образование продуктов жизнедеятельности
(токсины, ферменты), оказывающих повреждающее действие и приводящих к нарушению
гомеостаза организма.
• Распространение инфекционного агента из очага
проникновения. Наиболее часто микробы диссеминируют по лимфо- и/ или кровотоку.
[4]
Кровь здорового человека и животного стерильна,
так как она обладает сильным антимикробным свойством, обусловленным наличием в
ней системы комплемента и различных иммунокомпетентных клеток. Однако почти при
всех инфекционных процессах в крови появляются и циркулируют в течение
различного срока возбудитель заболевания или его токсин, а также образующиеся
при распаде возбудителя антигены. Выход возбудителя или его антигенов в большом
количестве в кровь, как правило, сопровождается лихорадкой, которая не только
служит сигналом попадания возбудителя в кровь, но и имеет защитное
значение.[42]
Для характеристики явлений, связанных с проникновением
в кровь возбудителя, его токсина и антигенов, введены следующие понятия:
антигенемия, бактериемия, вирусемия, сепсис, септикопиемия, септицемия,
токсемия, токсинемия.[2]
Антигенемия (антиген + греч. haima
- кровь) - циркуляция в крови чужеродных антигенов и аутоантигенов. При наличии
в крови антител к данному антигену формируются циркулирующие иммунные комплексы
- ЦИК (антиген + антитело), способствующие очищению организма от антигенов. С
помощью ЦИК антигены выводятся из организма. Выявляют антигены и ЦИК в крови с
помощью различных серологических реакций, например, при бруцеллезе - с помощью
реакции агрегат-гемагглютинации.
Бактериемия - наличие в циркулирующей крови
бактерий - возникает в результате проникновения возбудителя в кровь через
естественные барьеры макроорганизма, а также при трансмиссивных инфекциях после
укуса кровососущих членистоногих. [43] При заболеваниях, которые передаются
членистоногими (сыпной тиф, возвратный тиф, чума, туляремия, риккетсиозы и т.
д.), бактериемия - главная и обязательная стадия патогенеза болезни. Она
обеспечивает передачу возбудителя другому хозяину, т. е. сохраняет его как вид.
[44] Причиной бактериемии могут быть хирургические вмешательства, травмы,
лучевая болезнь, злокачественные опухоли, различные тяжелые формы заболеваний,
вызванные условно-патогенными бактериями, и т. п.[40] В отличие от сепсиса и
септикопиемии, бактерии в крови только циркулируют, но не размножаются. Таким
образом, бактериемия - симптом болезни и одна из ее стадий. Диагноз бактериемии
ставится путем выделения гемокультуры возбудителя или заражения кровью больного
лабораторного животного.[25]
Вирусемия - состояние организма, при котором в
его крови циркулируют вирусы.[40]
Сепсис, или гнилокровие (греч. sepsis
- гниение) - тяжелое генерализованное острое или хроническое лихорадочное
заболевание человека, обусловленное непрерывным или периодическим поступлением
в кровь возбудителя из очага гнойного воспаления. Для сепсиса характерно
несоответствие тяжелых общих расстройств местным изменениям и частое
образование новых очагов гнойного воспаления в различных тканях и органах. [42]
В отличие от бактериемии, при сепсисе из-за
снижения бактерицидных свойств крови возбудитель размножается в кровеносной и
лимфатической системах. [15]
Чаще всего сепсис является следствием
генерализации локализованных гнойных очагов. Наиболее частые его возбудители -
стафилококки, стрептококки, грамотрицательные бактерии из семейств Enterobacteriaceae
и Pseudomonadaceae,
менингококки, другие бактерии, в том числе условно и слабопатогенные, и
некоторые грибы. В зависимости от локализации первичного гнойного очага и места
входных ворот возбудителя различают пуэрперальный (послеродовый), отогенный,
одонтогенный, послеабортный, перитонеальный, раневой, ожоговый, пупочный, ротовой
(стоматогенный), уросепсис и другие формы болезни. Может наблюдаться сепсис
новорожденных (неонатальный сепсис), обусловленный инфицированием плода при
родах или в период внутриутробного развития. Кроме того, бывает сепсис
криптогенный, при котором первичный очаг гнойного воспаления остается
нераспознанным. [45]
Септикопиемия - форма сепсиса, при которой
наряду с интоксикацией организма происходит образование гнойных метастатических
очагов в различных тканях и органах, сочетающееся с присутствием и размножением
возбудителя в лимфатической и кровеносной системах. [25]
Септицемия - форма сепсиса, при которой не
происходит образования метастатических очагов гнойного воспаления, а
единственным местом обитания и размножения возбудителя в организме служат его
кровеносная и лимфатическая системы. [2]
Токсемия - состояние организма человека или
животного, при котором в его крови циркулируют бактериальные эндотоксины.
Наблюдается при тяжелых формах заболеваний, вызванных грамотрицательными
бактериями, имеющими эндотоксин (ЛПС), например при сальмонеллезах,
эшерихиозах, менингококковых и иных инфекциях. Нередко сочетается с
бактериемией и сепсисом. [11]
Токсинемия - состояние организма, при котором в
кровеносной системе циркулирует бактериальный экзотоксин или другой токсин.
Возбудитель при этом в крови, как правило, отсутствует, а токсин через
кровеносную или нервную систему проникает в клетки-мишени. [2] Наблюдается при
заболеваниях, возбудители которых продуцируют экзотоксины (ботулизм, дифтерия,
столбняк, анаэробная инфекция и др.; поэтому эти болезни называют
токсинемическими). [46]
Отдельные виды патогенных микроорганизмов могут
поражать любые органы и ткани (возбудитель туберкулеза, патогенные стафилококки
и др.). В то же время есть возбудители, для которых характерна органотропность,
т. е. способность избирательно поражать определенные ткани. [36] Так,
возбудитель туберкулеза чаще всего поражает легочную ткань, гонококки -
слизистую уретры и конъюнктиву глаза, вирусы гепатитов - клетки печени, вирус
гриппа - слизистую верхних дыхательных путей и т.д. [23] Избирательностью
действия обладают и бактериальные экзотоксины. Органотропность возбудителей и
их токсинов определяется тремя обстоятельствами. Во-первых, наличием для
возбудителей и их экзотоксинов соответствующих рецепторов на мембранах клеток.
Во-вторых, особенностями метаболизма микроорганизмов, в соответствии с которыми
они находят оптимальные условия для размножения в определенных клетках (или на
определенных клетках). В-третьих, это зависит от наличия или отсутствия в
данной ткани антимикробных веществ типа лизоцима, ингибина, интерферона и
других, подавляющих размножение возбудителя. [2] Локализацией возбудителя в
организме определяются и пути его выделения - с испражнениями, мочой,
гнойно-воспалительным материалом, мокротой, слюной, слизью и т. п. Эти
выделения, а также кровь, спинномозговая жидкость, пунктат лимфоидной ткани и
служат чаще всего материалом для бактериологической диагностики инфекционных
заболеваний. [14]
Названные состояния могут сопровождаться
клиническими проявлениями либо протекать бессимптомно. Нередко микроорганизмы
циркулируют в кровотоке временно, проникая в кровь при чрезмерных физических
нагрузках и стрессовых ситуациях (длительной бессоннице, переохлаждении или
перегреве организма). Как правило, их циркуляция протекает бессимптомно или
субклинически, хотя в кровотоке практически здоровых пациентов могут
циркулировать Staphylococcus epidermidis, Clostridium perfringens и др. [4]
Формы инфекционного процесса могут быть
разнообразными; далеко не всегда инфекционный процесс проходит все стадии
своего развития, так как при попадании патогена в невосприимчивый (иммунный)
организм процесс заканчивается на начальных стадиях. [46]
3.5 Особенности
инфекционных болезней
Общепринятый термин «инфекционные болезни» ввёл
немецкий врач Кристоф Вильгельм Гуфеланд. Основные признаки инфекционных
болезней:
• наличие специфического возбудителя как
непосредственной причины заболевания;
• контагиозность (заразность) или возникновение
нескольких (многих) случаев заболеваний, обусловленных общим источником
инфекции (зоонозы, сапронозы);
• нередко склонность к широкому эпидемическому
распространению;
• цикличность течения (последовательная смена
периодов болезни);
• возможность развития обострений и рецидивов,
затяжных и хронических форм;
• развитие иммунных реакций к Аг (антиген)
возбудителя;
• возможность развития носительства возбудителя.
[7]
Специфичность. Каждую инфекционную болезнь
вызывает конкретный возбудитель. Специфическими возбудителями инфекционных
болезней могут быть бактерии, риккетсии, хламидии, микоплазмы, грибы, вирусы,
прионы. Однако известны инфекции (например, гнойно-воспалительные процессы),
вызываемые различными микробами. [3]
Контагиозность (заразность) большинства
инфекционных и паразитарных заболеваний связана с тем, что больной, выделяя
возбудитель во внешнюю среду, становится источником инфекции и представляет
опасность для окружающих здоровых лиц. В разные периоды заболевания степень
контагиозности инфекционного больного неоднозначна.[25] Например, больные
гриппом наиболее контагиозны в первые 3 дня болезни, больные брюшным тифом - в
периодах разгара заболевания и ранней реконвалесценции, когда выделение
брюшнотифозных палочек с испражнениями достигает максимума. [18] Степень
контагиозности зависит не только от периода инфекционной болезни, но также от свойств
самого возбудителя (например, заразность при гриппе в целом значительно выше,
чем при дизентерии) и путей его передачи. Чем выше контагиозность заболевания,
тем больше его склонность к широкому эпидемическому распространению. Болезни с
максимально выраженной контагиозностью, характеризующиеся тяжёлым течением и
высокой летальностью, объединены в группу особо опасных инфекций (чума,
натуральная оспа, холера, жёлтая лихорадка, лихорадки Ласса, Эбола, Марбурга). [41]
Цикличность течения свойственна большинству
инфекционных заболеваний. Она выражается в последовательной смене определённых
периодов болезни - инкубационного (скрытого), продромального (начального),
периода основных проявлений (разгара болезни), угасания симптомов (ранней
реконвалесценции) и выздоровления (реконвалесценции).
Инкубационный период - период от момента
заражения до появления первых признаков заболевания. В течение этого периода в
организме происходит активное размножение и накопление возбудителя и его
токсинов до определенного порогового количества, после которого организм
начинает отвечать теми или иными клиническими проявлениями, т. е. наступает
следующий, продромальный период. Продолжительность инкубационного периода
варьирует в среднем от нескольких дней до нескольких недель, но он может быть
равен и нескольким часам и длиться несколько месяцев, а при лепре - несколько
лет.[36] Это зависит
от ряда причин - величины заражающей дозы и степени патогенности возбудителя, а
также от состояния резистентности организма.[25]
Продромальный период, или период предвестников.
Он характеризуется обычно неспецифическими, общими проявлениями - слабость,
разбитость, головная боль, общее недомогание, повышение температуры и т. п. Его
продолжительность варьирует в пределах 24
- 48
ч.
Период развития (расцвета) болезни. Он также
часто характеризуется известной цикличностью. Различают стадию нарастания
симптомов (стадия incrementum),
расцвета болезни (стадия асте) и период угасания симптомов (стадия Decrementum).
При типичной форме болезни этот период характеризуется проявлением
специфических для данной болезни симптомов, а также и некоторыми общими
симптомами, в частности, лихорадкой, интоксикацией, воспалением, иногда
появлением сыпи. [2]
Период исходов. В этот период может наступить:
· Рецидив заболевания - возврат клинических
проявлений болезни без повторного заражения, за счет оставшихся в организме
возбудителей;
· Суперинфекция - инфицирование
макроорганизма тем же возбудителем до выздоровления. Если это происходит после
выздоровления, то это называется ренинфекции, т.к. она возникает в результате
нового заражения тем же возбудителем, как это часто бывает при гриппе,
дизентерии, гонорее.
· Бактерионосительство, носительство
возбудителя какого-либо инфекционного заболевания без клинических проявлений;[47]
· Выздоровление, или реконвалесценции.
Клиническое выздоровление наступает обычно раньше патологоанатомического и
бактериологического выздоровления. Человек практически здоров, но на месте
локализации процесса еще остаются какие-либо патологоанатомические изменения
(например, после перенесенной дизентерии на слизистой оболочке толстой кишки).
[14] Реконвалесценция может быть полной: все процессы заканчиваются полностью
без каких-либо отягощающих последствий. Однако некоторые болезни оставляют тяжелые
последствия, например паралич мышц после полиомиелита, энцефалита; цирроз
печени после вирусного гепатита В и т. п. [41]
Особо
следует принимать во внимание бактериологическое выздоровление после
инфекционного заболевания, т. е. полное освобождение организма от возбудителя.
При различных инфекционных заболеваниях срок бактериологического выздоровления
варьирует, и это учитывается при выписке таких больных из больницы. Например,
при брюшном тифе до 80 % реконвалесцентов в течение первых двух недель являются
бактерионосителями. [47]
· Летальный исход. При этом необходимо
помнить, что трупы инфекционных больных подлежат обязательной дезинфекции, т.к.
представляют определенную эпидемиологическую опасность из-за высокого
содержания в них микробного агента. [45]
3.6 Формы
инфекционных заболеваний
Инфекционные болезни обычно сопровождаются
нарушениями гомеостаза организма и его физиологических функций. В зависимости
от эпидемиологической ситуации, типа и свойств возбудителя (например,
инфицирующей дозы, вирулентности и т.д.), состояния параметров гомеостаза
человека, а также от конкретных особенностей взаимодействия возбудителя и
организма инфицированного человека, инфекционный процесс может принимать
различные формы (от клинически выраженных до бессимптомных, от суперинфекций до
бактерионосительства). [25] Ниже
рассмотрены основные формы инфекционных процессов.
Манифестная инфекция, т. е. инфекционная
болезнь, которая может протекать типично, атипично, хронически и т. п.;
· Типичная для данного возбудителя форма инфекции.
Возбудитель проникает в организм, активно в нем размножается, вызывая
характерные (типичные) для данной болезни клинические проявления, которые также
характеризуются определенной цикличностью. [2]
· Атипичная форма. Возбудитель проникает в организм,
активно в нем размножается, организм отвечает соответствующими
иммунобиологическими реакциями, которые приводят к формированию активного
иммунитета, но клинические симптомы болезни носят невыраженный, стертый или
атипичный характер. Чаще всего это связано либо со слабыми патогенными
свойствами возбудителя, либо с высокой естественной резистентностью организма,
либо с эффективным антибактериальным лечением, либо с действием всех этих трех
факторов.
· Персистентная (хроническая). Возбудитель
проникает в организм, размножается в нем, вызывает активную форму болезни, но
под влиянием иммунных систем организма и химиопрепаратов подвергается L-трансформации.
Поскольку L-формы бактерий не
чувствительны ко многим антибиотикам и химиопрепаратам, чей механизм действия
связан с нарушением синтеза клеточной стенки, а также к антителам, они могут
длительное время переживать (персистировать, англ. persistance
- живучесть) в организме. [11] Возвращаясь в свою исходную форму, возбудитель
восстанавливает патогенные свойства, размножается и вызывает обострение
(рецидив) болезни. [21]
· Медленные инфекции. Возбудитель
проникает в организм и может долгое время - месяцы, годы - сохраняться в нем
внутриклеточно в латентном состоянии. В силу ряда биологических особенностей
возбудителей медленных инфекций организм не в состоянии от них избавиться, а
при благоприятных для возбудителя условиях он начинает беспрепятственно
размножаться, заболевание протекает все тяжелее и тяжелее и, как правило,
заканчивается смертью больного.[17] Медленные инфекции характеризуются
длительным инкубационным периодом, длительным прогрессирующим развитием
болезни, слабым иммунным ответом и тяжелым исходом. Типичным примером медленной
инфекции является СПИД. [41]
Бессимптомная инфекция (носительство, латентная,
абортивная, дремлющая и т. п.).[17]
В зависимости от свойств главных факторов
инфекционного процесса (т. е. возбудителя и макроорганизма) различают следующие
основные формы инфекции:
· Абортивная. Возбудитель проникает в
организм, но не размножается в нем или в связи с надежной естественной
резистентностью, или с приобретенным специфическим иммунитетом, подавляющим
возбудителя. Таким образом, инфекционный процесс обрывается, и возбудитель рано
или поздно погибает или удаляется из организма.
[26]
· Латентная (инаппарантная).
Возбудитель проникает в организм, размножается в нем, макроорганизм отвечает на
него соответствующими иммунобиологическими реакциями, ведущими к формированию
приобретенного иммунитета и удалению возбудителя из организма. Однако никаких
внешних клинических проявлений этой инфекции нет, она протекает скрыто
(латентно). [25] Нередко в такой латентной форме люди переносят полиомиелит,
бруцеллез, некоторые вирусные гепатиты и другие болезни. [7]
· Дремлющая инфекция. Бессимптомное
пребывание возбудителя в организме может сохраняться долгое время после
латентной инфекции или после перенесенного заболевания, например легочного
туберкулеза, закончившегося формированием первичного комплекса. Под влиянием
условий, понижающих сопротивляемость организма, сохраняющиеся в нем живые
микроорганизмы активизируются и вызывают заболевание или его рецидив.[15]
Таким образом, патогенные микробы находятся некоторое время как бы в
«дремлющем» состоянии. Такие «дремлющие» микробы могут проникать в организм из
внешней среды или быть результатом перехода в «дремлющее» состояние
микроба-возбудителя, подавленного в своей активности, но сохранившего
жизнеспособность и потенциальную готовность к активации при благоприятных для
него условиях. Поэтому они получили название «микробов, готовых к выходу»
(франц. «microbes de sortie»).
В тех случаях, когда «дремлющие» в организме микробы сосредоточены в местном
ограниченном очаге, откуда они могут распространяться и вызывать заболевание,
применяют термин «фокальная» инфекция (например, заглохший воспалительный
процесс в кариозном зубе, в котором его возбудитель - стрептококк - сохраняется
в «дремлющем» состоянии до поры до времени).[29]
· Бактерионосительство. Очень часто
после либо латентной инфекции, либо перенесенного заболевания организм человека
не в состоянии полностью освободиться от возбудителя. При этом человек, будучи
практически здоровым, становится его носителем в течение многих месяцев или
даже лет. [47] Являясь источником заражения для других лиц, бактерионосители
играют большую роль в эпидемиологии многих заболеваний (брюшного тифа, дифтерии
и др.), поскольку они выделяют их возбудителей в окружающую среду, заражают
воздух, воду, пищевые продукты. Около 5-8 % людей, переболевших брюшным тифом,
становятся хроническими (на срок более 3 мес.) носителями S.
typhi
и служат основным их резервуаром в природе.[44]
Существуют понятия реинфекции, суперинфекции,
микст-инфекции, вторичной инфекции.[17]
Реинфекция - повторное заражение и развитие
инфекции, вызванной тем же возбудителем, обычно в форме клинически выраженной
инфекционной болезни, так как после заболевания напряженный иммунитет не
вырабатывается. [20]
Суперинфекция - инфицирование организма
болеющего тем же возбудителем до наступления выздоровления.
Микст-инфекция (коинфекция) - одновременное
возникновение двух инфекционных процессов, вызванных различными
микроорганизмами. Противоположное понятие - моноинфекция.
[4]
Вторичная инфекция - возникает как следствие
ослабления иммунитета на фоне первичного инфекционного заболевания и может
вызываться различными возбудителями (бактериями, вирусами, грибами). Вторичные
инфекции, вызванные малопатогенными или непатогенными для здорового человека
микроорганизмами, у страдающего иммунодефицитом человека принято называть оппортунистическими.
[15]
Аутоинфекция - развитие инфекционного процесса,
вызванного собственной (как правило, условно-патогенной) микрофлорой,
населяющей кожу и слизистые оболочки, при попадании ее в другие биотопы
(например, в рану) в результате самозаражения.[29]
Различают также инфекцию экзогенную и эндогенную
(в том числе аутоинфекцию), очаговую (локальную) и генерализованную.[17]
4.
ЕПИДЕМОЛОГИЯ ИНФЕКЦИОННОГО ПРОЦЕССА
Основоположник учения об эпидемическом процессе
- Л.В. Громашевский, впервые детально разработавший теорию общей эпидемиологии,
понятие об источнике инфекции, механизме передачи и движущих силах эпидемии. По
определению Л.В. Громашевского, существование эпидемического процесса
обусловливает чередование пребывания возбудителя в организме хозяина с выходом
его во внешнюю среду.[48]
Таким образом, эпидемический процесс состоит из трёх элементов:
• источник инфекции (инфицированный организм
человека или животного);
• механизм, пути и факторы передачи возбудителя;
• восприимчивый организм человека или колектив.
Эти элементы тесно связаны между собой и
обеспечивают непрерывность течения эпидемического процесса. При устранении
одного из факторов распространение инфекционной болезни прекращается[49]
(рис.4).
4.1 Источники инфекции
Различные одушевленные и неодушевленные объекты
внешней среды, содержащие и сохраняющие патогенные микроорганизмы, обозначают
термином резервуары инфекции, но их роль в заболеваемости человека далеко не
одинакова. Для большинства инфекций человека основной резервуар и источник -
больной человек, в том числе лица, находящиеся в инкубационном периоде (ранние
носители) и на этапах реконвалесценции, либо бессимптомные (контактные)
микробоносители. [50] В соответствии с источником инфекции выделяют следующие
возможные источники инфекционных болезней.

Рисунок 4 - Эпидемический процесс при
антропонозах [48]
Антропонозы (от греч. anthropos
- человек, nosos, болезнь).
Заболеваня при которых единственным источником возбудителя является человек (например,
брюшной тиф, дизентерия, холера и др.). Характерная черта антропонозов - узкая
видовая специализация как возбудителя, так и хозяина инфекции, способная
возрастать в ходе сопряжённой эволюции.
Зоонозы (от греч. zооп
- животное и nosos - болезнь),
ими болеют только животные, например, чума рогатого скота, чума свиней и др.;
Зооантропонозны (от греч. zооп
- животное, anthropos,
человек и nosos - болезнь).
Заболеваня при которых источником возбудителя является животные, и заражающиеся
от них люди (в том числе и трупы умерших). [51]
Сапронозы. Инфекции, развивающиеся после
проникновения свободноживущих бактерий или грибов в организм человека с
объектов окружающей среды и поверхности тела (например при попадании в рану)
известны как сапронозы( от греч. sapros
- гнилой, nosos - болезнь).
Сапронозные инфекции, будучи самой древней в эволюционном плане группой
инфекций, характеризуются, как правило, отсутствием какой-либо специализации
возбудителя к человеку. [1]
Эпидемический очаг - место пребывания источника
инфекции с окружающей его территорией в тех пределах, в которых заразное начало
способно передаваться от него окружающим лицам, т.е. возможно развитие
эпидемического процесса. Пространственные и временные границы эпидемического
очага при каждой инфекционной болезни определяют особенности механизма передачи
инфекции и конкретные условия природно-социальной среды, обусловливающие
возможности и масштабы реализации этого механизма. [52] Однако при зоонозах и
особенно при сапронозах, когда человек, как правило, не служит источником
инфекции, эпидемический процесс качественно отличен и представляет сумму
разрозненных заболеваний, возникающих независимо друг от друга (рис.4.1). В
этих случаях происходит групповое заражение людей от общих источников инфекции
(животных, субстратов внешней среды), так что эпидемический процесс носит не
цепной, как при антропонозах, а «веерообразный» характер.
4.2 Механизмы, факторы
и пути передачи
«Любой паразитический вид, - писал Л.В.
Громашевский, - как бы хорошо он не был адаптирован к организму своего
биологического хозяина, не может ограничить свою природу только этой формой
своего приспособления. Всякий высший организм, служащий хозяином для паразита,
рано или поздно погибает. Поэтому ни один паразитический организм не может
существовать в природе как вид, если он не сменяет систематически своего
индивидуального хозяина». [48] Исходя из изложенного, Л.В. Громашевским было
предложено понятие «механизма передачи». Механизм передачи - эволюционно
выработанный способ перемещения возбудителя из одного организма хозяина в
другой, обеспечивающий ему поддержание биологического вида (рис. 4.2).
Механизм передачи возбудителя реализуется через
три стадии:
• стадию выделения из заражённого организма;
• стадию циркуляции во внешней среде;
• стадию внедрения в очередной организм.
Вторая и третья стадии механизма передачи
реализуются через факторы передачи. [51]
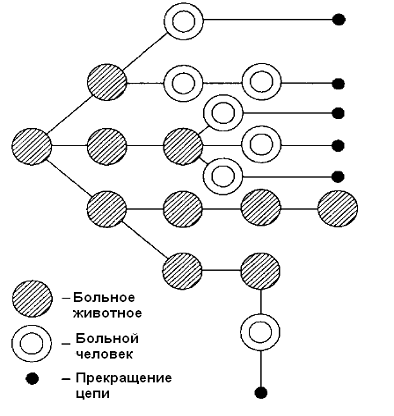
Рисунок 4.1 - Эпидемический процесс при зоонозах

Рисунок 4.2
- Схема механизма передачи инфекции
Факторы передачи - элементы внешней среды,
обеспечивающие перенос возбудителя от одного организма к другому. Ими могут
быть воздух, пища, вода, почва, предметы обихода, быта и производственной
обстановки, живые переносчики. Факторы передачи, на которые возбудитель
попадает при реализации первой стадии механизма передачи, называют первичными.
Факторы передачи, доставляющие возбудитель в заражающийся организм, называют
конечными, В тех случаях, когда первичный фактор передачи не может выполнять
функцию конечного фактора, в механизм передачи включаются промежуточные
факторы, доставляющие возбудитель с первичных факторов на конечные. [52]
Пути передачи - совокупность элементов внешней
среды, обеспечивающих перенос возбудителя из одного организма в другой
(распространение соответствующей болезни).
Способы выведения возбудителя из заражённого
организма и внедрение в восприимчивый организм определяет его специфическая
локализация в организме хозяина.[9] В свою очередь локализацию определяет
механизм передачи возбудителя от заражённого организма в заражающийся, т.е.
существует закон соответствия механизма передачи основной (эпидемиологической)
локализации возбудителя в организме хозяина (Громашевский Л.В.). На основе
анализа всего разнообразия инфекционных болезней Л.В. Громашевский разделил их
на четыре группы в зависимости от локализации возбудителя в организме хозяина и
механизма передачи. [48]
· Фекально-оральный механизм включает
алиментарный, водный или контактно - бытовой пути передачи.
· Кровяной (трансмиссивный) механизм
включает передачу возбудителей через укусы переносчиков, парентеральный и
половой пути передачи.
· Аэрогенный (респиратоный) механизм
включает воздушно - капельный и воздушно - пылевой пути передачи возбудителя.
· Контактный механизм включает раневой
и контактно - половой пути передачи. [39]
Распространение проникших в организм
возбудителей может происходить по-разному, в зависимости от свойств возбудителя
и имеющихся в клетках ткани рецепторов для них: контактным путем, т. е. от
клетки к клетке, лимфогенным или гематогенным путем; некоторые возбудители
распространяются по нервным путям. [54]
.3 Восприимчивость популяции
Восприимчивость - способность организма отвечать
на внедрение возбудителя рядом специфических патологических реакций.
Восприимчивость к инфекционным болезням прежде всего определяет неодинаковая
чувствительность организма разных людей к внедрению различных инфекционных
агентов. Она зависит от состояния организма человека, его возраста, пола,
качественной характеристики возбудителя, его дозы и конкретных условий места и
времени развития эпидемического процесса. [55]
Восприимчивость принято выражать контагиозным
индексом - численным выражением готовности к заболеванию при первичном инфицировании
каким-либо определённым возбудителем. Контагиозный индекс показывает степень
вероятности заболевания человека после гарантированного заражения. При высоком
контагиозном индексе индивидуальная предрасположенность не может оказывать
существенного влияния на заболеваемость, при низком индексе заболеваемость
больше зависит от предрасположенности человека к заболеванию. [49]
Контагиозный индекс выражают десятичной дробью
или в процентах. Так, при кори этот показатель приближается к 1 (100%), при
дифтерии он составляет 0,2 (20%), при полиомиелите - 0,001-0,03%. [1]
4.4 Проявления
эпидемического процесса
Эндемическая заболеваемость, или эндемия, -
постоянно регистрируемая на определённой территории заболеваемость конкретными
болезнями (в том числе неинфекционными), обусловленная социальными и природными
условиями.[56] Экзотическая заболеваемость - заболеваемость болезнями, не
свойственными данной местности. Она возникает в результате заноса или завоза
возбудителя с других территорий. Повсеместное распространение по всему земному
шару характерно для большинства антропонозных инфекций и ряда зоонозов домашних
животных. Территориальная неравномерность распределения заболеваний характерна
для зоонозов, резервуаром возбудителя которых служат дикие животные, и ряда
антропонозов, зависящих от природных и социальных условий. Территории
распространения заболеваний - нозоареалы.[48] С известной долей условности все
инфекционные болезни по особенностям их территориального распространения и типу
нозоареала можно объединить в две группы: с глобальным и региональным
распределением.
• Глобальное распространение характерно для
большинства антропонозных инфекций и ряда зоонозов домашних животных.
• Региональное распространение заболеваний
свойственно прежде всего природно-очаговым инфекциям. [57]
Зональные нозоареалы - территории
распространения болезней человека, эндемичных для вполне определённых зон
земного шара. Обычно эти нозоареалы в виде пояса охватывают весь земной шар
или, по крайней мере, большую его часть. Зональное распределение болезней
зависит от определённых климатических и ландшафтных зон земного шара. К таким
инфекционным болезням относят туляремию, блошиный эндемический тиф, аскаридоз.
4.5 Интенсивность эпидемического процесса
Интенсивность эпидемического процесса
обуславливает множество факторов, основными из которых выступает свойства и
распространенность возбудителя, характер иммунной «прослойки» в популяции, а
также и географическое положение конкретных территорий.
В зависимости от интенсивности распространения
болезни эпидемический процесс может проявляться в виде спорадической
заболеваемости, групповых заболеваний (эпидемических вспышек), эпидемий и
пандемий. [49]
Спорадическая заболеваемость (от греч. Sporadikos,
рассеянный) - единичные, не связанные между собой, неповсеместные и
нерегулярные заболевания. Как правило количество больных не превышает десяти
случаев на 100000 населения за год.
Эпидемическая вспышка. Групповые заболевания,
связанные с одним источником (путями и факторами передачи) инфекции и не
выходящие за пределы семьи, коллектива, населённых пунктов.
Эпидемия ( от греч. epi
- над, demos - народ). Более интенсивное и широкое распространение инфекционной
болезни, охватывающее население региона страны или нескольких стран. Она
представляет совокупность епидемических вспышек, возникающих на больших
территориях и наслаивающихся одна на другую. Наиболее часто эпидемии разделяют
по четырём признакам: временному, территориальному, по интенсивности и
механизму развития эпидемического процесса. [53]
· По временному признаку выделяют острые
(взрывоопасные) и хронические (длительно протекающие) эпидемии. Наиболее
типичными острыми эпидемиями бывают эпидемии, развивающиеся при одномоментном
заражении. Первый случай заболевания появляется по истечении минимального
инкубационного периода болезни, последний - после максимального. Наибольшее
количество заболеваний приходится на средний инкубационный период. Заболевания,
возникшие за пределами колебаний инкубационного периода, - результат вторичных
заражений. [44]
· По территориальному признаку
выделяют эпидемии локальные, приуроченные к определённой территории и группе
населения, а также распространённые, захватывающие смежные территории и группы
населения.
· По интенсивности развития
эпидемического процесса различают эксплозивные (взрывоопасные) и вяло
протекающие эпидемии.[56]
· По механизму развития различают три
группы эпидемий.
1. Эпидемии, связанные с веерообразной
передачей возбудителя от одного источника или фактора передачи сразу большому
количеству людей без последующей передачи возбудителя от заболевшего (зоонозы,
сапронозы). Эпидемии, обусловленные цепной передачей возбудителя от заражённых
индивидуумов здоровым (воздушно-капельным путём при аэрозольных инфекциях,
контактно-бытовым - при кишечных).
2. Эпидемии, развивающиеся за счёт передачи
возбудителя от заражённых лиц здоровым через различные факторы (пищу, воду,
членистоногих, предметы быта), без непосредственного контакта этих людей.
Пандемия (от греч. en
- в, demos - народ).
Повсеместная эпидемия, интенсивно распространяющаяся во многих странах или даже
во всех частях света. К счастью, подобные «сверхэпидемии», или пандемии
вызывают очень ограниченный спектр возбудителей (например, вирус гриппа).
Иногда под спорадической заболеваемостью
понимают регулярно наблюдаемый, сложившийся для данной местности уровень
заболеваемости, а под эпидемией - заболеваемость, превышающую обычную для
данной местности норму. [51]
Для инфекционных болезней характерны колебания
уровня заболеваемости в многолетней и годовой (помесячной) динамике.
• Многолетняя динамика определяет эпидемическую
тенденцию, цикличность и нерегулярные колебания заболеваемости.
• Годовая динамика включает межсезонный, средний
круглогодичный уровень и сезонное повышение заболеваемости. [53]
Инфекционные болезни неодинаково поражают разные
социально-возрастные группы населения. Интерпретация этих проявлений зависит от
эпидемиологических особенностей болезни. При инфекционных болезнях с активно
действующим аэрозольным механизмом передачи основное значение имеет
иммунологический фактор, болеют ими преимущественно дети раннего возраста,
посещающие организованные коллективы. Зоонозными инфекциями чаще заражаются
взрослые люди, в силу своей профессиональной деятельности, ухаживающие за
животными или занимающиеся переработкой животного сырья. В то же время
некоторые кишечные инфекции распространены среди определённых возрастных и
профессиональных групп населения, связанных с возможностью заражения через пищу
или воду. [49]
СПИСОК ЛИТЕРАТУРЫ
1. Инфекционные
болезни и эпидемиология: Учебник / В.И. Покровский, С.Г. Пак, Н.И. Брико, Б.К.
Данилкин. - 2-е изд. - М.: ГЭОТАР-Медиа, 2007. - 816 с.: ил.
2. Коротяев
А.И., Бабичев С.А. Медицинская микробиология, иммунология и вирусология. -
СПб.: СпецЛит, 2008. - 4-е изд., испр. и доп. - 767 с.: ил.
3. Воробьев
А.А., Кривошеий Ю. С., Широбоков В.П. Медицинская и санитарная микробиология:
Учеб.пособие для студ.высш. мед.учеб. заведений - М.: Академия, 2003. - 464 с.
4. Поздеев
О.К. Медицинская микробиология. - М.: ГЭОТАР-МЭД, 2001. - 765c.
. Павловский
Е.Н. Курс паразитологии человека (с учением о переносчиках инфекций и инвазий).
Изд. 2. Л.- М.: Гос. изд. биол. и мед. лит., 1934. - 592 с. 1961?
. Жданов
В.М. Эволюция заразных болезней человека. - СПб.:Фолиант, 1963.- 423с.
. Постовит
В.А. Инфекционные болезни: руководство. - СПб.: Фолиант, 1997.- 502с.
. Бухарин
О.В., Литвин В.Ю. Патогенные бактерии в природных экосистемах. - Екатеринбург.:
УрО РАН, 1997. -277с.
. Езепчук
Ю.В. Патогенность, как функция биомолекул. - М.: Медицина,1985. - 256с.
. Доморадский
Н.В. Нужен ли термин «сапронозы?»// Журн. микробиол. - 1988. - № 12. -
С.117-122.
. Прозоркина
Н. В., Рубашкина Л. А. Основы микробиологии, вирусологии и иммунологии: Учебное
пособие для средних специальных медицинских учебных заведений. - Ростов нД.:
Феникс, 2002. -416с.
. Руководство
к практическим занятиям по медицинской микробиологии и лабораторной диагностике
инфекционных болезней / Под ред. Ю.С. Кривошеина.
- К.: Вища шк., 1986. - 376 с.
13. Шлоссенберг
Д., Шульман Ионас А. Дифференциальная диагностика инфекционных болезней: Практ.
руководство для врачей и студ.: Пер. с англ.- М. Бином. - СПб.: Невский
Диалект, 2000.- 306с.
. Васильев
В.С., Комар В.И., Цыркунов В.М. Практика инфекциониста. - Минск.: Вышэйшая школа,
1993. - 480с.
. Рахманова
А.Г. и др. Инфекционные болезни: Руководство для врачей общ. практики
/А.Г.Рахманова, В.А.Неверов, В.К. Пригожина.- 2-е изд., перераб. и доп.- СПб.:
Питер, 2001.- 569с.
. Литвин
В.Ю., Пушкарева В.И. Факторы патогенности бактерий: функции в окружающей средe
/ Журн. микробиол.- 1994. - приложение. - С. 83 - 87.
. Краткий
курс медицинской микробиологии./ Г. М. Шуб, В. И. Корженович, И. О.Лунева, И.
Г. Швиденко. - Саратов, 2001г. - 342с.
. Флетчер
Р., Флетчер С., Вагнер Э. Клиническая эпидемиология.- М.: МедиаСфера, 1998.-
350с.
. Тимаков
В. Д., Левашев В. С., Борисов Л. Б. Микробиология. -М.: Медицина, 1983. -512 с.
. Люта
В.А., Заговора Г.І. Основи мікробіології, вірусології та імунології -
К.: Здоров’я, 2001. - 273 с.
. Борисов
Л.Б. Медицинская микробиология, вирусология и иммунология. М.: МИА, 2005. - 736c.
. Литвин
В.Ю., Емельяненко Е.Н., Пушкарева В.И. Патогенные бактерии, общие для человека
и растений: проблема и факты // Журн. Микробиол. - 1996. - № 2. - С. 101 - 104.
. Шувалова
Е.П. Инфекционные болезни: Учебник. - М.: Медицина, 1995. 656 с.
24. Ситник
І.О., Климнюк С.І. Мікробіологія, вірусологія, імунологія. - Тернопіль:
Укрмедкнига, 1998. - 389 с.
25. Гавришева
Н.А., Антонова Т.В. Инфекционный процесс. Клинические и патофизиологические
аспекты: Учебное пособие. - СПб.: Специальная литература, 1999. - 255 с.
26. Лекції
з загальної медичної мікробіології / За ред. В.К. Патратія. - Чернівці.: Медик
,1997. - 96 с.
. Вертиев
Ю.В. Бактериальные токсины: биологическая сущность и происхождение // Журн.
Микробиол. - 1996. - № 3.
. Рудаков
Н.В. Краткий курс лекций по медицинской микробиологии, вирусологии и
иммунологии. В 2 частях: Учебное пособие. - Омск.: ОмГМА, 2002.- 96с.
. Румянцев
С.Н. Микробы, эволюция, иммунитет. - Л.: Наука 1984г. -176с.
30. Finlay
B., Falkow S. Common Themes in Microbial Pathogenicity Revisited Microbiology
and Molecular Biology Reviews. - 1997. - Vol. 61, №2.
. Schmitt
C.K., Meysick K.C., O”Brien A. Bacterial Toxins: Friends or Foes? // Emerging
Infectious Diseases. - 1999. - Vol. 5, № 2. - Р.
224 - 234.
. Bhakdi
S., Bayley H., Valeva A. et al. Staphylococcal alpha-toxin, streptolysin-O and
Escherichia coli hemolysin: prototypes of pore-forming bacterial cytolysins //
Arch. Microbiol.
- 1996. - Vol. 165, № 1. - P. 73-79.
33. Halpern
J., Neale E. Neurospecific binding, internalization and retrograde axonal
transport // Curr Top Microbiol Immunol. - 1995. - Vol. 195, № 1. - P. 221-241.
. Arnon
S. Human tetanus and human botulism // In: Rood JI, McClane BA, Songer JG,
Titball RW, editors. The clostridia: molecular biology and pathogenesis. San
Diego: Academic Press; 1997. - P. 95-115.
. Schiavo
G., Montecucco C. The structure and mode of action of botulinum and tetanus
toxins. // In: Rood J., McClane B., Songer J., Titball R. editors. The
clostridia: molecular biology and pathogenesis. San Diego: Academic Press;
1997. P. 295-322.
36. Приобретенный
иммунитет и инфекционный процесс./ В.И. Покровский, М.М. Авербах, В.И. Литвинов
и др.- М.: Медицина, 1979. -280с.
. Черкасский
Б.Л. Инфекционные и паразитарные болезни человека - М.: Медицинская газета,
1994. - 477с.
. Громашевский
Л.В. Принцип классификации инфекционных болезней // Вестник Академии
медицинских наук СССР. - 1947. - № 4. - С.11-23.
. Ковалева
Е.П. О механизмах передачи инфекций в свете новых данных // Журн. Микробиол. -
1995. - № 2. - С. 105 - 106.
. Москалев
А. В.,. Сбойчаков В. Б. Инфекционная иммунология. - СПб.: Фолиант, 2006. -
174с.
. Черкасский
Б.Л.Особо опасные инфекции. Справочник. - М.: Медицина, 1996. - 160 с.
. Ерюхин
И.А., Гельфанд Б.Р., Шляпников С.А.Хирургические инфекции. Руководство. - СПб.:
Питер, 2003. - 864 с.
. Гратц
Н. Трансмиссивные инфекционные заболевания в Европе.- ВОЗ, 2005.- 168с.
. Руководство
по эпидемиологии инфекционных болезней: В 2т. / В.М. Болотовский, А.М.
Зарицкий, А.И. Кондрусев и др. /Под ред. В.И.Покровского. - М.: Медицина, 1993.
- Т.2 - 464с.
. Палеева
Н.Р. «Справочник медицинской сестры». - М.: Эксмо, 2006.- 544с.
. Инфекционные
болезни./ Т.В. Антонова, М.М. Антонов, В.Б. Барановская, и др. - СПб.: СпецЛит,
2000.- 509с.
. Бухарин
О.В., Усвяцов Б.Я. Бактерионосительство. - Екатеринбург.: УрО РАН, 1996. -206с.
. Громашевский
Л.В. Общая эпидемиология. - М.: Медицина, 1985. - 323с.
. Эпидемиология
Зуева Л.П., Яфаев Р.Х. - СПб.: Фолиант, 2005. - 752с.
. Вогралик
Г.Ф. Учение об эпидемических заболеваниях. - Томск.: СНМ, 1935. - 425с.
. Власов
В.В. Эпидемиология. - М.: ГЭОТАР-МЭД, 2004. -
459c.
. Елкин
И.И. Некоторые вопросы теории эпидемиологии // Журн. микробиол. - 1952. - № 8.
- С.58-63.
. Черкасский
Б.Л. Руководство по общей эпидемиологии.- М.: Медицина, 2001.- 559с.: ил.
. Лобзин
Ю.В. и др. Воздушно-капельные инфекции / .В.Лобзин, В.П.Михайленко, Н.И.Львов.-
СПб.: Фолиант, 2000.- 184с.
. Черкасский
Б.Л. Эпидемиологический диагноз. - М.: Медицина, 1990. - 208с.
. Ягодинский
В.Н. Динамика эпидемического процесса. - М.: Медицина, 1977. - 232 с.
. Громашевский
Л.В. Еще раз о классификации инфекционных болезней // Журн. микробиол. - 1954.
- № 5. - С.67-75.