Изохинолиновые алкалоиды и препараты на их основе
1. Классификация изохинолиновых алкалоидов
Группа изохинолиновых производных охватывает
большое число разнообразных алкалоидов, имеющих важное значение в качестве
лекарственных веществ и встречающихся в растениях довольно многих семейств.
Наиболее богато ими семейство маковых (Papaveraceae).
Группа изохинолиновых алкалоидов в настоящее
время очень подробно разработана как аналитически (в смысле методов
установления строения), так и синтетически. Здесь, пожалуй, наибольшее число
алкалоидов, полученных синтезом. Большинство алкалоидов этой группы является
производными не самого изохинолина, а его тетрагидропроизводного. Степень
сложности их строения весьма различна: начиная от простейших производных самого
изохинолина, вроде карнегина и сальсолина, встречаются все стадии постепенного
усложнения вплоть до высокомолекулярных эфирообразных оснований типа
оксиакантина.
Все эти алкалоиды могут быть сообразно их
строению разбиты на несколько групп, между которыми мыслимы переходы отчасти
чисто теоретические, отчасти осуществленные в действительности.
-я группа. Производные тетрагидроизохинолина и
1-метилтет-рагидроизохинолина

-я группа. Производные бензилизохинолина и
бензилтетрагидро-изохинолина

3-я группа. Алкалоиды группы апорфина

-я группа. Производные диизохинолина (тип
берберина и коридалина)

-я группа. Производные нафтофенантридина
(хелидонин)

-я группа. Производные индофенантридина
(ликорин)

-я группа. Производные типа морфина
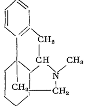
8-я группа. Алкалоиды с 10-членным кольцом (тип
протопина)

-я группа. Эфирообразные бимолекулярные
основания (тип оксиакантина)

-я группа. Основания сложного строения типа
эметина.
. Важнейшие реакции тетрагидроизохинолиновых
алкалоидов
Тетрагидроизохинолиновым производным свойственно
несколько характерных реакций. Как можно видеть по их формуле, 1-я стадия
гофманского распада легко может протекать, так как для нее имеется структурная
предпосылка в виде наличия водорода у β-углеродного
атома:

Вторая стадия гофманского распада не может
протекать с той же легкостью, так как такой β-водород
у дес-основания отсутствует. Применяя к этому дес-основанию реакцию Эмде, можно
достигнуть отщепления азота:

Такое течение гофманского распада, а именно
легкость в первой стадии и невозможность его во второй одновременно с легкостью
Эмде-реакции, характерно для этой группы алкалоидов.
Если же в положении 1, как это часто имеет
место, находится заместитель, то гофманский распад становится возможным в обеих
стадиях,- например:
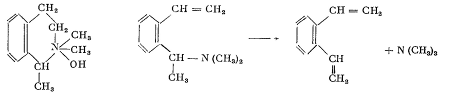
Далее, интересной реакцией, характерной для
этого типа веществ, является действие на них хлорангидридов кислот. При этом
происходит присоединение молекулы последнего с разрывом кольца:

В образующихся таким образом веществах имеется
кислотный радикал, связанный с азотом; ввиду этого они лишены основных свойств.
При окислении тетрагидроизохинолиновых
производных обычно происходит разрушение гидрированного кольца с образованием
соответствующего производного фталевой кислоты:
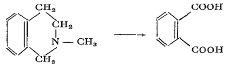
Такие реакции окисления часто дают очень ценные
данные для суждения о структуре алкалоидов этой группы.
. Главные синтетические методы получения
изохинолиновых алкалоидов
Среди синтетических методов, разработанных для
этой группы веществ, наиболее ценными являются две реакции, найденные еще в
1893 г. Бишлером и Напиральским и широко использованные Пиктэ, Перкином,
Робинсоном и др.
Первая из этих реакций заключается в действии
водоотнимающих веществ (Р2О5, РСl5,
РOСl3
и др.) на амиды кислот, получающихся из фенилэтиламина и его производных. При
этом можно представить себе, что эти амиды реагируют в таутомерной форме.
Получающиеся при этом дигидроизохинолиновые
производные при восстановлении легко дают соответствующие тетрагидропроизводные,
а при дегидрировании (химическом или, лучше, каталитическом при помощи
металлического Pd)
- производные самого изохинолина:

Вторая реакция, приводящая прямо к
тетрагидроизохинолиновым производным, заключается в действии альдегидов на
фенилэтиламин и его производные. При этом альдегиды применяются или в свободном
виде, или в форме ацеталей.
Для альдегидов можно представить себе, что они
реагируют в гидратной форме:
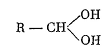
Конденсируя, например, фенилэтиламин с
формальдегидом, получают тетрагидроизохинолин:

Если вместо формальдегида взять другие
альдегиды, можно получить тетрагидроизохинолиновые производные, замещенные в
положении 1. Так, например, фенилэтиламин и фенилацетальдегид дают
1-бензилтетра-гидроизохинолин:
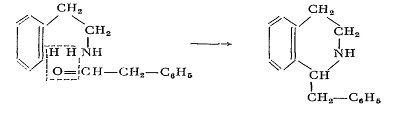
4. Алкалоиды группы апорфина глауцин С21Н25О4N
Глауцин был получен (в загрязненном виде)
Пробстом в 1839 г. В чистом виде его получил впервые Р. Фишер, выделивший его
из надземных частей Glaucium
luteum (из семейства маковых).
Позже (1933-1943) присутствие алкалоида было доказано (Манске) в некоторых
видах Dicentra.
Глауцин был найден так же в Corydalis
ternata Nakai,
Glaucium
flavum Crantz.
и G. serpieri
Heldr., относящихся к
тому же семейству.
Физические свойства
Глауцин - кристаллизуется в бесцветных
ромбических призмах, темп. пл. 119-120°C,
[α]D=
+113°. Рацемический глауцин (синтетический) имеет темп. пл. 137-139°C
и при помощи виннокислой соли может быть расщеплен на оптически активные
компоненты. Глауцин трудно растворим в бензоле и воде, легче в эфире, очень
легко в спирте и хлороформе. Дает хорошо кристаллизующиеся соли, например
хлоргидрат, темп. пл. 235°C.
Очень характерна растворимость этой соли в хлороформе.
Химические свойства и строение
Глауцин - довольно сильное третичное основание,
имеющее N-метильную группу.
Все кислородные атомы находятся в виде метоксильных групп.
Строение и синтез глауцина. Глауцин интересен
тем, что строение его было выведено исключительно на основе биогенетических
соображений, без всякой почти аналитической обработки, и было затем
непосредственно проверено путем синтеза, доказавшего правильность этих
теоретических соображений.
Синтез такого вещества облегчался тем, что
изохинолиновое производное соответствующего строения было уже известно. Это
есть не что иное, как нитропапаверин, получаемый непосредственным нитрованием
папаверина. Путем метилирования и восстановления из него было получено
соответствующее аминотетрагидроизохинолиновое производное (аминолауданозин), из
которого путем диазотирования и разложения диазосоединения порошком
металлической меди получился рацемический глауцин:

. Основания сложного строения типа эметина
В так называемом рвотном корне, или ипекакуане,
корнях южноамериканского растения Psychotria
ipecacuanha
Stokes (синон. Cephaelis
Iресасиапhа
Brot.) (сем. мареновых-Rubiасеае),
содержатся следующие алкалоиды:
1.
Эметин
С29Н40О4N2,
2.
Цефаэлин
С28H38O4N2.
3.
Психотрин
С28Н36O4N2.
4.
О-Метилпсихотрин
С29Н38O4N2.
5.
Эметамин
С29H36O4N2.
Все они близко связаны между собой рядом
переходов. Количество алкалоидов в корне ипекакуаны достигает 2,5-3%. Главными
являются эметин и цефаэлин, количество которых составляет 1,35 и 0,25%. Прочие
алкалоиды находятся в ничтожном количестве: О-метилпсихотрин 0,015-0,033%, а
эметамин 0,002-0,006%.
Алкалоиды находятся главным образом в коре
корней.
Впервые эметин был получен Пельтье в 1817 г., и
только в 1879 г. он был выделен в чистом виде Подвысоцким.
Физические свойства
Эметин - белый порошок, темп. пл. 74°С; [а]D
=- 25, 8° (С2Н5OН)
и [а]D
= -50° (в СНСl3).
Легко растворим в спирте, эфире и хлороформе, почти нерастворим в воде. Дает
хорошо кристаллизующиеся соли. В медицине применяются его хлоргидрат С29Н40О4N2·2НС1·7Н2O,
темп. пл. 235-255°C, и бромгидрат
С29Н40О4N2·2НВг·4Н2О,
темп. пл. 250-260°C.
Химические свойства и строение эметина
Кислородные атомы эметина находятся в нем в
форме четырех метоксильных групп. Один из атомов азота третичный, другой
вторичный. Метилимидной группы эметин не содержит. Один из атомов азота должен,
следовательно, стоять одновременно в двух кольцах. Формула эметина может быть
развернута в таком виде: С25Н27(ОСНз)4 (≡N)(=(NH).
Окисление эметина показало, что он относится к ряду изохинолина. При этом были
получены 6,7-диметоксиизохинолин-1-карбоновая кислота, коридальдин и
м-гемипиновая кислота:



В 1948 г. Робинсон, пришел теоретически к
формуле эметина, окончательное подтверждение этой формулы было найдено при
изучении полного гофманского распада эметина и продуктов его окисления и
дегидрирования:

Связь между эметином и прочими алкалоидами
Цефаэлин относится к эметину, как фенол к своему
метиловому эфиру. Цефаэлин содержит три метоксильные группы и одну свободную
фенольную гидроксильную группу, при метилировании которой получается эметин:

Эта реакция имеет производственное значение, так
как некоторые сорта ипекакуаны содержат много цефаэлина, который как таковой
применения в медицине не имеет, путем же метилирования может быть переведен в
ценный эметин.
Цефаэлин имеет строение, выражаемое формулой:

. Производные типа морфина морфин С17Н10О3N
и кодеин С18Н21O3N
Морфин является первым открытым алкалоидом. В
1803 г. Дерон, извлекая опий водой и осаждая экстракт поташом, получил
кристаллическое вещество, которое назвал «опийной солью». От него ускользнул
основной характер этого вещества, которое, вероятно, было меконатом морфина или
наркотином. В 1806 г. Сертюрнер описал получение из опия чистого основания
морфина. Однако только в 1817 г., когда Сертюрнер подробно описал это вещество
и ясно указал, что оно является растительным основанием, это наблюдение
получило широкую известность и вызвало к себе должный интерес. До тех пор
считалось, что растительный организм способен производить только кислоты и
нейтральные вещества. Открытие морфина послужило мощным стимулом для изучения
алкалоидов. Вскоре после морфина был открыт ряд других растительных оснований.
Правильная суммарная формула морфина была установлена Лораном в 1847 г.
Кодеин был открыт в опии Робикэ в 1832 г., но
только в 1842 г. Герхардт установил правильную суммарную формулу.
Морфин и кодеин настолько близки между собой по
строению, что изучение их шло все время параллельно. Над этой трудной проблемой
работало в течение более 50 лет много десятков химиков, и только в 1925 1927 г
решение этой проблемы, по-видимому, явилось окончательным. Среди химиков,
изучавших структуру морфина, нужно в первую очередь упомянуть Кнорра, Пшора,
Фрейнда и Фонгерихтена, а позже Робинсона и Шепфа.
Морфин и кодеин были до сих пор найдены только в
опии, получаемом из мака снотворного -Papaver
somniferum
L. Указание на его
присутствие в диком американском хмеле- Нитиlus
lириlиs
L. (сем. тутовых- Моrасеае)
нуждается в проверке.
Физические свойства
Морфин - кристаллизуется из разбавленного спирта
в мелких ромбических табличках, содержащих одну молекулу Н2O,
которую они теряют при 100°C.
Темп. пл. безводного основания 247-248°C
(или 253- 254°C, исправлен.), [а]D
= -140° (СН3ОН). Морфин трудно растворим в обычных органических
растворителях. Для его кристаллизации рекомендуют амиловый и метиловый спирты.
Растворимость морфина сильно зависит от его агрегатного состояния: в аморфном,
свежеосажденном виде он гораздо легче растворим, чем в кристаллическом виде.
Морфин легко растворяется в едких щелочах, немного растворяется в аммиаке и
углекислых щелочах.
Кодеин - кристаллизуется из бензола или сухого
эфира в мелких безводных призмах, темп. пл. 155°С, [а]D
= -134° (СН3ОН). Из воды или разбавленного спирта он выделяется в
крупных прозрачных призмах, содержащих одну молекулу Н2О. Кодеин
очень мало растворим в воде; нерастворим в едких щелочах; его растворимость в
органических растворителях значительно больше, чем для морфина.
Химические свойства и строение
Морфин и кодеин - довольно сильные третичные
основания, содержащие >NCH3-группу,
присутствие которой может быть доказано по методу Герциг - Мейера. Один из
кислородных атомов морфина находится, как показывает его растворимость в
щелочах, в виде свободной фенольной гидроксильной группы. При метилировании
морфина йодистым метилом в присутствии щелочи он переходит в кодеин. Этот
чрезвычайно важный переход, найденный Гримо в 1881 г., показывает, что кодеин
является О-метиловым эфиром морфина; таким образом, доказательство строения
обоих алкалоидов сводится к одному вопросу. Второй кислородный атом морфина и
кодеина находится в виде вторичноспиртовой группы. Поэтому морфин дает
диацетильное, а кодеин - моноацетильное производное.
При окислении кодеина образуется соответствующий
кетон - кодеинон С18Н19О3N.
Третий кислородный атом обоих алкалоидов находится в эфирной, индифферентной
форме («мостиковый кислород»).
Строение углеродного скелета морфина и кодеина.
Формулы морфина и кодеина могут быть развернуты в таком виде:
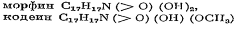 или
или

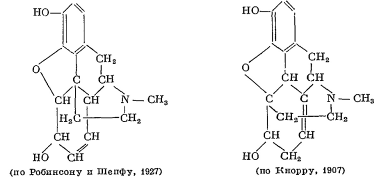
В результате длительной работы Кнорром была
установлена формула, отвечающая всем известным превращениям молекулы морфина.
Структура этого алкалоида представляет собой совершенно необычную и
оригинальную комбинацию колец, в которой кроме фенантренового ядра имеется еще
сложное семичленное азотистоуглеродное кольцо, соединяющее положения 5 и 9. В
1925 г. Робинсон и в 1927 г. Шепф пришли к небольшому видоизменению кнорровской
формулы, которое устраняет все имеющиеся трудности и, по-видимому, является
окончательным выражением структуры морфина:
. Тебаин С19Н21O3N
Тебаин был открыт в опии Пельтье и Тибумери в
1835 г. Сначала считали его за изомер морфина и дали ему название
«параморфина». Правильный состав тебаина С19Н21O3N
был установлен Андерсоном в 1852 г. Кроме опия, в котором содержание тебаина
колеблется между 0,2 и 1,0%, тебаин был найден Гадамером и Клее (1914) в маке
восточном - Papaver
orientale
L., В.В. Киселевым и
Р.А. Коноваловой (1941) в маке прицветниковом - P.
brancteatum
Lindl.
Физические свойства
Тебаин кристаллизуется из спирта в блестящих
листочках или в прямоугольных табличках, темп. пл. 193°C,
[а]D
= -218° (в спиртовых растворах). Удельное вращение мало зависит от концентрации,
но сильно уменьшается с повышением температуры. Хлоргидрат его имеет [α]D
= -163 (H2O).
Растворим в спирте, эфире, бензоле, хлороформе, почти нерастворим в воде,
аммиаке и едких щелочах.
Химические свойства и строение
Тебаин-сильное однокислотное основание,
содержащее >NCН3-группу.
Два атома кислорода находятся в нем в виде метоксильных групп, а третий имеет
индифферентный характер. Строение тебаина изучалось Pо-зером,
Фрейндом и многими другими авторами. Ввиду того, что его химизм очень близок к
химизму морфина и кодеина, оба ряда работ часто шли параллельно и взаимно
дополняли друг друга.
При нагревании с уксусным ангидридом тебаин
распадается на безазотистое вещество С16Н14О3,
названное тебаолом, и азотсодержащий остаток С3Н9ON
- N-монометиламиноэтанол.
Тебаин отличается от морфина тем, что обе
гидроксильные группы последнего (фенольная и спиртовая) метилированы и, кроме
того, в частично гидрированное кольцо введена еще вторая двойная связь. В то
время как морфин и кодеин являются тетрагидрированными производными, тебаин -
дигидрированное производное фенантрена. Ввиду существования столь близкой связи
между строением тебаина и кодеина менявшиеся воззрения на строение последнего
переносились и на строение тебаина. В настоящее время, когда формула Робинсона-Шепфа
может считаться установленной, и для тебаина принято аналогичное строение:

. Опий и опийные алкалоиды
Опий представляет собой засохший млечный сок,
вытекающий из искусственных надрезов не совсем зрелых головок снотворного мака Papaver
somniferum
L. (сем. маковых-Papaveraceae),
культивируемого для этой цели в большом масштабе. Опий является сложной смесью,
содержащей кроме алкалоидов белки, смолы, каучук, углеводы, минеральные соли и
другие вещества. Алкалоиды находятся в опии в виде солей с меконовой, серной и
молочной кислотами. Для сбора опия на почти созревших головках мака делаются
один или несколько надрезов, причем стенка не должна быть прорезана насквозь, с
тем чтобы семена могли дойти до стадии полного созревания. Млечный сок,
вытекающий из надреза, тщательно собирается. Резку мака повторяют через
несколько дней; иногда делают и третью резку, хотя опий, получаемый в последнем
случае, считается худшего качества. Высохший опий представляет собой густую смолистую
коричневую массу.
. Алкалоиды опия
Процентное содержание алкалоидов в опии
колеблется в широких пределах - от 2-3 до 15-20%. Ввиду того, что получение
опийных алкалоидов является крупным производством, эти вещества были для
исследователей легко доступны. Благодаря этому указанная группа алкалоидов
исследована весьма полно, хотя возможно, конечно, что и не все имеющиеся в нем
основания были выделены.
По числу находящихся в опии алкалоидов (это
число доходит до 22) мак занимает одно из первых мест между алкалоидоносными
растениями.
С химической точки зрения эта группа алкалоидов
неоднородна, в ней имеются представители трех типов, а именно:
а) производные 1-бензилизохинолина;
б) производные типа морфина;
в) производные типа протопина.
Кроме того, в опии находятся еще 3 алкалоида
неустановленного строения.
Методы выделения алкалоидов из опия
Алкалоиды находятся в опии в виде солей,
растворимых в воде; поэтому для отделения их от части балластных веществ опий
прежде всего подвергают экстракции теплой водой и отфильтровывают от
нерастворившейся части. Наркотин, являющийся очень слабым основанием, соли
которого сильно гидролизированы, при этой операции большей частью остается в
нерастворимом остатке и может быть получен из него извлечением соляной кислотой.
Водный раствор, в который перешли прочие алкалоиды, подвергается упариванию в
вакууме при возможно низкой температуре.
Для дальнейшей обработки этого сгущенного
раствора предложен был ряд методов, из которых наиболее распространенными
являются два, а именно: метод Грегори и метод Каневской и Клячкиной.
Метод Грегори. По этому методу к сгущенному
опийному экстракту прибавляется хлористый кальций; при стоянии выпадают
кальциевые соли серной, молочной и меконовой кислот, которые отфильтровываются.
Полученный маточник снова сгущают в вакууме до небольшого объема и оставляют на
холоду. При этом постепенно выделяется смесь хлоргидратов морфина и кодеина
(так называемая «соль Грегори»), которая отделяется от раствора отсасыванием; в
маточнике же остаются прочие алкалоиды. Для разделения морфина и кодеина
полученную соль Грегори сначала очищают кристаллизацией, а затем разлагают
аммиаком. При этом морфин осаждается, а кодеин остается в растворе.
Отфильтрованный морфин-основание переводится в хлоргидрат и очищается повторной
кристаллизацией. Из аммиачного фильтрата кодеин получается осаждением едкой
щелочью или извлечением бензолом и очищается кристаллизацией. Кодеин
применяется в медицине главным образом в виде фосфата. Для выделения прочих
алкалоидов (в производстве обычно ограничиваются выделением папаверина,
тебаина, наркотина и нарцеина, тогда как прочие редкие алкалоиды выделяются
только в исключительных случаях для научных целей) из маточника его разбавляют
водой и осаждают аммиаком. При этом выпадают наркотин, тебаин и часть
папаверина, а в маточнике остаются: нарцеин и часть папаверина (вместе с
нейтральным меконином).
Выпавший осадок извлекают горячим спиртом; при
охлаждении раствора выпадает наркотин. Фильтрат от него упаривают и
обрабатывают уксуснокислым свинцом, который осаждает наркотин и папаверин,
тогда как тебаин остается в растворе. Раствор освобождают от избытка свинца,
осаждают тебаин аммиаком и очищают переводом в труднорастворимый тартрат. Смеси
папаверина и наркотина, получающиеся при упаривании маточников, разделяют
обработкой разбавленной уксусной кислотой, в которой наркотин нерастворим. Из
уксуснокислого фильтрата папаверин осаждают аммиаком и очищают переводом в
трудно растворимый оксалат. Маточник, полученный после осаждения аммиаком и
заключающий нарцеин и папаверин, очищают осаждением уксуснокислым свинцом (в
осадок алкалоиды не переходят) и медленно упаривают до начала кристаллизации.
Нарцеин медленно выкристаллизовывается при стоянии на холоду. Из маточника
путем экстракции эфиром получается еще некоторое количество папаверина,
загрязненного меконином. Его очищают растворением в разбавленной соляной
кислоте (в которой меконин нерастворим), осаждением и переводом в оксалат.
Метод Каневской - Клячкиной. По этому методу
упаренный водный опийный экстракт разбавляется спиртом и осаждается, при
сильном перемешивании, строго определенным количеством аммиака. В этих условиях
осаждаются морфин и наркотин, а прочие алкалоиды остаются в растворе.
Для разделения морфина и наркотина их смесь
обрабатывается уксусной кислотой, в которой наркотин как очень слабое основание
не растворяется. Из фильтрата от наркотина морфин осаждают аммиаком.
Спиртово-аммиачный маточник, полученный после
осаждения морфина и наркотина, извлекается бензолом. Бензольный раствор очищается
взбалтыванием с 30%-ной едкой щелочью и обрабатывается 5%-ной уксусной кислотой
(с добавлением уксуснокислого натрия), которая растворяет кодеин и тебаин,
тогда как папаверин остается в бензольном растворе.
Водный кислый раствор (заключающий тебаин и
кодеин) подщелачивается аммиаком, который осаждает только тебаин. Последний
очищается через тартрат. Из водно-аммиачного маточника кодеин может быть
извлечен взбалтыванием с бензолом.
Ход разделения шести главных алкалоидов по
методу Грегори изображен на схеме:

Рис. 1

Рис. 2
. Производные бензилтетрагидроизохинолина
папаверин С20Н21О4N
Папаверин был открыт Мерном в 1898 г. в опии,
который содержит его в количестве около 1%. Строение папаверина было выяснено
многолетними работами Гольдшмидта (1876-1881). Первый синтез его осуществлен
Пиктэ и Гамсом в 1910 г.
Физические свойства
Папаверин кристаллизуется из смеси спирта и
эфира в призмах, темп. пл. 147°С. Оптически неактивен. Нерастворим в воде и
щелочах. Трудно растворим в бензоле, спирте, легко растворим в хлороформе.
Химические свойства и строение
Папаверин является слабым третичным основанием.
Метильной группы при азоте не содержит. Все четыре кислородных атома находятся
в виде метоксильных групп.
При сплавлении со щелочью папаверин распадается
на диметоксиизохинолин и на диметиловый эфир гомопирокатехина, а также на
продукты распада последнего: гомопирокатехин, вератровую и протокатеховую
кислоты.
Для папаверина, в ходе изучения процессов его
окисления и распада, выведена следующая формула строения, объясняющая все его
реакции:

. Производные фенантридина ликорин С16Н17O6N
Ликорин был выделен Моришима в 1897 г. из
луковиц Lycoris
radiata Herb.
(синон. - Nerine
Japonica). Моришима
приписывал ликорпну состав С32H3208N2.
Еще ранее (1877) Джеррард получил из луковиц Narcissus
pstudo-narcissus
L. алкалоид,
названный им нарциссином. Оба эти алкалоида оказались идентичными, и за ними
было оставлено название ликорина. Гортер (1919-1920) нашел этот же алкалоид в
ряде растении сем. амариллисовых, а именно:Buphane
disticha
Herb., Zephyranthes
rosea Lidl.,
Crinum asiaticum
L., С.giganteum
Andr., С. pratense
Herb., Amaryllis
belladonna
L.,Narcissus
orientalis
L.
В 1946 г. Н.Ф. Проскурнина и Л.Я. Арешкина
выделили из луковиц подснежника Воронова -Galanthus
woronowii
A.Los.
алкалоид, названный галантидином, оказавшимся идентичным с ликорином. Этот
алкалоид найден в последнее время Р.А. Коноваловой в луковицах белоцветника
летнего -Leucojum
aestivum
L. Наконец в 1950 г.
Н.Ф. Проскурнина и Н. Исмаилов выделили ликорин из Sternbergia
Fischeriana (Herb.)
Roem.и S.lutea
(L.) Ker-Gawl.
Физические свойства
Ликорин - кристаллизуется из спирта в призмах,
темп. пл.11 ^ 280°C
(с разлож.), [α]D
=-129° (С2Н5ОН). Нерастворим в воде, трудно растворим в
спирте и эфире. Дает хорошо кристаллизующиеся соли: хлор гидрат (иглы), темп.
пл. 217°С, [α]D
= +43°, и пикрат, темп. пл. 196°C.
Химические свойства и строение
Ликорин С16Н17O4N
- третичное основание, не содержит группы >NСН3.
Два кислородных атома находятся в виде метилендиоксигруппы, а два - в виде двух
гидроксильных групп, что подтверждается получением диацетильного производного.
Ликорин - ненасыщенное основание, переходящее
при каталитическом гидрировании в дигидроликорин. При окислении ликорина
перман-ганатом калия получается гидрастовая кислота, что указывает на положение
метилендиокси-группы в ароматическом кольце.
Получение фенантридина при перегонке ликорина с
цинковой пылью дало ценное указание на то, что ликорин является производным фе-
нантридина.
Третичный характер азота, отсутствие группы >NСН3
и двойной связи у азота позволили предположить, что азот в ликорине стоит в
узловой точке двух конденсированных колец, участвуя в образовании четвертого
цикла с двумя недостающими углеродными атомами. Это было подтверждено изучением
продуктов распада ликорина по Гофману и Эмде.
На основании этих и других данных, установленных
Кондо сотрудниками, для ликорина была предложена следующая формула:

12. Галантамин С17Н21O3N
Физические свойства
Галантамин - кристаллизуется из воды или
бензола, темп, пл. 117-119°С, [α]D=
-118,8° (С2Н5ОН). Легко растворим в спирте, ацетоне и
хлороформе, трудно растворим в бензоле, эфире и воде. Дает хорошо
кристаллизующиеся соли: хлоргидрат, темп. пл. 256-257°C,
бромгидрат, плавится при 246-247°C,
перхлорат, темп. пл. 223-224°C,
и нитрат, темп. пл. 224-225°C.
Химические свойства и строение
Галантамин С17Н21O3N-содержит
метилимидную, метоксильную и гидроксильную группы. Дает моноацетильное
производное, темп. пл. 129-- 130°С. Третий атом кислорода находится в
неактивной форме. Формула галантамина может быть развернута в С15Н14(NСН3)(ОСН3)(ОН)(O-).
При каталитическом гидрировании галантамина
медленно поглощаются два атома водорода, образуя дигидросоединение, темп. пл.
116- 118°С . Галантамин дает иодметилат, темп. пл. 278-279°С, [α]D=
- 94,5° (в воде). Подвергая иодметилат гофманскому распаду при нагревании со
щелочью, получают дес-N-метилгалантамин
С18Н23OзN,
темп. пл. 80-82°C. При
повторном гофманском распаде получается неизмененное вещество.
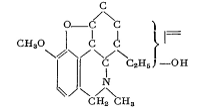
Свойства галантамина и его совместное нахождение
в растении с галантином и ликорином позволили Н. Ф. Проскурниной и А. П.
Яковлевой рассматривать галантамин как производное 1-этил-1N-метилфенантридина:
13. Гиндарин C21H25O4N
Получен из луковиц растения Stephania
glabra Miers.
сем. Menispermaceae
(луносемянниковые).
Физические свойства
Кристаллизуется из спирта, петролейного эфира и
ацетона, плавится при 147°С. Дает рая кристаллических солей, плавящихся с
разложением.
Строение:

Стефаглабрин С35H39O6N2
Физические и химические свойства
Температура плавления - 159°С, [α]D=
-91,5°.
Содержит три двойные связи, две метоксильные и одну метилендиокси-группы; оба
атома азота третичны и каждый связан с одной метильной группой [C30H25O2(OCH3)2(O2CH2)N(CH3)2].
Строение:

14. Трава Мачка Желтого - Herba
Glaucii Flavi
Мачок желтый - Glaucium
flavum Crantz
Сем. маковые - Papaveraceae
Ботаническая характеристика. Одно-, дву- или
многолетнее травянистое растение с крупными густоопушенными лировидно-перисторассеченными
прикорневыми листьями, собранными в розетку. Стебли 20-50 см высотой с
очередными перистолопастными стеблеобъемлющими листьями. Цветки одиночные,
правильные, 2-5 см в диаметре, верхушечные или пазушные. Чашелистиков 2, опадающих
при распускании цветка, лепестков 4, блестящих, желтых. Плод - стручковидная
линейная коробочка длиной 15-25 см. Семена почковидные, коричневые или почти
черные. Все части растения содержат млечный сок. Цветет в мае - июне, плоды
созревают в августе - сентябре.
Распространение. Мачок желтый встречается только
на побережье Черного моря - в Крыму и на Кавказе. Заготовки сырья в природных
зарослях экономически нецелесообразны, так как растение везде встречается
рассеянно. Оно успешно введено в культуру в России (Краснодарский край), на
Украине (южные районы, Крым), Молдавии и в Южном Казахстане.
Местообитание. Растет на хорошо дренированных
песчаных почвах, галечниках, реже на скалистых и щебнистых склонах. Иногда
встречается на залежах. Растение занесено в Красную книгу.
Химический состав. Все части растения содержат
алкалоиды - производные изохинолина. Сумма алкалоидов в фазу массового цветения
мачка желтого достигает 4 %, половину составляет глауцин. Найдены также
флавоноиды (рутин).
Фармакологические свойства. Глауцин
характеризуется выраженной противокашлевой активностью. Он угнетает кашлевой
центр.
Применение. Сырье используют для получения
препарата «Глауцина гидрохлорид», применяемого в качестве противокашлевого
средства. По своей противокашлевой активности глауцин превосходит кодеин и
вместе с тем не оказывает побочного действия, свойственного кодеину.
Трава мачка желтого также входит в состав
антиалкогольного сбора «Стопал».
. Глауцина гидрохлорид (Glaucini
hydrochloridum)
Фармакотерапевтическая группа. Противокашлевое,
альфа-адреноблокирующее средство.
СИНОНИМЫ: Глаувент, Glaucinum
hydrochloricum,Tussiglaucin.
Белый или светло-кремовый мелкокристаллический
порошок. Под воздействием света окраска усиливается. Растворим в воде, трудно -
в спирте.
Оказывает противокашлевое действие, связанное с
избирательным угнетением центральных механизмов кашлевого рефлекса. В отличие
от кодеина не угнетает центр дыхания, не оказывает тормозящего влияния на
моторику кишечника, не вызывает привыкания и пристрастия.
Применяют как противокашлевое средство при
заболеваниях легких и верхних дыхательных путей.
Назначают внутрь: взрослым по 0,05 г (50 мг) 2-3
раза в день после еды, детям - по 0,01-0,03 г (10-30 мг).
Препарат обычно хорошо переносится, в отдельных
случаях отмечаются головокружение, тошнота. Может наблюдаться умеренное
гипотензивное действие, связанное с адренолитическими свойствами препарата, в
связи с чем его не следует назначать при сниженном артериальном давлении и
инфаркте миокарда. В отличие от кодеина глауцин не угнетает дыхательный центр,
не подавляет двигательную активность кишечника, не вызывает привыкания и
лекарственной зависимости.
Форма выпуска: таблетки, покрытые оболочкой, по
0,05 г(50 мг) в упаковке по 20 штук.
Хранение: список Б.
. Бронхолитин (Broncholytinum)
Является комбинированным препаратом, содержащим
глауцин.
Выпускается в виде сиропа, в 125 г которого
содержится глауцина гидрохлорида 0,125 г, эфедрина гидрохлорида 0,1 г, масла
шалфея и лимонной кислоты по 0,125 г.
Применяют как противокашлевое и
бронхорасширяющее средство при острых и хронических бронхитах, астмоидных
состояниях.
Назначают взрослым по 1 столовой ложке 3-4 раза
в день, детям старше 3 лет - по 1 чайной ложке 3 раза в день, детям старше 10
лет - по 2 чайные ложки 3 раза в день.
Форма выпуска: во флаконах по 125 г.
Хранение: список Б.
. Корни Ипекакуаны - Radices
Ipecacuanhae
Ипекакуана - Cephaelis
ipecacuanha (Brot.)Tussac
Сем. мареновые - Rubiaceae
Ботаническая характеристика. Ипекакуана -
кустарничек с серо-бурым тонким горизонтальным корневищем, от которого отходят
корни с неравномерно утолщенной корой («чётковидные»). Надземная часть
представлена тонким до 30-40 см высоты стеблем с несколькими парами супротивных
вечнозеленых, эллиптических или ланцетных цельнокрайных. Цветки пятичленные,
белые, мелкие, собранные в головчатое соцветие. Плод - сочная костянка.
Распространение. Произрастает во влажных
тропических лесах Бразилии и Восточной Боливии. Культивируют в тропиках Индии,
Юго-Восточной Азии, Южной Америки. Разработана культура клеток корней
ипекакуаны.
Химический состав. Корни ипекакуаны содержат
2-2,5% (4%) изохинолиновых алкалоидов, главный - эметин (70%), цефалин и др.
Кроме того, содержится до 2 % сапонинов,
гликозид ипекакуанин, крахмал.
Проведены исследования, в ходе которых было
установлено, что возможно увеличение содержания эметина в культуре клеток до 24
раз, по сравнению с исходным содержанием, путем добавления к субстрату L-диоксифенилаланина
(L-ДОФА) и L-метионина.
Применение. Корни в малых дозах применяются в
форме настоя или отвара (1:400) как отхаркивающее средство, в больших дозах
(0,5-2 г) - как рвотное. Эметина гидрохлорид используется в виде инъекционных
растворов для лечения амебной дизентерии. Есть данные об эффективности лечения
опоясывающего лишая эметина гидрохлоридом.
. Эметина гидрохлорид (Emetini
hydrochloridum)
Белый кристаллический порошок, без запаха,
горький на вкус. Легко растворим в воде (1 : 8) и спирте.
Применяют при амебной дизентерии (при острых
кишечных проявлениях). Вводят под кожу или в мышцы взрослым по 1,5 мл 1 %
раствора 2 раза в сутки. Детям до 6 мес. эметин не назначают.
Продолжительность цикла лечения от 4 до 6 сут.,
максимум 7-8 сут. Когда стул принимает оформленный или полуоформленный вид,
введение эметина прекращают и переходят на другие противоамебные препараты.
При первых острых проявлениях амебной дизентерии
обычно достаточно 1-2 циклов лечения эметином.
Ввиду кумулятивных свойств эметина повторять
цикл лечения этим препаратом можно не ранее чем через 7-10 сут. после окончания
предыдущего цикла.
Имеются данные об эффективности эметина
гидрохлорида при лечении опоясывающего герпеса: вводили внутримышечно по 2 мл 1
% раствора 2 раза в день (утром и вечером). При раннем начале лечения быстро (в
течение 1-2 сут.) прекращались боли и высыпания.
Инъекции эметина обычно хорошо переносятся. При
передозировке могут наблюдаться слабость, тошнота, рвота, боли в мышцах
конечностей, сердечная слабость, полиневриты. При выраженных побочных явлениях
лечение эметином необходимо прекратить.
Формы выпуска: порошок; 1 % раствор в ампулах по
1 мл.
Хранение: список Б.
. Коробочки Мака - Capita
Papaveris
Мак снотворный
- Papaver somniferum L.
Сем. маковые - Papaveraceae
Ботаническая характеристика. Однолетнее
культивируемое травянистое растение высотой 1-1,5 м со стержневой корневой
системой. Стебель прямостоячий, в верхней части ветвистый, густооблиственный,
округлый, голый, покрытый сизоватым восковым налетом. Прикорневые листья
короткочерешковые, эллиптические или ланцетные, по краю крупнопильчатые или
надрезанно-лопастные с острозубчатым краем, длиной 20-30 см; стеблевые -
широкоэллиптические или яйцевидные, 10-20 см длиной, с неравномерно
крупнозубчатым краем, сидячие, стеблеобъемлющие, голые, голубовато-зеленые
из-за воскового налета. Цветки одиночные на верхушках побегов, с двойным
правильным околоцветником; бутоны до раскрытия цветков поникшие, голые. Чашечка
из 2 кожистых чашелистиков, опадающих при распускании цветка; венчик
раздельнолепестный, состоит из 4 широких лепестков различной окраски (от белой
до темно-фиолетовой), при основании лепестков имеется большое темное пятно.
Тычинок много, завязь верхняя. Плод - коробочка яйцевидной или почти шаровидной
формы 2-5 см в диаметре, открывается дырочками; наверху имеется разросшееся
сидячее многолучевое деревянистое рыльце в виде диска. Коробочка сначала
зеленого цвета, сочная, в зрелом виде соломенно-желтая, сухая. Семена
многочисленные, очень мелкие, почковидные, от почти белого до сизо-черного
цвета. Все части растения содержат белый млечный сок, содержащий алкалоиды, его
больше всего в незрелых коробочках. Семена мака съедобны, не содержат млечного
сока и алкалоидов. Цветет в июне, семена созревают в июле - сентябре.
Распространение. В диком виде не встречается.
Родина растения неизвестна.
Мак снотворный как масличное и лекарственное
растение известен с глубокой древности. Впервые его начали возделывать в Малой
Азии и Греции, затем Индии, Иране, Турции, Китае и других странах. С
доисторических времен мак снотворный возделывался с различными целями: в одних
странах мак культивировался главным образом для получения семян, в других - с
целью получения опия, представляющего собой высушенный млечный сок незрелых
коробочек. Различают масличные и опийные сорта мака снотворного. Масличные
сорта отличаются сравнительно небольшими коробочками и голубыми, серыми или
почти черными семенами, опийные - крупными коробочками и светло-желтыми или
белыми семенами.
В СССР мак снотворный для лекарственных целей
начали возделывать в 70-х годах XX
в. в Киргизии. Основные посевы опийного мака находились в Киргизии и
Казахстане. Масличный мак до революции культивировали на Украине и в
Воронежской губернии. Кроме указанных районов, его возделывали в Башкирии,
Самарской области, на юге Западной Сибири и в Краснодарском крае.
В настоящее время решениями международных
организаций культура опийного мака запрещена повсеместно, кроме района
«золотого треугольника» в Юго-Восточной Азии (Юго-Западный Китай, Бирма и
Таиланд).
Химический состав. В начале созревания плодов в
воздушно-сухой надземной части содержится до 20 % сухого млечного сока - опия.
В нем в виде солей меконовой и серной кислот содержится 10-25 % суммы
изохинолиновых алкалоидов, около половины которой составляет морфин (остальную
часть суммы алкалоидов составляют кодеин, папаверин, тебаин и др.). В зрелых
коробочках масличных сортов содержание морфина составляет 0,3-0,5 %.
Применение. Коробочки мака снотворного и опий
служат сырьем для получения алкалоидов морфина и кодеина. Морфин оказывает
сильное болеутоляющее действие и является наркотическим анальгетиком,
применяется при травмах, различных заболеваниях, сопровождающихся сильными
болями (инфаркт миокарда, злокачественные новообразования и др.). Кодеин
уменьшает возбудимость дыхательного центра, применяется в качестве
противокашлевого средства, входит в состав комплексных препаратов. При
многократном применении препаратов алкалоидов мака может возникнуть явление
привыкания (наркомания). Из тебаина получают различные производные,
используемые как наркотические анальгетики.
Семена мака широко используются для изготовления
всевозможных кондитерских изделий; содержат до 50 % жирного масла, уступая
только кунжуту и клещевине.
. Морфин (Morphinum)
Выпускается в виде гидрохлорида и сульфата.
Синонимы:
Morphine hydrochloride, Morphinum hydrochloricum.
Белые игольчатые кристаллы или белый
кристаллический порошок, слегка желтеющий при хранении. Медленно растворим в
воде, трудно растворим в спирте (1: 50). Несовместим со щелочами.
Является основным представителем группы
наркотических анальгетиков. Отличается сильным болеутоляющим действием. Понижая
возбудимость болевых центров, оказывает также противошоковое действие при
травмах. В больших дозах вызывает снотворный эффект, который наиболее выражен
при нарушениях сна, связанных с болевыми ощущениями.
Морфин вызывает выраженную эйфорию, и при его
повторном применении быстро развивается болезненное пристрастие (морфинизм).
Морфин оказывает тормозящее влияние на условные
рефлексы, понижает суммационную способность ЦНС, усиливает действие
наркотических, снотворных и местноанестезирующих средств.
Понижает возбудимость кашлевого центра.
Морфин вызывает возбуждение центра блуждающих
нервов с появлением брадикардии.
В результате активации нейронов
глазодвигательных нервов под влиянием морфина у людей появляется миоз. Эти
эффекты снимаются атропином или другими холинолитиками.
Рвота, которая может наблюдаться при применении
морфина, связана с возбуждением хеморецепторных пусковых (триггерных) зон
продолговатого мозга. Морфин угнетает рвотный центр, поэтому повторные дозы
морфина и рвотные средства, вводимые после морфина, рвоты не вызывают.
Под влиянием морфина повышается тонус гладкой
мускулатуры внутренних органов: сфинктеров желудочно-кишечного тракта,
мускулатуры антральной части желудка, тонкого и толстого отделов кишечника,
вследствие чего ослабляется перистальтика, замедляется продвижение пищевых
масс, что приводит к развитию запора. Может увеличиваться тонус мускулатуры
бронхов с развитием бронхоспазма.
Тормозится секреторная активность
желудочно-кишечного тракта.
Основной обмен и температура тела под влиянием
морфина понижаются.
Характерным для действия морфина является
угнетение дыхательного центра. Малые дозы вызывают урежение и увеличение
глубины дыхательных движений; большие дозы обеспечивают дальнейшее урежение и
уменьшение глубины дыхания со снижением легочной вентиляции. Токсические дозы
вызывают появление периодического дыхания типа Чейна-Стокса и последующую
остановку дыхания.
Опиоидные анальгетики занимают второе место
среди препаратов, вызывающих при аналгезии в качестве побочного эффекта острую
аллергическую реакцию. Анафилаксия при анестезии приводит к летальному исходу в
3-9% случаев. Недавно было установлено, что в организме человека вырабатываются
специфические антитела (IgE)
к опиоидам. Для определения точности диагностики антител к морфину, кодеину,
рокуронию, а также жирорастворимой и водорастворимой фракциям семян мака
снотворного, были проведены клинические исследования с участием 203 больных. В
ходе испытаний было доказано, что повышенную чувствительность к опиоидам у
пациентов можно диагностировать методом обычных кожных проб, что позволит
снизить частоту возникновения анафилактических реакций при аналгезии,
приводящих к летальному исходу. Также было установлено, что в группу особого
риска возникновения гиперчувствительности при введении опиоидов входят люди, у
которых аллергия на табак, при этом пыльцевая аллергия, столь широко
распространенная, не является фактором риска сенсибилизации.
Возможность развития наркомании и угнетение
дыхания являются крупными недостатками морфина, ограничивающими в ряде случаев
использование его мощных анальгезирующих свойств.
Применяют морфин при подготовке к операциям и в
послеоперационном периоде, при травмах и различных заболеваниях,
сопровождающихся сильными болевыми ощущениями (злокачественные новообразования,
инфаркт миокарда и др.), при бессоннице, связанной с сильными болями, иногда
при сильном кашле, сильной одышке, обусловленной острой сердечной
недостаточностью.
Для обезболивания родов морфин обычно не
применяют, так как он проходит через плацентарный барьер и может вызвать
угнетение дыхания у новорожденного.
Морфином иногда пользуются в рентгенологической
практике при исследовании желудка, двенадцатиперстной кишки, желчного пузыря.
Введение морфина повышает тонус мышц желудка, усиливает его перистальтику,
ускоряет его опорожнение и вызывает растяжение двенадцатиперстной кишки
контрастным веществом. Это способствует выявлению язв и опухолей желудка, язв
двенадцатиперстной кишки. Вызываемое морфином сокращение мышцы сфинктера Одди
создает благоприятные условия для рентгенологического исследования желчного
пузыря.
Назначают под кожу (взрослым обычно по 1 мл 1 %
раствора) и внутрь (0,01-0,02 г). Детям старше 2 лет назначают в зависимости от
возраста по 0,001-0,005 г на прием. Детям до 2 лет морфин не назначают.
При применении морфина возможны тошнота, рвота,
угнетение дыхания и другие побочные явления, связанные с особенностями его
влияния на разные органы и системы организма. Для уменьшения побочных явлений
часто назначают вместе с морфином атропин, метацин или другие холинолитики.
Морфин противопоказан при общем сильном
истощении, недостаточности дыхательного центра.
Осторожность необходима при применении морфина у
больных старческого возраста (замедляется обмен и выведение морфина; повышается
содержание морфина в плазме крови).
Формы выпуска: таблетки по 0,01 г; 1 % раствор в
ампулах и шприц-тюбиках по 1 мл.
21. Морфилонг (Morphilongum)
Пролонгированная лекарственная форма морфина
только для внутримышечного введения.
Представляет собой 0,5 % раствор морфина
гидрохлорида в 30 % водном растворе поливинилпирролидона (содержит в 1 мл
0,0055 г (5,5 мг) морфина).
Прозрачная вязкая жидкость желтого цвета со
слабым специфическим запахом поливинилпирролидона, растворимая в воде и спирте.
Применяют у взрослых и детей старше 7 лет в послеоперационном
периоде и при выраженном болевом синдроме у онкологических больных.
Вводят внутримышечно один раз в сутки из расчета
0,1 мл на 1 кг массы тела.
Возможные побочные явления, меры
предосторожности и противопоказания такие же, как для морфина.
Форма выпуска: в ампулах темного стекла по 2 мл.
22. Омнопон
(Omnoponum)
Синонимы:
Dormopon, Opialum, Pantopon, Papaveratum, Sompon.
Смесь гидрохлоридов алкалоидов опия; содержит 48
50 % морфина и 32-35 % других алкалоидов.
Порошок от кремового до коричневато-желтого
цвета. Растворим в воде (1:15), трудно растворим в спирте (1:50). Водный
раствор при взбалтывании сильно пенится.
Растворы омнопона содержат в 1 мл 1 % раствора
(и соответственно в 1 мл 2 % раствора): морфина гидрохлорида 6,7 мг (13,4 мг),
наркотина 2,7 мг (5,4 мг), папаверина гидрохлорида 0,36 мг (0,72 мг), кодеина
0,72 мг (1,44 мг), тебаина 0,05 мг (0,1 мг).
Показания те же, что и для морфина. Омнопон
иногда лучше переносится, чем морфин, реже вызывает развитое спазмов гладкой
мускулатуры.
Назначают под кожу (взрослым обычно по 1 мл 1 %
или 2 % раствора), внутрь (0,01-0,02 г на прием). Детям старше 2 лет назначают
по 0,001-0,0075 г на прием в зависимости от возраста.
При применении омнопона могут развиться
привыкание и болезненное пристрастие. Противопоказания такие же, как для
морфина.
Форма выпуска: 1 % и 2 % растворы в ампулах по 1
мл.
. Кодеин (Codeinum)
Метилморфин. Алкалоид, содержащийся в опии;
получается также полусинтетическим путем.
Бесцветные кристаллы или белый кристаллический порошок
без запаха, горького вкуса. На воздухе выветривается. Медленно и мало растворим
в холодной воде (1 : 150), растворим (1 : 17) в горячей воде, легко растворим в
спирте.
По характеру действия кодеин близок к морфину,
но болеутоляющие свойства выражены слабее; сильно выражена способность
уменьшать возбудимость кашлевого центра. В меньшей степени, чем морфин,
угнетает дыхание и тормозит деятельность желудочно-кишечного тракта, однако
может вызвать запор.
При повторном применении кодеина могут
наблюдаться явления пристрастия.
Назначают главным образом для успокоения кашля.
В сочетании с ненаркотическими анальгетиками (анальгин), кофеином,
фенобарбиталом применяют при головных болях, невралгиях и т. п.
Назначают внутрь в порошках, таблетках и
растворах взрослым по 0,01-0,02 г на прием; детям старше 2 лет по 0,001-0,0075
г на прием в зависимости от возраста.
Детям до 2 лет кодеин не назначают.
Формы выпуска: порошок и таблетки по 0,015 г (с
гидрокарбонатом натрия).
Входит в состав микстуры Бехтерева, применяемой
в качестве успокаивающего средства.
Кодеин входит в состав следующих комбинированных
таблеток:
Таблетки «Кодтерпин» (Tabulettae
«Codterpinum»). Состав: кодеина
0,015 г, натрия гидрокарбоната и терпин-гидрата по 0,25 г.
«Таблетки
от
кашля»
(Tabulettae contra tussim). Состав: кодеина 0,02 г, травы
термопсиса в порошке 0,01 г, натрия гидрокарбоната и корня солодки в порошке по
0,2 г.
. Кодеина фосфат (Codeini
phosphas)
Синонимы: Codeinum
phosphoricum, Codeine
phosphate.
Белый кристаллический порошок без запаха,
горьковатого вкуса. На воздухе выветривается. Легко растворим в воде (1 : 3,5),
мало - в спирте.
По характеру действия и показаниям к применению
аналогичен кодеину (содержит около 80 % кодеина основания), допускается к
применению у детей более раннего возраста и в несколько больших дозах.
Назначают детям старше 6 мес. по 0,002-0,01 г на
прием в зависимости от возраста. Взрослым назначают в тех же дозах, что кодеин
(основание).
Форма выпуска: порошок.
изохинолиновый алкалоид
лекарственный фармакологический
25. Клубни с корнями Стефании Гладкой - Tubera
cum radicibus
Stephaniae
Glabrae
Стефания гладкая
- Stephania glabra (Roxb.) Miers
Сем. луносемянниковые - Menispermaceae
Ботаническая характеристика. Двудомная
многолетняя травянистая тропическая лиана, в культуре достигающая 5-8 м в
длину. Подземные органы представлены почти круглым клубнем с отходящими от него
в нижней части мочковатыми корнями. Масса одного клубня может достигать 20-30
кг (в трехлетней культуре - 800-1500 г). Стебель лазящий, с возрастом у
основания одревесневающий. Листья длинночерешковые, очередные, щитовидные,
округлые, остроконечные, голые; длина листовой пластинки 15-20 см, черешка - до
40 см. Цветки раздельнополые, зеленовато-желтого цвета, собраны в повисающие
зонтиковидные соцветия. Мужские цветки состоят из 6 свободных чашелистиков и 3
обратнояйцевидных мясистых лепестков; женские цветки имеют 3 чашелистика и 3
лепестка. Плод - шаровидная костянка с сочным околоплодником; при созревании
сначала желтеет, затем становится красной. В условиях культуры на Черноморском
побережье начало цветения мужских соцветий наблюдается в первой половине июля,
женских - в середине июля. Начало созревания плодов - в середине сентября. При
первых заморозках (до -2 °С) надземная масса гибнет, вегетация прекращается.
Распространение. Произрастает в тропических и
субтропических горных районах Южного Китая, Японии, Бирмы, Вьетнама, Индии.
Была разработана техника возделывания в субтропиках Закавказья по типу
хозяйственно-однолетней пересадочной культуры. Основная масса сырья закупается
в Индии.
Химический состав. В клубнях стефании гладкой
накапливается до 6-8 % алкалоидов, производных изохинолина. В клубнях
индийского происхождения до 30 % приходится на гиндарин, 15-18 % составляет
стефаглабрин (стефарин). Клубни, выращенные в Закавказье, содержат около 6-7,5
% суммы алкалоидов, из них около 30 % составляет гиндарин и около 10 % циклеанин;
другие алкалоиды содержатся в меньших количествах.
Применение. Препарат «Стефаглабрина сульфат»
применяют в качестве антихолинэстеразного средства при боковом амиотрофическом
склерозе, миопатии у взрослых, парезах лицевого нерва и других заболеваниях
периферической нервной системы. Ранее выпускался препарат «Гиндарина
гидрохлорид», оказывающий седативное, легкое снотворное и гипотензивное
действие и применявшийся при функциональных расстройствах центральной нервной
системы.
. Стефаглабрина Сульфат (Stephaglabrini
sulfas)
Белый с серовато-розоватым оттенком
кристаллический порошок. Малорастворим в воде и спирте.
Обладает антихолинэстеразной активностью,
ингибируя истинную и ложную холинэстеразу.
Предложен для применения при заболеваниях
периферической нервной системы: миопатии (у взрослых), боковом амиотрофическом
склерозе, парезах лицевого нерва и др.
Вводят внутримышечно по 1-2 мл 0,25 % водного
раствора 2 раза вдень. Курс лечения 20-30 дней.
Противопоказания такие же, как для других
антихолинэстеразных препаратов.
Форма выпуска: 0,25 % раствор в ампулах по 1 мл
(2,5 мг).
Хранение: список Б.
27. Листья Унгернии Виктора - Folia
Ungerniae
Victoris
Унгерния Виктора
- Ungernia victoris Vved. ex Artjushenko
Листья Унгернии
Северцова
Резаные
- Folia Ungerniae Sewertzowii Concisa
Унгерния Северцова
- Ungernia sewertzowii (Regel) В.
Fedtsch.
Сем. амариллисовые - Amaryllidaceae
Ботаническая характеристика. Унгерния Виктора -
многолетнее луковичное растение. Луковица яйцевидная, 7-12 см в диаметре,
покрыта темно-коричневыми или черно-бурыми пленчатыми чешуями, вытянутыми в
длинную (до 17 см) шейку. Донце луковицы хорошо развито (длиной 2-3 см и такой
же толщины), от него отходят желто-розовые сочные ломкие придаточные корни
толщиной 0,3-0,4 см, длиной 10-25 см. Листья расположены двурядно, сочные,
мясистые, гладкие, линейные, на верхушке туповатые, длиной 20-40 см, шириной
1-4 см; начинают отрастать в конце февраля. Через 2-2,5 месяца развивается
сплюснутый цветонос высотой 12-30 см, заканчивающийся почти односторонним
зонтиковидным соцветием. Соцветие состоит из 2-11 почти правильных цветков.
Околоцветник воронковидный желтовато-розовый, с внутренней стороны с
розово-пурпуровой полоской. Плод - трехлопастная вздутая коробочка, 2-3 см в
диаметре. Цветет в конце июля - начале августа, плоды созревают в сентябре.
Унгерния Северцова - многолетнее луковичное
растение. Луковица продолговато-яйцевидная, довольно мощная, толщиной 5-10,
реже до 12 см, с многочисленными пленчатыми, обычно угольно-черными наружными
чешуями. Донце луковицы хорошо развито, от него отходят желто-розовые сочные,
мясистые, ломкие корни длиной до 10-50 см. Листья в количестве от 4 до 12,
расположены двурядно, линейные, почти равные, наружные длиной около 30-45 см,
шириной 1,5-2 см, сизые, гладкие, слегка скрученные по оси. Полного развития
листья достигают в апреле, в конце мая они засыхают. Через 2,5 месяца после
этого развивается цилиндрический цветонос высотой 7,5-45 см, несущий
зонтиковидное соцветие из 5-12 цветков. Околоцветник воронковидный с 6
узколанцетными островатыми кирпично-красными листочками. Отгиб длиной 20-25 мм,
в 3 раза длиннее трубки. Плод - трехлопастная коробочка с широкосердцевидными
створками. Цветет в начале августа, плоды созревают в сентябре.
Распространение и местообитание. Унгерния
Виктора - эндемик Средней Азии, встречается только в предгорьях Гиссарского
хребта на высоте 800-2500 м над уровнем моря. Обычно растет небольшими
группами, на старых стойбищах часто образует почти сплошные заросли. Ведутся
работы по введению растения в культуру в местах его естественного
произрастания. Включена в Красную книгу СССР (1978).
Унгерния Северцова - эндемик Средней Азии,
произрастает только в Западном Тянь-Шане на высоте 800-2700 м над уровнем моря,
в предгорьях и в среднем поясе гор. Приурочена к эфемерово-пырейным степям, где
растет разреженными зарослями. Проводятся работы по введению растения в
культуру в местах его естественного произрастания. Заготовки проводятся в
Киргизии и Казахстане.
Химический состав. Луковицы и листья обоих видов
унгернии содержат до 0,5 % алкалоидов, основными являются галантамин и ликорин.
В унгернии Виктора в основном содержится галантамин (около 0,15 %),
сопровождающийся ликорином, горденином, тацеттином и др. В унгернии Северцова
преобладает ликорин (до 0,8 %), остальные алкалоиды присутствуют в значительно
меньшем количестве.
Применение. Препарат «Галантамина гидробромид»,
получаемый из листьев унгернии Виктора, применяют для лечения остаточных
явлений полиомиелита, полиневрита, радикулита, а также при травматических
повреждениях чувствительных и двигательных нервов.
Препарат «Ликорина гидрохлорид», получаемый из
листьев унгернии Северцова, применяют в качестве отхаркивающего средства при
хронических и острых воспалительных процессах в легких, бронхах, при
бронхиальной астме.
. Галантамин (Galanthaminum)
Выпускается в виде гидробромида.
Синонимы: Нивалин, Nivalinum.
Белый мелкокристаллический порошок горького
вкуса. Трудно растворим в воде, практически нерастворим в спирте.
По фармакологическим свойствам является сильным
(обратимым) ингибитором холинэстеразы, повышает чувствительность организма к
ацетилхолину.
Облегчает проведение возбуждения в
нервно-мышечных синапсах и восстанавливает нервно-мышечную проводимость,
блокированную курареподобными препаратами антидеполяризуюшего действия
(тубокурарином и др.); усиливает действие деполяризующих миорелаксантов
(дитилина).
Вызывает повышение тонуса гладких мышц и
усиление секреции пищеварительных и потовых желез. Подобно физостигмину,
вызывает сужение зрачка; однако при введении раствора галантамина в
конъюнктивальный мешок может наблюдаться временный отек конъюнктивы.
Периферические мускариноподобные эффекты
галантамина снимаются холинолитическими веществами (атропином и др.), а
никотиноподобные - курареподобными и ганглиоблокирующими веществами.
Сравнительно с физостигмином галантамин менее токсичен.
Галантамин проникает через гематоэнцефалический
барьер, в соответствующих дозах облегчает проведение импульсов в
холинергических синапсах ЦНС и усиливает процессы возбуждения.
Применяют галантамина гидробромид при миастении,
прогрессивной мышечной дистрофии, двигательных и чувствительных нарушениях,
связанных с невритами, полиневритами, радикулитами, радикулоневритами, при
остаточных явлениях после нарушения мозгового кровообращения, при психогенной
импотенции и другой патологии. В восстановительном периоде острого полиомиелита
и при детских церебральных параличах применение галантамина, особенно в
комплексе с другими мероприятиями (лечебная гимнастика, массаж и др.), приводит
к улучшению и восстановлению двигательных процессов и общему улучшению
состояния больных. По имеющимся данным, применение галантамина в комплексной
терапии при спастических формах церебрального паралича не только улучшает нервно-мышечную
проводимость и увеличивает сократительную способность мышц, но и положительно
влияет на мнестические функции.
Галантамин можно применять при атонии кишечника
и мочевого пузыря, а также для функциональной рентгенодиагностики при
заболеваниях желудка и кишечника.
Дозы препарата устанавливают индивидуально в
зависимости от возраста больного, характера заболевания, эффективности и
переносимости препарата. Разовая доза для взрослых составляет обычно от 0,0025
г (2,5 мг) до 0,01 г (10 мг), т. е. 0,25-1 мл 1 % раствора. Вводят препарат под
кожу в виде водного раствора 1 -2 раза в сутки.
Как мощный антихолинэстеразный препарат
галантамин является эффективным антагонистом при отравлениях холинолитическими
веществами.
Как вещество, проникающее через гематоэнцефалический
барьер и стимулирующее центральные холинореактивные системы, галантамин стали в
последнее время применять за рубежом в комплексной терапии болезни Альцгеймера.
При правильном дозировании галантамин хорошо
переносится. При передозировке и индивидуальной повышенной чувствительности
возможны побочные явления в виде слюнотечения, брадикардии, головокружения и
др. В этих случаях следует уменьшить дозу. При необходимости применяют атропин
или другое холи политическое средство.
Галантамин, так же как и другие
антихолинэстеразные препараты, противопоказан при эпилепсии, гиперкинезах,
бронхиальной астме, стенокардии, брадикардии.
Форма выпуска: 0,1; 0,25; 0,5 и 1 % растворы в
ампулах по 1 мл.
Хранение: список А.
. Ликорина гидрохлорид (Lycorini
hydrochloridum)
Белый порошок с сероватым оттенком. Трудно
растворим в воде, мало - в спирте.
По основному действию ликорин близок к
апоморфину, являясь рвотным средством. В малых дозах оказывает отхаркивающее
действие.
Препарат предложен в качестве отхаркивающего
средства при хронических и острых воспалительных процессах в легких и бронхах.
Доза для взрослых внутрь 0,0001-0,0002 г (0,1 -
0,2 мг) 3-4 раза в день.
В больших дозах назначать ликорин не следует,
так как возможны тошнота и рвота.
Противопоказания такие же, как и для других
отхаркивающих и рвотных средств: открытые формы туберкулеза легких и другие
заболевания со склонностью к легочным кровотечениям, органические заболевания
ЦНС и сердечно-сосудистой системы, язвенная болезнь желудка и двенадцатиперстной
кишки, поражения пищевода со склонностью к кровотечениям.
Форма выпуска: таблетки по 0,0002 г (0,2 мг). В
состав каждой таблетки входит также 0,2 г натрия гидрокарбоната.
Хранение: список А.
Список литературы
1. Химия алкалоидов. А.П. Орехов,
2-е изд., М.; Изд. Академии Наук СССР, 1955.
. Фармакогнозия. Электронное учебное
пособие. Е.И. Гришина, И.С. Погодин, Е.А. Лукша, Омск, 2008.
. Атлас лекарственных растений СССР.
Под ред. Н.В. Цицина, М.; Государственное издательство медицинской литературы,
1962.
. Лекарственные средства: пособие
для врачей. Т.1,2, 14-е изд.; М.Д. Машковский, М.; ООО «Новая волна», 2002.
. Лекарственные растения, сырье и
фитопрепараты - учеб. пособие. Под ред.
С.Е.
Дмитрука,
Томск,
2004.
. T. Vetrichelvan, S. Kavimani,
R. Elango, and B. Jaykar Effect of l-dopa and l- methionine supplementation on
bioproduction of ementine in callus cultures of cephaelis ipecacuanha
7. Armentia A., Pineda F., Palacios
R., Martín-Gil F.J., Miguel A.S.,
Arenal J.J., Tejedor J., Tef B.M. Utility of opium seed extract tests in
preventing hypersensitivity reactions during surgery. Allergy Unit, Rio Hortega
University Hospital, UMDAI, Valladolid, Spain
. Лекарственные
растения,
сырьё
и
препараты.
Обухов
А.Н. - Краснодар: книжное издательство, 1962 - с.298