|
Цианобактерии
|
Anabaena
cylindrical Виды Gloeocapsa
|
|
Фототрофные
бактерии
|
Rhodospirillum
rubrum Rhodopseudomonas capsulata
|
|
Строгие
анаэробы
|
Clostridium
pasteurianum Desulfovibrio vulgaris
|
|
Облигатные
и факультативные анаэробы
|
Rhizobium
japonicum Frankia alni Klebsiella pneumonia Azotobacter vinelandii Bacillus
polymyxa Mycobacterium flavum Beijeerinckia indica Spirillum lipoferum
|
Ферментная система, катализирующая реакцию
восстановления N2 до аммиака, называется нитрогеназой. Нитрогеназа
состоит из двух белков, которые содержат железо, молибден, серу и кислотолабильный
сульфид. Молекула N2 является очень стабильной. Для осуществления
нитрогеназной реакции еще необходимо присутствие в качестве субстратов
восстановленного ферредоксина или флаводоксина. Восстановление молекулы N2
сопряжено с гидролизом 12 молекул ATP. Важно отметить, что биосинтез
нитрогеназного комплекса тормозится при накоплении аммиака, или снижении
количества ATP по отношению к ADP. Система фиксации азота должна быть
изолирована от молекулярного кислорода, который инактивирует нитрогеназу и
конкурирует за восстановитель. Стехиометрия суммарного процесса фиксации азота
следующая:
2+6e+12ATP+12H2O→2NH4++12ADP+12Pi+4H+
Нитрогеназа может также катализировать
восстановление соединений, содержащих тройные связи, например N2O,
NH3, HCN, и других нитрилов, а также ацетилен.
Симбиотическая фиксация азота происходит в
корневых клубеньках, которые образуются после инфицирования корневых волосков
микроорганизмами, относящимися к видам Rhizobium. Бактерии превращаются в
увеличенные в объеме клетки неправильной формы - бактероиды. Именно в них
происходит фиксация азота. N2 восстанавливается бактероидами до NH3,
который связывается глутамин-синтетазой, присутствующей в цитозоле растений.
Растение не только обеспечивает бактероиды органическими субстратами, но и
защищает нитрогеназу от действия кислорода. Азотфиксирующие клубеньки имеют
леггемоглобин, который служит переносчиком кислорода, подобно гемоглобину [5,
16, 24].
Нитраты и нитриты могут потребляться многими
бактериями в качестве источника азота (например, E.coli). При этом нитратный
азот восстанавливается при участии фермента нитратредуктазы, а затем при
участии нитритредуктазы нитрит восстанавливается до NH3.
Нитратредуктаза катализирует НАД∙Н2-зависимое восстановление:
3-
+НАД∙Н2→NO2-
+НАД+ +Н2О ,
в результате которого осуществляется перенос на
NO3- двух электронов. Нитритредуктаза катализирует шестиэлектронное
восстановление NO2- до NH3:
2-
+3НАД∙Н2+Н+→NH3+3НАД+
+2Н2О .
Ферменты нитратредуктаза и нитритредуктаза, как
и нитрогеназа, имеют в своем составе молибден, железо и кислотно-лабильный
сульфид. [1, 6, 16].
Некоторые бактерии восстанавливают нитрат только
до уровня нитрита, а другие могут его восстанавливать только до газообразного
азота. В ходе этого процесса, называемого денитрификацией, связанный азот
удаляется с высвобождением газообразного N2 в атмосферу [15].
Бактерии способны не только восстанавливать, но
и окислять нитриты. К таким видам относятся род Nitrobacter, Nitrospina,
Nitrococcus и Nitrospira. Все они являются аэробами, кроме Nitrobacter, которые
могут расти за счет анаэробного дыхания. В присутствии нитратов они образуют NO
и N2O. Известен один штамм Nitrobacter, способный окислять NO до
нитрата [26, 27].
Усвоение аммиака бактериями проходит легко, так
как атом азота аммиака имеет степень окисления -3, такой же, как и в
органических веществах в клетке. Существует три реакции ассимиляции NH3.
Одна из них приводит к образованию аминогруппы глутаминовой кислоты, вторая
ведет к появлению амидогруппы глутамина, а третья - к появлению карбамоилфосфата.
Из карбамоилфосфата синтезируется аспарагин и пиримидины. Другие два продукта
ассимиляции NH3 - непосредственные предшественники белков, а роль
аспарагина только в этом и заключается [15, 16].
Существуют бактерии, которые окисляют аммиак.
Этот процесс называется нитрификацией. Она проходит в два этапа: на первом
аммиак окисляется до нитрита, а на втором - до нитрата. Соответствующую
начальную реакцию катализирует монооксигеназа. К таким видам относят роды
Nitrosomonas, Nitrosococcus, Nitrosolobus, Nitrospira [15, 26, 28].
Следует отметить, что наиболее универсальным
источником азотного питания являются соли аммония. Аммиак при накоплении в
клетке вызывает ее гибель. При использовании солей (NH4)2SO4,
NH4Cl по мере их использования бактериями, среда подкисляется, что
не способствует нормальному развитию клеток.
Нитраты необходимы тем микроорганизмам, которые
боятся подкисления, так как при использовании NO3- остаются
ионы металлов Na+ и K+, которые создают щелочные условия
среды
Микроорганизмы, которые способные синтезировать
все необходимые им органические соединения (углеводы, аминокислоты и др.) из
глюкозы и солей аммония, называются прототрофами [3, 19].
2.2 Органические соединения азота
Существуют микроорганизмы, которые не способны
синтезировать все аминокислоты для своей клетки из солей аммония. Они
ассимилируют эти соединения и другие факторы роста в готовом виде из окружающей
среды или организма хозяина (человека, животного). Такие микроорганизмы
называют ауксотрофами. Ауксотрофами чаще всего являются патогенные или
условно-патогенные для человека микроорганизмы. Некоторые представители
пурпурных и зеленых бактерий растут на средах с мочевиной и аминокислотами.
Большими возможностями в отношении использования аминокислот обладают несерные
пурпурные бактерии [3, 25].
К органическим источникам азота относятся белки,
азотистые основания, пептон, пептиды, аминокислоты, мочевина. Белки усваивают
только те микроорганизмы, которые выделяют в среду протеиназы, расщепляющие
белковую молекулу до пептидов и аминокислот. Пептиды поступают в клетки и
гидролизуются внутриклеточными протеазами до аминокислот. Протеолитическую
активность бактерий обычно проверяют на питательных средах с желатином [7, 10,
11, 19].
Микроорганизмы, которые живут в почве, способны утилизировать
азот органических соединений. Минерализация органических веществ проводят
бактерии-сапрофиты. Азотистые соединения в присутствии воздуха разрушаются с
образованием аммиака. Часть азота ассимилируется самими микроорганизмами и
таким образом превращается в компоненты микробной клетки.
К аэробным микроорганизмам, которые окисляют
азотсодержащие вещества до полной минерализации, конечными продуктами которой
являются аммиак, CO2, H2O, H2S и другие
относят: Bac.mycoides, Bac.mesentericus, Bac.subtilis, Bac.megaterium, Serratia
marcescenc.
Разрушение белка в анаэробных условиях (гниение)
обычно не приводит к немедленному освобождению всего аминного азота в виде
аммиака. Некоторые аминокислоты превращаются в амины. К анаэробным
микроорганизмам относят Clostridium putrificum и Clostridium sporogenes [15,
22, 29].
Кислотный гидролизат казеина, пополненный
триптофаном, является столь же универсальным источником азота для всех
микробов, как и аммонийные соли [10].
Пептон для культивирования микроорганизмов
получают, обрабатывая белки ферментом пепсином. При этом разрывается только
часть пептидных связей. Пептон состоит примерно на 30% по весу из свободных
аминокислот, остальное составляют ди- и трипептиды, а также водорастворимые,
уже не осаждаемые нагреванием или кислотой полипептиды. Пептон добавляют в
основные питательные среды для культивирования, например мясо-пептонный бульон,
мясо-пептонный агар.
Более экономичный аналог мясо-пептонного бульона
- триптичный перевар по Хоттингеру. Для гидролиза белка в этом бульоне
используют панкреатин. [11, 12, 30].
Многие бактерии нуждаются в тех или других
аминокислотах (одной или нескольких), поскольку они не могут их самостоятельно
синтезировать, например клостридии - в лейцине, тирозине, а стрептококки - в
лейцине, аргинине. Палочки тифа и ботулизма неспособны синтезировать триптофан.
Глутаминовая кислота стимулирует рост гемолитических стрептококков, палочки
сибирской язвы, гонококка; цистин нужен для Proteus morganii и т.д. Обычно
микроорганизмы нуждаются в L-аминокислотах, но для некоторых из них характерна
потребность в D-аланине, необходимом, вероятно, для синтеза гликопептида
клеточной стенки. Концентрация аминокислот, обеспечивающие максимальный рост
ауксотрофов, обычно находятся в пределах 20-50 мкг на 1 мл.
Аминокислоты, которые не используются сразу,
подвергаются таким метаболическим превращениям: окислительное дезаминирование,
гидролитическое дезаминирование, переаминирование (трансаминирование),
декарбоксилирование. В большинстве случаев аминокислота сначала превращается в
соответствующую оксокислоту. Из аминокислот бактерии могут синтезировать не
только вещества для построения клетки, но и антибиотики: эдеин, грамицидин S,
бацитрацин и другие.
Стоит отметить, что имея полный набор
аминокислот в питательной среде, бактерии переключаются на аминогетеротрофный
тип питания (поглощают готовые аминокислоты), и не синтезируют аминокислоты
самостоятельно.
Хорошими источниками аминокислот, кроме мясных
бульонов и пептонов, являются кукурузный экстракт и дрожжевой экстракт из
клеток Saccharomyces cerevisiae. Эти источники дешевые, поэтому их можно
использовать на биотехнологических производствах [3, 5, 10, 19, 27, 31].
Разложение мочевины, выделяющейся с мочой,
осуществляют уробактерии, расщепляющие ее до аммиака, диоксида углерода и воды
[2].
Степень усвояемости источника азота определяется
тем, насколько он легко превращается в аммиак. Наиболее доступными являются
аммонийные соли и готовые аминокислоты. Иные источники менее доступны, но тем
не менее, бактерии могут усваивать и их [10].
Азот наряду с углеродом, водородом и кислородом
является одним из четырех основных элементов, участвующих в построении клетки.
Он необходим бактериям для синтеза жизненно важных молекул: нуклеиновых кислот,
белков, пуринов, пиримидинов, некоторых витаминов [1, 3, 6].
3.
Источники кислорода и водорода
Кислород и водород, наряду с азотом и углеродом
- основные компоненты органических соединений, содержащихся в тканях различных
организмов.
Источниками кислорода для микроорганизмов служит
O2, H2O, CO2 и органические соединения.
Источниками водорода служат H2, H2O
и органические соединения.
Данные элементы, вместе с углеродом, являются не
только основными компонентами клетки, но и служат важными субстратами для
получения микроорганизмами энергии [5].
3.1 Молекулярный кислород
По отношению к кислороду микроорганизмы делятся
на облигатных аэробов, факультативных анаэробов, аэротолерантных анаэробов и
облигатных анаэробов. Большинство микроорганизмов являются облигатными
аэробами, для их роста необходим молекулярный кислород. Отдельные виды могут
расти даже в атмосфере чистого кислорода. Наряду с этим есть микроорганизмы,
которые хотя и нуждаются в О2, но могут расти или лучше растут
только при низком его содержании (2-10%). Такие микроорганизмы называются
микроаэрофилами, а условия, в которых они растут, микроаэробными.
Факультативные анаэробы растут как в
присутствии, так и в отсутствии О2. Но в зависимости от условий
роста происходят изменения в их метаболизме, прежде всего в энергетических
процессах. Как правило, при наличии молекулярного кислорода такие
микроорганизмы переключаются на окисление субстрата с участием О2,
т.е. аэробное дыхание, поскольку оно более выгодно, чем получение энергии в
результате анаэробных процессов. Таковыми являются представители рода Bacillus,
Escherichia, Paracoccus denitrificans и ряд других.
К аэротолерантным анаэробам принадлежат многие
молочно-кислые бактерии, способны расти в присутствии молекулярного кислорода,
но при этом их метаболизм остается таким же, как и в анаэробных условиях. И в
том и в другом случае они осуществляют брожение.
Облигатные анаэробы не только не нуждаются для
роста в наличии молекулярного кислорода, но для многих видов он токсичен даже в
малой концентрации.
Стоит отметить, что в присутствии света кислород
может вызывать повреждающие эффекты, так как воздействие ультрафиолета на
компоненты клеток способствует образованию кислородных радикалов, разрушающих,
в том числе нуклеиновые кислоты [7, 28].
3.2 Диоксид углерода как источник кислорода
СО2 упоминался выше как источник
углерода для микроорганизмов. В качестве источника кислорода он носит не
первостепенный характер, в основном для анаэробных организмов.
Диоксид углерода ассимилируют фототрофные
бактерии через восстановительный пентозо-фосфатный цикл или восстановительный
цикл лимонной кислоты. Многие виды способны расти как хемоавтотрофы или
хемоорганотрофы. Именно этот источник кислорода используют аноксигенные
фототрофные бактерии [33].
3.3 Молекулярный водород
К число хемолитоавтотрофовных микроорганизмов,
окисляющих Н2, относятся водородные, метанобразующие бактерии,
отдельные представители ацетатобразующих, сульфат- и серовосстанавливающих
бактерий. Для штаммов использующих молекулярный водород, характерно присутствие
гидрогеназы. За счет молекулярного водорода идет восстановление СО2
[7, 25].
3.4 Вода
Из всех химических соединений для жизни на Земле
наиболее важна вода. Вода служит хорошим растворителем для большинства
биологически важных веществ, включая О2, СО2, неорганические
соли и органические соединения.
Количество воды в разных клетках колеблется от
60 до 90%, даже в спорах бактерий она содержится до 18…20%. Вода необходима
клеткам для их метаболизма и роста. Доступность воды определяется ее
активностью в среде (aw), а также зависит от осмотического давления
раствора (р). Минимальное значение aw, при котором бактерии способны
расти, значительно варьирует, однако для большинства видов оно превышает 0,99.
Некоторые галофильные бактерии растут при значении активности 0,8. Колебания
величины aw могут оказывать влияние на скорость роста бактерий, их
состав и метаболическую активность. Формула для расчета активности воды:
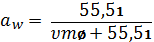
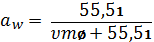 ,
,
где х - число ионов, образуемых на 1
молекулу раствора, m - моляльность жидкости и 
 - моляльный осмотический
коэффициент [6, 34, 35].
- моляльный осмотический
коэффициент [6, 34, 35].
Наиболее активно используют воду в
химическом плане фотосинтезирующие бактерии, у которых она является донором
электронов (цианобактерии). Также воду используют пурпурные и зеленые
серобактерии, когда они окисляют элементарную серу [25].
Несерные пурпурные бактерии могут использовать
вместо неорганического донора водорода различные органические вещества:
дикарбоновые кислоты, пируват, лактат, ацетат, формиат, бензоат, этанол, малат,
сукцинат, бутират, манит и другие.
Гетеротрофы получают эти элементы из основных
органических питательных веществ.
Чтобы удовлетворить потребности микробов в двух
органогенах - кислороде и водороде - в большинстве случаев бывает достаточно
тех атомов кислорода и водорода, которые содержатся в молекулах органических
веществ и в воде. Исключение представляют водородные бактерии, а также зеленые
и пурпурные бактерии. Аэробные микроорганизмы не могут развиваться без доступа
кислорода [10, 13, 25].
4.
Источники серы
Сера - еще один биогенный элемент, входит в
состав аминокислот (цистеин, метионин), витаминов и кофакторов (биотин,
липоевая кислота, кофермент А и другие). В природе сера находится в форме
неорганических солей, главным образом сульфатов, в виде молекулярной серы или
входит в состав органических соединений [1, 36].
К неорганическим источникам серы относят
сульфаты, тиосульфаты, сульфоновые кислоты, сульфиды, сероводород, элементарную
серу.
Сульфат - наиболее обильно представленная в
биосфере форма серы, усваиваемая живыми организмами - восстанавливается до H2S
в процессе диссимиляционной сульфатредукции бактериями родов Desulfovibrio,
Archaeoglobus и многих других. На образование конечного продукта - сероводорода
- используется восемь электронов. Донором электронов при этом может служить
молекулярный водород, а также разнообразные органические субстраты.
В процессе ассимиляционной сульфатредукции,
восстановление сульфата происходит в два этапа. Первый из них - это
двухэлектронное восстановление сульфата да сульфита, второй - шестиэлектронное
восстановление сульфита до H2S. Образующийся H2S
немедленно связывается с О-ацетилсерином с образованием цистеина - конечного
продукта ассимиляционной сульфатредукции. Сульфаты ассимилируют несерные
пурпурные бактерии и некоторые серные пурпурные бактерии.
Помимо сульфатов, хорошим источником серы является
тиосульфат. Он непосредственно взаимодействует с О-ацетилсерином с образованием
S-сульфоната, который далее восстанавливается до цистеина.
Сульфоновую кислоту бактерии редко используют в
качестве источника серы, так как связь C-S довольно устойчива. У аэробных
бактерий разложение сульфоновых кислот происходит при участии диоксигеназ или
монооксигеназ, осуществляющих отщепление сульфита при участии кислорода [25,
36, 37, 38].
Известны архебактерии, которые растут на
элементарной сере. Это некоторые экстремальные термофилы и гипертермофилы. В
анаэробных условиях они восстанавливают S0 до H2S, в
аэробных условиях окисляют H2S до H2SO4.
Донорами электронов служат Н2 или органические соединения [33].
Окисление H2S осуществляют
фотосинтезирующие и хемоавтотрофные бактерии. Оно может происходить в аэробных
условиях под воздействием бесцветных серобактерий или в анаэробных с помощью
фотосинтезирующих пурпурных и зеленых серобактерий. Такие окислительные реакции
приводят к образованию ионов водорода, поэтому серу обычно добавляют в щелочную
среду [15].
Микроорганизмы, утратившие способность
восстанавливать сульфаты, нуждаются в соединениях, содержащих атом серы в
восстановленной форме, как, например, сероводород, цистеин [19].
5.
Источники фосфора
Фосфор - необходимый компонент нуклеиновых
кислот, фосфолипидов, коферментов. Основной формой фосфора в природе являются
фосфаты. Для их ассимиляции не требуется восстановление. В живых организмах он
присутствует почти исключительно в степени окисления +5, в виде фосфата.
Доступность его в природе лимитирована в основном низкой растворимостью
фосфатов кальция и магния и способностью фосфата эффективно адсорбироваться на
органических и неорганических полимерах. Концентрация фосфора обычно не
превышает несколько микромоль, тогда как в клетках он содержится в
миллимолярном количестве. Следовательно, во многих природных местообитаниях он
лимитирует рост микроорганизмов.
Фосфат мобилизуется из неорганических
полифосфатов и органических фосфатов (производные нуклеиновых кислот,
нуклеотиды) под действием фосфатаз, которыми обладают прокариоты. Фосфат не
восстанавливается в реакциях биологического преобразования энергии.
Донором-переносчиком фосфата в клетке служит АТР.
Высокомолекулярные органические фосфаты, которые
клетки прокариот не способны поглощать, гидролизуются в периплазматическом
пространстве при участии эстераз. Высвобождающийся неорганический фосфат
переносится в клетку по механизму активного транспорта.
Многие бактерии в условиях избытка фосфора и
источника энергии, если рост лимитирован при этом другими факторами, образуют
полифосфаты - резервный источник энергии и фосфора. Расщепление
внутриклеточного пирофосфата (PPi→2Pi) осуществляет
фермент пирофосфатаза. Некоторые анаэробы используют PPi вместо АТР
для фосфорилирования тех или иных субстратов, например ацетата.
Присутствие неорганического фосфата подавляет
ассимиляцию альтернативных источников фосфора - органических фосфорных эфиров,
диэфиров, ангидридов и фосфоновых кислот, в которых фосфор непосредственно связан
с углеродом.
Следует отметить, что фосфорорганические
соединения могут служить источниками углерода, фосфора и энергии [1, 28, 36,
37, 39].
6.
Минеральные элементы
Помимо элементов-органогенов, из которых состоят
клеточные полимеры и растворимые органические соединения, для построения клеток
необходимы важные в качестве электролитов щелочные металлы (K, Na),
щелочноземельные металлы (Mg, Ca, выполняющие функции кофакторов ферментов) и
микроэлементы - металлы переходной группы (V, Mn, Fe, Co, Ni, Cu, Zn, Mo, W) и
неметаллы (Se, B, Cl и другие) [37].
Биоэлементы можно разделить еще на основные и
минорные. К основным элементам (помимо С, H, O, N, S, P) принадлежат K, Mg, Ca,
Fe. К минорным элементам относят Zn, Mn, Na, Cl, Mo, Co, Cu, W, Ni [5].
6.1 Основные биоэлементы (макроэлементы)
Данные минеральные элементы требуются в
сравнительно больших количествах - 0,2-0,5 г/л.
К+ является основным неорганическим
катионом в клетке и кофактором некоторых ферментов, важен для синтеза белка.2+
- кофактор многих ферментов (например, киназ); присутствует в клеточных
стенках, мембранах и эфирах фосфорной кислоты. Большинство биоактивных
фосфорных эфиров находится в клетках в виде комплексов с магнием.
Фосфолипопротеиды клеточной стенки бактерий также образуют хелатные комплексы с
ионами магния. Магний необходим для функционирования рибосом.2+ -
кофактор ферментов, присутствует в экзоферментах (в амилазе, протеазе);
Са-дипиколинат является важным компонентов эндоспор.2+, Fe3+ содержатся
в цитохромах, ферредоксинах и других железосеропротеидах - входят в состав
компонентов электронпереносящей цепи, кофактор ферментов (некоторые
дегидратазы).
Важную роль у бактерий играет способность к
поглощению железа, поскольку в природе содержание этого элемента часто
относится к лимитирующим рост факторам. В аэробных условиях железо присутствует
в среде в окисленной форме, Fe(III), образуя практически нерастворимые гидраты
оксида железа, карбонат железа, и магнетит [оксид Fe(II/III)], в связи с чем
большинство аэробных микроорганизмов для поглощения железа секретирует в среду
сидерофоры - органические соединения-переносчики железа, образующие хелаты с Fe3+
. В анаэробных условиях железо не является лимитирующим рост элементов,
присутствуя в форме Fe2+, хорошо растворимой, и в отсутствии
кислорода довольно устойчивой.
Известны бактерии, которые способны окислять
двухвалентное железо до трехвалентного - это железобактерии. Многие
ацидофильные железобактерии способны также окислять восстановленные соединения
серы с образованием серной кислоты, используются для выщелачивания металлов из
сульфидных руд [5,6, 37, 40].
6.2 Минорные биоэлементы (микроэлементы)
Набор требуемых микроэлементов зависит от вида
микробов. В природе микроэлементы обычно присутствуют в виде свободных катионов
или анионов, поглощаемых микробными клетками с помощью относительно специфичных
транспортных систем.
Некоторые из микроэлементов встречаются в форме
оксианионов, таких как SeO3-, WoO42-
и MoO42-. В клетках они подвергаются ферментативному
восстановлению, приобретая валентность, необходимую для ассимиляции [37].
Микроэлементы нужны в очень низких концентрациях
- 0,1-0,001 мг/л.2+ содержится в алкогольдегидрогеназе, щелочной
фосфатазе, альдолазе, РНК- и ДНК-полимеразе.2+ содержится в
бактериальной пероксиддисмутазе; кофактор некоторых ферментов
(фосфоэнолпируват-карбоксикиназы, цитрат-синтазы). Марганец способны окислять
представители различных систематических групп. В реакции образуется
нерастворимый MnO2.
Ионы цинка и марганца необходимы всем
микроорганизмам.+,Cl- необходимы галофильным и морским
бактериям в больших концентрациях. Однако эти организмы составляют исключения.
У большинства микроорганизмов потребность в ионах натрия и хлора невелика.
Потребность в Na+ у негалофилов обнаруживается только в том случае,
когда они выращиваются в присутствии специфических источников углерода и
энергии: например, E.coli нуждается в Na+ для роста с максимальной
скоростью на среде с L-глутаматом, а Enterobacter aerogenes - на среде с
цитратом. В обоих случаях количественная потребность невелика.содержится в
нитратредуктазе, нитрогеназе и формиатдегидрогеназе. Молибденпротеиды играют
важную роль в азотном обмене и в окислении формиата. Ксантиндегидрогеназа также
содержит молибден.содержится в глицинредуктазе и формиатдегидрогеназе.
Глицинредуктаза содержит селен в форме селенцистеина.2+ содержится в
коферменте витамин-В12-ферментов (глутаматмутазе, метилмалонил-СоА-мутазе).2+
содержится в цитохромоксидазе и оксигеназах - ферментах, переносящих электроны
от субстратов к кислороду.содержится в некоторых формиатдегидрогеназах.2+
содержится в уреазе; требуется для автотрофного роста водородных бактерий.
Небольшие молекулы и ионы поддерживают
оптимальный уровень обмена веществ в клетках, они вносят определенный и
существенный вклад в осморегуляцию микроорганизмов.
Присутствие в питательной среде хелатирующих
веществ является важным фактором, определяющим доступность ионов металлов;
поэтому, если необходимо добиться интенсивного роста бактерий, концентрация
этих агентов должна быть сбалансирована с количеством микроэлементов.
Хелатирующими свойствами обладают аминокислоты, цитрат, малат и др.
Минеральные элементы вносятся в питательную
среду в виде соответствующих солей, составляя ее минеральную основу [5, 6, 27,
40, 41].
7.
Факторы роста
К факторам роста относят аминокислоты, пуриновые
и пиримидиновые основания, витамины, и другие соединения.
Аминокислоты уже были упомянуты в источниках
азота и углерода [3].
7.1 Пуриновые и пиримидиновые основания
Некоторые микроорганизмы нуждаются в пуриновых и
пиримидиновых основаниях, или их производных, входящих в состав нуклеиновых
кислот. Эти вещества нужны в основном в качестве строительного материала для
нуклеотидов. Одно из пуриновых оснований - аденин - входит не только в
нуклеиновые кислоты, но и в состав коэнзимов, в частности коэнзима А (КоА). Они
являются факторами роста для разных видов стрептококков, стафилококков,
микоплазм и других видов. Потребность в пуриновых и пиримидиновых основаниях
больше всего выражена у молочнокислых бактерий.
Наряду с основными азотистыми основаниями,
микроорганизмы отзываются положительно еще на один пурин - ксантин.
Концентрация пуринов и пиримидинов, необходимые
для максимального роста микроорганизмов, обычно составляет 10-20 мкг на 1 мл. В
одних случаях азотистые основания только ускоряют рост микроорганизмов, в
других случаях они оказываются для них обязательными [3, 10, 19, 27].
7.2 Витамины и родственные соединения
Витамины осуществляют свои каталитические
функции в клетке обычно в качестве компонентов коферментов или как
простетические группы ферментов. Готовые витамины необходимы для ряда
бактерий.Аминобензойная кислота служит предшественником в биосинтезе фолиевой
кислоты и поэтому оказывает воздействие на метаболизм тимина, метионина,
серина, пуриновых оснований и витамина В12. В свою очередь,
присутствие этих компонентов в среде может оказывать влияние на увеличение или
снижение потребности бактерий (вплоть до нулевой) в n-аминобензойной кислоте.
Парааминобензойная кислота является ростовым фактором для многих патогенных
бактерий: пневмококков, гонококков, возбудителей дизентерии.
Некоторые формы фолиевой кислоты, встречающиеся
в природе, отличаются по своей усвояемости отдельными бактериями.
Птероил-L-глутаминовая кислота и ее N10-формильное производное
полностью усваиваются Lactobacillus casei и S.faecalis; птероилтриглутаминовая
кислота обеспечивает хороший рост L.casei, но мало активна в случае S.faecalis,
птероилгептаглутаминовая кислота вообще не стимулирует рост бактерий. N5-формилтетрагидроптероилглутаминовая
кислота (лейковорин) активна в случае L.casei и S.faecalis. Фолиевая кислота
участвует как кофактор в синтезе тимина, пуринов, серина, метионина и
пантотеновой кислоты. Если эти компоненты добавлены в среду, то потребность
бактерий в фолиевой кислоте часто отпадает.
Биотин участвует в разных реакциях биосинтеза,
требующих фиксации СО2, в том числе в синтезе оксалоацетата и жирных
кислот. Биоцитин (Nᵋ-биотиниллизин)
является природным соединением; он так же, как и биотин, активен в случае L.casei,
но не в случае Lactobacillus arabinosus.
Никотиновую кислоту и ее производные используют
большинство ауксотрофов. Коферментные формы витамина -
никотинамидадениндинуклеотид (NAD) и никотинамидадениндинуклеотидфосфат (NADP)
- участвуют в окислительно-восстановительных реакциях клеточного метаболизма.
Некоторые организмы не способны синтезировать NAD из никотиновой кислоты и
поэтому нуждаются в готовом коферменте.
Пантотеновая кислота является компонентом
кофермента А (СоА) и ацилпереносящего белка (АПБ), которые служат переносчиками
ацильной группы в процессах метаболизма. Некоторые бактерии используют
интактный кофермент как фактор роста, но для роста значительно большего числа
бактерий необходимы пантотеновая кислота или пантетеин. Потребность отдельных
видов бактерий в том или ином родственном соединении обусловлена способностью к
их синтезу и транспорту.
Относительно немногие виды бактерий требуют
рибофлавин (витамин В2). Почти все бактерии, очевидно, содержат этот
витамин, а некоторые виды синтезируют его в достаточно большом количестве, т.е.
могут служить источником выделения рибофлавина в виде препарата. ФМН
(флвинмононулеотид) и ФАД (флавинадениндинуклеотид) являются главными
коферментными формами рибофлавина, участвующими в окислительно-восстановительных
реакциях. Все эти три вещества одинаково активно поддерживают рост
рибофлавинового ауксотрофа L.casei. Этот витамин необходим всем аэробным
микроорганизмам.
Большое число бактерий являются ауксотрофными по
тиамину (витамин В1), его предшественникам или коферментной форме -
тиаминпирофосфату (ТПФ). ТПФ участвует в декарбоксилировании б-кетокислот и в
транскетолазной реакции.
Различные виды ауксотрофных по витамину В6
(пиридоксин, пиридоксаль, пиридоксамин) бактерий по-разному реагируют на его
фосфорилированные производные. Пиридоксаль наиболее широко используется как
фактор роста. Для роста некоторых бактерий необходим пиридоксамин-5’-фосфат;
однако для большинства ауксотрофов фосфорилированные формы витамина В6
неактивны, так как клетки не имеют для них соответствующих транспортных систем.
Пиридоксаль-5’-фосфат и пиридоксамин-5’-фосфат участвуют во многих реакциях
синтеза и деградации природных б-аминокислот.
Витамин В12 (кобаламин) синтезируется
в природе исключительно микроорганизмами, которые вместе с их побочными
продуктами являются источником выделения витамина в виде препарата.
Коферментная форма витамина В12 (кобаламин, связанный с
адениннуклеозидом) так же активно, как и витамин, стимулирует рост бактерий.
Кофермент участвует во многих метаболических реакциях изомеризации, а также
(прямо или косвенно) в биосинтезе дезоксирибонуклеозидов, метионина и,
вероятно, других веществ.
Липоевая кислота (тиоктовая кислота) -
необходимый фактор роста для различных молочнокислых бактерий и Butyribacterium
rettgeri. Липоевая и дигидролипоевая кислоты, а также различные смешанные
дисульфиды примерно одинаково стимулируют рост S.faecalis. Данная кислота
участвует в окислении пирувата и б-кетоглутарата.
Витамин К или родственные ему соединения
необходимы для роста некоторых видов Mycobacterium. Он является
предшественником менахинона, функционирующего как переносчик электронов
(например, в фумаратредуктазе) [5, 13,27].
Чаще всего наблюдается потребность в таких
витаминах, как биотин, n-аминобензойная кислота, тиамин, никотиновая кислота и
витамин В12.
Стоит отметить, что одни организмы требуют
витамины в виде целой молекулы, другие обходятся какой-нибудь частью молекулы,
третьи могут развиваться при полном отсутствии данного витамина [5, 10].
Потребность того или другого микроорганизма в
определенных ростовых факторах является стабильным признаком, который
используется для дифференциации и идентификации бактерий, а также при
изготовлении питательных сред для лабораторных и биотехнологических целей.
Источниками ростовых веществ могут служить
экстракты из органов животных (печень, сердце), растений (семена и проростки),
а также и самих бактериальных тел [3, 27].
Выводы
Прокариоты нуждаются в различных источниках
химических элементов, относящихся к органогенам и минеральным элементам в
различных количествах.
Источники питательных веществ можно поделить
относительно химических элементов на источники углерода, азота, водорода и
кислорода, серы, фосфора, а также минеральные соли - источники минеральных
элементов.
К источникам углерода относят неорганические
(углекислота, угарный газ) и органические вещества (углеводороды и их
производные, ароматические соединения, углеводы и другие). Наиболее
распространенным субстратом является глюкоза, она не только источник углерода,
но и энергии.
Источники азота также можно разделить на
неорганические (нитраты, нитриты, молекулярный азот) и органические (белки,
аминокислоты, органические останки). Наилучшими источниками являются аммонийные
соли и белковые гидролизаты.
Кислород и водород прокариоты получают вместе с
углеродным и азотным питанием. Кроме того, аэробные бактерии получают кислород
из воздуха, во время окисления различных субстратов.
Наилучшим источником серы являются сульфаты, а
фосфора - фосфаты. Если бактерии не могут восстанавливать серу из сульфатов, то
они нуждаются в уже восстановленной сере.
Минеральные соли являются источниками
минеральных элементов.
Факторы роста требуются для оптимального
развития прокариот и нормального функционирования метаболизма. Их можно разделить
на аминокислоты, азотистые основания и витамины.
Так, в данной работе были рассмотрены
потребности прокариот в питательных веществах, их источники, метаболизм в
клетке, относительная усвояемость.
Список использованой литературы
2. Микробиология. / А.А.
Воробьев, А.С. Быков, Е.П. Пашков, А.М. Рыбакова - М.: Медицина, 2003. - 336 с.
. Борисов Л.Б. Медицинская
микробиология, вирусология, иммунология: Учебник. - М.: Медицинское информационное
агентство, 2005. - 736 с.
. Ахметов Н.С. Общая и
неорганическая химия - М.: Академия, 2001. - 743 с.
. Готтшалк Г. Метаболизм
бактерий - М.: Мир, 1982. - 293 с.
. Елинов Н.П. Химическая
микробиология - М.: Высшая школа, 1989. - 448 с.
. Промышленная микробиология
/ З.А. Аркадьева, А.М. Безбородов, И.М. Блохина и др. - М.: Высш.шк.. 1989. -
688 с.
. Гальченко В.Ф.
Метанотрофные бактерии - М.: ГЕОС, 2001. - 495 с.
. Мишустин Е.М., Емцев В.Т.
Микробиология - М.: Агропромиздат., 1987. - 368 с.
. Иерусалимский Н.Р. Основы
физиологии микробов - М.: АН СССР, 1963. - 239 с.
. Шлегель Г. Общая
микробиология. - М.: Мир, 1987. - 367 с.
. Лабинская А.С.
Микробиология с техникой микробиологических исследований - М.: Медицина, 1978.
- 394 с.
. Гирард Б., Снелл Э.
Биохимические факторы // Методы общей бактериологии в 3т.. т.1 / Под.ред.
Ф.Герхардта и др. - М.: Мир, 1983., - с. 198-268.
. Ленинджер А. Основы
биохимии в 3т. - М.: Мир, 1985. - Т.2. - 368 с.
. Стейниер Р., Эдельберг Э.
Ингрэм Дж. Мир микробов. В 3т. - М.: Мир, 1979. - Т.3. - 334 с.
. Основы биохимии в 3т. /
А.Уайт, Ф. Хендлер, Э.Смит и др. - М.:Мир, 1981. - Т.2. - 617 с.
. Биотехнология. - М., 1988,
- (Высшая школа) - кн.2: Современные методы создания промышленных штаммов
микроорганизмов - 208 с.
. Методы частной
бактериологии. / Р.А. Васильев, А.А. Щербаков, Л.В. Карпунина, С.М. Золотухин -
Ульяновск : УГСХА, 2004. - 222 с.
. Мосичев М.С., Складнев А.А.
Котов В.Б. Общая технология микробиологических производств. - М.: Легкая и
пищевая пром-сть, 1982. - 264 с.
. Эткинс П. Молекулы. -
М.:Мир, 1991. - 216 с.
. Войнова-Райнова Ж., Ранков
В., Ампова Г. Микроорганизмы и плодородие. - М.: Агропромиздат, 1986. - 120 с.
. Жарикова Г.Г. Микробиология
продовольственных товаров. Санитария и гигиена. - М.: ACADEMA, 2005. - 304 с.
. Биоразрушение материалов и
изделий техники / С.А. Семенов, К.З. Гумаргалиева, И.Г. Калинина, Г.Е. Заиков
// Вестник МИТХТ. - 2007, - Т.2, №6 - с. 3-26.
. Красильников Н.А., Уранов
А.А. Жизнь растений. - М.: Просвещение, 1974. - 487с.
. Кондратьева Е.Н.
Фотосинтезирующие бактерии и бактериальный фотосинтез. - М.: Изд. МГУ, 1972. -
73с.
. Определитель бактерий
Берджи. В 2т. / Дж. Хоулт, М. Криг, П. Мир, 1997. - Т.2. - 368с.
. Колешко О.И., Завезенова
Т.В. Микробиология с основами вирусологии. - Иркутск: Изд.во Иркут. ун-та,
1999. - 452с.
. Шинк Б. Экофизиология и
экологические ниши прокариот // Современная микробиология. Прокариоты. В 2х
томах., т.2 / Под ред. Й. Ленгелера, Г. Древса, Г. Шлегеля. - М.: Мир, 2005. -
с. 209-217
. Мармузова Л.В. Основы
микробиологии, санитарии и гигиены в пищевой промышленности. - М.: Академия,
2004. - 136с.
. Практична мікробіологія. /
Климнюк С.І., Ситник І.О., Творко М.С., Широбоков В.П. - Тернопіль:
Укрмедкнига,2004. - 440с.
. Лукнер М. Вторичный
метаболизм у микроорганизмов, растений и животных. - М.: Мир, 1979. - 517 с.
. Елинов Н.П. Основы
биотехнологии. СПб.: Наука, 1995. - 600с.
. Определитель бактерий
Берджи. В 2т. / Дж. Хоуст, М. Крич, П. Смит и др. - М.: Мир, 2005. - с.
257-304.
. Шинк Б. Местообитание
прокариот // Современная микробиология. Прокариоты. В 2х т., т.2 / Под ред. Й.
Лейнгелера, Г. Древса, Г. Шлегеля. - М. Мир, 2005. - с.257-304.
. Костилоу Р. Биофизические
факторы // Методы общей бактериологии. В 3 т., т.1 / Под ред. Ф. Герхарда и др.
- М.: Мир, 1983. - с.165-195.
. Шинк Б. Глобальные
биохимические циклы // Современная микробиология. Прокариоты. В 2 т., т.2 / Под
ред. Й. Лейнгелера, Г. Древса, Г. Шлегеля. - М. Мир, 2005. - с.307-315.
. Фукс Г. Ассимилиция макро-
и микроэлементов // Современная микробиология. Прокариоты. В 2т., т.1 / Й.
Лейнгелера, Г. Древса, Г. Шлегеля. - М. Мир, 2005. - с.206-230.
. Буккель В. Анаэробный
энергетический метаболизм // Современная микробиология. Прокариоты. В 2т., т.1
/ Й. Лейнгелера, Г. Древса, Г. Шлегеля. - М. Мир, 2005. - с.346-402.
. Фукс Г. Биосинтез клеточных
строительных блоков // Современная микробиология. Прокариоты. В 2т., т.1 / Й.
Лейнгелера, Г. Древса, Г. Шлегеля. - М. Мир, 2005. - с.145-201.
. Куэнен Й. Окисление
неорганических соединений хемолитотрофами // Современная микробиология.
Прокариоты. В 2т., т.1 / Й. Лейнгелера, Г. Древса, Г. Шлегеля. - М. Мир, 2005.
- с.293-321.
. Стейниер Р., Эдельберг Э.,
Ингрэм Дж. Мир микробов. В 3х т. - М.: Мир, 1979. - Т.2. - 331 с.