Способы получения аммиака
Способы получения
аммиака
Сырьем в производстве аммиака
является азотоводородная смесь (ABC) стехиометрического состава N2: Н2 = 1: 3.
Так как ресурсы атмосферного азота практически неисчерпаемы, сырьевая база
аммиачного производства определяется вторым компонентом смеси - водородом,
который может быть получен разделением обратного коксового газа, газификацией
твердого топлива, конверсией природного газа (рис. 14.5).
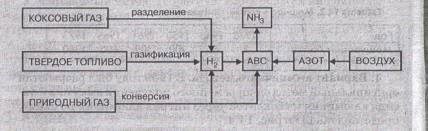
Рис. 14.5. Сырьевые ресурсы
производства аммиака
Структура сырьевой базы производства
аммиака менялась и свыше 90% аммиака вырабатывается на основе природ - 14.3
приведена динамика изменения структуры основных видов сырья аммиачного
производства.
Таблица 14.3. Изменение сырьевой
базы производства аммиака

Азотоводородная смесь, независимо от
метода ее получения, содержит примеси веществ, некоторые из которых являются
каталитическими ядами, вызывающими как обратимое (кислород, оксиды углерода,
пары воды), так и необратимое (различные соединения серы и фосфора) отравление
катализатора.
С целью удаления этих веществ ABC
подвергается предварительной очистке, методы и глубина которой зависят от их
природы и содержания, то есть от способа производства ABC, Обычно, ABC,
получаемая конверсией природного газа, содержит оксид углерода (IV), метан,
аргон, следы кислорода и до 0,4% Об. оксида углерода (II).
Для очистки ABC в промышленности
используются методы абсорбции жидкими поглотителями (мокрый метод) и адсорбции
твердыми поглотителями (сухой метод). При этом, процесс очистки может
производиться на различных стадиях производства:
- исходного газа перед подачей его
на конверсию;
конвертированного газа для удаления
из него оксида углерода (IV);
- азотоводородной смеси
непосредственно перед синтезом аммиака (тонкая очистка ABC).
Первые два процесса рассматриваются
при описании соответствующих производств.
Тонкая очистка ABC достигается
хемосорбцией примесей жидкими реагентами и, окончательно, каталитическим
гидрированием их или промыванием ABC жидким азотом.
Для удаления оксида углерода (IV) и
сероводорода ABC промывают в башнях с насадкой щелочными реагентами,
образующими с ними нестойкие термически соли: водным раствором этаноламина или
горячим, активированным добавкой диэтаноламина, раствором карбоната калия. При
этом протекают, соответственно, реакции:
H2S + CH2OH-CH2NH2[CH2OH-CH2NH3]+HS-
- ∆Н,
СО2 + К2СОз +
Н2O↔ 2КНСО3 - ∆Н.
Оксид углерода (II) удаляют из ABC
промывкой ее медноаммиачным раствором ацетата меди:
СО + NH3 + [Cu(NH3)2]+Ац
↔ [Cu(NH3)3CO]+Ац -∆Н,
Применяемые для хемосорбции
абсорбенты образуют с поглощаемыми из ABC нестойкие соединения. Поэтому, при
нагревании их растворов и снижении давления происходит десорбция растворенных
примесей, что позволяет легко регенерировать абсорбент, возвратить его в
процесс и обеспечить цикличность операции абсорбции по схеме:

где: П - поглощаемая из ABC примесь,
А - абсорбент, ПА - соединение примеси и абсорбента.
Более эффективным методом очистки
ABC от оксида углерода (II) является применяемая в современных установках
промывка ABC жидким азотом при -190 °С, в процессе которой из нее удаляются,
помимо оксида углерода (II), метан и аргон.
Окончательная очистка ABC
достигается каталитическим гидрированием, примесей, получившим название
метанирования или предкатализа. Этот процесс проводится в специальных
установках метанирования (рис. 14.6) при температуре 250-300 °С и давлении
около 30 МПа на никель-алюминиевом катализаторе (Ni + Al2O3). При этом протекают экзотермические реакции
восстановления кислородсодержащих примесей до метана, который не является ядом
для железного катализатора, а вода конденсируется при охлаждении очищенного
газа и удаляется из него:
СО + ЗН2 ↔ СН4
+ Н2О -∆Н,
СО2+ 4Н2 ↔СH4
+ 2Н2О - ∆Н,
О2 + 2Н2 ↔2Н2О
- ∆Н

Рис. 14.6. Схема установки
метанирования ABC: 1 - компрессор, 2 - подогреватель, 3 - реактор
метанирования, 4 - подогреватель воды, 5 - конденсатор, 6 - влагоотделитель
Если в предкатализе используется
железный катализатор, в процессе гидрирования также образуется некоторое
количество аммиака, в этом случае предкатализ называется продурующим.
Процесс метанирования прост, легко
управляем, а выделяющееся за счет протекающих экзотермических реакций
гидрирования тепло, используется в общей энерготехнологической схеме
производства аммиака. Очищенная ABC, поступающая на синтез, содержит до 0025
об. долей аргона, 0,0075 об. долей метана и не более, 00004 об. долей оксида
углерода (II), являющегося наиболее сильным каталитическим ядом.
В основе процесса синтеза аммиака
лежит обратимая экзотермическая реакция, протекающая с уменьшением объема газа:
2+3H2 + 2NH3 + Q.
В соответствии с принципом
Ле-Шателье при повышении давления и уменьшении температуры равновесие этой
реакции смещается в сторону образования аммиака. Для обеспечения оптимальной
скорости процесса необходимы катализатор, повышенное давление, температура 400…
500 °С и определенная объемная скорость вступающих в реакцию компонентов. В
промышленности используется железный катализатор с добавками оксидов Аl2О3,
К2О, СаО и SiO2.
Различают следующие промышленные
системы агрегатов синтеза аммиака: низкого давления (10…20 МПа), среднего (20…
45 МПа) и высокого давления (60…100 МПа). Мировой практике широко применяются
системы среднего давления, так как при этом наиболее удачно решаются вопросы
выделения аммиака из азотно-водородной смеси при достаточно высокой скорости
процесса.
СН4 + Н2О ↔
СО + 3Н2
Происходит частичное сгорание
водорода в кислороде воздуха:
Н2 + О2 = Н2О(пар)
В результате на этой стадии
получается смесь водяного пара, оксида углерода (II) и азота.
Конструктивно колонны различаются
главным образом размерами корпуса и устройством внутренней насадки. В верхней
части рассматриваемой колонны расположена катализаторная коробка 3, а в нижней
- теплообменник 8, обеспечивающий автотермичность процесса. Катализаторная
коробка связана с теплообменником центральной трубкой 7. Корпус колонны имеет
тепловую изоляцию 5. Катализатор загружается на колосниковую решетку 6. Для
обеспечения равномерного распределения температуры в слой катализатора вводятся
двойные трубы 1.

Рис. 1.1. Колонна синтеза аммиака с
двойными противоточными теплообменными трубками
В настоящее время колонны для
синтеза аммиака совмещаются с паровыми котлами для утилизации теплоты выходящих
газов (на 1 т аммиака приходится 0,6…1 т водяного пара при давлении 1,5…2 МПа).
Колонны синтеза аммиака под средним давлением имеют производительность около
150 т аммиака в сутки и работают без замены катализатора в течение четырех лет.
При синтезе аммиака под средним
давлением (рис. 1.1) азотно-водородная смесь (N2:Н2=1:3)
подается в колонну 1, где на катализаторе происходит синтез аммиака; из колонны
выходит азотно-водородно-аммиачная газовая смесь (содержание аммиака - 14…20%),
имеющая температуру около 200 °С. Эта смесь направляется в водяной холодильник
2, охлаждается до 35 °С и поступает в сепаратор 3. Здесь из газа выделяется до
60% образовавшегося в колонне аммиака (при давлении 30 МПа аммиак не может
сконденсироваться в холодильнике полностью). Полнее аммиак выделяется при
охлаждении азотно-водородной смеси до более низких температур. Эта смесь с
остатками аммиака из сепаратора 3 направляется в циркуляционный компрессор 4 и
далее в фильтр 6 для отделения компрессорного масла. На входе в фильтр к
оборотным газам добавляется свежая азотно-водородная смесь, сжатая до рабочего
давления с помощью многоступенчатого компрессора 5. Из фильтра газовая смесь
подается в систему вторичной конденсации аммиака, состоящую из конденсационной
колонны 7 и испарителя жидкого аммиака 8. В конденсационной колонне газ
предварительно охлаждается в расположенном в верхней части колонны
теплообменнике и затем направляется в испаритель 8, где за счет испарения
поступающего жидкого аммиака достигается охлаждение газа до - 5 °С и
конденсация аммиака из газа до остаточного содержания в нем около 2,5% NНз.
Сконденсировавшийся аммиак выделяется в нижней части конденсационной колонны 7,
являющейся сепаратором. После отделения аммиака азотно-водородная смесь
охлаждает в верхней части колонны 7 поступающий в нее газ, а затем вновь
направляется в колонну синтеза 1.
В случае синтеза аммиака под более
высоким давлением (45 МПа и выше) отпадает необходимость во вторичной его
конденсации, так как на выходе из водяного холодильника остаточное содержание
аммиака в азотно-водородной смеси незначительно.


Рис. 17.16. Схема установки для
синтеза аммиака под средним давлением
Описание
технологического процесса производства аммиака и его характеристика.
. Дуговой метод. Дуговой метод состоит в том, что через пламя электрической дуги
продувается воздух. При температуре около 3000 °С протекает обратимая реакция
2 + О2 ↔2NО - Q.
Образующийся оксид азота (II) может
быть окислен до оксида азота (IV) и переработан в азотную кислоту и другие
соединения. Для получения 1 т связанного азота этим способом расходуется 60
000…70 000 кВт-ч электроэнергии.
2. Цианамидный метод. Первым промышленным процессом, который использовался для получения
аммиака, был цианамидный процесс. При нагревании извести СаО и углерода получали
карбид кальция СаС2. Затем карбид нагревали в атмосфере азота и получали
цианамид кальция СаСN2; далее аммиак получали гидролизом цианамида:
СаСN2(тв) + 3Н2О
= 2NН3↑ + СаСО3(тв)
Этот процесс требовал больших затрат
энергии и экономически был невыгоден.
Современный процесс получения
аммиака основан на способности тонкоизмельченного карбида кальция при
температуре около 1000 °С взаимодействовать с азотом по уравнению
СаС2 + N2 =
CaCN2 + С + 302 кДж
Доля производства связанного азота
цианамидным методой весьма незначительна.
Аммиачный метод фиксации азота
заключается в его синтезе из азота и водорода с использованием специального
катализатора:
Этот метод имеет экономическое и
технологическое преимущество перед остальными способами связывания
элементарного азота
3. Аммиачный метод. Аммиачный метод связывания атмосферного азота состоит в соединении
азота с водородом и получении аммиака:
N2+3H2 ↔2NH3
+ Q.
Он наиболее экономичен (расход
электроэнергии составляет 4000…5000 кВт-ч на 1 т аммиака), технологически легче
осуществим по сравнению с другими методами связывания атмосферного азота. В
общем производстве азотных соединений свыше 90% приходится на аммиак. Водород
для этой реакции получают термическим крекингом углеводородов, действием паров
воды на уголь или железо, разложением спиртов парами воды или электролизом
воды.
4. Вариант аммиачного
метода. В 1909 году был разработан
оригинальный метод одновременного получения аммиака и оксида алюминия из
бокситов через нитрид алюминия по схеме, представленной на рис. 14.4.

Рис. 14.4. Производство аммиака из
бокситов
Промышленные установки по этому
методу были построены в период 1909-1918 гг. в ряде стран, но метод не нашел
применения вследствие низкой экономичности производства.
Химическая и
принципиальная схемы производства.
Основная стадия процесса синтеза
аммиака из азотоводородной смеси описывается уравнением:
N2 + 3H2 = 2NH3
Однако, так как преобладающим
методом получения ABC является конверсия метана воздухом и водяным паром, химическая
схема производства аммиака включает помимо этой реакции несколько реакций
воздушной и паровой конверсии:
СН4 + Н2О = ЗН2
+ СО,
СН4 + 0,5O2(N2)
= 2Н2(N2) + СО
и последующего превращения оксида
углерода (II) в оксид углерода (IV):
СО + Н2О = Н2
+ СО2
аммиак производство абсорбция
колонна
После удаления оксида углерода (IV)
из газовой смеси и коррекции ее состава получают ABC с содержанием азота и
водорода в отношении 1: 3.
Таким образом, современное производство
аммиака состоит из двух стадий: приготовления ABC и превращения ее в аммиак,
представляя единую энерготехнологическую схему, в которой сочетаются операции
получения ABC, ее очистки и синтеза аммиака и эффективно используются тепловые
эффекты всех стадий процесса, что позволяет в несколько раз снизить затраты
электроэнергии.

1-очистка природного газа от
сернистых соединений, 2 - паровая конверсия метана, 3-воздушная конверсия
метана, 4 - конверсия оксида углерода (II), 5-хемосорбционная очистка ABC, 6 -
метаниро - вание, 7-синтез аммиака, 8 - абсорбция аммиака, 9-сжатие аммиака,
I-природный газ, II-конвертированный газ, III-ABC, IV - метан
Принципиальная схема производства
аммиака состоит из трёх стадий:
Первая стадия - получение АВС
(азотоводородная смесь):
-я операция: очистка природного газа
от сернистых соединений;
-я операция: паровая конверсия
метана;
-я операция: воздушная конверсия
метана;
-я операция: конверсия оксида
углерода (II).
Вторая стадия - очистка газа от
балластных примесей и примесей, отравляющих катализатор:
-я операция: очистка АВС
абсорбционными методами от оксида углерода (II) и оксида углерода (IV);
-я операция: тонкая очистка АВС от
оксида углерода (II) и оксида углерода (IV) методом метанирования или
предкатадиза.
Третья стадия - синтез аммиака из
АВС в присутствии катализатора.