Определение pH раствора хингидронным электродом
Лабораторная
работа №3
«Определение
pH
раствора хингидронным электродом»
Хингидронный электрод относится к
окислительно-восстановительным электродам:
Е=φхг-φхс
(1)
Е - ЭДС хингидрона
φхг
- потенциал хингидронного электрода
φхс -
потенциал хлорсеребряного электрода
 (2)
(2)
хингидрон хинон гидрохинон
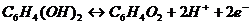 в водном растворе (3)
в водном растворе (3)
 (4)
(4)
R=8,315
Дж/град*моль
R=8,31
эрг/моль*град
T -
температура
F - число
Фарадея; F=96495,5
к/г*экв
φd -
диффузионный потенциал ячейки
Если φd элиминирован,
то:
 (5)
(5)
Пусть aх=aгх , то:
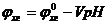 (6)
(6)
Зависимость стандартного потенциала
хингидронного электрода от температуры:
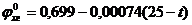 (7)
(7)
Подставим (6) в (1):
 (8)
(8)
хингидронный электрод
раствор потенциал
В нормальном растворе «солевая ошибка»
хингидронного электрода может достигать 0,03-0,05 единиц pH.
Хингидрон - двухосновная кислота, константы
диссоциации которой равны: К1=1,8*10-10 и К2=4*10-12.
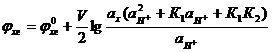
Ход работы:
1. стакан с насыщенным раствором KCl
. хлор-серебряный электрод
. электролитический ключ
(содержащий агар-агар+KCl)
. платиновый электрод
. стакан с исследуемым раствором
. осадок хингидрона
В стаканчик наливают исследуемый раствор и к
нему добавляют хингидрон из расчёта 0,1г на 25 мл раствора:
1. HCl
1Н
2. HCl
0,5Н
3. HCl
0,1Н
. раствор Вейбеля
5. HCl
0,01Н
Раствор тщательно перемешивают стеклянной
палочкой и производят измерение ЭДС; рассчитывают pH
по формуле (9).
Расчитывают теоретическое значение pH,
сравнивают с опытным и расчитывают процент ошибки.
Полученные данные:
|
Исследуемый
раствор
|
ЭДС,
В
|
pHпракт
|
pHтеор
|
Ошибка,
%
|
|
1. HCl 1Н
|
0,209
|
4,54
|
0
|
-
|
|
2. HCl 0,5Н
|
0,196
|
4,78
|
0,31
|
143,5
|
|
3. HCl 0,1Н
|
0,201
|
4,69
|
1
|
468
|
|
4.
Раствор Вейбеля
|
0,206
|
4,63
|
2,04
|
123,5
|
|
5. HCl 0,01Н
|
0,205
|
4,59
|
2
|
130,5
|
Расчёты:
Теоретическое значение pH:
1. 
. 
. 
. 
Практическое значение pH:
1. 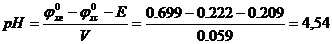
. 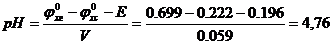
. 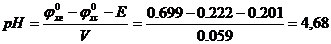
. 
. 
Относительная ошибка:
1. 
. 
. 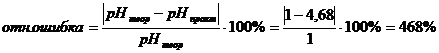
. 