Порівняння вмісту деяких металів у водах Дніпродзержинського та Запорізького водосховищ
Міністерство освіти і науки,
молоді та спорту України
Головне управління освіти і
науки Дніпропетровської облдержадміністрації
Комунальний позашкільний
навчальний заклад
«Мала академія наук
учнівської молоді Дніпропетровської обласної ради»
Відділення: Біології і хімії
Секція: Загальна біологія
Порівняння вмісту деяких
металів у водах Дніпродзержинського та Запорізького водосховищ
Роботу виконала:
Липовська Катерина Михайлівна,
учениця 11-В класу
комунального закладу «Технічний ліцей
м. Дніпродзержинська»
Науковий керівник:
Деміх Надія Олександрівна,
керівник гуртка «Основи біології»
КЗ «ДЕЦ м. Дніпродзержинська»
Дніпропетровськ 2013
Зміст
Вступ
. Фізико-географічна характеристика
Дніпродзержинського водосховища
. Забруднювачі води. Важкі метали, характеристика
впливу важких металів на біологічні об’єкти
.1 Поняття важких металів
.2 Важкі метали в екосистемах прісних водойм.
Токсикологічна характеристика деяких важких металів
. Практична частина
.1 Аналіз показників кількості важких металів у Дніпродзержинському
водосховищі, порівняння вмісту важких металів в Дніпродзержинському та
Запорізькому водосховищах
.2 Порівняння показників двох точок
Дніпродзержинського та Запорізького водосховища на кількість металів
Висновки
Перелік посилань
Додатки
Вступ
На сьогоднішній день води Дніпродзержинського водосховища
потребують глибокого дослідження, оскільки через значну кількість промислових
об’єктів в м. Дніпродзержинську, зростає загальне забруднення водних об’єктів.
Аналіз води - метод дослідження властивостей і якостей води.
Застосовується для визначення кількості різних речовин у складі води, що
знаходиться в контакті з людиною в промислових і в побутових цілях, або в
наукових.
Якість води - це показник ступеня забрудненості водного
об’єкта, який визначають за сукупністю встановлених показників складу і
властивостей води (фізичних, хімічних, біологічних, бактеріологічних) і який
задовольняє вимоги споживачів. Показники якості води поділяють на фізичні,
хімічні, гідробіологічні, бактеріологічні. Іншою формою класифікації показників
її якості є їх розподіл на загальні та специфічні.
Зміст речовини, розчиненої у воді, що не перевищує
встановлених норм, забруднювачем не є. Це відноситься до будь-якої води - від
дистильованої до неочищеної стічної. Тільки в разі перевищення ГДК речовина є
забруднювачем. ГДВ/ГДС - екологічні нормативи, що визначають граничні межі
викидів в атмосферне повітря і скидів у водні об'єкти забруднюючих речовин,
інших шкідливих впливів на навколишнє середовище. Цей норматив встановлюється
для кожного стаціонару, джерела забруднення і є диференційованим щодо кожної
забруднюючої речовини і кожного фактора фізичного або біологічного впливу.
Норми вмісту різних речовин для різних типів вод
відрізняються. Речовини, які можуть міститися у воді, можна класифікувати
по-різному. Одна із класифікацій - за змістом у воді макро- і мікроелементів.
Солевміст або мінералізація води складається з
макроелементів, присутніх в десятках і навіть сотнях мг на літр. Це, як
правило, хлориди, сульфати, гідрокарбонати (аніони), кальцій, магній, калій,
натрій (катіони). Макроелементи мають оптимальні радіуси іонів та атомів,
оптимальну електронну будову для утворення біомолекул. Вміст цих речовин у воді
може варіювати.
Мікроелементи містяться у воді в дуже низьких концентраціях
від десятих часток мг в літрі, до мкг, і підрозділяються на необхідні, токсичні
і ессенціальні. До мікроелементів належать, наприклад, важкі метали, ГДК деяких
з них дуже жорстка. Їх дія на живий організм може проявитися навіть у дуже невеликих
дозах, безпечні концентрації занадто малі, тому додаткове потрапляння у воду
токсичних і ессенціальних елементів може негативно позначитися на здоров'ї
споживачів.
В наукових дослідженнях було встановлено, що в Україні понад
13% водних об'єктів, за концентрацією у них Pb і майже 60% за вмістом Zn,
ідентифіковані за класом якості як "забруднені", "брудні"
та "дуже брудні". Токсичне забруднення поверхневих вод Cu, відносить
43% водойм до "забруднених", а 28% - до "брудних" і
"дуже брудних". Близько 80% водойм за вмістом Cd характеризуються як
"забруднені", "брудні" і "дуже брудні".[6]
Важкі метали особливо небезпечні по впливу на екологічну
систему водойм, маючи здатність накопичуватись у харчових ланцюгах водойми.
Більшість важких металів мають мутагенну і токсичну дію, різко зменшують
інтенсивність біохімічних процесів у водоймах. Деякі важкі метали, навпаки,
входять до складу біологічних сполук, як необхідні для здоров'я речовини. Але
надлишок їх у воді призводить до негативних наслідків.
Джерел забруднення води багато, основними з них є:
стічні води промислових підприємств;
побутові стоки комунального господарства;
стічні води сільського господарства;
води шахт, нафтопромислів, рудників;
відходи виробництв при видобутку різних корисних копалин;
відходи деревини в деревообробній промисловості;
скиди водного і залізничного транспорту тощо.
З усіх джерел забруднення води основне значення мають
виробничі стічні води. Промислові викиди, якщо порівняти їх із побутовими,
будуть більш токсичні і чинитимуть більш негативний вплив на навколишнє
середовище. Адже до промислових викидів відносяться викиди теплових
електростанцій, різноманітних промислових підприємств.
Якою б довершеною не була очистка стічних вод, але значна
кількість важких металів потрапляє в природне середовище.
Найбільшими забруднювачами поверхневих і підземних вод є:
хімічна промисловість;
чорна металургія;
кольорова металургія;
коксохімія;
важке, енергетичне і транспортне машинобудування;
комунальне і сільське господарство.
В залежності від виду підприємства буде змінюватися картина
викидів, в викидах автопідприємств переважають викиди сполук свинцю,
гальванічні цехи скидають в стічні води сполуки цинку, кобальту, кадмію.
В м. Дніпродзержинську діють такі великі промислові
підприємства: 1) ВАТ Дніпровський металургійний комбінат ім. Дзержинського; 2)
ВАТ «ДніпроАзот»; 3) ВАТ «Дніпродзержинський коксохімічний завод»; 4) ВАТ
«Дніпровагонмаш»; 5) ВО «Придніпровський хімічний завод»; 6)ВАТ «Баглійкокс»;
7) ТзОВ «Дніпровський автобусний завод».
Також відомо, що на території
колишнього Придніпровського заводу зберігається більше 30 мільйонів тон
радіоактивних відходів переробки уранових руд.
Оскільки у річку після очистки може
впадати значна кількість відходів підприємств (а відомо, що тільки Дніпровський
металургійний комбінат скидає більше 120 мільйонів кубічних метрів щороку)
потрібно контролювати вміст важких металів в Дніпродзержинському водосховищі.
Актуальність роботи в тому, що Дніпродзержинське водосховище
на наявність важких металів у воді досліджене не на високому рівні й потреба
удосконалювати знання у цій сфері існує і досі. Адже, використання водосховища
комплексне - для енергетики, водного транспорту, зрошування, водопостачання,
рибництва і рекреації. І тому якість води у ньому
повинна бути на належному рівні.
Мета роботи - прийняти участь в здійсненні
комплексного аналізу води з кількох точок Дніпродзержинського водосховища на
наявність важких металів, порівняти отримані дані з даними Запорізького
водосховища та вивести з них висновок.
У зв’язку із зазначеною метою ставляться такі завдання :
· Розглянути, що ж розуміють
під поняттям «важкі метали», якою є їх біологічна роль та вплив на екологічну
систему водойм.
· Провести оцінку якості
поверхневих вод в двох точках Дніпродзержинського водосховища (у верхній -
створі селища Аули, і у нижній - створ селища Таромське) на вміст важких
металів (залізо, свинець, ртуть, кадмій, цинк, мідь) і відповідності їх вимогам
питного і рибогосподарського використання.
· дослідити тенденцію змін якості поверхневих
вод Дніпродзержинського водосховища;
· Порівняти дві області Дніпра
- Дніпродзержинське та Запорізьке водосховище на наявність у них важких
металів;
Практичне значення роботи. Отримані дані можна використовувати
для подальшого дослідження гідрохімічного стану Дніпродзержинського
водосховища.
1. Фізико-географічна характеристика Дніпродзержинського
водосховища
Дніпродзержинське водосховище - одне з шістьох великих
українських водосховищ на Дніпрі. Розташоване частково у Кіровоградській,
Полтавській та Дніпропетровській областях.
Стік проходить транзитом, тому
коливання рівня не перевищують 0,5-1 м. Максимальні рівні спостерігаються у
період весняної повені.
Гребля завдовжки 35 км є однією з
найбільших у світі. Гребля розташована на захід від Дніпродзержинська. На ній
міститься Дніпродзержинська ГЕС, побудована у 1964 році.
Найбільші міста біля
Дніпродзержинського водосховища: Кременчук, Дніпродзержинськ, Комсомольськ і
Верхньодніпровськ.
Дніпродзержинське водосховище ділиться на три ділянки:
верхня ділянка - тягнеться від греблі Кременчуцького
водосховища до села Кам'яні Потоки. Вона являє собою затоплене русло Дніпра;
центральна ділянка - від села Кам'яні Потоки до села
Бородаївка - займає більше половини площі водосховища;
нижня ділянка - від села Бородаївка до греблі Дніпродзержинського
водосховища.
У Дніпродзержинське водосховище впадають вісім приток. У
Дніпродзержинське водосховище впадають річки: Ворскла, Псел, Орель (старе
гирло), Омельник, Домоткань, Самоткань.
У водосховищі поширені 177 видів водоростей та 39 видів вищих
водяних рослин, що займають площу близько 55 км².
Багато
планктонних і донних безхребетних (найпростіші, ракоподібні, молюски, комахи та
інші). Водиться 30 видів риб.
У Дніпродзержинському водосховищі переважають: плотва, окунь,
лящ, краснопірка, уклея, язь, ялець, вівсянка, густера, жерех, щука, судак,
сом.
Рідше зустрічаються: головень, лин, піскар, гірчак, сазан,
голець, щиповка, колючка, йорж, бички.
2. Забруднювачі води. Важкі метали, характеристика впливу
важких металів на біологічні об’єкти
Забруднювачами вважаються розчинені у воді речовини, вміст
яких перевищує встановлені норми.
Важкі метали відносяться до пріоритетних забруднюючих
речовин, спостереження за якими обов'язкове у всіх середовищах.
Надлишки фосфору та азоту у воді призводять до її цвітіння та
порушення біологічної рівноваги у водоймах. Органічні забруднення часто
призводять до зв'язування кисню у воді, загибелі живих організмів та
фітопланктону.
Господарсько-побутові стоки призводять до механічного,
хімічного та біологічного забруднення води, яке може викликати кишково-шлункові
захворювання (холеру, тиф) та захворювання печінки (гепатит). Особливо
небезпечні стічні води пунктів санітарної обробки білизни та спецодягу, стоки
лікарень тощо.
Радіоактивні речовини, потрапляючи до води, викликають її
іонізацію, що негативно відбивається на розвитку живих організмів. Більш того,
фітопланктон та риби здатні засвоювати велику кількість радіоактивних речовин
та накопичувати їх у своєму організмі. Споживання такої риби небезпечне для здоров’я
людей.
2.1
Поняття важких металів
Поняття «важкі метали» часто зустрічається у літературі, але
трактування цього поняття у різних авторів не співпадає. Тому визначимося, які
ж саме метали відносять до важких металі, які їхні характеристики є визначальними
при їх класифікації.
Термін «важкі метали», що характеризує широку групу
забруднюючих речовин, пов'язаний з високою відносною атомною масою елемента. Ця
характеристика звичайно ототожнюється з уявленням про високу токсичність. Також
однією із ознак «важких металів» є їхня густина. У сучасній кольоровій
металургії розрізняють важкі кольорові метали - густиною 7,14 - 21,4 г/см3
(цинк, олово, мідь, свинець, хром, кадмій, кобальт й ін.) і легкі кольорові
метали - густиною 0,53 - 3,5 г/см3 (літій, берилій й ін.).
Іншими ознаками для класифікації є поширеність у природному
середовищі, ступінь залученості в природні та техногенні цикли.
Відповідно до однієї класифікації [3], до групи важких
металів належить більше 40 елементів з високою відносною атомною масою й
густиною більшою 6 г/см3. По іншій класифікації, у цю групу
включають кольорові метали із густиною більшою, ніж у заліза (свинець, мідь,
цинк, нікель, кадмій, кобальт, олово, сурма, вісмут, ртуть).
Відповідно до відомостей, представлених в довіднику [4] до
важких металів віднесені елементи, густина яких більша за 5 г/см3.
Якщо виходити із цього показника, важкими можна вважати 43 з 84 металів
Періодичної системи хімічних елементів.
У деяких випадках під визначення важких металів потрапляють
елементи, які відносяться до крихких (наприклад, вісмут) чи металоїдів
(наприклад, миш'як).
У роботах, присвячених проблемам забруднення навколишнього
природного середовища та екологічного моніторингу, на сьогоднішній день до
важких металів відносять більше 40 металів періодичної системи з атомною масою
понад 50 атомних одиниць: V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Mo, Cd, Sn, Hg, Pb, Bi
та ін.
При цьому важливу роль у категоріюванні важких металів
відіграють такі умови : їх висока токсичність для живих організмів у відносно
низьких концентраціях, а також здатність до біоакумуляції і біомагніфікації.
Практично всі метали, які потрапляють під це визначення (за винятком свинцю,
ртуті, кадмію та вісмуту, біологічна роль яких на даний момент вивчається),
активно беруть участь у біологічних процесах, входять до складу багатьох
ферментів. За класифікацією Н. Реймерса, важкими слід вважати метали з густиною
більше 8 г/см3. Таким чином, до важких металів відносяться Pb, Cu, Zn, Ni, Cd,
Co, Sb, Sn, Bi, Hg. [5]
На думку дослідників, зайнятих практичною діяльністю,
пов'язаною з організацією спостережень за станом і забрудненням навколишнього
середовища, сполуки цих елементів далеко не рівнозначні як забруднюючі
речовини. Тому в багатьох роботах відбувається звуження рамок групи важких металів,
відповідно до критеріїв пріоритетності, зумовленими напрямом і специфікою
робіт. Так в роботах Ю.А. Ізраеля в переліку хімічних речовин, що підлягають
визначенню в природних середовищах на фонових станціях у біосферних
заповідниках, в розділі «важкі метали» названі Pb, Hg, Cd, As. З іншого боку,
відповідно до рішення Цільової групи з викидів важких металів, що працює під
егідою Європейської Економічної Комісії ООН та займається збором і аналізом
інформації про викиди забруднюючих речовин в європейських країнах, тільки Zn,
As, Se та Sb були віднесені до важких металів. За визначенням М. Реймерса
окремо від важких металів стоять благородні і рідкісні метали, відповідно
залишаються тільки Pb, Cu, Zn, Ni, Cd, Co, Sb, Sn, Bi, Hg. У прикладних роботах
до числа важких металів найчастіше додають Pt, Ag, W, Fe, Au, Mn. [5]
Іони металів є неодмінними компонентами природних водойм.
Залежно від умов середовища (pH, окисно-відновного потенціалу, наявності
лігандів) вони існують в різних ступенях окислення і входять до складу
різноманітних неорганічних і металоорганічних сполук, які можуть бути істинно
розчиненими, колоїдно-дисперсними чи входити до складу мінеральних та
органічних суспензій.
Істинно розчинені форми металів, у свою чергу, досить
різноманітні, що пов'язано з процесами гідролізу, гідролітичної полімеризації і
комплексоутворення з різними лігандами. Відповідно, як каталітичні властивості
металів, так і їх доступність для водних мікроорганізмів залежать від форм
існування їх у водній екосистемі.
Багато металів утворюють досить міцні комплекси з органікою;
ці комплекси є однією з найважливіших форм міграції елементів у природних
водах. Більшість органічних комплексів утворюються за хелатними циклами і є
стійкими. Комплекси, утворені ґрунтовими кислотами із солями заліза, алюмінію,
титану, урану, ванадію, міді, молібдену та інших важких металів, відносно добре
розчинні в умовах нейтрального, слабкокислого і слабколужного середовищ. Тому
металорганічні комплекси здатні мігрувати в природних водах на досить значні
відстані. Особливо важливо це для маломінералізованих і в першу чергу
поверхневих вод, в яких утворення інших комплексів неможливе.
Для розуміння факторів, які регулюють концентрацію металів в
природних водах, їх хімічну реакційну здатність, біологічну доступність і
токсичність, необхідно знати не тільки валовий вміст, а й частку вільних і
зв'язаних форм металу.
Перехід металів у водному середовищі в металокомплексну форму
має три наслідки:
1. може відбуватися збільшення сумарної концентрації
іонів металу за рахунок переходу його в розчин з донних відкладень;
2. мембранна проникність комплексних іонів може істотно
відрізнятися від проникності гідратованих іонів;
. токсичність металу в результаті комплексоутворення
може сильно змінитися.
Так, хелатні форми Cu, Cd, Hg менш токсичні, ніж вільні іони.
Як вже вище вказувалося, джерелами забруднення вод важкими
металами служать стічні води гальванічних цехів, підприємств гірничодобувної,
чорної і кольорової металургії, машинобудівних заводів. Важкі метали входять до
складу добрив і пестицидів і можуть потрапляти у водойми разом зі стоками з
сільськогосподарських угідь.
Підвищення концентрації важких металів у природних водах
часто пов'язане з іншими видами забруднення, наприклад, з закисленням.
Випадання кислотних опадів сприяє зниженню значення рН і переходу металів із
сорбованого на мінеральних і органічних речовинах стану у вільний.[9]
Встановлено, що найкращими акумуляторами важких металів є
біотичні складові гідроекосистеми рослини (водорості), та менше молюски, що
дозволяє зробити висновок про значну роль біотичних складових у перерозподілі
та акумуляції важких металів у гідроекосистемах. Зокрема, водорості можна
використовувати для моніторингу забруднених водойм. За результатами досліджень
у модельній гідро екосистемі, рослини (водорості) накопичують важкі метали лише
до певного критичного рівня, відповідно до гідрохімічного стану водойми, а
згодом відмирають, підвищуючи, концентрацію важких металів у воді та донних
відкладах. [10]
2.2
Важкі метали в екосистемах прісних водойм. Токсикологічна характеристика деяких
важких металів
За останні 50 років під впливом діяльності людини
(широкомасштабні меліорації, хімізація сільського господарства, збільшення
скидів стічних вод тощо) спостерігається суттєве забруднення водних об’єктів.
Внаслідок зростання антропогенного навантаження (АН) погіршуються як кількісні,
так і якісні показники поверхневих вод. Відбувається зростання мінералізації,
надходження сполук азоту, фосфору, а також специфічних речовин токсичної дії,
де в багатьох випадках першочерговий вплив мають важкі метали (ВМ). Якість вод
у більшості водних об’єктів України за станом хімічного і бактеріального
забруднення класифікується як забруднена і брудна (IV - V класи забрудненості). Найгостріший
екологічний стан спостерігається в басейнах р. Дніпро, Сіверського Дінця,
річках Приазов’я. Вода тут класифікується, як дуже брудна (VI клас забрудненості). Порушення норм
якості води досягло рівнів, які ведуть до деградації водних екосистем, зниження
продуктивності водойм, не кажучи вже про здоров’я населення водних басейнів.[7]
Дослідженнями Будза М.Д., Гриба Й.В., Клименка М.О, Хвесика
М.А., Мальцева В.І., Мольчака Я.О., Поліщука В.В., Мєльник В.Й., та інших
відомих вчених з’ясовано, що інтенсивне погіршення якості поверхневих вод під
впливом антропогенних чинників мало місце до 1990 року, а після зменшення
темпів економічного розвитку, була помічена тенденція деякого поліпшення їх
якості, завдяки самоочисній здатності річок. Проте, виходячи з даних Гончарова
Г.Д., Мєтелєва В.В., Скорнякова В.А., Осадчого В.І., має місце ефект
накопичення токсикантів у гідробіонтах, гідрофітах та донних відкладах,
внаслідок чого виникає реальна загроза для питного та рибогосподарського
водопостачання. У зв’язку з цим, постає необхідність
у вивченні питань міграції ВМ у водних екосистемах. Особливої уваги
заслуговують питання розподілу вмісту ВМ у ланцюгах живлення, закономірності їх
накопичення в різних видах риб та розподілу в тканинах їх організму. За рахунок
біоакумуляції, ВМ можуть бути вилучені із водної екосистеми разом з рибою,
проте понаднормативний вміст ВМ в рибній продукції може скласти загрозу людині.
[6]
Розглянемо властивості, шляхи попадання у водойми, гранично
допустимі концентрації деяких важких металів. Насамперед становлять інтерес ті
метали, які найбільше широко й у значних об'ємах використаються у виробничій
діяльності й у результаті нагромадження в зовнішньому середовищі становлять
серйозну небезпеку з огляду їх високої біологічної активності й токсичних
властивостей. До них відносять залізо, свинець, ртуть, кадмій, цинк, нікель,
мідь.
ЗАЛІЗО
Головними джерелами сполук заліза в поверхневих водах є
процеси хімічного вивітрювання гірських порід, що супроводжуються їх механічним
руйнуванням і розчиненням. У процесі взаємодії з мінеральними і органічними
речовинами, що містяться в природних водах, утворюється складний комплекс
сполук заліза, що знаходяться у воді в розчиненому, колоїдному і завислому
станах. Значні кількості заліза надходять з підземними стоками і зі стічними
водами підприємств металургійної, металообробної, текстильної, лакофарбової
промисловості та з сільськогосподарськими стоками.
Фазові рівноваги між формами сполук заліза у розчинах
залежать від хімічного складу води, РН, Eh і в деякій мере від температури.
Розчинене залізо у стічних та природних водах представлене сполуками, що
перебувають в іонній формі, у вигляді гідроксокомплексів й комплексів з
розчиненими неорганічними й органічними речовинами природних вод. В іонній
формі мігрує головним чином Fe (II), а Fe (III) під час відсутності
комплексоутворювачів може в значних кількостях перебувати в розчиненому стані.
У результаті хімічного й біохімічного (при участі
залізобактерій) окиснення Fe (II) переходить в Fe (III), іони якого,
гідролізуючись, випадають в осад у вигляді Fe(OH)3. Як для іонів Fе2+,
так і для Fe3+ характерна здатність до утворення гідроксокомплексів
типу [Fe(OH)2]+, [Fe2(OH)2]4+,
[Fe(OH)3]+, [Fe2(OH)3]3+,
[Fe(OH)3]- і інших, співіснуючих у розчині в різних
концентраціях залежно від РН. Основною формою знаходження Fe3+ у
поверхневих водах є комплексні сполуки його з розчиненими неорганічними й
органічними комплексоутворювачами, головним чином гумусовими речовинами. При РН
= 8,0 основною формою знаходження іонів тривалентного заліза в розчинах є
Fe(OH)3.
Вміст заліза в поверхневих водах суші складає десяті частки
міліграма, поблизу боліт - одиниці міліграмів. Підвищений вміст заліза
спостерігається в болотних водах, у яких воно перебуває у вигляді комплексів із
солями гумінових кислот - гуматів.
Найбільші концентрації заліза (до декількох десятків і сотень
міліграмів у 1 дм3) спостерігаються в підземних водах з низькими
значеннями рН.
Будучи біологічно активним елементом, залізо в певній мірі
впливає на інтенсивність розвитку фітопланктону та якісний склад мікрофлори у
водоймі.
Високий вміст заліза у воді призводить до несприятливого
впливу на шкіру людини, може позначитися на морфологічному складі крові, сприяє
виникненню алергічних реакцій. Також залізо негативно впливає на репродуктивну
систему.
Концентрація заліза схильна до помітних сезонних коливань.
Зазвичай у водоймах з високою біологічною продуктивністю в період літньої і
зимової стагнації помітне збільшення концентрації заліза в придонних шарах
води. Осінньо-весняне перемішування водних мас (гомотермія) супроводжується
окисленням Fe (II) у Fе (III) і випаданням останнього у вигляді Fe(OH)3.
Вміст заліза у воді вище 1-2 мг Fe/л значно погіршує
органолептичні властивості, надаючи їй неприємний в'язкий смак, і робить воду
малопридатною для використання в технічних цілях. ГДК заліза становить 0,3 мг
Fe/дм3 (лімітуючий показник шкідливості - органолептичний), ГДК для
заліза у воді водойми, яка використовується в рибогосподарських цілях, - 0,1
мг/дм3.[8]
КАДМІЙ
У природні води надходить при вилуговуванні ґрунтів,
поліметалевих і мідних руд, в результаті розкладання водних організмів, здатних
його накопичувати.
Сполуки кадмію виносяться в поверхневі води зі стічними
водами свинцево-цинкових заводів, гірничо-збагачувальних комбінатів, ряду
хімічних підприємств (виробництво сірчаної кислоти), гальванічного виробництва,
а також із шахтними водами. Зниження концентрації розчинених сполук кадмію
відбувається за рахунок процесів сорбції водними організмами, випадання в осад гідроксида й карбонатів
кадмію.
Розчинені форми кадмію в стічних водах являють собою головним
чином мінеральні та органо-мінеральні комплекси.
Основною формою кадмію є його сорбовані сполуки. Значна частина кадмію може
мігрувати в складі клітин гідробіонтів.
У річкових незабруднених й слабко забруднених водах кадмій
утримується в субмікрограммових концентраціях, у забруднених і стічних водах
концентрація кадмію може досягати десятків мікрограмів в 1 дм3.
Сполуки кадмію відіграють важливу роль у процесі
життєдіяльності тварин і людини. У підвищених концентраціях токсичний, особливо
в сполученні з іншими токсичними речовинами [5], [8].
ГДК становить 0,001 мг/дм3, ГДК у воді водойми, яка
використовується в рибогосподарських цілях, - 0,0005 мг/дм3 (лімітуюча ознака
шкідливості - токсикологічна).
МІДЬ
Мідь - один з найважливіших мікроелементів. Фізіологічна
активність міді зв'язана головним чином із включенням її до складу активних
центрів окислювально-відновних ферментів. Недостатній вміст міді в ґрунтах
негативно впливає на синтез білків, жирів і вітамінів і сприяє безплідності
рослинних організмів. Мідь бере участь у процесі фотосинтезу й впливає на
засвоєння азоту рослинами. Разом з тим, надлишкові концентрації міді
несприятливо впливають на рослинні й тваринні організми.
У природних водах найбільше часто зустрічаються сполуки
Cu(II). Зі сполук Cu(I) найпоширеніші важкорозчинні у воді Cu2O, Cu2S,
CuCl. При наявності у водному середовищі лігандів, поряд з рівновагою
дисоціації гідроксиду, необхідно враховувати утворення різних комплексних
сполук, що перебувають у рівновазі з акваіонами міді.
Основним джерелом надходження міді в природні води є стічні
води підприємств хімічної, металургійної промисловості, шахтні води, альдегідні
реагенти, використовуються для знищення водоростей. Мідь може з'являтися в
результаті корозії мідних трубопроводів й інших споруд системи водопостачання.
У підземних водах вміст міді обумовлений взаємодією води з гірськими породами,
що її містять.
Гранично припустима концентрація міді у воді водойм
санітарно-побутового водокористування становить 0,1 мг/дм3
(лімітуюча ознака шкідливості - загальносанітарна), у воді рибогосподарських
водойм - 0,001 мг/дм3. [7].
СВИНЕЦЬ
Природними джерелами надходження свинцю в поверхневі води є
процеси розчинення деяких мінералів (галенітанглезит, церусит та ін.).
Значне підвищення вмісту свинцю в навколишньому середовищі (в
тому числі і в поверхневих водах) пов'язане зі спалюванням вугілля,
застосуванням тетраетилсвинцю як антидетонатора в моторному паливі, з виносом у
водні об'єкти зі стічними водами рудозбагачувальних фабрик, деяких
металургійних заводів, хімічних виробництв, шахт і т.д.
Свинець перебуває в воді у розчиненому й звішеному
(сорбованому) стані. У розчиненій формі зустрічається у вигляді мінеральних й
органо-мінеральних комплексів, а також простих іонів, у нерозчинній - у вигляді
сульфідів, сульфатів і карбонатів.
Істотними факторами зниження концентрації свинцю у воді є
адсорбція його нерозчиненими речовинами і осадження з ними у донні відкладення.
У числі інших металів свинець витягується і накопичується гідробіонтами.
Первинна детоксикуюча функція у водоростей за дії свинцю пригнічується. За дії
свинцю виявлено активацію зв'язування аміаку у зелених, і в синьо-зелених
водоростей. При цьому синтез глутаміну пригнічується, особливо у синьо-зелених
водоростей. Своєрідність реакції водоростей на свинець вказує на те, що при
інтоксикації цим металом пригнічуються як вегетативні функції клітин, так і
функціонування довготривалих систем формування толерантності водоростей до
аміаку.[8, 9]
Свинець - промислова отрута, здатний при несприятливих умовах
виявитися причиною отруєння. В організм людини проникає через органи травлення.
Виводиться з організму дуже повільно, внаслідок чого накопичується в костях,
печінці й нирках [9]. ГДК свинцю становить 0,03 мг/дм3.
Лімітуючий показник шкідливості свинцю -
санітарно-токсикологічний. ГДК свинцю становить 0,03 мг/дм3, ГДК у воді
водойми, яка використовується в рибогосподарських цілях, - 0,1 мг/дм3.
ЦИНК
Попадає в природні води в результаті природних процесів
руйнування і розчинення гірських порід та мінералів, а також із стічними водами
гірничо-збагачувальних комбінатів та гальванічних цехів, виробництв
пергаментного паперу, мінеральних фарб, віскозного волокна й ін.
У воді знаходиться в іонній формі або у формі мінеральних й
органічних комплексів. Іноді зустрічається в нерозчинній формі: у вигляді
гідроксида, карбонату, сульфіду й ін. Цинк відноситься до числа активних
мікроелементів, що впливають на ріст і нормальний розвиток організмів. У той же
час багато сполук цинку токсичні, насамперед його сульфат і хлорид.
ГДК
Zn2+ складає 1 мг/дм3 (лімітуючий показник шкідливості - органолептичний), ГДК
Zn2+ у воді водойми, яка використовується в рибогосподарських цілях, - 0,01
мг/дм3 (лімітуюча ознака шкідливості - токсикологічна).[7]
РТУТЬ
У поверхневі води сполуки ртуті надходять в результаті
вилуговування порід у районі ртутних родовищ, в процесі розкладання водних
організмів, що накопичують ртуть.
У поверхневих водах сполуки ртуті перебувають у розчиненому й
нерозчинному станах. Співвідношення між ними залежить від хімічного складу води
й значення РН. Нерозчинна ртуть являє собою сорбовані сполуки ртуті.
Розчиненими формами є недисоційовані молекули, комплексні органічні й
мінеральні сполуки.
Зниження концентрації розчинених сполук ртуті відбувається в
результаті вилучення їх багатьма прісноводними організмами, що мають здатність
накопичувати її в концентраціях, що у багато разів перевищують її вміст у воді,
а також процесів адсорбції завислими речовинами і донними відкладеннями. Ртуть
- типовий представник кумулятивних отрут.
Сполуки ртуті високотоксичні, насамперед через їх
ліофільність і здатність більш ефективно взаємодіяти з елементами
ферментативних систем організму. Вони вражають нервову систему людини,
викликають зміни з боку слизової оболонки, порушення рухової функції й секреції
шлунково-кишкового тракту, зміни в крові й ін. Бактеріальні процеси метилювання
спрямовані на утворення метилртутних сполук, які у багато разів більш токсичні
від мінеральних солей ртуті. Метилртутні сполуки накопичуються у рибі і можуть
потрапляти в організм людини.
ГДК ртуті становить 0,0005 мг/дм3 (лімітуюча ознака
шкідливості - санітарно-токсикологічна), ГДК у воді водойми, яка
використовується в рибогосподарських цілях, - 0,0001 мг/дм3.[9]
Останні 50 років під впливом діяльності людини
(широкомасштабні меліорації, хімізація сільського господарства, збільшення
скидів стічних вод тощо) спостерігається суттєве забруднення водних об’єктів.
Внаслідок зростання антропогенного навантаження погіршуються як кількісні, так
і якісні показники поверхневих вод. До водойм надходять, крім всього,
специфічні речовини токсичної дії, де в багатьох випадках першочерговий вплив
мають важкі метали, які включаються в ланцюги живлення водойми. Дослідження
Дніпродзержинського водосховища на кількість та динаміку коливань вмісту важких
металів є проблемою, потребуючою подальшого вивчення.
3. Практична частина
.1 Аналіз показників кількості важких металів у
Дніпродзержинському водосховищі, порівняння вмісту важких металів в
Дніпродзержинському та Запорізькому водосховищах
Розглянемо загальні показники кількості важких металів, за
період 2010-2012 років, у двох точках - створищах Аули та Таромське. Для цього
із додатків А, Б, В виведемо в окрему Табл.1 середні показники по кожному
металу в поверхневій та глибинній пробі.
Табл. 1
|
№ п/п
|
Назва створу, місця взяття проби
|
Залізо загальне, мг/дм куб.
|
Свинець, мг/дм куб.
|
Ртуть, мг/дм куб.
|
Кадмій, мг/дм куб.
|
Цинк, мг/дм куб.
|
Мідь, мг/дм куб.
|
|
1
|
2
|
4
|
5
|
6
|
7
|
8
|
9
|
|
Назва створу, місця взяття проби
|
|
1
|
створ селища Аули:
|
|
2010 рік
|
правий берег поверхнева
|
0,173
|
0,00145
|
0,0000145
|
0,000128
|
0,116
|
0,0013
|
|
правий берег глибинна
|
0,17
|
0,0012
|
0,0000149
|
0,000128
|
0,117
|
0,00142
|
|
2011 рік
|
правий берег поверхнева
|
0,135
|
0,00146
|
0,0000145
|
0,000121
|
0,152
|
0,0032
|
|
правий берег глибинна
|
0,13
|
0,00147
|
0,0000146
|
0,000149
|
0,154
|
0,0032
|
|
2012 (1-3)
|
правий берег поверхнева
|
0,09
|
0,00157
|
0,0000122
|
0,000124
|
0,184
|
0,00215
|
|
правий берег глибинна
|
0,087
|
0,00159
|
0,0000123
|
0,19
|
0,00222
|
|
2
|
створ селища Таромське:
|
|
2010 рік
|
правий берег поверхнева
|
0,167
|
0,00145
|
0,0000153
|
0,00013
|
0,12
|
0,00156
|
|
правий берег глибинна
|
0,17
|
0,00155
|
0,000157
|
0,000136
|
0,121
|
0,00162
|
|
2011 рік
|
правий берег поверхнева
|
0,138
|
0,00152
|
0,0000193
|
0,000149
|
0,166
|
0,0026
|
|
правий берег глибинна
|
0,135
|
0,00156
|
0,0000192
|
0,000153
|
0,169
|
0,00273
|
|
2012 (1-3)
|
правий берег поверхнева
|
0,18
|
0,00159
|
0,0000128
|
0,00013
|
0,184
|
0,00213
|
|
правий берег глибинна
|
0,18
|
0,00103
|
0,000013
|
0,000133
|
0,203
|
0,00232
|
Залізо загальне: поверхнева проба
Аули
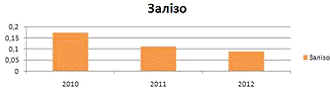
Середнє значення - 0,124.
Таромське
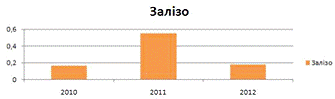
Середнє значення - 0,3.
Залізо загальне: глибинна
Аули

Середнє значення - 0,128. Вище, ніж в поверхневій воді на
0,004.
Таромське

Середнє значення - 0,161. Нижче, ніж у поверхневій на 0,139.
Мідь: поверхнева
Аули

Середнє значення - 0,0022.
Таромське

Середнє значення - 0,00258.
Аули (Середнє значення - 0,00652. Значно більший показник,
ніж у поверховій - на 0,00432)
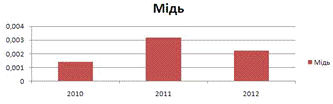
Таромське
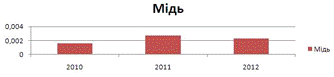
Середнє значення - 0,00222. Набагато менший показник, в
порівнянні з поверхневою - на 0,00036.
Ртуть: поверхнева
Аули (Середнє значення - 0,0000136)

Таромське (Середнє значення - 0,00001)

Ртуть: на глибині
Аули (Середнє значення - 0,000013)
Таромське (Середнє значення - 0,0000159)
Аналізуючи дані я помітила, що у точці Таромське у 2011 році
було помічено максимальний вміст ртуті. Особливих відмінностей між середніми
показниками поверхневої ті глибинної води не помічено. За Додатком Б нормою
ртуті є показник від 0,0005-0,002 мг/ дм3. Отримані дані набагато
менші, й тому ртуть не можна вважати забрудником.
Цинк: поверхнева
Аули (Середнє значення - 0,153)

Таромське (Середнє значення - 0,16)

Цинк: глибинна
Аули (Середнє значення - 0,156. Показник трохи перевищує
значення поверхневої проби)
Таромське(Середнє значення - 0,163. Норми для ГДК Для водойм
господарсько-побутового використання (Додаток В) не перевищує)
Свинець: поверхнева
Аули(Середнє значення - 0,0014)

Таромське(Середнє значення - 0,00152)

Свинець: на глибині
Аули (Середнє значення - 0,00141)
Таромське (Середнє значення - 0,00154)
Порівнюючи з ГДК Для водойм господарсько-побутового
використання (ГДКГП) (Додаток В) показники Дніпродзержинського
водосховища достатньо низькі. Якщо ж розглянути Додаток Б, то допустимою нормою
свинця є від 0,01-0,05 мг/ дм3, і отримані показники ніяк її не
перевищують.
Розглянемо динаміку зміни кількості важких металів в
осінньо-весняний період в точці створища Аули в 2011 році(Додаток А)
Залізо
Поверхнева:
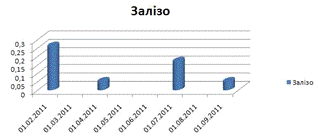
Глибинна:
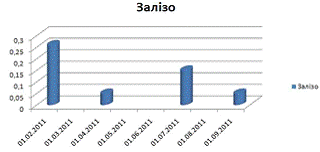
Згідно з графіками можна побачити, що кількість заліза різко
спадає в квітні, після чого в липні знову зростає. Якщо порівняти різницю
показів кількості заліза в різні періоди з періодами відмирання водної
рослинності, то між ними можна помітити тісну залежність.
Мідь
Поверхнева:
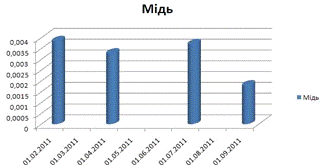
Глибинна:

Тут не видно таких різких сачків кількості міді на протязі
всього року. Хіба що, його кількість злегка коливається в ті ж періоди, що й
залізо.
Свинець
Поверхнева:
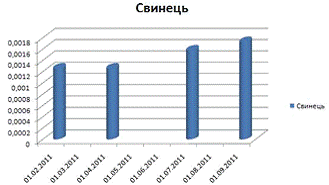
Глибинна:

Кількість свинцю поступово збільшується від лютого до
вересня. Це суттєво відрізняється від попередніх
Ртуть
Поверхнева:

Глибинна:
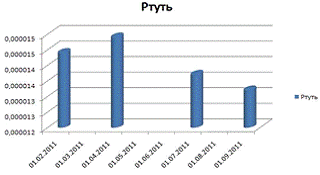
Кількість ртуті у воді різко збільшується з лютого на
квітень, після чого поступово зменшується. Можна припустити, що з початку весни
і на протязі року відбувалися викиди забруднюючих речовин, що спричинили
стабільне підвищення рівня ртуті у воді.
Цинк:
Поверхнева:

Глибинна:
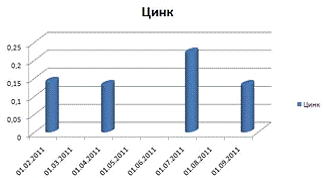
Цинк знаходиться в однаковій кількості і на поверхні, і на
глибині. Досліджуючи графік можна побачити, що відбулося різке підвищення цинку
в середині літа. Це може бути спричинено викидом забруднюючих речовин.
.2 Порівняння показників двох точок Дніпродзержинського та
Запорізького водосховища на кількість металів
токсикологічний важкий метал водосховище
Візьмемо показники свинцю, цинку, міді, кадмію та заліза з
двох точок: одну з Дніпродзержинського водосховища, другу - з Запорізького. Це
крайні точки - створ селища Таромське та село Військове. Період з 2010-2011
років (Додаток А,Є).
Свинець
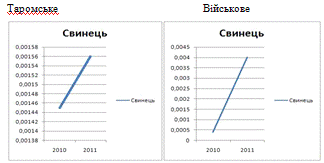
Цинк
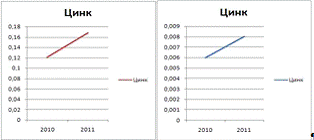
Мідь
Залізо

Кадмій

Діаграми і графіки чітко дають змогу зрозуміти, що в
порівнянні с Запорізьким водосховищем, у Дніпродзержинському підвищена
кількість таких металів як цинк, залізо і мідь. Свинець та кадмій у більшій
кількості спостерігається в Запорізькому водосховищі.
Висновки
В
ході роботи були проаналізовані науково-теоретичні джерела та статистичні дані
по якості поверхневих вод Дніпродзержинського водосховища, за матеріалами
Дніпродзержинської міської СЕС, та надані кафедрою гідробіології ДНУ матеріали
по дослідженню Запорізького водосховища. Проведений польовий збір зразків
поверхневих риб, що передані до ДНУ, аналітичні та статистичні дослідження
отриманих результатів. У результаті проведеного дослідження прийшли до таких
висновків і узагальнень :
1. Проаналізувавши показники двох точок Дніпродзержинського
водосховища на кількість металів (створ селища Аули і Таромське) було помічено,
що у нижній точці підвищений вміст металів. Це можна пояснити стоками
підприємств, що забруднюють воду.
. Загальний гідрохімічний стан Дніпродзержинського
водосховища можна вважати стабільним.
. Запорізьке і Дніпродзержинське водосховище не сильно
відрізняються один від одного показниками кількості металів у воді. Проте є
метали, що переважають у Дніпродзержинському водосховищі, а є ті, що в більшій
кількості спостерігаються у Запорізькому.
. Існує багато методів очищення стоків від забруднення
важкими металами: природне, хімічне, іонне, електрохімічне, екстракційне,
адсорбційне, флотаційне, біологічне. Проте краще контролювати кількість викидів
забруднювачів у воду, аніж постійно піддавати її очистці.
. Контроль за кількість важких металів у стічні води є дуже
важливим фактором для збереження цілісного водного середовища. Адже, надмірна
кількість металів у воді порушує стан гомеостазу живих організмів, а у риб, ще
й накопичується в організмі.
Перелік посилань
1. Географічна енциклопедія України: в 3-х томах /
Редколегія: О. М. Маринич (відпов. ред.) та ін. - К.:«Українська радянська
енциклопедія» імені М. П. Бажана, 1989.
2. Історія
міст і сіл Української РСР. Том 4. Дніпропетровська область. - К.: Головна
редакція УРЕ АН УРСР, 1971. - С. 222-247
3. Ритчи Г.
М., Эшбрук А. В. "Экстракция: принципы и применение в металлургии."
Пер. с англ. - М.: Металлургия, 1983.
. Химия:
Справочное издание под ред. В. Шретер, К.-Х, Лаутеншлегер, Х. Бибрак и др.:
Пер. с нем. - М.: Химия, 1989.- 648 с.
. Лурье Ю. Ю.
Унифицированные методы анализа вод. - М.: Химия, 1973, - 376 с.
6.
Бєдункова О.О. Міграція важких металів у водних екосистемах (на прикладі річки
Замчисько) : дис... канд. с.-г. наук: 03.00.16 / Національний ун-т водного
господарства та природокористування. - Рівне, 2006. - 223арк.
.
С.С. Маліков. Загальні заходи охорони водних об'єктів України з аналізом
закордонного досвіду. «Вісник Донбаської національної академії будівництва і
архітектури». Випуск 2010-3(83).
Інтернет-ресурси:
8. #"703293.files/image030.gif">
Додаток Д
Гранично допустимі концентрації (ГДК) гідрохімічних
показників
|
№
|
Гідрохімічний показник
|
ГДК
|
|
|
Для водойм рибогосподарського призначення1 (ГДКРГ)
|
Для водойм господарсько-побутового використання2 (ГДКГП)
|
|
1
|
Завислі речовини, мг/дм3
|
--------
|
0,25-0,75 від фонових значень
|
|
2
|
Розчинений кисень, мгО/дм3
|
--------
|
>4,0
|
|
3
|
Водневий показник,од.pH
|
6,5 - 8,5
|
6,5 - 8,5
|
|
4
|
БСК5, мгО2/дм3
|
--------
|
3,0
|
|
5
|
ХСК, мгО/дм3
|
--------
|
15,0
|
|
6
|
Сума іонів, мг/дм3
|
--------
|
1000
|
|
7
|
Хлоридні іони, мг/дм3
|
300
|
350
|
|
8
|
Сульфатні іони, мг/дм3
|
100
|
500
|
|
9
|
Іони магнію, мг/дм3
|
40
|
50
|
|
10
|
Іони кальцію, мг/дм3
|
180
|
--------
|
|
11
|
Іони натрію, мг/дм3
|
200
|
|
12
|
Азот амонійний, мг/дм3
|
0,39
|
1,5
|
|
13
|
Азот нітратний, мг/дм3
|
9,0
|
10,0
|
|
14
|
Азот нітритний, мг/дм3
|
0,02
|
1,0
|
|
15
|
Фосфатні іони, мг/дм3
|
--------
|
3,5
|
|
16
|
Мідь, мг/дм3
|
0,001
|
1,0
|
|
17
|
Цинк, мг/дм3
|
0,01
|
1
|
|
18
|
Марганець, мг/дм3
|
0,01
|
0,1
|
|
19
|
Хром загальний, мг/дм3
|
0,001
|
0,05
|
|
20
|
Свинець, мг/дм3
|
0,1
|
0,03
|
|
21
|
Нікель, мг/дм3
|
0,01
|
0,1
|
|
22
|
Кадмій, мг/дм3
|
0,005
|
0,001
|
|
23
|
Залізо загальне, мг/дм3
|
0,1
|
0,3
|
|
24
|
Нафтопродукти, мг/дм3
|
0,05
|
0,3
|
|
25
|
СПАР, мг/дм3
|
0,2
|
не нормується
|
|
26
|
Феноли, мг/дм3
|
0,001
|
0,001
|
1Обобщенный
перечень предельно допустимых концентраций (ПДК) и ориентировочно безопасных
уровней (ОБУВ) вредных веществ для воды рыбохозяйственных водоемов. Москва,
1990 г.
2Санитарные
правила и нормы охраны поверхностных вод от загрязнения СанПиН №4630-88.
Министерство здравоохранения СССР, Москва, ЗЗ, 1988 г.