Накопление хрома в донных отложениях водоёмов пригородной зоны отдыха
РЕФЕРАТ
Ключевые слова: тяжелые металлы, микроэлементы,
хром, донные отложения, осадки, седиментогенез, загрязнение, водоемы, озера.
Объект исследований: донные отложения водоемов
города Гомеля.
Метод исследования: эмиссионный спектральный
анализ микроколичеств хрома.
Цель работы: установление факторов, влияющих на
накопление хрома в донных отложениях водоемов г. Гомеля.
Результаты исследований: Установлено наибольшее
содержание хрома в донных отложениях оз.У-образное (131,8 мг/кг). Содержание
хрома в донных отложениях зависит как от их химического состава, так и от
возможного антропогенного поступления тяжелых металлов в водоемы. Наибольшее
влияние на содержание хрома в донных отложениях водоемов оказывает количество
органического вещества и концентрация окиси магния. Установлена прямая
корреляционная связь концентрации хрома и окиси магния в донных отложениях.
Накопление хрома в донных осадках озер Круглое, У-образное, Волотовское, Шапор,
Дедно зависит не только от химического состава отложений, но, очевидно,
обусловливается и дополнительным внешним источником поступления. Полученные
результаты могут быть использованы для оценки степени загрязнения донных
отложений тяжелыми металлами и прогноза экологической ситуации в отношении
водоемов города.
ВВЕДЕНИЕ
Развитие промышленности и сельского хозяйства в
последние десятилетия шло в основном с использованием традиционных методов без
особого учета современных экологических требований. Все это привело к проблеме
качества водных ресурсов, так как они наиболее подвержены антропогенному
прессу. Донные отложения водоемов играют значительную роль в формировании их
гидрохимического режима, являясь либо аккумулятором веществ-загрязнителей, либо
источником их поступления в поверхностные воды. Достаточно сильно выражена накопительная
способность донных отложений водоемов в отношении микроэлементов, в частности
тяжелых металлов. Вместе с тем, в определенных условиях, содержание многих
микроэлементов в природных объектах может достигать критических величин,
переводя эти элементы в разряд токсикантов. В этом аспекте донные отложения
являются более информативными по сравнению с поверхностными водами компонентами
водных экосистем. Изучение химического состава донных отложений дает
возможность проследить динамику накопления микроэлементов на протяжении
большого промежутка времени, тогда как концентрации металлов в поверхностных
водах варьируют в зависимости от метеоусловий и сезона [1].
В настоящее время все водные объекты Республики
Беларусь испытывают в той или иной степени антропогенное влияние. Особенно оно
контрастно для водоемов, находящихся на урбанизированных территориях, где
наряду с глобальным поступлением токсикантов с атмосферными осадками
присутствует риск локального загрязнения. В этом плане практически не изучено распределение
тяжелых металлов в донных отложениях озер под влиянием различных факторов среды
на территории крупного промышленного центра страны - г. Гомеля. Необходимость
данных исследований не вызывает сомнений, так как большинство водоемов
городской зоны используются для проведения культурно-массовых, спортивных и
других мероприятий.
Целью работы являлся анализ факторов, влияющих
на концентрирующую способность донных отложениях озер городской черты в
отношении хрома.
Практическое значение работы состоит в том, что
результаты проведенных исследований могут быть полезными для оценки
экологического состояния водных объектов и прогноза содержания тяжелых металлов
на основе данных по химическому составу донных отложений.
1. ОБЗОР ЛИТЕРАТУРЫ
.1 Пути поступления загрязняющих
веществ в водоемы и водотоки
донный отложение хром водоем
В современных условиях наблюдается устойчивая
тенденция усиления отрицательного антропогенного воздействия на водную среду и
расширения списка ингредиентов загрязнения. Пути поступления загрязняющих и
эвтрофирующих веществ в водоемы могут быть различными и их можно объединить в
две группы:
) сосредоточенные сбросы через канализационные
системы;
) рассеянные, в составе различных видов стока
(почвенные, грунтовые воды, плоскостной смыв и т.д.).
Вещества могут поступать как в растворенной
форме, так и в виде взвешенных частиц (коллоидов, глинистого и обломочного
материала). Количество поступающих соединений зависит от множества факторов и,
в первую очередь, от наличия на водосборе локальных источников загрязнения,
промышленных предприятий и населенных пунктов, степени сельскохозяйственной
освоенности территории, которая значительно менялась в историческое время и
продолжает развиваться.
Основными путями поступления загрязняющих
веществ в водоемы республики являются: локальные сбросы, поверхностный сток,
склоновый сток, атмосферные осадки. Источниками поступления химических и
загрязняющих веществ в водоемы могут являться локальные или рассеянные сбросы:
промышленных предприятий, сельскохозяйственных объектов и территорий,
территорий населенных пунктов, объектов рекреации.
Наиболее распространенными источниками, вредно
влияющими на качество вод водоемов, служат сосредоточенные стоки
животноводческих ферм и с территорий сельскохозяйственных угодий, стоки
мелиоративных систем, промышленных предприятий и предприятий по переработке
сельскохозяйственного сырья, бытовые и коммунальные стоки населенных пунктов и
объектов рекреации, пыле-газовые выбросы крупных промышленно - городских
агломераций.
Промышленные сточные воды имеют очень
разнообразный химический состав, зависящий от характера производства.
Наибольшее количество сточных вод образуется в нефтеперерабатывающей,
металлургической, химической и целлюлозно-бумажной отраслях промышленности. В составе
промышленных сточных вод, помимо взвешенных веществ, присутствуют различные по
химическому составу вещества: органические (кислоты, спирты, фенолы, пестициды,
СПАВ, нефтепродукты и др.), остроядовитые (цианиды, мышьяк, соли меди, цинка,
ртути и др.), остропахнущие, минеральные соединения (соли, кислоты, щелочи),
радиоактивные элементы и пр.
Сточные воды сельскохозяйственного производства
- коллекторные и дренажные воды орошаемых земель, сточные воды животноводческих
комплексов и ферм - наиболее распространены в районах интенсивного земледелия и
животноводства. Состав вымываемых минеральных солей зависит от характера
почво-грунтов, степени освоенности территории, вида вносимых удобрений и
средств борьбы с сорняками и вредителями урожая, состояния дренажных сетей и
других условий. Количество выносимых солей колеблется в больших пределах: от 1
до 200 т/га. Сооружение крупных животноводческих комплексов вызвало глобальное
загрязнение водных объектов их сточными водами, в составе которых преобладают
соединения биогенных элементов азота и фосфора. В связи с широким применением
удобрений часть их выносится вместе со сбросными и дренажными водами в водоемы
и водотоки, загрязняя их, а выносимые соединения азота и фосфора служат
причиной антропогенного эвтрофирования вод.
Хозяйственно-бытовые сточные воды - это сточные
воды городов и других населенных пунктов, образуются из бытовых сточных вод,
сточных вод коммунальных предприятий и дождевых (ливневых) вод, стекающих с
заселенной территории.
Хозяйственно-бытовые сточные воды хотя и имеют
разные концентрации растворенных веществ, но состав их более или менее сходен.
Объем сточных вод зависит от количества жителей и степени благоустройства
населенного пункта. Общий объем хозяйственно-бытовых сточных вод городов примерно
в 10 раз меньше объема промышленных сточных вод, но они представляют не меньшую
опасность для экосистем, чем промышленные, так как со сточными водами в водные
объекты поступает большое количество биогенных веществ, макрокомпонентов,
органических веществ и др.[1]. Практически повсеместно хозяйственно-бытовые
стоки городов смешиваются со стоками ливневой канализации, с которыми в водные
объекты поступают нефтепродукты, тяжелые металлы, взвешенные вещества и др.
Пыле-газовые выбросы промышленно-городских агломераций.
Атмосферные осадки являются источником поступления загрязняющих веществ в
водоемы, расположенные в зоне интенсивного атмосферного загрязнения
пыле-газовыми выбросами промышленных предприятий крупных городов республики:
Могилев, Гродно, Новополоцк, Минск, Орша, Жлобин и Гомель. Предприятия
промышленной зоны выбрасывают в атмосферу более 25 видов химических веществ
различной токсичности. Наряду с глобальным, в результате трансграничного
переноса воздушных масс, региональное (локальное) загрязнение атмосферы в виде
твердых и жидких осадков существенно влияет на формирование химического состава
поверхностных вод. Поступление примесей из атмосферы происходит, в основном,
двумя путями: в результате взаимодействия примесей с подстилающей поверхностью
(сухое осаждение) и вымыванием их атмосферными осадками [2]. Поведение
химических элементов в атмосфере исключительно сложно и обуславливается
разнообразием термодинамических и физико-химических условий, формирующихся под
воздействием техногенных факторов, а также спектром ингредиентов и их
совокупным воздействием. Максимальное загрязнение большинством химических
элементов, в том числе и тяжелыми металлами, распространяется в радиусе 2 км от
источника загрязнения. Для направлений, совпадающих с преобладающими ветрами,
загрязнение в 2-3 раза выше по сравнению с другими направлениями [2,3]. Тяжелые
металлы входят в критическую группу веществ-индикаторов стресса окружающей
среды, увеличение концентрации которых в воде, почве, воздухе и биоте являются
прямым показателем опасности для животных и человека [4]. Несмотря на высокую
скорость их рассеивания в биосфере, максимальные их количества
сосредотачиваются непосредственно в промышленных зонах и, как указывалось выше,
в радиусе до 10 км от них в направлениях преобладающих ветров. Основными
источниками поступления металлов в воздушную среду промышленного комплекса
являются теплоэнергетика, сжигание нефти и бензина, химическая промышленность и
др.
1.2 Механизмы аккумуляции тяжелых
металлов донными отложениями
Характерной особенностью режима тяжелых металлов
в водоемах замедленного стока является направленность большинства
внутриводоемных процессов на образование их труднорастворимых соединений и на
седиментацию последних [5]. Одновременно происходит и осаждение аллохтонной
взвеси, содержащей металлы. Поэтому донные отложения таких водоемов являются
хранилищем основных запасов соединений тяжелых металлов и, таким образом,
потенциальным источником вторичного загрязнения водоема.
Аккумуляцию металлов в осадках контролируют и
осуществляют пять основных процессов:
адсорбционное поглощение мелкодисперсными
частицами;
седиментация дискретных металлсодержащих
взвешенных веществ;
соосаждение металлов с гидроксидами железа и
марганца;
ассоциация с органическим веществом;
инкорпорация в кристаллической решетке.
Практически в каждом водоеме возможен свой
механизм фиксации. Однако интенсивность каждого из перечисленных выше процессов
определяется морфометрическими и гидрологическими характеристиками и
гидрохимическим режимом водоема. Общая направленность процессов миграции
металлов сверху вниз характерна для всех водоемов замедленного стока и
определяет их общую тенденцию к самоочищению водных масс от вносимых в них
любым путем соединений тяжелых металлов.
Неорганическая адсорбция является наиболее
эффективным способом уменьшения концентрации металлов в речных водах, причем
основную роль играют взвешенные вещества. Донные отложения - чрезвычайно
сложная сорбционная система, поскольку включает огромное количество минеральных
и органических соединений, способных сорбировать ионы и соединения тяжелых
металлов, причем часто конкурирующих между собой за связывание металлов [6].
Общая последовательность, в которой
располагаются природные сорбенты по их способности аккумулировать тяжелые металлы,
такова: гидрат оксида марганца > гуминовые кислоты > гидрат оксида железа
III > глинистые минералы [7].
Следует отметить, что даже основные классы
природных сорбентов изучены далеко не полностью. Наибольшее количество работ
посвящено гидратам оксидов железа и марганца, которые из-за высокой сорбционной
способности часто называют "сборщиками" микроэлементов [5].
Для трех металлов, загрязнителей природной
среды, установлена сорбционная емкость оксидов железа Fе3+ и Mn4+, которая
уменьшается в ряду: Pb2+ > Zn2+ > Cd2+ > [8].
Другим важным классом природных сорбентов
являются органические вещества. Донные отложения водоемов замедленного стока,
особенно высоко продуктивных, содержат значительные количества органики разного
состава и свойств, способных удержать металлы в осадках. Частично это
труднорастворимые вещества, осаждающиеся вместе со связанными с ними металлами,
как, например соединение металлов с липидами. Эти комплексы после отмирания
клеток хорошо сохраняются и, попадая в илы, обогащают их металлами.
Наибольшую роль в связывании металлов играют
гуминовые кислоты - конечный продукт распада органических остатков [9].
Связывая в комплексы тяжелые металлы в донных
отложениях, гуминовые кислоты являются важнейшим фактором уменьшения их
мобильности.
Высокомолекулярные органические вещества,
подобные гумусу, могут также сорбироваться минеральной фазой осадков и,
связывая затем металлы, выступать в роли "посредников" в процессе
сорбции металлов. Предложен следующий ряд металлов Hg2+ > Cu2+ > Pb2+
>Zn2+, расположенный по силе абсорбции их твердым органическим веществом
[10].
Последним в ряду природных сорбентов
представлены глины - коллоидная фракция донных отложений.
Глины - это силикаты алюминия и магния со
слоистоподобной структурой Взаимодействие их с металлами осуществляется в
результате ионного обмена. Прочность связывания металлов глинами гораздо
слабее, чем другими природными сорбентами. Глины, карбонаты и другие минералы
являются ядром для отложения оксидов железа и марганца. Поэтому фазу глинистых
минералов рассматривают как механический субстрат, на котором осаждаются
органические вещества и вторичные минералы [11].
Следует отметить, что микроэлементы могут
поступать в донные отложения не только сверху (из водной толщи), но и снизу, из
глубинных слоев самих осадков. В восстановительных условиях это приведет к
обогащению ими водных масс, в окислительных - к образованию трудно растворимых
оксидов, что благоприятствует процессам самоочищения водных масс от соединений
тяжелых металлов. Распределение металлов, не участвующих в
окислительно-восстановительных процессах, зависит главным образом от их
поглощения организмами и сорбцией на абиотическом сестоне. Экспериментальные
наблюдения показали, что порядок сорбции металлов на природном иле и отдельных
сорбентах (оксиды марганца, глины, гуминовые кислоты) таков: Cu2+ > Zn2+ »
Cd2+ [11].
Одним из важных факторов, влияющих на поглощение
металлов осадками, является величина рН. Так, в отношении цинка увеличение рН
выше 8.0 способствует переходу его растворенных форм в трудно растворимые
гидролизованные. При более низких значениях рН, когда образование
гидроксокомплексов и гидроксидов металлов выражено слабо (5.0 - 8.0), изменение
рН влияет главным образом на поглотительную способность донных отложений. Закисление
водной толщи озер вызывает уменьшение концентраций металлов по направлению к
поверхности донных отложений (особенно таких мобильных, как Cd, Zn, Ni, Cu, Al)
в результате, во-первых, снижения скорости седиментации элементов вследствие
уменьшенной адсорбции химических компонентов на осаждающихся частицах и,
во-вторых, десорбции (растворения) соединений металлов из уже осажденного
материала [12].
По относительному содержанию во взвесях, тяжелые
металлы убывают в следующем порядке: Fe > Mn > Pb > Ni > Co > Cu
> Zn > Cd. Такая последовательность объясняется высоким сродством ионов
Fe2+, Mn2+, Pb2+, Ni2+ к глинистым лигандам. Сорбция на поверхности взвешенных
частиц обеспечивается физической адсорбцией, катионным обменом, а также
химической адсорбцией, характеризующейся образованием химических ассоциатов
между ионами металлов и поверхностью частиц. Наибольшей сорбционной емкостью
характеризуются взвешенные вещества с размером частиц от 0.05 мм и менее,
которые в условиях высоких скоростей длительное время находятся в русловом
потоке и играют определенную роль в межфазовом распределении тяжелых металлов в
системе вода - взвешенное вещество. По данным Осадчего Н.И. [13] при анализе
воды Дуная практически на всем протяжении донные отложения представлены песчаными
отложениями с незначительной концентрацией тяжелых металлов, близкими к
фоновому для аналогичных природных образований. Максимальное содержание тяжелых
металлов характерно для мелкодисперсных илистых образований, залегающих как
правило в глубоководных зонах.
Исследование содержания тяжелых металлов в
различных гранулометрических фракциях донных отложений показало, что с
уменьшением их размера происходит рост концентрации практически всех металлов.
Наибольшую опасность представляют донные отложения с размером фракции < 0.05
мм. При изменении гидрологических условий водной среды они могут вовлекаться в
речной поток и трансформироваться на значительные расстояния. По мере перехода
от песков к глинистым илам в среднем растет содержание металлов: Мn - в 10 раз,
Cd - в 8, Со, Сu, Рb и Zn в 2-5 раз [14].
По данным Мур Дж. [15] можно выделить
соединения, в форме которых тяжелые металлы локализуются в донных отложениях.
Кадмий - максимум содержания его отмечен в
ассоциации с гидроксидами железа и марганца, не обнаружено связи с органическим
веществом и карбонатами.
Кобальт - в целом характеризуется низким
содержанием, а иногда и полным отсутствием мобильных форм, может находиться в
нерастворимой форме.
Медь - в илах распределяется со следующей
закономерностью: от 45% до 65% безвозвратно захоранивается, 25-52%
ассоциировано с органическим веществом, 2-15% - с гидроксидами, 3% - мобильные
формы.
Свинец - характеризуется низким содержанием
мобильных форм (0.6-10.9%). Основные же запасы распределяются между
труднодоступными (40- 75%) и совершенно недоступными (26-48%) для гидробионтов
формами.
Цинк - содержание мобильных форм составляет 3%.
Основные запасы - 50-72% ассоциированы с оксидами железа и марганца.
Резюмируя изложенное выше, можно отметить, что
процессы накопления микроэлементов и тяжелых металлов в донных отложениях
водоемов обусловлены многочисленными факторами. Их интенсивность зависит от
химического и гранулометрического состава отложений, их типа,
окислительно-восстановительных условий, рН среды, мощности осадков, а также
сезона и метеоусловий. При этом для каждого водоема может быть свойственен свой
механизм аккумуляции микроэлементов при сочетании некоторых перечисленных
факторов.
1.3 Особенности накопления тяжелых
металлов в организме гидробионтов
Поглощение металлов (как и вообще минеральных
элементов) растительным организмом - сложный процесс, состоящий из нескольких
сопряженных этапов, характеризующих своими механизмами, приуроченными к
определенным структурным компонентам тканей растений.
Исходя из современных сведений по данному
вопросу, в поглощении, транспорте и метаболизме минеральных элементов
растениями можно выделить следующие основные этапы:
обогащение ионами свободного пространства
апопласта (происходящее за счет обменной адсорбции, диффузии, пассивной
физико-химической адсорбции);
преодоление мембранного барьера - проникновение
ионов в симпласт;
радиальное передвижение по тканям корня и
сосудистым проводящим пучкам;
активное включение поступающих ионов в
метаболизм;
вертикальное передвижение ионов по стеблям,
черешкам и ветвящимся жилкам листьев;
поступление в синтезирующие клетки, утилизация и
реутилизация, отток в репродуктивные органы;
транспорт ассимилятов и ионов вниз по флоэме, в
корни [16].
При поступлении в растения тяжелых металлов наибольшее
значение приобретают первые три этапа, а также передвижение ионов из корней в
надземные органы растений. Показано, что для различных ионов апопластический
путь передвижения может иметь неодинаковое значение. Так, существуют данные
[17], что пассивное прохождение через апопласт играет важную роль не только в
поглощении Са и Mg, но и тяжелых металлов. Тяжелые металлы типа Pb, Cd, и Zn
аккумулируются в свободном пространстве корня. Концентрация Са и других двух- и
трехвалентных ионов в свободном пространстве влияет на поглощение тяжелых
металлов, поскольку она действует на проницаемость апопласта для ионного
транспорта. Поглощение свинца корнями растений уменьшается линейно с
увеличением логарифма концентрации Са в растворе. Катионообменная способность корней
также влияет на накопление ионов в свободном пространстве.
Важнейшим этапом в процессе поглощения
растениями ионов металлов является преодоление ими структурного барьера -
биологической мембраны. По-видимому, при поглощении тяжелых металлов происходит
сочетание быстрой адсорбции с активным поглощением. В кинетике поглощения цинка
растениями отмечены три стадии:
. начальная (60-90 мин) быстрая, в основном за
счет обменной адсорбции;
. более медленная (около 3 ч), отражающая
поступление ионов через наружные диффузные барьеры протопластов;
. длительная, с низкой скоростью активного
накопления цинка [17].
Есть основания полагать, что отмеченная схема
активных и пассивных процессов является общей для поглощения и других тяжелых
металлов. Путь по свободному пространству и пассивное поглощение имеют большое
значение при поступлении тяжелых металлов, особенно при повышенных
концентрациях их в среде. Haynes [18] считает, что пассивная физико-химическая
адсорбция весьма важна в поглощении тяжелых металлов корнями растений.
Возможно, для некоторых металлов типа свинца, концентрация которых в среде за
последнее время резко увеличилась, превалирование пассивного характера
поступления возросло. Электронно-микроскопическое исследование показало, что
ионы свинца при повышении их концентрации в растворе могут проникать путем
диффузии не только через клеточные стенки, но и сквозь плазмалемму и тонопласт
[19].
Весьма важное значение в дальнейшей судьбе
поглощенных ионов имеют их радиальное передвижение в кортексе корня и пути
попадания в ксилемный поток. После поглощения ионы могут передвигаться в тканях
корня как симпластическим, так и апопластическим путем. Оба пути транспорта
могут сменять друг друга. Механизмы поступления ионов в ксилему полностью еще
не выяснены. Во всяком случае, на пути ионов из корня в стебель они
преодолевают серьезный барьер, который при поступлении тяжелых металлов может
становиться решающим. Как известно, одним из механизмов устойчивости к тяжелым
металлам является ограничение поступления их из корней в надземную часть [20].
У многих растений тяжелые металлы, в первую очередь свинец и кадмий, остаются в
корнях и почти не проникают в надземные органы. Немаловажная роль в ограничении
вертикального передвижения металлов принадлежит, вероятно, корневой шейке.
Следует учитывать, что, поступая в живые системы
и проявляя токсичность, тяжелые металлы часто характеризуются аддитивным
действием. Это отмечено, например, по отношению к свинцу и кадмию, меди, никелю
и цинку. Возникают антропогенные биогеохимические провинции, характеризующиеся
повышенным содержанием целого комплекса металлов [21]. В то же время высокое
содержание металлов способно вызвать нарушение структуры клеточных мембран.
Это, в свою очередь, может явиться дополнительным фактором усиления пассивного
диффузного поступления тяжелых металлов в клетки растений.
В настоящее время для разработки оптимальной
программы регулирования и контроля качества природных сред много внимания
уделяется поиску биоиндикаторов загрязнения природной среды тяжелыми металлами.
Наиболее детально изучены в этом отношении растения вследствие того, что их
микроэлементный состав очень точно характеризует геохимические особенности
локальных участков их места произрастания. Способность макрофитов накапливать
преимущественно растворенные в воде металлы в сочетании со способностью в
течение продолжительного времени удерживать их в своих тканях позволила многим
исследователям рекомендовать водные растения в качестве организмов-мониторов.
По характеру накопления и распределения металлов
в зависимости от содержания их в почве растения делят также на 3 группы [22]:
«накопители» - характеризуются повышенным содержанием металлов в органах
независимо от концентрации последних в почве; у «исключителей» концентрация
данного металла в надземной части поддерживается на постоянно низком уровне
независимо от внешних концентраций; промежуточное положение занимают
«индикаторы», у которых поглощение и транспорт металлов в надземную часть
пропорциональны их концентрации в почве..A. Butler [23] впервые сформулировал
критерии выбора видов-индикаторов антропогенного загрязнения водных экосистем.
Организмы-индикаторы должны:
накапливать загрязняющее вещество и не погибать
под действием реально встречающихся его концентраций;
быть оседлым, массовым, легко доступным в
природе;
быть долгоживущим;
иметь приемлемые размеры, удобные для отбора
органов и тканей;
легко культивироваться в лабораторных условиях.
Известно [24], что растения, обитающие в богатых
питательными веществами средах, аккумулируют минеральных элементов больше, чем
растения, распространенные в средах, бедных питательными веществами. Однако
известно, что концентрирующая способность водных растений по отношению к
химическим элементам определяется многими факторами. Некоторые их них:
. Различная способность поглощения химических
элементов растениями - это зависит от вида растения, его физиологических
способностей, возраста и стадии развития, а также от анализируемого
растительного органа;
. Условия среды обитания - форма котловины,
конфигурация и размеры водоема, гранулометрический состав грунта, химический
состав воды и донных отложений, различный тип и уровень загрязнения водоема, а
также географическое положение водоема и климатические факторы.
Процесс накопления тяжелых металлов водными животными
обусловлен следующими механизмами: 1) поглощением взвеси, содержащей металлы;
2) поступление с пищей; 3) ассимиляция при секреции хелатирующих или
комплексообразующих агентов; 4) участие в физиологических процессах; 5) ионный
обмен и сорбция на тканях и клеточных мембранах [25]. Так, у морских моллюсков
растворенные формы металлов усваиваются непосредственно из воды на границе
активного контакта организма со средой, главным образом в жабрах, тогда как
металлы в форме взвешенных частиц поступают в организм в процессе
фильтрационного питания через пищеварительный тракт [26]. Особое положение
занимают двустворчатые, как активные фильтраторы-седиментаторы, содержание в
них металлов в одинаковых условиях обитания часто превосходит накопление у
других представителей макрозообентоса. Максимальная концентрация металлов
отмечена в жабрах и внутренностях (особенно в почках) двустворчатых моллюсков,
т.е. в органах, где происходит извлечение примесей из воды и пищи. Минимальные
уровни накопления обнаруживаются в мышечной ткани. Однако такие закономерности
наблюдаются не всегда. Содержание многих металлов в створках устриц и мидий
обычно значительно выше, чем в мягких тканях [27]. Особенно же выражены эти
различия в содержании железа, марганца, свинца, никеля, кобальта, кадмия, хрома
и стронция, что отражает их способность соосаждаться с карбонатами и необратимо
фиксироваться в створках моллюсков по мере их формирования. Меди и цинка,
находящихся в морской воде преимущественно в ионной форме, в створках моллюсков
содержится меньше, чем в мягких тканях.
Широкий диапазон концентраций микроэлементов в
телах различных видов пресноводных моллюсков установлен авторами работы [28].
По их мнению такая вариабельность обусловлена не только абсолютным содержанием
тяжелых металлов в субстрате воде, но и видовыми, возрастными особенностями
гидробионтов.
Внутривидовые различия в концентрации тяжелых
металлов могут быть связаны с размером тела и иногда с полом животного, с
особенностями питания и отражать потребности в некоторых металлах,
обусловленные разными стадиями жизненного цикла (линька, размножение и др.).
Поглощение металлов является, в основном пассивным процессом, и его регуляция
осуществляется после проникновения металла внутрь тела животного.
Предполагается, что регулируется поглощение только необходимых для метаболизма
металлов (таких как Cu, Zn и, видимо, Мn), но возможно и случайное перемещение
метаболитов и неметаболитов в результате связывания с необходимыми для
организма ионами или молекулами. Особенно интенсивно могут накапливаться в
организме микроэлементы, необходимые для его жизнедеятельности и активно
участвующие в физиолого-биохимических процессах дыхания, кроветворения,
депонирования, выделения и других, т.е. в тех процессах, в которых металлы
выполняют свои биокаталитические функции как необходимые компоненты сложных
белковых молекул и, прежде всего, ферментов, дыхательных пигментов, витаминов и
других биологически активных соединений [25, 28].
В общем случае, чем слабее выражена способность
организма противостоять проникновению в него ионов металла, тем выше уровень
накопления этого металла. Это обстоятельство более характерно для организмов,
стоящих в эволюционном плане на низком уровне организации, с отсутствием
специфических механизмов детоксикации [29] так, в конечных звеньях трофических
цепей (в мирных и хищных рыбах) выявлено отсеивание Fe и Mn и накопление Си и
Zn. Такой перенос на более высокие трофические уровни в значительной степени
может контролироваться процессами детоксикации и поглощения.
Хотя биохимические и физиологические механизмы
регулирования и функционирования живых систем носят универсальный характер, у
водных организмов, несомненно, обнаруживаются специфические черты, связанные с
особенностями их существования в воде [30], в том числе и в проявлении откликов
на воздействие различных токсикантов, включая тяжелые металлы. При
физиолого-биохимическом подходе к аккумуляции тяжелых металлов в гидробионтах
оказывается, что максимальная метаболическая потребность в них значительно
ниже, чем фактическое содержание в организме. Повышение концентрации
какого-либо металла в теле гидробионта или в его отдельных органах еще не
свидетельство токсического воздействия этого металла на организм, хотя такое
предположение кажется логичным. Скорее, наоборот: высокий уровень биологической
аккумуляции металла отражает нормальное физиологическое состояние и способность
этих организмов депонировать те или иные микроэлементы. Это подтверждается [31]
прямыми наблюдениями за накоплением и биологическим действием меди у морских
брюхоногих моллюсков.
Гидробионты различных таксономических групп в
разной мере аккумулируют металлы. Условно, по содержанию металлов, водные
организмы можно распределить на три группы: макро-, микро- и деконцентраторы
[32, 33]. В качестве критерия для такого разделения предлагается использовать
коэффициент биологического накопления - КН. под которым в данном случае
понимают отношение концентрации металлов в теле гидробионтов к их содержанию в
донных отложениях. К макроконцентраторам условно отнесены живые организмы с КН
> 2, к микроконцентраторам - организмы с КН = 1-2 и к деконцентраторам - с
КН < 1. Важно отметить, что выделяемые группы в значительной мере условны и
служат исключительно для удобства рассмотрения изучаемых организмов по содержанию
в них металлов. Вследствие искусственности классификации организмы одного и
того же вида при разной концентрации металлов в донных отложениях могут
одновременно относиться к различным классификационным группам. Кроме того,
коэффициенты накопления ряда элементов подвержены сезонным изменениям, что
по-видимому, связано с колебаниями температуры и освещенности водной среды,
физико-химического состояния элементов, концентрации химических элементов в
зонах гидрофронтов, т.е. в районах, гидрологически весьма активных [34].
Важным и до сих пор слабо изученным аспектом в
формировании микроэлементного состава как пресноводных, так и морских
гидробионтов является взаимосвязь между биологическим накоплением разных
металлов, т.е. зависимость концентрации одних металлов от содержания других.
Отмечена корреляция между накоплением в морских гидробионтах железа и марганца,
что отражает сродство химического и биогеохимического поведения этих элементов
в море, включая процессы аккумуляции в живых организмах [35 16].
В работе [36] показано, что в мягких тканях
мидий, обрастающих различные субстраты, величины концентрации многих
микроэлементов коррелируют между собой. Так, установлена положительная
корреляция для следующих пар элементов у морских мидий: Fe-Pb, Fe-Zn, Fe-Cu, Mn-Ni,
Cu-Pb, Ni-Сr, Сr-Cd и Pb-Cd. В мягких тканях донных мидий положительная
корреляция установлена для Fe-Zn, Сu-Mn, а отрицательная корреляция - для
Zn-Со. В раковине мидий обнаружена положительная корреляция между Fe-Mn, Fe-Zn,
Fe-Сu, Fe-Ni, Fe-Со, Fe-Сr, Fe-Pb.
Установленная тесная взаимосвязь между
концентрацией микро- и макроэлементов в воде и степенью их накопления в
организме гидробионтов является свидетельством того, что основной макро- и
микроэлементарный химический состав гидробионтов формируется уже на низших
уровнях их организации. Гидробионты, находящиеся на более высоких ступенях
эволюционного развития, получают с пищей химические элементы, находящиеся уже в
иных, более благоприятных для усвоения соотношениях по сравнению с теми, в
которых они присутствуют в морской воде [36].
Интересным является вопрос о реакции
гидробионтов на токсиканты различного происхождения.
Металлы в организме преимущественно находятся в
виде комплексов с белками, нуклеиновыми кислотами, взаимодействуя с активными
группами биокомплексов: -ОН, -СООН, -РОзН и лимонной кислотой. Известно, что
Нg, Cu, Ni, Pb, Zn, Со, Cd, Mn соединяются с аминокислотами преимущественно
через SH-группы (Нg, Аg, Pb, Cd, Zn, Со) и СООН-группы (Сu, Ni, Zn, Мg, Са)
[30]. Установлено также сродство некоторых металлов к определенным белковым
фракциям. Так, например, транспорт железа осуществляется специальным
глобулином, путем образования железосодержащего белка ферритина; медь
первоначально связывается с альбуминами, но в печени образуется новый комплекс
с глобулинами - церулоплазмин; марганец - с глобулином и т.д. Выявлена
зависимость между концентрацией микроэлементов в отдельных органеллах клетки и
активностью находящихся в них ферментных систем [37].
Таким образом, соединения многих тяжелых металлов
являются катализаторами биохимических процессов и оказывают на развитие водных
организмов стимулирующее, угнетающее или нейтральное воздействие, в зависимости
от природы металла, концентрации и формы его существования в воде [38].
Поскольку состояние ионов металлов в природных водах в значительной степени
определяет их биологическую активность, степень токсичности тяжелых металлов
зависит не только от их концентрации, но и от химических форм, в виде которых
они мигрируют в природной воде. Незакомплексованные ионы металлов обладают, как
правило, наиболее выраженной степенью токсичности для водных организмов [39,
40].
2. ОБЪЕКТ, ПРОГРАММА И МЕТОДИКА
ИССЛЕДОВАНИЙ
.1 Объект и программа исследований
Объектом исследований являлись донные отложения
водоемов города Гомеля, которые по антропогенному воздействию можно разделить
на следующие группы:группа: водоемы, принимающие сточные воды.
) Озеро Дедно принимает стоки двух коллекторов -
Прудковского и Хатаевичского, в который впадают ливневые стоки с улицы Крупской,
стоки двадцати девяти предприятий, одиннадцать из которых -автопредприятия, а
так же стоки фабрики "Спартак" и "8 Марта".
) Озеро Шапор принимает стоки АПДО
"Гомельдрев" и завода "Гомельобои".
) Озеро Круглое принимает стоки завода
"Электроаппаратура"группа: водоемы промышленных зон города.
) Озеро Малое подвержено влиянию предприятий
Северного промузла. Расположено в районе троллейбусного парка №1. Недалеко
находится железная дорога и автодром.
) Озеро У-образное находится на незначительном
расстоянии от микрорайона "Волотова". Вблизи проходит автотрасса и
располагаются новостройки микрорайона "Мельников луг".группа:
водоемы, имеющие непосредственный контакт с водами реки Сож.
) Озеро Володькино - помимо контакта с русловым
током реки Сож, принимает в свои воды реку Ипуть. Имеет рыбохозяйственное
значение.
) Гребной канал - искусственный водоем
расположенный в районе деревни Якубовка. По берегам расположены огороды
частного сектора.группа: водоемы городских зон отдыха.
) Озеро Любенское - расположено в Любенском
микрорайоне, приспособлено человеком для проведения культурно-массовых и
спортивных мероприятий.
) Озеро Волотовское - используется жителями близ
лежащих микрорайонов для активного отдыха в летний период.
В качестве контрольного водоема, не испытывающего
техногенного влияния городской среды, был выбран старичный комплекс реки Сож,
находящийся в окрестности д. Поляновка (Ветковский район, Гомельской области).
Программа исследований включала количественный
анализ хрома в пробах донных отложений.
Задачами исследований являлось:
. Отбор и подготовка проб донных отложений к
анализу;
. Анализ валового химического состава донных
отложений;
. Определение содержания хрома в пробах донных
отложений;
. Статистическая обработка полученных
результатов.
Содержание хрома измерялось у представителей
следующих видов высших водных растений и моллюсков:
Высшие водные растения: ряска малая (Lemna
minor); кубышка желтая (Nuphar luteum); рдест пронзеннолисгный (Potamogeton
perfoliatus), роголистник погруженный (Ceratophyllum demersum), элодея
канадская (Elodea canadensis); стрелолист обыкновенный (Sagittaria
sagittifolia), сусак зонтичный (Bulomus umbellatus), частуха подорожниковая
(Alisma plantago-aquatica).
Моллюски: Прудовик обыкновенный (Limnaea
stagnalis L.), катушка окаймленная (Planorbis planorbis L.), живородка речная
(Viviparus viviparus L.), беззубка обыкновенная (Anodonta cygnea L.), перловица
обыкновенная (Unio pictorum L.).
2.2 Методика отбора и хранения проб.
Подготовка проб к анализу
Метод анализа
Пробы донных отложений отбирались в трех-четырех
точках каждого водоема с верхнего пограничного слоя толщиной 10 см стандартным
дночерпателем (объём 1 л). Образцы донных отложений массой 300-500 грамм
переносились в стеклянные контейнеры.
Пробы воды в каждом водоеме отбирались один раз
в квартал в течение года в полиэтиленовые емкости.
Подготовка проб донных отложений для дальнейших
химико-аналитических исследований основывалась на методике, предложенной в
работе [32]. Выполнялись следующие операции:
отсасывание под вакуумом для отделения иловых
вод,
выслушивание до воздушно-сухого состояния,
просеивание через сито с диаметром пор 1мм,
растирание в фарфоровых ступках
сухое озоление (термическая обработка образцов в
муфельных печах при постепенном увлечении температуры до 450°С
в течении 6-20 ч до получения белой или слегка окрашенной в фиолетово-розовый
свет золы).
Извлечение металлов из подготовленных проб
донных отложений основывалось на экстракции их горячей 1 н азотной кислотой.
Содержание хрома в подготовленных пробах
определялось при помощи метода эмиссионного спектрального анализа, позволяющего
определить в одной пробе несколько элементов одновременно. Его достоинствами
являются многоэлементность определения, доступность и надёжность оборудования,
осуществление анализа по единой методике. Метод предназначен для определения
микроколичеств сурьмы, марганца, свинца, железа, висмута, ванадия, алюминия,
молибдена, олова, кадмия, меди, цинка, серебра, кобальта, никеля.
Отбор проб высшей водной растительности производился
вручную в период цветения каждого вида растения. Перед анализом собранные
растения промывались в воде соответствующих водоемов от ила и загрязнений.
Растения сушились в тени на открытом воздухе до воздушно-сухого, затем
абсолютно сухого состояния в сушильном шкафу при 105°С.
Высушенные образцы нарезались на небольшие кусочки ( 2-3 см) ножницами и
укладывались в фарфоровые стаканы.
Сбор особей моллюсков проводился ручным
способом, а на глубоких частях водоемов с помощью дночерпателя. Затем проводилось
отделение мягких тканей моллюсков от раковин и высушивание в сушильном шкафу
при температуре 105°С в фарфоровой посуде.
Подготовленные вышеуказанными способами пробы
растительности и тканей моллюсков подвергались сухому озолению (навеска пробы-
5-10 г) в муфельной печи при постепенном увеличении температуры до 450°С
в течении 6-20 ч.
Содержание хрома в подготовленных пробах
определялось при помощи метода эмиссионного спектрального анализа, позволяющего
определить в одной пробе несколько элементов одновременно. Его достоинствами
являются многоэлементность определения, доступность и надёжность оборудования,
осуществление анализа по единой методике. Метод предназначен для определения
микроколичеств сурьмы, марганца, свинца, железа, висмута, ванадия, алюминия,
молибдена, олова, кадмия, меди, цинка, серебра, кобальта, никеля.
2.3 Методы статистической обработки
результатов исследований
В качестве основного статистического параметра
совокупности данных использовалось среднее арифметическое ряда вариант:
 ,(1)
,(1)
где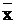 - среднее значение ряда вариант;
- среднее значение ряда вариант;
х1, х2 . . . . хn - частные значения
вариант;- число вариант.
Показатели вариации
экспериментальных данных оценивались по следующим критериям.
Стандартное отклонение:
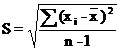 ,(2)
,(2)
где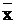 - среднее значение ряда вариант;
- среднее значение ряда вариант;
хi - частные значения вариант;-
число вариант.
Точность прямого измерения
(доверительный интервал):
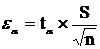 ,(3)
,(3)
гдеea - точность прямого измерения;a - критерий Стьюдента;-
стандартное отклонение;- число вариант.
Коэффициент вариации:
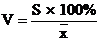 ,(4)
,(4)
Где V- коэффициент вариации;- стандартное
отклонение;
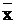 - среднее значение ряда вариант.
- среднее значение ряда вариант.
Анализ сопряженности вариабельности
двух рядов данных X и Y основывался на вычислении парного коэффициента
корреляции.
 ,(5)
,(5)
Где r - коэффициент парной
корреляции;- число вариант;
хi - частные значения вариант ряда
X;
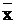 - среднее значение ряда вариант
ряда X;- частные значения вариант ряда Y;
- среднее значение ряда вариант
ряда X;- частные значения вариант ряда Y;
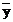 - среднее значение ряда вариант
ряда Y;и Sy - стандартные отклонения рядов X и Y [42].
- среднее значение ряда вариант
ряда Y;и Sy - стандартные отклонения рядов X и Y [42].
Расчет статистических параметров
производился с использованием программного обеспечения ПЭВМ.
3. РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ И ИХ
ОБСУЖДЕНИЕ
.1 Содержание хрома в донных
отложениях водоемов г. Гомеля
Изучение загрязненности водоемов г. Гомеля
хромом предусматривает обязательный анализ содержания металла в донных
отложениях как в основном компоненте, фиксирующем поступающие в водоем микроэлементы.
Поступающий в водоем хром в наибольшей степени
фиксируется донными отложениями. Однако его содержание в различных водоемах
значительно варьирует. В таблице 1 приводятся данные относительно содержания
данного микроэлемента в водоемах г.Гомеля. Анализ полученных результатов
показал, что самое высокое среди всех обследованных водных объектов среднее
содержание хрома (131,8 мг/кг) наблюдалось в оз.У-образное, его максимальная
концентрация в данном водоеме составляла 184,3 мг/кг. Однако в целом самый
высокий показатель содержания данного металла определен в одном из образцов,
отобранных в оз. Волотовское (192,0 мг/кг). Самое низкое среднее содержание
хрома определено в контрольном водоеме, не испытывающем антропогенной нагрузки
(7,18 мг/кг). При этом самое низкое значение содержания данного металла среди
всех обследованных образцов также получено в контрольном водоеме (0,13 мг/кг).
Таблица 1 - Содержание хрома в
донных отложениях водоемов г. Гомеля в мг/кг
|
Водоем
|
Среднее
|
Мин
|
Макс
|
|
Оз.
Малое
|
62,20
|
58,80
|
65,60
|
|
Оз.
Круглое
|
107,25
|
47,50
|
145,50
|
|
Оз.
У-образное
|
131,82
|
6,77
|
184,30
|
|
Оз.
Волотовское
|
94,05
|
27,44
|
192,00
|
|
Оз.
Шапор
|
40,85
|
28,80
|
68,60
|
|
Оз.
Дедно
|
69,04
|
6,30
|
115,20
|
|
Оз.
Любенское
|
37,22
|
4,95
|
58,20
|
|
Гребной
канал
|
36,32
|
29,70
|
43,65
|
|
Оз.
Володькино
|
22,77
|
17,82
|
31,68
|
|
Р.
Сож (среднее)
|
21,90
|
6,93
|
54,30
|
|
Р.
Сож, выше города (н.п. Кленки)
|
24,90
|
23,10
|
27,10
|
|
Р.
Сож, ниже города (н.п. Ченки)
|
34,30
|
6,93
|
54,30
|
|
Контрольный
водоем
|
7,18
|
0,13
|
17,34
|
В целом, необходимо отметить, что несмотря на
относительно высокое среднее содержание хрома в донных отложениях
оз.У-образное, Дедно и Любенское (131,8; 69,0 и 37,2 мг/кг соответственно),
минимальные показатели, определенные для данных водоемов весьма невысоки (3,8;
6,3 и 4,9 мг/кг). Следовательно, для оценки загрязненности донных отложений в
обязательном порядке, наряду со средним содержанием в них хрома, необходимо
учитывать варьирование данного параметра. В некоторых случаях высокая
вариабельность может свидетельствовать о локальном источнике загрязнения
водоема.
В таблице 2 отражена вариабельность содержания
хрома в различных водоемах г.Гомеля. Как видно из данных таблицы, самый высокий
коэффициент варьирования установлен в оз.Волотовское (он составляет более 92
%). Достаточно высокая вариабельность определена также в оз.Дедно (более 85 %).
Несмотря на незначительные, в целом, показатели содержания хрома в контрольном
водоеме, варьирование концентрации данного металла здесь существенно (73 %).
Тем не менее, максимальный показатель содержания хрома в донных отложениях
контрольного водоема столь невысок (17,34 мг/кг), что наличие там какого-либо
загрязнения исключается.
Таблица 2 - Вариабельность содержания хрома в
донных отложениях водоемов г. Гомеля в процентах
|
Водоем
|
Коэффициент
вариации
|
|
Оз.
Малое
|
7,73
|
|
Оз.
Круглое
|
42,80
|
|
Оз.
У-образное
|
56,09
|
|
Оз.
Волотовское
|
92,13
|
|
Оз.
Шапор
|
45,77
|
|
Оз.
Дедно
|
85,14
|
|
Оз.
Любенское
|
76,21
|
|
Гребной
канал
|
16,16
|
|
Р.
Сож (среднее)
|
27,04
|
|
Р.
Сож, выше города (н.п. Кленки)
|
48,15
|
|
Р.
Сож, ниже города (н.п. Ченки)
|
8,15
|
|
Контрольный
водоем
|
72,63
|
Наименьшая степень варьирования содержания хрома
в донных отложениях установлена в оз. Малое и р.Сож (н.п. Ченки), где она
составляет всего 8 %. Относительно невысокая вариабельность содержания хрома
определена в оз.Гребной канал (16 %).
На рисунке 1 отображены средние показатели
загрязненности хромом донных отложений обследованных водоемов в порядке
убывания данной ве личины. Как видно по рисунку, концентрация хрома в донных
отложениях снижается в следующей последовательности оз.У-образное > оз.Круглое
> оз.Волотовское > оз.Дедно > оз.Малое > оз.Шапор > оз.Любенское
> оз.Гребной канал > р.Сож (н.п.Ченки) > р.Сож (н.п.Кленки) >
оз.Володькино > р.Сож, среднее > контрольный водоем.
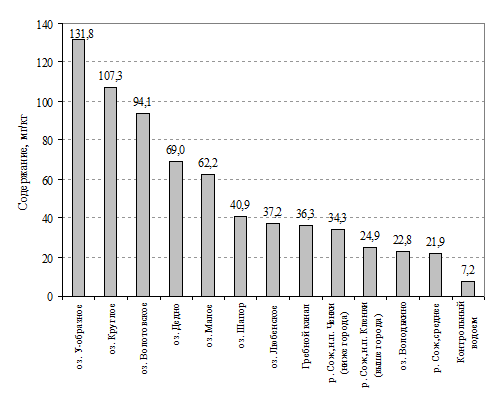
Рисунок 1 - Сравнительная характеристика
накопления хрома в донных отложениях водоемов г. Гомеля (в порядке убывания
концентрации)
Исходя из полученных данных, можно выделить
группу водоемов с максимальным загрязнением донных отложений хромом
(оз.У-образное, Круглое, Волотовское, Дедно, Малое), группу со средними
показателями накопления хрома (оз.Шапор, Любенское, Гребной канал, р.Сож у н.п
Ченки) и группу с наименьшей степенью аккумуляции хрома донными отложениями
(р.Сож у н.п Кленки, оз.Володькино, р.Сож в среднем, контрольный водоем).
Наряду с абсолютными показателями содержания
хрома в донных отложениях водоемов, для выявления наличия их антропогенного
загрязнения необходимо сопоставить полученные значения с кларковыми
параметрами. В таблице 3 приведены данные, полученные в результате деления
показателей содержания хрома в донных отложениях на значение кларкового уровня
(28 мг/кг). Из таблицы 3 видно, что существенное превышение кларка (почти в 5
раз) отмечено в оз.У-образное. Однако для большинства других обследованных
водоемов также характерна загрязненность донных отложений хромом, превышающая
естественный уровень.
Таблица 3 - Относительное содержание хрома в
донных отложениях водоемов г.Гомеля по сравнению кларковым значением (28 мг/кг)
для сапропелей
|
Водоем
|
Превышение
относительно регионального кларка сапропелей, раз
|
|
оз.
Малое
|
2,22
|
|
оз.
Круглое
|
3,83
|
|
оз.
У-образное
|
4,71
|
|
оз.
Волотовское
|
3,36
|
|
оз.
Шапор
|
1,46
|
|
оз.
Дедно
|
2,47
|
|
оз.
Любенское
|
1,33
|
|
Гребной
канал
|
1,30
|
|
оз.
Володькино
|
0,81
|
|
р.
Сож, среднее
|
0,78
|
|
р.
Сож, н.п. Кленки
|
0,89
|
|
р.
Сож, н.п. Ченки
|
1,23
|
|
Контрольный
водоем
|
0,26
|
Достаточно большое превышение кларка установлено
в оз.Круглое и Волотовское (в 3,8 и 3,4 раза соответственно). В то же время,
загрязненность таких водоемов, как р.Сож (у н.п.Ченки), оз.Любенское и Гребной
канал лишь на 20-30 % выше кларковые показателей, а содержание хрома на среднем
участке р.Сож, у н.п.Кленки и в оз.Вололдькино не превышает естественного
уровня. В контрольном водоеме содержание хрома также значительно ниже кларковых
параметров (почти в 4 раза).
В этой связи, о наличии или отсутствии
антропогенного источника поступления хрома в водоем можно судить лишь при
сопоставлении его загрязненности с уровнем контрольного водоема. Полученные
результаты подобного анализа приведены в таблице 4. Данные таблицы 4 позволили
определить самый высокий уровень загрязненности донных отложений хромом в
оз.У-образное (показатели выше контрольного более чем в 18 раз). Также наличие
источника антропогенного загрязнения хромом можно предположить практически для
всех обследованных водоемов г.Гомеля. В наименьшей степени показатели
контрольного водоема превышены в р.Сож (не более, чем в 5 раз).
Таким образом, проведенный анализ содержания
хрома в донных отложениях водоемов г.Гомеля позволил определить наибольший
уровень среднего загрязнения в оз.У-образное, самый высокий показатель среди
всех обследованных проб и наибольшее варьирование концентрации хрома в донных
отложения - в оз.Волотовское, превышение кларковых параметров содержания хрома
во всех обследованных водоемах, кроме контрольного, оз.Володькина и участка
р.Сож у н.п. Кленки, а также превышение уровня содержания хрома в донных
отложениях контрольного водоема во всех обследованных водных объектах.
Таблица 4 - Кратность превышения содержания
хрома в донных отложениях водоемов г.Гомеля по сравнению с контрольным водоемом
|
Водоем
|
Превышение
относительно содержания хрома в контрольном водоеме, раз
|
|
Оз.
Малое
|
8,64
|
|
Оз.
Круглое
|
14,90
|
|
Оз.
У-образное
|
18,31
|
|
Оз.
Волотовское
|
13,06
|
|
Оз.
Шапор
|
5,67
|
|
Оз.
Дедно
|
9,59
|
|
Оз.
Любенское
|
5,17
|
|
Гребной
канал
|
5,04
|
|
Оз.
Володькино
|
3,16
|
|
Р.
Сож (среднее)
|
3,05
|
|
Р.
Сож (н.п. Кленки)
|
3,46
|
|
Р.
Сож (н.п. Ченки)
|
4,76
|
3.2 Химический состав донных
отложений водных объектов г. Гомеля
Как известно, состав донных отложений
формируется, с одной стороны, под влиянием поверхностных вод, с другой -
материала подстилающих первичных грунтов. В этой связи, на элементный состав
донных отложений оказывают влияние как гидрологические факторы (проточность,
колебания уровня, активность гидробионтов), так и геоморфологические
(происхождение водоема, его территориальная и зональная расположенность).
Для наиболее обобщенной оценки содержания
тяжелых металлов в водоемах необходимы данные о типе и химическом составе
донных осадков. При этом первостепенное значение имеет, как указывалось ранее,
исследование органического вещества и минеральной части осадков, как основных
компонентов, депонирующих микроэлементы.
Данные об основных химических компонентах донных
отложений обследованных нами городских водоемов приведены в таблице 5. При
классификации донных отложений в качестве главного критерия используется
показатель содержания в них органического вещества. В соответствии с принятой
системой типовой градации донных грунтов, объекты с содержанием органики меньше
3 % следует относить к пескам, в пределах 3-10 % - к заиленным пескам, свыше 10
% но меньше 20 % - к песчанистым илам [43]. Согласно полученных нами данных,
донные отложения всех обследованных водоемов представляют собой пески, причем в
оз. Малое, Круглое, У-образное, Волотовское, Шапор они являются заиленными.
Так как степень заиления песчаных донных
отложений есть следствие различного гидрологического режима, то высокое
количество органического вещества характерно для донных отложений замкнутых, непроточных
озер. Поэтому максимальная степень заиления, отмеченная в наших исследованиях
для озера Малое, свидетельствует о переходным типе грунта в данном водоеме (от
песков к илам). С увеличением проточности водоема содержание органической
фракции снижается, при этом возрастает доля минеральных компонентов. Поэтому
закономерным является отмеченное нами наименьшее количество органики р.Сож.
Аналогично низкие показатели содержания органического вещества в иле
оз.Володькино свидетельствуют о высокой проточности данного водного объекта.
Как известно, озеро Володькино помимо контакта с русловым током реки Сож,
принимает в свои воды реку Ипуть
По мере роста интенсивности водообмена
обследуемых озер увеличивается содержание в осадках основного компонента
неорганической фракции донных отложений водоемов - кремнезема (SiO2). Его
максимальное количество также характерно для оз.Володькино.
Таблица 5 - Химический состав
донных отложений водоемов г. Гомеля в процентах
|
Водоем
|
Валовое
содержание
|
|
Органическое
вещество
|
SiO2
|
Fe2O3
|
MnO
|
TiO2
|
Al2O3
|
MgO
|
|
Оз.
Малое
|
10,00
|
75,15
|
5,19
|
0,09
|
0,71
|
11,91
|
1,22
|
|
Оз.
Круглое
|
4,75
|
65,31
|
4,88
|
0,09
|
0,54
|
10,90
|
1,60
|
|
Оз.
У-образное
|
4,67
|
67,98
|
6,66
|
0,13
|
0,57
|
1,58
|
|
Оз.
Волотовское
|
3,67
|
69,36
|
3,49
|
0,19
|
0,31
|
6,58
|
1,11
|
|
Оз.
Шапор
|
3,00
|
86,83
|
2,89
|
0,08
|
0,22
|
5,09
|
0,53
|
|
Оз.
Дедно
|
2,50
|
76,43
|
5,05
|
0,08
|
0,37
|
8,44
|
1,03
|
|
Оз.
Любенское
|
2,33
|
74,64
|
6,16
|
0,14
|
0,44
|
9,04
|
1,03
|
|
Гребной
канал
|
1,75
|
77,05
|
5,43
|
0,10
|
0,48
|
10,12
|
1,08
|
|
Оз.
Володькино
|
1,00
|
88,36
|
1,82
|
0,07
|
0,25
|
5,70
|
0,50
|
|
Р.
Сож (среднее)
|
1,71
|
79,33
|
3,98
|
0,31
|
0,40
|
6,97
|
0,81
|
|
Р.
Сож, выше города (н.п. Кленки)
|
2,33
|
71,94
|
5,24
|
0,51
|
0,50
|
8,17
|
1,01
|
|
Р.
Сож, ниже города (н.п. Ченки)
|
1,25
|
84,87
|
3,03
|
0,16
|
0,33
|
6,07
|
0,67
|
|
Контрольный
водоем
|
1,67
|
83,49
|
1,60
|
0,04
|
0,19
|
5,17
|
0,57
|
Относительное содержание оксидов алюминия
(Al2O3), титана (TiO2), магния (MgO) в анализируемых пробах отложений имеет
противоположную тенденцию к снижению от заиленных песков непроточных озер к
пескам речного типа. Генезис этих компонентов в донных отложениях напрямую
связан с присутствием глинистых минералов и подстилающих материнских пород
[43]. Использование этих элементов в качестве маркеров позволяет исследовать
влияние природных глин-сорбентов на процессы аккумуляции микроэлементов и
тяжелых металлов в озерных осадках. Максимальное количество оксидов алюминия,
титана и магния определено в оз.Малое, Круглое и У-образное.
Валовое содержание других природных сорбентов, а
именно оксида марганца (MnO) и железа (Fe2O3) в составе донных отложений
исследуемых водных объектов варьирует независимо от их гидрологического режима
и проточности. Однако присутствие Fe2O3 в осадках городских водоемов имеет
положительную корреляцию с содержанием в них окиси алюминия (r = 0,84), что
указывает на общность их происхождения. Отсутствие достаточно четкой картины в
распределении MnO возможно обусловлено сложным сочетанием факторов
(гидрологического, геохимического, антропогенного), воздействующих с различной
силой на каждый водоем.
3.3 Анализ факторов, определяющих
степень накопления хрома в донных отложениях водоемов г. Гомеля
Проведенный анализ содержания хрома в
обследованных водоемах показал различный характер их распределения в донных
отложениях (табл. 2).
Содержание хрома в донных осадках существенно
варьирует в различных водоемах. Различие между максимальной концентрацией
данного металла в озерах У-образное и Круглое и его наименьшим количеством в
контрольном водоеме и реке Сож составляет 5-18 раз. Менее значимые различия по
указанному показателю наблюдаются между оз.Любенское, Гребной канал, р.Сож.
Выявленное в ходе проведенных исследований
варьирование концентраций хрома в донных отложениях водоемов г.Гомеля может
определяться действием множества факторов как природного, так и техногенного
происхождения. Как отмечалось выше, весьма существенное значение в процессе
аккумуляции металлов в осадках имеют особенности химического состава донных
грунтов.
Таким образом, выводы о степени загрязнения того
или иного водоема должны осуществляться не только с помощью анализа данных по
абсолютному содержанию загрязнителей, но также и с учетом особенностей
происхождения и химического состава донных грунтов.
В таблице 6 представлены значения коэффициента
корреляции, показывающего связь концентрации хрома с основными компонентами
химического состава исследуемых проб донных отложений.
Таблица 6 - Результаты
корреляционного анализа связей между содержанием хрома и химическим составом
донных отложений
|
Элемент
|
Коэффициент
корреляции
|
|
Органическое
вещество
|
SiO2
|
Fe2O3
|
MnO
|
MgO
|
Al2O3
|
TiO2
|
|
Хром
|
0,51
|
-0,75
|
0,53
|
-0,19
|
0,83
|
0,54
|
0,47
|
Следует отметить, что в данном случае при
расчете коэффициента корреляции использовались обобщенные данные по всем
водоемам.
Как видно из таблицы 6, для хрома определены
высокие уровни корреляционной связи по большинству показателей. Самый высокий
коэффициент корреляции установлен между содержанием данного металла в донных
отложениях и концентрацией оксида магния, который является компонентом
природных сорбентов - глинистых минералов. Достаточно существенное, но менее
выраженное влияние на содержание хрома оказывают другие природные сорбенты:
органическое вещество, железомарганцевые оксиды. Наименее выражена связь с
концентрацией оксида марганца и титана.
В ходе проведенных исследований были получены
уравнения линейной связи между содержанием в донных отложениях хрома и
показателями химического состава донных отложений. Следует уточнить, что при
расчете параметров уравнений были выбраны только те водоемы, для осадков
которых отношение концентрации хрома к компоненту было сходно с таковым в контрольном
водоеме (старичный комплекс р. Сож, Ветковский район, д. Поляновка).
Линейная прямо пропорциональная связь содержания
хрома с количеством органического вещества в донных отложениях отображена на
рисунке 2. Аналогичный характер взаимосвязи наблюдался между содержанием хрома
в донных отложениях и количеством оксида магния (рисунок 3). Как видно по
рисункам 1 и 2, весьма высокое аномальное содержание хрома наблюдается в
оз.У-образное.
Таким образом, на накопление хрома в донных
отложениях водоемов городской черты непосредственное влияние оказывают
особенности химического состава отложений. Причем, наибольшим является
воздействие содержания в донных грунтах органического вещества, оксидов магния,
железа и титана.

Рисунок 2 - Зависимость
концентрации хрома от содержания органического вещества в донных отложениях
некоторых водоемов г. Гомеля
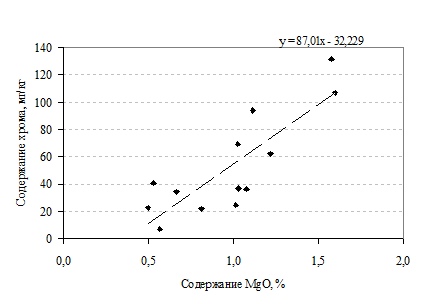
Рисунок 3 - Зависимость
концентрации хрома от содержания окиси магния в донных отложениях некоторых
водоемов г. Гомеля
В таблице 7 приведены значения коэффициентов
линейных уравнений, отражающие связь концентраций хрома с основными
компонентами химического состава донных отложений водоемов г. Гомеля.
Таблица 7 - Параметры
уравнения регрессии для расчета концентрации хрома в зависимости от химического
состава донных отложений
|
Показатель
|
Коэффициент
А
|
Коэффициент
B
|
Коэффициент
корреляции
|
|
Хром
|
|
Органическое
вещество
|
28,47
|
-20,37
|
0,91
|
|
MgO
|
87,01
|
-32,23
|
0,83
|
|
Fe2O3
|
12,76
|
-10.17
|
0,65
|
|
TiO2
|
84,73
|
-4,15
|
0,86
|
Полученные функциональные зависимости
концентраций хрома от состава донных отложений можно использовать как для
прогноза экологической ситуации, так и для выявления аномальных концентраций
этих элементов.
На рис. 4 представлены наблюдаемые и расчетные
значения концентрации хрома по полученным уравнениям связи «окись магния (MgO -
концентрация металла» для всех обследованных нами водоемов.
Из рисунка 4 видно, что для большинства водоемов
характерны близкие значения опытных и расчетных данных содержания хрома в
зависимости от количества в донных отложениях окиси магния. Это в целом
свидетельствует о применимости такого подхода для прогноза концентрации хрома
по известному содержанию окиси магния. Однако для водоемов Круглое, У-образное,
Волотовское, Шапор, Дедно обнаружено значительное расхождение величин
прогнозируемых и действительных концентраций хрома, причем для всех водоемов
реальное накопление этого элемента намного превышает предсказанное. Очевидно,
высокая концентрация хрома в донных отложениях данных водоемов обусловлена
наличием техногенного влияния.
Таким образом, загрязненность донных отложений
тяжелыми металлами и возможное антропогенное поступление поллютантов в водоемы
можно выявить при комплексном изучении абсолютного содержания микроэлементов в
донных грунтах, при анализе превышения количества металлов относительно
контрольного (индикаторного) водоема, при сопоставлении реальных результатов
содержания микроэлементов в донных осадках с прогнозируемыми значениями.

Рисунок 4 - Наблюдаемые и
расчетные значения концентрации хрома в донных отложениях водоемов г. Гомеля
3.4 Оценка миграционной способности
хрома из донных отложений в различные компоненты водных экосистем
Наиболее полная оценка загрязненности городских
водоемов тяжелыми металлами требует комплексного анализа их содержания в
различных биотических и абиотических компонентах водных объектов. Особое
значение при этом имеет изучение процессов миграции элементов-поллютантов в
пределах водоема, а также взаимосвязи и взаимозависимости их содержания в
донных отложениях, воде, растительности и животных организмах.
Наряду с исследованием содержания тяжелых
металлов в донных отложениях, значение которого принимает максимально высокие
показатели, большую роль в комплексной оценке загрязненности водоема тем или
иным тяжелым металлом имеет его содержание в воде. Это обусловлено тем, что
именно чистота воды в наибольшей мере важна для водоемов, находящихся в черте
города и испытывающих рекреационную нагрузку и водоемов, служащих источником
питьевой воды.
Проведенный анализ содержания хрома в воде
водоемов г.Гомеля (таблица 8) показал, что концентрация металла варьирует не
столь существенно, и для большинства водоемов ее средний показатель составляет
4,0 мкг/л. Более низкие показатели (3,3 и 3,6 мкг/л) определены в р.Сож
соответственно в среднем по ее течению и у н.п. Ченки. Более высокие показатели
определены в оз. Любенское и Гребной канал (7 и 5 мкг/л соответственно).
Особенно следует подчеркнуть относительно высокое содержание хрома в воде
контрольного водоема (8 мкг/л).
Наибольший же уровень средней концентрации хрома
в воде, превышающий средний показатель в 4 раза, определен в оз.Волотовское (16
мкг/л).
Необходимо отметить, что очень высокие максимальные
показатели загрязненности определены в оз.Волотовское и в среднем по течению
р.Сож (78,9 мкг/л). Данные параметры значительно превышают концентрацию хрома в
других водных объектах. В то же время, наименьший показатель содержания хрома
определен в контрольном водоеме (0,2 мкг/л). Следует подчеркнуть, что в
контрольном водоеме и в р.Сож (в среднем по ее течению) проявляется наибольшая
вариабельность концентрации хрома.
Очевидно, содержание хрома в воде является менее
лабильным показателем и в меньшей степени, по сравнению с донными отложениями,
связано с интенсивностью антропогенного загрязнения водоема. Минимальное
содержание хрома в воде р.Сож свидетельствует, что на данный параметр большее
влияние оказывает режим проточности водоема. В озерах со слабым течением,
очевидно, концентрация хрома в воде выше.
Кроме того, возможно, играет определенную роль
фиксирующая способность донных отложений, зависящая от их состава. В частности
в донных отложениях р.Сож наблюдалось достаточно высокое содержание оксида
марганца, превышающее показатели других водоемов в 1,5-13 раз.
Таблица 8 - Содержание хрома в
поверхностных водах, высшей водной растительности и в тканях моллюсков,
обитающих в различных водоемах г.Гомеля
|
Водоем
|
Вода,
мкг/л
|
Растения,
мг/кг
|
Моллюски,
мг/кг
|
|
Среднее
|
Мин
|
Макс
|
Среднее
|
Мин
|
Макс
|
Среднее
|
Мин
|
Макс
|
|
Оз.
Малое
|
4,0
|
0,9
|
7,7
|
3,83
|
0,27
|
18,60
|
4,31
|
1,09
|
11,76
|
|
Оз.
Круглое
|
4,0
|
1,0
|
11,7
|
3,19
|
0,53
|
10,50
|
2,33
|
1,14
|
3,47
|
|
Оз.
У-образное
|
4,0
|
1,1
|
10,5
|
1,65
|
0,58
|
2,50
|
1,48
|
1,03
|
2,89
|
|
Оз.
Волотовское
|
16,0
|
1,8
|
78,9
|
29,06
|
0,82
|
113,96
|
1,31
|
1,00
|
1,78
|
|
Оз.
Шапор
|
4,0
|
1,0
|
9,8
|
1,23
|
0,30
|
5,44
|
8,94
|
0,67
|
69,00
|
|
Оз.
Дедно
|
4,0
|
0,8
|
7,9
|
1,37
|
0,50
|
2,88
|
1,57
|
0,55
|
2,33
|
|
Оз.
Любенское
|
7,0
|
2,3
|
8,7
|
1,29
|
0,48
|
3,72
|
1,42
|
1,29
|
1,67
|
|
Гребной
канал
|
5,0
|
1,0
|
12,2
|
5,58
|
1,37
|
9,65
|
2,72
|
0,97
|
7,89
|
|
Оз.
Володькино
|
4,0
|
1,6
|
10,9
|
1,91
|
0,45
|
6,43
|
1,68
|
0,44
|
5,26
|
|
Р.
Сож (среднее)
|
3,3
|
1,0
|
78,9
|
5,49
|
0,51
|
14,72
|
2,04
|
0,57
|
8,63
|
|
Р.
Сож, выше города (н.п. Кленки)
|
4,2
|
1,1
|
5,7
|
2,75
|
0,51
|
14,48
|
1,88
|
0,57
|
4,64
|
|
Р.
Сож, ниже города (н.п. Ченки)
|
3,6
|
1,3
|
7,9
|
6,93
|
1,17
|
14,72
|
3,43
|
0,83
|
8,63
|
|
Контрольный
водоем
|
8,0
|
0,2
|
23,3
|
1,91
|
0,55
|
4,99
|
1,89
|
1,40
|
2,19
|
Определенную роль играет и состояние равновесия
природной экосистемы водоема. Очевидно, в случае постоянного избыточного
поступления металла в воду, его фиксация донными отложениями происходит не
сразу, и в течение некоторого времени повышенное содержание микроэлемента в
воде сохраняется.
В таблице 9 приведены показатели соотношения
содержания хрома в донных отложениях и воде для различных водоемов г.Гомеля
(вычислялось как концентрация Cr в донных отложениях деленная на концентрацию
Cr в воде). Как видно из таблицы, минимальное значение данного соотношения
(0,9) определено для контрольного водоема, не испытывающего антропогенной
нагрузки. В большинстве обследованных водных объектов рассматриваемое
соотношение составляет 5- 6. Видимо данный показатель соответствует состоянию
динамического равновесия, которое наступает после поступления в водоем
загрязнителей, их фиксации донными отложениями с последующим вымыванием поверхностными
водами. В то же время, в отдельных водоемах (оз.У-образное, Круглее, Малое,
Дедно и Шапор) данное соотношение несколько выше. Возможно, в данных озерах
имеет место избыточная фиксация хрома в донных отложениях либо из-за их высокой
аккумулятивной способности, либо за счет того, что стадия равновесия еще не
достигнута.
Проведенный корреляционный анализ позволил
выявить наличие достоверных связей между большинством показателей химического
состава донных отложений и соотношением донные отложения/вода (таблица 10).
Данный факт свидетельствует, что сорбционная способность водоемов оказывает
непосредственной влияние на интенсивность миграции хрома между водой и донными
отложениями.
Таблица 9 - Показатели соотношения донные
отложения / вода для различных водоемов г.Гомеля
|
Водоем
|
Соотношение
донные отложения/вода
|
|
Оз.
Малое
|
15,6
|
|
Оз.
Круглое
|
26,8
|
|
Оз.
У-образное
|
33,0
|
|
Оз.
Волотовское
|
5,9
|
|
Оз.
Шапор
|
10,2
|
|
Оз.
Дедно
|
17,3
|
|
Оз.
Любенское
|
5,3
|
|
Гребной
канал
|
7,3
|
|
Оз.
Володькино
|
5,7
|
|
Р.
Сож (среднее)
|
6,6
|
|
Р.
Сож, выше города (н.п. Кленки)
|
5,9
|
|
Р.
Сож, ниже города (н.п. Ченки)
|
9,5
|
|
Контрольный
водоем
|
0,9
|
Таблица 10 - Результаты
корреляционного анализа связей между химическим составом донных отложений и
соотношением донные отложения/вода по содержанию хрома
|
Элемент
|
Коэффициент
корреляции
|
|
Органическое
вещество
|
SiO2
|
Fe2O3
|
MnO
|
MgO
|
Al2O3
|
TiO2
|
|
Хром
|
0,50
|
-0,58
|
0,56
|
-0,21
|
0,57
|
0,62
|
0,77
|
Таким образом, избыточное поступление хрома в
водоем не всегда отражается на содержании метла в воде, т.е. концентрация хрома
в поверхностных водах в незначительной мере отражает общий уровень поступления
данного металла в водный объект, а зависит от ряда других дополнительных
факторов.
Оценка биодоступности тяжелых металлов в водоеме
невозможна без анализа их поступления в растительные и животные компоненты
водного объекта. В этой связи, особенно важно определить индикаторные
организмы, отражающие общую степень загрязненности водоема.
Проведенные исследования (таблица 8) показали,
что самая высокая средняя загрязненность растительности определена в
оз.Волотовское (29,1 мг/кг). В этом же водоеме определен максимальный
показатель содержания хрома среди всех обследованных образцов (114,0 мг/кг).
Загрязненность растений в контрольном водоеме
также характеризуется невысокими показателями (в среднем 1,9 мг/кг), однако они
превышают параметры ранее отмеченных водных объектов. Возможно, уровень
биологической доступности в контрольном водоеме несколько выше, чем в водоемах,
испытывающих антропогенную нагрузку и не достигших состояния равновесия.
Очень низкая концентрация хрома в растениях
определена в оз.У-образное (2,9 мг/кг). Особый интерес отмеченный факт
представляет в связи с тем, что в данном водоеме наблюдалось максимальное
содержание хрома в донных отложениях. Возможно, указанное явление обусловлено
высокой аккумулирующей способностью донных отложений оз.У-образное по отношению
к хрому и его низкой биологической доступностью. Также вероятной причиной может
быть преимущественное поступление хрома в растительность в данном водоеме из
воды, по сравнению с донными отложениями. Вариабельность накопления хрома
растениями в оз.У-образное также невелика.
Таким образом, наибольшее среднее содержание
хрома в растительности водоемов г.Гомеля наблюдалась в оз.Волотовское, а
минимальное - в оз.Шапор и Дедно. Накопление хрома растениями не всегда соотносится
с его концентрацией в донных отложениях, т.к. на уровень аккумуляции металла
живыми организмами зависит от ряда других факторов.
Биологическая доступность хрома животным
организмам может быть оценена с помощью анализа его содержания в тканях
моллюсков. Проведенные исследования показали значительные отличия данного
показателя в разных водоемах.
Наибольшая средняя концентрация хрома у
моллюсков (таблица 8) определена в оз.Шапор (8,94 мг/кг). При этом следует
отметить, что в данном водоеме отмечен также максимальный среди всех
обследованных образцов тканей моллюсков показатель загрязненности хромом (69,0
мг/кг) и самая высокая вариабельность данного параметра (минимальное значение
составляет 0,67 мг/кг). В следующем по уровню загрязненности моллюсков водоеме
- оз.Малое - среднее содержание хрома в 2 раза ниже - 4,3 мг/кг.
Минимальная средняя концентрация хрома в тканях
моллюсков определена в оз.Волотовское (1,31 мг/кг). Вариабельность содержания
хрома в данном водоеме также невысока. Указанная особенность противоречит
отмеченным ранее высоким показателям загрязненности данным металлом донных
отложений, воды и растений. Очевидно, поступление хрома в ткани моллюсков
подчиняется иным закономерностям и мало связано с содержанием данного металла в
других компонентах водоема.
Таким образом, загрязненность хромом тканей
моллюсков не всегда четко соотносится с показателями накопления данного металла
в других компонентах водных объектов. Это связано со сложными миграционными
процессами данного металла в пределах водоема и особенностями достижения
динамического равновесия после его поступления в водоем в результате
антропогенного воздействия.
Проведенный анализ корреляционных связей между
накопления хрома различными компонентами обследованных водоемов г.Гомеля показал
(таблица 11), что высокие статистически достоверные коэффициенты корреляции
(r=0,85) определены лишь между содержанием хрома в воде и растениях водоемов.
На основании этого можно предположить, что вода является основным источником
поступления хрома в водную растительность.
Подтвердить данное предположение позволяет
выраженная линейная зависимость накопления хрома растениями от его содержания в
воде, отображенная на рисунке 4. В то же время из рисунка видно, что в
оз.Волотовское, на отдельных участках р.Сож наблюдается более высокое
поступление хрома в растительность относительно его содержания в воде. Однако в
оз.Любенское и контрольном водоеме интенсивность аккумуляции металла несколько
снижена. Данные факты могут свидетельствовать о различной степени биологической
доступности металла в разных водоемах.
Таблица 11 - Результаты корреляционного анализа
взаимосвязи между содержанием хрома в различных компонентах обследованных
водоемов
|
Объект
|
Среднее
|
Стандартное
отклонение
|
Коэффициент
корреляции r
|
Коэффициент
детерминации r2
|
Критерий
Стьюдента t
|
Достоверность
p
|
|
Донные
отложения
|
53,06
|
37,61
|
0,17
|
0,03
|
0,58
|
0,57
|
|
Вода
|
5,47
|
3,45
|
|
|
|
|
|
Донные
отложения
|
53,06
|
37,61
|
0,27
|
0,07
|
0,92
|
0,38
|
|
Растения
|
5,09
|
7,44
|
|
|
|
|
|
Донные
отложения
|
53,06
|
37,61
|
-0,14
|
0,02
|
-0,48
|
0,64
|
|
Моллюски
|
2,69
|
2,07
|
|
|
|
|
|
Вода
|
5,47
|
3,45
|
0,85
|
0,73
|
5,42
|
0
|
|
Растения
|
5,09
|
7,44
|
|
|
|
|
|
Вода
|
5,47
|
3,45
|
-0,28
|
0,08
|
-0,95
|
0,36
|
|
Моллюски
|
2,69
|
2,07
|
|
|
|
|
|
Растения
|
5,09
|
7,44
|
-0,20
|
0,04
|
-0,67
|
0,52
|
|
Моллюски
|
2,69
|
2,07
|
|
|
|
|
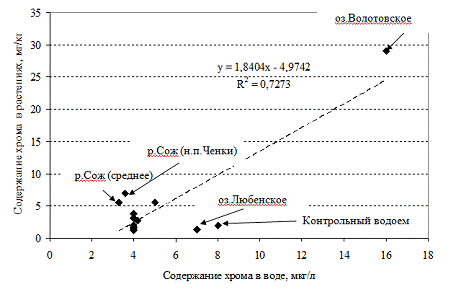
Рисунок 5 - Зависимость
содержания хрома в растительности от его концентрации в воде
В целом, достаточно сложно судить относительно
миграционных процессов хрома между остальными компонентами водоемов. Очевидно,
они подчиняются более сложным закономерностям и находятся под влиянием ряда
дополнительных факторов.
ЗАКЛЮЧЕНИЕ
Анализ загрязненности донных отложений хромом
позволил установить следующие закономерности:
Самое высокое среди всех обследованных водных
объектов содержание хрома (131,8 мг/кг) наблюдалось в оз.У-образное.
Минимальное значение содержания данного металла среди всех обследованных
образцов также получено в контрольном водоеме (0,13 мг/кг). Самый высокий
коэффициент варьирования установлен в оз.Волотовское (более 92%). Наименьшая
степень варьирования содержания хрома в донных отложениях установлена в оз.
Малое и р.Сож (н.п. Ченки), где она составляет всего 8%.
Максимальное превышение кларка по содержанию
хрома в донных отложениях (почти в 5 раз) отмечено в оз.У-образное, для
большинства других обследованных водоемов также характерна загрязненность
донных отложений хромом, превышающая естественный уровень. Содержание хрома на
среднем участке р.Сож, у н.п.Кленки, в оз.Володькино и контрольном водоеме
значительно ниже кларковых параметров (почти в 4 раза). Загрязненность донных
отложений оз.У-образное хромом выше уровня контрольного водоема более, чем в 18
раз. В наименьшей степени показатели контрольного водоема превышены в р.Сож (не
более, чем в 5 раз).
Установлены высокие уровни корреляционной
зависимости концентрации хрома в донных отложениях от содержания в них оксида
магнии, алюминия, железа, органического вещества (r=0,83; 0,54; 0,53 и 0,51
соответственно).
Содержание хрома в воде водоемов г.Гомеля варьирует
не столь существенно, и для большинства водных объектов ее средний показатель
составляет 4,0 мкг/л. Наибольший уровень средней концентрации хрома в воде
определен в оз.Волотовское (16 мкг/л), минимальный (3,3 и 3,6 мкг/л) - в р.Сож
соответственно в среднем по ее течению и у н.п. Ченки.
Минимальное значение соотношения донные
отложения / вода (0,9) определено для контрольного водоема, максимальное (33) -
в оз.У-образное.
Самая высокая загрязненность растительности
водоемов определена в оз.Волотовское (29,1 мг/кг). Минимальное среди всех
обследованных водоемов содержание хрома в растительности определено в оз.Малое
(0,27 мг/кг).
Наибольшая концентрация хрома у моллюсков
(таблица 5) определена в оз.Шапор (8,94 мг/кг). Минимальная средняя
концентрация хрома в тканях моллюсков определена в оз.Волотовское (1,31 мг/кг).
Высокие статистически достоверные коэффициенты
корреляции (r=0,85) определены между содержанием хрома в воде и растениях
водоемов.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
1. Законнов
В.В. Аккумуляция биогенных элементов в д.о. водохранилищ Волги / В.В. Законов
// Органическое вещество д.о. Волжских водохранилищ. СПб.: Гидрометиоиздат,
1993. - С. 3-16.
2. Козловская
В.И., Герман А.В. Полихлорированные бифенилы и полиароматические углеводороды в
экосистеме Рыбинского водохранилища / В.И. Козловская, А.В. Герман // Вод.
ресурсы. - 1997. Т.24. №5. - С.563-569.
. Лозановская
И.Н. Экология и охрана биосферы при химическом загрязнении: Учеб. Пособие для
хим., хим-технол. и биол. спец. вузов / И.Н. Лозановская, Д.С. Орлов, Л.К.
Садовникова. - «Высшая школа», -1998. - 287 с.
4. Chapman,
P.M. Synoptic measures of sediment contamination, toxicity, and infffaunal
community composition in San Francisco Bay / Р.М.Chapman
// Mar. Ecol.
Prog. Ser.1987.V.37.P.321-329.
. Денисова
А.И. Формирование гидрохимического режима водохранилищ Днепра и методы его
прогнозирования / А.И. Денисова. - Киев: Наук. думка, 1979.-290 с.
6. Forstner
U. Sediment oxygen demand chemical substances / U.Forstner // Water Res. -
1983. - Vol. 9. №17. - P. 1081-1093.
. Тарновский
А.А. Геохимия донных отложений современных озер / Тарновский. - Л.: Изд-во ЛГУ,
1980.- 172 с.
. Зайцева
Е.Д. Обменные катионы осадков Черного моря / Е.Д.Зайцева // Тр. ин-та
океанологии. - 1982. - 54. - С. 58-82.
. Кузнецов
С.И. Микрофлора озер и ее геохимическая деятельность / С.И. Кузнецов -Л.:
Наука, 1970.- 440 с.
. Прыткова
М.Я. Осадконакопление в малых водохранилищах / М.Я. Прыткова. - Л.: Наука,
1981.-152с.
. Лейбович
П.З. Закономерности пространственного распределения растворенных форм железа и
марганца в донных отложениях Байкал / П.З. Лейбович. - Лимнол. ин-т СО АН СССР.
Листвиничное на Байкале. -1980.- 20 с.
. Даувальтер
В.А. Концентрации металлов в донных отложениях заиленных озер / В.А. Даувальтер
// Водные ресурсы. - 1998. - Т.25, №3. - С. 358-365.
. Осадчий
Н.И. Химия и микробиология природных и сточных вод / Н.И. Осадчий. - М.: Мир,
1987.- 285 с.
. Нахимина
Т.А., Белоконь А.В. Водная токсикология. -М.: Стройиздат, 1987. - 120 с.
. Мур
Дж. Тяжелые металлы в тяжелых водах / Дж. Мур. - М.: Мир, 1985. - 280 с.
. Вахмистров
Д.Б. Исследование механизмов поглощения солей растениями / Д.Б. Вахмистров //
Агрохимия, 1968. - №1. - С.151-163.
. Кларксон
Д. Транспорт ионов и структура растительной клетки / Д. Кларксон. - М.: Мир,
1978. - 368 с.
18. Haynes
R.I. Ion exchange properties of roots and ionic interaction within the root
apoplasm. Their role in ion accumulation by plants / R.I.Haynes. - Bot. Rev.,
1980. - Vol. 46, №1. - P.75-99.
. Романенко
А.С. Электронно-микроскопическое изучение поступления тяжелых металлов в клетки
корней растений / Романенко, А.С., Саляев Р.К. // Цитология, 1978. - т.20, №5.
- С.491-495.
. Алексеева-Попова
Н.В. Эколого-физиологические исследования металлоустойчивости растений / Н.В.
Алексеева-Попова, А.В. Косицин // IX Всесоюзная конференция по проблеме
микроэлементов в биологии / Тез. докл. - Кишинев: ШТИИНЦА, 1981. - С.11-14.
. Ильин
В.Б., Степанов М.Д. О фоновом содержании тяжелых металлов в растениях / В.Б.
Ильин. // Изв. Сиб. отд-я АН УССР. Сер. биол. наук, 1981. - вып. I, №5. -
С.26-31.
. Лукина
Л.Ф. Физиология высших водных растений / Л.Ф. Лукина, Н.Н. Смирнова. - Киев:
Наукова думка, 1998. - 184 с.
23. Butler
P.A. Monitoring organisms / P.A. Butler, L. Andren, G.L.Bond // Food and
agricultural Organization Technical Conference on Marine Pollution and its
Effects on Living Researches and Fishing / Ed. by M. Ruivo. - London: Fishing
News (Books), Ltd., 1971. - P.101-112.
24. Диклева
Д., Петрова М.А. Химический состав макрофитов и факторы, определяющие
концентрацию минеральных веществ в высших водных растениях / Д. Диклева, М.А.
Петрова. - Гидробиологические процессы в водоемах; сб. статей под ред.
Распопова И.М. - Л.: Наука, 1983. - с.116-205.
. Брень
Н.В. Использование беспозвоночных для мониторинга загрязнения водных экосистем
тяжелыми металлами / Н.В. Брень // Гидробиологический журнал. - 1999. - Т. 35,
№4. - С. 75-88.
. Патин
С.А., Биогеохимия металлов в экосистеме бассейна Акрашон / С.А. Патин, А.А.
Тихомирова, Л.Л. Демина // Геохимия. 1976. - Вып. 9. - С. 1427-1433.
. Зубкова
Е.И. Мониторинг микроэлементов в Кучурганском водохранилище / Е.И. Зубкова //
Гидробиологический журнал. - 1998. - Т. 34, №4. - С. 105.
28. Wright
D.A. Heavy metal accumulation by aquatic invertebrates / D.A. Wright // Appl.
biol. - 1978. - 3. - P. 331-394.
29. Брень
Н.В., Домашлинец В.Г. Беспозвоночные как мониторы полиметаллического
загрязнения донных отложений / Н.В. Брень, В.Г. Домашлинец //
Гидробиологический журнал. - 1998. - Т.34, № 4. - С.80-93.
. Флеров
Б.Л. Эколого-физиологические аспекты токсикологии пресноводных животных / Б.Л.
Флеров - Л.: Наука, 1989. - 144 с.
31. Betzer
S.B., Yevich P.P. Copper toxicity in Busycon canaliculatum / S.B. Betzer, P.P.
Yevich // Biol. Bull. - 1975. - 48, № 1.- Р. 16-25.
. Никаноров,
А.М. Биомониторинг тяжёлых металлов в пресноводных экосистемах /А.В. Жулидов,
А.Д. Покаржевский. - М.: Гидрохимический институт, 1985.- С. 139.
. Никаноров
А.М. Биомониторинг металлов в пресноводных экосистемах / А.М. Никаноров, А.В.
Жулидов. - Л.: Гидрометеоиздат, 1991. - 279 с.
. Виноградова
З.А. Микроэлементы в планктоне и воде различных районов Черного моря / З.А.
Виноградова, Г.М. Коган // Биология моря. - Киев, 1971. - Вып. 22. - С. 16-47.
. Варенко
Н.И. Динамика содержания марганца в Днепродзержинском и Днепровском
водохранилищах / Н.И. Варенко; В.Т. Чуйко // Гидрохим. материалы. - 1975. - 64.
- С. 71-76.
. Морозов
Н.П. Основные черты биогеохимии микроэлементов группы металлов в экосистемах
океанов и морей / Н.П. Морозов, С.А. Патин, С.А. Петухов // Тр. ВНИРО. - 1987.
- 84. - С. 23-35.
. Левина
Э.М. Значение накопления металлов в клетке / Э.М. Левина // Актуальные проблемы
гигиенической токсикологии. - М.: 1980. - С. 53-66.
. Метелев
В.В. Водная токсикология / В.В. Метелев, А.И. Канаев, Н.Г. Дзасохова. - М.:
Пищевая промышленность, 1971. - 248 с.
. Линник
П.Н., Комплексообразование ионов металлов в природных водах / П.Н. Линник, Б.И.
Набиванец // Гидробиологический журнал - 1983. - Т.19, № 3. - С. 82-95.
. Мартин
Р. Бионеорганическая химия токсических ионов металлов. Некоторые вопросы
токсичности ионов металлов / Р. Мартин. - М.: Мир, 1993. - С. 25-61.
. Физико-химические
методы анализа. Практическое руководство: учеб. пособие для вузов /
В.Б.Алесковский и др. - Химия, 1998. - С.53-97.
. Лакин
Г.Ф. Биометрия / Г.Ф. Лакин. - М.: Высш. школа, 1980. - 293 с.
. Денисова
Л.И. Донные отложения водохранилищ и их влияние на качество воды / Е.П.
Нахшина, Б.И. Новиков. - Киев: Навукова думка, 1987. - 163 с.