Использование биологических объектов для изучения загрязнений окружающей среды тяжелыми металлами
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РЕСПУБЛИКИ
БЕЛАРУСЬ
Учреждение образования
"Гомельский государственный
университет имени Франциска Скорины"
биологический факультет
Кафедра химии
Использование биологических объектов
для изучения загрязнений окружающей среды тяжелыми металлами
Курсовая работа
Исполнитель: студент группы Б-42 В.В. Глушенкова
Научный руководитель
к. б. н., доцент Т.В. Макаренко
Гомель 2013
Реферат
Курсовая работа 34 страниц, 3 таблицы, 1 рисунок, 26
источника.
Ключевые слова: загрязнение окружающей среды, тяжёлые
металлы, биоиндикация, биоиндикаторы
Цель работы:
изучить использование биологических объектов в качестве
индикаторов загрязнения окружающей среды тяжелыми металлами.
Задачами курсовой работы являются:
. привести общую характеристику тяжёлых металлов, пути их
попадания в окружающую среду;
. раскрыть сущность биоиндикации и её методы;
. составить обзор литературы по проблеме использования
биологических объектов для изучения загрязнений окружающей среды тяжёлыми
металлами
Актуальность темы:
Все большее разнообразие загрязняющих веществ и вариантов
ответных реакций представителей биоты на разные дозы химического загрязнения
требуют разработки новых методов оценки состояния окружающей среды, в том числе
и составление кадастра концентраций химических элементов экосистем. Актуальными
остаются учет последствий процессов аккумуляции и рассеивания элементов,
выявление видов-индикаторов, чувствительных к составу среды.
Наилучшим показателям водных систем тяжелыми металлами
являются высшие растения, преимущество которых выражается в том, что они видны
невооруженным глазом, не перемещаются, так как прикреплены к грунту и в
процессе жизнедеятельности способны поглощать и накапливать вещества различной
химической природы.
Занимая прибрежную часть водоема и литературную его область.
Высшая водная растительность служит своеобразным барьером, предотвращающим
проникновение в водоемы и водотоки недостаточно очищенных сточных вод. В зоне
произрастания макрофитов происходят важные процессы задержания и переработки
многих биогенных элементов и загрязняющих веществ.
Содержание
Реферат
Введение
1. Обзор литературы
1.1 Общая характеристика тяжёлых металлов. Формы нахождения тяжёлых
металлов в окружающей среде
1.1.1 Источники поступления тяжелых металлов в окружающую среду
1.2 Теория и сущность биоиндикации
1.2.1 Методы биоиндикации
1.2.2 Особенности использования растений, животных и
микроорганизмов в качестве биоиндикаторов
1.3 Биологические объекты как индикаторы загрязнения окружающей
среды тяжелыми металлами
Заключение
Список литературы
Введение
Одной из важнейших проблем современности и обозримого
будущего является проблема загрязнения окружающей среды тяжелыми металлами.
Соединения этих элементов в силу высокой токсичности, подвижности и способности
к биоаккумуляции представляют опасность не только для человека, но и для всего
живого на планете. Кроме того, в отличие от токсикантов органической природы,
подвергающихся деструкции, однажды включившись в биогеохимические циклы, они
могут сохранять свою биологическую активность практически бесконечно. Поэтому
оценка загрязнения экосистем тяжелыми металлами является одной из важнейших
задач мониторинга природных сред.
Для контроля за состоянием объектов окружающей среды в
настоящее время как отечественной, так и зарубежной промышленностью создаётся
большое количество аналитических приборов, позволяющих с достаточной точностью
определять химический состав исследуемых сред, но в силу ряда причин (высокая
стоимость, большие сроки, необходимые для проведения исследований) они не
доступны для широкого применения. К тому же ещё не достаточно освещен вопрос
воздействия многих химических элементов на биологические объекты.
Безусловно, посредством методов
химического анализа можно установить присутствие вредных веществ в окружающей
среде даже в самых незначительных количествах. Однако этого оказывается
недостаточно для того, чтобы определить качественное воздействие этих веществ
на человека и окружающую среду, и тем более, отдаленные последствия.
Преимущество биологического мониторинга
определяется рядом обстоятельств. Во-первых, в изменение физических и
химических параметров загрязненности природной среды более трудоемко по
сравнению с методами биоиндикации. Во-вторых, в окружающей среде нередко
присутствует не один, а несколько токсических компонентов, которые в комплексе
воздействуют на живые организмы куда сильнее, чем каждый в отдельности.
окружающая среда индикатор биологический
1. Обзор
литературы
1.1 Общая
характеристика тяжёлых металлов. Формы нахождения тяжёлых металлов в окружающей
среде
Тяжелые металлы относятся к приоритетным загрязняющим
веществам, наблюдения за которыми обязательны во всех средах.
Термин тяжелые металлы, характеризующий широкую группу
загрязняющих веществ, получил в последнее время значительное распространение. В
различных научных и прикладных работах авторы по-разному трактуют значение
этого понятия. Так сложилось, что термины "тяжелые металлы" и
"токсичные металлы" стали синонимами. [12, 15]
В работах, посвященных проблемам загрязнения окружающей
природной среды и экологического мониторинга, на сегодняшний день к тяжелым
металлам относят более 40 металлов периодической системы Д.И. Менделеева с
атомной массой свыше 50 атомных единиц. При этом немаловажную роль в
категорировании тяжелых металлов играют следующие условия: их высокая
токсичность для живых организмов в относительно низких концентрациях, а также
способность к биоаккумуляции и биомагнификации. Практически все металлы,
попадающие под это определение (за исключением свинца, ртути, кадмия и висмута,
биологическая роль которых на настоящий момент не ясна), активно участвуют в
биологических процессах, входят в состав многих ферментов. По классификации Н.
Реймерса, тяжелыми следует считать металлы с плотностью более 8 г/см3.
Таким образом, к тяжелым металлам относятся Pb, Cu, Zn, Ni, Cd, Co, Sb, Sn, Bi,
Hg [12, 15].
О масштабах загрязнения тяжелыми металлами можно судить из
данных, характеризующих общемировое годовое производство. Однако необходимо
учитывать и другие источники. Например, 1,5-2 тыс. т ртути ежегодно поступает в
биосферу при переработке минералов и руд, 0,1-8 тыс. т - при сжигании топлива;
ежегодно в биосферу при сжигании угля попадает около 3,5 тыс. т свинца, 56 тыс.
т - в результате выветривания и 110 тыс. т выносят реки [20].
Степень токсичности тяжелых металлов для человека и животных,
а также для растений неодинакова и колеблется в весьма широких пределах. К
числу наиболее токсичных металлов следует отнести кадмий, ртуть, свинец, хром и
некоторые другие; они оказывают повреждающее действие на биообъекты в
концентрациях, не превышающих 1 мг/л. Так, цинк, титан характеризуются низкой
токсичностью для человека и теплокровных животных, но даже в низких
концентрациях они оказывают губительное действие на рыб и других обитателей
водных экосистем [20].
Кадмий.
Кадмий относится к числу металлов, которые, попав
в живой организм, влияют на него губительно. Весьма важным является фактор
длительности воздействия кадмия на организм человека и животных в связи с его
способностью накапливаться в печени, почках, поджелудочной и щитовидной железах
и др. Кадмий характеризуется выраженной нефротоксичностью при попадании в
организм с питьевой водой [20].
Высокой чувствительностью к действию кадмия характеризуются
водные организмы. Так, пребывание рыб (гуппи, карп, карась и др.) на протяжении
суток в воде с содержанием Сd2+ 0,001-0,3 мг/дм3 приводит к их гибели
[20].
В природные воды поступает при выщелачивании почв,
полиметаллических и медных руд, в результате разложения водных организмов,
способных его накапливать. Соединения кадмия выносятся в поверхностные воды со
сточными водами свинцово-цинковых заводов, рудообогатительных фабрик, ряда
химических предприятий (производство серной кислоты), гальванического
производства, а также с шахтными водами. Понижение концентрации растворенных
соединений кадмия происходит за счет процессов сорбции, выпадения в осадок
гидроксида и карбоната кадмия и потребления их водными организмами. Предельно
допустимая концентрация (ПДК) кадмия в природных водах составляет 0,005мг/дм3
[20,22,23].
Растворенные формы кадмия в природных водах представляют
собой главным образом минеральные и органоминеральные комплексы. Основной
взвешенной формой кадмия являются его сорбированные соединения. Значительная
часть кадмия может мигрировать в составе клеток гидробионтов. В речных
незагрязненных и слабозагрязненных водах кадмий содержится в субмикрограммовых
концентрациях, в загрязненных и сточных водах концентрация кадмия может
достигать десятков микрограммов в 1 дм3. Соединения кадмия играют
важную роль в процессе жизнедеятельности животных и человека. В повышенных
концентрациях токсичен, особенно в сочетании с другими токсичными веществами [12,
14, 20].
Кобальт.
В природные воды соединения кобальта попадают в результате процессов
выщелачивания их из медноколчедановых и других руд, из почв при разложении
организмов и растений, а также со сточными водами металлургических,
металлообрабатывающих и химических заводов. Некоторые количества кобальта
поступают из почв в результате разложения растительных и животных организмов [20].
Соединения кобальта в природных водах находятся в
растворенном и взвешенном состоянии, количественное соотношение между которыми
определяется химическим составом воды, температурой и значениями рН. Растворенные
формы представлены в основном комплексными соединениями, в т. ч. с
органическими веществами природных вод. Соединения двухвалентного кобальта
наиболее характерны для поверхностных вод. В присутствии окислителей возможно
существование в заметных концентрациях трехвалентного кобальта [12, 14]. ПДК
кобальта в поверхностных водах составляет 0,01 мг/дм3 [22,23].
Кобальт относится к числу биологически активных элементов и
всегда содержится в организме животных и в растениях. С недостаточным
содержанием его в почвах связано недостаточное содержание кобальта в растениях,
что способствует развитию малокровия у животных (таежно-лесная нечерноземная
зона). Входя в состав витамина В12, кобальт весьма активно влияет на
поступление азотистых веществ, увеличение содержания хлорофилла и аскорбиновой
кислоты, активизирует биосинтез и повышает содержание белкового азота в
растениях. Вместе с тем повышенные концентрации соединений кобальта являются
токсичными. В речных незагрязненных и слабозагрязненных водах его содержание
колеблется от десятых до тысячных долей миллиграмма в 1 дм3, среднее
содержание в морской воде 0.5 мкг/дм3 [12, 14].
Медь.
Медь - один из важнейших микроэлементов. Физиологическая
активность меди связана главным образом с включением ее в состав активных
центров окислительно-восстановительных ферментов. Недостаточное содержание меди
в почвах отрицательно влияет на синтез белков, жиров и витаминов и способствует
бесплодию растительных организмов. Медь участвует в процессе фотосинтеза и
влияет на усвоение азота растениями. Вместе с тем, избыточные концентрации меди
оказывают неблагоприятное воздействие на растительные и животные организмы.
Содержание меди в природных пресных водах колеблется от 2 до 30 мкг/дм3,
в морских водах - от 0.5 до 3.5 мкг/дм3. Повышенные концентрации
меди (до нескольких граммов в литре) характерны для кислых рудничных вод. В
природных водах наиболее часто встречаются соединения Cu (II). Из соединений Cu
(I) наиболее распространены труднорастворимые в воде Cu2O, Cu2S,
CuCl. При наличии в водной среде лигандов наряду с равновесием диссоциации
гидроксида необходимо учитывать образование различных комплексных форм,
находящихся в равновесии с акваионами металла [12, 14, 19].
Основным источником поступления меди в природные воды
являются сточные воды предприятий химической, металлургической промышленности,
шахтные воды, альдегидные реагенты, используемые для уничтожения водорослей.
Медь может появляться в результате коррозии медных трубопроводов и других
сооружений, используемых в системах водоснабжения. В подземных водах содержание
меди обусловлено взаимодействием воды с горными породами, содержащими ее [12,
14, 19]. ПДК меди в поверхностных водах составляет 0,005мг/дм3 [22,23].
Свинец.
Свинец попадает в окружающую среду в больших
количествах. Ежегодно в земную атмосферу выбрасывается около миллиона тонн его
соединений, значительная часть которых водорастворима, что обусловливает
экологическую опасность Рb2+. Основной источник - этилированный бензин.
Токсикологическая опасность свинца усугубляется его активным всасыванием в
пищеварительном тракте человека и животных, значительным объемом распределения
в тканях и накоплением в костях. Депонированный в костях свинец способен
поступать в кровь, с током которой доставляется в различные органы. Считают,
что в организм взрослого человека с водой и продуктами питания за сутки
поступает 0,3 мг свинца [20].
Случаи хронического отравления свинцом наблюдаются при
длительном употреблении питьевой воды, в которой его содержание достигает 0,04
- 1 мг/дм3.
В наибольшей степени опасному воздействию свинца подвергаются
рабочие, занятые на его добыче в шахтах, а также при выплавке. В этом случае
металл поступает в организм ингаляционным путем [20].
Проведенные в Гренландии исследования показали, что
содержание свинца во льду, образованном примерно в середине XVIII в., оказалось
примерно в 25 раз выше, чем во льду, образование которого было отнесено к VIII
в. до н.э. С 1750 г. накопление свинца в ледниках Гренландии постоянно
возрастает. С 40-х гг. XX в. этот процесс усилился и продолжается до настоящего
времени [20].
Определенную роль в накоплении свинца в экосистемах играют
растения, получающие металл не только из атмосферы, но и из почвы. Отмечается
видовая специфичность растений при его накоплении. Так, при выращивании
растений присутствующий в атмосфере свинец обнаружен в листьях салата и бобов,
но практически отсутствует в томатах, кочанной капусте, картофеле и моркови [20].
Свинцовая интоксикация вызывает нарушение биосинтеза
гемоглобина на уровне ингибирования левулинатдегидратазы и гемсинтетазы.
Имеются сведения о нарушении синтеза цитохрома Р-450 при свинцовой интоксикации
[20].
Главной мишенью воздействия свинца при хронических
отравлениях являются центральная и периферическая нервные системы (свинцовая
энцелопатия: появление головной боли, нарушение сна, памяти, возникновение
тремора, галлюцинаций и т.д.). Для различных вариантов отравления свинцом
характерно поражение почек, пищеварительного тракта [20].
ПДК свинца в поверхностных водах составляет 0,1мг/дм3
[22,23].
Ртуть.
Ртуть и ее соединения относятся к веществам
общетоксического действия, вызывающим у людей летальный исход, попадая в
организм с питьевой водой в количестве 75-300 мг в сутки. Наиболее токсична
двухлористая ртуть (сулема), однократная летальная доза которой составляет для
человека 0,2-0,5 г. Ртуть характеризуется высокой нефротоксичностью, приводящей
к быстро развивающейся почечной недостаточности. Выведение ртути осуществляется
почками, через пищеварительный тракт, потовыми и молочными железами [20].
Начиная с концентрации 0,006-0,01 мг/дм3 ртуть в
виде водорастворимых солей оказывает губительное влияние на рыб и другие водные
организмы [20].
При отравлениях ртутью, особенно ее органическими
соединениями, отчетливо выражены симптомы поражений нервной системы (парезы,
параличи, нарушения зрения и слуха) [20].
Нg2+ + донор метильной группы - > СН3 - Нg+,
СН3 - Нg+ + донор метильной группы СН3 - Нg+ - СН3.
Организмы, способные осуществлять эти реакции, в своих
обычных метаболических процессах используют трансметилирование, образуя такие
соединения, как метан; в этих системах могут реагировать также и металлы [20].
Метилртутные и некоторые другие ртутьорганические
соединения отличаются особой токсичностью. Они растворимы в жирах, и поэтому
хорошо всасываются, легко проникают через гематоэнцефалический барьер и
приводят к нейротоксическим эффектам [1].
Соединения ртути опасны для популяций позвоночных, так как,
проходя через пищевые цепи, способны повышать свою концентрацию в десятки раз
(см рис.1), а вследствие длительного биологического периода полураспада
медленно выводятся из организма [1].
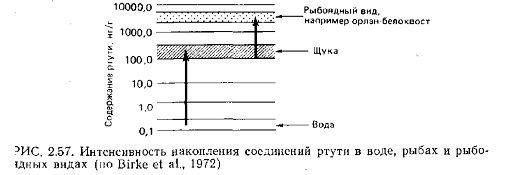
Рисунок 1. Интенсивность накопления соединений
ртути в воде, рыбах и рыбоядных видах
Хром.
Ионы хрома являются непременными компонентами природных
водоемов. В зависимости от условий среды (pH, окислительно-восстановительный
потенциал, наличие лигандов) они существуют в разных степенях окисления и
входят в состав разнообразных неорганических и металлорганических соединений, которые
могут быть истинно растворенными, коллоидно-дисперсными или входить в состав
минеральных и органических взвесей. Истинно растворенная формы металла, в свою
очередь, весьма разнообразны, что связано с процессами гидролиза,
гидролитической полимеризации (образованием полиядерных гидроксокомплексов) и
комплексообразования с различными лигандами. Соответственно, как каталитические
свойства металлов, так и доступность для водных микроорганизмов зависят от форм
существования их в водной экосистеме.
Переход хрома в водной среде в металлокомплексную форму имеет
три следствия: может происходить увеличение суммарной концентрации ионов
металла за счет перехода его в раствор из донных отложений; мембранная
проницаемость комплексных ионов может существенно отличаться от проницаемости
гидратированных ионов; токсичность металла в результате комплексообразования
может сильно измениться.
В поверхностных водах соединения хрома находятся в
растворенном и взвешенном состояниях, соотношение между которыми зависит от
состава вод, температуры, рН раствора. Взвешенные соединения хрома представляют
собой в основном сорбированные соединения хрома. Сорбентами могут быть глины,
гидроксид железа, высокодисперсный оседающий карбонат кальция, остатки
растительных и животных организмов. В растворенной форме хром может находиться
в виде хроматов и бихроматов. При аэробных условиях Cr (VI) переходит в Cr
(III), соли которого в нейтральной и щелочной средах гидролизуются с выделением
гидроксида.
В речных незагрязненных и слабозагрязненных водах содержание
хрома колеблется от нескольких десятых долей микрограмма в литре до нескольких
микрограммов в литре, в загрязненных водоемах оно достигает нескольких десятков
и сотен микрограммов в литре [3]. Средняя концентрация в морских водах - 0.05 мкг/дм3
[12, 14, 19]. ПДК хром (III) в поверхностных водах составляет 0,005 мг/дм3,
а хром (VI) - 0,001 мг/дм3 [22,23].
Цинк.
Цинк попадает в природные воды в результате протекающих в
природе процессов разрушения и растворения горных пород и минералов (сфалерит,
цинкит, госларит, смитсонит, каламин), а также со сточными водами
рудообогатительных фабрик и гальванических цехов, производств пергаментной
бумаги, минеральных красок, вискозного волокна и др. В воде цинк существует
главным образом в ионной форме или в форме его минеральных и органических
комплексов, иногда встречается в нерастворимых формах: в виде гидроксида,
карбоната, сульфида и др.
В речных водах концентрация цинка обычно колеблется от 3 до
120 мкг/дм3, в морских - от 1,5 до 10 мкг/дм3. Содержание
в рудных и особенно в шахтных водах с низкими значениями рН может быть
значительным.
Цинк относится к числу активных микроэлементов, влияющих на
рост и нормальное развитие организмов. В то же время многие соединения цинка
токсичны, прежде всего его сульфат и хлорид [3].
ПДК цинка в поверхностных водах составляет 0,5 мг/дм3
[22,23].
Никель.
Присутствие никеля в природных водах обусловлено составом
пород, через которые проходит вода: он обнаруживается в местах месторождений
сульфидных медно-никелевых руд и железоникелевых руд. В воду попадает из почв и
из растительных и животных организмов при их распаде. Повышенное по сравнению с
другими типами водорослей содержание никеля обнаружено в сине-зеленых
водорослях. Соединения никеля в водные объекты поступают также со сточными
водами цехов никелирования, заводов синтетического каучука, никелевых
обогатительных фабрик. Значительные выбросы никеля сопровождают сжигание
ископаемого топлива.
Концентрация его может понижаться в результате выпадения в
осадок таких соединений, как цианиды, сульфиды, карбонаты или гидроксиды (при
повышении рН), за счет потребления его водными организмами и процессов
адсорбции [3].
В поверхностных водах соединения никеля находятся в
растворенном, взвешенном и коллоидном состояниях, количественное соотношение
между которыми зависит от состава воды, температуры и значений рН. Сорбентами
соединений никеля могут быть гидроксид железа, органические вещества,
высокодисперсный карбонат кальция, глины. Растворенные формы соединений никеля
представляют собой главным образом комплексные ионы, наиболее часто с
аминокислотами, гуминовыми и фульвокислотами, а также в виде прочного
цианидного комплекса. Наиболее распространены в природных водах соединения
никеля, в которых он находится в степени окисления Ni2+. Соединения Ni3+
образуются обычно в щелочной среде.
Соединения никеля играют важную роль в кроветворных
процессах, являясь катализаторами. Повышенное его содержание оказывает
специфическое действие на сердечно-сосудистую систему. Никель принадлежит к
числу канцерогенных элементов. Он способен вызывать респираторные заболевания.
Считается, что свободные ионы никеля (Ni2+) примерно в 2 раза более
токсичны, чем его комплексные соединения.
ПДК никеля в поверхностных водах составляет 0,01 мг/дм3
[22,23].
1.1.1
Источники поступления тяжелых металлов в окружающую среду
Добыча и переработка не являются самым мощным источником
загрязнения среды металлами. Валовые выбросы от этих предприятий значительно
меньше выбросов от предприятий теплоэнергетики. Не металлургическое
производство, а именно процесс сжигания угля является главным источником
поступления в биосферу многих металлов. В угле и нефти присутствуют все
металлы. Значительно больше, чем в почве, токсичных химических элементов,
включая тяжелые металлы, в золе электростанций, промышленных и бытовых топок.
Выбросы в атмосферу при сжигании топлива имеют особое значение. Например,
количество ртути, кадмия, кобальта, мышьяка в них в 3-8 раз превышает
количество добываемых металлов. Известны данные о том, что только один
котлоагрегат современной ТЭЦ, работающий на угле, за год выбрасывает в
атмосферу в среднем 1-1,5 т паров ртути. Тяжелые металлы содержатся и в
минеральных удобрениях [3].
Наряду со сжиганием
минерального топлива важнейшим путем техногенного рассеяния металлов является
их выброс в атмосферу при высокотемпературных технологических процессах
(металлургия, обжиг цементного сырья и др.), а также транспортировка,
обогащение и сортировка руды [3].
Техногенное поступление тяжелых металлов в окружающую среду
происходит в виде газов и аэрозолей (возгона металлов и пылевидных частиц) и в
составе сточных вод [3].
Металлы сравнительно
быстро накапливаются в почве и крайне медленно из нее выводятся: период
полуудаления цинка - до 500 лет, кадмия - до 1100 лет, меди - до 1500 лет,
свинца - до нескольких тысяч лет [3].
Существенный источник
загрязнения почвы металлами - применение удобрений из шламов, полученных из
промышленных и канализационных очистных сооружений [3].
В выбросах
металлургических производств тяжелые металлы находятся, в основном, в нерастворимой форме. По
мере удаления от источника загрязнения наиболее крупные частицы оседают, доля
растворимых соединений металлов увеличивается, и устанавливаются соотношения
между растворимой и нерастворимыми формами. Аэрозольные загрязнения,
поступающие в атмосферу, удаляются из нее путем естественных процессов
самоочищения. Важную роль при этом играют атмосферные осадки. В итоге выбросы
промышленных предприятий в атмосферу, сбросы сточных вод создают предпосылки для
поступления тяжелых
металлов в почву, подземные воды и открытые водоемы, в растения, донные
отложения и животных [3].
Одним из основных
процессов, определяющих удаление катионов тяжелых металлов из раствора и
распределение их между твёрдой и жидкой фазами почв, является адсорбция -
поглощение тяжелых
металлов активной поверхностью компонентов, составляющих почву [19].
Дальность распространения
и уровни загрязнения атмосферы зависят от мощности источника, условий выбросов
и метеорологической обстановки. Однако в условиях промышленно-городских
агломераций и городской застройки параметры распространения металлов в воздухе
еще плохо прогнозируются. С удалением от источников загрязнения уменьшение
концентраций аэрозолей металлов в атмосферном воздухе чаще происходит по
экспоненте, вследствие чего зона их интенсивного воздействия, в которой имеет
место превышение ПДК, сравнительно невелика [3].
В условиях
урбанизированных зон суммарный эффект от регистрируемого загрязнения воздуха
является результирующей сложения множества полей рассеяния и обусловлен
удалением от источников выбросов, градостроительной структурой и наличием
необходимых санитарно-защитных зон вокруг предприятий. Естественное (фоновое)
содержание тяжелых
металлов в незагрязненной атмосфере составляет тысячные и десятитысячные
доли микрограмма на кубический метр и ниже. Такие уровни в современных условиях
на сколько-нибудь обжитых территориях практически не наблюдается. К основным
отраслям, с которыми связано загрязнение окружающей среды ртутью, относят
горнодобывающую, металлургическую, химическую, приборостроительную,
электровакуумную и фармацевтическую. Наиболее интенсивные источники загрязнения
окружающей среды кадмием - металлургия и гальванопокрытия, а также сжигание
твердого и жидкого топлива. [3].
Атмосферный путь
поступления химических элементов в окружающую среду городов является ведущим.
Однако уже на небольшом удалении, в частности, в зонах пригородного сельского
хозяйства, относительная роль источников загрязнения окружающей среды тяжелыми металлами может измениться
и наибольшую опасность будут представлять сточные воды и отходы, накапливаемые
на свалках и применяемые в качестве удобрений [3].
Максимальной способностью концентрировать тяжелые металлы обладают
взвешенные вещества и донные отложения, затем планктон, бентос и рыбы [3].
На протяжении ряда лет в Институте природопользования НАН
Беларуси осуществляется подготовка национальных данных о выбросах, которые
требуются для выполнения обязательств по Конвенции о трансграничном загрязнении
воздуха на большие расстояния. Приоритетной задачей является подготовка данных
о выбросах тяжелых металлов, учитываемых государственной статистической
отчетностью весьма неполно [17].
Результаты оценки выбросов ТМ по основным категориям
источников приведены в таблице 1:
Таблица 1 - Выбросы тяжелые металлы в атмосферу на территории
Беларуси в 2008 г., т. [17]
|
Категория
источника
|
As
|
Cd
|
Cr
|
Cu
|
Hg
|
Ni
|
Pb
|
Zn
|
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
|
Энергетика
общего пользования и производства тепла
|
0,07
|
0, 19
|
0,03
|
0,12
|
0,05
|
22,95
|
2,4
|
10,52
|
|
Сжигание
топлива в обрабатывающей промышленности и строительстве
|
0,68
|
1,54
|
1,35
|
1,74
|
0,74
|
34,46
|
16,63
|
|
Сжигание
топлива в жилом секторе
|
0,05
|
0,04
|
0,18
|
0,41
|
0,00
|
0,13
|
0,34
|
3,81
|
|
Прочее
стационарное сжигание топлива
|
0,03
|
0,01
|
0,06
|
0,11
|
0,00
|
1,75
|
3,50
|
0,35
|
|
Мобильные
источники
|
0,00
|
0,04
|
0,18
|
1,05
|
0,00
|
1,75
|
3,50
|
0,35
|
|
Химическая
промышленность
|
0,24
|
0,03
|
0,68
|
0,17
|
0,00
|
0,23
|
0,04
|
24,43
|
|
Производство
металлов
|
0,27
|
0,88
|
7,80
|
10,5
|
0,02
|
1,26
|
21,90
|
306,9
|
|
Сжигание
отходов
|
0,00
|
0,03
|
0,01
|
0,04
|
0,00
|
0,00
|
0,31
|
0,48
|
|
Прочие
|
0,00
|
0,00
|
0,11
|
0,09
|
0,00
|
0,09
|
0,02
|
0,01
|
|
Всего
|
1,34
|
2,75
|
10,4
|
14,2
|
46,51
|
63,09
|
364,3
|
1.2 Теория и
сущность биоиндикации
Все биологические системы - будь то организмы, популяции или
биоценозы - в ходе своего развития приспособились к комплексу факторов
местообитания. Они завладели внутри биосферы определенной областью,
экологической нишей, в которой находят подходящие условия существования и могут
нормально питаться и размножаться. Каждый организм обладает в отношении любого
действующего на него фактора генетически детерминированным, филогенетически
приобретенным, уникальным физиологическим диапазоном толерантности, в пределах
которого этот фактор является для него переносимым [1].
Физиологическая толерантность и экологическая потенция
организма определяют его индикаторную ценность. В результате каждая
биологическая система (организм, популяция, биоценоз) характеризует зависящее
от времени воздействие на нее факторов среды - природных, измененных человеком
или антропогенных. Метод оценки абиотических и биотических факторов
местообитания при помощи биологических систем называют биоиндикацией [1].
В соответствии с этим организмы или сообщества организмов,
жизненные функции которых так тесно коррелируют с определенными факторами
среды, что могут применяться для их оценки, называются биоиндикаторами [1].
Слово биоиндикация образовано от греческого bios - жизнь и
латинского indicare - указывать. Под биологическими объектами понимаются любые
биологические системы на различных уровнях организации живой материи (молекулы
органических веществ, клетки, ткани, органы, организмы, популяции, виды,
группировки, сообщества организмов), с включением при необходимости костных
компонентов (биогеоценозы, почвы, ландшафты). При этом в целях биоиндикации используются
генетические, биохимические и физиологические нарушения хромосом, биомембран,
органелл, обмена веществ (белков и аминокислот, углеводов, включая фотосинтез;
липидов, минерального и энергетического обменов); активности ферментов и
гормонов; морфологические, анатомические, биоритмические и поведенческие
отклонения; флористические, фаунистические, популяционно-динамические,
биогеоценотические и, наконец, ландшафтные изменения [18].
Универсальным показателем изменения гомеостаза тест-организма
является состояние стресса при попадании из "чистой" среды в
"загрязненную" [2].
В биологии под стрессом понимается реакция биологической
системы на экстремальные факторы среды (стрессоры), которые могут в зависимости
от силы, интенсивности, момента и продолжительности воздействия более или менее
сильно влиять на систему [2].
Опасность антропогенных стрессоров состоит в том, что
биологические системы - будь то организмы, популяции или биоценозы -
недостаточно адаптированы к ним. Антропогенные стрессоры создаются с такой
скоростью, что в живых системах часто не успевают активизироваться
соответствующие адаптационные процессы [2].
Стрессовое воздействие среды приводит к отклонению основных
параметров организма от оптимального уровня [2].
Для выяснения тесноты связи биоиндикаторов с отдельными
объектами индикации (индикатами) используют такие показатели, как
достоверность, распространённость и значимость индикатора. Достоверность (Д) и
распространённость (Р) индикатора представляет собой выраженные в долях от
единицы или в процентах отношения числа случаев нахождения индикатора на
объекте индикации (Т) к общему числу встреч индикатора (R) и индиката (S):
Д = Т / R;
Р = Т / S.
Значимость индикатора (Z) устанавливают путём сопоставления
показателей его достоверности и распространённости. Количественно она может
быть оценена в долях от единицы путём произведения достоверности на
распространённость в том же измерении и при необходимости выражена в процентах:
Z = Д·Р, или= T2/ (R·S) [18].
Абсолютные индикаторы встречаются почти исключительно
совместно с объектом индикации, их достоверность и распространённость превышают
90-95%, а значимость - 0,8. У хороших индикаторов эти показатели составляют
соответственно 80-95%, 75-90% и 0,6-0,8; у удовлетворительных - 60-80%, 50-75%
и 0,3-0,6%; у сомнительных - 50-60%, 20-50% и 0,1-0,3. В ряде случаев
целесообразно обращать внимание и на отрицательные индикаторы, распространённые
на объектах фона и не встречающиеся или очень редко встречающиеся на объектах
индикации [18].
Понятие индикации в большинстве случаев относительное. Так,
ботанические индикаторы, как правило, проявляют свои свойства в пределах
определённых природно-территориальных комплексов. По степени устойчивости связи
с индикатом они делятся на панареальные (сохраняют связь с индикатом на всей
территории ареала), зональные (имеют индикационное значение в пределах
географических зон и подзон), региональные (сохраняют своё значение в пределах
одной или нескольких областей со сходными физико-географическими условиями),
локальные (обнаруживают связь с индикатом в одном физико-географическом районе)
[18].
По характеру связи с индикатом индикаторы делятся на прямые -
имеющие непосредственную связь с индикатами, и косвенные - связанные с
индикатом через промежуточное звено. Хорошо и непосредственно видимые
индикаторы получили название экзоиндикаторов, а замаскированные и скрытые -
эндоиндикаторов [18].
Индикационные признаки индикаторов выявляют методами
пассивного и активного мониторинга. При пассивном мониторинге в популяциях, группировках,
сообществах свободно живущих организмов (вирусов, бактерий, грибов, лишайников,
растений, животных) исследуют их состав, количественные показатели, структуру,
видимые или незаметные отклонения от нормы, повреждения, обнаруживающие
положительные корреляционные связи с вполне определёнными индикатами и
являющиеся следствием их прямого или косвенного влияния. Широкое
распространение получили картографический и дистанционный методы с
использованием аэрофото - и космических снимков, перспективны биохимические и
генетические методы биоиндикационных исследований. К пассивному мониторингу
относятся также и экспериментальные вегетационные опыты, где оценивают ответные
реакции культивируемых организмов на действие различных по интенсивности
природных и антропогенных факторов. При активном мониторинге пытаются
обнаружить антропогенные стрессовые воздействия на тест-организмы или
тест-объекты, находящиеся в стандартизированных условиях. При этом
рекомендуется подвергать действию изучаемых факторов одновременно несколько
видов растений или других организмов (видовой подход), различающихся по
устойчивости к стрессорам, устанавливать особенности воздействия стрессоров в
зависимости от их дозы. В качестве биотестов используются бактерии (особенно
кишечная палочка), водоросли (в частности, хлорелла), низшие грибы, инфузории,
низшие ракообразные, беззубки, личинки хирономид, рыб, земноводных, семена
редиса, табака [18].
Круг объектов индикации в последние годы расширяется. К ним
относится индикация климата, геологического строения, горных пород,
тектельности, связанные с восходящим движением грунтовых вод по разрывам
[18].
Наибольшую ценность представляют биоиндикаторы,
присутствующие на объекте индикации в большом количестве и с высокой
достоверностью, отличающиеся однородными свойствами, не требующие больших
затрат для их выявления и получения достаточно точных и воспроизводимых
результатов, имеющие диапазоны погрешности по сравнению с другими методами не
более 20% [18].
Многолетний опыт ученых разных стран по контролю состояния
окружающей среды показал преимущества, которыми обладают живые индикаторы:
·в условиях хронических антропогенных нагрузок
могут реагировать даже на относительно слабые воздействия вследствие
кумулятивного эффекта; реакции проявляются при накоплении некоторых критических
значений суммарных дозовых нагрузок;
·суммируют влияние всех без исключения
биологически важных воздействий и отражают состояние окружающей среды в целом,
включая ее загрязнение и другие антропогенные изменения;
·исключают необходимость регистрации химических и
физических параметров, характеризующих состояние окружающей среды;
·фиксируют скорость происходящих изменений;
·вскрывают тенденции развития природной среды;
·указывают пути и места скоплений в экологических
системах различного рода загрязнений и ядов, возможные пути их попадания в пищу
человека;
·позволяют судить о степени вредности любых
синтезируемых человеком веществ для живой природы и для него самого, причем
дают возможность контролировать их действие [2].
Выделяют две формы отклика живых организмов, используемых в
целях биоиндикации, - специфическую и неспецифическую. В
первом случае происходящие изменения связаны с действием одного какого-либо
фактора. При неспецифической биоиндикации различные антропогенные факторы
вызывают одинаковые реакции [2].
В зависимости от типа ответной реакции биоиндикаторы
подразделяют на чувствительные и кумулятивные. Чувствительные
биоиндикаторы реагируют на стресс значительным отклонением от жизненных норм, а
кумулятивные накапливают антропогенное воздействие, значительно превышающее
нормальный уровень в природе, без видимых изменений [2].
В качестве биоиндикаторов могут быть использованы
представители всех "царств" живой природы. Для биоиндикации не
пригодны организмы, поврежденные болезнями, вредителями и паразитами. Идеальный
биологический индикатор должен удовлетворять ряду требований:
·быть типичным для данных условий;
·иметь высокую численность в исследуемом экотопе;
·обитать в данном месте в течение ряда лет, что
дает возможность проследить динамику загрязнения;
находиться в условиях, удобных для отбора проб;
·давать возможность проводить прямые анализы без
предварительного концентрирования проб;
·характеризоваться положительной корреляцией между
концентрацией загрязняющих веществ в организме-индикаторе и объекте
исследования;
·использоваться в естественных условиях его
существования;
·иметь короткий период онтогенеза, чтобы была
возможность отслеживания влияния фактора на последующие поколения [2].
Ответная реакция биоиндикатора на определенное физическое или
химическое воздействие должна быть четко выражена, т.е. специфична, легко
регистрироваться визуально или с помощью приборов [2].
При выборе индикатора необходимо принимать во внимание
соображения экономии и учитывать характер использования тех или иных
организмов. Например, широко распространенные на исследуемой территории и не
занесенные в "Красную книгу" [2].
На уровне популяции биоиндикация проводится в том случае,
если процесс распространения негативных изменений охватывает такое количество
особей, при котором заметно сокращается численность популяции, изменяется ее
половозрастная структура, сокращается продолжительность жизни, происходит сдвиг
фенологических фаз и др. [2].
Экосистемный подход к оценке среды дает возможность ранней
диагностики ее изменений. Сигналом тревоги служит разбалансировка
продукционно-деструкционных процессов. Диагностическими признаками таких
сдвигов являются, например, накопление органического вещества, заиление, зарастание
водоемов, усиленное развитие микроорганизмов [2].
В качестве объектов для биоиндикации применяются
разнообразные организмы - бактерии, водоросли, высшие растения, беспозвоночные
животные, млекопитающие. Для гарантированного выявления присутствия в природных
средах токсического агента неизвестного химического состава, как правило,
используется набор объектов, представляющих различные группы сообщества. С
введением каждого дополнительного объекта эффективность схемы испытаний
повышается, однако нет смысла бесконечно расширять ассортимент обязательных
объектов для использования в такой оценке [2].
Для биоиндикации необходимо выбирать наиболее чувствительные
сообщества, характеризующиеся максимальными скоростью отклика и выраженностью
параметров. Например, в водных экосистемах наиболее чувствительными являются
планктонные сообщества, которые быстро реагируют на изменение среды благодаря
короткому жизненному циклу и высокой скорости воспроизводства. Бентосные
сообщества, где организмы имеют достаточно длинный жизненный цикл, более
консервативны: перестройки происходят в них при длительном хроническом
загрязнении, приводящем к необратимости процессов [2].
В настоящее время оценка степени экологической опасности
традиционно осуществляется путем определения в окружающей среде отдельных
потенциально вредных веществ или воздействий и сравнения полученных результатов
с законодательно установленными для них предельно допустимыми величинами. В то
же время такой способ контроля имеет ряд существенных недостатков.
Аналитические методы, как правило, трудоемки, не всегда экспрессны, требуют
дорогостоящего, иногда дефицитного оборудования и реактивов, а также
высококвалифицированного обслуживающего персонала. Но главный их недостаток в
том, что эти методы не могут гарантировать достоверной оценки экологической
опасности, сколь бы широким не был спектр анализируемых веществ. Ведь важны не
сами уровни загрязнений и воздействий, а те биологические эффекты, которые они
могут вызвать и о которых не может дать информацию даже самый точный химический
или физический анализ [2].
1.2.1 Методы
биоиндикации
Методы биоиндикации основаны на наблюдениях отдельных
организмов, популяции или сообществ организмов в естественной среде обитания с
целью определения по их реакциям (изменениям) качества окружающей среды. В
сельском хозяйстве широко применяется метод биоиндикации для диагностики
питания сельскохозяйственных культур. Данный метод визуальной биоиндикации
основан на изучении внешних признаков фито - и биоценозов, которые отражают
качественные изменения среды обитания [21].
В качестве признаков визуальной биоиндикации используется
внешний вид растений. Таких признаков, связанных с нарушением питания растений,
множество, в частности: замедление роста стеблей; ветвей и корней; пожелтение;
бурение; загибание листьев; "краевые ожоги"; образование гнили;
одревеснение стеблей и др. [21].
Для целей биоиндикации качества окружающей среды могут
применяться популяционные и экосистемные критерии, которые характеризуются
показателями: численности и биомассы отдельных видов; соотношением в
сообществах различных видов, их распределение по обилию и т.п. [21].
Для получения более достоверных, долгосрочных прогнозов
наряду с видами-индикаторами отслеживаются изменения, происходящие в популяциях
устойчивых видов, способных выдерживать значительные возмущающие воздействия
(воздействия экологически неблагоприятных факторов) в течение длительного
времени [21].
Под влиянием загрязняющих веществ в организме происходят
перестройка структуры и функции клеток. Результаты гистологических исследований
таких изменений могут свидетельствовать о качестве окружающей среды.
Злокачественный рост клеток, дегенеративные изменения или появление
некротических очагов характеризуют высокую степень токсичности среды обитания [21].
Патолого-анатомические и гистологические методы биоиндикации
особое внимание уделяют изучению репродуктивной системы, любые изменения
которой непосредственно связаны с жизненно важными параметрами популяции.
Репродуктивная система очень чувствительна к стрессовым воздействиям, и любое
нарушение можно рассматривать как сигнал о наличии неблагоприятных изменений в
окружающей среде [21].
Эмбриональные методы диагностики базируются на том
обстоятельстве, что наиболее уязвимыми к воздействию внешних возмущений
являются ранние стадии развития многоклеточных организмов. На стадиях дробления
и формирования зародышевых органов и тканей даже незначительные воздействия,
как правило, приводят к видимым уродствам более поздних стадий или даже гибели
зародышей. В качестве биоиндикаторов обычно используются быстро развивающиеся и
дающие многочисленное потомство организмы (рыбы, моллюски, земноводные,
насекомые). Данные организмы могут быть использованы и как тест-объекты для
биотестирования окружающей среды [21].
Более тонкими и точными методами биодиагностики являются
иммунологические и генетические методы [21].
Иммунологические - основаны на измерениях показателей
иммунной системы под воздействием внешних возмущающих факторов. В результате любого
рода отрицательного воздействия на иммунную систему живых организмов в первую
очередь изменяется функциональное состояние иммунокомпетентных клеток -
спленоцитов и лимфоцитов. При введении в клетки организма специальных веществ -
стандартных мутагенов (липополисахаридов и др.) - в зависимости от вида
воздействия ингибирование реакции может свидетельствовать о нарушении
иммунологического статуса организма [21].
Генетические методы позволяют анализировать генетические
изменения, возникающие вследствие неблагоприятных внешних воздействий.
Появление таких изменений характеризует мутагенную активность среды, а
возможность их сохранения в клеточных популяциях отражает эффективность
иммунной потенции организма [21].
В нормальных условиях большая часть генетических аномалий
удаляется из популяций посредством иммунной системы организма. Наличие таких
аномалий можно использовать в качестве индикатора стресса, ведущего к продукции
аномальных клеток и снижению способности иммунной системы организма их уничтожать
[21].
Такое разнообразие методов биоиндикации говорит об их
несовершенстве. Действительно, биоиндикация предусматривает контроль уже
состоявшегося или происходящего загрязнения компонентов окружающей среды по
функциональным характеристикам их обитателей и экологическим характеристикам
организмов [21].
Разработка единой системы показателей токсичного загрязнения
окружающей среды на сегодняшний день встречает серьезные трудности. Постепенные
изменения видового состава формируются в результате длительного отравления и
становятся явными в случае далеко зашедших изменений. Таким образом, видовой
состав не даёт оценки на момент исследования. В этом плане методы биоиндикации
загрязнения окружающей среды инерционны. В холодное время года системы
биологической индикации малоэффективны [21].
Однако отличительная простота методов оценки экологической
обстановки методами биоиндикации, отсутствие потребности в специальном
инструментальном обеспечении являются их бесспорным достоинством [21].
Умение объединить в комплексную форму биоиндикацию,
биотестирование и химико-аналитические методы диагностики экологической
обстановки позволяет минимизировать затраты на исследования. Именно комплексное
использование методов обеспечивает перспективу биоиндикации [21].
1.2.2
Особенности использования растений, животных и микроорганизмов в качестве
биоиндикаторов
С помощью растений можно проводить биоиндикацию всех
природных сред. Индикаторные растения используются при оценке механического и
кислотного состава почв, их плодородия, увлажнения и засоления, степени
минерализации грунтовых вод и степени загрязнения атмосферного воздуха
газообразными соединениями, а также при выявлении трофических свойств водоемов
и степени их загрязнения поллютантами. Например, на содержание в почве свинца
указывают виды овсяницы, полевицы; цинка - виды фиалки, ярутки; меди и кобальта
- смолевки, многие злаки и мхи [2].
Чувствительные фитоиндикаторы указывают на присутствие
загрязняющего вещества в воздухе или почве ранними морфологическими реакциями -
изменением окраски листьев (появление хлорозов; желтая, бурая или бронзовая
окраска), различной формы некрозами, преждевременным увяданием и опаданием
листвы. У многолетних растений загрязняющие вещества вызывают изменение
размеров, формы, количества органов, направления роста побегов или изменение
плодовитости. Подобные реакции обычно неспецифичны [2].
Некоторые естественные факторы могут вызывать симптомы,
сходные с антропогенными нарушениями. Так, например, хлороз листьев может быть
вызван недостатком железа в почве или ранним заморозком. Поэтому при
определении морфологических изменений у растений необходимо учитывать
возможность действия других повреждающих факторов [2].
Индикаторы другого типа представляют собой
растения-аккумуляторы. Они накапливают в своих тканях загрязняющее вещество или
вредные продукты метаболизма, образуемые под действием загрязняющих веществ,
без видимых изменений. При превышении порога токсичности ядовитого вещества для
данного вида проявляются различные ответные реакции, выражающиеся в изменении
скорости роста и длительности фенологических фаз, биометрических показателей и,
в конечном счете, снижении продуктивности [2].
Получить точные количественные данные о динамике и величине
стрессовых воздействий на основе морфологических изменений невозможно, но можно
довольно точно определить величину потерь продукции и, имея график зависимости
"доза - эффект", рассчитать величину стрессового воздействия [2].
Биомониторинг может осуществляться путем наблюдений за
отдельными растениями-индикаторами, популяцией определенного вида и состоянием
фитоценоза в целом. На уровне вида обычно производят специфическую индикацию
какого-то одного загрязнителя, а на уровне популяции или фитоценоза - общего
состояния природной среды [2].
·являясь консументами, они находятся на разных
трофических уровнях экосистем и аккумулируют через пищевые цепи загрязняющие
вещества;
·обладают активным обменом веществ, что
способствует быстрому проявлению воздействия негативных факторов среды на
организм;
·имеют хорошо дифференцированные ткани и органы,
которые обладают разной способностью к накоплению токсических веществ и
неоднозначностью физиологического отклика, что позволяет исследователю иметь
широкий набор тестов на уровне тканей, органов и функций;
·сложные приспособления животных к условиям среды
и четкие поведенческие реакции наиболее чувствительны к антропогенным
изменениям, что дает возможность непосредственно наблюдать и анализировать
быстрые отклики на оказываемое воздействие;
·животных с коротким циклом развития и
многочисленным потомством можно использовать для проведения ряда длительных
наблюдений и прослеживать воздействие фактора на последующие поколения; для
долгоживущих животных можно выбрать особо чувствительные тесты в соответствии с
особо уязвимыми этапами онтогенеза [2].
Основное преимущество использования позвоночных животных в
качестве биоиндикаторов заключается в их физиологической близости к человеку.
Основные недостатки связаны со сложностью их обнаружения в природе, поимки,
определения вида, а также с длительностью морфо-анатомических наблюдений. Кроме
того, эксперименты с животными зачастую дороги, требуют многократной
повторяемости для получения статистически достоверных выводов [2].
Оценка и прогнозирование состояния природной среды с
привлечением позвоночных животных проводятся на всех уровнях их организации. На
организменном уровне с помощью сравнительного анализа оцениваются
морфо-анатомические, поведенческие и физиолого-биохимические показатели [2].
Морфо-анатомические показатели описывают особенности внешнего
и внутреннего строений животных и их изменение под воздействием определенных
факторов (депигментация, изменение покровов, структуры тканей и расположения
органов, возникновение уродств, опухолей и других патологических проявлений)
[2].
Поведенческие и физиолого-биохимические параметры особенно
чувствительны к изменению внешней среды. Токсиканты, проникая в кости или кровь
позвоночных животных, сразу же воздействуют на функции, обеспечивающие
жизнедеятельность. Даже при узкоспецифичном влиянии токсиканта на определенную
функцию ее сдвиги отражаются на состоянии всего организма вследствие взаимосвязанности
процессов жизнедеятельности. Достаточно отчетливо присутствие токсикантов
проявляется в нарушении ритма дыхания, сердечных сокращений, скорости
пищеварения, ритмике выделений, продолжительности циклов размножения [2].
Для того чтобы иметь возможность сравнивать материал,
собранный разными исследователями в различных районах, набор видов-индикаторов
должен быть един и невелик. Вот некоторые критерии пригодности различных видов
млекопитающих для биоиндикационных исследований:
принадлежность к разным звеньям трофической цепи -
растительноядным, насекомоядным, хищным млекопитающим;
оседлость или отсутствие больших миграций;
широкий ареал распространения (сравнительно высокая
эвритопность), т.е. этот критерий исключает использование в качестве тест-индикаторов
эндемиков;
принадлежность к естественным сообществам: критерий исключает
синантропные виды, питающиеся вблизи жилиша человека и неадекватно
характеризующие микроэлементный состав загрязнения данного региона;
численность вида должна обеспечивать достаточный материал для
анализа;
простота и доступность методов добывания видов [2].
Анализируя по данным критериям представителей всех отрядов
млекопитающих, встречающихся на территории стран СНГ, можно остановиться на
семи видах: обыкновенная бурозубка, европейский крот, алтайский крот, бурый
медведь, лось, рыжая полевка, красная полевка [2].
Микроорганизмы - наиболее быстро реагирующие на изменение
окружающей среды биоиндикаторы. Их развитие и активность находятся в прямой
связи с составом органических и неорганических веществ в среде, так как
микроорганизмы способны разрушать соединения естественного и антропогенного
происхождений. На этом основаны принципы биоиндикации с использованием
микроорганизмов. Необходимо иметь сведения о составе, количестве и
функциональной активности последних [2].
При прямом микроскопировании, например воды, количество
обнаруживаемых микроорганизмов оказывается небольшим, поэтому для изучения
морфологического разнообразия и оценок их общего числа в единице объема
проводят концентрирование пробы [2].
Для определения биомассы бактерий необходимо определить
размер клеток с помощью микрометра [2].
Чаще всего для оценки качества вод используют показатель
микробного числа (ОМЧ) - это число клеток аэробных сапрофитных организмов в 1
мл воды. В водопроводной воде согласно ГОСТ микробное число не должно превышать
50 КОЕ (число колониеобразующих единиц) в 1см3. В чистых водоемах
число сапрофитов может исчисляться десятками и сотнями, а в загрязненных и
грязных водоемах этот показатель достигает сотен тысяч и миллионов [26].
1.3
Биологические объекты как индикаторы загрязнения окружающей среды тяжелыми
металлами
В качестве биоиндикаторов используют живые организмы,
обладающие хорошо выраженной реакцией на воздействие тяжелых металлов [16].
В живых организмах тяжелые металлы в избыточном количестве
вызывают нарушения биохимических процессов обмена веществ, подавляя или
активируя деятельность многих ферментов. Тяжелые металлы представляют
наибольшую угрозу для первых стадий развития сельскохозяйственных растений
(проростков, всходов). Под их действием ухудшается рост корней побегов,
происходит некроз листьев. Не рекомендуется выращивать сельскохозяйственные
культуры на расстоянии менее 5-7 км от источников выбросов тяжелых металлов как
в открытом, так и в закрытом грунте. Тяжелые металлы, поступающие на
поверхность почвы, накапливаются в почвенной толще, особенно в верхних
гумусовых горизонтах, и медленно удаляются при выщелачивании, потреблении
растениями, эрозии и дефляции. Первый период полуудаления (удаление половины от
начальной концентрации) тяжелых металлов значительно варьирует для различных
элементов и составляет для цинка - 70-310, меди - 310-1500, кадмия - 13-110,
свинца - 740-5900 лет. Среди ТМ в 13 (Be, Al, Cr, As, Se, Ag, Cd, Sn, Sb, Ba,
Hg, Te, Pb) токсичны во всех своих водно-, щелоче-, кислорастворимых
соединениях. Среди них группу неорганических экотоксинов возглавляет кадмий,
свинец и ртуть [18].
Концентрация тяжелых металлов в растениях в значительной мере
зависит от их содержания в почве, а в теле животных - от их количества в пище.
Имеют значение также видовые особенности растений и животных. Животные
поглощают только подвижные формы элементов, поэтому концентрация загрязнителя в
животных будет отражать фактическую загрязненность экосистемы, а не
потенциальную, которую получают при определении концентрации загрязнителя в
почве или растениях [18].
Хорошим индикатором загрязнений окружающей среды тяжелыми
металлами является их содержание в организме позвоночных животных, особенно
млекопитающих, а также почвенных беспозвоночных. При выборе видов позвоночных в
качестве биоиндикаторов необходимо руководствоваться следующими критериями:
1. Выбранные виды должны принадлежать к разным звеньям трофодинамической
цепи. Степень концентрации тяжелых металлов и многих других токсикантов
постепенно увеличивается от биокостной среды (почвы) к автотрофам (зеленым
растениям) и далее к гетеротрофам, достигая максимума в организмах крупных
хищников. Следовательно, для биоиндикации необходимо отобрать представителей
растительноядных (зерноядных), насекомоядных, хищных позвоночных.
2. У избранных видов должны отсутствовать большие миграции,
так как накопление токсичных веществ в организме прямо пропорционально уровню
загрязнения окружающей среды.
3. Для сравнимости данных по различным районам лучше брать
для анализа особи одних и тех же видов с широкими ареалами.
4. Виды должны обладать сравнительно высокой
эврипотентностью, т.е. встречаться в различных местообитаниях.
5. Желательно использовать виды, живущие в естественных
сообществах и не связанные с человеком.
6. Виды должны быть многочисленными, легко добываемыми [18].
В водоемах этим требованиям удовлетворяет следующая цепь:
вода, донный грунт - водные растения - водные беспозвоночные - плотва - судак.
Судак - повсеместно одна из самых загрязненных рыб. Лучшим индикатором из
земноводных является зеленая жаба, из пресмыкающихся - прыткая ящерица, т.к.
они питаются наземными беспозвоночными. Птицы - наиболее подвижные позвоночные,
многие из них улетают на зимовку. В связи с этим они мало пригодны для целей
мониторинга загрязнения среды обитания. Более перспективны в этом отношении
оседлые виды [18].
Среди млекопитающихся в Европейской части России названным
критериям больше всего удовлетворяют: обыкновенная бурозубка, европейский крот,
рыжая и красная полевки. Тяжелые металлы у них больше всего накапливаются в
легких, печени, почках, костях, шкуре [18].
Для целей биоиндикации большой интерес представляет почвенная
фауна, составляющая 90-99% биомассы и 95% всех видов животных, входящих в
наземный биоценоз. Повсеместно наиболее чувствительной группой к воздействию
загрязнений оказались дождевые черви. Они достаточно точно отражают
концентрацию металлов в почве и накапливают металлы в 3-5 раз больше, чем их
содержится в почве. Дождевые черви в значительной степени концентрируют магний,
железо, медь, свинец, марганец, цинк. Обычно в лесостепи двупарноногие
многоножки, в частности кивсяки, также являются сапрофагами и отличаются
повышенными концентрациями в тканях магния, марганца, меди, цинка, свинца [18].
Одним из распространенных методов биоиндикации загрязнения
окружающей среды тяжелыми металлами и другими токсикантами является выбор
участков для исследований на различных расстояниях от источника загрязнений в
зависимости от его мощности и путей распространения загрязнителей. При этом
учитывается направление преобладающих ветров, течения водных потоков и т.д. Для
сравнительно мощных промышленных предприятий такие участки выбираются на
расстоянии 0-0,5, 0,5-1,0, 1,0-5,0, 5-10, 10-20, 20-50 км от источника
загрязнений. Для контроля исследования проводят на незагрязненной территории со
сходными экологическими условиями [18].
Учеты мелких млекопитающих и почвенной менофауны проводят на
следующих расстояниях от автомагистралей 5-7, 20-25, 70-250, 700-1500 м.
Придорожные (5-7 м) участки по сравнению с контрольными характеризуются более
высокой численностью и большим разнообразием видов мелких млекопитающих. При
этом в их микропопуляциях происходит увеличение доли самцов при снижении массы
и размеров тела животных, что является результатом повышенных концентраций
кадмия, цинка, никеля. Активно накапливают тяжелые металлы обыкновенная
бурозубка и рыжая полевка. Наиболее высокое содержание свинца, цинка, никеля
отмечается в костях; кадмия и меди - в печени обыкновенной бурозубки; свинца -
в печени, меди - в шкуре рыжей полевки [18].
У шоссе с интенсивным движением транспорта общая численность
почвенной фауны снижается в 5 раз, у шоссе со слабой интенсивностью движения -
в 1,5 раза. Наиболее сильно падает численность дождевых червей, пауков,
кивсяков, жужелиц, стафилинид. Вблизи автомобильных дорог возрастает
численность фитофагов и снижается обилие хищников и сапрофагов [18].
Для индикации среднего и высокого уровней загрязнения
тяжелыми металлами чаще используют микроорганизмы (бактерии, грибы, водоросли,
простейшие). В частности, при концентрации меди 300-400, а никеля 600-700 мг/кг
в почве начинает снижаться численность азотофиксирующих, нитрифицирующих,
аммонифицирующих бактерий. Затем уменьшается количество целлюлозоразрушающих
бактерий. При концентрации меди 400-1200, а никеля 600-700 мг/кг в почве
происходит смена доминатов, снижается количество неспорообразующих сапрофитных
бактерий [18].
Одной из перспективных групп организмов-индикаторов являются
протисты, в том числе и инфузории. Они играют значительную роль в пищевых
цепях. Как консументы II уровня инфузории являются важным звеном переноса
энергии на более высокие трофические уровни. Также инфузории играют важную роль
в процессах самоочищения водоемов. Высокая чувствительность инфузорий к
токсическому действию различных поллютантов позволяет обнаруживать загрязнения
на самых ранних стадиях и при незначительных концентрациях [4].
В последние годы возрос интерес к эпифитным лишайникам как
биоиндикаторам качества воздуха, поскольку эти растительные организмы получают
все необходимое для своей жизнедеятельности из воздуха [8].
Основные причины низкой устойчивости лишайников к
атмосферному загрязнению следующие: высокая чувствительность водорослевого
компонента лишайников, пигменты которого под действием загрязнителей быстро
разрушаются; отсутствие защитных покровов и связанное с этим беспрепятственное
поглощение газов слоевищами лишайников; повышенная требовательность к
кислотности субстрата, изменение которой сверх определенного предела приводит к
гибели лишайников; небольшие размеры их тела и значительная продолжительность
жизни. Аккумулируя загрязняющие вещества из атмосферы, лишайники гибнут при
хроническом воздействии даже их низких концентраций. Лишайники аккумулируют
также значительное количество тяжелых металлов. Их высокие дозы изменяют
мембранную проницаемость для катионов калия, влияют на скорость фотосинтеза,
свойства хлорофилла лишайников [18].
Содержание тяжелых металлов в лишайниках более адекватно
отражает распределение этих элементов в различных точках приземного слоя
атмосферы, чем содержание этих же элементов в сосудистых растениях. Эти
сравнения приведены в таблице 2 [8].
Таблица 2. Средняя концентрация тяжелых металлов
в растениях при фоновой концентрации металлов в воздухе (мкг/г сухой массы) [7]
|
Вид
растения
|
свинец
|
цинк
|
медь
|
железо
|
хром
|
никель
|
ртуть
|
кадмий
|
марганец
|
|
Сосудистые
растения
|
1,5
|
2
|
6,2
|
140
|
0,2
|
3
|
0,02
|
0,45
|
630
|
|
Лишайники
|
14
|
102
|
8,5
|
1000
|
1,84
|
4
|
0,85
|
240
|
Грибы как объекты биомониторинга хорошо зарекомендовали себя
в качестве индикаторов загрязнения окружающей среды.
Микромицеты. При загрязнении почв тяжелыми металлами у многих
микромицетов происходит усиление споруляции. Так, при содержании кадмия
100мг/кг почвы количество грибных спор возрастает в 2-5 раз. Напротив,
содержание мицелия почвенных микромицетов при высоком загрязнении тяжелыми
металлами может снижаться в 2-3 раза [18].
При промышленном и транспортном загрязнении тяжелыми
металлами комплекс почвенных микромицетов обедняется, снижается разнообразие
видов, упрощается структура, индекс разнообразия Шеннона уменьшается в 1,5-2
раза. Чем беднее почвы, тем более сильное влияние оказывают тяжелые металлы на
микромицеты. При небольших дозах загрязнения разнообразие видов может несколько
увеличиваться. При высоком загрязнении соединениями ртути и кадмия в
дерново-подзолистых почвах начинают преобладать виды аспергиллус черный и
земляной, не типичные для этих почв [18].
Наибольшая чувствительность к тяжелым металлам проявляется у
видов, имеющих узкие ареалы распространения. В оподзоленных почвах один из
самых чувствительных видов - мортнерелла римская, в черноземах - пенициллиум
шерстистый. Более устойчивы к загрязнению виды с широкими ареалами. В
черноземных почвах с высоким содержанием тяжелых металлов обильно представлены
грибы рода пенициллиум (шерстистый и красный). Они устойчивы также к внесению высоких
доз удобрений. Высокие концентрации кадмия выдерживает пациломицесс лилиевидный
[18].
Устойчивые к высоким загрязнениям тяжелых металлов виды рода
пенициллиум обладают фитотоксичным действием на прорастание семян. У
чувствительных видов тяжелые металлы тормозят развитие спорангиев, снижают
скорость спорообразования, прорастания спор, роста мицелия [18].
Макромицеты. Высшие шляпочные грибы - макромицеты из группы
гименомицетов класса базидиальных - как микоризообразователи, вступая в
симбиотические отношения с корнями древесных растений, способствуют
транслокации элементов минерального питания, в том числе и микроэлементов, из
почвы и лесной подстилки в деревья. Иными словами, микоризообразующие грибы как
передаточное звено усиливают поступление химических элементов, в частности
тяжелых металлов, в деревья. К высокомикотрофным древесным породам относятся
дуб, береза, осина, бук, граб, лещина, ель, сосна. Микоризу на корнях образуют
грузди, подберезовик, подосиновик, рыжик, боровик, маслята и др. [18].
Хорошим показателем загрязнения почв тяжелыми металлами
является их содержание в плодовых телах шляпочных грибов. Для этого в пробу
отбираются несколько экземпляров плодовых тел грибов. После высушивания они
озоляются при 3500 С, зола растворяется в одном из растворителей. В
растворах определяют содержание тяжелых металлов. При установлении
индикационных связей в качестве показателя микроэлементной нагрузки
используются концентрации металлов в верхних двух сантиметрах почвы, взятой в
точке отбора грибов, при выпадении тяжелых металлов из воздуха. Коэффициент
корреляции между содержанием свинца и кадмия в почве и капрофорах
подберезовиков, подосиновиков и груздей составляет около 0,7. При росте
концентрации в почве меди, цинка и марганца степень их накопления в капрофорах
уменьшается [18].
Также следует отметить, что покровобразующие виды мхов уже
несколько десятилетий используются для оценки атмосферных выпадений тяжелых
металлов в странах Северной Европы. Мхи не имеют корневой системы, поэтому их
микроэлементный состав определяется составом атмосферных выпадений, в том числе
минеральных частиц почвы, осаждающихся на поверхности растения под влиянием
ветра. Также проводилось исследование, в ходе которого было выявлена
зависимость осаждения тяжелых металлов от форм рельефа, направления ветрового
переноса, количества осадков. На наветренных склонах даже небольших
возвышенностей наблюдается более интенсивное осаждение тяжелых металлов, а в
понижениях между крупными структурами рельефа формируются "ветровые коридоры"
[7].
Также перспективно использовать в качестве биоиндикаторов
наземных сообществ насекомых. В частности, была проведена работа, объектом
которой были пчёлы как индикаторы загрязнения окружающей среды некоторыми
поллютантами. Пчёлы не только подвергаются влиянию окружающей среды, но и
воздействуют на неё путём опыления многочисленных цветущих растений. Было
выявлено, что производимые пчёлами прополис и обножка могут выступать в роли
индикатора загрязнения окружающей среды, т.к. являются активными биосубстратоми,
накапливающими тяжелые металлы [6].
В начале 50-х годов в результате применения
метилртутьдициандиамида для протравливания посевного материала в Швеции
произошла массовая гибель зерноядных птиц: серой куропатки, фазана, вяхиря,
обыкновенной овсянки, садовой овсяной, что привело к значительному
сокращению численности их популяций. Пострадали и хищники, питающиеся этими
видами [1].
Такие факты стимулировали исследования,
завершившиеся разработкой чувствительных методов определения концентрации ртути
в популяциях животных. Особое значение приобрел тест на присутствие ртути в
птичьих перьях, позволяющий проследить динамику ртутного загрязнения с
использованием чучел. Удалось ясно продемонстрировать, что начиная с 40-х годов
содержание ртути в перьях фазана, серой куропатки, белой куропатки,
сокола-сапсана и других видов возросло в 10-20 раз по сравнению с периодом
1840-1940 гг. [1].
Установлено, что у грача существует зависимость между
загрязнением ртутью и развитием популяции. Аналогичный результат был получен
при сравнительных исследованиях других видов [1].
Наряду с прямым влиянием на численность популяций показано и
отрицательное воздействие ртути на рождаемость у птиц. У перелетных птиц можно
установить время и место загрязнения по содержанию ртути в перьях. Разработан
метод, позволяющий использовать концентрацию ртути в утиных крыльях, собранных
охотниками в популяционно-биологических целях, для оценки общего загрязнения [1].
У крякв экспериментально была установлена доза ртути, выше
которой загрязнение яиц приводит к снижению воспроизводства и нарушениям
поведения у утят (3 млн-1 в пище в течение длительного времени) [1].
У водоплавающих птиц была также доказана
зависимость между способом питания и интенсивностью загрязнения. У рыбоядных
видов, таких, как большой крохаль и полярная гагара, загрязнение
достигает 100 млн-1, что десятикратно превышает загрязнение у видов,
захватывающих пищу исключительно с поверхности воды [1].
Всё же следует отметить, что наиболее
изученными и используемыми организмами в качестве биоиндикаторов загрязнения
природной среды являются гидробионты. Водоемы служат коллекторами всех видов
загрязнений, а донными отложениями аккумулируются загрязняющие вещества. Водные
организмы находятся в большей зависимости от условий среды обитания, чем
млекопитающие и птицы. Поглощение тяжелых металлов, большинство из которых
является жизненно необходимыми микроэлементами, происходит не только с пищей,
но и в процессе дыхания и через наружные покровы. У низших животных и растений
поглощение осуществляется всеми частями организма.
В Республике Беларусь также активно
ведутся исследования в этой области.
Для изучения экосистемы р. Березина в
качестве организмов - биоиндикаторов загрязнения тяжелыми металлами - были
использованы 3 вида рыб разного трофического уровня - планктонобентософаги
(плотва), весь цикл онтогенеза которых в основном проходит в поверхностных
слоях воды, и хищники - окунь и щука (в питании первого, наряду с рыбой, важное
место принадлежит бентосным организмам; рацион щуки состоит исключительно из
рыбы). С этой же целью были использованы два вида моллюсков (катушка и
прудовик), являющиеся кормовой базой для птиц и рыб, что делает их важными
объектами биомониторинга [13].
Сравнение состава тканей рыб показало
постепенное нарастание концентраций Zn, Cu, в меньшей степени Cr от рыб, в
питании которых доминируют планктонные и бентосные организмы, к плотоядным
рыбам, что закономерно отражает концентрации этих поллютантов в трофической
цепи. Mn и Sn, наоборот, интенсивнее накапливаются в мышцах планктонофагов и
уменьшаются в тканях хищных видов. Ni и Pb обнаружены лишь в одном экземпляре
плотвы [13].
Также авторы отмечают, что в заповедной
Березине накопление тяжелых металлов в мышцах рыб и теле моллюсков очень
невелико по сравнению с сопоставимыми по величине реками в других регионах [13].
При изучении растений различных
экологических групп водоёмов были получены результаты, указывающие на различные
уровни накопления некоторых тяжелыми металлами [11].
Были выделены 4 экологические группы:
I - свободноплавающие неприкрепленные;
II - плавающие
прикрепленные;
III - подводные
(погруженные) растения;
IV - надводные (земноводные
или воздушно-водные) [11].
Максимальное содержание всех изучаемых
элементов (Pb,
Cu, Zn, Mn, Co, Cr, Ni), за исключением цинка,
наблюдается у растений I-ой экологической группы. В наибольшей степени эта разница
заметна для меди, никеля и хрома. Известно, что чем больше растение связано с
водой, тем в большей степени в его тканях накапливаются медь, свинец и цинк, а
свободноплавающие гидрофиты I-ой группы получают элементы питания преимущественно из воды [11].
На аккумуляция тяжелых металлов
водорослями влияют режимы освещения и рН водной среды, что было зафиксировано в
экспериментах [9, 10].
В таблице 3 приведены данные по оценке степени
загрязнения водных экосистем тяжелыми и другими металлами, которая проводилась
на основе определения их содержания в воздушно-сухой массе водных растений
методом спектрального анализа [5].
Таблица 3. Содержание тяжелых металлов в гидрофитах водоемов
и водотоков Беларуси (мг/кг сухого веса) [5]
|
Элемент
|
Содержание
в гидрофитах по данным натурных наблюдений
|
Среднее
содержание в растениях по лит. данным
|
|
|
среднее
фоновое
|
мах в
чистых водоемах и водотоках
|
мах в
загрязн. водоемах и водотоках
|
|
|
1
|
2
|
3
|
4
|
5
|
|
Cr
|
0,34
|
11,25
|
43,0
|
2,0-5,0
|
|
Ni
|
0,30
|
11,25
|
40,8
|
0,05-5,0
|
|
Ti
|
8,39
|
130,40
|
130,4
|
0,15-80,0
|
|
Zn
|
1,41
|
42,10
|
177,5
|
15,0-100,0
|
|
V
|
3,55
|
13, 20
|
18,7
|
0,1-1,0
|
|
Cu
|
3,48
|
135,5
|
2,0-15,0
|
|
Pb
|
2,38
|
12,63
|
832,9
|
0,1-5,0
|
|
Mn
|
301,15
|
3180,50
|
3180,5
|
>500
|
Так, содержание никеля в водных растениях
колеблется от следовых количеств до 40,8 мг/кг сухого веса (частуха
подорожниковая в оз. Любенское), что в 135 раз превышает среднее фоновое
содержание никеля в гидрофитах республики и 8 раз выше уровня естественного его
содержания в растениях. Больше всего никеля накапливают гидрофиты водоемов и
водотоков, расположенных в окрестностях городов Минск, Гомель и Могилев, причем
избирательности в накоплении этого элемента определенными видами гидрофитов не
отмечено [5].
Среднее фоновое содержание меди в гидрофитах
республики 3,48 мг/кг сухого веса. В водоемах и водотоках Гомеля и Могилева
содержание меди в водных растениях намного превышает фоновые величины, причем
максимальные концентрации меди зафиксированы в воздушно-водных растениях (135,5
мг. кг - сусак зонтичный). В гидрофитах водоемов и водотоков, не подверженных
загрязнению, содержание меди, находится на уровне фоновых величин или имеет
незначительное превышение [5].
Самое высокое содержание свинца фиксируется в
разных видах гидрофитов во всех водоемах в окрестностях Гомеля. При средней
фоновой величине содержания свинца в гидрофитах 2,38 мг/кг максимальные
значения отмечаются в воздушно-водных растениях, в частности в тростнике -
832,9 мг/кг сухого веса. В растениях водоемов и водотоков г. Могилева
содержание свинца 6-56 мг/кг сухого веса, что в 3-20 раз превышает фоновую
величину. В относительно чистых водоемах гидрофиты накапливают свинец на уровне
фона [5].
Среднее фоновое содержание цинка в гидрофитах
республики 1,41 мг/кг сухого веса, а максимально зафиксированное количество
цинка - в элодее канадской и штукении гребенчатой (177,5 и 107,5 мг/кг сухого
веса) в водотоках городов Могилева и Новополоцка, что в 125 раз выше среднего
значения по республике и в 4 раза выше верхнего порога естественного содержания
цинка в растениях (по литературным данным) [5].
Наибольшее содержание тяжелых металлов
отмечается в водных растениях водотоков и водоемов, расположенных вблизи
крупных промышленных узлов.
Таким образом, выявлено, что индикаторной
значимостью тяжелых металлов водоёмов РБ обладают: Частуха подорожниковая,
Роголистник тёмно-зелёный, Роголистник подводный, Элодея канадская, Манник
плавающий, Манник большой, Водокрас обыкновенный, Трёхдольница трёхбороздчатая,
Рдест блестящий, Рдест узловатый, Рдест пронзеннолистный, Многокоренник
обыкновенный, Телорез алоэвидный, Рогоз широколистный, Харовые водоросли [5].
Заключение
Среди разнообразных загрязняющих веществ тяжелыми
металлами и их соединения выделяются распространенностью, высокой токсичностью,
многие из них - также способностью к накоплению в живых организмах. Многие
металлы образуют стойкие органические соединения, хорошая растворимость этих
комплексов способствует миграции тяжелых металлов в природных водах.
Техногенное поступление тяжелых металлов в окружающую
среду происходит в виде газов и аэрозолей (возгона металлов и пылевидных
частиц) и в составе сточных вод.
Основными источниками тяжелых металлов являются
теплоэнергетика и металлургическая промышленность.
Для контроля за
состоянием окружающей среды всё большую значимость приобретают методы
биоиндикации, в том числе и тяжелые металлы.
Многолетний опыт ученых разных стран по контролю состояния
окружающей среды показал преимущества, которыми обладают живые индикаторы:
·в условиях хронических антропогенных нагрузок
могут реагировать даже на относительно слабые воздействия вследствие
кумулятивного эффекта; реакции проявляются при накоплении некоторых критических
значений суммарных дозовых нагрузок;
·суммируют влияние всех без исключения
биологически важных воздействий и отражают состояние окружающей среды в целом,
включая ее загрязнение и другие антропогенные изменения;
·исключают необходимость регистрации химических и
физических параметров, характеризующих состояние окружающей среды;
·фиксируют скорость происходящих изменений;
·вскрывают тенденции развития природной среды;
·указывают пути и места скоплений в экологических
системах различного рода загрязнений и ядов, возможные пути их попадания в пищу
человека;
·позволяют судить о степени вредности любых
синтезируемых человеком веществ для живой природы и для него самого, причем
дают возможность контролировать их действие [16].
Методы индикации тяжелых металлов
биообъектами, а также выбор самих объектов, интенсивно разрабатываются и в
нашей стране, на что указывает многообразие научных трудов.
Таким образом, дальнейшие исследования
влияния тяжелых металлов на живые организмы очень актуальны, т.к. загрязнение
окружающей среды увеличивается.
Список
литературы
1. Биоиндикация
загрязнений наземных экосистем: Пер. с нем. / Под ред.Р. Шуберта. - М.: Мир,
1988. - 350 с.
2. Биологический
контроль окружающей среды: биоиндикация и биотестирование. Мелехова, О.П.,
Егорова, Е.И., Евсеева Т.И. и др.; под ред. Мелеховой, О.П. и Егоровой, Е. И.:
учеб. пособие для студ. высш. учеб. заведений. - М.: Издательский центр
"Академия", 2007. - 288 с.
. Будников,
Г.К. Тяжёлые металлы в экологическом мониторинге водных систем. // Соросовский
образовательный журнал. - N 5,
1998. - С.23.
4. Васин,
А.Е. Адаптация инфузорий Paramecium multicronucleatum
к солям некоторых тяжёлых металлов // Вестник СамГУ - Естественнонаучная серия.
2006. - N 7 (47)
. Власов,
Б.П., Гигевич, Г.С. Использование высших водных растений для оценки и контроля
за состоянием водной среды: Метод. рекомендации. - Мн.: БГУ, 2002. С.84
. Кадиров,
А. Пчёлы как индикаторы загрязнения окружающей среды некоторыми поллютантами: Дис. на соискание ученой
степени канд. биол. наук - 16.00.06, Москва, 1999 г.
. Королёва,
Ю.В. Биоиндикаторы атмосферных выпадений тяжёлых металлов на территории
Калининградской области // Вестник Рос. гос. унив-та им. Канта. - 2010. -
выпуск 7. С.39-44
. Кузнецова,
В.Ф. Эпифитные лишайники как индикаторы загрязнения атмосферного воздуха
газообразными поллютантами, тяжёлыми металлами и радионуклидами: Дис. на соискание ученой
степени канд. биол. наук, Нижний Новгород, 2004.
9. Кудряшов,
А.П., Морозова, О.В., Барыбин, Л.Н. Влияние освещения на аккумуляцию тяжёлых
металлов в водорослях NITELLA FLEXILIS // Мн.: БГУ, 2008 г.
. Кудряшов,
А.П., Морозова, О.В., Барыбин, Л.Н. Влияние рН среды на аккумуляцию тяжелых
металлов водными растениями // Молекулярные, мембранные и клеточные основы
функционирования биосистем. Матер. междунар. конф.8 съезд БООФБ, Минск. - 2008.
ч.1. - С.362-364.
. Макаренко,
Т.В. Содержание тяжёлых металлов в растениях различных экологических групп
водоёмов г. Гомеля и прилегающих территорий. // Известия ГомГУ им.Ф. Скорины. -
N 3 (60). - 2010. С.101
. Мур,
Дж.В., Рамамурти С. Тяжелые металлы в природных водах. - М.: "Мир",
1987.
. Натаров,
В.М., Савченко, В.В. Гидробионты как индикаторы загрязнения поверхностных вод
тяжёлыми металлами // Материалы научно-практической конференции
"Беловежская пуща на рубеже 3-го тысячелетия", 1999 г.
. Никаноров,
А.М., Жулидов, А.В., Покаржевский, А.Д. Биомониторинг тяжелых металлов в
пресноводных экосистемах. - Л.: Гидрометеоиздат, 1985. - 143 с.
. Реймерс,
Н.Ф. Азбука природы. Микроэнциклопедия биосферы. М.: "Знание", 1980.
. Содержание
кадмия и свинца в высших растениях на территории Красненского района
Белгородской области. // Научные ведомости. Серия - Естественные науки, 2011. -
N3 (98), вып.14
. Состояние
природной среды Беларуси: экологический бюллетень 2008. / Под ред. В.Ф.
Логинова. - Мн., 2009. - 406с (с.56)
. Туровцев,
В.Д., Краснов, В.С. Биоиндикация: Учеб. пособие. - Тверь: Твер. гос. ун-т,
2004. - 260 с.
. Химия
тяжелых металлов, мышьяка и молибдена в почвах. / Под ред. Н.Г. Зырина и Л.К.
Садовниковой. - М.: Изд. МГУ, 1985.
. Юрин,
В.М. Основы ксенобиологии: Учеб. пособие / В.М. Юрин. - Мн.: БГУ, 2001. - 234
с.
. Якунина,
И.В. Методы и приборы контроля окружающей среды. Экологический мониторинг:
учебное пособие / И.В. Якунина, Н.С. Попов. - Тамбов: Изд-во Тамб. гос. техн.
ун-та, 2009. - 188 с. - 100 экз.
. ТКП
17.06-08-2012 (02120). Технический кодекс установившейся практики. Охрана
окружающей среды и природопользование. Гидросфера. Порядок установления
нормативов допустимых сбросов химических и иных веществ в составе сточных вод.
. Показатели
качества воды рыбохозяйственных водных объектов. Нормативы предельно допустимых
концентраций химических и иных веществ в воде рыбохозяйственных водных
объектов. Минск, 2007г.
. Инструкция
по нормированию сбросов сточных вод в поверхностные водные объекты.
Министерство природных ресурсов и охраны окружающей среды Республики Беларусь
№2 от 20.04.2006г.
. Разрешение
на специальное водопользование № Бел-Гом.112 КПУП "Гомельводоканал"
г. Гомель. Министерство природных ресурсов и охраны окружающей среды Республики
Беларусь. Гомельский областной комитет природных ресурсов и охраны окружающей
среды.
. Соответствие
СанПиН 10-124 РБ 1999г.