Механизм действия нейротоксинов ядов змей
Реферат
по биохимии
Тема
Механизм действия нейротоксинов ядов
змей
Введение
химия змеиный яд
Змеиные яды являются уникальной по химическому составу и физиологическому
действию группой биологически активных соединений. Токсические и лечебные
свойства их известны человечеству с древнейших времен. Долгое время интерес к
изучению этих ядовитых продуктов ограничивался потребностями медицинской
практики. Большая часть работ была посвящена описанию клинической картины
отравления, изысканию методов специфической и неспецифической терапии, а также
использованию ядов змей и их препаратов в качестве лечебных средств.
Рациональное применение змеиных ядов в медицине невозможно без
экспериментального изучения и теоретического обоснования сущности реакций,
развивающегося в организме в ответ на введение того или иного яда. Исследование
отдельных механизмов действия на организм ядов змей необходимо для создания
научно обоснованных методов лечения.
Недостаточная разработка о механизмах отравляющего действия змеиных ядов
часто не позволяет врачам быстро и эффективно облегчить состояние
пострадавшего. В ряде случаев принимается во внимание только внешняя картина
отравления, и клиническая помощь ограничивается симптоматическими средствами
без учета специфики действия яда на жизненно важные системы организма.
Следует отметить, что змеиные яды оказывают сильное токсическое
воздействие только в летальных и сублетальных дозах. Небольшие дозы никаких
клинических проявлений отравления не вызывают и издавна используются практической
медициной. Однако терапевтическое применение часто проводится эмпирически без
достаточного теоретического обоснования, что влечет за собой ошибки. Не
приходится доказывать, что эффективное использование змеиных ядов в клинике
должно опираться на глубокие знания их состава и свойств и в первую очередь на
экспериментальные исследования, которые должны вскрыть физиологическую природу
и механизмы действия этих ядовитых веществ и помочь врачам научно обоснованно
применять яды в терапевтических целях. В исследовательских лабораториях резко
возрос интерес к зоотоксинам, а в частности к змеиным ядам, в связи с
получением из них в чистом виде ряда компонентов, которые обладают
высокоспецифичным действием, а определенные биологические структуры.
Цель этой работы осветить современное состояние экспериментального
изучения змеиных ядов, вскрыть механизмы патофизиологического воздействия на
важнейшие функциональные системы организма.
Состояние
химии змеиных ядов.
Получение
ядов и его физико-химические свойства.
Наиболее простым способом получения ядовитого секрета у змей является
механический массаж ядовитых желез. Сейчас часто вместо механического массажа
применяют стимуляцию электрическим током.
Электростимуляция не только является более щадящим методом сбора яда, но
и позволяет получать большее его количество. Количества яда, получаемого от
одной особи, зависит от размеров тела змеи, ее физиологического состояния,
числа повторных взятий яда, а также от ряда условий внешней среды. Необходимо
отметить, что содержание змей в неволе отражается не только на количестве
получаемого яда, но и на его токсичности. Так у яда кобры понижение токсичности
наблюдается уже после полугода содержания в неволе. Яд гюрзы изменяет
токсичность только после 2 лет содержания в питомнике. Что касается мелких змей
(гадюка, щитомордник, эфа), то содержание их в серпентариях в течение года не
отражается на свойствах ядов. [6] Свежедобытый змеиный яд представляет собой
слегка опалесцирующую, вязкую, достаточно прозрачную жидкость цвет яда варьирует
от светло-желтого до лимонного. [4]
Активная реакция ядов обычно кислая. Водные растворы их нестойки и теряют
токсичность через несколько суток. Гораздо более устойчивы к воздействию
факторов внешней среды становятся они после высушивания над хлористым кальцием
или лиофилизации. Яды довольно термостабильны и в кислой среде выдерживают
нагревание до 120 градусов Цельсия без потери активности. Разрушающе действуют
на яды химические реагенты: КМnO4,
эфир, хлороформ,
этанол метиленовый синий. Также воздействуют физические факторы: УФ-облучение,
рентгеновские лучи. Химический анализ показывает наличие в змеиных ядах как
органических, так и неорганических веществ. По современным представлениям
токсическая активность и биологические свойства змеиных ядов связаны с их
белковыми компонентами. [3]
Основные
этапы изучения химического состава и структуры токсических полипептидов змеиных
ядов. Вопросы о химической природе и механизмах действия змеиных ядов
привлекали внимание исследователей. В ранних работах токсическое действие
связывали с активностью присутствующих в ядах ферментов. В настоящее время
общепринятой точкой зрения, согласно которой основные токсические свойства
определяется неэнзиматическими полипептидами, наряду с которыми в ядах
содержатся мощные ферментные системы, от природы и специфичности действия
которых в большинстве случаев зависит своеобразие интегральной картины
отравления. Достижения и успехи в области изучения химического состава ядов
тесно связаны с развитием и совершенствованием методов фракционирования и
очистки сложных смесей высокомолекулярных соединений. До 60-х годов при
изучении ядов в основном использовали диализ через полупроницаемые мембраны и
электрофоретическое разделение. Развитии методов гельфильтрации, ионообменной
хроматографии, ультрацентрифугирования, а также разработка и автоматизация
методов анализа первичной структуры макромолекул позволили в сравнительно
короткие сроки расшифровать последовательность аминокислотных остатков
токсических полипептидах большинства змей. [1]
1. Терминология
и классификация токсических полипептидов
химия змеиный яд
До последнего времени существовали терминологические трудности при
попытке сравнительного анализа функциональных и структурных особенностей
различных неэнзиматических токсических полипептидов змеиных ядов. В основном
это касается полипептидов, выделенных из яда змей семейства Elapidae. На первых этапах изучения
химического состава ядов подобные трудности были неизбежны и объяснялись
недостаточной степенью очистки индивидуальных полипептидов, что в большинстве
случаев затрудняло определение специфического характера их действия. В
результате различные авторы разные наименования полипептидам, которые оказались
чрезвычайно близкими, а подчас идентичными по своей химической структуре и
фармакологическим эффектам. В частности, группа кардиотоксинов обозначалась как
фактор, деполяризующий скелетную мускулатуру; токсин Y; прямой литический фактор - ПЛФ; кобрамины Аи В; цитотоксины
1и 2.
Одни авторы при выборе названия основывались на патофизиологических
эффектах (кардиотоксин, ПЛФ, цитотоксин), другие подчеркивали некоторые
химические свойства полипептида, например его основной характер(кобрамин),
третьи присваивали фракции цифровое или буквенное обозначение . только в
последние годы установлено близкое сходство в химической структуре этих
полипептидов. Были получены доказательства , гемолитическая, цитотоксическая,
кардиотоксическая и другие виды активности присущи большинству этих токсинов.
Поэтому группу основных полипептидов, не обладающих специфической
нейротоксической активностью, но эффективно действующих на биологические
мембраны, назвали мембранно-активными полипептидами(МАП).
Кроме МАП, в ядах элапид содержится другая группа основных полипептидов,
обладающих высокой токсичностью и специфическим нейротоксическим пре- или
постсинаптическим эффектом. Терминология этой группы нейротоксинов также
неоднородна. В названии некоторых отражено систематическое положение змеи, из
яда которой они получены: a-бунгаротоксин,
кобротоксин.
Основываясь на сравнительном анализе первичной структуры и
физиологического действия, показавших большое сходство нейротоксических
полипептидов между собой, их объединили общим термином - нейротоксин. Таким
образом, все выделенные до настоящего времени из яда змей семейства Elapidae токсические полипептиды не
обладающие энзиматическими свойствами и по механизму действия разделяются на
три группы. К первой группе относятся полипептиды, избирательно и специфически
блокирующие холинорецепторы субсинаптической мембраны нервно - мышечного
соединения, - постсинаптические нейротоксины(пост-НТ). Вторая группа
представлена полипептидами, действующие избирательно на пресинаптические
окончания мионевральных синапсов и нарушающими процесс высвобождения
ацетилхолина - пресинаптические нейротоксины (пре-НТ).
В третью группу включены полипептиды, активно воздействующие на
мембранные структуры клеток, в том числе возбудимых, вызывая их деполяризацию -
мембранно-активные полипептиды(МАП). [3]
2. Химия
постсинаптических нейротоксинов
Несмотря на то, что по своим фармакологическим свойствам пост - НТ,
выделенные из яда кобр, близки, с точки зрения химического строения они могут
быть разделены на два типа.
К типу 2 относятся пост - НТ, состоящие из 71-74 остатков аминокислот,
имеющие 5 дисульфидных мостика (Рис 1, Б), молекулярный вес около 8000 (пост -
НТ-2).
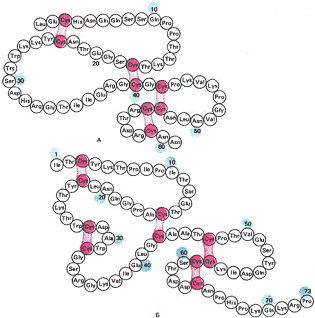
Рис
1. Первичная структура нейротоксина II (А) и нейротоксина I (Б) из яда
среднеазиатской кобры
Пост
- НТ-1 построены из 15 общих аминокислотных остатков, в их составе, как
правило, отсутствует Ала, Мет и Фен. Напротив, а пост - НТ-2 аланин
встречается. Интересной особенностью яда среднеазиатской кобры является
присутствие в нем нейротоксинов обоих типов. Причем в нейротоксине, содержащем
73 аминокислотных остатка, Арг или Лиз 51, характерные для всех пост - НТ-2
замещены на Глу.
Насыщенность
пост - НТ 1 и 2 дисульфидными связями наводит на мысль об их важном
функциональном значении в поддержании биологически активной конформации
молекулы. Восстановление дисульфидных связей приводит к потере 92% активности
пост - НТ-1 и 50% пост - НТ-2. повторное окисление восстанавливает
первоначальную активность нейротоксинов. По-видимому, большая устойчивость пост
- НТ-2 к химическим воздействиям связано с наличием пятой дисульфидной связи,
стабилизирующей участок полипептидной цепи. В тоже время у пост - НТ-1 этот же
участок молекулы наиболее удлинен и лишен дисульфидных мостиков. Наличие
мостиков обуславливает устойчивость пост - НТ и к термическому воздействию.
Так, в кислой среде пост - НТ выдерживают нагревание до 100°С в течение 30
минут без заметной потери активности или обработку 8М мочевиной в течение 24
часов, но инактивируется щелочами.
Расшифровка
первичной структуры нейротоксических полипептидов позволила поставить вопрос о
локализации и строении активного центра молекулы, вступающего в связь с
холиновым рецептором. Изучение строения этих полипептидов указывает на наличие
в молекулах нейротоксинов как α так и β-структур. Центральная часть молекулы пост -НТ -1 свободная
от дисульфидных связей, может обладать большей α-спирализацией. Кроме того, гидрофильный характер
большинства боковых цепей аминокислотных остатков, составляющих
последовательность от позиций 24-25 до положения 39-40, может обусловить
проекцию этой петли на внешнюю сторону молекулы, поэтому не исключено, что
активный центр локализуется в этом участке.
Важное
значение имеет анализ местоположения и химическая модификация инвариантных
аминокислот, встречающихся в гомологичных нейротоксинах в одних и тех же
участках. Эти аминокислоты, сохранившиеся в процессе эволюции в одинаковых
участках полипептидной цепи, могут участвовать в организации активного центра
или обеспечивать поддержание активной конформации молекулы. Наличие постоянных
аминокислот требует наличие инвариантного триплетного генного кода в молекуде
ДНК, необходимого для синтеза данной аминокислотной последовательности.
Поскольку
мишенью для пост - НТ ,так же как и для ацетилхолина, является холинорецептор,
то видимо активные участки нейротоксинов должны иметь сходство с четвертичной
аммониевой и карбонильной группами ацетилхолина. Было установлено, что
свободные аминогруппы, в том числе и N-концевые, не являются
облигатными для обеспечения токсической активности. Ацитилирование 6 аминогрупп
в нейротоксине из яда таиландской кобры привело к потере 1/3 активности.
Можно
было предполагать, что карбонильные группы пептидного состава всегда
присутствующие в молекуле пост - НТ могут иметь значение при обеспечении
токсичности. Однако они малодоступны в реакции взаимодействия с рецептором. В
большей степени отвечают этому требованию боковые группы боковых цепей
инвариантных аспарагиновой кислоты и аспарагина. Модификация аспарагиновой
кислоты метиловым эфиром глицина приводит к потере активности на 75% от
первоначального значения.
Необратимое
связывание между пост - НТ и холинорецептором нельзя объяснить только
взаимодействием гуанидиновых и карбонильных групп пост - НТ с соответствующими
участками рецептора. Их взаимодействие должно носить в основном электростатический
характер, однако, комплекс рецептор - токсин не диссоциирует в
концентрированных солевых растворах. Вероятно эти две функциональные группы
служат «участками узнавания» при первичном контакте пост - НТ и рецептора.
Конечное же необратимое связывание обуславливается протеин - протеиновым
взаимодействием, включающие уже другие участки пост - НТ и холинорецептора. [2]
3.
Химия пресинаптических нейротоксинов
Нейротоксины
второй группы,пресинаптические нейротоксины (пре - НТ), редко встречаются в
змеиных ядах. Только некоторые из них выделены в очищенном виде и изучены. В
семействе Elapidae пресинаптические НТ обнаружении в яде австралийского
тайпана - тайпоксин, австралийской тигровой змеи - нотексин, и в яде крайта - β-бунгаротоксин. Кротоксин - нейротоксин яда гремучих
змей обладает преимущественным пресинаптическим действием на нервно - мышечные
соединения у амфибий и постсинаптическим у млекопитающих. в отличие от пост -
НТ нейротоксины 2 группы построены из большего числа аминокислотных остатков и
соответственно имеют больший молекулярный вес. Кроме того некоторые из них
являются комплексом состоящим из субъединиц.
Одним
из первых пре - НТ, полученных с помощью зонального электрофореза на
крахмальном геле и в дальнейшем очищенных хроматографией на КМ-сефадексе с
повторной рехроматографией, был β-бунгаротоксин. Β-бунгаротоксин построен приблизительно из 179
аминокислотных остатков, среди которых преобладают аспарагиновая кислота(22
остатка), глицин (16), лизин (13),аргинин (14),тирозин (13). Наличие 20
остатков цистина указывает, что молекула β-бунгаротоксина стабилизированы по крайней мере 10 сульфидными связями.
Молекулярная масса нейротоксина 28500.
Предполагали,
что β-бунгаротоксин лишен энзиматических свойств и является
гомогенным. Однако установили, что β-бунгаротоксин состоит из двух субьединиц с молекулярным весом 8800 и
12400, изучая влияния β-бунгаротоксина на окислительное фосфолирирование в
митохондриях нервных окончаний, пришли к выводу о наличии у токсина
фосфолипазной активности.
Нотексин
был получен ионообменной хроматографией в градиенте ацетата аммония. Основной
нейротоксический компонент нотексина, составляющий 6% сырого неочищенного яда,
выделен в виде препарата, содержащего 27% нотексина путем повторного
хроматографирования.
Нотексин
представляет собой полипептид, состоящий из 119 аминокислотных остатка и 7
дисульфидных мостиков; молекулярный вес 13547. большинство очищенных препаратов
нотексина обладают фосфолипазной активностью. При определении N-концевой
последовательности следы загрязненности не были найдены, но следует иметь ввиду
что этот метод позволяет определить содержание примесей не менее чем 5 - 10%.
Поэтому энзиматическая активность может быть связана с незначительной примесью
фермента. Не исключено, что нотексин может быть родственен фосфолипазе А, ранее
выделенной из яда черношейной кобры, состоящей из 117 аминокислотных остатков и
7 дисульфидных мостиков. Сравнение нотексина и фосфолипазы А указывает на
сходство их первичных структур. [2]
4. Действие
ядов на передачу нервно-мышечную передачу
Механизм нарушения передачи возбуждения в мионевральном синапсе под
влияние змеиных ядов наиболее изучен. Уже первые наблюдения за картиной гибели
отравленного животного, в которой доминировали симптомы паралича скелетной и
дыхательной мускулатуры, вызвали необходимость изучения этого феномена в
строгих лабораторных условиях. Многочисленными опытами на изолированных
нервно-мышечных препаратах было показано, что змеиные яды блокируют передачу
возбуждения с нерва на мышцу, снижают возбудимость на прямую и непрямую
стимуляцию и вызывают деполяризацию нервных и мышечных мембран.
Угнетение нервно-мышечной передачи под действием яда может реализоваться
с помощью двух механизмов. Один из них связан с блокирующим действием яда на концевую
пластинку. В основе второго лежит деполяризующее действие на возбудимые
мембраны. Однако при использовании цельного яда трудно отдифференцировать эти
два механизма, так как его деполяризующее действие приводит к блокированию
распространяющегося возбуждения в нервных волокнах, а в высоких концентрациях
яд вызывает мышечную контрактуру. Яд предупреждает деполяризующее действие
ацетилхолина на изолированные мышцы, в то время как ацетилхолинэстеразные
соединения снижают его блокирующий эффект.
В опытах кротоксин блокировал мышечное сокращение на непрямую стимуляцию
и не оказывал влияния на мембранный потенциал. Однако изучение действия ядов
двух разновидностей (с кротамином и без него) сообщили о практически
необратимом блокирующем действии на нервно мышечную передачу у кошек и крыс яда
без кротамина, причем как на мышечные мембраны, так и на специфические
рецепторы постсинаптической мембраны. Нервно-мышечный блок под влиянием яда,
содержащего кротамин, достигался путем деполяризации мышечных мембран. Яд гадюковых
также способен нарушать нервно-мышечную передачу, вызывая периферический
паралич, обусловленный необратимой блокадой специфических ацетилхолиновых
рецепторов. Он угнетает также электрическую активность мышечных волокон.
Иммунохимический анализ показал наличие в яде белковой фракции, сходной с
постсинаптическим α-токсином из яда черношейной кобры. [2]
В
институте биоорганической химии им. академиков М.М. Шемякина
<http://www.ibch.ru/about/history/personalia/740>и Ю.А. Овчинникова
<http://www.ibch.ru/about/history/personalia/738> РАН (ИБХ) в лаборатории
молекулярной токсинологии проводятся работы по выделению и установлению
строения новых пептидов и белков из различных ядов, установлению мишеней
биологического действия изучаемых пептидов и белков, исследование механизма их
взаимодействия с соответствующими рецепторами, а также проводятся биологические
испытания, которые могут дать информацию для создания новых медицинских
препаратов.Поиск новых полипептидов ведется по двум основным направлениям, включающим
токсины, направленные против лиганд-управляемых ионных каналов, и соединения,
влияющие на процессы гемостаза.
Из
яда африканской шумящей гадюки Bitis arietans выделен блокирующий никотиновый
холинорецептор (нХР), белок с молекулярной массой 27,4 кДа. N-концевая
последовательность этого белка, названного битанарином, гомологична N-концевым
аминокислотным последовательностям фосфолипаз А2 из ядов змей, имеющих
молекулярную массу около 14 кДа и не обладающих способностью блокировать
холинорецепторы. С использованием метода радиолигандного анализа установлено
взаимодействие битанарина с нХР мышечного и альфа7 типа, а также с
ацетилхолин-связывающими белками моллюсков L. stagnalis и A. californica. По
своей активности битанарин близок так называемым необычным или слабым
трехпетельным токсинам из ядов кобр. Этот белок обладает также фосфолипазной
активностью, сопоставимой с активностью фософлипаз А2 яда кобр. Битанарин
представляет собой фосфолипазу А2 нового типа и является первой фосфолипазой,
для которой показано взаимодействие с нХР. [9]
5.
Постсинаптические нейротоксины (пост - НТ)
В отличие от цельного яда кобры пост - НТ избирательно блокируют передачу
возбуждения в нервно-мышечном соединении, не оказывая влияния на электрические
свойства нерва и мышцы. Инкубация в течение часа изолированных нервно-мышечных
препаратов в растворе, содержащем пост - НТ в концентрации около 1 мкг/мл,
приводит к прогрессивному уменьшению амплитуды потенциала концевой пластинки -
ПКП. Угнетающий эффект возрастает при увеличении частоты стимуляции,
одновременно уменьшается амплитуда ПКП без существенных изменений их частоты.
Даже в высоких концентрациях пост - НТ не оказывали влияния на потенциалы покоя
и мышцы и моторных терминалей.
Наибольшей чувствительностью к действию пост - НТ обладают
холинорецепторные мембраны скелетной мускулатуры позвоночных животных. В то же
время соматическая мускулатура морских моллюсков и сердце миноги устойчивы к
действию нейротоксинов кобры. Видовые различия в чувствительности
холинорецепторов на разнообразных представителях позвоночных (лягушки, цыплята,
котята, крысы). Было высказано предположение, что пост - НТ не являются прямыми
конкурентами ацетилхолина за активный центр холинорецептора. [9]
6.
Пресинаптические нейротоксины (пре - НТ)
Нейротоксины с пресинаптическим характером действия избирательно поражают
механизм высвобождения ацетилхолина, не влияя на чувствительность к медиатору
постсинаптических структур. Обработка изолированного нервно-мышечного препарата
β-бунгаротоксином после начального
периода увеличения частоты приводит к полному устранению ПКП. Скорость
наступления угнетающего эффекта зависит как от концентрации пре - НТ, так и от
частоты стимуляции. Также была установлена зависимость времени наступления
блока нервно-мышечной передачи от температуры окружающей среды. Так, тайпоксин
(1мкг/мл) при температуре 37 °С вызывал угнетение препарата в течение часа, при
снижении температуры до 28 °С проводимость сохранялась до 4 часов инкубации.
Пре - НТ не снижают ответ изолированных мышц на экзогенный ацетилхолин и не
влияют на проведения возбуждения по нервным терминалям. Другие доказательства
избирательного пресинаптического характера действия β-бунгаротоксина были получены на
лишенной нервных окончаний культуре тканей, полученных из миобластов 10 дневных
эмбрионов цыпленка. Предварительная инкубация α-бунгаротоксином полностью устраняла
деполяризацию вызванную последующим введением в среду ацетилхолина. В этих
условиях β-бунгаротоксин оказался не эффективным. На поздних стадиях
действия β-бунгаротоксина наблюдается разрушение везикул с ацетилхолином
вплоть до полного их исчезновения. Отмечается также и вакуолизация митохондрий
моторных нервных терминалей.
Действие β-бунгаротоксина сходно с действием токсины ботулизма,
также поражающего механизм высвобождения ацетилхолина из нервных окончаний.
Однако имеются и различия: токсин ботулизма не вызывает начального увеличения
ПКП; в отличие от токсина ботулизма β-бунгаротоксин взаимодействует только
с холинэргическими окончаниями; при действии токсина ботулизма не замечены
изменения в пресинаптической области.
На синаптосомах из мозга крысы выявлена способность β-бунгаротоксина снижать накопление
ГАМК, серотонина, норадреналина и холина. Поскольку β-бунгаротоксин в основном вытесняет
уже накопленные нейромедиаторы, можно предположить, что его действие связано с
поражение процесса хранения, а не транспорта медиаторов. [9]
Заключение
Механизм действия змеиных ядов еще окончательно не расшифрован учеными.
Но прозрачная капелька яда, попав в кровь, разносится ею по всему организму и в
определенной дозе оказывает благоприятный эффект на организм больного.
Установлено, что небольшие количества яда кобры обладают болеутоляющим
действием и могут даже использоваться как заменитель морфия у больных,
страдающих злокачественными новообразованиями. При этом в отличие от морфия
змеиный яд действует более длительно и, что самое главное, не вызывает
привыкания. Кроме того, созданы препараты на основе яда кобры, улучшающие общее
состояние больных, страдающих бронхиальной астмой, эпилепсией, стенокардией.
Потребность в змеином яде возрастает из года в год и змеепитомники,
созданные в ряде районов нашей страны, пока еще не могут удовлетворить эту
потребность. Поэтому назрела необходимость охранять ядовитых змей в природных
условиях, а также добиваться их размножения в неволе. [5]
Следует помнить, что в руках неопытных людей змеиный яд становится не
союзником в борьбе за сохранение здоровья, а опасным врагом и может вызвать
тяжелые отравления. О необходимости правильно подбирать дозу лечебного вещества
говорил еще Теофраст Парацельс, утверждая, что «...все есть яд, ничто не лишено
ядовитости, и все есть лекарство. Одна только доза делает вещество ядом или
лекарством». Это изречение знаменитого ученого не потеряло своего смысла и в
наши дни и, пользуясь ядами змей, больные обязаны строго соблюдать предписания
лечащего врача. [7]
Яды змей, как известно, опасны для многих видов млекопитающих. Но среди
более низко организованных животных, особенно среди насекомых, известны виды,
не восприимчивые к действию змеиного яда, что позволяет использовать их в
качестве противоядий.
Подводя итог рассмотрению круга вопросов, охватывающих особенности
химического строения и механизмов действия ядов, нельзя не упомянуть что
Природа - этот искуснейший экспериментатор - дала в руки исследователей
уникальные инструменты для изучения фундаментальных вопросов строения и
функционирования живой клетки.
Зоотоксины - прекрасные модели для молекулярной биологии, позволяющие
решать вопросы взаимосвязи структуры и функции в биомолекулах. [8]
Список литературы
1. Орлов Б.Н « Ядовитые животные и
растения СССР». М.: Высшая школа, 1990г. - 272 с.
. Орлов Б.Н «Яды змей» Издательство
«Медицина», Ташкент, 1987г. -252с.
. Г.И. Оксендендлер «Яды и
противоядия» Л.: Наука, 1982. - 192 с
. Е. Дунаев, И. Кауров «Рептилии.
Амфибии». М.: Астрель, 2010г. - 180с.
. Б.С Туниев, Н.Л. Орлов «Змеи
Кавказа». М.: Товарищество научных изданий КМК, 2009. - 223с.
. www.zmeuga.ru
. www.zoovet.ru
. http://www.ncbi.nlm.nih.gov/pubmed