Диазосоединения
Контрольная работа
Диазосоединения
Содержание
1. Представители
2. Получение диазосоединений
3. Строение диазогруппы
4. Устойчивость
5. Реакции без выделения азота
6. Реакции диазоалканов с выделением азота
7. Реакции солей диазония с выделением азота
Литература
Введение
Диазосоединения представляют собой органические молекулы,
содержащие два связанных между собой атома азота, причем один из них не
соединен с атомами других элементов. Связь N-N можно изобразить как в
виде двойной, так и в виде тройной; атомы азота имеют sp-гибридизацию.
Диазосоединения могут быть нейтральными молекулами либо катионами.
1.
Представители
Алифатические соединения устойчивы только в нейтральной
форме, поэтому солей алкилдиазония не существует. Сопряжение весьма эффективно
стабилизирует диазогруппу, поэтому диазокетоны, эфиры диазокислот и диазоалкены
(особенно циклические) устойчивее обычных диазоалканов. Примеры нейтральных
(ковалентных) диазосоединений:
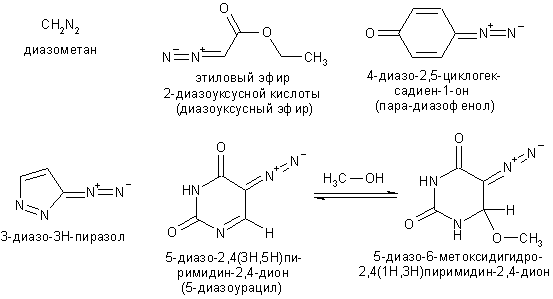
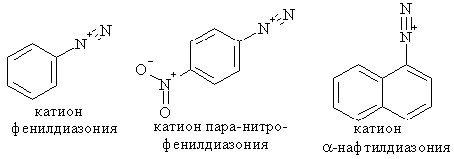
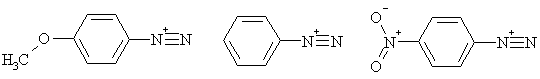
В ароматическом ряду известны катионные формы диазосоединений
(катионы диазония). Возможность их существования обеспечивается резонанасной
стабилизацией с участием ароматического секстета кольца и (+М) заместителей в орто
- и пара-положениях кольца, если таковые присутствуют. Многие катионы
арилдиазония устойчивы при температуре выше 0оС и успешно
применяются в органическом синтезе.
2. Получение
диазосоединений
Низкая устойчивость алкандиазониевых солей не позволяет
синтезировать диазоалканы посредством реакции диазотирования аминов в кислой
среде. Возникающая в результате действия азотистой кислоты на алкиламин
промежуточная соль алкилдиазония тотчас распадается, выделяя азот. Образующийся
карбокатион быстро реагирует с любым нуклеофилом, присутствующим в реакционной
среде, поэтому реакция аминов с азотистой кислотой в водом растворе приводит,
главным образом, к образованию спиртов. При диазотировании алкиламинов в
безводной уксусной кислоте продуктами превращения оказываются соответствующие
алкилацетаты.
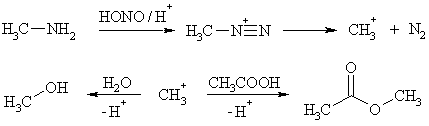
Приведенные реакции протекают с хорошим, зачастую количественным,
выходом, и поэтому они иногда используются для синтеза спиртов либо сложных
алкилацетатов в тех случаях, когда соответствующий амин достаточно доступен.
На практике для синтеза диазометана сначала получают устойчивое N-нитрозосоединение, которое гидролизуют до диазометана
щелочью под слоем эфира. Чаще всего применяют N-нитрозо-N-метилмочевину,
при разложении которой образуются только газообразные продукты, диазометан
поглощается эфирным слоем.

Для получения ароматических солей диазония применяют реакцию
диазотирования (П. Грисс), которая представляет собой взаимодействие первичных
ариламинов с азотистой кислотой в избытке сильной минеральной кислоты.
Неустойчивую азотистую кислоту генерируют, как правило, in situ,
внося нитрит натрия или калия в кислый реакционный раствор, содержащий
ариламин.
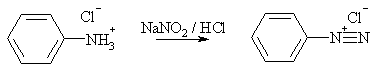
Некоторые катионы диазония имеют структурные возможности
стабилизации путем превращения с ковалентные диазосоединения, которые
оказываются продуктами диазотирования.
В отдельных случаях применяют так называемый метод обратного
диазотирования. Так, п-диазобензолсульфокислоту получают, приливая
щелочной раствор сульфаниловой кислоты и нитрита натрия к соляной кислоте.
Труднорастворимая в воде внутренняя соль п-диазобензолсульфокислоты выпадает
в осадок.

Диазотирование малоосновных аминов проводят в растворах с более
высокой концентрацией кислоты и нередко используют более сильные кислоты. Так,
если диазотирование анилина проводят в водном растворе, содержащем 3-4-кратный
избыток соляной кислоты, то реакцию с нитроанилинами ведут в концентрированной
серной кислоте.
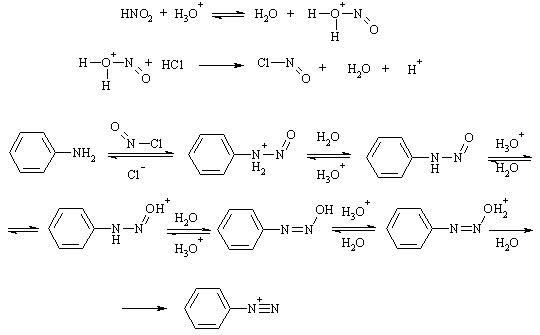
Реакция начинается атакой непротонированного амина активной формой
нитрозония. Эта стадия является лимитирующей, за ней следует ряда быстро
протекающих стадий:
3. Строение
диазогруппы
Диазониевая группа состоит из sp-гибридных атомов азота,
и, соответственно, имеет линейную геометрию. Длина связи N-N короче, чем в
соединениях с одинарными и двойными N-N-связями и колеблется около значения 110 пм. Это означает,
что данную связь можно рассматривать как почти чисто тройную. В схеме,
приведенный ниже длины связей даны пикометрах (пм).
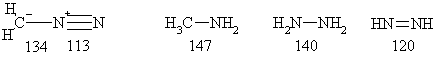

Электронное строение диазометана можно представить следующими
резонансными структурами:

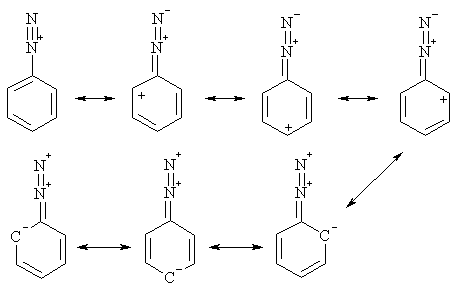
В катионе фенилдиазония положительный заряд делокализован с
участием p-электронной системы кольца, что снижает энергию частицы. В то же
время сопряжение дизогруппы с кольцом увеличивает порядок C-N-связи. Все это
делает катионы арилдиазониев намного более термодинамически стабильными
системами в сравнении с алкилдиазониями.
Как показывают данные квантовомеханических расчетов, положительный
заряд присутствует на обоих атомах азота, на концевом - он вдвое меньше
(+,0270), чем на центральном (+0,5842).
Разница длин связей N-N в солях диазония (109пм) и в ковалентных дизазосоединениях
(113 пм) свидетельствует, что "кумуленовая" граничная форма вносит
больший вклад в состояние нейтральных диазосоединений нежели в состояние
катионов арилдиазония. Это подтверждается большей устойчивостью нейтральных
диазосоединений.
4.
Устойчивость
Понятия "устойчивость" и "реакционная
способность" тесно связаны отношением: чем более устойчиво соединение, тем
ниже его активность в химических реакциях. Говоря об устойчивости
диазосоединений, имеют в виде два основных типа: термодинамичекую и
кинетическую. Термодинамическая устойчивость относится к способности в ходе
разложения отщеплять молекулу азота, тогда как кинетическая устойчивость
характеризует степень электрофильности диазосединения.
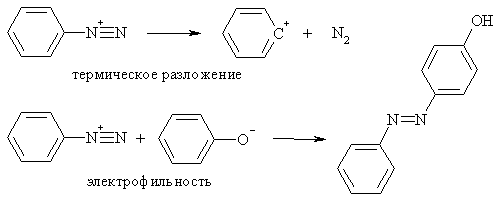
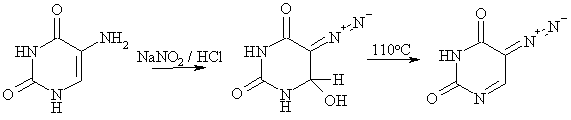
Ковалентные диазосоединения, в которых диазогруппа сопряжена с
кратными связями, например, диазопиразол или диазоурацил, термодинамически
весьма устойчивы. Так, 5-диазоурацил не изменяется при нагревании в
кристаллическом состоянии до 120оС, 3-диазопиррол может без
разложения перегоняться с водяным паром.
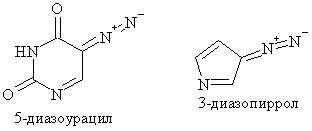
Среди алифатических диазосоединений самым нестойким является
диазометан, он разлагается со взрывом и поэтому работа с ним требует особой
осторожности. Кроме того, он очень ядовит. В то же время диазокетоны,
диазоуксусный эфир по причине сопряжения диазогруппы с карбонильной
(карбоксильной) группой проявляют более высокую стабильность.
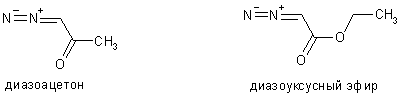
Многим нейтральным диазосоединениям свойственна также высокая
кинетическая устойчивость и лишь некоторые из них могут вступать в качестве
диазосоставляющей в реакции азосочетания при обычных условиях.
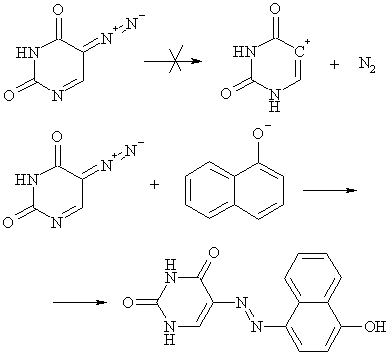
Термодинамическая стабильность солей диазония, которую можно
оценить их отношением к нагреванию, приводящему к разложению с выделением
азота, заметным образом определяется характером и расположением заместителей в
ароматическом кольце. Термическое разложение солей замедляется при введении в пара-положение
как донорных, так и акцепторных заместителей, обладающих мезомерным эффектом.
Кинетическая стабильность, т.е. электрофильная активность
арендиазониев также сильно зависит от заместителей в кольце. Так, реакция
азосочетания с фенолами ускоряется акцепторными заместителями и замедляется
донорными. Однако влияние природы заместителей на термодинамическую
устойчивость и электрофильность катионов диазония зачастую не совпадают, что
наглядно иллюстрирует сравнение относительных скоростей реакции разложения и
азосочетания трех катионов фенил-, пара-метоксифенил и пара-нитрофенилдиазония:
Относительные скорости реакции:
разложение 0,11 740 3,1
сочетание с фенолом 0,1 1 1300
Механизм влияния заместителей легко представить с помощью
резонансных структур, в которых заместитель включен в общую систему
распределения электронной плотности

5. Реакции
без выделения азота
Реакции азосочетания
Наличие положительного заряда на центральном атоме азота
придает катионам диазония и нейтральным диазосоединениям свойства слабых N-электрофилов. Несмотря
на то, что положительный заряд на концевом атоме азота почти в два раза меньше,
чем заряд на центральном атоме азота реагирующим электрофильным центром
является концевой атом азота.

Реакция азосочетания представляет собой бимолекулярное
электрофильное замещение (SE2)
атома водорода при электроноизбыточном атоме углерода, когда в качестве
электрофила выступает диазониевый ион. Для описания реакций азосочетания часто
применяют специальную терминологию: нуклеофильный реагент называют
"азосоставляющей", электрофильный - "диазосоставляющей". В
качестве азосоставляющей чаще всего выступают высоко p-избыточные ароматические
субстраты - фенолы (предпочтительно в форме фенолятов), ариламины, гетероциклы.
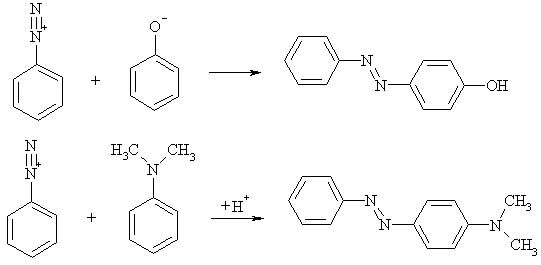
Продукты реакции содержат - N=N-группу и называются азосоединениями,
многие из них являются азокрасителями. Следует подчеркнуть, что окраска
вещества, обусловленная присутствием в молекуле заместителей, которые называются
хромофорами (в данном случае - это азогруппа), является необходимым, но
недостаточным условием принадлежности соединения к красителям. Молекула
окрашенного соединения должна иметь заместители, которые углубляют окраску и
обеспечивают прочную связь с волокном (хлопком, шерстью и др.). Такие
заместители называются ауксохромами. К ним относятся группы - OH, - NR2, - SO3H, - CN.

Сочетание с фенолами проводят в слабощелочной среде (pH<9), чтобы повысить концентрацию более
нуклеофильных фенолят-анионов; в сильнощелочной среде реакция не идет из-за
превращения диазосоставляющей в инертный диазотат (см. ниже). Амины лучше всего
сочетаются в слабокислой или нейтральной среде (pH 4-7); сильнокислая среда пассивирует амин за счет протонирования.
Диазониевые ионы активно сочетаются с СН-кислотами типа
b-дикетонов и b-кетоэфиров, особенно, в присутствии оснований; это
неудивительно, т.к. электронное строение азосоставляющих - енолов и
енолят-анионов - имеет много общего с фенолами и фенолятами. Продукт данной
реакции существует в виде смеси таутомерных форм азоенола (А) и кетогидразона
(Б), причем преобладает последняя.
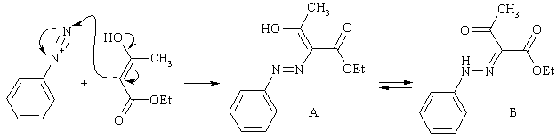
Если при активном центре СН-кислоты имеется карбоксильная группа,
то она в ходе азосочетания легко отщепляется путем декарбоксилирования. Как и в
случае b-кетокарбоновых кислот, декарбоксилирование протекает через
шестицентровое циклическое переходное состояние.
Реакции с гетеронуклеофилами
Для солей диазония известны такие реакции, где в качестве
нуклеофила выступает не атом углерода, но атомы других элементов - азота,
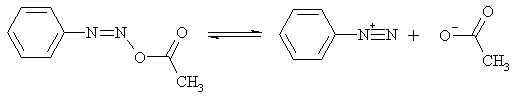
кислорода, серы и др. Так, при подщелачивании раствора соли арилдиазония
образуется сначала ковалентный аддукт - диазогидрат, а затем, при повышении pH - ионное соединение, называемое солью
диазотовой кислоты, или диазотатом. Как и другие азосоединения, диазогидрат и
диазотат могут существовать в виде син - и анти-изомеров. Анти
- (транс) - изомеры устойчивее син-изомеров, хотя последние все
же могут быть получены и зафиксированы в растворе.

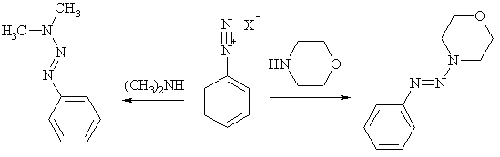
Присоединение к диазогруппе азотцентрированных нуклеофилов можно
проиллюстрировать на примере диалкиламинов: выделенная из диазораствора и
высушенная соль диазония в безводной среде быстро реагирует с диметиламином или
морфолином, давая соответствующие триазены.
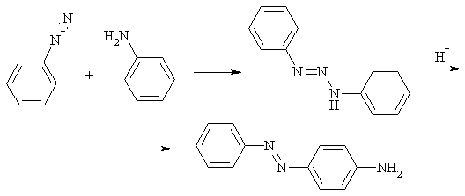
Соли диазония сочетаются по аминогруппе с молекулами анилина,
которые еще не успеди продиазотироваться. Поэтому при диазотировании анилина
иногда наблюдается побочная реакция образования дифенилтриазена (N-фениламиноазобензола), который является продуктом
сочетания анилина с фенилдиазонием по атому азота. Обычно это происходит при
недостаточной концентрации минеральной кислоты. N-Фениламиноазобензол до действием сильных кислот
перегруппировывается в пара-аминоазобензол.
Как правило, О-азо - и N-азосоединения
сравнительно неустойчивы, существуют в таутомерном равновесии с парой
соответствующих ионов или гидролизуются (особенно в присутствии кислот) с
выделением исходных - нуклеофила и соли диазония. Последняя затем вступает в
дальнейшие превращения.
Восстановление
Как электрофил соль арилдиазония образует аддукт с нуклеофилом -
гидросульфит-ионом. Это малоустойчивое солеобразное соединение в растворе
склонно к присоединению молекулы гидросульфита. Разложение N,N’-дигидросульфитпроизводного
при подкислении приводит к образованию арилгидразина; лучшие результаты
достигаются при добавлении более мощного восстановителя в кислой среде -
цинковой пыли. Эта реакция позволяет получать арилгидразины, зачастую
труднодоступные другими методами.
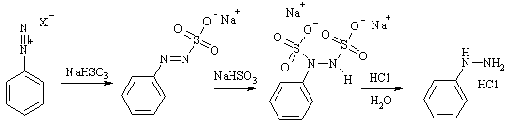
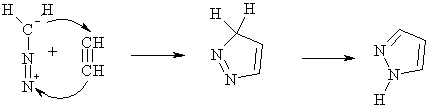
Циклоприсоединение
Диазосоединения алифатического ряда легко вступают в реакции
циклоприсоединения в качестве 1,3-диполей. Это превращение используется для
синтеза гетероциклических соединений - пиразолов и конденсированных
гетероциклов, содержащих пиразольное ядро.
6. Реакции
диазоалканов с выделением азота
Выше было показано, что одним из характерных свойств
диазосоединений является склонность к распаду с выделением молекулы азота.
Движущей силой этого процесса являются низкая термодинамическая устойчивость
алкилдиазониев и образование в ходе разложения устойчивой молекулы азота. Это
свойство является причиной целого ряда превращений, многие из которых имеют синтетическое
значение.
Простейшая реакция диазоалканов с выделением азота -
кислотный гидролиз в момент образования из аминов - была рассмотрена выше.
Диазоалканы и, в первую очередь, диазометан, подвергаются
ацилированию по электроноизбыточному атому углерода действием хлорангидридов и
ангидридов карбоновых кислот. Взаимодействие диазометана с ацилхлоридами лежит
в основе одного из важных способов удлинения длины углеродной цепи карбоновых
кислот. На одной из промежуточных стадий реакции возникает a-диазокетон,
который является сравнительно устойчивым соединением. При обработке последнего
влажной окисью серебра происходит разрыв связи C-N, выделяется молекула
азота, и образуется кетокарбен - неустойчивое нейтральное соединение с двумя
электронами на атоме углерода. Кетокарбен стабилизируется путем [1,2] - сдвига,
в ходе которого заместитель при карбонильной группе переходит к карбеновому
С-атому, что приводит к образованию производного кетена. Гидролиз последнего
дает карбоновую кислоту.
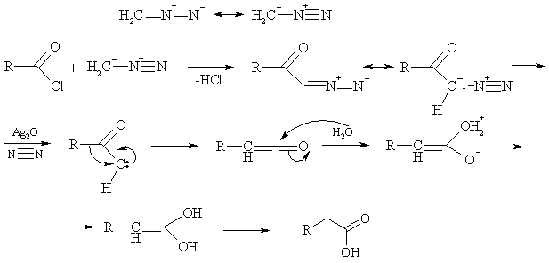
Стадия превращения диазокетона в кетен носит название
перегруппировки Вольфа. Рассмотренное превращение имеет аналогию с реакцией
расщепления амидов кислот по Гофману. Различие этих двух реакций состоит в том,
что в реакции Гофмана [1,2] - миграция заместителя от карбонила осуществляется
к нитреновому атому азота.
7. Реакции
солей диазония с выделением азота
Превращения солей диазония, протекающие с выделением азота,
весьма разнообразны. Они протекают с промежуточным возникновением ионных,
радикальных и ион-радикальных частиц.
Реакции мономолекулярного ароматического
нуклеофильного замещения (SN1 Ar)
Соли арилдиазония, как подчеркивалось выше, в меньшей
степени, чем их алифатические аналоги, способны к гетеролитической диссоциации
с выделением молекулы N2. Когла такое превращение реализуется, образуется
арильный катион, не стабилизированный резонансом. Эту частицу называют
s-катионом, потому что он при наличии заселенных p-орбиталей обладает
вакантной sp2-гибридной орбиталью, которая находится вне ароматического кольца.
Строение s-катиона можно также описать не только в виде ароматического кольца с
одной вакантной внешней орбиталью, но также как частицу, в которой один
электрон, "вырванный" из ароматического секстета, находится на
внешней s-орбитали, другой - в кольце. Последнее имеет подтвержения данными
спектроскопии электронного парамагнитноо резонанса (ЭПР).

Нуклеофильное замещение диазониевой группы гидроксилом происходит
при нагревании сернокислого раствора соли фенилдиазония в 40% -серной кислоте.
Возникающий в результате диссоциации s-катион реагирует с водой, давая фенол.
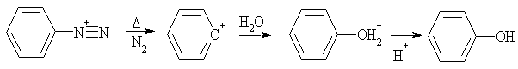
Реакция имеет синтетическое значение, и используется для получения
труднодоступных фенолов из нитроаренов через анилины и, далее, через соли
диазония.
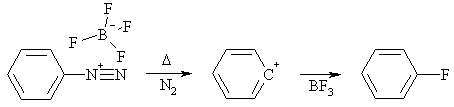
Другое важное превращение, протекающее через стадию образования
арильных катионов, - реакция Шимана, состоящая в термическом разложении сухих
тетрафторборатов арилдиазония. Механизм этой реакции до конца не выяснен.
По-видимому, в условиях термолиза происходит диссоциация катиона диазония на
арил-катион и азот, и противоиона - на трифторид бора и фторид-ион. Последний
сразу же присоединяется к положительно заряженному центру, что приводит к фторпроизводному
арена.
Не исключается, однако, возможность того, арильный катион, обладая
высокой активностью способен прореагировать с анионом тетраброфторида по пути
прямого электрофильного замещения трифторида бора при одном из атомов фтора в
анионе. Реакция Шимана имеет важное значение для синтеза фторароматических
соединений, которые, как известно, не могут быть получены путем прямого
фторирования аренов.
Отметим, что ионные реакции солей диазония - единственный пример
реализации мономолекулярного нуклеофильного замещения в ароматическом ряду (SN1Ar);
другие функциональные производные аренов не способны к самопроизвольной
диссоциации с образованием арильных катионов.
Радикальные реакции
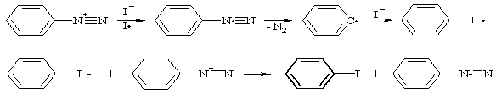
Замещение диазониевой группы иодом протекает легко и не требует
присутствия катализатора. Причина легкости реакции замещения заключается в том,
что иодид-ион является сильным одноэлектронным восстановителем. Он превращает
соль диазония в радикал. После элиминирования азота развитие цепи происходит в
результате взаимодействия фенильного радикала с иодид-ионом, возникший
анион-радикал далее реагирует с катионом диазония.
Т. Зандмейер нашел, что, в отличие от замещения диазогруппы иодом,
замещение хлором, бромом, циано-группой требует применения в качестве
катализатора солей меди (I). Механизм реакции Зандмейера окончательно не
установлен, но предполагается, что катионы Cu+1 одноэлектронно
восстанавливают катион диазония до диазорадикала. Медь при этом переходит в
высшую степень окисления (+2). Диазо-радикал сразу же после образования
распадается на арил-радикал и молекулу азота. Далее арильный радикал окисляется
ионом Cu (II) до катиона, который сразу же соединяется с нуклеофилом.
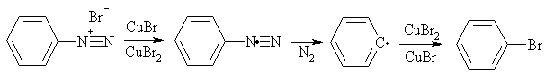
Реакция Зандмейера носит практически универсальный характер, и
позволяет ввести в молекулу атоматического соединения целый ряд нуклеофилов -
галогены, нитро-, циано-, меркаптогруппу и т.д. Для ее успешного проведения
нужно использовать соответствующие соли одновалентной меди - галогениды,
нитрит, цианид, сульфид.
Восстановление
По свободнорадикальному механизму идет восстановление солей
диазония фосфорноватистой кислотой H3PO2. На первой стадии этого превращения тоже предполагается одноэлектронное
восстановление катиона диазония и затем - распад диазо-радикала. Это
подтверждается тем, что H3PO2 катализирует другие свободно-радикальные реакции солей диазония.
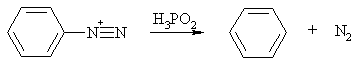
Сначала происходит передача одного электрона от аниона
фосфорноватистой кислоты катиону диазония и распад арилдиазорадикала с
образованием арильного радикала (инициирование цепи)

На следующих стадиях (развитие цепи) проявляется способность
фосфорноватистой кислоты одноэлектронно восстанавливать соли диазония за счет
легкости гомолиза связи Р-Н
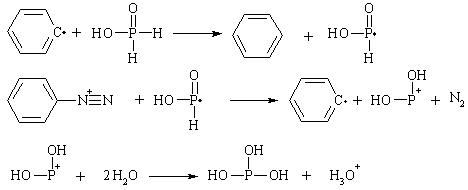
Реакция имеет большое значение в синтезе различных замещенных
бензолов. Например:
диазосоединение органическая молекула азот
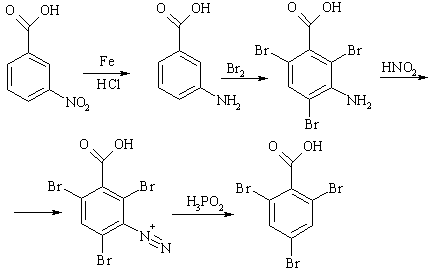
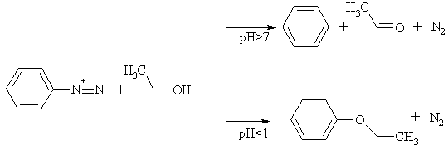
С участием свободных радикалов протекает восстановление катионов
диазония спиртами. В зависимости от кислотности среды в результате выделения
молекулы азота образуются с разными выходами два продукта: арен и алкиловый
эфир фенола.
При разложении солей диазония в слабо щелочном водном растворе в
присутствии аренов присходит арилирование этих углеводородов. Реакция получила
название арилирование аренов по Гомбергу-Бахману. Считается, что она протекает
по радикальному механизму.
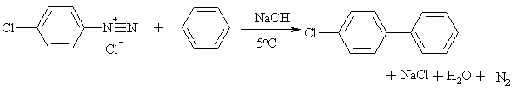
Литература
1.
Глинка Н.Л. Общая химия: Учебное пособие для вузов. - 22-е изд., испр. / Под
ред. Рабиновича В.А. - Л. о. "Химия", 1982.
.
Кукрашева К.К. Химия в таблицах и схемах. - М.: "Лист Нью". 2005.
.
Химия и физика в косметологии. Косметическое сырье, аппаратная косметология:
Учебное пособие, том 5/Под ред. к. м. н.А.П. Безуглого. - Издательство Cosmetic
Forum, 1998.
.
Хомченко И.Г. Общая химия. Учебник. - 2-е изд., испр. и доп. - М.: ООО
"Издательство Новая Волна": Издатель Умеренников, 2005.
.
Химия: Школьная энциклопедия / Гл. ред. Ю.А. Золотов. - М.: Большая Российская
энциклопедия, 2003.