Тонкослойные покрытия для микрореактора
Химия веществ и материалов
ВЫПУСКНАЯ КВАЛИФИКАЦИОННАЯ РАБОТА
Тема: ТОНКОСЛОЙНЫЕ ПОКРЫТИЯ ДЛЯ
МИКРОРЕАКТОРА
Реферат
Дипломная работа выполнена на ___ страницах, включает __
таблиц, ___ рисунок, ___ формул, при написании использовалось 40 литературных
источников.
Ключевые слова: оксидное покрытие, микрореактор,
алюмоциркониевая композиция, суспензия, реология, пористая структура,
механическая прочность, активность катализатора, окисление СО и Н2.
Дипломная работа посвящена исследованию реологических свойств
алюмоциркониевой суспензии и влияние данных свойств наносимости на носитель
(пластины); посвящена исследованию Ni-катализаторов. В процессе работы
производились синтез и исследование образцов катализатора; были оценены
структурно-прочностные свойства образцов катализатора и их активности в реакции
окисления СО и водорода.
Содержание
Введение
1. Аналитический обзор
1.1 Водородная энергетика
1.2 Микроканальные каталитические реакторы в процессах водородной
энергетики
1.3 Способы формирования тонкослойных оксидных покрытий
1.4 Композиты на основе ZrO2-Al2O3 и
перспективы их использования в качестве катализатора
1.4.1 Свойства активного оксида алюминия - носителя катализаторов
1.4.2 Строение и свойства диоксида циркония
1.4.3 Влияние нанокристалловZrO2 на стабилизацию
аморфного состояния оксида алюминия в системе ZrO2-Al2O3
1.5 Катализаторы на основе закиси никеля и металлического никеля
1.6 Патентный поиск
2. Цели и задачи работы
3. Экспериментальная часть
3.1 Исходные материалы, реактивы, приборы и оборудование
3.2 Методики получения и исследования свойств образцов суспензий,
носителей и катализаторов
3.2.1 Методика приготовления суспензии Al2O3-ZrO2
3.2.2 Методика формирования тонкослойного оксидного покрытия на
пластинчатых носителях
3.2.3 Методики исследования свойств синтезированных образцов
3.2.3.1 Свойства покрывных суспензий
3.2.3.2 Определение дисперсности порошка
3.2.3.3 Структурно-прочностные характеристики оксидных композитов
3.2.4 Рентгенофазовый анализ синтезированных образцов
3.2.5 ИК-спектроскопия образцов оксидных композитов
3.2.6 Методики исследования каталитических свойств образцов
3.2.6.1 Исследования образцов катализаторов в реакции окисления СО
3.2.6.2 Исследование образцов катализаторов в реакции окисления
водорода
3.3 Исследование влияния условий механохимического синтеза на
свойства покрывных суспензий
3.4 Выбор условий получения базовых покрывных суспензий
3.5 Влияние продолжительности измельчения на свойства покрывных
суспензий
3.6 Приготовление и исследование образцов катализаторов
3.7 Испытание образцов катализаторов в реакции окисления СО и Н2
3.8 Результаты ИК и РФА
4. Стандартизация
5. Охрана труда и окружающей среды
5.1 Опасные и вредные производственные факторы
5.2 Категория помещения по взрывопожароопасности
5.2.1 Класс взрывоопасной и пожароопасной зоны
5.2.2 Средства тушения пожара
5.3 Вентиляционная установка
5.4 Освещение помещения, воздух и шум
5.5 Аптечка и её содержание
5.6 Безопасность выполнения работы
5.7 Обеспечение электробезопасности
5.8 Анализ технологических операций с точки зрения опасности и
вредности их проведения
5.9 Меры первой медицинской помощи при случаях травматизма
5.10 Охрана окружающей среды
Выводы по работе
Список использованных источников
Введение
Создание катализаторов в виде покрытий на металлических
носителях с высокими адгезионными и регулируемыми структурными характеристиками
является актуальным, особенно применительно к технологии микроканальных
реакторов, разработка и исследование которых вызывают все больший научный и
практический интерес.
В настоящее время широко исследуется процесс получения
водорода в реакции паровой конверсии метанола или метана в микрокаталитических
системах.
Применение микроканальных систем для проведения
каталитического процесса паровой конверсии метанола или метана позволяет
создать компактные высокоэффективные генераторы для малотоннажного производства
водорода, которые можно использовать для мобильных энергоустановок. Однако в
настоящее время еще существует ряд проблем, решение которых необходимо для
организации производства микроканальных реакторов. Одной из них является
отсутствие простой методики надежного закрепления высокоактивного катализатора
на микроструктурированном металлическом носителе.
Для формирования каталитического покрытия в микроканальных
реакторах в используются различные приемы, каждый из которых имеет свои
положительные и отрицательные стороны.
Достаточно успешным на практике и перспективным для
формирования микроканальных пластин является метод нанесения на первичный
носитель суспензии, полученной из предшественников компонентов вторичного
оксидного носителя, в виде тонкого покрывного слоя с последующим закреплением
при сушке - прокаливании, обеспечивающих формирование его прочности и пористой
структуры. В рамках этого метода возможно управлять свойствами вторичного
носителя, изменяя условия синтеза суспензий, в том числе их состав и режимы
обработки. Перспективно использование механохимического активирования исходных
гидроксидов и оксидов алюминия, циркония в композиции с предшественниками других
компонентов и модифицирующими и пептизирующими добавками.
В связи с вышесказанным дипломная работа посвящена
исследованию условий формирования тонкослойного оксидного покрытия и
катализатора на его основе для микроканальных пластин каталитического реактора.
1.
Аналитический обзор
1.1
Водородная энергетика
В последние десятилетие стало очевидным фактом, что
дальнейшее интенсивное развитие современной энергетики и транспорта ведет
человечество к крупномасштабному экологическому кризису. Стремительное
сокращение запасов ископаемого топлива будет принуждать индустриально развитые
страны расширять сеть атомных энергоустановок, которые во все возрастающей
степени станут повышать опасность их эксплуатации. Резко обострится проблема
утилизации радиоактивных отходов. Учитывая эту тревожную тенденцию, многие
ученые и практики определенно высказываются в пользу ускоренного поиска
альтернативных источников энергии. В частности, их взоры обращаются к водороду,
запасы источников которого неисчерпаемы. Неоспоримым достоинством водородного
топлива являются относительная экологическая безопасность его использования,
приемлемость для тепловых двигателей без существенного изменения их
конструкции, высокая калорийность, возможность долговременного хранения,
транспортировки по существующей транспортной сети, не токсичность и т.д. [1,2]
Водородная энергетика - отрасль энергетики, развивающаяся в
направлении выработки и потребления энергии человечеством, основанном на
использовании водорода в качестве средства для аккумулирования, транспортировки
и потребления энергии людьми, транспортной инфраструктурой и различными
производственными технологиями. [2].
Водородная энергетика сформировалась как одно из направлений
развития научно-технического прогресса в середине 70-х годов прошлого столетия.
По мере того, как расширялась область исследований, связанных с получением,
хранением, транспортом и использованием водорода, становились все более
очевидными экологические преимущества водородных технологий в различных
областях народного хозяйства. Успехи в развитии ряда водородных технологий
(таких как топливные элементы, транспортные системы на водороде,
металлогидридные и многие другие) продемонстрировали, что использование
водорода приводит к качественно новым показателям в работе систем или
агрегатов. Выполненные технико-экономические исследования показали: несмотря на
то, что водород является вторичным энергоносителем, то есть стоит дороже, чем
природные топлива, его применение в ряде случаев экономически целесообразно уже
сейчас. Поэтому работы по водородной энергетике во многих, особенно промышленно
развитых странах относятся к приоритетным направлениям развития науки и техники
и находят все большую финансовую поддержку со стороны, как государственных
структур, так и частного капитала.
1.2
Микроканальные каталитические реакторы в процессах водородной энергетики
Химические процессы получения водорода, связанные с
протеканием каталитических реакций, широко распространены в современной
промышленности.
Уникальные свойства водорода позволяют считать его
универсальным и экологически чистым химическим энергоносителем, пригодным для
использования в любых видах тепловых двигателей и устройств получения
электроэнергии. Особое значение при этом имеют "топливные процессоры"
- каталитические газогенераторы водорода, использующие в качестве его исходного
носителя органические соединения типа углеводородов, спиртов и эфиров. Так,
использование природного газа или жидких углеводородов в качестве источника
синтез - газа является перспективным направлением в водородной энергетике [2].
тонкослойное покрытие микрореактор катализатор
В настоящее время широко исследуется процесс получения
водорода в реакции паровой конверсии метанола или метана в микрокаталитических
системах.
Применение микроканальных систем для проведения
каталитического процесса паровой конверсии метанола или метана позволяет
создать компактные высокоэффективные генераторы для малотоннажного производства
водорода, которые можно использовать для мобильных энергоустановок. Однако в
настоящее время производство микроканальных реакторов находится лишь на стадии
создания опытных образцов. Основными проблемами, препятствующими широкому
распространению микроканальных реакторов, являются высокая стоимость их
изготовления и отсутствие простой методики надежного закрепления
высокоактивного катализатора на микроструктурированном носителе с высоким
коэффициентом теплопроводности.
Каталитическая микроканальная система (МКС) представляет
собой компактный реактор, внутри которого размещены пластины с каналами
субмиллиметровых размеров (рисунки 1,2) [1,4]. Микроканальные пластины (МКП)
являются носителями каталитически активного компонента и их обычно
изготавливают из материалов с высокой теплопроводностью. Примеры МКП
представлены на рисунках 3, 4.
Конструкция КМС позволяет решить ряд разных проблем,
возникающих в традиционных химических реакторах. Среди таких проблем - низкая
радиальная теплопроводность неподвижного слоя катализатора, затрудняющая
теплообмен в зоне реакции, а также недостаточно эффективное использование
катализатора. Экспериментальные исследования подтверждают, что использование
каталитических микроканальных систем в процессах получения водорода существенно
увеличивает эффективность процессов по сравнению с традиционными химическими
реакторами [1,4,5].

Рисунок 1 - Блочный микрореактор паровой конверсии метанола
размером 65х90х85 мм, изготовленный из латуни

Рисунок 2 - Микрореактор каталитического парциального окисления
метана. Полезный объем МР, занимаемый микроканальными пластинами МКП,
составляет 4,0 см3
Перечисленные достоинства МКС приводят к существенному
увеличению их удельной производительности, а в ряде случаев и к повышению
селективности проходящих в них реакций. Наиболее ярко эти достоинства
проявляются при осуществлении быстрых реакций с малым временем контакта и
высокими тепловыми эффектами, например, в ходе полного и парциального окисления
углеводородов.
Испытания одной секции микрореактора паровой конверсии
метанола (рисунок 1), проведенные с использованием МКП, изготовленных из
пеноникеля с катализатором Cu-Ce-Al-O (рисунок 3), показали, что при входном
потокежидкой смеси метанола и воды 80 см3/ч и температуре реактора
260оС конверсия метанола составила 80%. При этом производительность
по водороду одной секции микрореактора составила 106 дм3/ч, а
удельная производительность микрореактора в пересчете на суммарный объем МКП
равнялась 4,9 дм3/ (см3ч) [4].
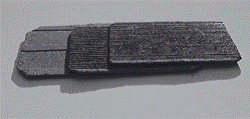
Рисунок 3 - МКП из пеноникеля с внедренным с помощью ультразвука
порошком готового катализатора с последующим запрессовыванием его под давлением
250 ат до толщины 0,3-0,8 мм; содержит каналы сечени-ем от 0,1 до 0,5 мм и
длиной 12 мм

Рисунок 4 - МКП из нержавеющей стали - лазерная литография с
элек-трохимическим травлением поверх-ности; каналы в формы спиралей с сечением
0,2 мм; нанесение и закрепление готового катализатора
Cu/ZnO - запрессовывание его частиц (1-5) мкм в смеси со
связующим - псевдобемитом
1.3 Способы
формирования тонкослойных оксидных покрытий
Для достижения максимальной эффективности работы
микроканального реактора наряду с исследованием протекания в нем процесса
паровой конверсии УВ требуется не только оптимизация конструкции реактора,
геометрии микроканальных пластин/сотовых структур, но и разработка простых и
эффективных способов закрепления катализатора.
Микроканальный реактор состоит из трех базовых составляющих:
корпус, микроканальные пластины (МКП) или другие элементы теплопроводящего
носителя и закрепленный на них катализатор. Хотя для создания эффективно
работающего устройства важны все три составляющих, создание тонкослойного,
прочно закрепленного на теплопроводящей поверхности эффективного катализатора,
устойчивого в условиях реакции, по нашему мнению, является наиболее сложной
задачей.
При изготовлении МКП в качестве первичного металлического
носителя используют пластины - плоские или гофрированные - из фольги (50 мкм)
из нержавеющей стали или фехраля, а также пластины из пеноматериала, в
частности, из пеноникеля.
Залогом качества в получении катализатора в виде тонких слоев
на каком-либо носителе является выбор метода формирования пористой оксидной
пленки с геометрическими и структурно-прочностными характеристиками
позволяющими [5-8]:
рационально и высокодисперсно распределить каталитически
активный компонент или его соединение-предшественник;
оптимально использовать каталитически активный компонент при
эксплуатации в составе реактора;
прочно закрепить слой оксидного носителя или катализатора на
поверхности первичного носителя, обеспечив необходимый ресурс.
Для формирования каталитического покрытия в микроканальных
реакторах в настоящее время используются различные приемы, каждый из которых
имеет свои положительные и отрицательные стороны [5]:
напыление каким-либо способом на поверхность первичного
носителя тонкодиспергированного готового катализатора с последующим его
запрессовыванием под высоким давлением с образованием рельефа каналов;
подготовка рельефа поверхности первичного носителя лазерной
литографией и электрохимическим травлением с последующим запрессовыванием смеси
тонкодиспергированного готового катализатора со связующим;
нанесение на металлическую пластинку с помощью объемного
взрыва корунда в качестве промежуточного слоя, последующее наращивание на эту
поверхность в ходе химической реакции высокопористого слоя γ-Al2O3 c внутренней пористостью около 300 м2/г в
качестве вторичного носителя; нанесение методом "пропитка/прокалка"
активного компонента.
В [5] указываются недостатки микроканальных пластин с
закрепленным механическим способом катализатором: осыпание катализатора в
процессе работы; необходимость специального оборудования и тщательного контроля
процесса изготовления; недостаточное количество закрепляемого катализатора, что
в совокупности с его осыпаемостью сокращает срок службы микрореактора. Автор
считает, что закрепление катализатора на поверхности пластины химическим
способом (терминология автора) - методом пропитки-прокаливания или из суспензии
(с предварительной подготовкой поверхности) - снимает основные проблемы и
позволяет получать достаточно прочный слой катализатора регулируемой толщины.
Положительным является возможность нанесения этим способом катализатора на
пластины сложной геометрической формы, например, гофрированные. К недостаткам
этого способа автор относит низкую устойчивость слоя к термоциклированию.
В [5] разработана методика закрепления катализатора в порах
пластин из пенометалла, причем в качестве исходной системы использована водная
суспензия компонентов катализатора, а ее распределение в порах осуществляется
под воздействием ультразвука. После сушки пластинам придается требуемая форма
запрессовыванием со связующим, в качестве которого используется псевдобемит в
количестве 30-40 % масс.
Достаточно успешным на практике и перспективным для
формирования МКП, по нашему мнению, является метод нанесения на первичный
носитель суспензии, полученной из предшественников компонентов вторичного оксидного
носителя, в виде тонкого покрывного слоя с последующим закреплением при сушке -
прокаливании, обеспечивающих формирование его прочности и пористой структуры. В
рамках этого метода возможно управлять свойствами вторичного носителя, изменяя
условия синтеза суспензий, в том числе их состав и режимы обработки.
Перспективно использование механохимического активирования исходных гидроксидов
и оксидов алюминия, циркония в композиции с предшественниками других
компонентов и модифицирующими и пептизирующими добавками. Так, на формирование
прочного, с развитым объемом пор вторичного Al2O3-носителя
оказывают влияние следующие условия их механохимического синтеза [6-8,9]:
продолжительность измельчения исходных псевдобемита (ПБ) и
активного оксида алюминия (АОА) до различной реакционноспособности и
дисперсности - до 1-5 мкм;
кристаллохимическая модификация оксида алюминия - γ-, θ - или ά-Al2O3;
плотность суспензии (концентрация дисперсной фазы), как
правило, в интервале (1,1-1,3) г/см3;
рН и расход кислот-пептизаторов, аммиака, др.;
концентрация добавок оксидов металлов или их солей -
предшественников компонентов оксидной матрицы;
продолжительность стадий механохимического синтеза суспензий
и других условий его проведения (объем загрузки, скорость вращения и диаметр барабана,
размер и форма мелющих тел, др.)
Важной характеристикой, определяющей во многом успех
формирования оксидного слоя на пластинах и их прочность, пористость, являются
реологические характеристики суспензий и их взаимосвязь со
структурно-прочностными показателями получаемого вторичного оксидного носителя,
его термостойкостью. Очевидно, что в общем случае увеличение плотности
суспензии приводит к увеличению вязкости, но для суспензий различного состава
характер ее изменения отличен [8-11].
Для обеспечения прочного закрепления тонкого слоя пористой
оксидной матрицы на металлической поверхности, ее предварительно
подготавливают, создав переходный слой. На практике, при использовании в
качестве материала первичного носителя фольги (50 мкм) из стали специальных
алюминий - содержащих составов, например, Х15Ю5 или Х23Ю5, это достигается
оксидированием поверхности металла [8]. Окисление поверхностных атомов алюминия
при высокотемпературном прокаливании металлической ленты в присутствии
кислорода приводит к образованию на поверхности слоя оксида алюминия,
выполняющего одновременно и функцию антикоррозионной защиты. Частицы
поверхностного оксида алюминия становятся центрами закрепления при дальнейшем
нанесении оксидной матрицы. [12]
Нанесение суспензий на первичные носители - оксидированные
металлические пластины производится посредством многократного (3-14 раз)
повторения следующих операций: окунания пластины в суспензию, центрифугирования
для снятия излишков суспензии, отверждения термообработкой при 300 С.
Завершающей операцией после нанесения требуемого слоя
(контролируется по увеличению массы носителя) является термообработка пластины
с оксидным слоем при конечной температуре, обеспечивающей формирование
необходимой фазы оксида - индивидуального или композита.
Необходимая кратность операций "нанесения-отверждения
при 300 С покрывной суспензии зависит как от свойств суспензии, ее вязкости,
плотности, концентрации твердой фазы в пересчете на MеnOm,
так и от способа и условий снятия излишков суспензии (центрифугирование).
1.4 Композиты
на основе ZrO2-Al2O3 и перспективы их
использования в качестве катализатора
В качестве перспективного компонента катализаторов
рассматривается оксидные системы ZrO2-Al2O3,
обеспечивающие термостабилизацию фазовой и пористой структуры как носителя, так
и непосредственно катализатора.
Достаточно широкое применение как основа активных
катализаторов находит в последнее время наноструктурированный диоксид циркония,
обладающий многими уникальными свойствами. Так, в работе [13,14] авторы рассмотрели
кристаллическую структуру и текстурные свойства диоксида циркония,
модифицированного молибдат - анионами. В результате было установлено, что
молибдат - анионы ингибируют образование метастабильной формы оксида при
механоактивации высокодисперсного гидроксида. В то же время они эффективно
способствуют формированию метастабильной формы оксида при высокотемпературном
прокаливании. Одним из факторов, который может обуславливать ингибирование
процесса формирования высокотемпературной модификации ZrO2 оксидом
молибдена, возможно, является то, что МоО3, для которого характерны
сдвиговые структуры, в механохимической системе проявляет эффект
"смазки". Энергия механохимического импульса в этом случае
расходуется на образование сдвиговых структур в МоО3, что приводит к
неблагоприятным кинетическим (уменьшению "локальной" температуры) и
термодинамическим (снижению градиента механического давления) условиям
протекания реакции в фазе ZrO2.
Особый интерес представляет синтез нанокристаллов диоксида
циркония в гидротермальных условиях ввиду возможности получения монодисперсного
материала с заданным размером частиц и кристаллической структурой.
Гидротермальное модифицирование является эффективным приемом изменения текстуры
и регулирования пористой структуры оксидных неорганических адсорбентов и
катализаторов.
Перспективной для использования в качестве носителей
катализаторов окисления водорода является гидротермально структурированная
система ZrO2-Al2O3. Ее перспективность связана
с тем, что наночастицы ZrO2 диспергированы в матрице
рентгеноаморфного Al2O3, которая препятствует росту
частиц диоксида циркония за счет процесса перекристаллизации, протекающей при
высоких температурах. В то же время среднее расстояние между наночастицами ZrO2
значительно меньше критического размера зародыша Al2O3,
что в свою очередь препятствует образованию кристаллического оксида алюминия.
Именно такое строение системы дает возможность предполагать, что нанокомпозит
на основе ZrO2-Al2O3, обладает выраженными
каталитическими свойствами.
Анализ экспериментальных результатов, полученных при
выполнении предшествующих работ по синтезу и исследованию пористых оксидных
систем ZrO2: Al2O3 (от 90: 10 до 50: 50)
показал следующее [13-15].
В работе [16] были синтезированы покрывные суспензии ZrO2:
Al2O3 при использовании различного сырья для формирования
оксидноциркониевой составляющей - порошка ZrO2 и раствора нитрата
цирконила. В результате исследований структурно-прочностных характеристик
оксидных матриц было установлено, что образцы обладают высокой механической
прочностью, развитым объемом пор, величина которых мало зависит от соотношения
ZrO2: Al2O3, а определяется в основном выбором
исходного сырья для синтеза. Значения эквивалентных радиусов пор
свидетельствуют о том, что образцы полидисперсны и с явно выраженными тремя
видами пор: 8-17, 20-150 и 240-250 нм. Удельная поверхность всех образцов
хорошо развита, причем независимо от природы образца проходит через максимум,
что, по мнению авторов [16], обусловлено протеканием двух противоположных процессов.
С одной стороны, увеличение удельной поверхности при введении азотнокислого
цирконила связано с процессами растворения-осаждения при приготовлении
суспензии, а также последующей термообработкой образцов. При сушке происходит
более плотная упаковка частиц ZrO2: Al2O3, что
обусловливает увеличение удельной поверхности. С другой стороны, при получении
суспензии с более чем 30 % оксида циркония, удельная поверхность оксидной
матрицы, полученной отверждением суспензии, начинает падать, что связано с
развитием макропористой структуры.
Исследование влагопоглотительной способности оксидных: Al2O3
- ZrO2 матриц показало, что с увеличением относительного давления
паров воды от 0,1 до 0,95 количество сорбируемой влаги возрастает, что
свидетельствует о полидисперсности сорбирующих мезопор [16].
Рентгенографические исследования показали наличие различных
модификаций оксида алюминия и оксида циркония в композиции в зависимости от
соотношения компонентов и от использованного для синтеза покрывных суспензий
сырья - нитрата цирконила или же оксида циркония, ПГА или же оксида алюминия, а
также от температуры прокаливания [15,16].
1.4.1
Свойства активного оксида алюминия - носителя катализаторов
Исследование оксида алюминия имеет большое значение, потому
что он представляет собой многотоннажный продукт химического рынка. Хотя
преобладающая часть оксида алюминия потребляется при производстве
металлического алюминия, все возрастающее его количество находит применение и в
иных областях, например для получения адсорбентов и катализаторов.
Из большого многообразия оксидов, которые могут быть
использованы в качестве носителей, оксид алюминия обладает всеми качествами
хорошего носителя и на его примере можно рассматривать многие проблемы,
возникающие при выборе носителя. Следует отметить некоторые свойства оксида
алюминия, его физические и химические характеристики [17-20]. Во-первых, его
амфотерность: в кислой среде он проявляет основные свойства, а в основной -
кислотные, что позволяет наносить каталитически активные компоненты как в виде
катионов, так и анионов, а это значительно расширяет возможности синтеза
нанесенных катализаторов.
Ценным для носителя качеством является высокая температура
плавления оксида алюминия - несколько выше 2300К. Он относится к тугоплавким
оксидам, т.е. обладает замечательной способностью стабилизировать
мелкодисперсные частицы катализатора и предотвращать их спекание или слипание,
являясь как бы термическим стабилизатором катализатора.
Особенностью оксида алюминия является многообразие его
модификаций и наличие фазовых переходов между ними в широком интервале
температур [17-20]. Эти фазы, которые обычно характеризуются шпинельной
структурой, отличаются друг от друга наличием дефектов в кристаллической
решетке. Согласно общепринятой классификации различают низкотемпературные
оксиды алюминия γ-Al2O3,
устойчивые до 800С и высокотемпературные, к которым относят продукты
терморазложения при температурах 900-1200-1400 С (900-1000 - θ, выше 1100 - α). Роль носителя
заключается и в повышении устойчивости метастабильной дисперсии мелких
кристаллитов металла на поверхности Al2O3 к агломерации и
спеканию.
Кроме того, благодаря развитой внутренней пористости и, как
правило, наличию пор крупных разновидностей, оксид алюминия облегчает диффузию
реагентов и продуктов реакций к каталитическим активным центрам и от них. Это
обстоятельство может быть очень важным в случае каталитических реакций,
лимитированных диффузией реагентов, т.е. в процессах, идущих с очень большой
скоростью [21].
Важным преимуществом оксида алюминия по сравнению с другими
носителями является простота формования из него экструзией различных
сферических частиц, обладающих хорошей механической прочностью [9,17,18].
Благодаря высокоразвитой и термостойкой поверхности оксид
алюминия широко используется в качестве носителя для большого числа
металлических катализаторов. Высокая удельная поверхность оксида алюминия
обусловлена небольшими размерами кристаллитов. На поверхность, доступную для
пропитывающего раствора, выходят катионы кислорода и гидроксильные группы,
которые прочно сорбируют многие соли металлов и уменьшают миграцию металла в
процессе высушивания [20,22,23].
Выбор оксида алюминия в качестве носителя осуществляется
путем подбора оптимальных параметров: текстурных (удельная поверхность,
распределение пор), структурных и морфологических (форма и ориентация
кристаллов), химических (содержание примесей, сила поверхностных центров), а
также размерных и механических.
В заключение можно привести положительные свойства и стороны
использования оксида алюминия в качестве собственно носителя или компонента
носителей и катализаторов: [17-19].
оксид алюминия позволяет стабилизировать каталитически
активные нанодисперсные частицы и предотвращает их агломерацию;
за счёт большого количества различных модификаций оксида
алюминия возможно регулирование соотношения микропор и переходных пор (величины
удельной поверхности), а также развития системы транспортных пор;
наличие на поверхности кислотных и основных центров расширяет
возможности модифицирования и нанесения каталитически активных компонентов;
развитая внутренняя поверхность оксида алюминия снижает
диффузионные сопротивления;
термическая устойчивость в обычных условиях катализа;
доступность в больших количествах и умеренная цена.
1.4.2
Строение и свойства диоксида циркония
Диоксид циркония благодаря своей высокой температуре
плавления, значительной электропроводности в сочетании с низкой
теплопроводностью находит все большее применение в промышленности. При этом
разделяются два вида продукта - природный диоксид циркония (бадделеит) и
синтетический диоксид циркония. Порошки диоксида циркония используются в
производстве огнеупоров, различных видов керамики, материалов для электроники и
каталитических фильтров-нейтрализаторов выхлопных газов автомобилей и т.д. Значительное
количество диоксида циркония идет на производство керамики, фарфора и стекла.
Диоксид циркония образует три кристаллические модификации:
моноклинную, тетрагональную и кубическую, существующих стабильно в различных
температурных интервалах [19]. Моноклинный диоксид циркония имеет искаженную
решетку, промежуточную между решетками флюорита и рутила. Переход ZrO2
из моноклинной формы в тетрагональную сопровождается значительным изменением в
объеме. Полиморфные превращения не сопровождаются диффузией и заканчиваются при
температуре около 1300°С. Тетрагональный ZrO2 имеет решетку в
определенной степени близкую к флюориту. При 23000С происходит
превращение тетрагональной формы в кубическую модификацию. При охлаждении
кубическая модификация переходит обратно в тетрагональную, превращение не
сопровождается глубоким изменение структуры, а происходит за счет
незначительной перестройки атомов в решетке, оно идет с поглощением тепла и
характеризуется сжатием структуры.
Большое количество исследований посвящено получению
ультрадисперсного порошка ZrO2, стабилизированного методом
совместного соосаждения из растворов солей ZrO2; это направление считается
достаточно перспективным, так как позволяет получать изделия из тонкодисперсных
порошков с низкой температурой спекания и высоким показателем прочностных
свойств [13-15].
В последние годы диоксид циркония привлекает большое внимание
специалистов при использовании его в качестве компонента носителей или одного
из компонентов катализаторов для высокотемпературных процессов: при
производстве синтез - газа методом паровой конверсии метана, восстановлении
оксидов азота, окисления оксида углерода, гидрообессеривания, дегидрирования
этилбензола. Использование ZrO2 в качестве носителя нанесенных
катализаторов глубокого окисления обусловлено его уникальной способностью
стабилизировать активные металлы в процессе работы при высоких температурах.
Высокая термическая и гидротермическая стабильность диоксида циркония
обуславливает высокую перспективу его использования для применения в процессах
в среде водяного пара. Однако наибольший интерес привлекают композиции на
основе сульфатированного диоксида циркония в качестве катализатора изомеризации
алканов, нитрования бензола и многих других реакций, катализируемых сильными
твердыми кислотами [22,23].
1.4.3 Влияние
нанокристалловZrO2 на стабилизацию аморфного состояния оксида
алюминия в системе ZrO2-Al2O3
Изучению взаимного влияния компонентов на скорость химических
и структурных превращений в гетерогенных смесях оксидов с различной дисперсностью
посвящено большое число работ [17,18,22,23]. Были обнаружены эффекты как
повышения скорости химических и структурных превращений при увеличении
поверхности контакта между различными оксидами, так и понижение скорости
процессов.
В [15] рассмотрены превращения в системе ZrO2-Al2O3,
в которой диоксид циркония представлен нанокристаллами. Исследование процесса
гидротермальной дегидратации системы ZrO2-Al2O3-H2O,
полученной путем осаждения гидроксида алюминия в суспензии нанокристаллов
диоксида циркония, показало, что в ходе гидротермальной обработки композиции
фиксируется первая стадии дегидратации с образованием бемита, а дальнейшее
повышение температуры гидротермальной обработки приводит к образованию
рентгеноаморфного оксида алюминия. При этом изменения параметров элементарной
ячейки ZrO2, а также роста частиц диоксида циркония не наблюдается,
из чего можно заключить, что наночастицы ZrO2 диспергированы в
матрице рентгеноаморфного Al2O3, которая препятствует
росту частиц диоксида циркония за счет процесса перекристаллизации до высоких
температур. С другой стороны, вероятно, среднее расстояние между наночастицами
ZrO2 значительно меньше размера критического зародыша Al2O3,
что в свою очередь препятствует образованию кристаллического оксида алюминия.
Именно такое строение системы дает возможность предполагать,
что нанокомпозит на основе ZrO2-Al2O3 может
обладать хорошими каталитическими свойствами.
1.5
Катализаторы на основе закиси никеля и металлического никеля
В ряду катализаторов конверсии углеводородов в качестве
эффективных признаны никельсодержащие композиты [19,21,22]. В исследованиях по
разработке МКС для генерации водородсодержащего топлива также используются Ni -
и NiO-катализаторы - как в виде индивидуальной активной фазы на пористом тонкослойном
носителе, так и в составе многокомпонентного катализатора.
Бинарные оксидные системы состава NiO - MexOy
служат исходными веществами при получении катализаторов типа Ni-оксид. Свойства
исходных веществ оказывают большое влияние на характер никель - оксидных
катализаторов, поэтому их рассмотрение представляет интерес. Важной
особенностью этих систем является способность к восстановлению с образованием
металлического никеля, характеризующая прочность связи Ni2+ в
комплексе NiO - MexOy.
В связи с большим научным и практическим значением в [19]
была исследована cистема NiO-Al2O3. Миллиген показал, что
осадки, полученные взаимодействием растворов аммиака и солей Ni и Al, имеют
рентгенограммы соответствующих гидроксидов. В противоположность этому, осадки,
образующиеся из смешанных растворов нитратов никеля и алюминия и ряда других
соединений, рентгеноаморфны. Это было объяснено увеличением дисперсности
гидроксидов вследствие взаимной защиты от кристаллизации. Также в исследовании
показано, что отсутствие аддитивности свойств бинарных систем не ограничивается
торможением скорости кристаллизации. Было сделано предположение, что при
осаждении гидроксидов Ni и Al между композитами осадка происходит
взаимодействие, в результате которого образуется гидроалюминат никеля.
Исследование методом ИК - спектроскопии бинарных гидроксидов позволило сделать
вывод, что в процессе осаждения между компонентами происходит взаимодействие, в
результате которого образуется гидроалюминат никеля. Сведения о фазовом составе
cистемы NiO-Al2O3 после прокаливания противоречивы.
Образцы, содержащие от 20 до 50 мол. % Al2O3, прокаленные
при 500oС, рентгеноаморфны, а образцы, содержащие менее 20 и более
50 мол. % Al2O3, дают только дифракционную картину NiO
или Al2O3, соответственно. При прокаливании на воздухе
при 700оС в образцах с эквимолярным соотношением NiO к Al2O3
образуется шпинель, дающая твердые растворы как с NiO так и с Al2O3./Al
является двухфазной и состоит из шпинели (твердого раствора NiO в γ - Al2O3) и твердого раствора на основе NiO. При термической
обработке в токе водорода образовавшиеся никель - алюминиевые соединения в
большей или меньшей степени восстанавливаются, образуя фазу металлического
никеля. Степень восстановления зависит и от состава катализатора.
При использовании никелевых катализаторов в реакциях,
связанных с переработкой углеводородов (применительно к задачам водородной
энергетики - процессы паровой конверсии углеводородов), следует учитывать
вероятность протекания нежелательного образования на поверхности катализатора
углеродистых (коксовых) отложений. Это приводит к блокировке активной
поверхности и дезактивации катализатора.
В литературе описаны 2 различных механизма закоксовывания
катализаторов, в том числе и NiO/Al2O3 иNi/Al2O3
(или Ni/ (Al2O3-ZrO2) [22]:
Консекутивный механизм образования углеродистых
отложений реализуется на поверхности оксидных катализаторов, имеющих
льюисовские и бренстедовские кислотные центры. Этот механизм представляется как
ряд последовательных реакций образования "мономеров уплотнения" и
промежуточных продуктов уплотнения на основе полимеризации, конденсации,
дегидроциклизации, связывания ароматических колец и обеднения водородом вплоть
до графитоподобной структуры.
Механизм "карбидного цикла"реализуется при
разложении углеводородов на поверхности металлов. У (III) группы подгруппы
железа, в т. ч. Ni. Механизм состоит из двух этапов:
химического этапа, включающего в себя каталитическое
разложение адсорбированных на поверхности металлической частицы углеводородов
до атомов углерода через промежуточные поверхностные карбидоподобные
соединения;
физического этапа, заключающегося в миграции образовавшихся
атомов углерода путем диффузии через металлическую частицу к центрам
кристаллизации графитовой фазы на тыльной стороне этой частицы.
Характер протекания процесса зауглероживания по
"карбидному циклу" обусловливает особую морфологию углеродных
отложений, называемых каталитическим волокнистым углеродом. Обычно это волокна
или нити, в головной части которых находится частица металла.
В [22] описан Ni/Al2O3-катализатор,
содержащий наряду с никелем и оксидом алюминия также фазу алюмоникелевой
шпинели; последняя препятствует спеканию дисперсных частиц никеля в условиях
реакции углеродообразования, протекающей в условиях эксплуатации достаточно интенсивно.
1.6 Патентный
поиск
Результаты патентного поиска (1994-2009 гг.) способов
формирования тонкослойных оксидных покрытий для микрореактора представлен в
таблице 1.
Таблица 1 - Результаты патентного поиска
|
Страна
|
Индекс МПК
|
№ патента
|
Название изобретения
|
Дата публикации
|
|
Россия
|
B01J8/00
|
2013117
|
Устройство для рекомбинации водорода и
кислорода
|
30.05.1994
|
|
Россия
|
C25D11/02, C25D15/00
|
2086713
|
Тонкослойное керамическое покрытие и способ его
получения
|
10.08.1997
|
|
Россия
|
C23C14/35
|
2138094
|
Установка для нанесения тонкослойных покрытий
|
20.09.1999
|
|
Россия
|
H01J37/317
|
2151439
|
Магнетронная распылительная система
|
20.06.2000
|
|
Германия
|
С07 С\522
|
6514262
|
Кислый катализатор и способ его изготовления
|
24.01.2002
|
|
Россия
|
В01J8/04
|
2264853
|
Способ рекомбинации водорода и кислорода,
находящихся в газовой смеси, рекомбинатор водорода и кислорода
|
25.02.2004
|
|
Россия
|
C01G25/02
|
2003123701
|
Способ получения порошка диоксида циркония
|
27.02.2005
|
|
Россия
|
С04В35/81
|
2289555
|
Способ получения кера-мического материала на
основе диоксида цирко-ния, армированного дис-кретными волокнами оксида
алюминия
|
20.12.2006
|
|
Россия
|
E21B 47/10
|
009346
|
Пластинчатый микрореактор с катализаторов
|
10.09.2007
|
|
Россия
|
В01J37/04
|
2348457
|
Способ приготовления катализатора и катализатор
для очистки выхлопных газов двигателей внутреннего сгорания
|
10.03.2009
|
|
Россия
|
B01J37/025
|
2360734
|
Пассивный каталитический рекомбинатор водорода
|
10.07.2009
|
В патенте № 2138094 Россия изобретение относится к плазменной
технике и предназначено для нанесения различных покрытий на поверхность
диэлектрических материалов, преимущественно листовых, с большой площадью
поверхности.
В патенте №2289555 Россия патентуется изобретение,
относящееся к области композиционных керамических материалов, которые могут
быть использованы в космической, авиационной, автомобильной и других отраслях
промышленности.
В патенте №2003123701 Россия описывается способ получения
порошка диоксида циркония, включающий осаждение гидроксида циркония и его
смесей с гидроксидами стабилизирующих элементов из водных растворов нитратов и
хлоридов этих элементов раствором аммиака, отделение осадка от маточного
раствора, его промывку и обезвоживание, отличающийся тем, что осаждение
гидроксида циркония и его смесей ведут при рН не ниже 8, а пульпу после
осаждения обрабатывают в автоклаве при температурах 105-2000С.
В патенте № 2086713 Россия изобретение относится к области
металловедения, касающейся тонкослойных керамических покрытий на основе
глобульной керамики и их нанесения электролитическим методом, а более
конкретно, к получению на поверхности черных и цветных металлов износостойких
покрытий методом микродугового оксидирования, и может быть использовано в
машиностроении, химической и нефтеперерабатывающей промышленности.
В патенте № 2151439 Россия - магнитная распылительная система
(МРС) относится к области плазменной техники и предназначена для нанесения
тонких пленок на поверхность твердых тел, преимущественно листовых материалов.
МРС, как и прототип содержит анод, являющийся корпусом системы, катодный узел и
кассету для обрабатываемого материала. Катодный узел представляет собой
магнитный блок, закрытый плоской распыляемой мишенью с возможностью поджигания
тлеющего разряда между катодным узлом и анодом. В предлагаемой системе
магнитный блок выполнен в виде магнитопроводного каркаса, пространство между
ребрами которого заполнено постоянными магнитами. Такое выполнение магнитного
блока дает возможность поджигания тлеющего разряда по меньшей мере с двух
симметричных его сторон, каждая из которых закрыта распыляемой плоской мишенью.
При этом кассета с обрабатываемыми образцами может быть установлена с каждой
(или любой) стороны магнитного блока, где возможно поджигание разряда.
Техническим результатом является увеличение производительности системы без
увеличения ее весогабаритных характеристик.
В патенте №651426 Германия предлагается эффективный твердый
катализатор на основе диоксида циркония.
В патенте № 2264853 Россия заявляемая группа изобретений
относится к методам и устройствам, предназначенным для обеспечения водородной
взрывобезопасности, и может быть использована в атомной энергетике,
транспортном, химическом машиностроении и других отраслях техники.
В патенте № 2348457 Россия изобретение относится к области
получения катализаторов очистки выхлопных газов и может быть использовано в
технологии производства каталитических бифункциональных нейтрализаторов
выхлопных газов двигателей внутреннего сгорания, а так же технологии
производства катализаторов очистки отходящих газов промышленных производств от
оксидов углерода и азота, углеводородов.
В патенте №2360734 Россия изобретение относится к области
атомной энергетики, в частности, к устройствам удаления водорода из герметичных
помещений атомных электростанций (АЭС) и может быть использовано в системе
безопасности АЭС.
Проведенный патентный поиск показал, что существует
устойчивый интерес к материалам на основе диоксида циркония и его композициям с
оксидом алюминия. Однако, синтез каталитических материалов на его основе еще
мало изучен. В частности, алюмоциркониевая композиция ранее практически, не
исследовалась, области использования подобных материалов являлись, как правило,
корпоративной тайной. Представляется интересной и актуальной разработка способа
получения тонкослойного каталитического покрытия на основе оксидного алюмоциркониевого
композита для микроканальных реакторов с использованием суспензионного метода
нанесения.
2. Цели и
задачи работы
Цель дипломной работы:
Исследование условий формирования тонкослойного оксидного
покрытия и катализатора на его основе для микроканальных пластин
каталитического реактора
Задачи работы:
Выбор конструкции элемента микроканального реактора и
компонентов:
профиль металлического носителя: высота гофры, сочетание
гладкого и гофрированного материала, укладка;
состав и геометрические параметры оксидного покрытия: оксид
алюминия-оксид циркония, толщина слоя
Исследование влияния условий приготовления суспензии на ее
реологические характеристики: - дисперсность исходных порошков; -
продолжительность механохимического синтеза; - pH; - плотность.
Определение структурно-прочностных характеристик оксидных
композитов в виде тонкослойных покрытий на пластинах и элементах
микроканального реактора, а также в виде гранул, получаемых из суспензий.
Получение и исследование свойств образцов Ni-катализаторов при
варьировании способа введения активного компонента и его содержания: нитрат и
карбонат никеля, пропитка и введение в суспензию; 7-12% NiО.
Исследование образцов катализатора в процессах окисления СО и
Н2
3.
Экспериментальная часть
3.1 Исходные
материалы, реактивы, приборы и оборудование
Исследование условий получения образцов тонкослойных
катализаторов проводилось для композиций состава "50% ZrO2-50%
Al2O3" с использованием в качестве исходных
материалов реактивного диоксида циркония, цирконила нитрата,
тонкодиспергированного активного оксида алюминия и псевдобемита (ПБ). При этом
варьировались рН, плотность суспензии.
В качестве исходных материалов были использованы
следующие реактивы:
псевдобемита AlOOH (ПБ);
цирконил азотнокислый ZrO (NO3) 2;
Аl₂O₃ в виде порошка, полученного измельчением в шаровой мельнице
активного оксида алюминия марки АОА-1 (г. Рязань), ГОСТ 8136-85 в течение 12 ч;
дистиллированная вода;
аммиак водный NH4OH;
кислота азотная HNO3;
диоксид циркония ZrO2 в виде порошка, полученного
измельчением в шаровой мельнице реактивного оксида циркония ТУ 6-09-17-167-82,
выпускаемого в форме таблеток, в течение 12 ч;
Приборы и аппаратура:
вытяжной шкаф;
устройство для механохимического синтеза суспензии (барабан
емкостью 0,5 дм3, вращающийся со скоростью 4200 об/ч);
прибор для определения реологических характеристик суспензий
РЕОТЕСТ-2;
шкаф лабораторный сушильный до 300 С;
муфельная электропечь до 900 С;
весы аналитически лабораторные ВДР - 200, с погрешностью не
более ± 0,0002 г;- метр (pH-673);
хроматограф "Цвет 100";
измеритель прочности гранул МП-2;
весы торсионные WAGATORSYJNA - WT;
компрессор воздушный;
электроплитка;
посуда лабораторная фарфоровая;
посуда лабораторная стеклянная, включая мерную (цилиндры,
бюретки, пипетки);
фарфоровая ступка с пестиком;
шприц-устройство для экструзии пластичных масс;
доски грануляторные;
электрохимический преобразователь концентрации водорода типа
H2-12;
портативный компьютер.
3.2 Методики
получения и исследования свойств образцов суспензий, носителей и катализаторов
3.2.1
Методика приготовления суспензии Al2O3-ZrO2
Приготовление суспензии из исходных материалов и реактивов
состоит из следующих операций:
подготовка исходных компонентов
активного оксида алюминия (γ-Al2O3)
и гидроксида алюминия посредством тонкого диспергирования на шаровой мельнице
до размера частиц 3-5 мкм;
оксид циркония реактивный, представляющий собой
тонкодисперсный порошок, и цирконила нитрат, представляющий собой
кристаллическую водорастворимую соль, используются в исходном виде и не требуют
специальной подготовки;
смешение Al2O3-, ZrO2-компонентов
с дистиллированной водой в заданном количестве (таблица) в ступке до полной
визуальной однородности и перенесение полученной смеси (около 200 см3)
в барабан емкостью 400 смі с предварительно загруженными мелющими телами
фарфоровыми шарами диаметром 10 мм общей массой 250 г;
шаровой помол суспензии 3 часа в фарфоровом барабане при 1,3
об /сек.;
измерение ρ суспензии после
трехчасового помола;
введение в суспензию воды и доведение ρ до заданного стабилизирующего систему значения;
дополнительное измельчение на шаровой мельнице 1 ч и контроль
ρ суспензии.
Для синтезированных суспензий, свежеприготовленных и в
процессе формирования на их основе образцов оксидных композитов, определялись
значения рН и плотности (ρ, г/см3) и
исследовались реологические характеристики в зависимости от этих показателей.
Регулирование рН и плотности суспензий до требуемых значений проводилось
добавлением рассчитанных количеств:
рН - (в зависимости от требуемого снижения или увеличения его
значения) - 10 н. азотной кислоты или 25% -го аммиака;
ρ - дистиллированной воды,
с последующим дополнительным 15-минутным перемешиванием на шаровой мельнице.
3.2.2
Методика формирования тонкослойного оксидного покрытия на пластинчатых
носителях
Для получения пластинчатых образцов алюмоциркониевых оксидных
носителей и катализаторов в качестве первичных металлических носителей
использовали плоскую и гофрированную ленты из фольги холоднокатанной стали
сплава Х23Ю5. Металлический носитель предварительно обезжиривали и оксидировали
(950 С в воздухе, 15 ч) до образования 0,5-1 % масс. поверхностного слоя оксида
алюминия, улучшающего адгезионное сцепление металла и наносимого впоследствии
оксидного слоя. Формирование тонкослойных (до 50 мкм) оксидных покрытий на
пластинах осуществлялось последовательным многократным выполнением операций
"нанесение суспензии - центрифугирование-сушка", а именно:
окунание пластины/блока в суспензию;
снятие излишков суспензии с поверхности пластины или из
каналов блока посредством центрифугирования;
закрепление тонкого слоя суспензии на поверхности
пластины/блока посредством отверждения термообработкой при 300 С.
Количество наслаиваемого оксидного композита контролируется
взвешиванием образцов после каждой операции; по достижении заданного привеса
образца (от 10 до 20 % масс, в зависимости от задания) пластину
термообрабатывают при заданной конечной температуре (600 С). Количество этих
операций (кратность) нанесения зависит от свойств суспензии, условий снятия излишков
и требуемой конечной толщины (или массы) покрытия. Выше сказанное выполняют
следующим образом.
Взвешивают исходный образец оксидированной пластины на
аналитических весах - mо, г. Наливают в стаканчик
суспензию "С" (предварительно перемешивают взбалтыванием). Опускают
пинцетом пластину в "С" на 50-60 с, передвигая ее в горизонтальной
плоскости, затем вынуть и дать стечь излишкам "С". Образцы пластины
помещают (до 4 шт.) вертикально в пластиковый стакан для центрифугирования.
Устанавливают в гнезда центрифуги попарно (напротив для уравновешивания)
стаканы с образцами. Если центрифугируется образец в одном стакане, то
противоположное гнездо должно быть уравновешено аналогичным грузом.
Центрифугируют образцы - 2 минуты, 600 об/мин. После полной остановки центрифуги,
вынимают стаканы, достают образцы и размещают их равномерно на поддоне для
термообработки помещают на 30 минут в муфельную печь, предварительно разогретую
до 300 С. Печь - в вытяжном шкафу.
По истечении 30 минут вынимают поддон с образцами, охлаждают
на воздухе до комнатной температуры. Взвешивают образец пластины или блока на
аналитических весах - mп, илиm1, m2,
г и т.д. "С" наносят многократно повторением до достижения
увеличения массы образца на 10-20%: (mi - mо) 100/mо,
% масс. После этого образец прокаливают в муфельной печи
при 600 С в течение 60 мин, после чего охлаждают на воздухе и взвешивают - mн,
г (окончательное количество вторичного носителя на образце).
3.2.3
Методики исследования свойств синтезированных образцов
3.2.3.1
Свойства покрывных суспензий
Значения рН определяли с использованием прибора рН -
метр/иономер ИПЛ-201 со стеклянным электродом ЭСЛ 43-07." при 20+0,5 С,
помещая электроды "стеклянный" и "вспомогательный-КС1" в
суспензию, налитую в стеклянный стаканчик (с последовательной тщательной
отмывкой поверхности электродов дистиллированной водой.
Плотность суспензии ρ, г/см3 - определяли как частное от деления массы
на объем пробы суспензии при 20+0,5 С, используя калиброванный шприц
медицинский с известным объемом заполнения 10 см3 и массой
(аналитические весы); при заполнении шприца обеспечивалось отсутствие пузырьков
воздуха в объеме суспензии;
Плотность суспензии вычисляется по формуле (1):
Р=m1-m2/V, (1)
где: m1 - масса шприца с суспензией,
г;
m2 - масса сухого шприца, г;
V - объем суспензии в шприце, см3;
Р - плотность суспензии, г.
Реологические характеристики покрывных суспензий
Определение реологических характеристик - вязкости η и скорости сдвига Dr в зависимости
от сдвигающего напряжения F - ведут с помощью ротационного вискозиметра
РЕОТЕСТ при помощи цилиндрических измерительных устройств. При этом измеряемый
материал (суспензия) помещается в кольцевую щель, образующуюся между двумя
коаксиальными цилиндрами.
Наружный, неподвижный цилиндр радиусом R выполнен в
качестве измерительной ёмкости. В него помещается измеряемый материал, а сам
цилиндр помещается с целью выдерживания определённой температуры в ёмкость с
термостатирующей жидкостью, подключаемую к жидкостному циркуляционному
термостату. Внутренний цилиндр радиусом r и длиной l, вращающийся со скоростью
вращения ω, соединён через измерительный вал с
цилиндрической винтовой пружиной, отклонение которой является мерой для
вращающего момента, действующего на внутренний цилиндр. Отклонение пружины
воспроизводится потенциометром, включённым в мостовую схему, причём изменение
тока, протекаемого по диагонали мостовой схемы, является пропорциональным
вращающему моменту M пружины.
Сдвигающее напряжение F и скорость сдвига D
поддаётся в случае коаксиальной цилиндрической системы точному расчёту. Обе
величины не являются постоянными для кольцевой цели. Поэтому нужно стараться
работать с отношением между радиусами, равным δ≤1,3 R/r, а вычисленные параметры F и D
переводятся на радиус r внутреннего цилиндра.
Сдвигающее напряжение:
=M/2 π/l/r2. (2)
Скорость сдвига:
Dr=2* ω*R2/ (R2-r2). (3)
Вязкость:
η= F/Dr. (4)
При проведении работы измеряется α, после чего рассчитывается F по формуле:
F = α*z. (5)
где α - отсчитываемое значение
шкалы на индикаторном приборе (дел. шкалы)
Таблица 1 - Коэффициенты насадок
|
Тип насадки
|
Коэффициент z
|
|
N
|
3,28
|
31,8
|
|
S1
|
5,81
|
56,3
|
|
H
|
27,5
|
267,3
|
3.2.3.2
Определение дисперсности порошка
Для проведения седиментационного анализа [10] взвешивают 1
грамм исследуемого порошка. Навеску переносят в фарфоровую ступку, туда же из
стакана добавляют небольшое количество дисперсионной среды (не более 5 мл).
Полученную таким образом пасту тщательно растирают в течение 2-3 минут, а затем
добавляют еще небольшое количество дисперсионной среды и аккуратно переносят
содержимое ступки в стакан с 1 дм3 дисперсионной среды. Затем суспензию
тщательно перемешивают в стакане, быстро вводят чашечку из фольги, подвешивая
ее на проволоку, сцепленной с измерителем массы. После дополнительного
перемешивания суспензии с помощью торсионных весов фиксируют изменение массы
чашечки по мере оседания на нее частиц дисперсионной фазы (исследуемого
образца).
Седиментационный анализ применяется для определения размеров
частиц в системах относительно низкой степени дисперсности (суспензия,
эмульсия).
Целью дисперсионного анализа является получение кривых
распределения, анализ которых позволяет установить, каково относительное
содержание частиц в заданных интервалах радиусов (фракционный состав системы).
Седиментационный анализ основан на зависимости размеров
частиц от скорости их оседания, выражающейся уравнением:
= (9*η*u/2/ Δρ /g) 0,5, (6)
где r - эквивалентный радиус частиц, нм;
η - вязкость среды, Па*с;
u - линейная скорость движения частиц, м/с;
Δρ - разность между
значениями плотностей дисперсной фазы и дисперсной среды, кг/м3;
g - ускорение силы тяжести, м/с2.
Так как для данной системы все величины, кроме скорости,
являются постоянными, то уравнение (7) можно представить в следующем виде:
= K*u0,5, (7)
где К= (9*η*u/2/ (D-d) /g) 0,5.
u = H/τ, (8)
где H-высота оседания частиц (высота химического
стакана или столба жидкости), м;
τ - время оседания частиц,
мин.
Определив экспериментально эти величины и рассчитав константу
Стокса, можно вычислить эквивалентные радиусы частиц, оседающих за те или иные
промежутки времени.
По полученным экспериментальным данным строится кривая
седиментации - зависимость веса седиментационного осадка Р от времени оседания τ. В реальных полидисперсных системах кривые имеют плавный ход и
приближаются к параболам. Полученную седиментационную кривую обрабатывают
графическим способом, то есть путем построения касательных в точках кривой,
соответствующих разным значениям времени оседания. В результате получают данные
для построения интегральной и дифференциальной гистограмм и кривых
распределения частиц по размерам [10].
Если к нескольким точкам на реальной седиментационной кривой,
соответствующим разному времени оседания (τ1, τ2, τ3…. τmax), провести касательные,
они отсекут на оси ординат отрезки, равные весу фракций, оседающих за
соответствующие промежутки времени: Р1 - за время τ1, Р2 - за время τ2,…. Рmax - за
время τmax, то есть Рmax - максимальный вес седиментационного осадка за все
время оседания.
Значение Рmax получается тогда, когда седиментационный
анализ доведен до конца, то есть когда осели частицы самых малых размеров. Если
в системе содержатся очень мелкие частицы, анализ не всегда удается довести до
конца (время оседания мелких частиц весьма велико, а прибавление осадка
ничтожно). В этих случаях предел, к которому стремится кривая седиментации
(Рmax), находят аналитическим путем. Один из таких путей описан в.
Зная вес частиц отдельных фракций, а также общий вес
седиментационного осадка (Рmax), можно определить процентное содержание
отдельных фракций
= P/Pmax*100, (8)
где Q-процентное содержание фракции;
Р - вес фракции, мг;
Рmax - общий вес седиментационного осадка, мг.
Очевидно, что Q1+Q2+ …+Qn = 100%, так как Р1+Р2+…+Рn = Рmax. По полученным
данным строят интегральную (суммарную) кривую, для чего на оси абсцисс
откладывают значения эквивалентных радиусов, начиная с самых мелких частиц, а
на оси ординат - нарастающее суммарное процентное содержание всех частиц от
наименьшего до данного радиуса включительно, относя его к наибольшему в данной
фракции радиусу.
Величину эквивалентного радиуса, соответствующего наиболее
часто встречающемуся размеру частиц в данной системе, находят из
дифференциальной кривой распределения, для построения которой обрабатывают
интегральную кривую следующим образом: через равные интервалы радиусов, которые
выбираются произвольно (в нашем случае 1 мк), строят координаты до пересечения
с интегральной кривой, сносят эти точки на ось ординат и находят значения ∆Q
- разности между двумя соседними ординатами. Затем, откладывая на оси абсцисс
значения эквивалентных радиусовr, а по оси ординат ∆Q/∆r, строят
прямоугольники, беря за основание равные интервалы радиусов ∆r, а затем
высоту - ∆Q/∆r, соответствующую данному радиусу r.
Соединив плавной кривой середины верхних оснований
прямоугольников, получают дифференциальную кривую распределения, по которой
можно определить rmax-радиус частиц, которых больше всего в данной дисперсной
системе.
Площадь каждого прямоугольника представляет собой процентное
содержание фракции с определенным интервалом размера частиц. Площадь фигуры,
описываемой кривой, должна быть равна сумме площадей всех прямоугольников.
3.2.3.3
Структурно-прочностные характеристики оксидных композитов
Для определения параметров пористой структуры и прочностных
свойств тонкослойных пористых оксидных покрытий использовали образцы оксидных
композитов, полученных отверждением соответствующих образцов суспензий в
условиях, аналогичных отверждению в тонком слое, за исключением его толщины, а
именно, соответствующую покрывную суспензию выливали в поддон слоем 10 мм,
высушивали на воздухе при комнатных условиях с образованием зерен двумя
способами:
сушили до приобретения твердости, а затем дробили на зерна
размером около 2 мм или мм;
сушили до состояния пасты, а затем вмазывали в грануляторные
доски и досушивали в них при комнатных условиях с последующим вытряхиванием из
досок цилиндрических гранул диаметром 2 мм;
Зерна на поддонах термообрабатывали последовательно в
сушильном шкафу и муфельной печи:
-120 С 2 ч,
-660 С 2 ч.
Определение удельной поверхности Sуд,
м2/г
Удельная поверхность - межфазная поверхность, приходящаяся на
единицу объема дисперсной фазы. Чем меньше размеры частиц, тем больше удельная
поверхность, и наоборот.
Установка предназначена для определения удельной поверхности
дисперсных и пористых тел методом тепловой десорбции аргона [24]. Метод
тепловой десорбции аргона основан на способности дисперсных и пористых тел к
монослойной адсорбции аргона при температуре жидкого азота и с последующей его
десорбцией при комнатной температуре. При проведении адсорбции аргона из
газовой смеси с гелием и его десорбции количество адсорбированного и
десорбированного аргона определяется хроматографическими методами и фиксируется
на диаграмме самопишущего прибора в виде хроматографических пиков, площади
которых пропорциональны количествам адсорбированного и десорбированного аргона,
а также непосредственно величинам удельной поверхности исследуемых образцов.
Калибровочный коэффициент рассчитываем по формуле:
= mэт *57/ Sпика эт, (9)
где K - калибровочный коэффициент;
57 - удельная поверхность эталона, м2/г;
m - масса эталона, г;
Sпика эт - площадь пика эталона
(калибровочного пика), м2.
После этого рассчитываем удельную поверхность образца по
формуле:
уд=K*Sпика обр/ mобр,
(10)
где Sуд - удельная поверхность
образца, м2/г;
K - калибровочный коэффициент;
Sпика обр - площадь пика образца, м2;
mобр - масса образца, г.
Величина погрешности определения удельной поверхности
хроматографическим методом не превышает ±5%
Суммарный объем пор V∑, см3/г
Определение ведут с двумя параллельными
навесками. Берут около 1,5 г. навески и помещают в колбу. Носитель заливают
водой и кипятят 20 мин на электрической плитке. Воду сливают и извлекают
навеску, затем с помощью фильтровальной бумаги убирают избыток влаги с навески
и взвешивают ее. Затем взвешенную навеску ставят в электрическую печь и сушат 2
часа при температуре 2000С и снова взвешивают. Объем пор
рассчитывают по формуле:
= (m2-m1)
/m1 или V=100 (m2-m1) /m1, (11)
где V - суммарный объем пор, см3/г
или %;
m1-масса сухой навески, г.
m2-масса навески с порами,
заполненными водой, г.
Объем пор рассчитывают как среднее
арифметическое двух определений.
Механическая прочность гранул носителя,
катализатора
Определение ведут на приборе МП-2С. Определение разрушающего
усилия на приборе производится посредством пружинного силоизмерителя. Прибор
охватывает усилия от 5 г до 100 кг. Обеспечивает постоянную скорость нагружения
образцов.
Из пробы образцов отбирают по 26 грунул с равными торцевыми
поверхностями. Раздавливание производим при горизонтальном положении гранул (по
образующей), когда усилие направлено перпендикулярно оси образца и раскалывание
происходит в вертикальной плоскости, и при вертикальном положении гранул (по
торцу). Для этого гранулу ставим в центр столика прибора, затем вращением
маховика производим постепенный нажим на гранулу. Одновременно следим за
стрелкой манометра.
Прочность катализатора характеризуют индексом механической
прочности. Его получают делением значения раздавливающего усилия на площадь
минимального поперечного сечения гранулы. Среднее значение индекса вычисляют
как среднеарифметическое из измерения прочности 20 гранул (три наибольших и три
наименьших значения отбрасываем).
Прочность образцов по образующей находим по формуле:
0= F*0,03/h*d, (12)
где P0 - прочность образца, кг/см2;
F - среднее разрушающее усилие образцов, дел;
h - высота гранулы, см;
d - диаметр гранулы, см;
0.03 - калибровочный коэффициент прибора, кг/дел.
Прочность образцов по торцу находим по формуле:
п= F*0,03/π*r2, (13)
где PΠ - прочность образца,
кг/см2.
Механическая прочность тонкослойных оксидных
покрытий
Пластинка с нанесённой суспензией
помещается в чашку Петри типа ЧБН d=100 мм, засыпается 25 смі сухого песка с
фракцией 0.5-2 мм и прикрывается другой чашкой. Чашки упаковываются в пакет,
чтобы при проведении исследования не повредить посуду.
Прочность держания суспензии на пластинке, определялась с
помощью прибора, который работает следующим образом:
горизонтально-колебательное движение от эксцентрика, вращаемого
электродвигателем через зубчатую передачу. На средней части шатуна расположен
диск, который предназначен для установки набора ячеек (в которые укладываются
упакованные пластинки). Диск, встречая сопротивление упора, поворачивается за
каждый ход шатуна на определённый угол; скоба, укреплённая на подвижной стойке
и соединенная с помощью пружин с неподвижными стойками, ударяет бойками по
набору ячеек, в результате чего происходит истирание суспензии песком.
Прочность рассчитывалась по формуле (17):
и = (P2 - Р0) / (Р1
- Р0) *100, (14)
где Р1 - вес пластинки с нанесённой
суспензией, г;
Р0 - вес исходной пластинки, г;
Р2 - вес пластинки с нанесённой суспензией
после обработки песком, г.
3.2.4
Рентгенофазовый анализ синтезированных образцов
Во многих природных и синтезированных, технически важных
материалах кристаллическое вещество находится в виде поликристалла и важно
иметь возможность изучить его структуру и свойства именно в таком состоянии.
Поликристаллический материал состоит из множества мелких кристалликов. Это
может быть или агрегат плотно сцепленных между собой мелких кристаллов
(например, металлы, сплавы, многие минералы, керамические материалы), или
измельченный порошок данного вещества. Поликристаллическое вещество может
состоять из кристалликов различных фаз.
Наиболее полно рентгеновские данные приведены в порошковой
рентгенометрической картотеке (ASTM), издаваемой Объединенным комитетом по
порошковым дифракционным стандартам. В настоящее время в этой картотеке
приведены данные более чем на 40000 неорганических соединений. Существует
несколько разработок информационных систем на основе ЭВМ для автоматического
проведения качественного фазового анализа
Сущность метода рентгеновского фазового анализа [24]
В методе РФА используется явление дифракции рентгеновских
лучей на кристаллической решетке, применяется излучение с длиной волны λ порядка величины межатомных расстояний в кристалле. Если любая
точка (узел) кристаллической решетки способна рассеивать падающее рентгеновское
излучение, то при определенных условиях между волнами, рассеянными отдельными
электронами за счет разнести фаз, возникает суммарная амплитуда рассеяния
атомами. При этом считается, что:
электроны атома рассеиваются как свободные электроны, т.е.
связь с ядром слабая;
период движения электрона по орбите намного больше периода
колебаний падающего излучения, т.е. рассеяние происходит на неподвижном
электроне.
Рентгенограмма многофазной системы представляет собой
результат наложения линий различных фаз. Определение фазового состава изучаемого
вещества производят путем сравнения экспериментального набора значений 2, (dhkl
l) и I/Iо, найденных из рентгеновских спектров, с табличными
значениями dhkl и I/Iо, которые представлены в картотеке
ASTM.
Прежде чем приступить к поиску и идентификации фаз, нужно
определить, с группой соединений какого элемента начать поиск. Для этого
необходимо знать, с каким материалом проводят исследование, иметь данные о
химическом составе, условиях получения, легирующих элементах, режиме
термообработки и т.д.
Поиск и идентификация фаз начинается с самой сильной линии
рентгенограммы. Определив предположительно принадлежность ее к какой-то
определенной фазе (по совпадению межплоскостного расстояния), определяют
принадлежность к этой фазе других линий рентгенограммы путем сравнения с
табличными данными. Анализ ведут по мере уменьшения интенсивности линии. Если
межплоскостные расстояния совпадают и соотношения интенсивностей для
исследуемой и табличной рентгенограмм пропорциональны, значит фаза
идентифицирована верно. Точно так же поступают с остальными линиями
рентгенограммы.
Вещество может быть принято в качестве вероятной фазы, если
его наиболее сильные линии совпали с линиями образца. Различия в измеренных и
табличных межплоскостных расстояниях (за пределами ошибки) могут быть
следствием отклонения состава от стехиометрического, образованием твердого
раствора на основе данного соединения и т.д. Допустимые в таких случаях
различия между dhkl исследователь устанавливает на основе
дополнительных данных или кристаллохимических расчетов.
3.2.5
ИК-спектроскопия образцов оксидных композитов
В этом методе используется явление специфического поглощения
веществами ИК - излучения волн определенных длин. Поглощение излучения,
проходящего через исследуемое вещество, записывают с помощью ИК -
спектрофотометра в виде графика, отображающего зависимость степени поглощения
от длины волны. Измерения обычно проводят в диапазоне 2,5-16 мкм или 4000-625
см-1. Фиксируемые в ИК - спектрах полосы поглощения обусловлены
переходами между колебательными энергетическими уровнями в молекулах вещества.
Положение полосы в ИК - спектре определяется в основном типом связи и массой
колеблющихся групп: чем сильнее связь и меньше масса атомов, тем выше частота
поглощения данной связи. Колебания связанных атомов в молекулах подразделяют на
два основных типа: валентные и деформационные [24].
Полосы поглощения, обусловленные определенными группами
атомов, называются характеристическими; они используются для идентификации этих
групп в исследуемых соединениях. По набору характеристических полос колебаний в
ИК - спектрах с помощью специальных таблиц можно определить наличие в веществе
различных химических групп.
Процедура анализа методом ИК - спектроскопии проста и не
занимает много времени.
Метод ИК - спектроскопии позволяет идентифицировать вещества
с аморфной или слабо выраженной кристаллической структурой.
ИК-спектроскопия позволяет выявить определенные
функциональные группы, а не их количество в соединении и способ связи друг с
другом. Для исследования образцов использовали ИК-спектрометр с фурье -
преобразованием модели "ФСМ 1202" фирмы Мониторинг. Возможности
прибора позволяют проводить сканирование в широком диапазоне (400-4000 см-1)
ИК - спектра с малым шагом сканирования.
Для исследования берут твердые образцы, измельчают, смешивают
с порошком КВr и прессуют таблетки при давлении 3000 бар. Мешающее влияние
воздуха устранили вакуумированием прибора. Анализируют предварительно
высушенные образцы, так как вода сильно поглощает излучение с длиной волны более
1,5 мкм. Присутствие воды в веществе может сильно исказить его истинный спектр
и затруднить идентификацию в нем компонентов и химических групп. Кроме того,
вода воздействует на материалы, из которых обычно изготовляют кюветы (NaCl, КВг
и др.), а также на КВг, применяемый для приготовления таблеток. Применение
специальной микроскопической техники позволяет работать с объектами очень малых
размеров (доли мм).
3.2.6
Методики исследования каталитических свойств образцов
3.2.6.1
Исследования образцов катализаторов в реакции окисления СО
Определение каталитической активности образцов катализаторов
в реакции окисления оксида углерода проводилось на динамической проточной
установке, схема которой представлена на рисунке 5 [25].
Условия проведения испытаний.
а) объемная скорость газовоздушного потока 1л/мин;
б) температура 20-500оС;
в) концентрация оксида углерода исходная: 0.6-0.7% об.;
г) влажность ГВП исходная: 30-40% отн. (прив. к 200С).
Воздух подают в систему микрокомпрессором
3, снабженным распределителем 4 и зажимом для регулировки расхода и сброса
избыточного давления.
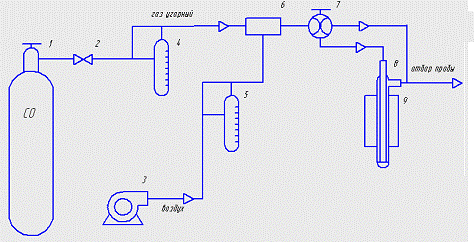
Рисунок 5 - Схема установки для определения каталитической
активности образцов по монооксиду углерода 1 - баллон с СО; 2 - реометр; 3 -
микрокомпрессор; 4 - распределитель 3-х ходовой; 5 - смеситель; 6 - ротаметр; 7
- четырехходовой кран; 8 - металлический трубчатый реактор; 9 - трубчатая печь
Оксид углерода подают из баллона 1,
регулировку осуществляют вентилем редуктора. Для индикации расхода оксид углерода
служит реометр 2. Газовые потоки смешиваются в смесителе 5. Для измерения
общего расхода потока используют ротаметр 6.
Поток после ротаметра 6 четырехходовым
краном 7 направляют на "выход" - для отбора проб потока и определения
исходной концентрации оксида углерода либо в помещенный в нагревательное
устройство 9 стеклянный трубчатый реактор 8 с катализатором и далее - на отбор
проб потока для определения "проскоковой" концентрации оксида
углерода.
Отбор проб производят в стеклянные шприцы,
для определения количества оксида углерода в газовом потоке применяют методику
АЮВ 0.005.104. МВИ, базирующуюся на методе реакционной газовой хроматографии.
Температуру регулируют с помощью ЛАТРа, контролируют с помощью термопары,
закрепленной у слоя катализатора, и прибора типа КВП.
Расчет степени окисления СО проводится по
формуле:
СО=100 (Сисх-Ск)
/Сисх, (15)
где: Сисх - концентрация
СО в ГВП исходная, % об.;
Ск - концентрация СО в ГВП
на выходе из реактора, % об.;
ХСО - степень окисления СО,
%;
Определение оксида и
диоксида углерода методом реакционной газовой хроматографии [26].
Для определения содержания оксида углерода в ГВП на входе и
выходе из реактора диапазоне 3-12000 мг/м3 (0.00025-1% об.), и СО2
185-46200мг/м3 (0.001-2.5% об.) при их одновременном присутствии,
использовали методику предназначенную для измерений массовых концентраций.
Определение основано на применении метода реакционной газовой
хроматографии, включающего предварительное разделение метана, оксида и диоксида
углерода. При помощи газоадсорбционной хроматографии с последующей конверсией
разделенных оксидов углерода в метан в присутствии никелевого катализатора и
водорода. Детектирование осуществляется пламенно-ионизационным детектором
(ПИД).
Метод реакционной газовой хроматографии является наиболее
чувствительным при определении оксидов углерода в воздухе. Определению не
мешают другие соединения присутствующие в пробе. целью упрощения газовой схемы
хроматографа используется водород, как для питания (ПИД) и метанирования, так и
в качестве газа-носителя. Электрический сигнал детектора записывается на
диаграммной ленте потенциометра КСП-4 в виде хроматографического пика, высота
которого пропорциональна количеству вещества пропущенного через ПИД.
Условия выполнения измерений:
а) температура термостата колонок - 80оС;
б) температура испарителя - 150оС;
в) температура термостата реактора - 300оС;
г) объемная скорость газа-носителя водорода - 30 см3/мин;
д) объемная скорость воздуха - 300см3/мин;
е) скорость движения диаграммной ленты - 240мм/час;
ж) объемная скорость пробы через кран-дозатор - 100см3/мин;
з) время продувки крана-дозатора - 1мин;
и) объем дозы крана-дозатора - 1см3.
Условия окружающей среды:
а) температура окружающей среды от +10 до +40оС;
б) атмосферное давление от 100*103 до 105*103
Па;
в) относительная влажность воздуха от 20 до 90%.
Отбор проб.
Пробу воздуха отбирают при помощи стеклянного шприца на
50-150 см3, предварительно промыв шприц исследуемым воздухом. После
отбора пробы шприц закрывают заглушкой. Пробу воздуха из шприца продавливают
через дозирующую петлю хроматографа в течении 1-2 минут. Затем краном-дозатором
вводят пробу в хроматографическую колонку и включают одновременно секундомер.
Фиксируют время выхода пиков оксида и диоксида углерода, которые в данных
условиях составляют соответственно 58 секунд и 5 минут 10 секунд. На
диаграммной ленте записывают дату и время начала опыта, чувствительность
хроматографа.
Методика обеспечивает выполнение измерений с относительной
погрешностью +/ - 25% при доверительной вероятности 0.95.
3.2.6.2
Исследование образцов катализаторов в реакции окисления водорода
Активность синтезированных образцов катализатора определялась
на проточной установке, схема которой приведена на рисунке 6 [27].
Из баллона 1 окись углерода, расход которой регулируется
запорным краном 2 и измеряется реометром 4 в соответствии с калибровкой
капилляра, поступает в смеситель 6, куда одновременно подается воздух из
воздуходувки 3. Расход воздуха регулируется и измеряется реометром 5 в
соответствии с калибровкой капилляра. Смесь газов после смесителя проходит
через четырехходовой кран и поступает в реактор 8, помещенный в печь 9. При
положении четырехходового крана в обход реактора отбирается проба газовой смеси
на хроматографический анализ исходной концентрации окиси водорода. При
положении четырехходового крана через реактор отбирается проба газовой смеси на
хроматографический анализ проскоковой концентрации Н2.
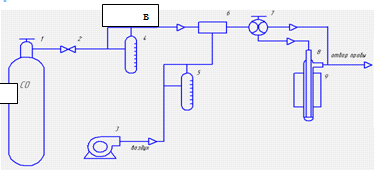
Рисунок 6 - Схема установки для определения активности
катализаторов окисления водорода: 1 - баллон с водородом; 2 - кран запорный; 3
- воздуходувка, 4, 5 - реометры для водорода и воздуха, соответственно; 6 -
смеситель водорода и воздуха; 7 - кран четырехходовой; 8 - реактор, 9 - печь
реактора
Условия проведения испытаний:
а) объемная скорость - 0,2 л/мин;
б) концентрация водорода - 2,5-3% об.;
в) температура - 20-4000С;
г) влажность ГВП исходная: 30-40% отн. (прив. к 200С).
Определение концентрации Н2 в воздухе
методом реакционной газовой хроматографии
Определение концентрации водорода в
газовоздушной смеси проводили с использованием газохроматографического метода
анализа по методике АЮВ.2.840.033 МВИ с диапазоном измеряемых концентраций0,01
- 10% об.
Хроматографический метод анализа [28]
основан на различном времени удержания насадкой (сорбентом) хроматографических
колонок различных газов (и паров). В связи с этим скорость продвижения газов по
делительной колонкеи их поступление в детектор по теплопроводности (ДТП)
различны [19]. Электрический сигнал с ДТП хроматографа является результатом
разбаланса его мостовой схемы в момент прохождения через ДТП анализируемого
газа в смеси с газом-носителем (аргоном). При анализе газовоздушной смеси
"водород + воздух" в качестве газа - носителяиспользуется аргон.
Электрический сигнал с ДТП хроматографапоступает
на регистрирующий прибор - КСП-4, на диаграммнойленте которого
вычерчивается кривая, площадьпод которой (Sпик, мм2)
пропорциональна количеству газа, прошедшего через ДТП.
Зависимость площади под кривой на
диаграммной ленте от содержания в смеси водорода определяют градуировкой
хроматографа по газовой смеси: аргон - водород на основании результатов
градуировки.
На полученных хроматограммах измеряют
значения Sпик i. Концентрацию веществ в воздухе (С, % об.)
определяют по градуировочному графику или вычисляют по формуле;
С = КSпик i, (16)
где: К - градуировочный
коэффициент,
Sпик i., - приведенное значение
площади пика.
Расчет степени окисления водорода XH2
образцами катализатора проводился по формуле:
ХН2=100 (Сисх-Ск)
/Сисх (17)
где: ХН2 - степень
окисления Н2, %;
Сисх - концентрация Н2
в ГВП исходная, % об.;
Ск - концентрация СО в ГВП
на выходе из реактора, % об.;
3.3
Исследование влияния условий механохимического синтеза на свойства покрывных
суспензий
Для обоснования условий синтеза покрывных суспензий важным
является определение их реологических характеристик во взаимосвязи с такими
параметрами как: компонентный состав дисперсной фазы и
соединений-предшественников, использованных для его обеспечения; качественный и
количественный состав дисперсионной среды, суммарными показателями которых
являются рН и плотность суспензии.
Характеристикой реологических характеристик покрывных
суспензий являются реологические кривые - зависимости значений эффективной
вязкости и скорости сдвига от прилагаемых нагрузок, определяемые с
использованием прибора РЕОТЕСТ.
При сравнении этих величин следует учитывать, что при
центрифугировании пропитанных пластинчатых слои суспензии на их поверхности
испытывают воздействие нагрузок, близких к 20 Па.
Таблица 2 - Состав и условия получения базовой суспензии
|
Компоненты суспензии
|
Количество, вносимое в суспензию, г
|
Условия МХ синтеза
|
|
Al2O3
|
226.2
|
Исходные оксиды: Al2O3 -
12 ч ШП ZrO2 - 12 ч ШП Пб - 3 ч ШП Связующее: (Пб+Al (NO3)
3) - 3ч ШП Суспензия: (Смесь сухих порошков + Н2О) - 3
ч ШП ШП - измельчение в на шаровой мельнице при 70 об/мин.
|
|
ZrO2
|
440
|
|
|
Zr (NO3) 2 * 6H2O
|
106.1
|
|
|
Связующее: Пб - А1ООН Al (NO3) 3*9H2O
|
200,5 131,7
|
|
|
Н2О
|
1,4 дм3
|
|
3.4 Выбор
условий получения базовых покрывных суспензий
Выбор условий синтеза покрывных суспензий для формирования на
металлических пластинчатых носителях прочных и пористых оксидных
алюмоциркониевых покрытий проводили с использованием результатов
предварительных исследований, целью которых было установление влияния плотности
наносимой суспензии на качество покрытия. Для этого была использована суспензия
Аl2O3: ZrO2 (из нитрата цирконила) =50: 50 с
рН=2 (добавление аммиака) с ее разбавлением водой до различной плотности
1,3-1,2-1,1. Для этих образцов суспензии были определены реологические
характеристики и проведены пробные нанесения покрытий на пластинчатые носители.
Результаты приведены на рисунке 7.
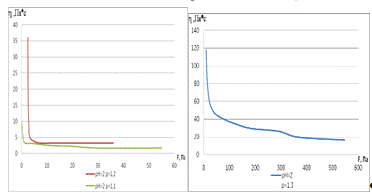
Рисунок 7 - Зависимость значений эффективной вязкости от
прилагаемой нагрузки для образцов покрывной суспензии Аl2O3:
ZrO2 (из нитрата цирконила) =50: 50 с рН=2 и плотностями 1.3-1,1
г/см3
Характер кривых свидетельствует, что с разбавлением суспензии
1,3 г/см3 до плотности 1,2 и еще в большей мере - до 1,1 г/см3 значение
прилагаемой нагрузки, вызывающей разрушение структурированной коллоидоподобной
системы, резко снижается. При сравнении этих величин следует учитывать, что при
центрифугировании пропитанных пластин слои суспензии на их поверхности
испытывают воздействие нагрузок, превышающих 100 Па. Если в случае
неразбавленной суспензии начало разрушения структурированности суспензии
соответствует нагрузке более 70 Па, то для суспензии с 1,3 г/см3 эта
нагрузка уже менее 30 Па, для суспензии плотностью 1, г/см3 нагрузка 4 Па, а
для 1,11 г/см3 - даже менее 2 Па. При этом величины эффективной вязкости,
соответствующие этим нагрузкам, также различны, а именно: 60; 5; 3 Пас. На
рисунке 8 приведены реологические кривые, определенные для суспензии различной
степени разбавления дистиллированной водой, - от исходной плотности 1,3 г/см3
до ее значений 1,2, 1,1 г/см3 при одинаковых значениях рН=2.
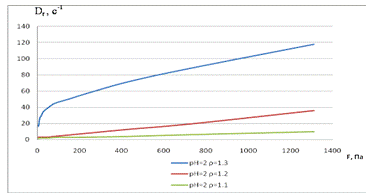
Рисунок 8 - Изменение кривой течения суспензии с рН=3 в
зависимости от ее разбавления
В случае рН=3,0 для всех образцов покрывной суспензии
(плотность 1,3-1,2-1,1 г/см3) увеличение прилагаемой нагрузки в начальный
период приводит к росту значений эффективной вязкости с последующим достаточно
быстрым ее выходом на мало изменяющийся уровень; скорость сдвига при этом в исследуемом
интервале нагрузок монотонно возрастает.
Количественная оценка оксидного слоя, сформированного за 1
операцию "нанесение-центрифугирование-сушка" показала увеличение его
массы с ростом плотности суспензии: от 0,8 до 2,2 и 3,6 % масс. для трех образцов
суспензии, соответственно (1,1-1,2 и 1,3 г/см3).
По результатам определения механической прочности оксидного
композита в виде тонкослойного покрытия (прочность на истирание) и в виде
гранул (прочность на раздавливание) и на основании реологических характеристик
(рисунки 7 и 8) была выбрана для дальнейшей работы суспензия с плотность 1,2 г/
см3, как обеспечивающая формирование равномерного и прочного
покрытия и оксидного композита с более высокой когезионной прочностью.
Таблица 3 - Характеристика оксидных композитов, полученных в
виде тонкослойных покрытий и гранул из суспензии с различной плотностью
|
Пластины
|
Гранулы
|
|
Образец
|
pH
|
ρ, г/см3
|
Оксидное покрытие, % масс.
|
Нанесение за один слой, % масс.
|
Пистирание, %
|
Прочность на раздавливание, МПа
|
|
|
|
|
|
|
по торцу
|
по образующей
|
|
1
|
2,0
|
1,3
|
11,7
|
3,6
|
90
|
10,9
|
5,3
|
|
2
|
2,0
|
1,2
|
11,5
|
2,2
|
92
|
14,9
|
6,3
|
|
3
|
2,0
|
1,1
|
11,9
|
0,8
|
91
|
12,4
|
4,8
|
3.5 Влияние
продолжительности измельчения на свойства покрывных суспензий
Была использована суспензия Аl2O3: ZrO2
(из нитрата цирконила) =50: 50 с рН=3 (добавление аммиака) с ее разбавлением
водой до плотности 1,3г/см3. Производилось измельчение мелющими
телами в барабане в течении 3, 6 и 10 часов. Данные о реологических
характеристиках суспензий представлены и на рисунке 9 и 10.
Приведенные на рисунке 9 и 10 реологические кривые
показывают, что начало разрушения суспензии различной продолжительности
соответствует нагрузке менее 10 Па для всех трех образцов.
При этом величины эффективной вязкости, соответствующие этим
нагрузкам, также близки, а именно: 50; 45; 50 Пас. В данном случае скорость
сдвига в исследуемом интервале нагрузок резко возрастает. Кривые течения
суспензий, полученных при различной продолжительности измельчения, мало
отличаются друг от друга.
Соответственно практически не отличаются как количественные
показатели нанесения суспензии (4,5-4,7 % масс. за 1 операцию), так и значения
оксидного слоя, прочности сформированного на поверхности пластины.

Рисунок 9 - Зависимость значений эффективной вязкости от
прилагаемой нагрузки для образцов покрывной суспензии Аl2O3:
ZrO2 (из нитрата цирконила) =50: 50 с различной продолжительностью
измельчения
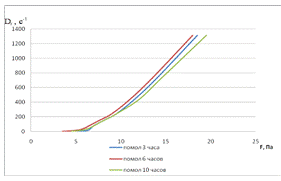
Рисунок 10 - Изменение кривой течения суспензии с различной
продолжительностью измельчения
Таблица 4 - Влияние продолжительности измельчения при синтезе
суспензии на механическую прочность оксидного композита
|
Пластины
|
Гранулы
|
|
Образец
|
Продолжительность, τ, час
|
pH
|
ρ, г/см3
|
Оксидное покрытие, % масс.
|
Пистирание., %
|
Sуд, м2/г
|
|
4
|
3
|
3,05
|
1,3
|
4,5
|
96
|
106
|
|
5
|
6
|
3,15
|
1,3
|
4,7
|
96
|
115
|
|
6
|
10
|
3,10
|
1,3
|
4,6
|
95
|
119
|

Рисунок 11 - Дифференциальные кривые распределения частиц
дисперсной фазы суспензии (рН=3 и ρ=1,3 г/см3) по их
эквивалентным радиусам при различной продолжительности измельчения
Вид дифференциальных кривых, рассчитанных по результатам
седиментационного анализа суспензий различной продолжительности измельчения,
свидетельствует о преобладании в их дисперсной фазе частиц размером менее 1
мкм.
На основании полученных результатов выбрана продолжительность
измельчения суспензии при ее синтезе, равная 3 часам как достаточная для
обеспечения высокой дисперсности частиц оксидной составляющей и стабильных
значений рН и реологических характеристик структурированной системы, что
обеспечивает высокую механическую прочность покрытия.
3.6
Приготовление и исследование образцов катализаторов
В качестве покрывной суспензии был выбран образец 50% ZrO2-50%
Al2O3 pH=3 ρ=1.2 Получение образцов
катализатора проводилось для композитов как в виде гранул, так и для
тонкослойных покрытий на пластинах плоских и гофрированных. Компоновкой
последних предполагалось сформировать элемент микроканального реактора.
В качестве предшественника каталитически активного
компонента, вносимого непосредственно в суспензию, использованы:
никель углекислый (II) основной водный NiCO3* mNi
(OH)2*nH2O, содержание никеля в котором в пересчете на
NiO составляет 45 % масс.
никель азотнокислый, гексогидрат Ni (NO3)2.6H2O
Были получены по три образца гранулированного и пластинчатого
катализатора, приготовленные различным способами внесения активного компонента:
внесение в исходную суспензию NiCO3* mNi (OH) 2*nH2O;
внесение в исходную суспензию Ni (NO3) 2*
6H2O;
пропитка отвержденных гранул раствором Ni (NO3) 2*
6H2O.
Количество вносимого в суспензию карбоната никеля было рассчитано,
исходя из заданного содержания в готовом катализаторе 7% масс. NiO. Вносимый в
суспензию порошок карбоната был предварительно был измельчен в шаровой мельнице
в течение 24 часов до преобладающего радиуса частиц 1,4 мкм. После внесения
порошкаNiCO3* mNi (OH) 2*nH2O в суспензию
полученная композиция гомогенизировалась в барабане с мелющими телами при
скорости вращения 4200 об/ч в течение 0,5 ч. При этом корректировалось значение
рН до 3,0 добавлением азотной кислоты.
Количество вносимого в суспензию гексогидрата рассчитывалось,
исходя из данных по твердому остатку Al2O3; таким образом
в катализаторе содержание NiO составило также 7%. Гексогидрат Ni (NO3)
2*6H2O - зеленые кристаллы триклинной сингонии. Температура
плавления 54°С; (плотность 2,04 г/см3; C0p 462,3 Дж/моль*К)
При нагревании гидраты никеля нитрата вначале частично
дегидратируются, выше 150°С разлагаются с образованием гидроксосолей
переменного состава, конечный продукт разложения-NiOx; в справочной литературе
[29] указывается температура разложения нитрата никеля до NiO - выше 500 С.
Нанесение приготовленных суспензий, содержащих соли никеля,
на пластины проводили аналогично формированию оксидных алюмоциркониевых
покрытий по следующим многократным операциям: - нанесение суспензии - центрифугирование
- сушка при указанных выше условиях.
После нанесения заданного количества композиции образцы
пластин термообрабатывали при 600 С.
Результаты исследования свойств образцов покрытий и гранул
катализатора, полученных из синтезированных суспензий, приведены в таблице 5.
При использовании в качестве первичного носителя
гофрированных пластин по сравнению с плоскими формируется при прочих равных
условиях слой меньшей толщины, что связано с увеличением в гофрированных
каналах (по сравнению с плоскими) центобежного усилия, удаляющего излишки
суспензии при центрифугировании. При этом для данной суспензии за одну операцию
нанесения увеличение массы в среднем составляет 1,5/2,1 % масс.
(гофрированная/плоская) при введении карбоната никеля и 1,4/1,9 % масс. (гофрированная/плоская)
- нитрата никеля.
Величины механической прочности покрытия пластин и гранул, а
также удельной поверхности образцов катализаторов, полученных при использовании
в качестве соединений предшественников - нитрата или карбоната никеля, при прочих
равных условиях (введение их в состав суспензии, содержание NiO - 7 % масс.)
практически не отличаются друг от друга и свидетельствуют об их развитой
пористой структуре и достаточно высокой прочности.
Таблица 5 - Свойства образцов катализаторов в виде пластин и
гранул
|
Покрытие
|
Гранулы
|
|
Образец носителя
|
Суспензия
|
Оксидное покрытие, % масс.
|
Нанесение за один слой, % масс.
|
Пистирание, %
|
Sуд, м2/г
|
Прочность на раздавливание, МПа
|
|
|
|
|
|
|
по торцу
|
по образующей
|
|
NiCO3* mNi (OH) 2*nH2O
|
|
Гофрированные
|
pH=3 ρ=1,2 г/см3
|
10,4
|
1,5
|
91
|
112
|
9,6
|
3,9
|
|
Плоские
|
|
14,9
|
2,1
|
88
|
|
|
|
|
Ni (NO3) 2* 6H2O
|
|
Гофрированные
|
pH=3 ρ=1,2 г/см3
|
10,5
|
1,4
|
92
|
90
|
8,4
|
5,0
|
|
Плоские
|
|
15
|
1.9
|
89
|
|
|
|
|
|
|
|
|
|
|
|
|
На рисунке 12 представлены микрофотографии образцов плоских
пластин с тонкослойным покрытием из катализатора, полученных введением в
покрывную суспензию а) карбоната никеля и б) нитрата никеля с одинаковым
содержанием активного компонента (прокаливания при 600 С - 7 % масс. NiO).
Внешний вид пластин с 7-кратным увеличением показал их схожесть и достаточную
равномерность, отсутствие видимых трещин и разрывов, сколов. Видно, что
покрытие сформировано из тонкодисперсных частиц микронных размеров.

а) б)
Рисунок 12 - Микрофотография образцов пластин с нанесенным NiCO3*
mNi (OH) 2*nH2O и Ni (NO3) 2* 6H2O
В таблице 7 приведены результаты оценки свойств образцов
катализатора, полученных в виде покрытия на плоских и гофрированных пластинах
методом нанесения ранее сформированного оксидного покрытия из избытка раствора
нитрата никеля с последующим прокаливанием при 600 С.
Таблица 6 - Свойства образца катализатора, полученного метом
пропитки пластин
|
Образец
|
pH
|
ρ, г/см3
|
Оксидное покрытие, % масс.
|
Пистирание, до про- пропитки, %
|
Влагоемкость пластин,
|
Пропитка %
|
Пистирание после пропитки,%
|
|
Гофрированные
|
2,0
|
1,2
|
11,5
|
91
|
0,55
|
12
|
90
|
|
2,0
|
1,2
|
20
|
83
|
0,41
|
8
|
83
|
|
Плоские
|
2,0
|
1,2
|
17,5
|
82
|
0,40
|
12
|
82
|
|
|
|
25
|
79
|
0,40
|
10
|
78
|
Данные таблицы 6 согласуются с ранее приведенными
результатами о том, при одинаковых условиях на плоских пластинах формируется
слой большей толщины, мало отличающийся от слоя на гофрированных пластинах по
показателям механической прочности. Примечательно, что после погружения
образцов в раствор нитрата никеля и последующего прокаливания прочность
покрытия не изменяется и составляет (83-90) % масс. у гофрированных образцов и
(78-82) % масс. у плоских.
Меньшие значения прочности на истирание - у пластин с большей
толщиной оксидного покрытия - как у гофрированных, так и у плоских пластин.
Образцы катализатора таблицы 6, полученные нанесением из
избытка раствора, содержат NiO в количестве, большем расчетного по их
влагоемкости, что свидетельствует о сорбции активного компонента на поверхности
пор оксидного композита.
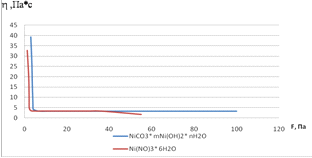
Рисунок 13 - Зависимость значений эффективной вязкости от
прилагаемой нагрузки для суспензий с внесенными карбонатом и нитрата никеля
Вид реологических кривых (рисунок 13, 14) также практически
одинаков у суспензий с различными соединениями-предшественниками NiO, что
согласуется с близостью показателей формирования слоев и их прочностью.
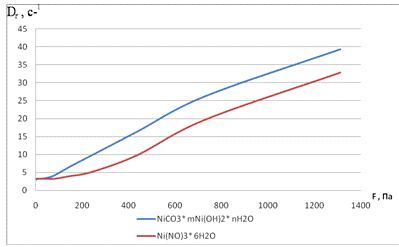
Рисунок 14 - Кривые течения для суспензий, содержащих
карбонат никеля и нитрата никеля в количестве, эквивалентном 7% NiO
Гранулы отвержденной суспензии Al2O3-ZrO2
пропитывали раствором Ni (NO) 3* 6H2O так, чтобы
содержание в готовом катализаторе также составляло 7% NiO. Для получения
точного количества вносимого нитрата никеля был проведен расчет по влагоемкости
гранул из исходной суспензии. Так, на 5 см3 гранулированного
катализатора необходимо 3,8 г соли Ni (NO) 3* 6H2O.
Пропитанные гранулы были термообработаны при температурах: -
100 0С 2 ч, - 300 0С 2 ч, - 600 0С 2 ч.
3.7 Испытание
образцов катализаторов в реакции окисления СО и Н2
Синтезированные образцы катализаторов предназначены для
процесса конверсии углеводородов и получения водородсодержащего газа. Для
подтверждения перспективности их применения в целевом процессе и выбора
оптимальных условий формирования в виде микросруктурированного элемента
каталитического реактора была проведена сравнительная оценка их каталитической
активности в модельных реакциях окисления оксида углерода и водорода.
Технологическая операция восстановления NiO в Ni не проводилась; частичное
восстановление оксида никеля в образцах катализатора происходило при окислении
ими СО, после чего соответствующий образец испытывали в реакции окисления
водорода.
Результаты определения степени окисления СО и Н2
полученными образцами катализатора представлены на рисунках 15 и 16,
соответственно.

Рисунок 15 - Зависимость степеней превращения от температуры
для образцов катализатора в реакции окисления СО
Наиболее активным (из исследованы) катализатором, работающим
при более низких температурах, является катализатор, полученный методом
пропитки гранул Ni (NO) 3* 6H2O. Температура начала его
работы составляет 2650С, далее при повышении температуры степень
превращения катализатора резко возрастает таким образом, что при достижении
температуры 3300С степень превращения составляет уже 96%.
В отличие от катализатора, полученного методом пропитки,
образцы с активным компонентом, введенным в суспензию, начинают работать лишь
при температуре от 300-320 0С и достигают высокой степени
превращения лишь при повышенных температурах (500 0С). Причем,
катализатор, полученный внесением в суспензию Ni (NO) 3, при
максимальных (в условиях испытаний - 500С) температурах достигает степени
превращения лишь 69%.
Образец катализатора из суспензии с карбонатом никеля,
начиная эффективно работать, как и образец с нитратом никеля, лишь выше 300С,
отличается от последнего более резким повышением активности в области
температур выше 400С и "демонстрирует" тенденцию к достижению степени
превращения, близкой к 100 %.
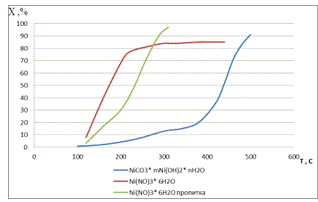
Рисунок 16 - Зависимость степеней превращения от температуры
для образцов катализатор в реакции окисления Н2.
Реакция окисления водорода также показала наибольшую
реакционную способность катализатора, полученного методом пропитки Ni (NO) 3*
6H2O. При температуре 300 0С степень превращения
составляет 97%. Отвержденный образец, полученный внесением в суспензию Ni (NO) 3*
6H2O также начинает работать при 100 0С, но не только не
достигает показателей Х, близких к 100 %, но и не "стремится" к ним.
Причиной, по-видимому, является взаимодействие нитрата никеля с
алюмогидроксидной составляющей суспензии, протекающее при термообработке
композиции.
Катализатор с введением в состав NiCO3* mNi (OH) 2*
nH2O начинает окислять водород при значительно более высоких температурах (до
400 С), что не является предпочтительным для проведения данной реакции, однако
не исключает перспективности применения данного катализатора в
высокотемпературных процессах, например, конверсии углеводородов, реализуемой
при температрах около 800 С.
3.8
Результаты ИК и РФА
Исследования проводились на приборе SHIMADZUFTIR - 8400 S и
представлены на рисунке 17.
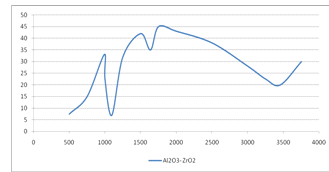
Рисунок 17 - Кривые ИК спектров поглощения образца оксидного
композита

В результате анализа ИК - спектров было установлено, что во
всех представленных спектрах имеется наличие полос поглощения, которые
соответствуют:
-3500 1/см - высокочастотные валентные колебания ОН-групп,
связанных водородной связью друг с другом;
-1600 1/см - деформационное колебание адсорбированной на
поверхности молекулы воды (Н-О-Н), при движении атомов водорода в плоскости
молекулы;
-635 - деформационное колебание молекулы воды (Н-ОН);
В области поглощения 820 - 680 наблюдаются деформационные
колебания Al-O, Zr-O.
Колебания 500-650 1/см - деформационные колебания групп СО32
- и NO3-
Согласно проведенному анализу определено, что во всех
образцах существует оксидная составляющая, а также гидроксильный покров и
молекулы воды, сорбированные на поверхности оксидной матрицы. Все полученные
спектры достаточно близки, что указывает на изоструктуру формирующейся оксидной
матрицы.
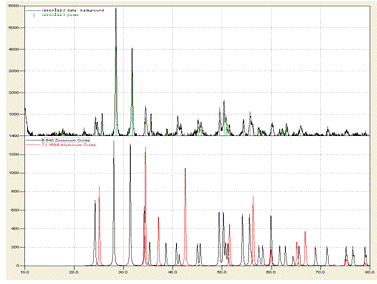
Рисунок 19 - Результаты РФА для образца катализатора
(Al2O3 - ZrO2 (50-50%) +Ni
(NO3) 2, введенный в состав суспензии) - 600 С
На рисунках 19 и 20 - верхние спектры относятся к
исследуемому образцу катализатора, внизу приведены характерные линии спектров
образцов сравнения
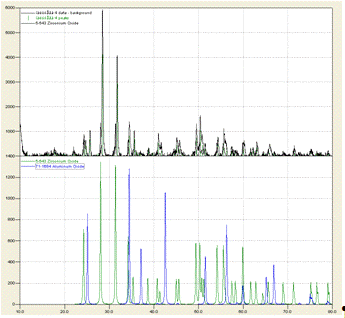
Рисунок 20 - Результаты РФА для образца катализатора Al2O3 -
ZrO2 (50-50%) +NiCO3*mNi (OH) 2* nH2O, введенный в состав суспензии) - 600 С
В результате рентгенофазового исследования было установлено,
что в образцах, присутствует моноклинный ZrO2 и Al2O3 в ромбоэдрический
модификации.
4.
Стандартизация
Структура и основное содержание структурных частей дипломной
соответствуют СТП СПБГТИ.017 - 97 "КС УКДВ. Дипломный проект, работа,
работа - проект. Общие требования".
Дипломная работа оформлена в соответствии с ГОСТ 7.32 - 2001
"СИДИБ. Отчет по научно - исследовательской работе. Структура и правила
оформления".
Наименование и обозначение физических величин и единиц
соответствует ГОСТ 8.417 - 81 "ГСИ. Единицы физических величин" и СТП
2.005.005 - 2002 "КС УКДВ. Единицы физических величин".
Таблица 7 - Стандарты и правила по охране труда и окружающей
среды
|
Обозначение
|
Наименование стандарта
|
|
Нормы пожарной безопасности (НПБ 105-03)
|
Определение категорий помещений, зданий
|
|
ГОСТ 12.1.003-83*
|
ССБТ. Шум. Общие требования безопасности
|
|
ГОСТ 12.1.004-91*
|
ССБТ. Пожарная безопасность. Общие требования
|
|
ГОСТ 12.4.021-75*
|
ССБТ. Системы вентиляционные. Общие требования
|
|
ГОСТ 12.1.005-88*
|
ССБТ. Санитарно-гигиенические требования к
воздуху рабочей зоны
|
|
ГОСТ.12.1.007-76*
|
ССБТ. Вредные вещества. Классификация и общие
требования
|
|
ГОСТ 12.1.010-76*
|
ССБТ. Взрывоопасность. Общие требования
|
|
ГОСТ 12.1.018-93*
|
ССБТ. Пожарная безопасность.
Электростатическаяискробезопасность. Общие требования.
|
|
ГОСТ 12.1.030-81*
|
ССБТ. Электробезопасность. Защитное заземление,
зануление
|
|
ПУЭ-76-М
|
Правила устройства электроустановок
|
|
СНиП 26-05-95*
|
Естественное и искусственное освещение
|
5. Охрана
труда и окружающей среды
Охрана труда является заранее спланированной и тщательно
проработанной системой по обеспечению защиты жизни и здоровья людей, трудящихся
на производстве. В рамках этой системы проводятся различные мероприятия для
обучения, оздоровления и реабилитации сотрудников предприятия. В рамках данной
системы, изучаются и внедряются в жизнь достижения науки в сфере гигиены труда,
промышленной санитарии, техники безопасности, технической эстетики и других.
Современное производство работает в достаточно сложных
условиях, поэтому руководители всех предприятий должны с полной
ответственностью подходить к такому понятию, как охрана труда. Глава
предприятия должен всеми методами и способами обеспечивать полную безопасность
каждого сотрудника. В таком случае, это обеспечение всех сотрудников
индивидуальными средствами для защиты на производстве, безопасность
оборудования, зданий и сооружений, оптимальный режим труда и отдыха,
безопасность процесса производства.
Как производственная, так и экологическая безопасность любого
промышленного объекта или процесса во многом определяется решениями, которые
принимаются ещё на стадии проведения опытно-конструкторских работ и разработки
новой технологии. Охрана окружающей среды направлена, прежде всего, на
ограждение от природы отрицательного воздействия, вызванного деятельностью
человека. Так же охрана окружающей среды предусматривает ограничения на
несанкционированные выбросы мусорных отходов, которые загрязняют окружающую
среду и портят экологию. Перед началом проведения исследовательской работы
нужно продумать, как обеспечить безопасность в первую очередь людям,
задействованным в исследовательской работе, а также безопасность помещения и
зданий от возможных разрушительных факторов.
Так как при выполнении исследовательской работы используются
различные химические вещества, то нужно обратить внимание на их токсичность,
огне - и взрывоопасность. Нужно предусмотреть возможные опасные моменты при
работе на оборудовании, а также способы их предупреждения. Необходимо учесть
возможные травмы при выполнении работы и принять меры для оказания первой
помощи.
5.1 Опасные и
вредные производственные факторы
На человека в процессе его трудовой деятельности могут
воздействовать опасные (вызывающие травмы) и вредные (вызывающие заболевания)
производственные факторы.
Вредный производственный фактор - фактор, воздействие
которого на работающего, в определённых условиях, приводит к заболеванию или
снижению работоспособности.
Опасный производственный фактор - фактор, воздействие
которого на работающего, в определённых условиях, приводит к травме или другому
внезапному ухудшению здоровья.
Вредный производственный фактор, в зависимости от
интенсивности и продолжительности воздействия, может стать опасным. Согласно
[30] опасные и вредные производственные факторы разделяются по природе действия
на человека на следующие группы:
Физические факторы, которые включают в себя такие вредные и
опасные моменты производства, как движущиеся машины и механизмы или их
элементы, разрушающиеся конструкции; повышенная или пониженная температура
поверхностей оборудования; повышенные уровни шума, вибраций, статистического
электричества; неудовлетворительного освещения.
Химические факторы опасное и вредное воздействие на организм
человека сырья, полупродуктов, готовой продукции и отходов производства.
Биологические факторы включают в себя патогенные
микроорганизмы (вирусы, бактерии, грибы, простейшие и др.) и продукты их
жизнедеятельности, а также микроорганизмы (растения и животные).
Психофизиологические факторы - по характеру подразделяются на
физические (статистические и динамические) и нервно-психические перегрузки
(умственное перенапряжение, монотонность труда, эмоциональные перегрузки). В
данной работе имели место группы вредных химических и физических
производственных факторов. Сведения о них представлены в таблице 8.
Таблица 8 - Стандарты и правила по охране труда и окружающей
среды
|
Обозначение стандарта
|
Наименование стандарта
|
|
ГОСТ 12.1.003-83
|
ССБТ. Шум. Общие требования безопасности.
|
|
ГОСТ 12 Л.004-91
|
ССБТ. Пожарная безопасность. Общие требования.
|
|
ГОСТ 12.1.005-88
|
ССБТ. Санитарно-гигиенические требования к
воздуху рабочей зоны.
|
|
ГОСТ 12.1.007-76
|
ССБТ. Вредные вещества. Классификация и общие
требования безопасности.
|
|
ГОСТ 12.1.010-76
|
ССБТ. Взрывоопасность. Общие требования.
|
|
ГОСТ 12.1.018-93
|
ССБТ. Пожарная безопасность. Электростатическая
искробезопасность. Общие требования.
|
|
ГОСТ 12.1.0 19-79
|
ССБТ. Электробезопасность. Общие правила и
номенклатура видов защиты.
|
|
Обозначение стандарта
|
Наименование стандарта
|
|
ГОСТ 12.1.030-81
|
ССБТ. Электробезопасность. Защитное заземление,
зануление.
|
|
ПУЭ-76-М
|
Правила устройства электроустановок.
|
|
СНиП-П-4-79
|
Естественное и искусственное освещение. Нормы
проектирования.
|
Таблица 9 - Характеристика физико-химических пожароопасных и
токсических свойств сырья, готового продукта и отходов производства
|
Вещество
|
Физико-химические свойства [31]
|
Пожаровзрывоопасность [32]
|
Токсичные свойства [33]
|
|
Агрегат, состояние
|
Тплав.,°С
|
Ткип.,°с
|
Плотность, кг/м3
|
Температура,°С
|
Пределы распространения пламени
|
Характер действия на человека
|
Класс опасности
|
Пдк р. з., мг/м3
|
|
|
|
|
|
Вспышки
|
Самовоспламенение
|
Температурные,°С
|
Концентрационные, об. %
|
|
|
|
|
|
|
|
|
|
|
Ниж.
|
Верх.
|
Ниж.
|
Верх.
|
|
|
|
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
11
|
12
|
13
|
14
|
|
AL2O3
|
Т
|
2010 - 2050
|
2980
|
3.5 - 3.97
|
-
|
-
|
-
|
-
|
-
|
-
|
Вызывает механическое раздражение легочной
ткани. Поражаются легкие при вдыхании пыли или дыма. Заболевание называется
алюминозом легких.
|
3
|
2
|
|
ZrO2
|
т
|
-
|
-51
|
1,25
|
-
|
-
|
-
|
-
|
-
|
-
|
Химические ожоги.
|
|
11
|
|
Аl (NO3) 3*9Н2О
|
т
|
|
70
|
1,5
|
-
|
-
|
-
|
-
|
-
|
-
|
Раздражение слизистых оболочек органов дыхания
|
|
|
|
Псевдобемит
|
-т
|
|
2700
|
7.132
|
-
|
-
|
-
|
-
|
-
|
-
|
Мало раздражает здоровую кожу, на значительно
поврежденной вызывает зуд и сухость.
|
2
|
3
|
|
Азотная кислота (HNO3)
|
аэрозоль
|
42
|
83.4
|
1.502
|
Не горючая жидкость
|
-
|
-
|
-
|
-
|
-
|
Вызывает тяжелые ожоги. Туман чистой кислоты
раздражает дыхательные пути, может вызвать поражение роговицы глаза.
|
3
|
2
|
|
NH4OH
|
жидк
|
77.75
|
33.35
|
0.694
|
В смеси с воздухом, О2N2O
|
-
|
-
|
-
|
15
|
28
|
При высоких концентрациях боль в глазах,
удушье, головокружение.
|
2
|
1
|
|
Цирконил азотнокислый
|
т
|
-
|
-
|
1.3
|
-
|
120
|
-
|
-
|
-
|
-
|
Способен к воспламенению. Вызывает ожог. При
вдыхании пыли раздражает слизистую носа
|
3
|
3
|
5.2 Категория
помещения по взрывопожароопасности
5.2.1 Класс
взрывоопасной и пожароопасной зоны
Определение пожароопасной категории помещения осуществляется
при сравнении максимального значения удельной временной пожарной нагрузки [35].
При пожарной нагрузке, включающей в себя различные сочетания горючих,
трудногорючих веществ и материалов в пределах пожароопасного участка, пожарная
нагрузка Q (МДж) может определяться по формуле:
= Σ Gi * QHi, (18)
где Gi - количество i-ro пожарной нагрузки, кг;
Qm - низшая теплота сгорания первого материала
пожарной нагрузки, МДж/кг.
Удельная пожарная нагрузка q, МДж/м2, определяется из
соотношения:
= Q/S, (19)
где S - площадь размещения пожарной нагрузки, м2 (но
не менее 10 м2)
Данная работа проводилась в помещении кафедры технологии
катализаторов, которое согласно, относится по пожарной опасности к категории
ВЗ, как помещение, в котором работают с горючими и трудно горючими жидкостями,
веществами и материалами. Определение пожароопасной категории помещения
приведено в таблице 10.
Таблица 10 - Пожароопасная категория помещений
|
Наименование материала пожарной нагрузки
|
Вес, кг/и2
|
Кол-во, шт., м2
|
Общий вес, кг
|
Низшая теплота сгорания, МДж/кг
|
Пожарная нагрузка, МДж
|
|
Парта
|
11
|
17
|
187
|
18.7
|
3426.9
|
|
Наименование материала пожарной нагрузки
|
Вес, кг/и2
|
Кол-во, шт., м2
|
Общий вес, кг
|
Низшая теплота сгорания, МДж/кг
|
Пожарная нагрузка, МДж
|
|
Лабораторный стол
|
83
|
8
|
664
|
18.7
|
12416.8
|
|
Оконный блок
|
50
|
4
|
200
|
18.7
|
3740.0
|
|
Дверь
|
10
|
7
|
70
|
18.7
|
1309.0
|
|
Линолеум
|
1.3
|
70
|
91
|
13.7
|
1246.7
|
|
Общая пожарная нагрузка помещений, МДж
|
22209.4
|
|
Площадь помещений, м2
|
70
|
|
Удельная пожарная нагрузка, МДж/м2
|
317.3
|
Класс зоны по ПУЭ В-1Б - зона, расположенная в помещении, в
котором при нормальной эксплуатации взрывоопасные смеси горючих газов или паров
ЛВЖ с воздухом не образуется, а возможно только в результате аварий или
неисправностей.
5.2.2
Средства тушения пожара
Если в лаборатории возник пожар и есть угроза его
распространения, то следует использовать имеющиеся под рукой средства тушения,
одновременно нужно также вызвать местную пожарную охрану. [36].
Средства тушения:
песок (ящик или ведро с песком) используется, если горят
деревянные предметы или нерастворимые в воде органические вещества;
асбест;
пенные огнетушители - тушение твёрдых или жидких веществ и
материалов. В тех случаях, когда водопенный раствор способствует развитию
процесса горения или является проводником электрического тока, пенные
огнетушители применять нельзя;
газовые огнетушители для тушения небольших очагов горения
веществ, материалов и электроустановок, за исключением веществ, горение которых
происходит без допуска кислорода воздуха;
порошковый огнетушитель - тушение небольших очагов загорания
щелочных металлов, металлоорганических и других соединений;
углекисло-бромэтиловый для тушения небольших очагов горения
волокнистых и других твёрдых материалов, а также электроустановок.
Запрещается применение химического огнетушителя при
воспламенении электрооборудования. В случае возгорания электрооборудования
последнее необходимо обесточить, сообщить дежурному электрику, при
необходимости вызвать пожарную охрану.
5.3
Вентиляционная установка
Так как дипломная работа была связана с использованием
вредных, газообразных веществ, то все эксперименты проводились в вытяжном шкафу
при включённой проточно-вытяжной циркуляции. Скорость движения воздуха в
рабочем проёме не менее 1,5 м/с [36,37]
5.4 Освещение
помещения, воздух и шум
Помещение лаборатории, в которой проводилась дипломная
работа, имеет естественное и искусственное освещение. Естественное боковое
освещение происходит за счёт окон. Искусственное освещение лаборатории,
предназначенное для постоянного пребывания людей, обеспечивается лампами
дневного света. Освещённость рабочей поверхности составляет 300 лК. Класс
зрительных работ IIIA [38,39].
Воздух рабочей зоны имеет температуру 18-20°С, относительная
влажность воздуха не превышала 70%.
Шум от работающего вытяжного шкафа не превышает 80 дБ.
5.5 Аптечка и
её содержание
В лаборатории бывают случаи, требующие неотложной медицинской
помощи, порезы рук стеклом, ожоги горячими предметами, кислотами, щелочами,
газообразными веществами.
При особо серьёзных случаях травм необходимо немедленно
обратиться к врачу и вызвать скорую помощь.
Для оказания первой медицинской помощи во всех случаях в
лаборатории всегда должны быть:
бинты;
гигроскопическая вата;
3% раствор йода;
2 % раствор борной кислоты;
2% раствор уксусной кислоты;
3 - 5 % раствор двууглекислого натрия (питьевой соды);
5 % марганцовокислый калий;
96 % этиловый спирт;
валидол.
5.6
Безопасность выполнения работы
Опасность и вредность связана с работой со стеклом и с
баллонами высокого давления.
При выполнении работы использовались следующие газообразные
вещества:
азот
гелий
Опасность работы с баллонами высокого давления связана не
только с токсичностью, горючестью и взрывоопасностью газов, но и с высоким
давлением газа в самих баллонах. Поэтому все меры предосторожности при работе с
газами направлены на то, чтобы исключить возможность неконтролируемой утечки
газа в атмосферу. Газы подавались из баллонов только через краны Гофера,
контролировались на давление и расход. Все эксперименты и анализы проводились в
перчатках и, если было нужно, использовались другие средства защиты.
Как уже упоминалось выше, газы, используемые в работе,
подавались из баллонов, вследствие чего не содержали примесей.
При выполнении данной исследовательской работы были соблюдены
все меры по обеспечению безопасности. Работ с токсичными веществами проводилась
в вытяжном шкафу, в котором не было посторонних предметов и источников
открытого огня. При проведении экспериментов была соблюдена герметичность
оборудования. При работе с высокотемпературной установкой были использованы
средства индивидуальной защиты, такие как рукавицы - для избежания термических
ожогов.
С точки зрения безопасности, стекло имеет ряд серьёзных
недостатков. Основные - хрупкость и невысокая стойкость к резким перепадам
температур. Правила работы со стеклом просты и не требуют особых пояснений.
Стекло - хрупкий материал, имеющий малое сопротивление при
ударе и незначительную прочность при изгибе. Поэтому применение физической силы
при работе со стеклянными деталями связано с опасностью их поломки.
Стеклянная посуда не предназначена для работы при повышенном
давлении.
Категорически запрещается использовать посуду, имеющую
трещины или отбитые края.
Осколки разбитой посуды убирают только с помощью щётки и
совка.
Стеклянные приборы и посуду больших размеров можно
переносить, держа крепко двумя руками. Поднимать крупные бутыли за горлышко
запрещается.
Все работы, в которых использовалась стеклянная лабораторная
посуда, проводились с большой осторожностью, чтобы избежать возможных травм и
порезов.
5.7 Обеспечение
электробезопасности
По опасности поражения электрическим током помещение
относится к помещениям без повышенной опасности [36].
Всё используемое электрооборудование было заземлено и
занулено, чтобы избежать возможного поражения электрическим током.
Присоединённые провода имеют надёжную изоляцию.
Необходимо наличие диэлектрических ковриков, перчаток.
Помещение лаборатории оборудовано огнетушителями ОУ-5, ХП-10, асбестовым
одеялом, ящиком с песком. Необходим свободный проход к электрощитам и приборам.
Всё электроприборы потребляющие напряжение свыше 36 В и требующие по
техническим причинам заземления, проверялись перед началом работы [40]. После
окончания работы всё электрооборудование проверялось и выключалось.
5.8 Анализ
технологических операций с точки зрения опасности и вредности их проведения
Данный раздел представлен в виде таблицы 11.
Таблица 11 - Анализ технологических операций с
точки зрения опасности и вредности их проведения
|
Наименование технологических операций
|
Оборудование для проведения операций
|
Реактивы, необходимые для проведения операций
|
Возможные опасности и вредности при проведении
данной технологической операции
|
Причины проявления данной опасности и вредности
|
Меры по безопасному проведению данной
технологической операции
|
Причины проявления данной опасности и вредности
|
Меры по безопасному проведению данной
технологической операции
|
|
Получение образцов
|
Ступка и пестик, вытяжка, стеклянное
оборудование
|
Аl2O3, AlOOH, вода
дистиллированная, ZrO2, NH4OH, Аl (NO3) 3*9Н2О,
Zr (NO3) 2 * 2Н2О
|
Наименование технологических операций
|
Оборудование для проведения операций
|
Реактивы, необходимые для проведения операций
|
|
|
|
Обжиг в электрической печи
|
Печь, тигель.
|
-
|
Термические ожоги Поражение электрическим
током.
|
Работа без средств защиты. Нарушение изоляции,
отсутствие заземления.
|
Установка защитных экранов, рукавицы, проверка
изоляции, заземления.
|
|
|
|
Анализ образцов
|
Лабораторная посуда.
|
-
|
Травмы, порезы.
|
Работа без средств индивидуальной защиты.
|
Рукавицы, фартук.
|
|
|
|
Работа на компьютере
|
Рабочее место оператора ЭВМ.
|
-
|
Поражение электрическим током. Нервные и
психологические нагрузки. Нарушение зрения
|
Пробой изоляции на корпус. Воздействие
электромагнитного излучения, несоблюдение режима труда и отдыха.
|
Проведение планового обслуживания ПК. Приведение
рабочего места в соответствие с СНиП. Расстояние от монитора 0,8 м.
|
|
|
5.9 Меры
первой медицинской помощи при случаях травматизма
При ранении стеклом необходимо удалить его осколки из раны,
если они в ней остались, и, убедившись, что там их больше нет, смазать рану
йодом и перевязать поражённое место. [40].
При термических ожогах первой и второй степени обожжённое
место нужно полчаса держать под холодной водой. Хорошо помогают примочки из
свежеприготовленных растворов питьевой соды (2 %) или марганцовокислого калия
(5 %).
При более тяжёлых или обширных ожогах необходимо немедленно
отправить пострадавшего к врачу.
При ожогах химическими веществами (главным образом кислотами
и щелочами) поражённый участок кожи быстро промывают большим количеством воды.
Затем на обожжённое место накладывают примочку:
при ожоге кислотой - из 2 % содового раствора
при ожоге щёлочью - из слабого раствора уксусной кислоты
При всех случаях отравления следует немедленно вызвать врача
или отправить пострадавшего в медпункт.
При поражении электрическим током:
а) Освободить пострадавшего от тока
б) Проверить пульс и дыхание
в) Сообщить о случившемся в медпункт
г) Приступить к искусственному дыханию
. Запрещается брать поражённого голыми руками. Чтобы
освободить поражённого электрическим током человека нужно отключить прибор.
5.10 Охрана
окружающей среды
Все источники конвективного тепла обеспечены теплоизоляцией.
В помещении применяется искусственная и естественная вентиляция.
Характеристика отходов представлена в виде таблицы 12.
Таблица 12 - Характеристика производственных отходов
|
Отходы
|
Агрегатное состояние
|
Кол-во отходов
|
Примечание (куда направляется отход)
|
|
Азотная кислота
|
ж
|
50мл
|
В емкость для неорганических отходов
|
|
Технологические отходы: Пыль (ZrO2, Al2O3 и
др.)
|
т
|
1,5г
|
В вытяжку
|
|
Хозяйственно-бытовые отходы (вода)
|
ж
|
0,3м3
|
В канализацию
|
Выводы по
работе
1 На основании анализа литературных и патентных источников
выбраны в качестве перспективных объекты исследования:
элемент микроканального реактора, конструируемый укладкой
между двумя плоскими пластинами одной гофрированной с высотой гофры 0,7 мм;
материал первичного носителя - сплав Х23Ю5 в виде
холоднокатанной фольги толщиной 50 мкм;
вторичный носитель в виде тонкослойного покрытия - оксидный
композит Al2O3: ZrO2= 1: 1;
каталитически активный компонент - оксид никеля;
способ формирования тонкослойного покрытии - нанесение из
суспензии.
2 Исследовано влияние условий приготовления
суспензии на ее реологические характеристики. Установлено следующее:
.1 Для получения качественного покрытия нанесением суспензий
из оксида алюминия и циркония необходимо их использование в виде
тонкодиспергированных частиц с преобладающим радиусом (1-3) мкм, что
достигалось в работе измельчением в шаровой мельнице в течение 12 часов;
проведение измельчения оксидов раздельно и совместно равноценно как в отношении
дисперсности частиц, так и свойств суспензии.
.2 Изменение плотности суспензии в диапазоне 1,3-1,1 г/см3
существенно снижает значение прилагаемой нагрузки, вызывающей разрушение
структурированной коллоидоподобной системы (от 70 до 4 Па), при уменьшении
эффективной вязкости, соответствующей этим нагрузкам (от 60 до 3 Пас).
Количественная оценка оксидного слоя, сформированного за 1 операцию
"нанесение-центрифугирование-сушка", показала увеличение его массы с
ростом плотности суспензии: от 0,8 до 2,2 и 3,6 % масс.
.2 Изменение рН от 3 до 2 практически не сказывается
показателях нанесения покрытия при плотности и реологических характеристиках
суспензии при прочих равных условиях.
.3 Для обеспечения высокой дисперсности частиц оксидной составляющей
суспензии, стабильных значений рН и реологических характеристик
структурированной системы достаточной является ее синтез при измельчении в
течение 3-х часов.
Определены структурно-прочностных характеристики оксидных
композитов в виде тонкослойных покрытий на пластинах и элементах
микроканального реактора, а также в виде гранул, получаемых из суспензий:
.1 По результатам определения механической прочности
оксидного композита в виде тонкослойного покрытия (прочность на истирание) и в
виде гранул (прочность на раздавливание) подтвержден выбор суспензии с
плотностью 1,2 г/ см3 и рН=2-3, как обеспечивающая формирование
равномерного и прочного покрытия и оксидного композита с более высокой
прочностью.
.2 Удельная поверхность оксидного композита, формируемого из
суспензии выбранного состава составляет 110 м2/г, суммарный объем пор 0,40
см3/г.
Получены и исследованы свойства образцов Ni-катализаторов при
варьировании способа введения активного компонента и его содержания: нитрат и
карбонат никеля, пропитка и введение в суспензию; 7-12% NiО.
Анализ ИК спектров поглощения показал, что во всех образцах
катализатора существует оксидная составляющая алюминия, циркония и никеля, а
также гидроксильный покров и молекулы воды, сорбированные на поверхности
оксидной матрицы. Все полученные спектры достаточно близки, что указывает на
изоструктуру формирующейся оксидной матрицы.
Исследованы образцы катализатора (в виде гранул и элемента
микроканала) в процессах окисления СО и Н2
Наиболее активным (из исследованых) катализатором, работающим
при более низких температурах, является катализатор, полученный методом
пропитки оксидного композита Ni (NO) 3. Температура начала его
работы при окислении СО составляет 2650С, далее при повышении
температуры степень превращения катализатора резко возрастает и достигает при
3300С степени превращения 96%. При окислении Н2 температуре 300 0С
соотвествует степень превращения 97%.
Таким образом, исследованы условия формирования тонкослойного
оксидного покрытия и катализатора на его основе для микроканальных пластин
каталитического реактора и показана эффективность его применения в реакциях
окисления СО и Н2.
Список
использованных источников
1
Макаршин Л.Л., Пармон В.Н. Микроканальные каталитические системы для водородной
энергетики / Рос. Хим.Ж. (Ж. Рос. хим. общества им.Д.И. Менделеева), 2006, т.1,
№6. - С 19-25
Малышенко
С.П. Энергия: Экономика. Технология. Экология, 2012, №7. - С.33-39
Крылов
О.В. Катализ в промышленности, 2004, №3. - С.56-61
Макаршин
Л.Л. Эффективность работы катализаторов в реакции парциального окисления метана
/ Л.Л. Макаршин и др. // Катализ в альтернативной энергетике. Катализ в
процессах получения синтез-газа и водорода // Международный научный журнал
"Альтернативная энергетика и экология" (АЭЭ), №2 (46), 2007. - С.132-134.
Грибовский
А.Г. Изучение особенностей и диагностика протекания реакции паровой конверсии
метанола в микроканальных реакторах / Автореферат дисс. на соиск. уч. степени
к. т. н. Новосибирск: РИО ИК СО РАН, 208. - 17 с
Киршин
А. И Пористые алюмооксидные слои, закрепленные на металлической поверхности, -
вторичные носители платиновых катализаторов для блочных нейтрализаторов ВГ АТ /
А. И Киршин, Е. А Власов, Н.В. Мальцева, И. Б Морозова // В кн. "Сборник
материалов У Международного конгресса химических технологий" -
Санкт-Петербург, 12-14 октября 2004 г. - СПб: Изд. "Менделеев". -
2009. - С.91-93.
Мальцева
Н.В. Особенности формирования тонкослойных покрытий на металлической
поверхности блоков сотовой структуры / А.И. Киршин, Т.А. Вишневская, Н.В. Мальцева,
Л. И Бояркина. // Сб. тезисов докладов 6-го Международного симпозиума
"Термохимические процессы в плазменной аэродинамике". - СПб.12-14
мая, 2008 г.
Отчет
по проекту: №30184 "Разработка и подготовка к мелкосерийному выпуску
бифункционального каталитического, с повышенным ресурсом при сниженном
содержании драгоценных металлов, блочного нейтрализатора выхлопных газов
двигателей внутреннего сгорания" / программа: "Развитие научного
потенциала высшей школы". - СПб ГТИ (ТУ). - 2010. - 120 с.
Власов
Е.А. Физико-химические основы формирования поверхности сферических
алюмооксидных носителей и катализаторов для процесса окисления. Дисс. на соиск.
Уч. Ст.д. х. н. СПб, 2000.420 с.
Руководство
к лабораторным работам по коллоидной химии. Часть 111. Л.: РИО ЛТИ им. Ленсовета,
1972. - 78 с.
Ильин
А.П., Прокофьев В.Ю. Физико-химическая механика в технологии катализаторов и
сорбентов. - Иваново: ГОУВПО "ИГХТУ", 2009.315 с.
Киршин
А.И. Пористые алюмооксидные слои, закрепленные на металлической поверхности, -
вторичные носители платиновых катализаторов для блочных нейтрализаторов ВГ АТ /
А.И. Киршин, Е.А. Власов, Н.В. Мальцева, И.Б. Морозова // В кн. "Сборник
материалов У Международного конгресса химических технологий" -
Санкт-Петербург, 12-14 октября 2004 г. - СПб: Изд. "Менделеев". -
2004. - С.91-93.
Артамонова
О.В. Гидротермальный синтез нанокристаллов на основе ZrO2 в системе
ZrO2 - А2Oз / О.В. Артамонова [и др] // Журнал
неорганической химии. - 2010. - Т.49. №11. - С.1657-1661.
Черняк
М.Ю., Григорьева Н.А. Сборник трудов конференции молодых ученых ИХХТ СО РАН.
Красноярск, 2009. с 29-32
О.В.
Альмяшева, В.В. Гусаров. Влияние нанокристаллов ZrO2 на стабилизацию
аморфного состояния оксидов алюминия и кремния в системах ZrO2-Al2O3,
ZrO2-SiO2.Ж. Физика и химия стекла. т.32. №2.2006.
С.224-229
Выпускная
квалификационная работа инженера "Тонкослойные оксидные покрытия и
катализаторы на их основе” /Н.Л. Ли. - СПбГТИ (ТУ). - СПб, 2010. - 100 с.
Дзисько
В.А. Основы методов приготовления катализаторов. /В.А. Дзисько. - Новосибирск.
- Наука, 1983. - 263 с.
Дзисько
В.А., Карнаухов А.П., Тарасова Д.В. Физико-химические
основы
синтеза окисных катализаторов / Новосибирск: СО "Наука", 1978 г. -
382 с.
Строение
и свойства адсорбентов и катализаторов /Под ред.Б. Линсена. М.: Мир, 1973.653
с.
Ермоленко
Н.Ф., Эфрос М.Д. Регулирование пористой структуры окисных адсорбентов и
катализаторов. Минск: Наука и техника, 1971.285 с.
Мухленов
И.П. Технология катализаторов/И.П. Мухленов, Е.И. Добкина, В.И. Дерюжкина, В.Е.
Сороко. - Л.: Химия, 1979. - 328 с.
Пахомов
Н.А. Научные основы приготовления катализаторов // Методическое пособие. Курс
лекций. Новосибирск: РИО ИК СО РАН, 2010. - 281 с.
Пахомов
Н.А. Научные основы приготовления катализаторов // в кн.: Промышленный катализ
в лекциях. М.: Калвис, 2010. - С 87-130.
Практикум
по общей химической технологии / Учебное пособие для студентов вузов / Под ред.
И.П. Мухленова. - 3-е изд., перераб. и доп. - М.: Высш. школа, 1979. - 421с
Динамический
стенд для исследования катализаторов в реакции окисления СО. Инструкции по
эксплуатации. АЮВ 25001.00008 ИЭ. 2002. - 18 с.
Методика
выполнения измерений концентраций монооксида углерода, диоксида углерода и
метана методом реакционной газовой хроматографии. АЮВ 0.005.093 МВИ. 2009. - 22
с.
Динамический
стенд для определения параметров каталитического горения водородсодержащих
смесей. Инструкции по эксплуатации. АЮВ 25006.00011 ИЭ. - 25 с.
Методика
выполнения измерений концентрации водорода методом газовой хроматографии. АЮВ
0.005.084 МВИ. 2001. - 18 с.
Краткий
справочник физико-химических величин /под. ред.А. А. Равделя и А.М.
Пономаревой, ид. 8-е перераб. Л.: Химия ЛО, 1983. - 230 с.
ГОСТ
12,0,003 - 74 СБТТ. Опасные и вредные производственные факторы. Классификация.
Утв. и введен. от 18 ноября 1974
Баратов
А.Н. Пожаровзрывоопасность веществ и материалов и средства их тушения: Справ.
изд.: в 2-х книгах/Под ред.А.Н. Баратова, А.Я. Корольченко. - М.: Химия, 1990.
- 496 с.
Правила
устройства электроустановок. - М.: Главгосэнергонадзор России, 1998. - 607с.
Бадман
А.Л. Вредные химические вещества.: Справ. изд. /А.Л. Бадман, Н.В. Волкова. -
Л.: Химия, 1989. - 592с.
Кноп
В., Теске В. Техника обеспечения чистоты воздуха, перевод с немецкого Л.К.
Хоцянова, М.: "Медицина", 1970. - 199 с.
НПБ
105-30 Определение категорий помещений, здание наружных установок по
взрывопожарной и пожарной безопасности., 1996
.
Правила устройства электроустановок. - М.: Главгорэлектронадзор России, 2009 -
т 1,2,3. - С 706
ГОСТ
12.4.021-75. Система стандартов безопасности труда. Системы вентиляционные. Общие
требования. - М.: Издательство стандартов, 1981. - С 8
Кирюшкин
А.А. - Охрана труда и окружающей среды. А.А. Кирюшкин, З.В. Капитоненко. - СПб:
СПбГТИ (ТУ), 2005. - С 27
СНИП
23-05-95. Естественное и искусственное освещение. - М.; Стройиздат, 1995
Захаров
Л.Н. Техника безопасности в химической лаборатории /Л.Н. Захаров. - Л.; Химия,
2011. - с 336