Исследование процессов кристаллизации барий-боратных стекол с добавками фторидов редкоземельных элементов
ФЕДЕРАЛЬНОЕ
АГЕНТСТВО ПО ОБРАЗОВАНИЮ РФ
РОССИЙСКИЙ
ХИМИКО-ТЕХНОЛОГИЧЕСКИЙ УНИВЕРСИТЕТ имени Д.И. Менделеева
ИНЖЕНЕРНЫЙ
ФИЗИКО-ХИМИЧЕСКИЙ ФАКУЛЬТЕТ
КАФЕДРА ХИМИИ
И ТЕХНОЛОГИИ КРИСТАЛЛОВ
ДИПЛОМНАЯ
РАБОТА
НА ТЕМУ:
Исследование
процессов кристаллизации барий-боратных стёкол с добавками фторидов
редкоземельных элементов
Заведующий
кафедрой Проф., д.т.н. Жариков Е.В.
Руководитель работы Асс., к.х.н. Петрова О.Б.
Консультант по экономической части Ст. преп., к.э.н. Плакатин П.А.
Консультант по охране труда и противопожарной технике
Ст.преп., к.х.н. Шарифуллина Л.Р.
Консультант по охране окружающей среды Проф., д.т.н. Зайцев В.А.
Дипломант Аршанская Е.П.
Москва 2007
год
Содержание
СОДЕРЖАНИЕ
ВВЕДЕНИЕ.
ОБЗОР ЛИТЕРАТУРЫ.1 ОБЩИЕ ПОНЯТИЯ, СВЯЗАННЫЕ С ТЕХНОЛОГИЕЙ ПОЛУЧЕНИЯ СИТАЛЛОВ И
СТЕКЛОКРИСТАЛЛИЧЕСКОГО МАТЕРИАЛА.2 ТЕОРЕТИЧЕСКИЕ ОСНОВЫ КРИСТАЛЛИЗАЦИИ СТЕКЛА.3
ХАРАКТЕРИСТИКА БАРИЙ-БОРАТНОГО СТЕКЛА И ЕГО КРИСТАЛЛИЗАЦИИ.4 ФТОРИДНЫЕ
СТЁКЛА.4.1 Составы фторидных стёкол.4.2 Некоторые свойства фторидных стёкол.4.3
Влияние иона F- на структуру щелочно-боратного стекла.5. ЛЮМИНЕСЦЕНЦИЯ ИОНА
ER3+В СТЁКЛАХ, КРИСТАЛЛАХ И НЕКОТОРЫХ СТЕКЛОКРИСТАЛЛИЧЕСКИХ СИСТЕМАХ.5.1
Свойства иона Er3+..5.2 Люминесценция Er3+ в стёклах.5.3 Люминесценция Er3+ в
кристаллах.5.4 Люминесценция Er3+ в многокомпонентных системах.6 ВЛИЯНИЕ
ФТОРИДОВ РЗЭ НА СВОЙСТВА ОКСИДНЫХ СТЁКОЛ.6.1 Основные свойства фазы LaF3.6.2
Влияние наличия фторида на стеклообразование и кристаллизацию стекла на
воздухе.7 ВЫВОДЫ ИЗ ОБЗОРА ЛИТЕРАТУРЫ. ЦЕЛИ И ЗАДАЧИ РАБОТЫ. МЕТОДИКА
ЭКСПЕРИМЕНТА.1 ХАРАКТЕРИСТИКА РЕАКТИВОВ.2 МЕТОДИКА ВАРКИ И ОТЖИГА СТЁКОЛ.
ОБОРУДОВАНИЕ.2.1 Печь синтеза.2.2 Печь отжига стекла.2.3 Вспомогательное
оборудование.3 МЕТОДИКА АНАЛИЗА ПОЛУЧЕННЫХ МАТЕРИАЛОВ.3.1 Определение
напряжений в стёклах.3.2 Дилатометрический метод.3.4 Измерение
микротвёрдости.3.5 Рентгенофазовый анализ.3.6 Гидростатическое взвешивание.3.7
Спектры комбинационного рассеяния света.3.8 Измерение спектров пропускания в
видимой и УФ области.3.9 Оптическая спектроскопия.3.10 Дифференциальный
термический анализ. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ.1 СИНТЕЗ ИСХОДНЫХ СТЁКОЛ.1.1 Состав
шихты и соотношения компонентов.1.2 Варка стёкол.1.3 Термические напряжения в
стёклах и отжиг.2 ОПРЕДЕЛЕНИЕ ХАРАКТЕРИСТИЧЕСКИХ ТЕМПЕРАТУР СТЁКОЛ.2.1
Результаты дилатометрических измерений.2.2 Результаты дериватографических
измерений.2.3 Подбор условий термообработки с целью кристаллизации исходных
стёкол.3 ПОДГОТОВКА ПЛОСКОПАРАЛЛЕЛЬНЫХ ОБРАЗЦОВ.3.1 Шлифовка.3.2 Полировка.4
ИЗМЕРЕНИЕ МИКРОТВЁРДОСТИ.5 ИЗМЕРЕНИЕ ПЛОТНОСТИ.6 ОПРЕДЕЛЕНИЕ ФАЗОВОГО СОСТАВА И
СТРУКТУРЫ СТЕКЛОКРИСТАЛЛИЧЕСКИХ МАТЕРИАЛОВ.6.1 Определение кристаллических фаз,
выделяющихся при термообработке.6.2 Определение структурных изменений в стекле
при термообработке.7 СПЕКТРОСКОПИЧЕСКИЕ ИССЛЕДОВАНИЯ.7.1 Спектр пропускания
стёкол и стеклокристаллических материалов.7.2 Поглощение Er3+ в стёклах и
стеклокристаллических материалах. ЗАКЛЮЧЕНИЕ И ВЫВОДЫ. ОХРАНА ТРУДА.
ЭКОНОМИЧЕСКАЯ ЧАСТЬ. ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ. СПИСОК ЛИТЕРАТУРЫ
Введение
Прозрачный стеклокристаллический материал представляет собой прозрачную
стеклянную матрицу, в которой диспергированы кристаллы с размерами, существенно
меньшими длин волн оптического диапазона. В последнее время эти материалы
представляют большой интерес для науки и техники как оптические материалы.
Синтез и исследования ведутся на широком спектре стеклообразующих оксидных,
фторидных, халькогенидных и прочих систем. В результате станет возможным
создание как пассивных оптических элементов и преобразователей оптического
излучения, так и активных лазерных элементов.
Стеклокерамика по сравнению с монокристаллами обладает таким
достоинством, как простота технологии, которая сходна со стекольной. К тому же
есть возможность получать изделия различной формы и требуемых размеров, в том
числе стекловолокна. Многие свойства прозрачной стеклокерамики близки или даже
превосходят свойства монокристаллов.
Фторидные материалы, в особенности фториды редкоземельных элементов,
перспективны с точки зрения своих спектрально-люминесцентных свойств; эти свойства
фторидных материалов существенно отличаются от свойств оксидных материалов, и
поэтому позволяют существенно расширить возможности оптических и лазерных
приборов. Однако при синтезе кристаллов и стёкол на основе фторидов различных
элементов существует ряд сложностей. В частности, синтез необходимо проводить в
атмосфере инертных газов или фторирующих агентов; на воздухе всегда есть
вероятность получения оксифторидных включений. К тому же фториды обладают
высокой реакционной способностью, в том числе и к конструкционным материалам,
гигроскопичностью и склонны к пирогидролизу. Всё это препятствует широкому
внедрению фторидных материалов в лазерную и оптическую технику.
Настоящая дипломная работа посвящена получению прозрачного
стеклокристаллического материала в системе BaO-B2O3-LaF3, представляющего собой
оксидную матрицу, в которой распределены кристаллы фторидной фазы, а также
легированный ионами Er3+ стеклокристаллический материал состава
xBaO·yB2O3·zLaF·0,01ErF3.
При удовлетворительных результатах прозрачная оксидная стеклокерамика,
содержащая кристаллическую фазу фторида редкоземельного элемента,
активированная редкоземельными ионами, может рассматриваться как материал,
пригодный для применения в лазерной технике, в качестве активных элементов, а
также усилителей, световодов, сцинтилляторов, волоконных лазеров.
I. Обзор литературы
I.1 Общие понятия, связанные с технологией получения ситаллов и
стеклокристаллического материала
Ситалл - это искусственный материал микрокристаллического строения,
который получен методом кристаллизации из стекла соответствующего состава и
обладающий лучшими с точки зрения использования физико-химическим свойствами по
сравнению с исходным стеклом [1].
Гомогенное стекло - однофазное вещество; ситаллы же являются
гетерофазными: в них всегда присутствует остаточная стеклофаза и одна или
несколько микрокристаллических фаз.
По свойствам ситаллы можно разделить на группы: химически стойкие,
оптические, электроизоляционные, термостойкие, радиопрозрачные,
износоустойчивые. Также существует классификация и по фазовому составу,
например, сподуменовые, кордиеритовые, боросвинцовые и прочие.
Для выделения нового класса материалов, интерес к которым появился с
развитием фотоники и спектроскопии разупорядоченных сред, сейчас используется
отдельное понятие «стеклокристаллические материалы» (СКМ). Размер кристаллов в
них не превышает 0,01мкм [1]. За счёт этого СКМ обладают высокой прозрачностью.
Сегодня известны стеклокристаллические материалы с разнообразным строением,
составом и соотношением фаз в них. Состав СКМ и ситаллов на сегодняшний день
зависит от конечной цели их получения.
Для изготовления ситаллов необходимо выбрать соответствующий состав,
ввести в него катализатор кристаллизации при необходимости (то есть такую
добавку, которая обеспечит зарождение кристаллической фазы; это могут бать
оксиды, сульфиды, фториды и т.д.), произвести варку и соответствующую
термообработку отформованного стекла. Таким образом, важную роль играет подбор
оптимальной температуры отжига и режима термообработки стекла для получения
необходимого стеклокристаллического материала. Назначение термической обработки
- обеспечить максимальное число центров кристаллизации в стекле, оптимальную
степень закристаллизованности и заданный фазовый состав.
В промышленных масштабах для получения ситаллов (рис.1.1) [2] используют
видоизменённую технологию получения стёкол, то есть обычная технологическая
схема получения стекла дополняется таким технологическим элементом, как
вынужденная кристаллизация изделий; тогда как процесс изготовления изделий из
стекла представляется схематично так: получение шихты ® варка стекла ® формование изделий ® отжиг изделий. После отжига изделие
подвергается дополнительной термической обработке по заданному режиму с целью
кристаллизации. Однако кристаллизация изделия может быть как сразу после стадии
формования, минуя отжиг, так и непосредственно после отжига полученного
стеклянного изделия.

Рис.
1.1 [2]. Технологическая схема промышленного получения стеклокристаллического
материала.
Первый
этап - приготовление шихты. Шихтой называют однородную смесь сырьевых
материалов с определёнными составом и влажностью. Её компоненты определяются
заданным составом будущего ситалла. Соответственно, состав шихты разнообразен.
Однако, независимо от набора исходных реактивов, к шихте предъявляются
следующие общие требования: 1) постоянство химического состава; 2) определённый
гранулометрический состав; 3) заданная влажность; 4) минимальное содержание
примесей. Последний критерий особенно важен в нашем случае, поскольку для
изготовления СКМ для оптического применения необходимо получить стекло высокой
чистоты. Также при выборе шихты следует учитывать состав паровой фазы,
образующейся при термической обработке. После подбора компонентов шихты
сырьевые материалы дозируют в соответствии с методикой изготовления того или
иного ситалла.
Далее
идёт процесс варки стекла.
Под
стекловарением понимается совокупность физико-химических процессов в шихте и
расплаве по мере повышения температуры по заданному режиму. В результате варки
получают однородную по составу и не содержащую газовых включений стекломассу в
расплавленном состоянии. Из этой стекломассы осуществляется последующее
формование изделия.
Согласно
классификации Тёрнера (1931г.) [3], при стекловарении происходят физические и
химические изменения.
К
числу первых относятся:
)
нагрев шихты; 2) испарение влаги; 3) плавление компонентов шихты; 4)
растворение компонентов в расплаве; 5) полиморфные превращения; 6) улетучивание
некоторых компонентов.
Среди
химических изменений:
)
диссоциация гидратов; 2) удаление химически связанной воды; 3) диссоциация
карбонатов, сульфатов и других солей; 4) химическое взаимодействие компонентов.
Скорость
стеклообразования связана с температурой расплава, и при увеличении температуры
скорость растёт, так как происходит снижение вязкости, благоприятствующее
диффузии компонентов. Также на скорость стеклообразования влияют поверхностное
натяжение (чем оно ниже, тем лучше расплав смачивает тугоплавкие компоненты
шихты), размеры и форма частиц (зёрна неправильной формы - угловатые и неровные
- растворяются быстрее, чем круглые).
Конечный
продукт стадии стеклования - непрозрачный расплав, содержащий пузырьки газа и
неоднородный по составу. Для устранения применяют гомогенизацию, например,
перемешиванием и удалением газов, и выравнивание состава по всему объёму
посредством диффузии компонентов.
На
последнем этапе варки стекла - студка: понижение температуры до температуры
формования. Охлаждение должно осуществляться путём медленного и непрерывного
понижения температуры при контроле состава и давления паровой фазы над
стекломассой.
Предваряя
описание следующей за варкой стадии - формования стекла - введём определения
некоторых важных характеристик и критериев стёкол, играющих существенную роль в
нашей работе.
Одной
из важнейших характеристик стекла является температурная зависимость вязкости
от температуры η
= f(T) или lg(η) = f(Tg/T), где Тg - температура стеклования. Переход от
расплава в стеклообразное состояние и обратно происходит постепенно. При этом
вязкость системы непрерывно растёт от 108 до 1012 Па·с без образования новой
фазы. Температура при вязкости 108 Па·с называется температурой текучести Тf.
Температура, при которой вязкость равна 1012 Па·с, есть температура стеклования
Тg. Интервал температур Тf - Тg называется интервалом стеклования. Температура
Тх - температура кристаллизации стекла. В литературе принят критерий
устойчивости стёкол, равный разнице температуры кристаллизации Тх и температуры
стеклования Тg: ∆Т. Ниже для примера приводится общий вид графика lg(η) =
f(Tg/T) стёкол [4].
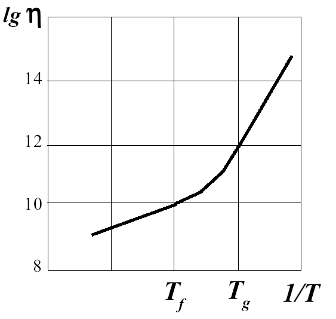 ис.1.2
[4]. Общий вид зависимости вязкости расплавов стёкол.
ис.1.2
[4]. Общий вид зависимости вязкости расплавов стёкол.
Формованием
называется стадия, на которой стекломасса приобретает заданную форму с
последующей её фиксацией в результате отвердевания стекломассы при охлаждении.
Температурная область формования соответствует изменению вязкости в интервале
от 1×102 до 4×107 Па×с. Разным способам формования соответствуют разные
вязкости. Для стёкол с минимальными вязкостями применяют литьё; в
противоположном случае - вытягивание. Существуют другие способы формования, для
которых необходима корректировка химического состава для достижения
определённой зависимости вязкости от температуры [3].
После
формования чаще всего следуют отжиг или закалка. Необходимость этих этапов
обусловлена наличием в стекле остаточных напряжений сжатия и растяжения после
охлаждения. Это сопровождается изменением объёмов слоёв: внешние слои сжимаются
при охлаждении, внутренние остывают медленнее и занимают прежний объём, когда
внешние слои уже сжались. Величина напряжений в стекле зависит от его КТР,
теплопроводности и толщины изделия. Отжигом называют тепловую обработку для
снижения остаточных напряжения до минимального значения. Основные стадии
отжига: а) нагрев от комнатной температуры до максимальной температуры отжига
(высшей) за время t1; б) выдержка изделия при высшей температуре в
течение t2; в) медленное снижение температуры с высшей
температуры отжига до низшей за время t3; г) охлаждение
изделия от низшей температуры отжига до комнатной температуры за время t4. Высшая температура отжига близка к температуре стеклования и
подбирается так, чтобы ей соответствовала вязкость стекла порядка 1012 Па×с. При этой температуре остаточные напряжения
уменьшаются в 10 раз через 5 минут выдержки. При низшей температуре отжига
напряжения уменьшаются в 10 раз через 500 минут выдержки. Эта температуры
должна соответствовать вязкости стекла порядка 1014 Па×с. Стадия (а) отжига - самая быстрая, наиболее
медленная - (в). После достижения низшей температуры отжига скорость процесса
снова возрастает. Скорость процесса, времена выдержек при той или иной
температуре и прочие параметры отжига определяются с учётом толщины изделия,
состава стекла, конфигурации.
Закалкой
называется процесс тепловой обработки, в результате которой остаточные
напряжения равномерно распределяются по всему объёму стеклянного изделия,
причём во внешних слоях распределены напряжения сжатия, во внутренних -
растяжения. Это достигается за счёт применения особого режима термообработки.
Сначала происходит быстрый нагрев до температуры, превышающей температуру
стеклования на 80-100°С (температура закалки), далее следует резкое
охлаждение поверхности. Время выдержки при температуре закалки должно быть мало
(около 5 минут для образца толщиной 6 мм). Закалённые стёкла имеют высокие
термостойкость и механическую прочность [3].
При
изготовлении ситаллов и стеклокристаллических материалов, как уже сказано выше,
далее следует дополнительная термическая обработка с целью кристаллизации
стекла.
I.2 Теоретические основы кристаллизации стекла
Термин «вынужденная кристаллизация» в нашем случае означает, что
температурно-временные условия термообработки исходного стекла подбираются так,
чтобы в стекле образовывались микрокристаллы одной или нескольких фаз; размер
кристаллов не должен превышать 1мкм, относительное содержание
микрокристаллической фазы должно составлять 30-90% [1]. Инициированная
кристаллизация стекла может быть осуществлена при соблюдении следующих условий:
а) введение в исходную шихту добавок, катализирующих процесс кристаллизации
(если это необходимо по методике); б) строгое соблюдение режима термической
обработки. Соблюдение указанных условий позволит осуществить равномерную
кристаллизацию стекла по всему его объёму и даст возможность обеспечить
выделение нужных фаз.
Скорость, с которой необходимо увеличивать температуру, может зависеть от
разных причин: а) склонности изделия к деформации; б) возникновения опасного
температурного градиента; в) появления предельных напряжений; г) возможностей
используемого нагревательного устройства. Пределом темпа нагревания сверху
управляют другие факторы. Во-первых, это вероятность разрушения толстостенного
изделия при скорости нагрева выше 20-30°С/мин вследствие достижения критических значений напряжений.
Особенно это опасно для стёкол с большим коэффициентом теплового расширения
(КТР). Во-вторых, опасность заключается в возможности деформаций изделия, если
при заданной скорости роста температуры не успевает пройти процесс образования
внутреннего каркаса изделия, который его армирует, защищая от деформаций при
нагревании. Третья причина ограничения большой скорости нагрева - образование
предельных напряжений в изделии при отсутствии оптимального градиента
температур по его толщине. Таким образом, практически скорость нагревания
составляет 2-5°С/мин, для
тонкостенных изделий - до 10°С/мин [3].
Реально процесс термообработки идёт в несколько стадий (ступеней) и
температуру первой ступени определяется экспериментально [1]. Число
образовавшихся на первой ступени центров кристаллизации будет определяться
размером кристаллов, их числом, степенью кристаллизации и свойствами данного
ситалла. Вторая ступень термической обработки отвечает температуре максимума
роста кристаллов, а её продолжительность соответствует времени, необходимому
для кристаллизации по всему объёму. Однако нахождение температуры второй
ступени осложняется, если в процессе кристаллизации образуется несколько фаз;
тогда как длительность второй ступени определяется относительно точно по
изменению свойств СКМ.
Отличительной особенностью гетерогенной кристаллизации является её
осуществление не из расплава, а из пластичного или твёрдого состояния стекла.
Ниже для сравнения приведены рисунки 1.3 и 1.4 для гомогенного и гетерогенного
зародышеобразования соответственно. Видно, что скорость образования зародышей
и, следовательно, роста кристаллов выше при гетерогенном механизме. Это
объясняется снижением поверхностной энергии за счёт искусственного создания
границы раздела фаз.

Рис.1.3 [2]. Зависимость скорости образования зародышей V и рост
кристаллов J от степени переохлаждения ∆Т при гомогенном
зародышеобразовании.

Рис.1.4
[2]. Зависимости скорости роста кристаллов на зародышах Jr, скорости роста
кристаллов катализаторов J и скорости их зарождения V от степени переохлаждения
∆Т при гетерогенном зародышеобразовании.
К катализаторам также предъявляются определённые требования.
Во-первых, соединение должно хорошо растворяться в расплаве данной
стекломассы, но растворимость его в стекле должна быть ограниченной в области
более низких температур. Во-вторых, граница раздела фаз «центр кристаллизации -
стекло» должна иметь низкую поверхностную энергию для возможности хорошего
смачивания кристаллов стекломассой. Также необходимо, чтобы скорость диффузии
атомов (ионов) катализатора кристаллизации в области низких температур была
выше скорости диффузии основных компонентов исходного стекла. Соблюдение
последнего требования даёт возможность осуществления процесса
зародышеобразования в области сравнительно низких температур [1].
В высокотемпературных расплавах стекломассы катализатор растворяется
полностью. В этом случае может происходить достаточно быстрое переохлаждение
расплава без кристаллизации. Дополнительная термообработка в области низких
температур приводит к выделению микрокристаллов каталитической добавки
вследствие её ограниченной растворимости в данном стекле при низких
температурах. Эти кристаллики выполняют роль центров кристаллизации в стекле.
На них при дальнейшей термической обработке происходит рост кристаллов заданной
основной фазы. По причине низкой растворимости катализатора кристаллизации при
пониженной температуре образование центров кристаллизации будет равномерным по
всему объёму, поэтому рост кристаллов основной фазы в стеклоизделии также будет
равномерным.
Разные соединения во многих случаях обладают избирательной каталитической
способностью, то есть в одном стекле при соблюдении режима кристаллизации
приведут к образованию кристаллической фазы, а в стекле другого состава могут
даже подавлять кристаллизацию. Таким образом, при синтезе ситаллов после выбора
составов стёкол бывает необходимо тщательно подбирать катализатор (или
катализаторы) кристаллизации, а также их количество в исходном стекле,
поскольку в некоторых случаях существенное влияние на свойства ситаллов и их
фазовый состав оказывают даже примесные содержания катализаторов [3].
Исследование механизма действия катализаторов - одна из наиболее сложных
задач в рассматриваемой технологии. В [1, 3, 4]
рассмотрены результаты анализов некоторых ситаллов. Был привлечён широкий
комплекс физических и физико-химических методов: рентгенофазовый анализ,
электронная микроскопия, локальный рентгеноспектральный анализ, ИКС, ЭПР, g-спектроскопия, электронография,
малоугловое рассеяние рентгеновских лучей и прочие.
Результаты анализов и исследований показали, что гетерогенное
зародышеобразование может возникать по двум механизмам:
- через образование микрокристаллов катализаторов, на которых
происходит эпитаксиальный рост;
- через процесс микроликвации.
Ликвация - это процесс, свойственный многим жидким системам. Её
особенность - протекание ниже температуры ликвидуса, когда стекло находится в
твёрдом состоянии либо в него переходит (ниже температуры стеклования Тg).
Таким образом, это метастабильный процесс в жидкости, находящейся в
метастабильном состоянии.
Ликвация может протекать как по нуклеационному механизму с преодолением
энергетических барьеров при образовании зародышей, так и без образования
зародышей. Поэтому структура процесса также может быть двух типов: в виде
отдельных капель в первом случае и в виде двух взаимосвязанных фаз -
двухкаркасная - во втором.
Действие микроликвации на кристаллизующееся стекло может быть различным.
Во-первых, это уменьшение поверхностной энергии за счёт образования границы
раздела фаз; во-вторых, это изменение состава образующихся стекловидных фаз,
что повышает их кристаллизационную способность; в-третьих, микрокапли
кристаллизуются и играют роль зародышей основных фаз в соответствии с принципом
кристаллохимического подобия [2].
При последующей кристаллизации стекла выпадают метастабильные фазы,
близкие по структуре и составу к исходному стеклу и образование которых требует
преодоления меньших энергетических барьеров. Таким образом, образованию
основной кристаллической фазы предшествует большое количество фазовых
переходов. Многостадийность процесса позволяет останавливать его на различных
этапах и, соответственно, получать ситаллы с различными фазовым составом,
структурой и свойствами [1].
I.3 Характеристика барий-боратного стекла и его кристаллизации
Оксид бора В2О3 - хороший стеклообразователь. Стёкла на его основе
представляют большой интерес как основа для создания новых материалов. Свойства
таких материалов сильно зависят от ионов-модификаторов и отличаются от свойств
самого стеклообразователя - чистого оксида бора [5, 6, 7].
На рис.1.5 представлен квазибинарный разрез сводной фазовой диаграммы
рассматриваемой бинарной системы B2O3-BaO.

Рис.1.5 [8]. Квазибинарный разрез диаграммы состояния ВаО-В2О3.
В рассматриваемой системе известны различные кристаллические фазы [9], то
есть кристаллизация в данном бинарном стекле разнообразна и зависит от
температур и соотношения оксидов. Каждая из возможных фаз имеет различную
кристаллическую структуру и обладает различными свойствами. Согласно сводной
фазовой диаграмме системы ВаО - В2О3 (рис.1.5), соотношения между этими двумя
оксидами при образовании различных фаз строго определены. Встречаются следующие
соотношения (ВаО : В2О3): 4:1, 3:1, 2.5:1, 2:1, 1:1, 1:2, 1:2.5, 1:4. Свойства
фаз различны, поскольку различны они все по своей кристаллической структуре. К
примеру, самую высокую температуру плавления имеет фаза (3:1) Ва3В2О6 (Тпл ≈
1383˚С), относящаяся к ромбической сингонии. Она же обладает наибольшей
плотностью: 5,112 г/см3.
Актуально выделить фазу с нелинейно-оптическими свойствами, так как такие
материалы представляют интерес в современной фотонике, такой фазой является
низкотемпературная модификация бората бария β-BaB2O4.
Борат бария BaB2O4 образуется при соотношении оксидов бария и бора один к
одному. Имеется две его модификации: высокотемпературная α, устойчивая выше 925°С, и
низкотемпературная β. Фаза α-BaB2O4 имеет пространственную группу RL3ic,
кристаллы центросимметричны, параметры гексагональной ячейки a = b
= 7,325Å, с
= 39,192Å. Низкотемпературная
форма бората бария β-BaB2O4 имеет пространственную группу R3c с
параметрами ячейки в гексагональных осях a = b = 12,519
Å, c =
12,723Å. [10].
В структуре β-BaB2O4 чередуются катионы Ва2+ и анионные
кольца (В3О6)3-. Гексагональная ячейка делится на шесть так называемых слоёв,
каждый из которых состоит из трёх подслоёв: два из них образованы
(В3О6)3--кольцами, один же состоит только из катионов бария. Связи между
подслоями ионные, тогда как связи между самими слоями имеют Ван-дер-Ваальсову
природу. Анионные кольца (В3О6)3- представляют собой три компланарные
группировки ВО33-, соединённые общими атомами кислорода [11,12].
Кристаллы β-BaB2O4 обладают нелинейными оптическими
свойствами при низких температурах. Примечательно, что нелинейность оптических
свойств наблюдается в широкой спектральной области. К тому же, коэффициент
преобразования достаточно высок. Это указывает на перспективность
кристаллического β-бората бария как преобразователя частоты лазерного
излучения в видимой и ультрафиолетовой областях.
Температуры стеклования барий-боратных стёкол Тg лежат в интервале
450-605˚С. Составы стёкол находятся в пределах от 32 до 83 мольных %
оксида бора [8,9].
Некоторые физические свойства стёкол в системе ВаО-В2О3 в зависимости от
соотношения оксидов представлены в таблице 1.1.
Таблица 1.1.
Некоторые физические свойства барий-боратного стекла [8].
|
Молярное отношение ВаО к
В2О3
|
Плотность, г/см3 (± 1%)
|
Тx, °С (±7°С)
|
Тg, °С (±7°С)
|
УФ край пропускания, нм (±5
нм)
|
|
0,6
|
3,71
|
─
|
603
|
─
|
|
0,9
|
4,09
|
─
|
559
|
─
|
|
1,2
|
4,22
|
551
|
512
|
210
|
|
1,3
|
4,31
|
553
|
497
|
210
|
|
1,5
|
4,40
|
571
|
485
|
213
|
Боратные стекла, как и ряд других, имеют цепочечное строение. Структура
чистого стеклообразного оксида бора состоит из плоских треугольников (BO3)3-,
расстояние между атомами В и О составляет 13,7 нм, угол О-В-О составляет 120о
(рис.1.6).
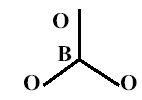
Рис.1.6 [9]. Треугольник (ВО3)3-.
Обзор литературы показывает, что в структуре рассматриваемого стекла
образуются шестичленные гексагональные бороксольные кольца (ВО3)3, состоящие из
трёх атомов В и трёх атомов О (рис.1.7):
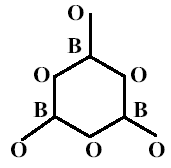
Рис.1.7 [9]. Бороксольное кольцо (ВО3)3.
Непрерывные двумерные цепи из треугольников (BO3)3- и бороксольных колец
(BO3)3 волнистые и скрученные. Они образуют постранственную сетку боратного
стекла.
В литературе [6,12,13] известно, что основными структурными группировками
в системе В2О3 - ВаО являются [ВО4]- -тетраэдры и треугольники [ВО3]. Однако
эти единицы могут образовывать так называемые «суперструктурные» группы:
бороксольные и метаборатные кольца, метаборатные цепочки, пентабораты,
тибораты, дибораты, полибораты и так далее. Что же касается [ВО3] -
треугольников, их существует два типа. Первый тип - симметричные треугольники с
тремя мостиковыми или двумя немостиковыми атомами кислорода. Другой тип -
асимметричные [ВО3] - треугольники, о наличии которых свидетельствуют две линии
в спектрах поглощения, тогда как симметричные треугольники [ВО3] дают только
одну линию на спектре.
I.4 Фторидные стёкла
.4.1 Составы фторидных стёкол
Началом активного изучения и использования фторидных стёкол принято
считать 1974 год, когда Мишель Поулайн синтезировал стекло состава ZrF4 - NaF -
BaF2 - NdF3(LaF3) [14].
До этого были известны стеклообразующие системы на основе BeF2 и ZnCl2.
Эти системы не получили распространения из-за очень большой гигроскопичности,
ограничений пропускания в ИК-области и токсичности (в случае фторида бериллия).
На сегодняшний день обнаружено большое количество стеклообразующих систем на
основе фторидов металлов. Для многих из них определены области стеклообразования
и найдены составы наиболее устойчивых к кристаллизации систем. Среди таковых
можно выделить группы:
ü стёкла на основе фторидов металлов IV группы - Zr, Hf, Th -
фторцирконатные, фторгафнатные, ториевые стёкла;
ü стёкла на основе AlF3 - фторалюминатные стёкла;
ü стёкла на основе фторидов переходных и редкоземельных
элементов, таких, как Zn, Cd, Pb, Ln, Y.
Из всех вышеперечисленных наиболее распространены и изучены
фторцирконатные стёкла. Для них основополагающей является система ZrF4-BaF2, в
которой область стеклообразования охватывает составы с концентрацией ZrF4 от 50
до 80 мол.%. Двухкомпонентные фторидные системы циркония и бария легко
кристаллизуются. Для их стабилизации, а также регулирования вязкости и
коэффициента преломления фториды циркония и бария частично замещают фторидами
редкоземельных элементов, щелочных металлов, алюминия, тория, индия и некоторых
других элементов [14].
Известны стёкла, содержащие тетрафториды гафния, тория. Эти системы
отличаются наличием более длинноволновой границы пропускания в ИК-области, но
менее устойчивы к кристаллизации.
I.4.2 Некоторые свойства фторидных стёкол
В таблице 1.2. приведены свойства наиболее изученного стекла состава
57ZrF4 - 34BaF2 - 5LaF3 - 4АlF3.
Таблица 1.2.
Некоторые свойства фторидных стёкол [14].
|
Физическое свойство
|
Величина
|
|
Температура размягчения
|
320°С
|
|
Температура плавления
|
513°°С
|
|
Плотность, г/см3
|
4,54
|
|
КТР, град-1
|
168·107
|
|
Теплопроводность,
Вт/см*град
|
6·103
|
|
Модуль Юнга, ГПа
|
55,1
|
|
Микротвердость, кг/мм2
|
250
|
|
Удельное сопротивление (20ºС), Ом/см
|
109
|
|
Показатель преломления
|
1,519
|
Стёкла на основе фторидов прозрачны в ультрафиолетовом, видимом, ближнем
и среднем ИК диапазонах. Коротковолновый край поглощения находится в районе 0,2
¸ 0,3 мкм, длинноволновый - 6 ¸ 9 мкм [14]. Такая величина
длинноволновой границы позволяет использовать фторидные стеклянные матрицы как
перспективные материалы лазеров среднего ИК-диапозона. В стёклах можно
создавать большие концентрации активных ионов, в частности редкоземельных.
Как говорилось выше, вид температурной зависимости вязкости стекла
является его характеристикой. Для фторидных систем эта зависимость в
координатах lg (η) - 1/T нелинейна. Энергия активации
существенно возрастает при вязкости ~105 Па·с. Это значит, что в расплаве
происходят структурные изменения по достижении этого значения. При высоких
температурах расплав фторидного стекла состоит из коротких цепей или колец из
групп МFn. Также при росте температуры понижается степень ассоциации, что
приводит к изменению энергии активации. Резкая температурная зависимость
вязкости является одной из причин образования центров кристаллизации, поскольку
даже незначительные перегревы расплава ведут к сильному снижению вязкости и
увеличению вероятности образования центров кристаллизации и скорости их роста.
Эффект кристаллизации проявляется даже для наиболее устойчивых фторидных стёкол
[14].
Параметр
ΔТ для фторидных стёкол довольно высок. Например, для
стекла ZBLAN с высоким содержанием фторидов лития и натрия разность между
температурой начала кристаллизации и стеклования составляет 100°°C, а для
стекла ZrF4 - BaF2 - LaF3 - YF3 - AlF4 - NaF (ZBLYAN) - 125ºС [15].
Прогресс в области систем передачи информации в значительной мере связан
с разработкой бескислородных оптических материалов, которые могут служить
основой для различных приборов с качественно новыми характеристиками.
Высокочистые галогенидные, в частности фторидные, стёкла перспективны для
изготовления оптических устройств, работающих в УФ, видимом и ИК диапазонах
спектра. Также эти материалы могут использоваться в качестве световодов,
волоконных лазеров и так далее [16].
Стёкла на основе фторидов редких земель и переходных металлов исследуются
прежде всего как материал для лазерных матриц, магнитных и электрических
преобразователей [14, 17].
I.4.3 Влияние иона F- на структуру щелочно-боратного стекла
В работе [18] авторы среди прочего сравнивают структуру и свойства стёкол
xМе2O·B2O3 и xМе2O·yLiF·B2O3 (Ме = Li, Na) и приходят к выводу, что при
переходе к тройной системе увеличивается проводимость, уменьшаются плотность и
температура стеклования. Для объяснения подобных явлений выдвинута гипотеза о
внедрении галогена в каркас щелочно-боратного стекла с образованием структурных
группировок [ВО3/2F]-. Авторы предполагают, что группа [ВО3/2F]- представляет
собой искажённый тетраэдр: избыточный отрицательный заряд сосредоточен на
фторе; щелочной катион зафиксирован со стороны фтора; длина связи B--F меньше,
чем B--O и имеет более ионный характер. Энергия диссоциации группировок
Me+[BO3/2F]- меньше, чем у исходных Me+[BO4/2]-, по мнению исследователей [18]
Поэтому образование смешанных борофторкислородных ионогенных групп находит
отражение в увеличении проводимости стекол.
Авторы публикации утверждают также существование двух координационных
состояний основного стеклообразователя - бора - в сетке стекла. В общем случае
образование связи B-F может происходить при замещении кислорода либо в тройных
группах бора, либо в тетраэдрах; фтор может способствовать переходу бора из
тройной координации в четверную.
Соотношение количеств 3- и 4-координированного бора зависит от отношения
[O]/[B]. Выбор этого отношения или исходного состава щелочно-боратного стекла
должен быть таким, чтобы в стекле присутствовало сопоставимое число тройных и
четверных групп бора. Именно при соблюдении этих условий авторы указывают на
изменение вида спектров комбинационного рассеягия света при увеличении
содержания фторида лития в системе (20-y)Li2O·yLiF·80B2O3. При полной замене
оксида фторидом (y = 20 мол.%) на спектре полностью исчезает пик,
соответствующий симметричным бороксольным кольцам, т.е. тройной координации
бора. Это подтверждает гипотезу о формировании тетраэдрических групп [BO3/2F]-
[18].
I.5 Люминесценция иона Er3+в стёклах, кристаллах и некоторых
стеклокристаллических системах
I.5.1 Свойства иона Er3+
Редкоземельный ион эрбия Er3+ представляет интерес в оптике и лазерной
технике, так как является f-элементом. Его электронная конфигурация на
последних уровнях такова: 4f125s25p65d06s2. Таким образом, f-подуровень
экранируется двумя последующими слоями при переходах f-f, которые очень
разнообразны и многочисленны у редкоземельных элементов и могут быть как
безызлучательными, так и люминесцентными. Также за счёт преимущественного
заполнения f-оболочки спектры пропускания и поглощения РЗ ионов узкие, в
отличие от второй группы активных лазерных ионов - ионов 3d, например, Cr3+
[19].
Энергетическая схема для иона эрбия в упрощённом виде представлена на
рис.1.10 [20].
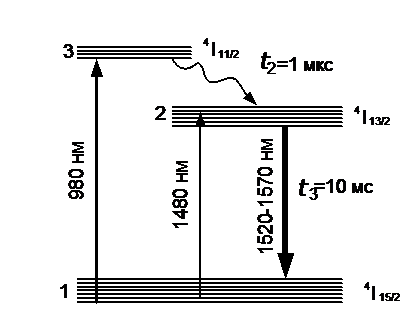
Рис.1.10
[20]. Упрощённая схема энергетических переходов Er3+ в кварцевом стекле. При
переходе 4I13/2→4I15/2 наблюдается люминесценция (λср ≈ 1,54 мкм).
В [20] рассматривается возможность применения эрбия в волоконном
усилителе.
Усиление света в эрбиевом усилителе происходит благодаря переходу между
уровнями 2→1 (4I13/2→4I15/2). Каждый из этих уровней расщеплён на
ряд подуровней из-за эффекта Штарка. За счёт поглощения фотонов накачки ионы
Er3+ переходят из основного состояния (уровень 1) в верхнее возбуждённое
(уровень 3), которое является короткоживущим (время жизни τ3=1мкс). За счёт процессов релаксации
ионы переходят в долгоживущее состояние - на метастабильный уровень энергии 2.
Термин «метастабильный» означает, что время пребывания иона на этом уровне
относительно велико (τ2=10мс). Поэтому число ионов, находящихся на уровне 2,
при соответствующей мощности накачки может превышать число ионов на уровне 1.
Уровень 1 называется основным состоянием, т.к. в отсутствии накачки практически
все ионы эрбия находятся в этом энергетическом состоянии. Доля частиц,
находящихся на остальных уровнях, в отсутствии накачки мала.
В отсутствии накачки населённость основного уровня максимальна, а
населённости возбуждённых энергетических уровней уменьшаются с увеличением
энергии уровня. Состояние, при котором населённость верхних уровней превышает
населённость нижнего, называется инверсией населённости. Если в среду с
инверсной населённостью попадает излучение с энергией фотона, совпадающей с
энергией перехода из метастабильного состояния в основное, то с большой
вероятностью происходит переход с метастабильного уровня 2 на основной уровень
1 с одновременным рождением ещё одного фотона. Увеличение числа фотонов при их
взаимодействии с ионами эрбия означает, что происходит усиление света,
распространяющегося в среде с инверсией населённости.
Не все ионы эрбия находятся в метастабильном состоянии и обеспечивают
усиление. Часть из них находится на уровне 1. Они взаимодействую с фотонами,
энергия которых совпадает с энергией перехода. Происходит эффективное поглощение
фотонов и переход на возбуждённый уровень 2.
Для создания инверсии населённости необходимо перевести примерно половину
ионов эрбия на метастабильный уровень 2. Мощность накачки оптического
усилителя, при которой населённость уровней 1 и 2 равны, называется пороговой
мощностью. По достижении пороговой мощности происходит «просветление» активного
волоконного световода, т.е. достигаются нулевые потери. При превышении
пороговой мощности накачки начинается усиление сигнала. В зависимости от
структуры активного волоконного световода, концентрации легирующей примеси и
длины волны накачки величина пороговой мощности составляет от долей до
нескольких мВт [20].
I.5.2 Люминесценция Er3+ в стёклах
В статье [21] рассматривается люминесценция эрбия в стекле состава
4ZnO-3B2O3. Стёкла варились в платиновом тигле при 1250°С в течение 4 часов; в
шихту добавлен 1 моль. % Er2O3. Затем образцы подвергали двенадцатичасовому
отжигу при 500°С. Далее образцы полировались для достижения оптического
качества, позволяющего применить спектроскопические исследования. Спектры
снимались в видимой и ближней ИК областях при комнатной температуре. Накачка
осуществлялась He-Ne лазером мощностью 25 мВт.
Ниже в таблице 1.3 приведены результаты расчётов вероятностей спонтанных
переходов А и излучательные времена жизни уровней τr для различных переходов.
Таблица 1.3.
Вероятности спонтанных переходов и времён жизни Er3+в цинк-боратном
стекле [21].
|
Исходный уровень
|
Конечный уровень
|
Вероятность спонтанного
перехода, А, с-1
|
Излучательное время жизни, r,
мс
|
|
4S3/2
|
4F9/2 4I9/2 4I11/2 4I13/2
4I15/2
|
1,0 105,3 66,7 830,9 2002,5
|
0,333
|
|
4F9/2
|
4I9/2 4I11/2 4I13/2 4I15/2
|
9,0 124,6 109,3 2149,2
|
0,418
|
|
4I9/2
|
4I11/2 4I13/2 4I15/2
|
3,0 85,3 193,1
|
3,554
|
|
4I11/2
|
4I13/2 4I15/2
|
42,1 245,0
|
3,483
|
|
4I13/2
|
4I15/2
|
228,4
|
4,378
|
Данные таблицы 1.3. подтверждают, что самым долгоживущим из рассмотренных
является уровень 4I13/2.
Возбуждение попадает c уровня 4S3/2 на уровень 4F9/2, с которого, в свою
очередь, происходит безызлучательная релаксация на 4I13/2. С возбуждённого
уровня 4I13/2 происходит переход с испусканием энергии на 4I15/2. На рисунке
1.11 сплошной линией показан спектр испускания Er3+ в цинк-боратном стекле.
Максимальный пик соответствует переходу 4I15/2 → 4I13/2. Длина волны
этого перехода составляет 1530 нм [21].
На этом же рисунке показан и спектр поглощения - пунктирная линия. Его
максимум практически совпадает с пиком испускания и равен 1528 нм.

Рис.
1.11 [21]. Спектры поглощения и испускания Er3+ в стекле 4ZnO-3B2O3 при
комнатной температуре. Сплошная линия - испускание, пунктир - поглощение.
Таким
образом, в исследованных стёклах [21] самым интенсивным для иона Er3+ является
переход 4I15/2 → 4I13/2 с длиной волны 1,53 мкм. Возможность получения
такого излучения РЗЭ в стекле, в частности, боратном, позволяет рассматривать
такие материалы в качестве лазерных.
Авторы
статьи [22] рассматривают легированное эрбием литий-боратное стекло. Рис.1.12
иллюстрирует вид спектров поглощения Er3+ в стекле LBO.
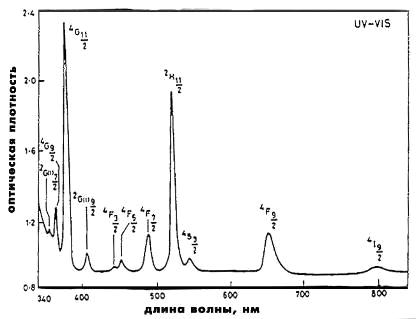
а)
видимая и УФ области;
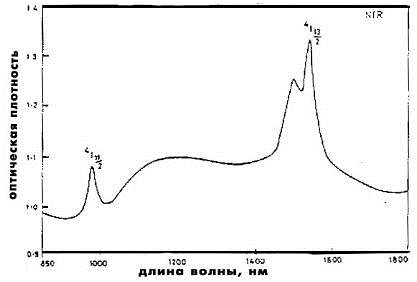
б)
ближняя ИК область
Рис.1.12
[22]. Спектр поглощения иона эрбия в литий-боратном стекле.
Главный
лазерный переход 4I15/2 → 4I13/2 лежит в ближней инфракрасной области
спектра. Авторы публикации [22] делают вывод о хороших оптических свойствах
редкоземельного иона эрбия в стеклянной матрице.
I.5.3 Люминесценция Er3+ в кристаллах
В [23] рассматриваются спектроскопические свойства иона эрбия в кристалле
YAl3(BO3)4 - YAB.
Кристалл YAl3(BO3)4 был выращен из расплава с использованием флюса
K2O/MoO3/B2O3 в соотношении 1:3:0,5. Шихта состояла из стехиометрической смеси
оксидов: Y2O3:3Al2O3:4B2O3 с добавлением оксида эрбия Er2O3 в количестве
0,01-0,15 атомов эрбия/моль YAB.
Кристалл YAl3(BO3)4 относится к тригональной сингонии - R32. Ионы иттрия
Y3+ занимают тригонально-призматические позиции аналогично ионам кислорода;
ионы Al3+ находятся в октаэдрической координации. Радиус иона алюминия меньше
радиуса иона иттрия, редкоземельный Er3+ встает в позиции Y3+ в соответствии с
геометрическими условиями [23].
Образцы рассматриваемого кристалла YAl3(BO3)4, легированного Er3+,
подвергались спектроскопии. Были получены спектры поглощения в при 100К в УФ,
видимой и ближней ИК областях (рис.1.13).
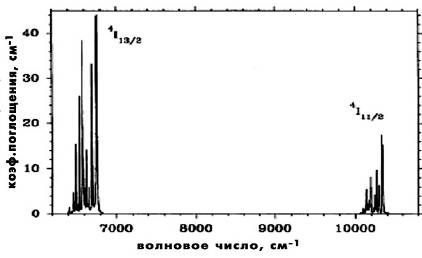
а) ближняя ИК область;

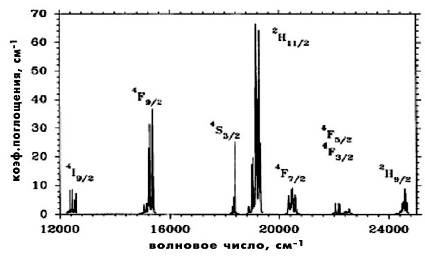
 б) видимая и УФ области.
б) видимая и УФ области.
Рис.1.13 [23]. Спектр поглощения Er3+ в кристалле YAB. Образец параллелен
направлению (0001).
Низкотемпературный спектр поглощения Er:YAB состоит из чётких острых
линий. Число спектральных линий и их форма подтверждают теоретические ожидания
исследователей [23], поскольку доказывает, что эрбий встраивается только в одну
специфическую подрешётку - позиции иттрия.
I.5.4 Люминесценция Er3+ в многокомпонентных системах
Люминесцентные свойства иона эрбия исследовались и в системах, содержащих
фториды, в том числе редкоземельных элементов. В этом случае нас прежде всего
интересует информация о воздействии на люминесцентные свойства трехвалентного
эрбия окружения фторидных ионов и кристаллических фаз фторидов, в частности,
LaF3. Поскольку ионами F- окружение активного лазерного иона отличается от окружения
в оксидных системах. Об этом речь пойдёт ниже. Также необходимо убедиться, что
при наличии компонента LaF3 в исходном стекле возможно образование этой фазы в
виде кристаллов при термообработке стекла.
В [24] рассмотрено образование кристаллической фазы в оксифторидном
стекле следующего состава: 16,5Al2O3·1,6AlF3·12,7LaF3·4,3Na2CO3·64,9SiO2,
легированного ErF3. Отмечено не только увеличение интенсивности высвечивания и
сужение линий люминесценции, но и изменение их вида (смещение максимума), от
типичного для стекла к типичному для соответствующего кристалла (рис.1.14).
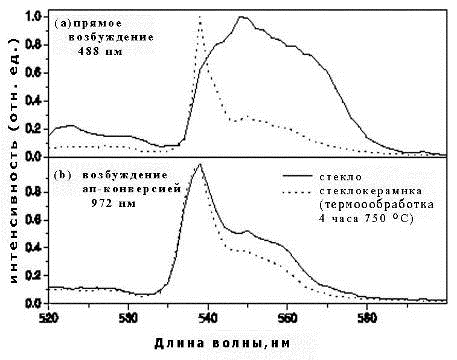
Рис.1.14 [24]. Спектр люминесценции Er3+ (переход 4S3/2 - 4I15/2) в
стекле и стеклокерамике при длине волны накачки а) 488 нм, b) 972 нм.
На рис.1.14 видно, что при прямом возбуждении спектр стеклянного образца
имеет вид, типичный для кислородного окружения иона Er3+, тогда как спектр
стеклокерамического образца имеет вид, типичный для фторидного окружения [24].
Такие изменения спектров так же подтверждают, что при термообработке выпадают
кристаллы фторида лантана.
Исследования кинетики флюоресценции, времён жизни на возбуждённом уровне
и кинетики ап-конверсии для стекла и СКМ, легированных Er3+, показало, что в
стеклянном образце есть два вида мест Er3+ - с короткими и длинными временами
жизни; в стеклокерамике имеется только один вид центров - с большими временами
жизни (рис.1.15).

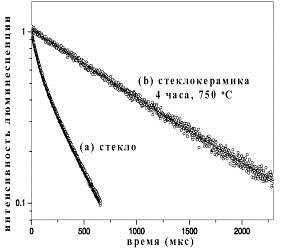
Рис. 1.15 [24]. Кривая затухания люминесценции иона Er3+
) при накачке 488 нм. 2) при накачке ап-конверсией 965 нм.
При ап-конверсионной накачке (рис. 1.27 (2)) так же наблюдается переход
от описываемой двумя экспоненциальными зависимостями кривой спада люминесценции
для стекла к описываемой одной экспоненциальной зависимостью кривой для
стеклокерамики. Увеличение времени жизни на возбуждённом уровне в
закристаллизованном стекле так же подтверждает, что выпадают фторидные
кристаллы [24].
Качество люминесценции Er3+ зависит от его окружения [25, 26], то есть от
матрицы, в которую его вводят. Например, если в состав входят гидроксильные
ионы ОН-, может наблюдаться тушение люминесценции, поскольку частоты колебаний
гидроксильных ионов лежат в интервале длин 2,77-3,57 мкм [25]. Локальное
окружение редкоземельного иона Er3+ оказывает влияние на оптические свойства
материалов. Это подтверждает спектр люминесценции - рис.1.16.
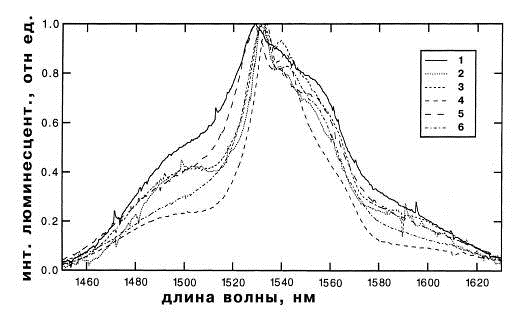
Рис. 1.16 [25]. Спектр люминесценции Er3+ в различных системах при
возбуждении светом с длиной волны 514,5 нм.
. фторидное; 2. силикофосфатное; 3. щелочнофосфатное;
. силикатное;.5. фторосиликатное; 6. алюмисиликатное.
Видно, что самый широкий спектр наблюдается во фторидной матрице. В
значениях длин волн пиков и ширины линий также имеется некоторое расхождение в
зависимости от состава образца, подвергавшегося исследованию. В таблице 1.4
приводятся величины длин волн пиков люминесценции эрбия в различных
многокомпонентных стёклах и значения ширины линии каждого из этих пиков.
Таблица 1.4.
Пики люминесценции Er3+ в различном окружении [25].
|
Стекло-матрица
|
Длина волны пика, нм
|
Ширина линии, нм
|
|
Алюмосиликатное
|
1532
|
59,3
|
|
Щелочносиликатное
|
1534
|
49,3
|
|
Фторосиликатное
|
1529
|
69,1
|
|
Щелочнофофатное
|
1532
|
67,9
|
|
Силикофосфатное
|
1531
|
61,2
|
|
Фторидное
|
1529
|
77,4
|
Таким образом, люминесценция активного редкоземельного иона сильно
зависит от состава стекла. Имеет место влияние локального окружения, как
сказано выше. Например, во фторидном окружении кординационное число Er3+
больше, чем в любом оксидном. В среднем, на 1 ион эрбия приходится 10 ионов
фтора на расстоянии 2,31Å [25,26].
I.6 Влияние фторидов РЗЭ на свойства оксидных стёкол
.6.1 Основные свойства фазы LaF3
Последняя глава литературного обзора посвящена фазе LaF3, поскольку мы
получаем стекло состава xBaO-yB2O3-0,2LaF3 с добавкой 1% масс. фторида эрбия.
Таким образом, при кристаллизации такого стекла возможно образование не только
барий-боратных кристаллических фаз, но и кристаллитов фторида лантана. Поэтому
кратко рассмотрим соединение LaF3 и его поведение при стеклообразовании и
кристаллизации стекла.
Кристаллы фторида лантана относятся к гексагональной сингонии с
параметрами кристаллической ячейки a=7,187Å, c=7,351Å. Пространственная группа Р63/mcm.
Плотность вещетсва сотавляет 5,01 г/см3. Температуры плавления и кипения
довольно высокие: 1493°С и 2330°С, соответственно. Это свойственно всем
фторидам РЗЭ. Фторид лантана, также как флюорит и ThF4, обладает минимальной
растворимостью в воде - ≤ 0,25 мг/л.
Среди фторидов можно встретить соединения с различными типами химической
связи. В молекуле LaF3 преобладает ионный тип связи, что объясняется большой
разницей в электроотрицательности металла и фтора. Известно, что фториды с
ионной химической связью характеризуются высокими значениями энергии
кристаллической решётки и высокими температурами плавления и кипения [27].
I.6.2 Влияние наличия фторида на стеклообразование и кристаллизацию
стекла на воздухе
С точки зрения стеклообразования более высокая степень ионности связи во
фторидных стёклах по сравнению с оксидными способствует большей упорядоченности
структурной сетки и, соответственно, уникальным оптическим свойствам:
минимальным значениям показателей преломления, максимальной дисперсии, узким
полосам люминесценции ионов-активаторов. Однако увеличение ковалентного вклада
связи компонентов фторидного стекла приводит к снижению температур плавления и
сохранению ближнего порядка стекла за счёт «замораживания» структуры фторида
при стеклообразовании.
На воздухе фториды, в том числе редких земель, часто подвергаются гидролизу
и пирогидролизу - взаимодействию с парами воды при высоких температурах. В
случае фторидов лантаноидов схема процесса такова:
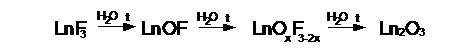
Таким
образом, чаще всего со фторидами работают в тщательно осушенной газовой среде [27].
В нашем случае работа осуществляется на воздухе. Поэтому следует иметь в
виду возможное присутствие кислорода. Наличие примеси кислорода во фторидах
резко меняет их химические и физические свойства - понижает температуры
плавления и перехода в высокотемпературные модификации (например, у трифторидов
РЗЭ), стабилизирует неустойчивые модификации (например, фазу высокого давления
у BiF3). Могут возникать ошибки при поиске новых фаз, поскольку и фторидная, и
оксофторидная фаза могут существовать одновременно либо диспропорционировать.
Яркий пример - фторид висмута, который в твёрдом состоянии оказался
оксофторидным образцом, поскольку существует в газообразной фазе как BiF и
диспропорционирует при охлаждении.
Другой экспериментальной проблемой является практическая неразличимость
ионов F- и O2- (или OH-) в твёрдых фазах. Возможность частичного замещения
фтора на кислород связана с близостью ионных радиусов (R(O2-)=1.36Å,
R(F-)=1.33Å), электронных
конфигураций и электроотрицательностей атомов фтора и кислорода. При помощи
рентгеноструктурного анализа различить атомы фтора и кислорода не удаётся из-за
близости факторов атомного рассеяния. Наиболее надёжным способом распознавания
является метод нейтронографии [27].
Однако в нашем исследовании такой анализ проводиться не будет, поэтому о
наличии тех или иных фаз в стеклокристаллическом образце будем судить по
результатам рентгенофазового анализа и спектров рамановской спектроскопии.
Также ион F- оказывает влияние на структуру стекла, о чём говорилось в
разделе I.4.4 настоящего обзора литературы.
I.7 Выводы из обзора литературы
1. Развитие оптики и фотоники требует получения новых материалов с
хорошими оптическими свойствами и обладающими химической стойкостью и
механической прочностью. Система ВаО-В2О3 с добавками фторидов редких земель
отвечает этим требованиям, вследствие чего является объектом исследований.
Стеклокерамика на основе барий-боратных стёкол с добавками фторидов РЗЭ должна
обладать многими уникальными свойствами, в том числе довольно широким интервалом
пропускания и высокой степенью прозрачности. К тому же технология получения
стеклокристаллического материала выгодна с экономической точки зрения.
2. Температуры стеклования барий-боратных стёкол лежат в интервале
450-605˚С. Составы стёкол находятся в пределах от 32 до 83 мол.% оксида
бора.
. Фториды могут играть роль катализаторов кристаллизации в
оксидных стёклах. Фторидный ион влияет на структуру барий-боратного стекла и
его физические свойства, в частности, понижает температуру плавления и величину
показателя преломления.
. Если при вынужденной кристаллизации системы ВаО-В2О3-LaF3,
легированной ионами Er3+, в качестве кристаллической фазы будет преобладать
фторид лантана, то материал должен проявлять спектроскопические свойства,
характерные для фторидных материалов.
II. Цели и задачи работы
Цель работы можно сформулировать так: получить прозрачный
стеклокристаллический материал в системе ВаО-В2О3-LaF3, в том числе
легированный ионами РЗЭ.
Задачи работы таковы:
1) синтезировать барий-боратное оксифторидное стекло;
2) посредством термической обработки при определённых условиях
провести кристаллизацию с целью образования кристаллитов фторида лантана;
3) изучить исходные свойства такого стекла, а также влияние
термообработки на свойства;
) для образцов, легированных фторидом эрбия, дополнительно
исследовать поглощение и люминесценцию иона Er3+, как в исходных стёклах, так и
в стеклокристаллическом материале.
III. Методика
эксперимента
.1
Характеристика реактивов
В работе были использованы реактивы, приведённые в таблице 3.1.
Таблица 3.1.
Исходные реактивы.
|
№ п/п
|
Название реактива
|
Химическая формула
|
Марка или квалификация
|
ГОСТ или ТУ
|
|
1
|
Оксид бора
|
В2О3
|
ОСЧ 12-3
|
ТУ 6-09-3558-79
|
|
2
|
Карбонат бария
|
Ва2СО3
|
ОСЧ 9-2
|
МРТУ 6-09-1605-64
|
|
3
|
Фторид лантана
|
LaF3
|
|
МРТУ-6-09-3069-66
|
|
4
|
Фторид эрбия
|
ErF3
|
ХЧ
|
МРТУ-6-09-3335-66
|
В работе применялись материалы, описанные в таблице 3.2.
Таблица 3.2.
Материалы,
используемые в работе.
|
№ п/п
|
Название материала
|
Марка
|
ГОСТ или ТУ
|
Свойства
|
|
1
|
Тигли корундовые
|
КВПТ-56
|
ТУ 1595-008-00188162-96
|
Емкость - 0,011 л Размеры
(мм): Д = 34+2; Д1 = 18+1; Sстенки = 1,5+3; Н = 26+2
|
|
2
|
Стержни нагревательные
силитовые (трубчатые с утолщёнными выводами)
|
КЭН АПС 8/150/150
|
ТУ 1598-001-00187046-97
|
Сопротивление - 1,6-3,3 Ом
Рабочая часть: d=8 мм, длина 150 мм максимальные температуры: 1500 оС - в
воздушной и нейтральной атмосфере, 1250 оС - в восстановительной
|
|
3
|
Графит
|
ОСЧ 7-4
|
|
|
|
4
|
Трубки из корундовой
керамики
|
|
|
Термопарные (с двумя
отверстиями)
|
|
5
|
Термопара
|
Термопара хромель-алюмель
(ТХА)
|
ГОСТ 6616-94
|
Диапазон измерения при
длительном измерении -200 ... +1000°С
|
III.2 Методика варки и отжига стёкол. Оборудование
Как говорилось в обзоре литературы, получение СКМ делится на два основных
этапа: изготовление образцов маточного стекла и последующий их отжиг с целью
кристаллизации.
III.2.1 Печь синтеза
Для синтеза стёкол была использована печь сопротивления с четырьмя
силитовыми стержнями КЭН АПС 8/150/150, схема которой представлена на рис. 3.1.
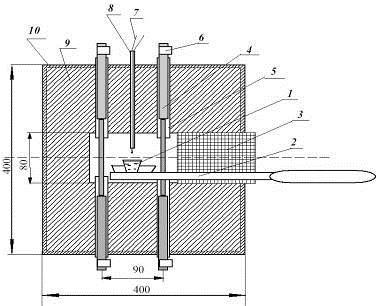
Рис.3.1. Схема печи синтеза.
- тигель с расплавом; 2 - держатель тигля; 3 - теплоизоляция (каолиновая
вата); 4 - силитовый стержень; 5 - керамическая трубка; 6 - хомутик для
подключения стержня к электропитанию; 7 - платиновая термопара; 8 -
керамическая трубочка для изоляции термопары; 9 - теплоизоляция (каолиновая
вата с шамотной крошкой); 10 - металлический корпус.
Температура в печи контролировалась платиновой термопарой. Регулирование
температуры осуществлялось тиристорным регулятором РИФ-101. Максимальная
температура составляла 1500 оС
ТермоЭДС измерялась вольтметром универсальным цифровым В7-38.
III.2.2 Печь отжига стекла
Для отжига сваренных стёкол применялась печь сопротивления со спиралью из
нихромовой проволоки. На рисунке 3.2 представлена схема печи для отжига и
термообработки маточного стекла.
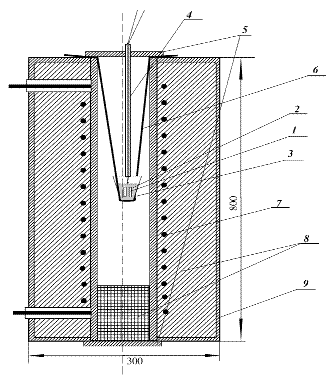
Рис.3.2. Схема печи отжига.
- образцы стекол; 2 - графитовая засыпка; 3 - тигель; 4 -
хромель-алюмелевая термопара; 5 - крышки; 6 - подвес тигля; 7 - нагревательная
проволока; 8- теплоизоляция; 9 - металлический корпус.
Температура в печи контролировалась хромель-алюмелевой термопарой и
задавалась с помощью ЛАТРа. Печь выходила на стабильный режим за 1 - 2 часа в
зависимости от необходимой температуры.
ТермоЭДС хромель-алюмелевой термопары измерялась терморегулятором ТП-400.
III.2.3 Вспомогательное оборудование
· Для
взвешивания шихты применялись торсионные весы WAGA TOSYJNA - WT (производства
Польши). Цена деления 2 мг, максимальная навеска 1000 мг, градуировка при 20 оС.
· Для измельчения и смешивания шихты была использована
вибромельница KM 1 с агатовой ступкой и агатовым шаром. Вибромельница снабжена
таймером и регулятором амплитуды колебаний.
III.3 Методика анализа полученных материалов
.3.1 Определение напряжений в стёклах
Так как охлаждение расплава при литье в форму происходит неравномерно, в
стекле могут возникать напряжения. Наиболее простым, наглядным и
распространённым методом определения наличия и величины напряжений в прозрачных
материалах является поляризационно-оптический метод, основанный на искажении
напряжениями конфигурации оптической индикатрисы. В результате шаровая
индикатриса оптически изотропного вещества превращается в эллипсоид вращения,
соответствующий оптически одноосным кристаллам. В итоге под действием
напряжений возникает двойное лучепреломление.
Закалочные напряжения растяжения уравновешиваются напряжениями сжатия,
поэтому в стекле должны наблюдаться участки с положительным и отрицательным
двупреломлением.
Напряжения наблюдались с помощью полярископа ПКС-500.
III.3.2 Дилатометрический метод
Дилатометрический метод определения температуры
стеклования стёкол [28] основан на исследовании зависимости расширения стекла
от температуры. На экспериментальной кривой термического расширения стекла при температуре,
соответствующей Tg, наблюдается перегиб. В измерениях использовался дилатометр
Ботвинкина.
III.3.3 Измерение микротвёрдости
Величина микротвёрдости стёкол и стеклокристаллических материалов
измерялась на микротвердомере ПМТ-3.
Твёрдость материала характеризует его способность сопротивляться
вдавливанию в него другого тела или царапанию. Эта величина не постоянна, а
является свойством, зависящим от прочности, пластичности, а также метода
измерения. Самыми распространёнными являются методы измерения твёрдости,
основанные на вдавливании в материал под определённой нагрузкой индентора. В
нашем случае индентором служит алмазная пирамида (метод Виккерса и Роквелла).
Индентор вдавливается в материал тем слабее, чем твёрдость материала выше.
Бывает необходимость измерения твёрдости отдельных микрофаз материала, граней
кристаллов, которые могут быть, к тому же, разных размеров. Поэтому имеет смысл
говорить о микротвёрдости материала [29].
Прибор ПМТ-3 представляет собой микроскоп, к тубусу которого прикреплён
специальный механизм: шток, подвешенный на пружинах, расположенных внутри
корпуса. В нижний конец штока вставлена оправка с штока. Поворотом столика
микроскопа подводится выбранный участок материала под алмазный индентор. Для
измерения отпечатков пирамиды алмазной пирамидкой, на утолщённую его часть
кладутся гири. С помощью специальных ручек осуществляется подъём, арретирование
и опускание установлен окуляр-микрометр. Угол при вершине алмазной пирамидки
составляет 136˚.
Величина микротвёрдости рассчитывается так:
H
= 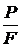 кг/мм2, (1)
кг/мм2, (1)
Где:
Р - нагрузка, кг;- боковая поверхность пирамиды отпечатка, которую для данной
пирамиды (α=136˚)
с длиной диагонали основания L вычисляют
по формуле:
 (2)
(2)
Учитывая значение α и подставляя в (1), окончательно имеем:
 кг/мм2
(3).
кг/мм2
(3).
III.3.4 Рентгенофазовый анализ
Рентгенофазовый анализ - РФА - в данной работе использовали для
идентификации состава фаз, выделяющихся при кристаллизации стёкол.
РФА заключается в том, что предварительно истёртые в порошок образцы
исследуются с помощью монохроматического пучка рентгеновских лучей. Если длина
волны рентгеновского излучения соизмерима с межатомными расстояниями в
кристаллическом теле, то возникает дифракционная картина, дающая информацию о
взаимном расположении атомов.
Метод основан на применении формулы Вульфа-Брэгга. Для упрощения описания
дифракционной картины допускают, что имеют место отражения только первого
порядка. Тогда формула Вульфа-Брэгга выглядит так:
2dhkl·sin θ = λ (4)
В формуле (4):- межплоскостное расстояние;
sin θ - синус угла отражения рентгеновских
лучей;, k, l - дифракционные индексы;
λ - длина волны рентгеновского излучения.
Рентгенограммы снимали на дифрактометре ДРОН-3М со скоростью съёмки
1о/мин (образец вращался в собственной плоскости) и шагом 0,05°. Съёмка
проводилась в интервале углов 2 = 10÷60 (излучение CuK c длиной волны =1,541874Å).
Режим трубки
БСВ-27(Сu)20mA, 30kV. Точность определения параметров решётки +5%·d.
Чувствительность - до 5% примесной фазы.
Обработка экспериментальных данных и интерпретация фазового состава
исследуемых образцов производится с помощью электронного каталога PCPDFWIN;
база JCPDS-ICDD.
III.3.5 Гидростатическое взвешивание
Гидростатический метод определения плотности (твёрдых тел состоит во
взвешивании образца на воздухе (масса m1) и того же образца, погружённого в
жидкость (масса m2) с известной плотностью (ж). При этом по закону Архимеда:
Измерения массы проводились на аналитических весах ВЛР-20 (абсолютная
погрешность показаний на всём диапазоне шкалы 0,05 мг, ГОСТ 24105-80). В
качестве жидкости использовалась дистиллированная вода (,99823 г/см3 при 20оС).
III.3.6 Спектры комбинационного рассеяния света
Одним из методов изучения структуры является метод комбинационного
рассеяния света (КРС). В основе метода лежит связь спектра КРС со структурой
исследуемого вещества.
Спектры КРС исследуемых образцов регистрировались при комнатной
температуре, при возбуждении непрерывным аргоновым лазером ILA-120. Рассеянное
излучение фокусировалось объективом на щель спектрометра, перед которой был
установлен анализатор. Для получения спектра использовался двойной монохроматор
фирмы «Spex» (модель 1403) с голографическими дифракционными решётками и
дополнительными щелями, которые вводились в действие с помощью поворотных
плоских зеркал, расположенных внутри монохроматора, обладающего крайне низким
уровнем паразитного рассеянного света от возбуждающей линии (Iv/Iv <
10-14 при v >20 см-1). Максимальное спектральное разрешение для
данного монохроматора составляло примерно 0,15 см-1. Регистрация сигнала КРС
производилась с помощью ФЭУ RСА-С31034 (с фотокатодом из GaAs), охлаждаемого до
240 К, подключённого через усилитель-дискриминатор к цифровому счётчику
фотонов, осуществляющему счёт импульсов сигнала за выбранное время накопления и
выдающий информацию в виде скорости счёта импульсов сигнала (импульсы в
секунду).
III.3.7 Измерение спектров пропускания в видимой и УФ области
Измерения спектров пропускания проводились на спектрофотометре SPECORD
M40 (двухлучевой спектрофотометр регистрирующий, с цифровой индикацией и
печатью). Спектральный диапазон 54 000 - 11 000 см-1 (185-900 нм). Оптическая
система - двойной монохроматор для УФ области спектра (предварительный
монохроматор - дифракционная решетка с 1302 штр./мм, главный монохроматор -
дифракционная решётка с 1302 штр./мм).
Источник излучения - дейтериевая лампа D2E для УФ области, галогеновая
лампа 6В, 20 Вт для видимой области. Приемник фотоумножитель, 11-ти каскадный,
фронтальный катод с ф50мм. Спектральная ширина щели ступенчато регулируется.
Точность волнового числа от +10 см-1 (0,03 нм) при 54 000 см-1 до +3см-1
(0,25 нм) при 11 000 см-1. Воспроизводимость волнового числа от +5см-1 (0,02
нм) при 54 000 см-1 до +1,5см-1 (0,1 нм) при 11 000 см-1. Фотометрическая
точность +0,005, фотометрическая воспроизводимость +0,002. Минимальное значение
шага 1 см-1.
стекло кристаллизация фторидный отжиг
III.3.8 Оптическая спектроскопия
Был проведён цикл спектроскопических исследований ионов Er3+ в стёклах и
стеклокерамике. Для измерений использовался двойной монохроматор СДЛ-1 с
набором стандартных светофильтров и различные источники возбуждения. Для
возбуждения люминесценции Er3+ использовались полупроводниковый лазерный диод
на основе AlGaAs с длиной волны излучения 803 нм, работающий в непрерывном
режиме. Сигнал регистрировался охлаждаемым фотоумножителем ФЭУ-83 и
оцифровывался осциллографом С 9-8, полученные спектры обрабатывались на
компьютере. Измерения проводились при комнатной температуре.
III.3.9 Дифференциальный термический анализ
Дифференциальный термический анализ (ДТА) даёт важную информацию для
ориентировочной оценки кристаллизационных свойств стекла и позволяет определить
характеристические температуры образцов, поскольку большинство фазовых
переходов при термообработке стёкол сопровождается большими экзотермическими
эффектами. Эти эффекты хорошо отражаются на дериватограммах ДТА - кривых ДТА.
Однако такие процессы, как размягчение стекла, плавление фаз, имеют
эндотермический эффект. По виду кривой также можно сделать выводы о склонности
стекла к ликвации. В нашем случае ДТА необходим для сравнения результатов
определения характеристических температур исследуемых стёкол дилатометрическим
методом.
ДТА проводился на дериватографе «Seteram»; в качестве эталона
использовался оксид алюминия -Al2O3.
В качестве образца стекла выбирали крупно дисперсионный порошок стекла
(размер 0,5-1мм), полученный после измельчения стекла просеиванием через сита с
разными размерами ячеек.
Образцы помещали в платиновые тигли так, чтобы спай термопары
непосредственно контактировал с образцом. Нагревание проводили при скорости
подъёма температуры 10оС/мин в диапазоне температур от 20 до 1200оС. Точность
определения температуры +2 оС.
Спектроскопические исследования материалов и ДТА проводились в Научном
центре Лазерных материалов и технологий Института Общей Физики РАН.
VI. Экспериментальная часть
IV.1 Синтез исходных стёкол
.1.1 Состав шихты и соотношения компонентов
Для проведения данной научно-исследовательской работы были выбраны
составы стёкол в системе xBaO·yB2O3·zLaF3 с различным соотношением массовых
долей оксидов бария и бора x и y, соответственно; параметр z выбирали
эмпирически: он составлял в разных экспериментах от 0,15 до 0,5. В таблице 4.1
приводятся соотношения и количества компонентов шихты, исходя из выбранного
состава. Легирование фторидом эрбия осуществлялось в количестве 1 масс.% ErF3
для каждого образца.
Таблица 4.1.
Количества исходных соединений.
|
№ п/п
|
Формула стекла
|
Количество компонентов, г
|
|
|
ВаСО3
|
В2О3
|
LaF3
|
ErF3
|
|
1
|
1,5ВаО·В2О3·0,5LaF3·0,01ErF3
|
6.38
|
1.50
|
2.11
|
0.10
|
|
2
|
ВаО·В2О3·0,5LaF3·0,01ErF3
|
5.41
|
1.91
|
2.64
|
0.10
|
|
3
|
ВаО·1.5В2О3·0,5LaF3·0,01ErF3
|
4.94
|
2.61
|
2.44
|
0.10
|
|
4
|
ВаО·В2О3·0,15LaF3
|
6.71
|
2.37
|
0.92
|
0
|
|
5
|
ВаО·1.5В2О3·0,15LaF3
|
7.40
|
1.74
|
0.73
|
0
|
|
6
|
1.5ВаО·В2О3·0,15LaF3
|
7.30
|
1.72
|
0.97
|
0
|
|
7
|
1.5ВаО·В2О3·0,2LaF3
|
5.2
|
3.06
|
1.15
|
0
|
|
8
|
1,5ВаО·В2О3·0,2LaF3·0,01ErF3
|
7.25
|
1.71
|
0.96
|
0.10
|
|
9
|
ВаО·В2О3·0,2LaF3·0,01ErF3
|
6.40
|
2.26
|
1.27
|
0.10
|
|
10
|
ВаО·1,5В2О3·0,2LaF3·0,01ErF3
|
5.76
|
3.05
|
1.15
|
0.10
|
|
Общее количество, г
|
63.30
|
22.0
|
14.34
|
0.60
|
Масса навески шихты для одного эксперимента составляла примерно 10г.
IV.1.2 Варка стёкол
Варка стёкол осуществлялась в корундовых тиглях в силитовой печи при
температурах 1150-1350оС на воздухе в течение 1-2 часов. Во всех случаях после
синтеза расплавы отливали в форму из стеклоуглерода, нагретую до 200-250оС.
Толщина образцов составляла около 6 мм. Фотография одного из образцов
сваренного стекла представлена на рис. 4.1.

Рис.
4.1. Вид сваренного стекла состава 1,5ВаО·В2О3·0,2LaF3·0,01ErF3
После литья в стёклах имеются термические напряжения, которые необходимо
снимать с помощью отжига.
В стёклах, в которых содержание LaF3 составляло 25 %мол. (параметр z =
0,5) при остужении расплава происходила ликвация. В результате такие стёкла
показывали уменьшение пропускания света, большое рассеяние, многочисленные
свили. Для получения стёкол таких составов лучшего качества необходимо
доработка технологии их синтеза, например, увеличение температуры синтеза и
увеличение скорости остужения расплава. В связи с этим для дальнейших
исследований были выбраны стёкла с z = 0,2.
IV.1.3 Термические напряжения в стёклах и отжиг
Термические напряжения сваренного стекла можно наблюдать на полярископе -
рис. 4.2 (а).


а) б)
Рис.4.2. Изображения стекла состава1,5ВаО·В2О3·0,2LaF3·0,01ErF3 в
поляристкопе:
а) до отжига; б) после отжига при 500°С в течение 2 часов.
Снятие термических напряжений и анизотропии свойств в стекле возможно с
помощью отжига при температуре стеклования Tg. В нашей работе снятие напряжений
проводилось при Т≈500°С. Такая температура близка к температурам
стеклования барий-боратных стёкол, согласно литературным данным [9]. Время
выдержки подобрано эмпирически так, чтобы после отжига на полярископе не
наблюдалось двулучепреломления (рис.4.2 (б)). В данном случае оптимальное время
- 2 часа. Охлаждение образцов проводилось со скоростями, не превышающими
5°С/мин.
IV.2 Определение характеристических температур стёкол
IV.2.1 Результаты дилатометрических измерений
Как сказано в главе III, для нахождения характеристических температур
стекла можно использовать дилатометрический метод. Для отожжённых при 500°С в
течение 2 часов стёкол составов ВаО·В2О3·0.2LaF3, 1,5ВаО·В2О3·0.2LaF3,
ВаО·1,5В2О3·0.2LaF3 были построены зависимости относительного удлинения
образцов от температуры, которые дают возможность определить температуры
стеклования Тg, температуры кристаллизации Тx, температуры максимальной
кристаллизации Тр и вычислить, соответственно, критерий устойчивости ∆Т.
Кривые расширения образцов приведены на рис.4.3. Измерения проводились по
два раза для каждого состава. Рисунок 4.3 представляет усреднённые результаты.
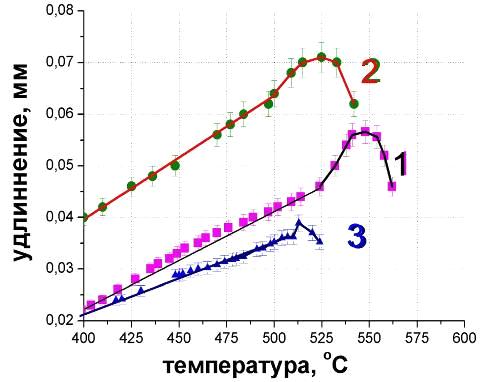
Рис.4.3. Кривые термического расширения стёкол.
- ВаО·1,5В2О3·0.2LaF3;
- ВаО·В2О3·0.2LaF3;
- 1,5ВаО·В2О3·0.2LaF3.
Таблица 4.2 содержит информацию о найденных по кривым расширения
характеристических температурах и критерии устойчивости исследуемых стёкол.
Таблица 4.2.
Результаты дилатометрических измерений.
|
№ п/п
|
Состав стекла
|
Темпера-тура стеклова-ния
Тg, оС
|
Темпера-тура
кристал-лизации Тx, оС
|
Темпера-тура максимальной
кристал-лизации Тр, оС
|
Устойчи-вость ∆Т, оС
|
|
1
|
ВаО·1,5В2О3·0,2LaF3
|
525
|
546
|
558
|
21
|
|
2
|
ВаО·В2О3·0,2LaF3
|
499
|
523
|
536
|
24
|
|
3
|
1,5ВаО·В2О3·0,2LaF3
|
508
|
521
|
533
|
13
|
Измерения проводились трижды для каждого состава. Ошибка определения
температур составляет ± 2
оС.
По данным таблицы 4.2 можно сделать следующие выводы:
§ температуры стеклования Тg лежат вблизи 500°С (режим отжига для снятия
термических напряжений был выбран верно);
§ устойчивость стёкол немного снижается с увеличением содержания оксида
бора;
§ температуры кристаллизации стёкол Тx системы xВаО·yВ2О3·LnF3 оказались
ниже температур кристаллизации бинарных барий-боратных cтёкол - таблица 1.1.
Дилатометрический метод позволяет определять значение коэффициента
линейного термического расширения стекла. По определению, КЛТР тела есть
относительное изменение его длины при изменении температуры на один градус;
объёмный КЛТР - аналогичное увеличение объёма материала. Графически значение
коэффициента термического расширения можно найти из уравнения усредняющей
прямой. Это есть тангенс угля наклона этой прямой, отнесённый к длине образца.
В таблицу 4.3 занесены результаты расчёта КЛТР исследуемых стёкол.
Таблица 4.3.
Величины коэффициентов линейного термического расширения исследуемых
стёкол.
|
№ п/п
|
Состав стекла
|
КЛТР, град-1·106
|
|
1
|
ВаО·1,5В2О3·0,2LaF3
|
9,55 ± 0,06
|
|
2
|
ВаО·В2О3·0,2LaF3
|
11,85 ± 0,08
|
|
3
|
1,5ВаО·В2О3·0,2LaF3
|
6,95 ± 0,05
|
Значения КТР довольно велики; при варьировании содержания оксидов бария и
бора его изменение незначительно.
IV.2.2 Результаты дериватографических измерений
Для проверки данных, полученных дилатометрическим методом, были проведены
дериватографические исследования стекла ВаО·1,5В2О3·0,2LaF3 с помощью
дифференциальной термопары.
Как указано в методике, в качестве эталона использовался -Al2O3;
скорость подъёма температуры 10 оС/мин.
На рис.4.4. приведена дифференциальная термограмма стекла
ВаО·1,5В2О3·0,2LaF3.
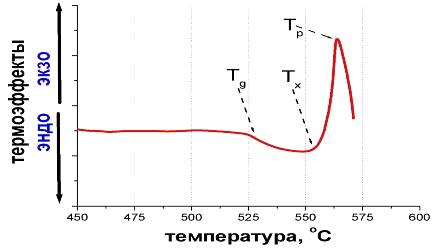
Рис.4.4. Дифференциальная термограмма стекла ВаО·1,5В2О3·0,2LaF3
Из рисунков
4.3. и 4.4. видно, что при измерении различными способами температуры
стеклования стекла практически совпали, а температуры кристаллизации и
максимальной кристаллизации, измеренные методом ДТА, оказались несколько выше
измеренных дилатометрически. Скорее всего, это связано с особенностями методов.
Таблица 4.4 показывает результаты сравнения значений найденных различными
методами характеристических температур.
Таблица 4.4.
Разница в значениях характеристических температур, измеренных разными
методами для стекла ВаО·1,5В2О3·0.2LaF3.
|
Метод
|
Температура стеклования Тg,
оС
|
Температура кристал-лизации
Тx, оС
|
Температура максимальной
кристал-лизации Тр, оС
|
Устойчи-вость ∆Т, оС
|
|
дилатометрический
|
525
|
546
|
558
|
21
|
|
ДТА
|
526
|
557
|
563
|
31
|
IV.2.3 Подбор условий термообработки с целью кристаллизации исходных
стёкол
Исходя из результатов дилатометрического анализа были выбраны режимы
термообработки стёкол с целью их кристаллизации. Для получения прозрачной
стеклокерамики условия термообработки таковы:
§ образцы состава ВаО·1,5В2О3·0.2LaF3 подвергали термообработке при температуре
550°С;
§ образцы состава ВаО·В2О3·0,2LaF3подвергали термообработке при температуре
525°С;.
§ образцы состава 1,5ВаО·В2О3·0,2LaF3 термически обрабатывалось при
температуре 535°С;
Образцы подвергались термообработке в несколько этапов для лучшего контроля
протекания кристаллизации. На первом этапе они выдерживались при необходимой
температуре 4 часа, на втором - ещё 4 часа.
Внешний вид не изменился, материалы не потеряли прозрачность. Кромки
оставались острыми (рис.4.5).

Рис.4.5. Внешний вид образцов состава ВаО·В2О3·0,2LaF3·0,01ErF3
- стекло, 2 - СКМ
Для исследования кристаллических фаз проводилась термообработка исходных
стёкол с целью получения непрозрачного стеклокристаллического материала,
содержащего большую долю кристаллической фазы. Для этой цели образцы
подвергались термообработке при температурах, значительно выше
характеристических.
IV.3 Подготовка плоскопараллельных образцов
Для измерения микротвёрдости и спектроскопических исследований образец
должен быть плоским, прозрачным и хорошо отполированным. Поэтому подготовка
стёкол и стеклокристаллических материалов включает в себя стадии шлифовки и
полировки. Каждая операция производилась поочерёдно для каждой стороны стекла
или стеклокерамического материала.
IV.3.1 Шлифовка
Обработка поверхности производилась на станке, снабжённом двигателем,
вращающим вал, на который надевается планшайба. Процесс осуществлялся с водой в
три стадии - с использованием планшайб различной зернистости для сокращения
времени шлифовки и улучшения качества поверхности: 200/160, 80/63, 40/28.
IV.3.2 Полировка
Полировка образцов проводилась на том же станке. В ряде случаев
отшлифованный образец наклеивали на кич при помощи мастики; затем производилась
полировка с использованием керамической планшайбы. По достижении необходимого
качества полировки кич нагревали для размягчения мастики и отклеивания образца.
Некоторые образцы полировались без кича (придерживались рукой) на оловянной
планшайбе без воды.
Качество поверхности оценивалось визуально. Толщина образцов в среднем
составила 3 мм.
IV.4 Измерение микротвёрдости
Для плоскопараллельных образцов, изготовленных как описано в главе IV.3,
были измерены микротвёрдости на микротвердомере ПМТ-3.
Рис.4.6 иллюстрирует результаты измерения микротвёрдости.
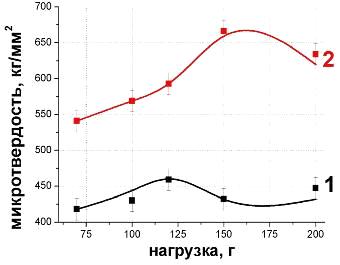

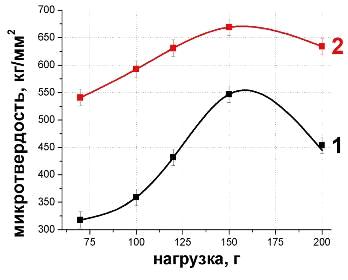
Рис.4.6. Зависимость микротвёрдости Н от нагрузки Р.
а - ВаО·1,5В2О3·0.2LaF3; б - ВаО·В2О3·0.2LaF3; в - 1,5ВаО·В2О3·0.2LaF3 (1
- стекло, 2 - СКМ).
Измерения проводились на обеих сторонах образцов, для каждой нагрузки
делалось по 5 отпечатков, каждый отпечаток измерялся дважды. Средняя
погрешность измерений составила ± 15 кг/мм2.
В таблице 4.5 приведены средние значения микротвёрдостей для каждого
состава до и после термической обработки. В данном случае «средней
микротвёрдостью» является среднее арифметическое из результатов нескольких
измерений.
Таблица 4.5.
Результаты измерения микротвёрдости.
|
Состав
|
Микротвёрдость, кг/мм2
|
% увеличения
|
|
До термообработки
|
После термообработки
|
|
|
ВаО·1,5В2О3·0,2LaF3
|
437
|
601
|
27
|
|
ВаО·В2О3·0,2LaF3
|
457
|
536
|
15
|
|
1,5ВаО·В2О3·0,2LaF3
|
422
|
613
|
31
|
Термообработка приводит к увеличению средней микротвёрдости. Это
свидетельствует о частичной закристаллизованности исследуемых стёкол после
термообработки. Значения микротвёрдости стёкол близки к таковым для многих
лазерных стёкол - силикатных, фосфатных, у которых эта величина находится в
интервале ~450-500 кг/мм2.
Наибольшее значение увеличения микротвёрдости показывают стёкла
1,5ВаО·В2О3·0,2LaF3, наименьшее - ВаО·В2О3·0,2LaF3.
График Н=f(P) позволяет вычислять также предел упругости материала и
предел текучести материалов. Предел упругости можно определить в случае, если
кривая зависимости имеет максимум. Тогда точка пересечения касательных к
участкам графика справа и слева от экстремума даст значение предела упругости
образца. Предел текучести можно определить по точке перегиба следующей за
максимумом. То есть для исследуемых материалов возможности прибора не позволяют
найти значение предела текучести, поскольку для используемого микротвердомера
предельная нагрузка составляет 200 г.
Таблица 3.6.
Передел упругости.
|
Состав
|
Передел упругости, кг/мм2
|
% увеличения
|
|
До термообработки
|
После термообработки
|
|
|
ВаО·1,5В2О3·0,2LaF3
|
469
|
683
|
31
|
|
ВаО·В2О3·0,2LaF3
|
520
|
618
|
16
|
|
1,5ВаО·В2О3·0,2LaF3
|
590
|
695
|
15
|
Таким образом, при образовании кристаллических фаз в стекле повышается
предел упругости материала.
IV.5 Измерение плотности
Для тех же образцов было проведено гидростатическое взвешивание (таблица
4.5). Наблюдается небольшое увеличение плотности после термической обработки в
течение 4 часов при температурах, несколько превышающих Тx. Это подтверждает
появление кристаллических фаз в стёклах. С увеличением концентрации оксида бария
плотность увеличивается, что согласуется с литературными данными о
барий-боратном стекле - таблица 1.1. Можно сказать, что, несмотря на наличие
фторидных компонентов, система ведёт себя аналогично барий-боратным без
содержания фторидов, однако значения плотностей данных стёкол ниже, чем
бинарных xBaO·yB2O3 с аналогичным отношением x:y, согласно таблице 1.1.
Как сказано выше, эти образцы были подвергнуты термообработке на втором
этапе выдержке в течение 4 часов. После второго этапа термообработки было произведено
повторное гидростатическое взвешивание.
Измерения проводились дважды для каждого образца, средняя погрешность
измерений составила ±
0,05 кг/мм2.
Таблица 4.5.
Плотности образцов по результатам гидростатического взвешивания.
|
Состав
|
Плотность, г/см3
|
% увеличения
|
|
до термообра-ботки
|
Термообра-ботка 4 часа
|
Термообра-ботка 8 часов
|
|
|
ВаО·1,5В2О3·0,2LaF3
|
2,96
|
3,03
|
3,20
|
7,5
|
|
ВаО·В2О3·0,2LaF3
|
3,17
|
3,22
|
3,30
|
4
|
|
1,5ВаО·В2О3·0,2LaF3
|
3,30
|
3,35
|
3,52
|
6,3
|
Наибольшие значения увеличения плотности показывают стёкла
1,5ВаО·В2О3·0,2LaF3, наименьшие - ВаО·В2О3·0,2LaF3, также как и значения
микротвёрдости.
По данным таблицы можно сделать вывод, что увеличение времени
термообработки при температуре выше температуры кристаллизации стёкол
способствует дальнейшей кристаллизации, о чём свидетельствует некоторое
увеличение значений плотностей.
Исходя из полученных результатов построен график зависимости плотности
исследуемых образцов от времени термической обработки при Т ≥ Тx -
рис.4.7.
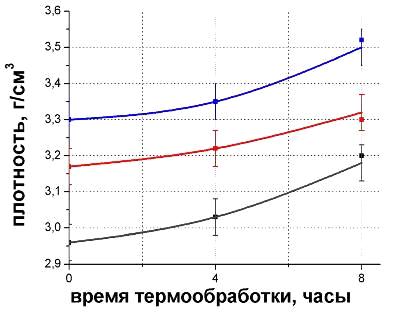
Рис. 4.7. Зависимость значения плотностей образцов от времени выдержки
при температурах, превышающих Тx.
. ВаО·1,5В2О3·0,2LaF3;
. ВаО·В2О3·0,2LaF3;
. 1,5ВаО·В2О3·0,2LaF3.
Кривые (рис.4.7) иллюстрируют тенденцию роста плотности материалов при
увеличении длительности термообработки. Это свидетельствует о продолжении
процесса образования кристаллитов в структуре стекла, как отмечалось выше.
IV.6 Определение фазового состава и структуры стеклокристаллических
материалов
IV.6.1 Определение кристаллических фаз, выделяющихся при
термообработке
После термообработки материал был изучен с помощью РФА. На рис. 4.8.
приведены рентгенограммы исходного стекла и СКМ.
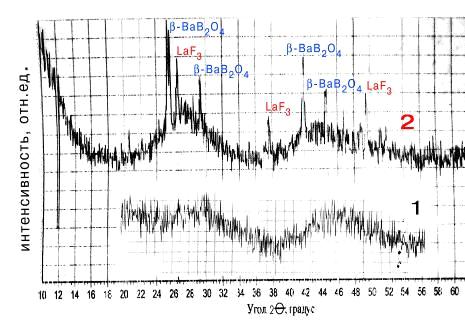
Рис. 4.8. Рентгенограммы 1) стекла, 2) стеклокристаллического материала
состава ВаО·В2О3·0,2LaF термообработка 525оС, 4 часа.
В стекле выделяются в основном две фазы - LaF3 и -BaB2O4.
Концентрация метабората бария превосходит концентрацию фторида лантана.
В некоторых случаях для получения нужных кристаллических фаз применяют
двухступенчатую термообработку, при этом первая короткая по времени стадия
происходит при температурах, значительно выше температуры пика кристаллизации.
Это позволяет селективно выделить только высокотемпературные кристаллические
фазы.
Исследовать подробнее фазовый состав кристаллитов при кристаллизации в
рассматриваемых стёклах позволяет получение непрозрачной стеклокерамики при
температурах, существенно превышающих Тх и Тр. На рис.4.9 приведены
рентгенограммы этих образцов.
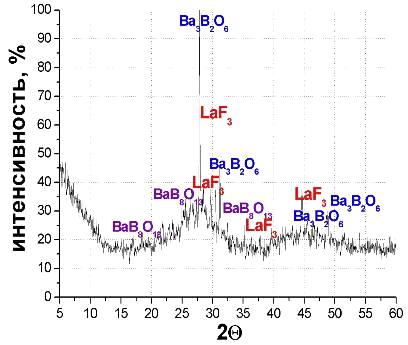
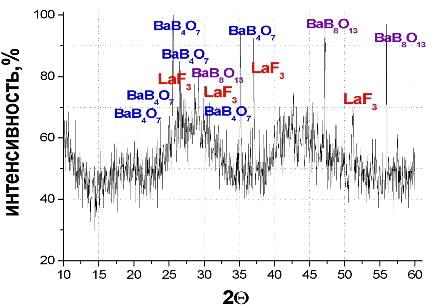
Рис.4.9. Рентгенограммы непрозрачных стеклокристаллических материалов.
а)ВаО·1,5В2О3·0,2LaF3, термообработка при 750ºС 4 часа;
б) ВаО·В2О3·0,2LaF3, термообработка при 900ºС 4 часа.
После термообработки при средних температурах 750оС образец получается
непрозрачным, (рис. 4.9 (а)): кристаллизуются барий-боратные фазы - Ва3В2О6 и
ВаВ8О13 - и фторид лантана в меньшей степени.
После термообработки образца ВаО·В2О3·0,2LaF3 при 900ºС состав барий-боратных фаз меняется:
вместо Ва3В2О6 появляются пики ВаВ4О7.
Таким образом, картина кристаллизации с ростом температуры термообработки
усложняется, появляются фазы, обогащённые барием по сравнению с составом
стекла. Видно, что во всех случаях кристаллизации выделяются различные
барий-боратные соединения и фторид лантана. Однако LaF3 не является основной
фазой ни при одном из выбранных режимов термообработки. Проводить двухстадийную
термообработку для увеличения доли фторида лантана в таком случае неэффективно.
IV.6.2 Определение структурных изменений в стекле при термообработке
Для определения структурных изменений в стекле при термообработке была
осуществлена попытка съёмки спектра комбинационного рассеяния света в частично
закристаллизованном образце.
Условия съёмки: 180-градусная геометрия рассеяния, длина волны
возбуждения 4880 Ǻ (20492 см-1) аргонового лазера, щели монохроматора 150
микрон.
Однако длина волны возбуждающего света поглощается ионами Er3+, что
приводит к возникновению интенсивной люминесценции, которая «засвечивает»
возможные линии КРС. (рис.4.10).
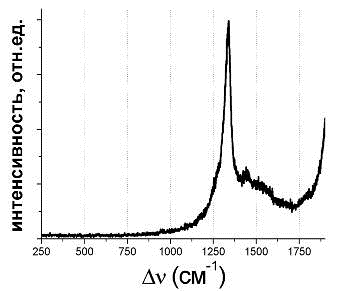
Рис. 4.10. Спектр, полученный при попытке снять КРС
стеклокристаллического материала состава ВаО·В2О3·0,2LaF3·0,01ErF3
(термообработка 525оС, 8 часов).
Таким образом, получить достоверный спектр КРС на образцах, содержащих
Er3+, не удалось. В дальнейших исследованиях подобных систем нужно использовать
нелегированные образцы.
IV.7 Спектроскопические исследования
IV.7.1 Спектр пропускания стёкол и стеклокристаллических материалов
На рис. 4.11 приведён спектр пропускания материалов состава
ВаО·В2О3·0,2LaF3·0,01ErF3 в видимой и ближней ИК области.
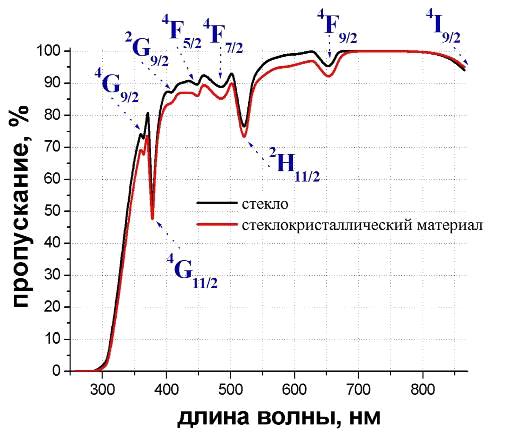
Рис.4.11. Спектр пропускания стекла и стеклокристаллического материала
состава ВаО·В2О3·0,2LaF3·0,01ErF3. Толщина образцов 3 мм
На спектре пропускания как стекла, так стеклокристаллического материала,
отчётливо видны практически все полосы поглощения, характерные для иона Er3+ в
стёклах (см. рис.1.12 (а)).
Коротковолновый край пропускания для стекла равен 339 нм, для СКМ - 343
нм. Край пропускания оксифторидного стекла смещён в длинноволновую область по
сравнению с чистыми барий-боратными стёклами.
Снижение пропускания в коротковолновой части спектра после термообработки
может служить косвенным подтверждением возникновения в материале большого числа
кристаллитов размерами до 100 нм. То, что в районе 700 нм пропускание стекла и
стеклокристаллического материала сравнивается и выходит на 100%,
свидетельствует о хорошем качестве СКМ и отсутствии в нём крупных рассеивающих
центров.
IV.7.2 Поглощение Er3+ в стёклах и стеклокристаллических материалах
Нами были исследованы спектры поглощения на уровень 4I11/2 (рис. 4.12.).
Поглощение в этом диапазоне важно для накачки эрбиевых лазеров, поскольку этот
уровень является короткоживущим и обеспечивает населённость нижележащего
метастабильного уровня 4I13/2.
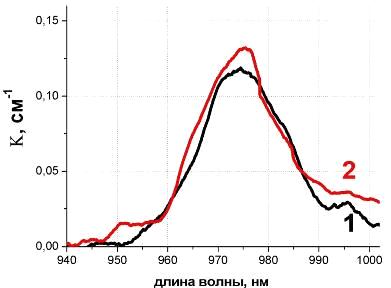
Рис. 4.12. Спектр поглощения Er3+ в материале ВаО·В2О3·0,2LaF3·0,01ErF3
на уровень 4I11/2 1 - стекло, 2 - СКМ.
Спектр поглощения, как стекла, так и стеклокристаллического материала,
представляет собой неоднородно уширенную полосу с максимумом в районе 975 нм и
полушириной около 20 нм для обоих спектров.
Интенсивность поглощения в стеклокристаллическом материале в районе
максимума немного превосходит интенсивность поглощения в стекле, что также
может служить подтверждением произошедших в стекле при термообработке
структурных изменений.
V. Заключение и выводы
1. В ходе работы были получены барий-боратные оксифторидные стёкла с
разным соотношением оксидов бария и бора и разной концентрацией фторида РЗЭ.
Выбранная методика позволила получить стёкла с содержанием LaF3 до 10 мол.%.
Для таких стёкол отработаны параметры синтеза и отжига.
2. Определены характеристические температуры для стёкол составов:
ВаО·1,5В2О3·0,2LaF3; ВаО·В2О3·0,2LaF3; 1,5ВаО·В2О3·0,2LaF3. По этим данным
выбраны режимы термообработки стёкол.
. Проведены термообработки стёкол в различных режимах, получены
прозрачные стеклокристаллические материалы, а также непрозрачные, содержащие
большую долю кристаллической фазы. Кристаллические фазы, выделяющиеся при
кристаллизации в разных режимах таковы: во всех случаях это различные
барий-боратные фазы (-BaB2O4, ВаВ4О7, Ва3В2О6, ВаВ8О13) и фторид
лантана.
. Исследовано влияние термообработки на свойства материалов. Показано,
что плотность возрастает после термообработки на 4-8%; микротвердость и предел
упругости возрастают на 15-30%; уменьшается пропускание в коротковолновой
области, край смещается в длинноволновую область на 4 нм.
. Исследовано поглощение иона Er3+ в стекле и прозрачном
стеклокристаллическом материале. Показано, что интенсивность поглощения в
стеклокристаллическом материале в районе максимума немного превосходит
интенсивность поглощения в стекле.
Таким образом, можно сделать вывод о том, что в системе ВаО-В2О3-LaF3
проведено исследование процесса кристаллизации стёкол, на основе которого
получен стеклокристаллический материал, по своим механическим и оптическим
свойствам отличный от исходного стекла.
VI. Охрана труда
VI.1 Краткая характеристика выполняемой работы
.1.1 Опасные и вредные производственные факторы
Экспериментальную часть данной дипломной работы можно разбить на
несколько этапов:
1. взвешивание компонентов шихты;
2. варка образцов стёкол;
. отжиг образцов для снятия термических напряжений либо с целью
кристаллизации исходного стекла;
. подготовка образцов для различного вида исследований.
На первом этапе возможно распыление порошков; на втором и третьем главную
опасность для здоровья представляет работа с электроприборами и высокие
температуры. На этапе подготовки образцов возможно также распыление частиц
стекла и СКМ. Самыми опасными этапами являются синтез и термообработка
материалов.
Вывод: при выполнении работы существуют следующие вредные и опасные
производственные факторы:
§ высокое напряжение - 220В
§ высокие температуры - максимально 1500°С
§ пыль реактивов и полученных образцов.
VI.1.2 Характеристика используемых веществ
Карбонат бария ВаСО3
Белый порошок; нерастворим в воде, но растворим в кислотах с бурным
выделением СО2. Тпл=1500°С, плотность 4,25 г/см3. При температуре выше 1000°С
диссоциирует на ВаО и СО2. Ядовит.
ПДК 0,5 мг/м3.
Класс опасности - 2.
Оксид бора В2О3
Бесцветное стеклообразное вещество; плавится в интервале 325-450°С.
плотность 2,46 г/см3, Ткип=2225°С. Термически стоек - не разлагается даже при
1000°С. Энергично ремгирует с водой, давая Н3ВО3. Расплавленный оксид бора
растворяет многие металлы.
ПДК 5 мг/м3.
Класс опасности - 3.
Вдыхание пыли В2О3 раздражает слизистые оболочки, попадание на кожу
вызывает зуд. Путь поступления в организм - ингалляционный. Вызывает
хронический бронхит [1].
Фториды РЗЭ - лантана, эрбия LaF3, ErF3- белые кристаллы. Фторид лантана
мало растворим в воде и разбавленных кислотах; растворяется в концентрированных
растворах щелочных металлов; Тпл=1427°С , Ткип=2327°С, плотность 5,93 г/см3.-
розовые кристаллы. Растворим в воде.
ПДК = 5мг/м3
Класс опасности - 3.
Вызывают изменения в лёгких, сердечный бронхит, снижение гемоглобина в
крови, сильно раздражают повреждённую кожу, накапливаются в коллагеновой
фракции костной ткани. В организм попадают ингалляционным путём [30].
Графит порошок С
Аллотропная модификация углерода. Жирное на вид вещество чёрного или
серо-чёрного цвета. Теоретическая плотность 2,27 г/см3.
Инертен при нормальных условиях. Окисляется на воздухе до СО2 выше 400°С.
С молекулярным азотом практически не реагирует. С большинством металлов и
оксидов, а также с неметаллами даёт карбиды.
Графит стоек к действию кислот, растворов солей, расплавов фторидов,
сульфидов, теллуридов, органических соединений, жидких углеводородов и др.,
реагирует с растворами щелочей, жидкими окислителями и рядом хлор- и
фторорганических соединений [31].
ПДК 4 мг/м3.
Класс опасности - 3.
При попадании в глаза возможны конъюктивиты, раздражение роговицы.
Раздражает и сушит кожу, может привести к образованию гнойничков, дерматитам,
аллергическим дерматозам. При попадании пыли на слизистые оболочки рта и носа
вызывает заболевания дёсен и зубов. При накоплении в лёгких выводится в течение
многих лет после прекращения работы [30].
VI.1.3 Режим личной безопасности
К работе в лаборатории допускаются лица не моложе 18 лет.
Лица, приступающие к работе в лаборатории, проходят личный инструктаж по
технике безопасности по технике безопасности. На рабочем месте каждый
работающий в лаборатории проходит первичный инструктаж. В дальнейшем необходим
повторный инструктаж не реже одного раза в год. Все лабораторные работы
проводятся в халатах; по мере необходимости используются резиновые перчатки,
защитные очки, маска, респиратор. Имеется аптечка, в которой находятся
медикаменты для оказания первой медицинской помощи. Также в каждой лаборатории
имеются средства пожаротушения: огнетушитель углекислотный, асбестовое одеяло.
Работы с горячими частями печи проводятся в брезентовых рукавицах [32,
33].
VI.2 Производственная санитария
.2.1 Помещения
Площадь лаборатории, в которой выполняется работа, составляет 16 м2,
объём лаборатории 56 м3. В помещении находится одновременно не более 2 человек
- исполнитель и руководитель. На одного человека приходится 8 м2 площади и 28
м3 объёма при норме 4,5 м2 площади и 18,7 м3 объёма на человека. Таким образом,
условия работы не противоречат санитарным нормам.
Выполнение дипломной работы не сопровождается значительным тепло- и
влаговыделением, не требует значительных энергозатрат исполнителя [33].
VI.2.2 Организация работы с вредными веществами
· При работе с порошками использовать респираторы типа
«Лепесток»;
· при хранении вредных веществ каждая банка или ёмкость должна
быть снабжена чёткой надписью;
· перед использованием внимательно прочитать надпись;
· работы проводить в вытяжном шкафу при включённой тяге, должна
работать вентиляция;
· остатки вредных и ядовитых веществ собирать в специальную
посуду;
· хранение обязательно в толстостенной посуде с притёртой
крышкой под тягой.
Правила поведения в аварийной ситуации:
работу прекратить, сообщить администрации. При просыпании большого
количества фторидов использовать противогаз, перчатки и собрать в
полиэтиленовый мешок.
признаки отравления: оцепенение, слабость, слюноотделение, судороги,
тошнота. Меры доврачебной помощи: промыть желудок 2% раствором соды, дать пить
молоко с яичным белком (2 яичных белка на стакан молока) и взвесь чистого мела.
средства индивидуальной защиты - респираторы ШБ-1 ("Лепесток"),
резиновые перчатки. [32,33].
VI.2.3 Метеорологические условия
В лаборатории поддерживается температура воздуха 18-20°С при допустимой температуре по
санитарным нормам 17 - 22°С,
влажность воздуха 55-60% (допустимо до 75%) [34].
VI.2.4 Вентиляция. Освещение
В лаборатории предусмотрена естественная вентиляция. По способу
воздухообмена естественная вентиляция является общеобменной и осуществляется
через форточку, окно и дверь.
Освещение комбинированное: естественное освещение боковое - окно 2x2,5 м
[6]. Для зрительных работ 4 класса точности КЕО = 1,5%.
Искусственное освещение - 16 люминесцентных ламп ЛД мощностью 30Вт. На
рабочем месте имеется настольная лампа мощностью 60Вт. Для зрительных работ 4
класса точности Е=300 лк.
Организация освещения соответствует нормам [35].
VI.2.5 Шумы и вибрации
Источники шумов и вибраций отсутствуют. Уровень шума в лаборатории
определяется ПС-45 [34].
VI.2.6 Водоснабжение. Канализация. Отопление
Источник воды - городской водопровод.
Лаборатория подключена к городской системе канализации.
Отопление центральное водяное. В зимний период обеспечивается температура
в помещении до 20°С [36].
VI.3 Техника безопасности
.3.1 Электробезопасность
В соответствии с [37] электробезопасность обеспечивается:
· конструкцией электроустановок;
· техническими способами и средствами защиты;
· организационно-техническими мероприятиями.
Требования по электробезопасности:
· к работе с действующими электроустановками допускаются лица
не моложе 18 лет, прошедшие предварительный медосмотр, прошедшие под расписку
инструктаж по данной инструкции и аттестацию на группу безопасности.
· категорически запрещается пользоваться открытыми реостатами и
плиткам, бытовыми электронагревательными приборами.
· запрещается оставлять без надзора установки под напряжением.
По поражению током помещение относится к категории с повышенной
опасностью.
Питание приборов осуществляется переменным током 220В частотой 50Гц.
Токовыводящие провода изолированы, заземлены [33].
VI.4 Пожарная профилактика
.4.1 Категорирование производственных помещений
и зон по пожаро-, взрывоопасности
· помещение относится к категории В по похароопасности; степень
огнестойкости здания - II.
· по взрывобезопасности: категория В-Iб [32, 39].
VI.4.2 Защита от статистического электричества
Т.к. все приборы заземлены, то условия для возникновения зарядов
статистического электричества отсутствуют.
VI.4.3 Средства пожаротушения
В лаборатории имеются следующие средства защиты и тушения пожаров:
асбестовое одеяло, огнетушитель ОУ-4 [38].
VII. Экономическая часть
VII.1 Технико-экономическое обоснование работы
Сегодня оптика и микроэлектроника стремительно развиваются, поэтому
необходим постоянный поиск новых материалов, обладающих лучшими с точки зрения
применения свойствами. Особенно важны материалы с нелинейно оптическими
свойствами. Существуют способы получения таких веществ в виде кристаллов путём
их выращивания различными методами. Распространён также и способ создания нано-
и микрокристаллических фаз в матрице стекла. Такие материалы называются
стеклокристаллическими (СКМ) или ситаллами.
Ситаллы - материалы искусственные, их получают кристаллизацией стёкол при
термической обработке последних. В 1953 г. Дональд Стукей опубликовал статью о
механизированном производстве новых материалов, и уже в 1957 г. он получил ряд
патентов на их изготовление. Первое официальное сообщение о создании новой
отрасли по превращению стекла в тонкокристаллическую «стеклокерамику» было
сделано фирмой «Дау Корнинг» 23 мая 1957 года. Новый материал получил название
«пирокерам». В ходе исследования новых материалов во всём мире им давались
различные названия. Например, в Англии СКМ называли «пиросил», «слагцерам»; в
Польше - «силитал», «квазикерам», «шлаковый квазикерам». В СССР подобные
силикатные поликристаллические материалы получили названия «ситаллы» или
«шлакоситаллы» [40].
Синтез ситаллов может быть осуществлён с учётом заранее заданных свойств.
Благодаря этому ситаллы могут отличаться каким-либо одним главным свойством,
например, механической или термической прочностью, химической устойчивостью,
износостойкостью, прозрачностью, или обладать комплексом необходимых свойств.
Это предопределило широкий спектр использования СКМ. В промышленных масштабах
ситаллы стали широко использовать с начала 60-х годов XX века. Сегодня они
широко используются в промышленности в качестве облицовочного материала,
элементов слоистых панелей в конструкциях промышленных зданий. Незаменим ситалл
и в быту. Из него изготавливают жаропрочную хозяйственную посуду - кастрюли,
жаровни, сотейники. Стеклокерамику применяют в авиационной промышленности,
например, в обтекателях ракет. Очень большое распространение в химическом
машиностроении получили стеклокристаллические покрытия, наносимые на
поверхность различных металлов для защиты их от коррозии, окисления и износа
при обычных и повышенных температурах. На предприятиях химической, коксохимической
и нефтеперерабатывающей отраслей промышленности используют ситалловые трубы
[1,40].
Всё шире области применения ситаллов в электронной промышленности. Их
используют в качестве диэлектрической изоляции микросхем и межслойной изоляции
печатных схем на керамических и других подложках. Ситаллы на основе горных
пород (перлита и доломита) рекомендуются для изготовления высоковольтных
стержневых и штыревых электроизоляторов. Стеклокерамические корпуса нашли
применение для герметизации полупроводниковых приборов и интегральных схем.
Литиево-алюмосиликатная стеклокерамика в сочетании с барийалюмосиликатным
стеклом в наши дни служит наполнителем в материалах для пломбирования зубов
[41].
Ситаллы разнообразны по составу, поскольку кристаллизации может быть
подвержено любое стекло при определённых условиях. Чаще всего для оптических
целей получают стеклокристаллический материал, который легируется ионом,
обладающим люминесцентными и лазерными свойствами. Также подбирается такой
состав исходного стекла, чтобы при кристаллизации образовывалась фаза, ценная с
точки зрения фотоники, в частности, обладающая нелинейно оптическим свойствами.
Целью данной дипломной работы является получение прозрачного
стеклокристаллического материала в системе ВаО-В2О3-LaF3 с добавлением ErF3 для
последующего исследования полученных образцов.
Такой состав выбран неслучайно. Фторидные стёкла - новый материал,
привлекающий много внимания. Разработки различных составов таких стёкол ведутся
в лабораториях всего мира. Эти материалы представляют интерес для применения в
качестве световодов, дисплеев, сцинтилляторов, лазерных окон.
β-борат бария также привлекательный
материал для оптики. Широкая область прозрачности указывает на перспективность
применения кристаллов низкотемпературного метабората бария в качестве
преобразователя частоты лазерного излучения в видимой и УФ областях спектра,
как сказано в главе «Обзор литературы» настоящей работы. К тому же, стёкла и
ситаллы на основе оксидов бария и бора обладают высокой прочностью, химической и
термической стойкостью.
Однако для успешного внедрения указанных материалов на рынок необходимо
тщательное изучение всех свойств веществ и испытания в качестве оптических
материалов. Следует поэкспериментировать с составами исходной шихты и
соотношениями реактивов; использование различных режимов термообработки стёкол
также даст возможность эффективнее получать ситаллы в рассматриваемой системе.
При успешных разработках фторидного стекла и барий-боратного СКМ с добавлением
редкоземельных ионов у потребителей появится новый материал для производства
оптических волокон, световодов, сцинтилляторов, преобразователей излучения в
широком спектральном диапазоне.
Поскольку работа носит научно-исследовательский характер, сделаем расчёт
затрат на НИР [42].
VII.2 Расчёт затрат на выполнение
научно-исследовательской работы
.2.1 Расчёт материальных затрат
Расчёт затрат на основные материалы работы производится по формуле:
См = ∑ Рi·Цi ,
где Рi - количество израсходованного i -го материального ресурса;
Цi - планово-заготовительная цена единицы i -го материального ресурса,
руб/ед;
= 1…n.
Расчёты сведены в таблицу 7.1.
Таблица 7.1.
Расчёт материальных затрат.
|
№
|
Наименование материального
ресурса, квалификация
|
Единицы измерения
|
Стандарт
|
Количество, г
|
Планово-заготовительная
цена, руб/г
|
Сумма, руб.
|
|
1
|
Карбонат бария ВаСО3 ОСЧ
9-2
|
г
|
МРТУ 6-09-1605-64
|
63,30
|
0,105
|
6,65
|
|
2
|
Оксид бора В2О3 ОСЧ 12-3
|
г
|
ТУ 6-09-3558-79
|
22,0
|
0,186
|
4,10
|
|
3
|
Фторид лантана LaF3
|
г
|
МРТУ-6-09-3069-66
|
14,34
|
3,422
|
49,07
|
|
4
|
Фторид эрбия ErF3
|
г
|
МРТУ-6-09-3335-66
|
1
|
54,2
|
54,2
|
|
5
|
Графит порошок ОСЧ 7-4
|
г
|
|
83,33
|
0,049
|
4,08
|
Итого: См = 118 руб. 10 коп.
VII.2.2 Расчёт затрат на электроэнергию
Затраты на электроэнергию составят:
Сэл/эн = ∑ Мi·K·Ti·Ц,
где Мi - паспортная мощность электрооборудования;
К - коэффициент использования мощности, К = 0,8-0,9;
Тi - время работы электрооборудования, ч;
Ц - цена 1 кВт·ч, руб/кВт·ч.
Результаты расчёта сведены в таблицу 7.2.
Таблица 7.2.
Расчёт затрат на электроэнегию.
|
№
|
Наимено вание оборудования
|
Число единиц оборудования
|
Номинал. мощность ед.
оборудования, кВт
|
Коэф. использо вания
мощности
|
Время работы обору дования,
ч
|
Цена за 1кВт·ч, руб/кВт·ч
|
Сум ма, руб.
|
|
1
|
Печь синтеза
|
1
|
2,2
|
0,9
|
100
|
1,5
|
297
|
|
2
|
Печь отжига
|
1
|
0,8
|
0,85
|
160
|
1,5
|
163,2
|
|
3
|
Весы аналити ческие
|
1
|
0,2
|
0,85
|
1
|
1,5
|
0,26
|
Итого: Сэл/эн = 460 рублей 50 коп.
VII.2.3Расчёт затрат на воду
Вода используется в работе только для хозяйственно-бытовых нужд.
Таблица 7.3.
Расчёт затрат на воду.
|
№
|
Вид ресурса
|
Израсходованное количество
|
Цена, руб/м3
|
Сумма затрат, руб
|
|
1
|
Вода холодная
|
8
|
13,5
|
108
|
Таким образом, Свод = 108 рублей.
VII. 2.4 Затраты на заработную плату и
отчисления на социальное страхование
Затраты на заработную плату складываются из зарплаты исполнителя -
студента - и его руководителя, а также зарплаты преподаватеоей-консультантов:
по охране труда, экономической части и охране окружающей среды.
Общая сумма затрат складывается из основной заработной платы и
дополнительной - Оотп - оплаты отпуска, равной 20% от основной суммы.
Заработная плата исполнителя (основная):
ЗПисп = См·n,
где См - месячная стипендия дипломанта, См = 1030 руб;= 5 - число
месяцев выполнения дипломной работы.
ЗПисп осн = 1030·5 = 5150 руб.
Основная заработная плата руководителя работы рассчитывается по формуле:
ЗПрук = Нр·Трук,
где Нр - общая нагрузка руководителя на дипломную работу студента, Нр =
35 часов;
Трук = 120 руб/час - часовая оплата труда руководителя; тогда:
ЗПрук осн = 32·120 = 3840 руб.
Оплата труда консультантов рассчитывается аналогично, учитывая:
Нр = 1 час, Тконс охр тр = 120 руб/час, Тконс эк = 130 руб/час, Тконс охр
ОС = 140 руб/час.
Тогда: ЗПосн конс охр тр = 120 руб, ЗПосн конс эк = 130 руб, ЗПосн конс
охр ОС = 140 рублей.
Суммарная дополнительная зарплата:
Оотп = 0,2(5150+3840+120+130+140) = 1876 рублей.
Единый социальный налог взимается в размере 26%:
ЕСН = 0,26(4230+1876) = 1588 рублей.
Итого: Сзп+ЕСН = 12844 рубля.
VII.2.5 Амортизационные отчисления
Сумма амортизационных отчислений определяется, исходя из стоимости
используемого оборудования и приборов, годовых норм амортизации и времени их
использования.
Сам = ∑[(Фi·Нрi·Ti)/100·12],
где Фi - стоимость оборудования (прибора) по данным кафедры, руб;
Нрi - годовая норма амортизационных отчислений;- время работы
оборудования (прибора), мес.
Результаты расчётов сведены в таблицу 7.4.
Таблица 7.4
Расчёт амортизационных отчислений.
|
№
|
Наименование
|
Стоимость, руб.
|
Время работы оборудования
(прибора), мес.
|
Но, %
|
Сумма амортизационных
отчислений, руб.
|
|
1
|
Печь отжига
|
12250
|
3
|
20
|
612,5
|
|
2
|
Печь синтеза
|
14500
|
2
|
20
|
483,3
|
|
3
|
Весы аналитические
|
14488
|
2
|
15
|
362,2
|
|
4
|
Нагреватель
|
100
|
3
|
10
|
2,5
|
Итого: Сам = 1460 рублей 50 коп.
VII.2.6 Накладные расходы
Накладные расходы включают затраты на страхование учебно-вспомогательного
и административно-управленческого персонала, освещение, вентиляцию, содержание
библиотеки, общежития, ремонт зданий и прочие хозяйственные расходы. Накладные
расходы составляют 100% от суммарной заработной платы.
Сн = 12844 рубля.
VII.2.7 Смета затрат на проведение дипломной
научно-исследовательской работы
Смета затрат на проведение дипломной НИР сведена в таблицу 7.5.
Таблица 7.5.
Смета затрат.
|
№
|
Статья затрат
|
Сумма, руб.
|
%
|
Примеча-ние
|
|
1
|
Затраты на сырьё и
материалы
|
118,1
|
0,42
|
|
|
2
|
Затраты на электроэнергию
|
460,5
|
1,65
|
|
|
4
|
Затраты на воду
|
108
|
0,39
|
|
|
3
|
Заработная плата основная:
- исполнителя - руководителя - консультантов Оплата отпуска
|
5150 3840 390 1876
|
18,50 13,80 1,40 6,74
|
|
|
5
|
ЕСН
|
1588
|
5,71
|
|
|
6
|
Амортизационные отчисления
|
1460,5
|
5,25
|
|
|
7
|
Накладные расходы
|
12844
|
46,14
|
|
|
ИТОГО
|
27835,1
|
100
|
|
По результатам расчётов можно сделать вывод, что данная НИР не носит
материалоёмкий и энергоёмкий характер и является трудоёмкой [42].
VII.3 Заключение
При успешных исследованиях и подборе оптимальных условий синтеза и
режимов изготовления ситаллов на основе барий-боратных стёкол с добавками
фторидов редкоземельных элементов появится возможность расширить спектр
оптических материалов, обладающих хорошей химической и термической стойкостью,
высокой плотностью, широкой областью прозрачности, нелинейно оптическими свойствами
образующихся кристаллических фаз. Такие свойства ценны с точки зрения
применения полученных ситаллов в качестве лазерных, сцинтилляторных материалов,
световодов и оптических волокон. Простая технология изготовления и возможность
варьирования формы изделий также является достоинством стеклокристаллических
материалов.
В масштабах дипломной работы затраты на сырьё, материалы, энергетические
и водные ресурсы составили 1,91% от суммарных затрат на выполнение
научно-исследовательской работы.
VIII. Охрана окружающей среды
VIII.1 Введение
Цель данного раздела состоит в установлении возможных экологических и
эколого-экономических результатов практического использования работы, а также
последствий проведения данной дипломной работы за время её выполнения.
Сегодня экологические проблемы с каждым годом усложняются. Главным
направлением развития промышленных предприятий является реконструкция
устаревших производств или строительство новых, работающих по принципу
ресурсосберегающих или безотходных технологий. Это позволит создать новый тип
производства, не нарушающий устойчивого функционирования биосферы [43].
Химия и химическая технология занимают важнейшее место в ускорении
научно-технического прогресса; ведётся постоянный поиск новых веществ и
материалов, а также разработки новых технологий и усовершенствование старых
методов синтеза. Для успешного дальнейшего развития науки и техники с
минимизацией ущерба окружающей среде необходимы квалифицированные специалисты.
VIII.2 Экологическое обоснование темы работы
Данная дипломная работа носит научно-исследовательский характер и состоит
в получении барий-боратного стекла, содержащего фториды редкоземельных
элементов La и Er, получении стеклокристаллического материала путём вынужденной
кристаллизации этого стекла в ходе его термической обработки при определённых
условиях. Полученные образцы исследуются различными физико-химическими методами
анализа для определения основных свойств и оценки пригодности синтезированных
ситаллов для применения в качестве оптических материалов, для изготовления
оптического волокна, использования в лазерной технике.
В целом, изготовление барий-боратных фторидных стёкол, легированных
редкоземельными элементами, для оптических целей малоотходно. Условно работа
делится на несколько этапов, на каждом из которых выделяется некоторое
количество отходов.
На этапе подготовки к синтезу стекла отходом является пыль порошков
исходных веществ, образующаяся в процессе их взвешивания и смешения. На этапе
варки стекла отходом является диоксид углерода, образующийся при разложении
карбоната бария на BaO, являющийся компонентом стекла, и СО2. Также диоксид
углерода выделяется при окислении порошка графита при синтезе. Пыль графита
также можно считать отходом, загрязняющим воздух. После получения стекла корундовый
тигель с малыми остатками шихты выбрасывается. Далее стекло подвергается отжигу
с целью снятия термических напряжений и кристаллизации. При исследовании
образцов СКМ (стеклокристаллический материал) на качественный состав - РФА -
необходимо получить порошок. Поэтому образуется пыль компонентов
стеклокристаллического материала. Жидких отходов в ходе выполнения работы не
образуется.
При выполнении работы в промышленных масштабах целесообразно было бы
повторно утилизировать остаток шихты и использовать тигель многократно, очищая
его после каждой варки ветошью, смоченной в этиловом спирте. Однако для
проведения исследований в рамках дипломной работы необходимость в этом
отпадает. Количества исходных веществ малы.
Ниже приводится упрощённая технологическая схема процесса, включающая
стадии, на которых образуются отходы.

VIII.3 Токсикологическая характеристика используемых
веществ
Карбонат
бария ВаСО3
Белый
порошок; нерастворим в воде, но растворим в кислотах с бурным выделением СО2.
Тпл=1500°С, плотность 4,25 г/см3. При температуре выше 1000°С диссоциирует на
ВаО и СО2. Ядовит.
ПДКрз
0,5 мг/м3.
Пыль
карбоната бария вызывает раздражение кожи и слизистых оболочек. Путь
поступления в организм - ингалляционный. Обладает гонадотропным и
эмбриотоксическим действием [30].
Оксид
бора В2О3
Бесцветное
стеклообразное вещество; плавится в интервале 325-450°С. плотность 2,46 г/см3,
Ткип=2225°С. Термически стоек - не разлагается даже при 1000°С. Энергично
ремгирует с водой, давая Н3ВО3. Расплавленный оксид бора растворяет многие
металлы.
ПДКрз
5 мг/м3.
Вдыхание
пыли В2О3 раздражает слизистые оболочки, попадание на кожу вызывает зуд. Путь
поступления в организм - ингаляционный. Вызывает хронический бронхит [30].
Фториды
РЗЭ - лантана, эрбия LaF3, ErF3- белые кристаллы. Фторид лантана мало растворим
в воде и разбавленных кислотах; растворяется в концентрированных растворах
щелочных металлов; Тпл=1427°С , Ткип=2327°С, плотность 5,93 г/см3.- розовые
кристаллы. Растворим в воде.
ПДКрз
= 5мг/м3.
Вызывают
изменения в лёгких, сердечный бронхит, снижение гемоглобина в крови, сильно
раздражает повреждённую кожу, накапливается в коллагеновой фракции костной
ткани. В организм попадает ингалляционным путём.
Графит
порошок С
Аллотропная модификация углерода. Жирное на вид вещество чёрного или
серо-чёрного цвета. Теоретическая плотность 2,27 г/см3.
Инертен при нормальных условиях. Окисляется на воздухе до СО2 выше 400°С.
С молекулярным азотом практически не реагирует. С большинством металлов и
оксидов, а также с неметаллами даёт карбиды.
Графит стоек к действию кислот, растворов солей, расплавов фторидов,
сульфидов, теллуридов, органических соединений, жидких углеводородов и др.,
реагирует с растворами щелочей, жидкими окислителями и рядом хлор- и фторорганических
соединений [31].
ПДКрз 4 мг/м3 (пыль графита в воздухе рабочей зоны).
При попадании в глаза возможны конъюктивиты, раздражение роговицы.
Раздражает и сушит кожу, может привести к образованию гнойничков, дерматитам,
аллергическим дерматозам. При попадании пыли на слизистые оболочки рта и носа
вызывает заболевания дёсен и зубов. При накоплении в лёгких выводится в течение
многих лет после прекращения работы.
Материал тигля - корунд α-Al2O3
Тугоплавкое вещество. Не взаимодействует с водой. Хорошо растворим в
расплавленном криолите. Амфотерен. Обладает высокой плотностью - 2,4 г/см3. Тпл
= 2046°С, Ткип=2980°С.
ПДК = 6 мг/м3.
Порошок оксида алюминия является аэрозолем фиброгенного действия [30].
Ниже приведена таблица 8.1, в которой приводятся основные загрязняющие
вещества и их характеристики в данной научно-исследовательской работе.
Таблица 8.1.
Перечень загрязняющих веществ.
|
№ п/п
|
Наиме-нование
|
Предельно допустимые
концентрации, мг/м3
|
Класс опас- ности
|
Количество образования
|
Приме-чания
|
|
|
ПДКрз
|
ПДКмр
|
ПДКсс
|
ВДКав*
|
|
усл т·104
|
т·104
|
|
|
|
|
|
|
|
|
|
|
|
|
1.1
|
BaCO3
|
0.5
|
0.01
|
0.004
|
0.011
|
4
|
0.033
|
|
|
1.2
|
Пыль графита
|
4
|
0.4
|
0.05
|
0.04
|
4
|
0.028
|
1.16
|
|
|
1.3
|
LaF3
|
5
|
0.46
|
0.5
|
0.046
|
3
|
0.014
|
0.2
|
|
|
1.4
|
В2О3
|
5
|
0.46
|
0.5
|
0.046
|
3
|
0.0120
|
0.118
|
|
|
1.5
|
ErF3
|
5
|
0.46
|
0.5
|
0.046
|
3
|
0.001
|
0.02
|
|
|
|
|
|
|
|
|
|
|
|
|
2.1
|
α-Аl2О3
|
6
|
|
|
|
4
|
|
|
|
* - значение временно допустимых концентраций в атмосферном воздухе
найдены из регрессионного уравнения lgВДКав i = 0,62lgПДКрз I - 1,77
VIII.4 Охрана атмосферного воздуха от
загрязнений
Всю пыль, попадающую в атмосферу, можно улавливать вытяжкой, снабжённой
фильтрами. В последующем отходы можно захоранивать, либо разделять. При малых
объёмах разделение нерационально. Специальная очистка воздуха не требуется
из-за малых количеств пыли.
VIII.5 Охрана водоёмов от загрязнения сточными
водами
В данной технологии жидких отходов нет. Вода используется исключительно
для хозяйственно-бытовых нужд.
VIII.6 Экологически безопасное обращение с
отходами
Твёрдыми отходами при выполнении данной дипломной работы считается
корундовый тигель с остатками шихты после синтеза исходного стекла. В силу
малых количеств остатков компонентов нецелесообразно очищать тигель и
утилизировать вещества повторно. К тому же, тигли часто портятся после
однократного использования.
В крупных масштабах возможна очистка тигля спиртом и повторное
использование материалов. В таблице 8.2 дано описание твёрдых отходов дипломной
работы.
Таблица 8.2.
Способы удаления твёрдого отхода дипломной работы.
|
№
|
Наи менование отхода
|
Опас- ные компо- ненты
|
Опасные свойства
|
Класс опасности
|
Способы удаления
|
Примеча ния
|
|
1
|
Корунд α-Al2О3
|
Оксид алюми- ния
|
В виде порошка является
аэрозолем фиброгенного действия
|
4
|
а) захоронение б)повторное
использование после промывки
|
Вариант б)-в случае больших
масш табов полу чения СКМ
|
VIII.7 Эколого-экономическая оценка ущерба
.7.1 Укрупнённая оценка эколого-экономического
ущерба от загрязнения атмосферы
Антропогенное загрязнение атмосферного воздуха происходит в результате
выброса в атмосферу химических веществ, наносящих вред населению и другим
реципиентам. Величина ущерба от выброса в атмсосферу Уатм рассчитывается по
формуле:
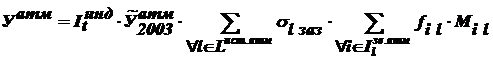 ,
,
где Itинд
- коэффициент, учитывающий инфляцию, равный 1,3 [44];
 =144
руб./усл.т. - удельный экономический ущерб от выброса 1т условного
загрязняющего вещества;
=144
руб./усл.т. - удельный экономический ущерб от выброса 1т условного
загрязняющего вещества;
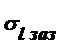 -
показатель относительной опасности зоны активного заражения (для центральной
части города с плотностью населения свыше 300000 человек
-
показатель относительной опасности зоны активного заражения (для центральной
части города с плотностью населения свыше 300000 человек 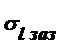 = 8,0 (табл.6.1 [43]);
= 8,0 (табл.6.1 [43]);
- 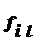 - поправка на характер рассеяния загрязняющих веществ
в атмосфере ( в нашем случае -
- поправка на характер рассеяния загрязняющих веществ
в атмосфере ( в нашем случае - 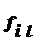 = 10
[43]);
= 10
[43]);
 -
приведённая масса годового выброса i-го загрязняющего вещества l-го источника.
-
приведённая масса годового выброса i-го загрязняющего вещества l-го источника.
Приведённая
масса Мil = Aiатм·mil (усл т/г).
Коэффициент
относительной агрессивности вещества Aiатм рассчитывается по формуле:
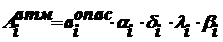 .
.
В
этом произведении:
аiопас
- показатель относительной опасности i-го воздействия вещества на человека
ингаляционным путём.
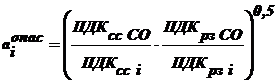
αi - поправка на возможность воздействия i-го вещества на человека
неингаляционным путём.
δi - поправка, связанная с возможностью воздействия вещества на других
реципиентов.
λi - поправка на вероятность повторного попадания вещества в атмосферу.
βi - поправка на вероятность образования вторичных более токсичных
веществ.
В таблице 8.3 сведены результаты расчётов приведённой массы выбросов.
Таблица 8.3.
Расчёт количества выбросов в атмосферу.
|
№
|
Вещество
|
ПДКрз, мг/м3
|
ПДКсс, мг/м3
|
аi, усл т/т
|
αi,
|
δi
|
λi
|
βi
|
Aiатм
|
mil (масса выброса) усл
т·104
|
масса Мil ·104 т
|
|
1
|
ВаСО3
|
0,5
|
0,004
|
173,2
|
1
|
1
|
1
|
1
|
173,2
|
0,033
|
5,72
|
|
2
|
В2О3
|
5
|
0,5
|
4,9
|
2
|
1
|
1
|
1
|
9,8
|
0,012
|
0,118
|
|
3
|
LaF3
|
5
|
0,5
|
4,9
|
2
|
1,5
|
1
|
1
|
14,7
|
0,014
|
0,2
|
|
4
|
ErF3
|
5
|
0,5
|
4,9
|
2
|
1,5
|
1
|
1
|
14,7
|
0,001
|
0,02
|
|
6
|
Пыль углерода графита
|
4
|
0,05
|
17,32
|
2
|
1,2
|
1
|
1
|
41,57
|
0,028
|
1,16
|
Итого: М = 7,218·10-4 усл т.
Ущерб от загрязнения атмосферы в ходе дипломной работы составит:
Уатм = 1,3·144·8·10·7,218·10-4 = 10 руб. 81 коп.
При улавливании пыли фторидов (гипотетически) ущерб составит:
Уатм = 10 руб. 50 коп.
Таким образом, в данной работе дополнительная очистка воздуха не является
целесообразной.
VIII.7.2 Укрупнённая оценка
эколого-экономического ущерба от загрязнения почв твёрдыми отходами
Загрязнения почвы происходит в данной работе только при выбрасывании
корундовых тиглей в ходе работы. Контейнер выбрасывается, затем захоранивается.
Вещество не является токсичныи и относится к классу малоопасных отходов. Отход
от шихты - её остаток на стенках тигля - пренебрежимо мал и, учитывая его
состав, не наносит существенного вреда окружающей среде. Концентрация
компонентов шихты не превышает их ПДК, поэтому плата за ущерб не взимается
(допустимый уровень загрязнения земель [43]).
Рассчитаем величину ущерба от загрязнения почвы веществом α-Al2O3
по формуле:
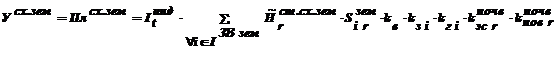 ,
,
где: 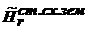 = 1445,6 тыс руб/га (Москва и Московская область) -
норматив стоимости освоения новых земель взамен изымаемых сельскохозяйственных
угодий (табл.8.3 [43]);
= 1445,6 тыс руб/га (Москва и Московская область) -
норматив стоимости освоения новых земель взамен изымаемых сельскохозяйственных
угодий (табл.8.3 [43]);
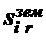 -
площадь загрязнённой территории, га;
-
площадь загрязнённой территории, га;
 -
коэффициент пересчёта для периода времени по восстановлению земель (табл.8.6
[43]);
-
коэффициент пересчёта для периода времени по восстановлению земель (табл.8.6
[43]);
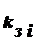 -
коэффициент, задающий степень загрязнения i-тым веществом [43];
-
коэффициент, задающий степень загрязнения i-тым веществом [43];
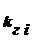 -
коэффициент, учитывающий глубину загрязнения земель i-тым веществом (табл.8.14
[43]);
-
коэффициент, учитывающий глубину загрязнения земель i-тым веществом (табл.8.14
[43]);
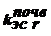 -
коэффициент экологической ситуации и значимости, учитывает фоновый уровень
загрязнения r-го региона (табл.10.7 [43]);
-
коэффициент экологической ситуации и значимости, учитывает фоновый уровень
загрязнения r-го региона (табл.10.7 [43]);
 -
повышающий коэффициент (
-
повышающий коэффициент ( =1 для данного случая [43]).
=1 для данного случая [43]).
Для
материала тигля - корунда:
Плсх
зем = 1,3·1445,6·103·10-4·3,8·0,3·1,3·1,6·1=445 руб.61 коп.
Плата за размещение отхода в пределах установленных лимитов
рассчитывается по формуле:
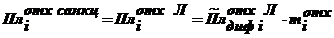 ,
,
где miотх
- масса отхода, т;
 ,
,
где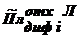 - дифференцированная ставка платежа за размещение i-го
отхода;
- дифференцированная ставка платежа за размещение i-го
отхода;
Плбаз
iотх Л - базовый норматив платы за размещение тонны отходов (497 руб/т
(табл.10.6 [43]).
Тогда
Плдиф iотх Л = 1,3·497·1,6·1=1033,76 руб/т.
Плата
за размещение отхода корунда при выполнении дипломной работы: 1033,76·50·10-6 =
0,05 руб.
Итого:
Упочв = 445 рублей 70 коп.
Общий
ущерб составляет 445,70+10,81 = 456,51 рублей.
VIII.8 Анализ рисков чрезвычайных (аварийных)
ситуаций
Главную опасность при выполнении данной дипломной работы представляют
электроприборы. Ток переменный частотой 50Гц, напряжение 220В. Несоблюдение
правил работы с электроустановками может вызвать поражение током или
возгорание. Для снижения риска аварийных ситуаций, связанных с электричеством,
оборудование заземлено и изолировано. Работа ведётся при соблюдении техники
безопасности. Других потенциально опасных для окружающей среды и людей факторов
нет.
VIII.9 Заключение
Получение и исследование стёкол и ситаллов в системе ВаО-В2О3-LaF3-ErF3 в
рамках научно-исследовательской работы малоотходно. Загрязнение атмосферы
происходит в результате распыления веществ при подготовке шихты для синтеза, а
также для изготовления образцов в виде порошков, в особенности для
рентгенофазового анализа. Компоненты шихты не обладают повышенной токсичностью,
поэтому эколого-экономический ущерб от загрязнения атмосферного воздуха
составил 12 рублей 37 копеек. Отход корундового контейнера после варки стекла
также не является токсичным при загрязнении материалом тигля почвы. Однако
ущерб составляет 445 рублей 70 коп. за счёт высокого норматива стоимости земель
на территории Москвы, где происходит выброс. Общий эколого-экономический ущерб
составил 458,07 рублей.
Основным аварийным риском являются последствия несоблюдения техники
безопасности при работе с электрическими приборами. Снижению вероятности аварии
способствует заземление и изоляция приборов, а также обращение исполнителя и
руководителя с электроустановками, которое должно строго соответствовать
требованиям безопасности.
Среди нерешённых проблем технологии является утилизация выбрасываемой в
атмосферу пыли, в частности фторидов редкоземельных элементов. Пыль может
улавливаться специальными приспособлениями и затем перерабатываться.
Стеклокристаллические материалы на основе ВаО-В2О3-LnF3 могут быть
использованы при изготовлении оптического волокна, световодов, сцинтилляторов и
так далее.
IX. Список литературы
1. Павлушкин
Н.М. «Основы технологии ситаллов». Учебное пособие для ВУЗов. М: Стройиздат,
1979.
. Саркисов
П.Д. «Направленная кристаллизация стекла - основа получения многофункциональных
стеклокристаллических материалов». М: РХТУ им.Д.И.Менделеева, 1997.
3. Артамонова
М.В. «Химическая технология стекла и ситаллов. Текст лекций». М: МХТИ
им.Д.И.Менделеева, 1984.
. C.A.Angel,
C.A.Scamehorm, D.J.List, J.Kieffer «Glassforming liquid oxides at the fragile
limit of the viscosity temperature relationship». Glass’89. Proc. XV Intern.
Congress on glass. 1989. V.1a. Leningrad. Nauka, 1989. P 204-209. 5.
. P.Lu,
Y.Wang, J.Lin, L.You «A novel synthesis route to rare earth polyborates».//
Chem. Commun, 2001, p.1178-1179.
. P.Pernice,
S.Esposito, A.Aronne, V.N.Sigaev «Structure and crystallization behavior o
glasses in the BaO-B2O3-Al2O3 system».// Journal of Non-Crystalline Solids,
v.258, 1999, p.1-10.
. Мазаев
Л.Я. Боратные стёкла. Изд-во Академии Наук БССР. Минск, 1958.
. S.
Kapoor, H. B. George, A. Betzen, Mario A.atigato, S. Feller. «Physical
properties of barium borate glasses determined over a wide range of
compositions». // Journal of Non-Crystalline Solids, v. 270, 2000, p. 215-222
. «Диаграммы
состояния систем тугоплавких оксидов. Справочник, выпуск 5 «Двойные системы»
ч.1». Ленинград, изд. «Наука», 1985.
. Шелег
А.У., Зуб Е.У., Стремоухова Л.А., Лугинец А.М. «Рентгенографические
исследования кристаллографических параметров и теплового расширения кристаллов β-ВаВ2О4».// Физика твёрдого тела,
1997, т.39, №6, с.1038-1040.
11. C.
Joo, U. Werner-Zwanziger, J.W. Zwanziger. The ring structure of boron trioxide
glass.// Journal of Non-Crystalline Solid, v.261, 2000, p. 282-286.
. Фёдоров
П.П., Соболь А.А., Ткаченко Е.А., Кононова Н.Г., Кох А.Е., Каргин Ю.Ф., Боярков
В.С., Закалюкин Р.М. «Фазовые равновесия при выращивании монокристаллов
метабората бария β-BaB2O4». Журнал Неорганической Химии, том 47,
№7, 2002., с.1150-1158.
13. <http://www.nsc.ru/win/sbras/rep/rep2002/t1-2/49/49.htm>,
Бердников В. С., Каплун А. Б. «Развитие научных основ технологии выращивания
совершенных объёмных оксидных многофункциональных монокристаллов».
. J. Lucas.// The
history of fluoride glasses. (Mater. Sci. Forum. Procceedings of the IVth
international Simposium on Halid Glasses. 26-29 January 1987). P. 3
. Дианов Е.М., Дмитрук
Л.Н. и др. «Волоконные световоды на основе высокочистых фторидных стёкол». //
Журнал «Высокочистые вещества», 1987, №3, с.10.
. L.Batterrati,
M.Baricco, M.Braglia et al. «Nucleation and growth of cristals in ZBLYAN
glasses» (Mater. Sci. Forum. Xth international Simposium on Non-oxid
Glasses.June 19-22, 1996, Corning, NY USA) P.77.
. Фёдоров В.Д.,
Сахаров В.В. и др. «Разработка высокочистых фторидных стёкол и световодов для
приборостроения», Рос. Хим. Ж. (Ж. Рос. хим. общества им.Д.И.Менделеева), 2001,
т.XLV, №5-6, с.51-57.
. Куприянов А.А.,
Карпухина Н.Г. «Оксигалогенидные силикатные стёкла». // Журнал «Физика и химия
стекла» Том 32, № 1, 2006 год.
. Конспект лекций
д.т.н., зав. Кафедрой химии и технологии монокристаллов Жарикова Е.В. по курсу
«Введение в физику лазеров».
. Курков А.С., Наний
О.Е. «Эрбиевые волоконные усилители» Lightwave Russian Edition, №1, 2003,
p.14-19.
. G. Pozza, D.Ajo
«Absorption and luminescence spectroscopy of Nd3+ and Er3+ in a zinc borate
glass». // Solid State Communications, Vol.97, №6, 1996, p.521-525.
. A.Renuka Devi,
C.K.Kayasankar «Optical properties of Er3+ ions in lithium borate glasses and
comparative energy level analyses of Er3+ ions in various glasses».// Journal
of Non-Crystalline Solids, v.197, 1996, p.111-128.
. I.Foldvari,
E.Beregi, A.Munoz F., R.Sosa, V.Horvath «The energy levels of Er3+ ion in YAB
single crystals».// Optical Materials, v.19, 2002, p.241-244.
. Goutaland, P.
Jander, W.S. Brocklesby, Guojun Dai. «Crystallization effects on rare earth
dopants in oxyfluoride glass ceramics». // Optical Materials, v.22, 2003, p.383-390.
. P.M. Peters 1, S.N.
Houde-Walter «Local structure of Er3+ in multicomponent glasses».// Journal of
Non-Crystalline Solids, v.239, 1998, p.162-169.
. Matthew J. Dejneka
«The luminescence and structure of novel transparent oxyfluoride glass-ceramics».//
Journal of Non-Crystalline Solids, v.239, 1998, p. 149-155
. Ардашникова Е.И.
«Неорганические фториды».//Соросовский образовательный журнал, том 6, №8, 2000,
с.54-60.
. Павлушкин Н. М.,
Сентюрин Г. Г., Ходаковская Р. Я. «Практикум по технологии стекла и ситаллов».
М.: Изд-во литературы по строительству, 1970, с.297-300.
. А.А.Майер
«Лабораторный практикум по кристаллооптике», М.: МХТИ им.Д.И.Менделеева, 1973
год.
. «Вредные и
химические вещества в промышленности. Неорганические вещества I-IV групп. Справочное
издание» под ред. Филова В.А. Л.: Химия, 1988.
. Веселовский В.С.
«Угольные и графитовые материалы», М., 1966г.
. Г.В.Макаров,
А.Я.Васин и др. «Охрана труда в химической промышленности» М.:Химия, 1989.
. Паспорт лаборатории
№413 каф. Химии и технологии монокристаллов, РХТУ им.Д.И.Менделеева.
34. Санитарные
нормы проектирования промышленных предприятий СН 245-71 М.: Госстрой, 1972,
97с.
35. СНИП
23-05-95 Естественное и искусственное освещение: Минземстрой России - 1998г.
. СНиП
33-75. Отопление, вентиляция и конденсация воздуха. М.: Стройиздат, 1982.
. ГОСТ
12.1.019-79. ССБТ. Электробезопасность. Общие требования.
. Дудин
В.В. и др. «Методические указания по разделу «Охрана труда» в дипломных
проектах и работах» М.: типография МХТИ им.Д.И.Менделеева, 1990.
. НПБ-105-95
Определение категорий помещений по взрыво-пожароопасности. М. - МВД России -
1987г.
. Макмиллан
П. У., “Стеклокерамика”, пер. с англ., М., 1967.
. Бережной
А.И. “Ситаллы и фотоситаллы”. - М., Машиностроение, 1981.
. Методические
указания по выполнению экономической части дипломного проекта (работы) для
студентов всех химико-технологических специальностей. РХТУ им. Д.И. Менделеева;
Сост.: К.И. Бурмистров, Л.И. Кошкин, Н.С. Маркина, Л.Ф. Поспелова. М., 1995 г.
. Н.П.
Тарасова, Б.В. Ермоленко, В.А. Зайцев, С.В. Макаров «Охрана окружающей среды» в
дипломных проектах и работах. Методическое пособие, Москва, 2006.
. Закон
«О федеральном бюджете на 2006 год», статья 21.