Расчет основных параметров горения и взрыва
Введение
Горение - основной процесс на пожаре, поэтому
изучение явления горения следует начинать с рассмотрения механизма протекания
элементарных реакций, а затем переходить к представлениям о нем на уровне
брутто - реакций с позиций общей и химической термодинамики. Такой подход к
проблеме горения обеспечивает понимание разнообразных практических вопросов, с
которыми сталкиваются специалисты пожарной охраны в своей повседневной
деятельности, будь то профилактика пожаров, динамика их развития или же вопросы
тушения.
На молекулярно - кинетическом уровне
представлений о химических реакциях возможность возникновения и протекания
горения обусловлена числом и энергией столкновения молекул горючего и
окислителя. В свою очередь оба этих параметра являются функцией температуры. С
увеличением температуры возрастает скорость теплового движения молекул,
увеличивается число эффективных соударений, появляются условия для реагирования
горючего с окислителем, т.е. возникновения и развития горения. Здесь уместно
вспомнить законы химической кинетики, которые изучались в курсе общей химии.
Представив, как протекают реакции в горючей
смеси на молекулярном уровне, становится понятным смысл суммарных характеристик
процесса - скорости и теплового эффекта. При изучении этого материала обратите
внимание на основные законы химической кинетики, зависимость скорости реакции
от температуры (закон Аррениуса) и давления горючей смеси, закон действия масс,
т.е. увеличение скорости реакции с возрастанием концентрации реагентов.
Скорость реакции максимальна при стехиометрическом составе смеси.
Соответственно при этой концентрации максимальна и интенсивность тепловыделения
экзотермических реакций.
Упомянутые вопросы из раздела химической
кинетики важны в физике и химии процессов горения для объяснения понятий
концентрационных пределов воспламенения, механизма действия огнетушащих
веществ, гасящего влияния «холодной стенки» и т.д.
Законами химической кинетики строго можно
описать только один вид горения - гомогенное кинетическое, когда горючее и окислитель
находятся в одной фазе и предварительно перемешаны, тогда скорость собственно
химической реакции зависит от природы реагирующих веществ. Но поскольку
интенсивность протекания процесса горения зависит в общем случае от характера
передачи вещества и тепла в зону реакции, т.е. от движения газа, пара, воздуха,
диффузии и теплопроводности, то степень подготовленности горючей смеси в
газодинамические условия, в которых находится горючая смесь, оказываются
факторами, определяющими все параметры горения на пожаре. Следует различать
диффузионное и кинетическое горение, гомогенное и гетерогенное, ламинарное и
турбулентное, знать, что степень турбулизации газового потока определяется
числом Рейнольдса и зависит от плотности и вязкости среды, скорости потока, его
поперечного сечения. При Re<Reкр, равного 2300, движение носит ламинарный
характер. При более высоких числах - турбулентный, что в значительной степени
определяет режим горения.
Вид горения, его параметры определяются
физическими процессами и условиями, они являются доминирующими, но в основе
горения лежит химическое превращение горючего и окислителя в продукты горения.
Поэтому все характеристики процесса горения в конечном итоге определяются
условиями протекания химической реакции. В этой связи важно уметь составлять
уравнения материального и теплового баланса реакции горения, учитывать влияние
коэффициента избытка воздуха на состав продуктов горения и температуру горения,
т.к. они определяют пожароопасные характеристики веществ и материалов, дают возможность
оценивать реальную обстановку на пожаре и правильно организовывать деятельность
пожарных.
Исходные данные
|
Номер
варианта
|
Номер
задачи
|
|
1
|
1,
2, 4, 5, 6
|
|
2
|
1,
3, 4, 5, 6
|
|
3
|
2,
3, 4, 5, 6
|
|
4
|
1,
2, 4, 5, 6
|
|
5
|
2,
3, 4, 5, 6
|
|
6
|
1,
3, 4, 5, 6
|
|
7
|
1,
2, 4, 5, 6
|
|
8
|
2,
3, 4, 5, 6
|
|
9
|
1,
2, 4, 5, 6
|
|
10
|
2,
3, 4, 5, 6
|
Задача 1
Вычислить состав и объем продуктов горения
соединения анилин, если горение протекает при коэффициенте избытка воздуха aВ=1.1,
потери тепла излучением зоны горения составляют h=0.20, %.
Решение. Из возможных способов решения задачи
следует остановиться на расчете объема воздуха и продуктов горения по уравнению
химической реакции, т.к. в условии задачи указана химическая формула горючего
вещества (или ее можно записать по названию соединения). Следовательно,
необходимо записать уравнение реакции горения анилина в воздухе:
H5NH2+7.75O2+7.75×3,76N2=6CO2+3.5H2O+7.75×4,76N2.
Определив молекулярную массу горючего, можно,
составив пропорцию, рассчитать и количество воздуха, необходимое для сгорания
анилина, а также и объем продуктов горения.
Молекулярная масса анилина=93
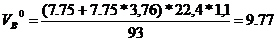 м3/кг
м3/кг
Действительное количество воздуха с
учетом коэффициента избытка воздуха aВ=1,3
рассчитывается по выражению: VВ=1,1×9.77=10.75 м3, а избыток воздуха: VВ-VВ0=10.75-9.77=0.98
м3.
Объем продуктов горения также
определяется по уравнению реакции: из 93 кг анилина образуется 6×22,4 м3
углекислого газа, 3.5×22,4 м3
водяного пара, 7.5×4,76×22,4 м3
азота, расчетный объем продуктов горения анилина находятся из выражения:
 м3.
м3.
С учетом избытка воздуха полный
объем продуктов горения:
VП.Г. =
10.89+9.77=20.66 м3.
Определяем низшую теплоту сгорания
анилина:
н = ∑(ni*∆HI-nj*∆Hj)
Теплота образования анилина=29.7
кДж/моль
Теплота образования СО2=369,9
кДж/моль, Н2О=242,2 кДж/моль
Qн =
6*369.9+3.5*242,2-29.7*1=3037.4кДж/моль
Так как по условию задачи 20% тепла
теряется, то определяем количество тепла пошедшее на нагрев продуктов горения
пг = Qн*(1-η)
н = Qпг
=3031.4*(1-0,20)=2429.92 кДж/моль
Определяем действительную
температуру горения:
Тг =Т0+
Таким образом, практический объем
продуктов горения при t=1509.66 К
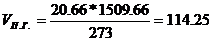 м3/м3
м3/м3
Задача 2
Вычислить состав и объем продуктов горения
вещества церезин, если элементный состав его: C-85%,
H-14%, O-1%,
S-%, N-%,
W-%, золы-%. Горение
протекает при избытке воздуха aВ=1,2 потери тепла излучением
составляют h=0,20 %.
Решение. Для решения задачи необходимо записать
балансы элементарных реакций горения углерода, водорода с учетом процентного
содержания каждого элемента в 1 кг горючего, но есть уже готовые формулы,
которыми можно воспользоваться, например, объем воздуха:
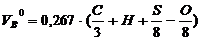 м3/кг.
м3/кг.
Поскольку азот, влага и зола не
горят. Тогда объем воздуха, пошедший на горение, будет:  м3/кг.
м3/кг.
Объем продуктов горения
рассчитывается исходя из элементного состава горючего следующим образом. Из
уравнений элементарных реакций известно, что объем углекислого газа при горении
1 кг углерода составляет 1,86 м3,сернистого газа из 1 кг серы - 0,7 м3 и т.д.
Но в условии задачи углерода в горючем 85 %, что составляет 0,85 кг углерода,
равно  . В состав
продуктов горения войдут азот, углекислый газ, водяной пар с учетом влаги из
горючего вещества:
. В состав
продуктов горения войдут азот, углекислый газ, водяной пар с учетом влаги из
горючего вещества: 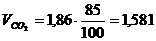 м3/кг;
м3/кг;
 м3/кг;
м3/кг;
 м3/кг,
м3/кг,
 м3/кг.
м3/кг.
Qн =
339,4С+1257Н-108,9(О-S)-25,1(9Н+W)
н=339,4*0,85+1257*0,14-108,9*1-25,1(9*0,14)=323.944
кДж/моль
Так, как по условию задачи потери
тепла излучением составляют h=0,20
%,то
Qпг = Q*(1-η)
н = Qпг
=323.944*(1-0,2)=259.155 кДж/моль
Определяем действительную
температуру горения:
Тг=Т0+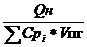
Тг 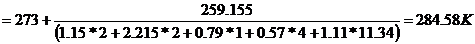
Таким образом, практический объем
продуктов горения при t=284.58 К
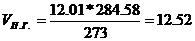 м3/м3
м3/м3
Задача 4
Рассчитать температуру самовоспламенения
вещества 2,3-диметил-4-этил-октан по средней длине углеродной цепи, определив
число концевых групп и число цепей. При решении задачи воспользоваться табл.1-3
прил. данного пособия.
Решение. 1. Записываем структурную формулу
соединения, нумеруя все атомы углерода:
CH3 - 2CН
- 3CН - 4CH
- 5СН2 - 6СН2- 7СН2 - 8СН3
СН3 10СН3 11СН2 - 12СН3
. В молекуле соединения определяем число цепей:
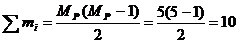 .
.
. Определяем состав цепей:
1-2-3-4-5-6-7-8 1-2-9 1-2-3-10 1-2-3-4-11-12
12-11-4-5-6-7-8 10-3-4-11-12
-2-3-4-5-6-7-8 C=3
9-2-3-10 9-2-3-4-11-12 10-3-4-5-6-7-8 C=5
С=8 C=4
C=6 C=7
m=2 m=2
m=2 m=2
4. Рассчитываем среднюю длину цепи:
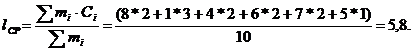
. По табл.1 прил. находим
температуру самовоспламенения 2,3-диметил-4-этил-октан, отыскивая ее по
значению средней длины цепи в молекуле соединения: ТСВ=567К.
6. Находим по справочной литературе ТСВ
2,3-диметил-4-этил-октан и сравниваем с расчетной.
Твсп=300+3.8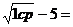 303.4 К
303.4 К
Задача 5
Вычислить температуру вспышки Твсп метанола по
формуле В.И. Блинова. Постоянная прибора А=40 и коэффициент диффузии паров
жидкости D0=13,2 * 10-6 м2/с.
Решение. Для решения задачи по формуле В.И.
Блинова необходимо иметь значение коэффициента β, для
чего записываем уравнение реакции горения метанола:
OH + 1,5О2 +1,5 ·3,76N2
= СО2 +2Н2О + 1,5·3,76N2,
откуда β=1,5.
2. Вычислим произведение
 ,
,
рвпс·Твсп = 40/(13,2 * 10-6 ·1,5) =
2,02020202020*10-6 Па·К.=
=2020202,020202 Па·К
. Принимаем Т=278,0 К, находим, что
давление пара при этой температуре составляет 5332,88 Па (табл.4 прил.). Тогда
(р·Т)278,0К = 278,0*5332,88 = 1482540,64 Па·К, что меньше, чем произведения р·Т
при Твсп.
. Принимаем Т=285,1 К, находим, что
давление пара 7999,32 Па. (р·Т)285,1К = 285,1*7999,32 = 2280606,132 Па·К, что
уже больше произведения рвсп·Твсп.
. Поскольку рвсп·Твсп находится
между найденными значениями произведений р·Т при 278,0 и 285,1 К интерполяцией
находим искомую Твсп:

.Справочное значение Твсп=278К
Погрешность расчета Δ=(282,78-278)/278*100%=1,72%
Задача 6
горение химический тепловой материальный
Рассчитать концентрационные пределы
воспламенения метилового спирта, значения которых вычислить по теплоте
сгорания.
Решение. Зная, что предельная теплота сгорания
1м3 газовоздушной смеси равна приблизительно 1830 кДж/м3, НКПВ находим по
формуле
НКПВ = 1830·100/Qн,
НКПВ = 1830·100/71600,0 = 2,56 %.
Экспериментально найденное значение предела -
2,56 %. В таблице приведены значения низших теплот сгорания некоторых веществ.
Низшая теплота сгорания некоторых горючих
материалов
|
Наименование
вещества
|
Низшая
теплота сгорания, кДж/м3
|
Наименование
вещества
|
Низшая
теплота сгорания, кДж/м3
|
|
Метан
|
35874,78
|
Пропилен
|
86087,74
|
|
Этан
|
63838,84
|
Бутилен
|
113620,23
|
|
Пропан
|
91350,38
|
Ацетилен
|
56091,53
|
|
Бутан
|
118761,36
|
Бензол
|
142560,56
|
|
Этилен
|
59104,14
|
|
|
|
Метиловый
спирт
|
71600,0
|
|
|
|
Амиловый
спирт
|
20190.0
|
|
|
Заключение
Приступая к изучению курса «Теория горения и
взрыва», необходимо представлять, что горение есть главный и основной процесс
на пожаре. Знание химической и физической сути явления и законов горения
необходимо для успешной работы инженера противопожарной техники и безопасности
в любой области его деятельности. Этот курс является теоретической основой ряда
специальных дисциплин.
Использованная литература
1.
Абдурагимов И.М., Андросов А.С., Исаева Л.К., Крылов Е..В. Процессы горения:
Учеб. пособие - М.: ВИПТШ МВД СССР, 1984.
.
Абдурагимов И.М., Говоров В.Ю., Макаров В.Е.. Физико-химические основы развития
и тушения пожаров: Учеб. пособие. - М.: ВИПТШ МВД СССР, 1980.
.
Монахов В.Т. Методы исследования пожарной опасности веществ. - М.: Химия, 1979.
Приложение
Таблица 6
|
Номер
варианта
|
Название
соединения
|
aВ
|
h, %
|
|
1
|
Анилин
|
1,1
|
0,20
|
|
2
|
Гексан
|
1,3
|
0,30
|
|
3
|
Бутанол-1
|
1,2
|
0,40
|
|
4
|
Толуол
|
1,2
|
0,30
|
|
5
|
Амиловый
спирт
|
2
|
0,40
|
|
6
|
Глицерин
|
1,5
|
0,20
|
|
7
|
Этиленгликоль
|
1,3
|
0,25
|
|
8
|
Пропанол-1
|
1,6
|
0,20
|
|
9
|
Диэтиловый
эфир
|
1,1
|
0,40
|
|
10
|
Уксусноэтиловый
эфир
|
1,2
|
0,30
|
Таблица 7
|
Номер
варианта
|
Название
соединения
|
Содержание
веществ, %
|
aВ
|
h, %
|
|
|
C
|
H
|
O
|
S
|
N
|
W
|
зола
|
|
|
|
1
|
Церезин
|
85
|
14
|
1
|
-
|
-
|
-
|
-
|
1,2
|
0,20
|
|
2
|
Уголь
|
70
|
4
|
3,4
|
3
|
0,6
|
19
|
-
|
1,3
|
0,10
|
|
3
|
Древесина
|
46
|
6
|
37
|
-
|
2
|
9
|
-
|
1,2
|
0,20
|
|
4
|
Бензин
|
85
|
15
|
0,1
|
-
|
0,1
|
-
|
-
|
1,1
|
0,30
|
|
5
|
Соляровое
масло
|
87
|
13
|
0,3
|
0,4
|
-
|
-
|
-
|
1,2
|
0,30
|
|
6
|
Мазут
|
83
|
11
|
1
|
4
|
-
|
1
|
-
|
1,3
|
0,20
|
|
7
|
Керосин
|
80
|
14
|
0,3
|
-
|
-
|
6
|
-
|
1,5
|
0,30
|
|
8
|
Горючий
сланец
|
35
|
5
|
10
|
4
|
1
|
15
|
30
|
1,2
|
0,10
|
|
9
|
Горючий
сланец
|
24
|
1,8
|
4,1
|
2,9
|
-
|
20
|
47
|
1,3
|
0,20
|
|
10
|
Антрацит
|
67
|
2,7
|
3,4
|
0,4
|
0,5
|
5,5
|
21
|
1,1
|
0,20
|
Таблица 8
|
Состав
смеси, % объемн.
|
Номер
варианта
|
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
|
Окись
углерода
|
-
|
10
|
-
|
-
|
-
|
-
|
-
|
-
|
-
|
11
|
|
Водород
|
50
|
-
|
-
|
-
|
-
|
-
|
-
|
-
|
10
|
-
|
|
Метан
|
-
|
15
|
-
|
-
|
35
|
-
|
35
|
-
|
-
|
|
Этан
|
-
|
-
|
-
|
42
|
-
|
-
|
24
|
-
|
-
|
-
|
|
Пропан
|
-
|
-
|
-
|
-
|
60
|
-
|
-
|
-
|
-
|
9
|
|
Бутан
|
8
|
-
|
-
|
-
|
-
|
-
|
-
|
-
|
-
|
-
|
|
Пентан
|
-
|
-
|
5
|
3
|
-
|
8
|
-
|
-
|
-
|
10
|
|
Этилен
|
20
|
22
|
28
|
-
|
-
|
-
|
-
|
-
|
-
|
-
|
|
Пропен
|
-
|
-
|
-
|
-
|
-
|
-
|
16
|
-
|
-
|
-
|
|
Бутен
|
-
|
-
|
-
|
20
|
-
|
-
|
-
|
15
|
-
|
-
|
|
Пентен
|
-
|
-
|
-
|
-
|
14
|
19
|
-
|
-
|
35
|
20
|
|
Бензол
|
-
|
-
|
-
|
5
|
-
|
-
|
-
|
-
|
-
|
-
|
|
Ацетилен
|
-
|
8
|
-
|
-
|
10
|
-
|
10
|
20
|
25
|
-
|
|
Углекислый
газ
|
20
|
10
|
18
|
15
|
-
|
17
|
10
|
13
|
-
|
-
|
|
Азот
|
-
|
50
|
24
|
-
|
16
|
-
|
15
|
-
|
10
|
30
|
|
Кислород
|
2
|
-
|
10
|
15
|
-
|
21
|
25
|
17
|
20
|
20
|
|
aВ
|
1,2
|
2
|
1,3
|
1,1
|
1,1
|
1,2
|
1,2
|
1,1
|
1,5
|
1,4
|
|
h, %
|
0,10
|
0,15
|
0,20
|
0,20
|
0,15
|
0,15
|
0,20
|
0,20
|
0,15
|
0,10
|
Таблица 9
|
Номер
варианта
|
Название
соединения
|
|
1
|
2,3-диметил-4-этил-октан
|
|
2
|
2,2,4-триметилпентан
|
|
3
|
1,3-диметил-4-пропилбензол
|
|
4
|
2,
2,3,3 - тетраметилбутан
|
|
5
|
1-метил-4,5-диизопропилбензол
|
|
6
|
2,2-диметилбутанол-1
|
|
7
|
2,2-диметил-3-этил-пропанол-1
|
|
8
|
2,3-диметил-3-этил-бутанол-1
|
|
9
|
1-метил-2этил-3пропилбензол
|
|
10
|
2,2-диэтилпентанол-1
|
Таблица 10
|
Номер
варианта
|
Вещество
|
Т0
|
А
|
D0×106 , м2/с
|
|
1
|
Метанол
|
15
|
40
|
13,2
|
|
2
|
Этанол
|
17
|
45
|
10,2
|
|
3
|
Пропанол
|
20
|
40
|
8,5
|
|
4
|
Бутанол
|
20
|
40
|
7,0
|
|
5
|
Амиловый
спирт
|
20
|
40
|
5,9
|
|
6
|
Ацетон
|
20
|
45
|
8,6
|
|
7
|
Октан
|
20
|
40
|
6,0
|
|
8
|
Сероуглерод
|
23
|
40
|
8,8
|
|
9
|
Толуол
|
100
|
45
|
7,1
|
|
10
|
Этиловый
эфир уксусной кислоты
|
19
|
40
|
7,1
|
Таблица 11
|
Номер
варианта
|
Название
соединения
|
Метод
расчета КПВ
|
|
1
|
Метиловый
спирт
|
По
теплоте сгорания
|
|
2
|
Уксусный
альдегид
|
По
аппроксимационной формуле
|
|
3
|
Амиловый
спирт
|
По
теплоте сгорания
|
|
4
|
Ацетон
|
По
аппроксимационной формуле
|
|
5
|
Октан
|
По
аппроксимационной формуле
|
|
6
|
Диэтиловый
эфир
|
По
аппроксимационной формуле
|
|
7
|
Бутиловый
спирт
|
По
аппроксимационной формуле
|
|
8
|
Пропиловый
спирт
|
По
аппроксимационной формуле
|
|
9
|
Бензол
|
По
аппроксимационной формуле
|
|
10
|
Этиловый
спирт
|
По
аппроксимационной формуле
|
Связь единиц параметров с постоянной прибора А
|
Определяемый
параметр
|
Численное
значение постоянной А
|
Коэффициент
диффузии
|
Давление
|
Температура
|
|
|
Единица
измерения
|
|
Твсп
|
40
К·Па·м2/с м2/сПаК м2/сПаК
|
|
|
|
|
Твоспл
|
45
К·Па·м2/с
|
м2/с
|
Па
|
К
|
|
Твсп
|
3000
К·мм рт. ст.·см2/с
|
см2/с
|
мм
рт. ст.
|
К
|
|
Твоспл
|
3400
К·мм рт. ст.·см2/с
|
см2/с
|
мм
рт. ст.
|
К
|
Низшая теплота сгорания некоторых горючих
материалов
|
Наименование
вещества
|
Низшая
теплота сгорания, кДж/м3
|
Наименование
вещества
|
Низшая
теплота сгорания, кДж/м3
|
|
Метан
|
35874,78
|
Пропилен
|
86087,74
|
|
Этан
|
63838,84
|
Бутилен
|
113620,23
|
|
Пропан
|
91350,38
|
Ацетилен
|
56091,53
|
|
Бутан
|
118761,36
|
Бензол
|
142560,56
|
|
Этилен
|
59104,14
|
|
|
|
Метиловый
спирт
|
71600,0
|
|
|
|
Амиловый
спирт
|
20190.0
|
|
|
Значения констант а и в зависимости от β
|
Область
применения
|
а
|
в
|
|
Для
вычисления нижнего предела
|
8,684
|
4,679
|
|
Для
вычисления верхнего предела при β ≤ 7,5 при β >
7,5
|
1,550
0,768
|
0,560
6,554
|
Температура самовоспламенения (К) некоторых
предельных углеводородов в зависимости от средней длины углеродной цепи
|
lср
|
lср
|
Тс
|
lср
|
Тс
|
lср
|
Тс
|
|
3,0
|
743
|
6,0
|
507
|
9,0
|
482
|
12,0
|
477
|
|
3,1
|
738
|
6,1
|
505
|
9,1
|
481
|
12,1
|
477
|
|
3,2
|
733
|
6,2
|
504
|
9,2
|
481
|
12,2
|
477
|
|
3,3
|
728
|
6,3
|
503
|
9,3
|
481
|
12,3
|
477
|
|
3,5
|
717
|
6,5
|
501
|
9,5
|
480
|
12,5
|
477
|
|
3,6
|
712
|
6,6
|
500
|
9,6
|
480
|
12,6
|
477
|
|
3,7
|
706
|
6,7
|
499
|
9,7
|
480
|
12,7
|
477
|
|
3,8
|
699
|
6,8
|
498
|
9,8
|
479
|
12,8
|
477
|
|
3,9
|
693
|
6,9
|
497
|
9,9
|
479
|
12,9
|
477
|
|
4,0
|
686
|
7,0
|
496
|
10,0
|
479
|
13,0
|
477
|
|
4,1
|
680
|
7,1
|
495
|
10,1
|
479
|
13,1
|
477
|
|
4,2
|
673
|
7,2
|
494
|
10,2
|
479
|
13,2
|
477
|
|
4,3
|
665
|
7,3
|
494
|
10,3
|
479
|
13,3
|
477
|
|
4,4
|
654
|
7,4
|
493
|
10,4
|
478
|
13,4
|
477
|
|
4,5
|
643
|
7,5
|
492
|
10,5
|
478
|
13,5
|
476
|
|
4,6
|
631
|
7,6
|
491
|
10,6
|
478
|
13,6
|
476
|
|
4,7
|
617
|
7,7
|
490
|
10,7
|
478
|
13,7
|
476
|
|
4,8
|
601
|
7,8
|
489
|
10,8
|
478
|
13,8
|
476
|
|
4,9
|
581
|
7,9
|
489
|
10,9
|
478
|
13,9
|
476
|
|
5,0
|
560
|
8,0
|
488
|
11,0
|
478
|
14,0
|
476
|
|
5,1
|
547
|
8,1
|
487
|
11,1
|
478
|
14,1
|
476
|
|
5,2
|
535
|
8,2
|
486
|
11,2
|
478
|
14,2
|
476
|
|
5,3
|
528
|
8,3
|
486
|
11,3
|
478
|
14,3
|
476
|
|
5,4
|
522
|
8,4
|
485
|
11,4
|
478
|
14,4
|
476
|
|
5,5
|
517
|
8,5
|
484
|
11,5
|
478
|
14,5
|
476
|
|
5,6
|
513
|
8,6
|
484
|
11,6
|
477
|
14,6
|
476
|
|
5,7
|
511
|
8,7
|
483
|
11,7
|
477
|
14,7
|
476
|
|
5,8
|
509
|
8,8
|
483
|
11,8
|
477
|
14,8
|
476
|
|
5,9
|
508
|
8,9
|
482
|
11,9
|
477
|
14,9
|
476
|
|
|
|
|
|
|
15,0
|
475
|
Температура самовоспламенения (К) некоторых
предельных одноатомных спиртов в зависимости от средней длины углеродной цепи
|
lср
|
Тс
|
lср
|
Тс
|
lср
|
Тс
|
lср
|
Тс
|
|
2,0
|
737
|
4,4
|
610
|
6,8
|
545
|
9,2
|
518
|
|
2,1
|
736
|
4,5
|
606
|
6,9
|
543
|
9,3
|
517
|
|
2,2
|
734
|
4,6
|
602
|
7,0
|
542
|
9,4
|
516
|
|
2,3
|
732
|
4,7
|
599
|
7,1
|
540
|
9,5
|
516
|
|
2,4
|
730
|
4,8
|
595
|
7,2
|
539
|
9,6
|
515
|
|
2,5
|
728
|
4,9
|
592
|
7,3
|
537
|
9,7
|
514
|
|
2,6
|
725
|
5,0
|
588
|
7,4
|
536
|
9,8
|
513
|
|
2,7
|
721
|
5,1
|
585
|
7,5
|
535
|
9,9
|
513
|
|
2,8
|
716
|
5,2
|
582
|
7,6
|
534
|
10,0
|
512
|
|
2,9
|
711
|
5,3
|
579
|
7,7
|
533
|
10,5
|
509
|
|
3,0
|
706
|
5,4
|
577
|
7,8
|
531
|
11,0
|
507
|
|
3,1
|
696
|
5,5
|
574
|
7,9
|
530
|
11,5
|
506
|
|
3,2
|
693
|
5,6
|
572
|
8,0
|
12,0
|
505
|
|
3,3
|
686
|
5,7
|
569
|
8,1
|
528
|
12,5
|
505
|
|
3,4
|
678
|
5,8
|
567
|
8,2
|
527
|
13,0
|
504
|
|
3,5
|
669
|
5,9
|
564
|
8,3
|
526
|
13,5
|
504
|
|
3,6
|
658
|
6,0
|
562
|
8,4
|
525
|
14,0
|
503
|
|
3,7
|
649
|
6,1
|
560
|
8,5
|
524
|
14,5
|
503
|
|
3,8
|
642
|
6,2
|
557
|
8,6
|
523
|
15,0
|
502
|
|
3,9
|
634
|
6,3
|
555
|
8,7
|
522
|
15,5
|
502
|
|
4,0
|
628
|
6,4
|
553
|
8,8
|
521
|
16,0
|
501
|
|
4,1
|
623
|
6,5
|
551
|
8,9
|
520
|
16,5
|
501
|
|
4,2
|
619
|
6,6
|
549
|
9,0
|
519
|
17,0
|
500
|
|
4,3
|
614
|
6,7
|
547
|
9,1
|
519
|
17,5
|
500
|
Температура самовоспламенения (К) некоторых
ароматических углеводородов в зависимости от средней длины углеродной цепи
|
lср
|
Тс
|
lср
|
Тс
|
lср
|
Тс
|
|
-
2
|
843
|
-
|
-
|
-
|
-
|
|
-1,9
|
842
|
0,1
|
810
|
2,1
|
702
|
|
1,8
|
841
|
0,2
|
794
|
2,2
|
701
|
|
-1,7
|
840
|
0,3
|
774
|
2,3
|
701
|
|
-1,6
|
840
|
0,4
|
753
|
2,4
|
700
|
|
-1,5
|
839
|
0,5
|
733
|
2,5
|
700
|
|
-1,4
|
838
|
0,6
|
723
|
2,6
|
699
|
|
-1,3
|
837
|
0,7
|
718
|
2,7
|
699
|
|
1,2
|
837
|
0,8
|
715
|
2,8
|
698
|
|
-1,1
|
836
|
0,9
|
713
|
2,9
|
698
|
|
-1,0
|
835
|
1,0
|
712
|
3,0
|
697
|
|
-0,9
|
835
|
1,1
|
711
|
3,1
|
697
|
|
-0,8
|
834
|
1,2
|
710
|
3,2
|
697
|
|
-0,7
|
833
|
1,3
|
709
|
3,3
|
697
|
|
-0,6
|
832
|
1,4
|
708
|
3,4
|
696
|
|
-0,5
|
831
|
1,5
|
707
|
3,5
|
696
|
|
-0,4
|
830
|
1,6
|
706
|
3,6
|
696
|
|
-0,3
|
829
|
1,7
|
705
|
3,7
|
696
|
|
-0,2
|
827
|
1,8
|
704
|
3,8
|
696
|
|
-0,1
|
824
|
1,9
|
703
|
3,9
|
696
|
|
0
|
819
|
2,0
|
703
|
4,0
|
695
|
Константы уравнения для давления пара некоторых
органических жидкостей в области температур от точки плавления до точки кипения
|
Жидкость
|
а
|
в
|
с
|
|
Ацетон
|
19,557
|
3,966
|
2203
|
|
Метиловый
спирт
|
22,43
|
4,634
|
2661
|
|
Н-бутиловый
спирт
|
40,21
|
10,35
|
4100
|
|
Н-амиловый
спирт
|
46,49
|
12,42
|
4189
|
|
Н-гексиловый
спирт
|
51,00
|
13,80
|
5068
|
|
Н-гептиловый
спирт
|
56,20
|
15,41
|
5580
|
|
Н-октиловый
спирт
|
65,21
|
18,40
|
6190
|
|
Бензол
|
26,07
|
6,203
|
2610
|