Методические аспекты экспериментальной оценки термодинамической константы Na/Ca-обмена
Методические
аспекты экспериментальной оценки термодинамической константы Na/Ca-обмена.
Самарин Е.Н., Фомичева Е.Н.
Явление
ионного обмена уже более 150 лет остается предметом пристального внимания
исследователей. Предложено множество уравнений для константы ионообменной
реакции 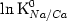 [1], однако каждое имеет серьезные
ограничения. Тем не менее часто в практических расчетах используются значения
[1], однако каждое имеет серьезные
ограничения. Тем не менее часто в практических расчетах используются значения 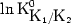 без учета специфики их
получения. Особенное большое влияние на
без учета специфики их
получения. Особенное большое влияние на 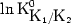 оказывают концентрация
глинистой суспензии и внешнего электролита, а также емкость катионного обмена
глинистого грунта (ЕКО) [1,3].
оказывают концентрация
глинистой суспензии и внешнего электролита, а также емкость катионного обмена
глинистого грунта (ЕКО) [1,3].
|

|
|
Рис.1. Влияние концентрации суспензии на величину термодинамической
константы Na/Ca-обмена.
|
Настоящее
исследование выполнено на монтмориллоните с катионной парой Са2+-Nа+.
Монокатионные формы минерала приготовлены по методу К.К. Гедройца после
отмучивания фракции < 5 мкм из "киловых" глин (К2s) - отобранных
из Бахчисарайского разреза II гряды Крымских гор. Содержание монтмориллонита в
образцах не менее 98,5 %; в составе примесей: кварц, кальцит и иллит.
Химический состав образцов соответствует высокозарядному Al-монтмориллониту,
тип Wyoming, ЕКО 1,31 мг-экв./г.
Экспериментальные
изотермы ионного обмена получены по общепринятой методике [4] для прямой Ca  Na и
обратной Na
Na и
обратной Na  Ca реакций при pH=7 в бинарных растворах хлоридов (мольные
доли Na+ и Са2+ изменялись от 0 до 1 in contrary) суммарной концентрации от
0,0018 до 1,0 экв./л. Константы селективности
Ca реакций при pH=7 в бинарных растворах хлоридов (мольные
доли Na+ и Са2+ изменялись от 0 до 1 in contrary) суммарной концентрации от
0,0018 до 1,0 экв./л. Константы селективности 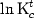 реакции обмена при
Ip-pa = const рассчитаны по Е.Н.Гапону и по В.Д.Аргензингеру [1]. Экстраполяция
значений
реакции обмена при
Ip-pa = const рассчитаны по Е.Н.Гапону и по В.Д.Аргензингеру [1]. Экстраполяция
значений 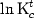 , соответствующих фиксированному составу
обменного комплекса (ОК), к нулевой ионной силе выполнена по методу
В.П.Васильева. Использованы два варианта расчета: (1) для фиксированной
концентрации суспензий (Cсусп), если
, соответствующих фиксированному составу
обменного комплекса (ОК), к нулевой ионной силе выполнена по методу
В.П.Васильева. Использованы два варианта расчета: (1) для фиксированной
концентрации суспензий (Cсусп), если 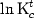 рассчитан по
В.Д.Аргензингеру (классическая методика); (2) для фиксированного соотношения
катионов "обменный комплекс - внешний раствор" (
рассчитан по
В.Д.Аргензингеру (классическая методика); (2) для фиксированного соотношения
катионов "обменный комплекс - внешний раствор" (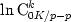 ),
если
),
если 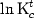 рассчитан по Е.Н.Гапону. Термодинамическая
константа Na/Ca-обмена _ рассчитана по методу Г.Гейнеса и Х.Томаса [2] для
обоих вариантов представления коэффициентов селективности.
рассчитан по Е.Н.Гапону. Термодинамическая
константа Na/Ca-обмена _ рассчитана по методу Г.Гейнеса и Х.Томаса [2] для
обоих вариантов представления коэффициентов селективности.
|
|
|
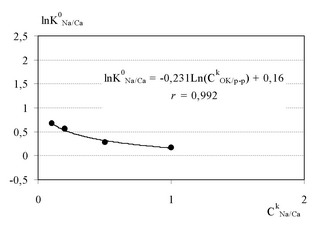
Рис.2. Влияние соотношения содержания катионов "ОК -
раствор" на величину термодинамической константы Na/Ca-обмена.
|
Показано,
что с увеличением Cсусп в системе экспериментально получаемое значение 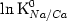 уменьшается и стремится к постоянному
значению (рис.1). По-видимому, это обусловлено невозможностью развития
равновесного профиля ДЭС, а при больших концентрациях суспензий перекрытием
диффузных оболочек, развитых вокруг частиц и, возможно, структурированием
осадка глины.
уменьшается и стремится к постоянному
значению (рис.1). По-видимому, это обусловлено невозможностью развития
равновесного профиля ДЭС, а при больших концентрациях суспензий перекрытием
диффузных оболочек, развитых вокруг частиц и, возможно, структурированием
осадка глины.
Расчет
значений 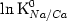 по второму варианту приводит к аналогичному
результату: с увеличением
по второму варианту приводит к аналогичному
результату: с увеличением 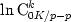 значение
значение 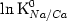 уменьшается
(рис.2). Тем не менее, именно такой способ расчета, предлагаемый авторами
впервые, является более предпочтительным, поскольку получаемое значение
уменьшается
(рис.2). Тем не менее, именно такой способ расчета, предлагаемый авторами
впервые, является более предпочтительным, поскольку получаемое значение 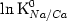 не зависит от концентрации суспензии в
системе, а определяется только величиной ЕКО глинистого грунта и концентрацией
электролита, Кроме того, в этом случае возможно непосредственно из значения
не зависит от концентрации суспензии в
системе, а определяется только величиной ЕКО глинистого грунта и концентрацией
электролита, Кроме того, в этом случае возможно непосредственно из значения 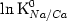 рассчитать изотерму ионного обмена для
исследованного диапазона концентраций и значения коэффициентов селективности для
любого состава обменного комплекса.
рассчитать изотерму ионного обмена для
исследованного диапазона концентраций и значения коэффициентов селективности для
любого состава обменного комплекса.
Список литературы
Bolt G.H. Cation-exchange equations used in soil science - A
review. //Neth. J. Agric. Sci. 1967, v.15, pp.81-103.
Gaines G.L., Thomas H.C. Adsorption Studies on Clay Minerals. II. A
Formulation of the Thermodynamics of Exchange Adsorption. //The Journal of
Chemical Physics. 1953, v.21, N 4, pp.714-718.
Maes A., Cremers A. Charge density effects in ion exchange. I -
Heterovalent exchange equilibria. //J.C.S. Faraday transactions. I. 1977, v.73,
pp.1807-1814.
Van Bladel R., Laudelout H. Apparent irreversibility of
ion-exchange reactions in clay suspensions. //Soil Science. 1967, v.104,
N 7, pp.134-137.
Для
подготовки данной работы были использованы материалы с сайта http://geo.web.ru/