Транспортные свойства и структура композитных мембран МФ-4СК/полианилин, полученных в условиях электродиализа
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
Федеральное государственное бюджетное образовательное
учреждение
высшего профессионального образования
«КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
(ФГБОУ ВПО КубГУ)
Кафедра физической химии
ДИПЛОМНАЯ РАБОТА
ТРАНСПОРТНЫЕ СВОЙСТВА И СТРУКТУРА КОМПОЗИТНЫХ МЕМБРАН
МФ-4СК/ПОЛИАНИЛИН, ПОЛУЧЕННЫХ В УСЛОВИЯХ ЭЛЕКТРОДИАЛИЗА
Работу
выполнил Д. В. Луценко
Факультет
химии и высоких технологий
Нормоконтролёр,
внс, кхн. О. А. Дёмина
Краснодар
2012г.
Реферат
ИОНООБМЕНЫЕ МЕМБРАНЫ, ПОЛИАНИЛИН,
ЭЛЕКТРОПРОВОДНОСТЬ, ДИФФУЗИОННАЯ ПРОНИЦАЕМОСТЬ, ЭЛЕКТРОДИАЛИЗ, КИНЕТИКА, СИНТЕЗ
В УСЛОВИЯХ ЭЛЕКРИЧЕСКОГО ПОЛЯ.
Получены композитные мембраны на основе
перфторированной сульфокатионитовой мембраны МФ-4СК. Синтез полианилина в
матрице мембраны МФ-4СК выполнен в условиях внешнего электрического поля. В
качестве модифицирующих растворов использовались 0,01М раствор C6H5NH2
на 0,01M
H2SO4
и 0,01M раствор FeCl3
на 0,01M
H2SO4.
Проведены измерения электропроводности и диффузионной проницаемости полученных
композитов и выявлены их сравнительные характеристики.
Введение
Сейчас особый интерес представляют композиты на
основе ионообменных мембран и проводящих полимеров.
Среди проводящих полимеров полианилин (ПАн)
занимает особое место. Под действием различных окислителей из раствора анилина
в водной кислоте выделяется тёмно-зелёный осадок соли ПАн, получивший название
эмеральдин.
Редокс-превращения ПАн сопровождаются
отщеплением протонов от атомов азота или их присоединением, что обеспечивает
ПАн в форме эмеральдина самую высокую из проводящих полимеров теоретическую
зарядовую ёмкость. Привлекательным является весьма высокая стабильность ПАн в
различных средах, простота его синтеза и доступность сырья. Особый интерес
представляют композиты на основе ионообменных мембран и полианилина. Однако
проводящие свойства этих материалов существенно зависят от условий синтеза и
степени окисления цепей полианилина в мембране.
В связи с этим актуальной проблемой является
исследование возможности модифицирования перфторированных мембран полианилином
в условиях электродиализа и исследование кинетических характеристик процесса с
использованием полученных композитов.
В настоящее время методы электромембранной
технологии эффективно применяются не только в водоподготовке, но и в областях,
связанных с разделением и очисткой биохимических и медицинских препаратов, а
также в пищевой промышленности. Электродиализ с ионоселективными мембранами
оказывается достаточно эффективным и экологически целесообразным для
деминерализации и очистки продуктов сахарного производства, молочной сыворотки,
ряда аминокислот и ферментов, сывороточного альбумина, в производстве фруктовых
соков, для корректировки рН.
Целью работы было исследование
электротранспортных свойств композитов на основе перфторированных
сульфокатионитовых мембран и полианилина, полученных в условиях внешнего
электрического поля.
1. Литературный обзор
.1 Структура и свойства
перфторированных сульфокатионитовых мембран
Перфторированные сульфокатионитовые мембраны
типа Нафион и МФ-4СК имеют сложную полимерную архитектуру, которая состоит из
гидрофобных фторэтиленовых цепей и регулярно расположенных эфирных боковых
цепей, которые заканчиваются сильно гидрофильными сульфо-группами. Механическая
прочность мембраны определяется взаимодействием фторэтиленовых цепей, поэтому
влагоемкость мембраны ограничена их упругой деформацией и не превышает ≈25%.
Многочисленные данные [27, 28, 29]
свидетельствуют о пористой структуре ионообменных мембран. Однако распределение
пор по радиусам неравномерно вследствие стремления к ассоциациям участков с
гидрофобными полимерными цепями, с одной стороны, и гидрофильными участками
содержащих функциональные группы − с другой стороны. Размер пор является
практически важной характеристикой мембранных и сорбционных материалов.
Классификация Дубинина, основанная на механизмах, протекающих в порах
адсорбционных и капиллярных явлений, позволяет выделить следующие разновидности
пор в сорбентах: микропоры радиусом 0,6-0,7 нм; супермикропоры радиусом от
0,6-0,7 до 1,5 нм; мезопоры радиусом от 1,5 до 100-200 нм и макропоры радиусом
более 100-200 нм. Для ионообменных материалов и исходных сополимеров подобная
классификация предложена Мулдером [32], при этом выделяются микропоры с
радиусом до 2 нм, мезопоры от 2 до 50 нм и макропоры - с радиусом более 50 нм.
Поры мембран, содержащих
гидрофильные функциональные группировки, склонны к гидратации. В сухих
гомогенных ионообменных мембранах нафион и МФ-4СК практически отсутствует
пористость. Процесс набухания мембран в воде, сопровождающийся образованием
пор, обусловлен гидратацией ионогенных групп. Эти мембраны имеют различное
расположение и количество фторированных и сульфированных участков полимерной
цепи. Плёнки из таких полимеров имеют глобулярную структуру и содержат
достаточно большое количество полостей, возникшее из-за отталкивания
электроотрицательных групп. В водной среде эти полости вследствие
взаимодействия с гидрофильными SO3H-
фрагментами заполняются значительным количеством воды [27, 31]. Образование
разветвлённых водородных связей в кластерах, содержащих функциональные группы и
молекулы воды, приводит к дополнительному укрупнению кластеров. Согласно модели
Гирке [0, 32], до сих пор наиболее широко используемой, ионообменная мембрана
представлена с точки зрения инвертированной мицеллярной структуры (рис. 1.1), в
которой ионообменные участки отделены от фторэтиленовых цепей и таким образом
формируют сферические поры (кластеры) диаметром примерно 4 нм с расположенными
на их внутренней поверхности SO3-группами. Кластеры соединены каналами средней
шириной 1 нм.
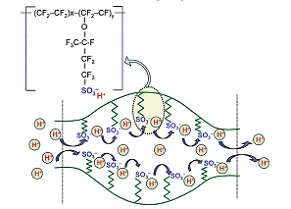
Рисунок 1- Химическая структура
перфторированной сульфокатионитовой мембраны в рамках модели Гирке
1.2 Свойства
полианилина и его формы
Среди проводящих полимеров полианилин занимает
особое место. С фундаментальной точки зрения это связано с особенностями его
допирования.
Явление допирования как общий метод придания
полисопряженным полимерам высокой “металлической” электропроводности было
открыто для полиацетилена и представляло собой мягкое окисление, приводящее к
возникновению свободных носителей заряда. В случае ПАн протонирование приводит
к образованию σ-связей N-H, т.е. к
превращению основания ПАн в другое стехиометрическое соединение - соль ПАн (рис.
1). Редокс превращение ПАн также обычно сопровождается отщеплением протонов от
атомов азота или их присоединением, т.е. изменением числа σ-связей.
Механизм окисления-восстановления обеспечивает ПАн самую высокую из проводящих
полимеров теоретическую зарядовую емкость в расчете на одно мономерное звено.
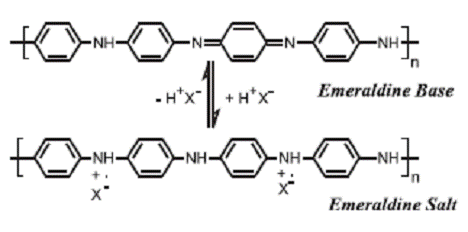

Рисунок 2- Допирование основания ПАн с
образованием проводящей соли ПAн
В действительности эта идеальная структура может
быть реализована в идеальных условиях (ПАн легко и полностью протонируется
только в очень разбавленных растворах). В твёрдой фазе протонирование ПАн и его
композитов лимитируется стадией диффузии допанта (кислоты) к азотсодержащим
группам, процесса, который может зависеть от размера аниона допанта и
морфологии полимерной матрицы. С другой стороны проводящие свойства ПАн
являются функцией не только степени протонирования и окисления полимерной цепи,
но также структурных и конформационных факторов, которые напрямую определяются
условиями синтеза ПАн.
После открытия синтеза и превращений ПАн в 1840
году, было изучено влияние различных факторов на его электропроводность, и
затем на основе этого был создан химический источник тока (ХИТ) - первый
источник с проводящим полимером. Обширное исследование ПАн в последние годы
началось после опубликования работы. Существует большое число работ,
посвященных получению и исследованиям структуры и физико-химических свойств
полианилина. Лишь недавно строение ПАн как поли-n-фениламинимина. А было
доказано наиболее надежным способом: синтезом соединения приписываемой структуры
с последующим сравнением его свойств со свойствами ПАн, полученного обычными
способами (химическим, электрохимическим, окислительной поликонденсацией
анилина).
Под действием таких окислителей, как персульфат
аммония (NH4)2S2O8, хлорат натрия NaClO3, бихромат калия К2Сr2O7, иодат калия
КIO3, из раствора анилина в водной кислоте выделяется тёмно-зелёный осадок соли
ПАн, за свой цвет, получивший название эмеральдин. Обработка его раствором
аммиака или щёлочи даёт тёмно-синее основание эмеральдина. Эмеральдин
получается количественно: если окислитель берётся из расчёта 1,25 атома О на
молекулу анилина, выход достигает 97%. Эти результаты согласуются с
предлагаемой на основе элементного анализа и количественного восстановления
формулой эмеральдина с содержанием хинониминных звеньев ¼,
брутто формула С6Н4,5N.
С6Н5NH2 + 1,25 [O] → С6Н4,5N + 1,25 H2O (1)
Конечно, эта формула является приближённой, но
достаточно близкой к действительности. Реакция окисления анилина
экзотермическая, протекает с индукционным периодом. Наблюдения показывают, что
индукционный период снимается полианилином, т.е. химическое окисление является
автокаталитическим процессом, как и электрохимическое. Свойства продукта
практически не зависят от выбора окислителя из перечисленных выше, если он не
взят в избытке; лишь применение пероксида водорода даёт ПАн с худшими
свойствами. При избытке окислителя наблюдается снижение выхода полимера за счёт
разложения, а образовавшийся продукт несколько более окислен,
электропроводность его ниже. В качестве метода инициирования процесса
образования полианилина в литературе описывается метод фотоинициирования. При
этом раствор мономера в HNO3 в присутствии растворимой соли серебра облучают
определённое время ртутной лампой, дающей излучение с длиной волны 365 нм. В
зависимости от времени синтеза может быть получен осадок соли ПАн, окрашенный в
зелёный цвет разной интенсивности.
ПАн, как и другие проводящие полимеры, легко
получается в виде плёнки на аноде при окислении раствора мономера в подходящих
условиях. Образование плёнок с хорошей адгезией к электроду существенно для
применения ПАн в электронике и электрохимии. Чаще всего ПАн получают из
раствора анилина в водной 0,1-2,0М кислоте, т.к. в этой среде полимер является
основным продуктом реакции. Начало окисления наблюдается при 0,45-0,65 В (отн.
нас. к.э.) на платиновом электроде. Большая серия работ посвящена также синтезу
и исследованию полимера в безводной кислой среде. В других средах окисление
анилина либо протекает по иному пути, либо вообще быстро прекращается
вследствие покрытия электрода изолирующей плёнкой. Электрохимическим методом
можно получить продукты, которые синтезируются путём химического окисления или
восстановления полианилинов, начиная от полностью восстановленного
лейкоэмеральдина (у=1), эмеральдинового основания (у=0,5) и заканчивая
полностью окисленным пернигранилином (у=0)[6] (рис. 3).
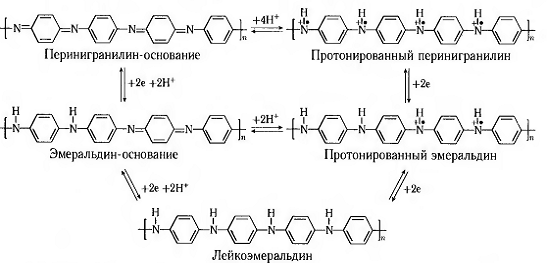

Рисунок 3- Различные формы полианилина
1.3 Механизм
полимеризации анилина в матрице МФ-4СК
В кислой среде анилин в
растворе присутствует в протонированной форме - ионов фениламмония (An+),
которые являются противоионами для сульфокатионитовой мембраны МФ-4СК.

 (2)
(2)
Под действием таких окислителей
как хлорид железа (III) или персульфат аммония в водном растворе кислоты в
прозрачной плёнке МФ-4СК, предварительно насыщенной ионами фениламмония,
образуется изумрудно-зелёный полимер - полианилин.
Рассмотрим стадии темплатного синтеза
полианилина с применением FeCl3 в качестве редокс-катализатора. Для указанной
системы в процессе ионного обмена из фазы мембраны ионы Н+ вытесняются
катионами фениламмония, и одновременно может происходить необменная сорбция
мономера в фазе мембраны.
RSO3 -H+ + An+ → RSO3 -An+ +
H+ (3)
Ранее с помощью электрохимических методов было
установлено, что диффузия ионов фениламмония и их накопление в матрице мембраны
за счёт сорбции и ионного обмена является лимитирующей стадией процесса
полимеризации анилина в темплатной матрице мембраны. Сорбция и ионный обмен
ионов железа (III) из раствора 0,01 M FeCl3 + 0,5 M H2SO4 в общем случае
протекает по уравнению:
3RSO3 H+ + Fe3+ → (RSO3)3Fe 3+
+ 3H+ (4)
Ионы железа (III) являются
окислительно-восстановительным катализатором процесса полимеризации. В ходе
реакции они восстанавливаются до ионов железа (II), при этом электроны инициируют
полимеризацию анилина:
Fe3+ + 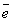 →
Fe2+ (5)
→
Fe2+ (5)
Интенсивность окраски зависит от
соотношения окисленной и восстановленной форм и времени выдержки в рабочих
растворах
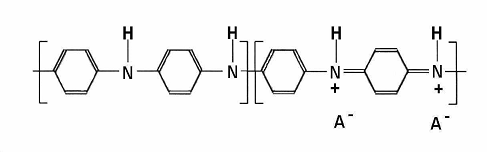 (6)
(6)
Анионами А- являются -SO3- группы темплатной
матрицы МФ-4СК. Более детально химические формы полианилина описаны в работах
[15, 17].
В многостадийном процессе химической
полимеризации анилина в матрице перфторированной мембраны большую роль играет
явление самоорганизации противоионов фениламмония с образованием ароматических
цепей полианилина. Поскольку эффект самоорганизации сопровождается видимым
изменением окраски исходной пленки, этот факт использовался для визуального
наблюдения за образованием полимера. Одним из условий появления самоорганизации
в системе является наличие среди стадий реакции автокаталитической стадии. Эта
стадия как раз и необходима для инициации полимеризации полианилина за счёт
окислительно-восстановительных реакций с участием электронов. В работе в
качестве химического инициатора применялась также следующая
редокс-каталитическая система: (NH4)2S2O8, К2S2O8: S2O82- + 2 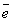 - ® 2SO42-,
являющаяся коионом по отношению к мембране МФ-4СК.
- ® 2SO42-,
являющаяся коионом по отношению к мембране МФ-4СК.
Результаты исследования позволяют
выделить 3 стадии синтеза (рис.4):
1. Сорбция противоионов
фениламмония по ионообменному механизму и его самоорганизация вблизи заряженных
центров перфторированной матрицы (эффект «узнавания» противоионами An+
фиксированных ионов -SO3-) и необменная сорбция вблизи кислородных групп на
боковых сегментах матрицы.
2. Инициирование
полимеризации ионов фениламмния электронами редокс-систем Fe3+/Fe2+ или
S2O82-/SO42-.
3. Собственно полимеризация ионов фениламмония
с образованием цепочек полианилина в наноразмерных структурных полостях
темплатной матрицы. Формирование редокс-системы полианилина в разных степенях
окисления в зависимости от параметров синтеза.

Рисунок 4 - Схема темплатного
синтеза композитов ПАн/МФ-4СК
1.4
Получение металлокомпозитов на основе перфторированных мембран и дисперсии
платины
В настоящее время все большее внимание исследователей
привлекает синтез металлокомпозитов. Для получения таких композитов на
мембранные материалы наносят различные металлы: платину, палладий, медь,
серебро.
Эти материалы обладают широким спектром полезных
свойств, которые не наблюдаются у раздельно используемых компонентов.
Рассмотрим более детально получение композитов на основе мембран типа нафион и
платины, которые находят применение в топливных элементах с протонпроводящей
мембраной, катализе, электрокатализе, синтезе органических соединений, для осуществления
окислительно восстановительной сорбции, получения обескислороженной воды
высокой чистоты. Эти материалы используют также для изготовления промежуточного
проводящего слоя в ионселективных электродах для получения устойчивого
потенциометрического сигнала. Металлические дисперсии можно наносить как с
одной стороны мембраны, так и с обеих сторон. Известно применение ионообменных
мембран с односторонним покрытием в ионной хроматографии, где они используются
в качестве барьера, который разделяет камеру генерации элюента и резервуар
источника ионов.
При этом электронпроводящий пористый слой из
платины на поверхности мембраны является катодом или анодом. Слой платины
наносится как на катионообменную, так и на анионообменную мембрану. Результат
модифицирования заключается в устранении мешающего влияния газа в элюенте и
снижение тепловыделения. В топливных элементах применяют мембраны с
двухсторонним покрытием дисперсией платины, которая является катализатором
окисления водорода и метанола [8].
Наиболее распространенным методом получения
наноразмерных частиц металлов в полимерах является химическое восстановление
соединений металлов [10]. Размер формирующихся наноразмерных частиц металла
зависит от условий взаимодействия и параметров пористой структуры полимера [8].
Перспективным направлением является нанесение каталитического слоя
непосредственно на поверхность мембраны, которая может служить в качестве
носителя нанодисперсной платины.
2. Экспериментальные
методы исследования
.1 Объекты исследования
и их физико-химические характеристики
Объектом исследования являлась
сульфокатионитовая перфторированная мембрана МФ-4СК п.29 в Н+ форме.
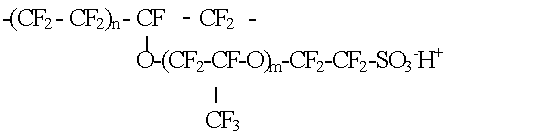
Рисунок 5 - Фрагмент химической
структуры мембраны МФ-4СК
Подготовка мембраны МФ-4СК включала
в себя несколько стадий. Образец гомогенной мембраны помещали в термостойкий стакан,
заливали 5% раствором HNO3 и кипятили в течение 3
часов. После кислоту сливали, за тем заливали мембрану 10% раствором H2O2 и кипятили
в течение 3 часов. В дальнейшем мембрану промывали дистиллированной водой до
нейтральной среды по лакмусу. После этого залили Н2О дист. и кипятили в течение
3 часов. Перед исследованием мембраны приводились с равновесие с раствором H2SO4 нужной
концентрации.
Так же в процессе электродиализа
использовались образцы промышленной гетерогенной анионообменной мембраны МА-41.
Анионообменная мембрана МА-41 изготовлена на основе высокоосновного анионита
АВ-17 с четвертичными аммониевыми основаниями.

Рисунок 6 - Фрагмент химической
структуры мембраны МА-41
Исследуемые образцы кондиционировались
по общепринятой методике. Поверхность анионообменной мембраны МА-41 протиралась
ватным тампоном, смоченным в четыреххлористом углероде CCL4 для
удаления масляной пленки. Через 10 минут растворитель улетучивался с
поверхности мембраны, и её погружали в этиловый спирт на 6 часов. Затем
мембрану заливали 5-кратным объемом раствора хлорида натрия в следующей
последовательности: насыщенный раствор NaCl на 24 часа;
раствор NaCl с
концентрацией 100 г/л на 24 часа, и раствор соли NaCl, содержащий
30 г/л на 24 часа. После образцы отмывали от раствора NaCl
дистиллированной водой с контролем сопротивления воды над мембраной и затем
также приводились в равновесие в раствором H2SO4 нужной
концентрации.
Таблица 1 - Физико-химические
свойства ионообменных мембран мембраны
|
Мембрана
|
l, см
|
Q,ммоль/гсух
|
W, %
|
nm,моль Н2О/ моль SO3-
|
|
МФ-4СК (п.29)
|
0,01905
|
0,93
|
26
|
20,6
|
|
МА-41
|
0,04600
|
1,01
|
|
|
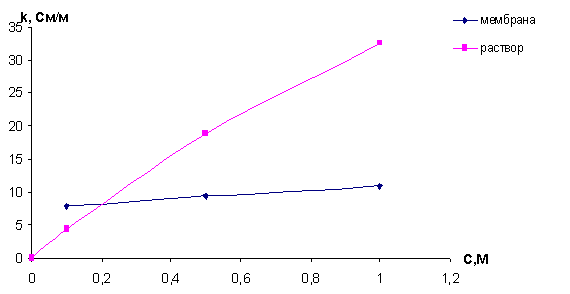
а)
б)
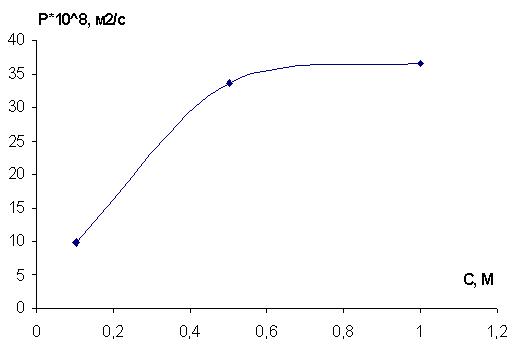
Рисунок 7- Концентрационные зависимости
электропроводности (а) и диффузионной проницаемости (б) для исходной мембраны
приведены
2.2 Методы
модифицирования ионообменных материалов полианилином
.2.1 Синтез методом последовательной
диффузии
Предварительно мембрана в Н+- форме закреплялась
ячейке для определения ддифузионной проницаемости (рис. 8). В одну камеру
ячейки заливали 1М солянокислый анилин, в другую - дистиллированную воду.
Сопротивление в камере с водой регистрировалось кондуктометрическим методом с
помощью измерителя иммитанса Е7-21 (частота 1 кГц).
Раствор мономера заменялся на 0,1М раствор
персульфат аммония, в камеру заливалась свежая порция воды и регистрировалось
сопротивление в камере с водой. Воздействие мономера составляло 15 мин,
окислителя - 60 мин.

Рисунок 8- Схема диффузионной ячейки:
1-электрическая мешалка, 2 прокладки из вакуумной резины, 3-иследуемая
мембрана, 4-платенированные платиновые электроды, 5-мост переменного тока Е7-13
2.2.2 Синтез в условиях
внешнего электрического поля
Метод синтеза композитных мембран МФ-4СК/ПАн в
условиях внешнего электрического поля (ЭП) основан на одновременном воздействии
на мембрану в процессе синтеза градиентов концентрационного и электрического
полей [37]. Синтез проводился в лабораторной электродиализной установке, схема
которой представлена на рис. 9, - шестикамерная электродиализная ячейка
содержит 3 катионообменные и 2 анионообменные мембраны (5), снабжена двумя платиновыми
электродами (6), рабочая поверхность которых 36 см2, включает две электродные и
две буферные камеры, камеры концентрирования и обессоливания. Электрическая
часть схемы установки состоит из источника постоянного тока 7, амперметра 9 и
вольтметра 8. Процесс проводился при постоянной плотности электрического тока и
постоянной скорости циркуляции рабочего раствора. Гидравлическую функцию
выполняют циркуляционные насосы 3, и ёмкости с растворами 4. Скорость протока
раствора в камере обессоливания и камере концентрирования составляет 100
мл/мин, что соответствует линейной скорости 0,19 см/с. Объем раствора,
циркулирующего в камерах обессоливания и концентрирования, равняется 400 мл, в
электродных и буферных камерах 200 мл. Через ячейку пропускали ток 200 различной
плотности в зависимости от условий синтеза.
Пропускание тока через мембрану МФ-4СК в
катодном направлении в исследуемой схеме играет роль только направляющего
фактора по отношению к потокам компонентов, но не приводит к окислению
мономера. При помощи моста переменного тока 2, присоединенного к проточным
ячейкам 1, снабженных платиновыми электродами, регистрировали сопротивление
раствора в камерах обессоливания и концентрирования. Модифицирование
проводилось в несколько последовательных стадий, каждая из которых заключалась
в воздействии на базовую мембрану различными растворами.
Предварительно проводился процесс электродиализа
0,01 М H2SO4 с исходной мембраной МФ-4СК в течение 30 минут. На первой стадии,
не разбирая ячейки после электродиализа с раствором кислоты, в камеру
обессоливания вводили раствор, содержащий 0,01 М раствор анилина на фоне 0,01 М
H2SO4, проводили процесс электродиализа в течение 60 или 30 мин Таким образом,
происходило насыщение базовой мембраны ионами ФА+ в условиях внешнего электрического
поля. В остальных камерах при этом циркулировал рабочий раствор 0,01 М H2SO4.
На второй стадии, не разбирая ячейку, раствор в камере обессоливания заменяли
другим модельным раствором, содержащим инициатор полимеризации анилина 0,01М
FeCl3 на фоне 0,01 М H2SO4, процесс электродиализа проводили в течение 1 часа.
При этом на ячейку подавалась сила тока 148 или 100 мА, что соответствует
плотности тока 27 или 41 А/м2.


Рисунок 9 - Схема электродиализной установки для
получения композитов в условиях внешнего электрического поля.
- ячейка для регистрации сопротивления рабочего
раствора; 2 - измеритель иммитанса E7-21; 3 - циркуляционные насосы; 4 -
емкости с раствором; 5 - платиновые электроды; 6 - электродиализная ячейка; 7 -
источник постоянного тока Б5-50; 8 - вольтметр Щ4313; 9 - амперметр М253.
Мембрану МФ-4СК/ПАн №1 использовали в повторном
электродиализе, как вспомогательную для модифицирования мембраны МА-41. При
этом в качестве окислителя использовали 0,05М раствор (NH4)2S2O8
на фоне 0,01 М H2SO4 (время воздействия 60 мин.). В результате эксперимента
окраска мембраны изменилась от лазурно - зеленой до непрозрачной
однородно-черной (МФ-4СК/ПАн №4 в табл. 2.2).
На протяжении всех трёх стадий через каждые 5
минут регистрировали следующие параметры: сила тока и напряжение в системе,
сопротивление растворов в камере обессоливания и в камере концентрирования.
В результате синтеза был изготовлен набор
композитов, полученных в различных условиях синтеза, представленный в таблице
2.
Таблица 2- Режимы проведения синтеза в условиях
электродиализа
|
образец
|
i, A/м2
|
tпропускания 0,01M
C6H5NH2+0,01M
H2SO4, мин
|
tпропускания 0,01M
FeCl3+0,01M
H2SO4,мин
|
tпропускания
0,05M (NH4)2S2O8+0,01M H2SO4, мин
|
tпропускания 0,05M
C6H5(NH2)+ 0,01M
H2SO4, мин
|
|
МФ-4СК
№1
|
27
|
60
|
60
|
-
|
-
|
|
МФ-4СК
№3
|
27
|
30
|
60
|
-
|
-
|
|
МФ-4СК
№2
|
41
|
60
|
60
|
-
|
-
|
41
|
30
|
60
|
-
|
-
|
|
МФ-4СК/ПАн
№4
|
27
|
-
|
-
|
60
|
60
|
* Композитная мембрана изготовлена Долгополовым
С.В
Был выполнен процесс электродиализного
концентрирования раствора 0,01 М H2SO4
с применением исходной мембраны МФ-4СК и композитов на ее основе и проведен
расчет параметров процесса электродиализа.
Концентрация электролита (c) в камерах
обессоливания и концентрирования рассчитывается по формуле:
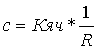 (7)
(7)
Одним из важнейших параметров, характеризующих
работу электродиализатора, является выход по току, который представляет собой
отношение перемещенных грамм-эквивалентов электролита к прошедшему количеству
электричества. Интегральный выход по току (η)рассчитывается
по формуле
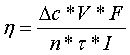 , (8)
, (8)
где n - число камер обессоливания (в данной
работе n=1); V - объём обессоливаемого раствора, л (V = 0,200л); I - сила тока,
А; F - число Фарадея, равное 96500 Кл/г-экв; τ - время,
с; ∆с - изменение концентрации за время τ, моль-экв/л.
Величина, характеризующая эффективность работы
электродиализатора - это удельный расход электроэнергии (Q), расходуемого на
перенос одного грамм-эквивалента вещества
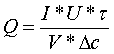 , (9)
, (9)
где U - напряжение в системе, В.
Степень обессоливания (ω)
рассчитывается
по формуле
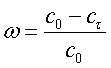 , (10)
, (10)
где С0 - начальная концентрация, моль/л; Сτ
- концентрация
к моменту времени τ в камере
обессоливания, моль/л;
2.2.2.1 Методика
платинирования электродов
Для лучшей воспроизводимости результатов
выполнили платинирование платиновых электродов в проточных ячейках. Для этого
электроды погрузили в раствор H2PtCl6
и в течение 30 минут пропускался ток. Через каждые 5 минут изменяли полярность
электродов с помощью переключателя 4 (рис. 8). Затем проводится уплотнение
осадка платины, пропусканием более сильного тока в течение 5 минут. Для
вытеснения газообразных продуктов электролиза (Cl2)
из осадка платины на электродах, в ячейку заливался 10% раствор Н2SO4, оба
электрода служили катодом, в качестве анода использовали вспомогательный
электрод. Электролиз проводился в течение 30 минут, после чего электроды
тщательно промывали водой.
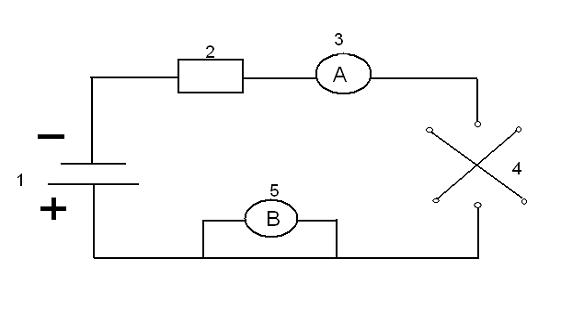
Рисунок 10-Схема установки для платинтрования:
1-источник питания постоянного тока, 2-магазин сопротивления, 3-прибор, комбин.
Цифровой Ц 4313, 4-ключ для изменения направления тока, 5- Amperevoltmetr
Ц 4311
Геометрические константы:
Ккк=2,4688 Кко= 5,1671
Геометрические константы, полученные в
результате повторного платинирования после проведения нескольких синтезов, с
целью восстановления исходных значений констант:
Ккк=2,7891 Кко= 5,9694
2.2.3 Получение
нанодисперсной платины на поверхности мембраны МФ-4СК/ПАн
Получение композита МФ-4СК/ПАн/Pt
проводили в чашке Петри под вытяжным шкафом в несколько стадий. Образец
МФ-4СК/ПАн, полученный методом последовательной диффузии, обрабатывали
гидразингидратом и наблюдали за изменением окраски (из зеленого в
пепельно-серый) в течении 3 часов. Затем были проведены исследования ее
диффузионных свойств.
После этого мембрану повторно обработали
гидразингидратом и в течение 5 минут наблюдали за изменением окраски (мембрана
стала более светлая, а так же наблюдалось выделение газа). Полученный образец
промыли дистиллированной водой и на 1 час залили раствором H2PtCl6.
Во время протекания процесса мембрана темнеет, и на ней образовываются черные
вкрапления.
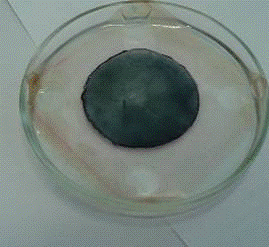

а б

в
Рисунок 11- изменения цветности мембраны в
процессе получения нанодисперсной платины на поверхности мембраны: а- мембрана
МФ 4СК/ПАн после обработки гидразингидратом; б- после повторной обработки
гидразингидратом; в- мембрана после взаимодействия с раствором H2PtCl6
2.3 Методы определения
электротранспортных свойств мембран
.3.1 Методы определения
электропроводности
Одним из наиболее простых и распространенных
методов определения электропроводящих свойств мембран является разностный
метод. В этом методе используют пинцетную ячейку, схема которой указанна на
рис. 12.
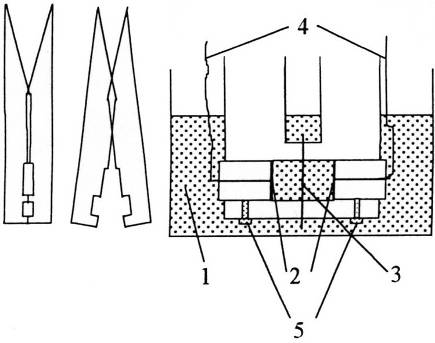
Рисунок 12- Схема пинцетной ячейки: 1-стакан с
равновесным раствором; 2-платинированные платиновые электроды; 3-мембрана;
4-изолированные проводники; 5-винты, фиксирующие положение электродов
Удельную электропроводность мембраны (k,
См/м) вычисляли по формуле
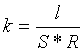 , (11)
, (11)
где l
- толщина мембраны, м; R
- измеряемое сопротивление, Ом; S
- площадь электродов (S
= 1,032 см2).
Для определения удельной электропроводности
полученных композиционных мембран был использован так же ртутно-контактный
метод. На рисунке 1 представлено схематическое изображение ртутно-контактной
ячейки. Данный метод является экспрессным и достаточно точным способом
определения сопротивления мембран, а также позволяет измерять сопротивление
образцов мембраны без нарушения их механической целостности и химического
состояния. Кроме того, в качестве контактирующей среды между мембраной и
платиновыми электродами ячейки, используется ртуть, которая и предохраняет
мембрану от высыхания. Перед измерением сопротивления образцы мембран были
приведены в равновесие с раствором 0,005 М H2SO4
и термостатированы при 250 С.

Рисунок 13 - Схематическое изображение
ртутно-контактной ячейки:
- измерительные платиновые электроды; 2 - мембрана;
3 - ртуть
Образец мембраны размером 2´5
см закрепляют с помощью винта между камерами ячейки заполненной ртутью. Затем
ячейку поворачивают на 180°. При этом платиновые
электроды, закреплённые на дне ячейки, погружаясь в ртуть, обеспечивают
электрический контакт мембран с ртутью. Пузырьки воздуха удаляются поворотом
ячейки в разные стороны. Сопротивление измеряют с помощью измерителя импеданса
ТESLA ВМ-507 на частоте ≈200
кГц. При измерениях сопротивления мембраны частота переменного тока подбирается
таким образом, чтобы фазовый угол, характеризующий величину реактивной части
импеданса системы ртуть-мембрана-ртуть, был равен нулю. Величина относительной
систематической погрешности определения сопротивления импедансом ВМ-507 не
превышала 5%. Как показано, применение высокочастотной схемы для измерения
импеданса мембраны между ртутными электродами позволяет значительно уменьшить
вклады сопротивлений переходных границ ртуть/мембрана. Эти вклады вносят
погрешность в измерение импеданса в ртутно-контактной ячейке на частоте 1 кГц,
которая может достигать 100 % и занижать истинное значение удельной
электропроводности мембраны. Согласно методике, измерение сопротивления каждой
мембраны проводится не менее трёх раз, при условии, что полученные значения
отличаются друг от друга в пределах погрешности. Измерение толщины образцов
проводилось микрометром типа МК с погрешностью не более 20 % и определялась
путем измерения в 10 точках образца.
Удельную электропроводность мембраны (k,
См/м) вычисляли по формуле (11).
2.3.2 Метод определения
диффузионной проницаемости
Определение интегрального коэффициента
диффузионной проницаемости мембран проводилось в непроточной ячейке, состоящей
из двух полукамер объемом 100мл (рисунок 6)Одна камера заполнялась раствором
электролита (Н2SO4), а другая - дистиллированной водой. Растворы перемешивались
со скоростью 60 об/мин. Через каждые 30 секунд регистрировалось изменение
концентрации электролита в камере с водой.
Поток электролита через мембрану
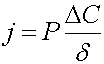 (12)
(12)
где  -
интегральный коэффициент диффузионной проницаемости мембраны,
-
интегральный коэффициент диффузионной проницаемости мембраны, 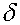 -
толщина мембраны,
-
толщина мембраны, 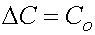 , т.е. концентрации
раствора в камере І, т.к. концентрация раствора в камере ІІ близка к нулю в
начальный момент времени. За время Δ
, т.е. концентрации
раствора в камере І, т.к. концентрация раствора в камере ІІ близка к нулю в
начальный момент времени. За время Δ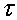 в камере ІІ концентрация увеличится на Δ
в камере ІІ концентрация увеличится на Δ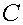 за счет переноса электролита через мембрану.
за счет переноса электролита через мембрану.
При этом количество вещества Δ ,
перенесенного через мембрану за Δ
,
перенесенного через мембрану за Δ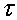 ,
определяется как
,
определяется как
Δ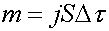
а изменение концентрации
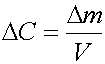
где  -
площадь мембраны,
-
площадь мембраны, 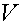 - обьем
электролита. Отсюда
- обьем
электролита. Отсюда
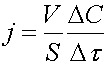 или
или 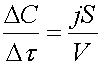 (13)
(13)
При стационарном режиме 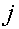 ,
,
 ,
,
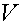 -
постоянные величины, поэтому зависимость концентрации от времени линейна. Из
уравнения (12) и (13) получается уравнение (14) для расчета коэффициента
проницаемости
-
постоянные величины, поэтому зависимость концентрации от времени линейна. Из
уравнения (12) и (13) получается уравнение (14) для расчета коэффициента
проницаемости
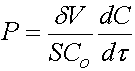 (14)
(14)
3. Результаты и
обсуждение
.1 Синтез композитных
мембран МФ-4СК/полианилин в условиях внешнего электрического поля
На рисунке 14 представлены кинетические кривые
переноса полимеризационных растворов в процессе синтеза композиционных мембран
в условиях внешнего электрического поля.
а)

б)
Рисунок 14 - Кинетическая зависимость изменения
сопротивления растворов Н2SO4 (0,01М), C6H5(NH2)
(0,01М) + Н2SO4 (0,01М), FeCl3.
(0,01М) + Н2SO4 (0,01М) от времени в камере концентрирования и камере
обессоливания: а) i=27 А/м2, б)
i=41 А/м2
Видно, что при появлении в растворе крупного
органического фениламмония, который является мономером полимеризации анилина,
происходит резкое снижение скорости относительно переноса серной кислоты. Это
связанно с тем, что ион фениламмония способен накапливаться не только на
механизме ионного обмена около фиксированных зарядов, но и за счет
сверхэквивалентной сорбции околофиксированных атомов кислорода боковых
сигментов [39].
При появлении полизарядных ионов Fe3+
(окислитель) происходит дополнительное снижение скорости электродиффузионного
переноса не смотря на то, что под действием окислителя происходит полимеризация
мономера и образование жестких ароматических цепей полианилина. Это снижение
связанно с дополнительной сшивкой кластерной зоны за счет комплексообразования
ионов железа с фиксированными сульфогруппами.
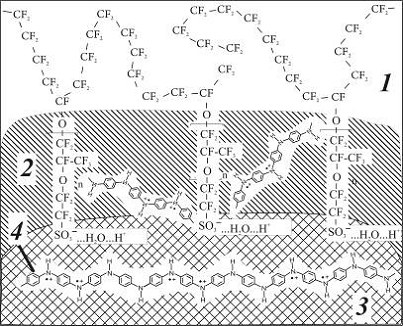
Рисунок 15 - Строение композита МФ-4СК/ПАн
1 - фторэтиленовые
цепи, 2 - область интермедиата, 3 - кластерная зона, 4 - цепи Пан
Видно, что при увеличении плотности тока в 1,5
раза происходит значительное увеличение скорости переноса рабочих растворов не
зависимо от их природы.
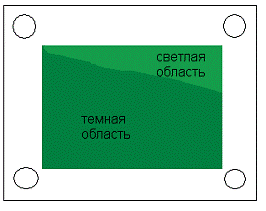
В результате был получен композит с неоднородной
изумрудно-зеленой окраской (рис. 16а). Около 20% рабочего окна имело более
светлую окраску, что связанно с плохим омыванием раствором рабочей поверхности.
Наличие такой окраски связано с образованием внутри мембраны полианилина в
форме эмеральдина. В случае проведения синтеза с большей плотностью тока
наблюдается равномерное окрашивание всего рабочего окна (рис. 16б).
а б
Рисунок 16 - Вид образцов в результате
модифицирования: а - мембрана №1(i=21
А/м2), б - мембрана №2 (i=21
А/м2)
После определения электротранспортных
характеристик композит №1 подвергли повторному модифицированию в процессе
электродиализа с применением в качестве окислителя S2O82-
- коиона по отношению к перфторированной мембране. Таким образом предполагалось
получить поверхностно модифицированный композит. В результате эксперимента был
получен композит №4, при этом окраска мембраны изменилась от лазурно - зеленой
до однородно черной не прозрачной (рис. 17).
полианилин электротранспортный мембрана

Рисунок 17- Мембрана МФ-4СК/ПАн после повторного
модифицирования
3.2 Электротранспортные
свойства композитных мембран
В задачу исследования входило исследование
диффузионных и электропроводящих свойств полученных мембран. Диффузионная
проницаемость набора полученных композитных мембран представлена в таблице 3 и
на рисунке 18.
Таблица 3- диффузионная проницаемость
ионообменных мембран.
|
мембрана
|
Р*108, см2/с
|
|
0,1М
Н2SO4
|
η
|
1М
Н2SO4
|
0,5М
Н2SO
|
η
|
|
Рs
|
Рw
|
|
Рs
|
Рw
|
Рs
|
Рw
|
|
|
МФ-4СК
п.29
|
9,8
|
9,8
|
1
|
36.6
|
36.6
|
33,7
|
33,7
|
1
|
|
МФ-4СК/Пан №1
|
9,7
|
9,6
|
1
|
33.8
|
33.8
|
|
|
|
|
МФ-4СК/Пан №2
|
9,9
|
10,3
|
0,96
|
|
|
|
|
|
|
МФ-4СК/Пан
№4
|
2,9
|
3,6
|
0,81
|
|
|
|
|
|
|
МФ-4СК/ПАн №3
|
|
|
|
|
|
25,1
|
26,4
|
0,95
|
|
МФ-4СК/Пан*
|
2,6
|
3,2
|
0,81
|
|
|
|
|
|
* Данные получены Долгополовым С.В.

Рисунок 18 - Влияние режима модифицирования
мембран МФ-4СК полианилином в условиях внешнего электрического поля на их
диффузионные характеристики в 0,1М растворе Н2SO4
Видно, что после модифицирования во всех случаях
происходит снижение диффузионной проницаемости. Так же проявляется
ассиметричный характер этого параметра в зависимости от ориентации мембраны к
потоку электролита. Для оценки этого эффекта использовали коэффициент
асимметрии: η=Ps/Pw,
где Ps -
соответствует случаю, когда модифицированная сторона встречает поток
электролитов, а Pw
- когда немодифицированная сторона обращена к потоку электролитов. Применение
мягких режимов модифицирования (i=27
A/м2, i=41
A/м2) практически не
наблюдается асимметрия диффузионной проницаемости (η=0,96).
В случае применения в качестве окислителя коиона
S2O82-
c высоким значением
стандартного редокс-потенциала (E0=2,13)
полимеризация протекает преимущественно в поверхностных слоях мембраны и
коэффициент асимметрии достигает 0,81. Однако это сопровождается резким
снижением диффузионной проницаемости примерно в 3 раза за счет блокирования
поверхности мембраны положительно заряженными цепями полианилина.
Аналогичную зависимость от режима
модифицирования имеет электропроводность. Для композита, который имеет
неоднородную окраску, было выполнено измерение сопротивления в светлой и темной
областях. Электропроводность светлой области близка к электропроводности
исходной мембраны, а в темной области она ниже на 20-40% (табл. 5). Аномальным
является увеличение электропроводности композита при увеличении плотности тока
в процессе модифицирования. Это вероятно связанно с вкладом
протонно-электронной проводимости полианилина в суммарную электропроводимость
композитной мембраны.
Таблица 5 - Электропроводность композитных
мембран МФ-4СК/ПАн в растворах H2SO4,
измеренная разностным методом
|
мембрана
|
k, Ом-1м-1 0,1М Н2SO4
|
k, Ом-1м-1 0,5М
Н2SO4,
|
k, Ом-1м-1 1М Н2SO4,
|
|
МФ-4СК
|
7,8
|
9,4
3,7*
|
10,8
|
|
МФ-4СК/ПАн
№1
|
темн.обл.
5,5 светл.обл. 7,2
|
-
|
темн.обл.
8,9 светл.обл. 9,8
|
|
МФ-4СК/ПАн
№2
|
7,6
|
-
|
-
|
|
МФ-4СК/Пан
№4
|
0,1
|
-
|
-
|
|
МФ4-СК/ПАн №3
|
-
|
8,5
1,2*
|
-
|
*Величина электропроводности измерена
ртутно-контактным методом

Рисунок 19 - Влияние режимов модифицирования
мембран МФ-4СК полианилином в условиях внешнего электрического поля на их
электропроводность в 0,1М растворе Н2SO4
Более высокие значения плотности тока в процессе
синтеза способствуют лучшему распределению, как мономера, так и окислителя в
объеме матрицы МФ-4СК. Это обуславливает образование более протяженных цепей
полианилина. В процессе модифицирования под действием внешнего электрического
поля происходит «ламинирование» кластерной зоны темплатной матрицы и
локализации цепей в области фиксированных сульфо-групп (рис. 20).

Рисунок 20 - «Ламинирование» системы
транспортных каналов темплатной матрицы МФ-4СК цепями полианилина
В случае применения в качестве окислителя S2O82-
одновременно со снижением диффузионной проницаемости, происходит снижение
электропроводности мембран примерно в 80 раз. Это связанно с вытеснением
свободного раствора из мембраны, что приводит к снижению протонной проводимости.
В работе [40] показана перспективность
применения таких композитов в процессах электродиализного концентрирования
растворов NaCl. Таким
образом на основании выбранных исследований можно сделать выводы о влиянии
режимов модифицирования на электротранспортные характеристики мембран. Более
предпочтительным является проведение синтеза при i=41
A/м2 при этом время
проработки мембраны мономером должно составлять 30 минут, а окислителя 60
минут.
3.3 Поведение мембран в
условиях электродиализного концентрирования раствора H2SO4
Выбор модельного раствора обусловлен тем, что
ключевой характеристикой мембраны в топливном элементе является протонная
проводимость. На рисунке 21 и 22 приведены кинетические кривые изменения
концентрации H2SO4
в камере концентрирования и камере обессоливания для исходной и
модифицированных мембран.
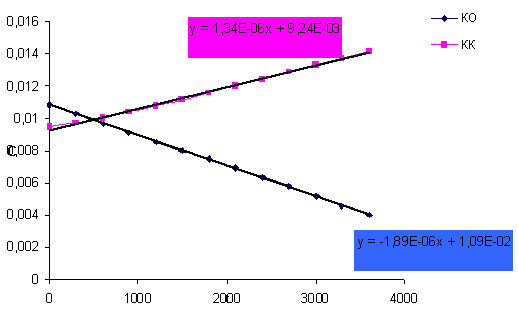
Рисунок 21- Кинетическая зависимость изменения
концентрации раствора Н2SO4 от времени в камере концентрирования и в камере
обессоливания
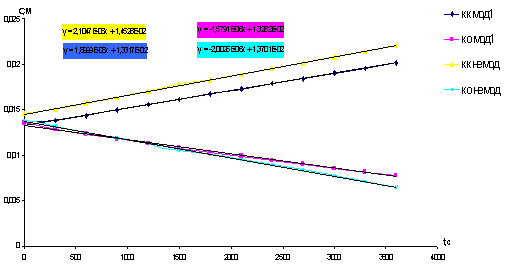
Рисунок 22 - Кинетическая зависимость изменения
концентрации раствора Н2SO4 от времени для мембраны МФ-4СК и композита №3
В случае применения композита скорость переноса
протонов через мембрану выше, чем для исходной мембраны. Независимо от
ориентации композита к потоку протонов в работе [41] было показано, что
протонная проводимость композитных мембран МФ-4СК/ПАн, полученных методом
последовательной диффузии в статических условиях, выше в 2-4 раза по сравнению
с протонной проводимостью МФ-4СК. Это связано с вкладом протонной проводимости
полианина. Оценка энергии активации электропроводности для данных мембран
показало, что таковая на 10-12% выше для композитов по сравнению с исходной
мембраной.
Таблица 6 - сводная таблица параметров процесса
электродиализа
|
Мембрана
МФ-4СК
|
η,%
|
Q,кВ
|
W
|
U,В
|
I,mA
|
|
ко
|
ко
|
кк
|
ко
|
|
|
31,70
|
7,8
|
5,4
|
0,6235
|
22,75
|
|
МФ-4СК/ПАн
№3 к кк
|
52,22
|
4,2
|
9,3
|
0,4174
|
19,12
|
|
МФ-4СК/ПАн№3
к ко
|
67,47
|
5,3
|
19,6
|
0,7548
|
36,30
|
Расчет параметров процесса электродиализа
показал, что одновременно с асимметрией диффузионной проницаемости наблюдается
ассиметрия параметров электродиализа. В случае, когда мембрана обращена
модифицированной поверхностью в камеру обессоливания, удается достигнуть более
высокие степени концентрации и выходы по току по сравнению с исходной мембраной
и со случаем, когда мембрана обращена немодифицированной стороной к камере
обессоливания.
3.4 Композиты мембран
МФ4-СК/ПАн/Pt
В ряде работ [42] была показана перспективность
модифицирования перфторированных мембран полианилином для уменьшения подсыхания
и сохранения высокой протонной проводимости последних при рабочих температурах
низкотемпературного топливного элемента. Описаны также работы по получению
гибридных материалов на основе мембран типа Нафион и дисперсии платины [43]. В
настоящей работе была предпринята попытка получить трехкомкомпонентный композит
МФ-4СК/ПАн/Pt, которые
помимо высокой протонной проводимости, обладал бы каталитической активностью по
отношению к реакции восстановления кислорода. Для этого композитную мембрану
МФ-4СК/ПАн, полученную методом последовательной диффузии, подвергли воздействию
восстановителя - гидразин гидрата. При этом происходит восстановление
эмеральдина до полностью восстановленной формы лейкоэмеральдина, что
сопровождается изменением окраски мембраны из зеленого в пепельно-серый (рис
9а). Далее мембрану погрузили в раствор H2PtCl6
и провели матричное восстановление платины, что сопровождалось потемнением
мембраны и образованием на ней черных вкраплений (рис 9в).
При таком методе модифицирования в качестве
восстановителя платины выступает полианилин в форме лейкоэмеральдина, который
возвращается в проводящую форму эмеральдина (рис. 23).
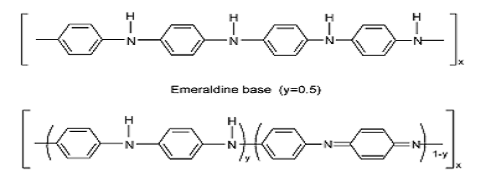

Рисунок 23 - формы полианилина
Получена гибридная мембрана МФ-4СК/ПАн/Pt.
На всех этапах химических превращений состояние мембраны контролировалась
диффузионная проницаемость и электросопротивление мембраны в растворе 1М НСl
(Табл.7, Табл.8, рис.24).
Таблица 7 - Диффузионная проницаемость мембраны
МФ-4СК на различных этапах ее модифицирования платиной в растворе 1н HCl
|
мембрана
|
Ps, см2/с
|
Pw
|
η
|
|
МФ-4СК
|
7,13*10-7
|
7,13*10-7
|
1
|
|
МФ-4СК/ПАн
|
5.78*10-7
|
6.38*10-7
|
0,91
|
|
МФ-4СК/ПАн
(после обработки гидразин гидратом)
|
4.68*10-7
|
4.84*10-7
|
0,97
|
|
МФ-4СК/ПАн/Pt
|
4.13*10-8
|
3.70*10-8
|
0,89
|
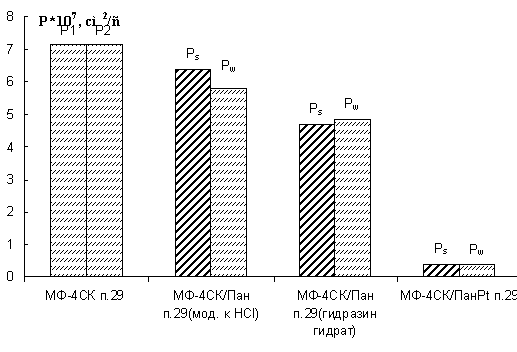
Рисунок 24 - Изменение диффузионной
проницаемости мембраны МФ 4СК в процессе ее модифицирования платиной
Так, после поверхностного модифицирования
мембраны МФ-4СК полианилином происходит снижение ее диффузионной проницаемости
и появление эффекта асимметрии данной характеристики. Это связано с тем, что
матричный синтез полианилина протекает под действием градиента концентрации
рабочих растворов, а природа окислителя S2O82-
- коион по отношению к сульфокатионитовой мембране, способствует образованию
полианилина преимущественно в поверхностных слоях мембраны. В работе [38]
методом Сканирующей Электронной Микроскопии поверхностей мембран (рис.25)
показано, что на поверхности мембраны, контактировавшей в процессе синтеза с полимеризующими
растворами, образуется микроразмерный слой полианилина (0,3-2,3 мкм), имеющий
чешуйчатую структуру. При этом обратная сторона мембраны содержит выходы из
гранул полианилина размером не более 20-50 нм, “проросшего” через мембрану в
процессе автокаталитической полимеризации.



а б в
Рисунок 25 - СЭМ-микрофотографии поверхности
исходной (а) и композитной (б, в) мембран б - модифицированная сторона, в -
немодифицированная сторона
После воздействия восстановителя диффузионная
проницаемость мембраны перестает носить асимметричный характер, поскольку форма
лейкоэмеральдина является незаряженной, отсутствует влияние плотного слоя
положительно-заряженного полианилина в поверхностных слоях анизотропной
мембраны. В гибридной мембране МФ-4СК/ПАн/Pt
и диффузионная проницаемость, и электропроводность уменьшились практически на
порядок. Снижение диффузионной проницаемости связано с возникновение
стерических затруднений для диффузионного потока в виде частиц металла.
На рисунке 26 представлено изменение
электропроводности мембраны в процессе модифицирования полианилином и платиной.
Так после формирования анизотропных композитов МФ-4СК/ПАн происходит снижение
проводимости в 5 раз, что согласовывается с результатами [44]. После
восстановления эмеральдина до лейкоэмеральдина происходит увеличение
проводимости, обусловленное переходом полианилина не проводящей не заряженной
формы. Таким образом невелируется эффект электростатического отталкивания
катиона Н+ и положительных центров на азоте.
Таблица 8 -Измерение электропроводности
разностным методом мембран (lср=0,0193см)
в 1М НСl.
|
Æ, Ом-1м-1
|
Вид
мембраны
|
|
10
|
МФ-4СК
|
|
1.9
|
МФ-4СК/ПАн
|
|
5.3
|
МФ-4СК/ПАн
(после обработки гидразин гидратом)
|
|
1.17
|
МФ-4СК/ПАн/Pt п.29
|
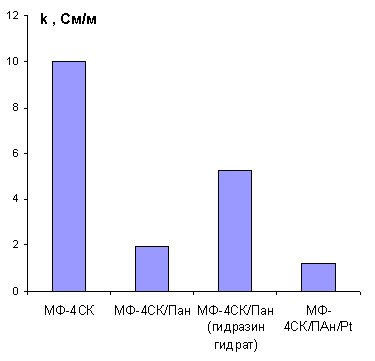
Рисунок 26 - Изменение электропроводности
мембраны МФ-4СК в процессе ее модифицирования платиной
Полианилин создает лишь стерические затруднение
для переноса Н+, что сказывается на снижении электропроводности данной формы
мембраны относительно начальной в два раза. После осаждения дисперсии платины,
полианилин переходит в форму эмеральдина, что приводит к снижению величины
электропроводности до уровня проводимости МФ-4СК/ПАн.
Заключение
Исследована возможность получения и
приготовления мембран МФ-4СК/ПАн в различных режимах с применением разбавленных
полимеризующих растворов. Проведены измерения электропроводности и диффузионной
проницаемости полученных композитов и выявлены их сравнительные характеристики.
Выбран режим процесса модифицирования в условиях внешнего электрического поля,
позволяющий получить композиты с хорошим выходом по току (50-67%). Обнаружена
асимметрия характеристик процесса электродиализа (по камере концентрирования и
камере обессоливания, выходу по току, энергозатратам), зависящая от ориентации
композита к потокам полимеризующих растворов. Выполнены предварительные
исследования возможности получения гибридных мембран, содержащих дисперсии
платины, с использованием полианилина как восстановителя.
Список использованных источников
1.
Kang, Y. Doping of polyaniline by thermal acid-base exchange reaction / Y.
Kang, S.K. Kim, C. Lee // Materials Science and Engineering C. - 2004. - Vol.
24. P. 39-41.
.
Ray, A. Polyaniline - protonation deprotonation of amine and imine sites / A.
Ray, A.F. Richter, A.G. MacDiarmid, A.J. Epstein // Synthetic Metals. - 1989. -
Vol. 29. - №1. - P. E151-E156.
.
Javadi, H.H.S. Charge transport in the emeraldine form of polyaniline / H.H.S.
Javadi, F. Zou, K.R. Cromack, M. Angelopoulos, A.G. MacDiarmid, A.J. Epstein
Synthetic Metals. - 1989. - Vol. 29. - №1. - P. E409-E416.
4.
Алпатова, Н.М. Электрохимический темплатный синтез композита полианилина с
полимерным перфторированным сульфокатионитом / Н.М. Алпатова, В.Н. Андреев,
А.И. Данилов, Е.Б. Молодкина, Ю.М. Полукаров, Н.П. Березина, С.В. Тимофеев,
Л.П. Боброва, Н.Н. Белова // Электрохимия. - 2002. - Т. 38. - №8. - С.
1020-1025.
5.
Pud, A. Some aspects of preparation methods and properties of polyaniline
blends and composites with organic polymers / A. Pud, N. Ogurtsov, A.
Korzhenko, G. Shapoval // Progress in Polymer Science. - 2003. - Vol. 28. - P.
1701-1753.
6.
Сари, Б. Электрохимическая полимеризация анилина при низких концентрациях
индифферентного электролита и свойства полученных плёнок Б. Сари, М. Талу, Ф.
Йилдирим. // Электрохимия. - 2002. - Т. 38. - №7. - С. 797-804.
.
Березина, Н.П. Физико-химические свойства ионообменных материалов / Н.П.
Березина, Н.А. Кононенко, Г.А. Дворкина, Н.В. Шельдешов. - Краснодар: Изд-во
Кубан. гос. ун-та, 1999. - 82 с.
8.
Юттнер, К. Получение и свойства композитных каталитических систем полипиррол-Pt
/ К. Юттнер, К.-М. Мангольд, М. Ланге, К. Боузек // Электрохимия.− 2004.−
Т.
40, №3.− С.
359-368.
.
Hatchett, D.W. Reduction of PtCl62- and PtCl42- in polyaniline: Catalytic
oxidation of methanol at morphologicall different composites / D.W. Hatchett,
R. Wijeratne, J.M. Kinyanjui // Journal of Electroanalytical Chemistry.- 2006.-
V. 5.- P.
203-210.
.
Андреев, В.Н. Строение и свойства композитных электродов нафион полианилин-Pd
/ В.Н. Андреев, В.И. Золотаревский // Электрохимия. − 2005. Т. 41, №2. −
С.213-218.
11.
Березина, Н.П. Протон-электронная проводимость и структура композитных мембран
МФ-4СК, модифицированных полианилином или платиной / Н.П. Березина, А.А.-Р.
Кубайси, И.А. Стенина, Р.В. Смолка, С.В. Тимофеев // Серия. Критические
технологии. Мембраны.− 2006.− Т. 32, №4.− С. 48-55.
12.Гурский,
В.С. Электрохимический генератор ионов для калибровки проточных анализаторов /
В.С. Гурский, Ю.А. Олейникова, Е.Ю. Харитонова, А.Г. Шматко // Тезисы докладов
VII Научно-технического совещания «Проблемы и перспективы развития химического
и радиотехнического контроля в атомной энергетике». Сосновый Бор.− 2009.
.
Электрохимия полимеров / Под ред. М.Р. Тарасевича, С.Б. Орлова, Е.И.
Школьникова и др. - М.: Наука, 1990. - 238 с.
14. Bessarabov, D. Solid
polyelectrolyte (SPE) membranes with textured surface / D. Bessarabov, R.
Sanderson // Journal of Membrane Science
<http://elibrary.ru/issues.asp?id=614&selid=585661>.- 2004
<http://elibrary.ru/issues.asp?id=614&jyear=2007&selid=585661>.
15.
Электрохимия полимеров / Под ред. М.Р. Тарасевича, С.Б. Орлова, Е.И.
Школьникова и др. - М.: Наука, 1990. - С. 120-143.
16.
Elyashevich, G.K. Properties of polymer
conducting thin layer on the surface of microporous polyethylene / G.K.
Elyashevich, V.K. Lavrentyev, I.S. Kuryndin, E.Yu. Rosova // Synthetic Metals.
- 2001. - Vol. 119. - P. 277-278.
.
Chiang, J.-C. “Polyaniline”: protonic acid
doping of the emeraldine form to the metallic regime / J.-C. Chiang, A.G.
MacDiarmid // Synthetic Metals. - 1986. - Vol. 13. - P. 193-205.
.
Bartlett, P.N. Oxidation of beta-nicotinamide
adenine dinucleotide (NADH) at poly(aniline)-coated electrodes / P.N. Barklett,
P.R. Birkin, E.N.K. Wallace // J. of the Chemical Society - Faraday
Transactions. - 1997. - Vol. 93. - № 10. - P. 1951-1960.
20.
Вода в полимерах / Под ред. С. Роуленда. - М.: Мир, 1984. - С. 443-468.
21.
Xu, T. Effect of asymmetry in a bipolar membrane on water dissociation - a
mathematical analysis // Desalination. - 2002. - Vol. 150. - № 1. - P. 65-74.
.
Bae, B.C. Preparation and characterization of nafion/poly(1-vinylimidazole)
composite membrane for direct methanol fuel cell application / B.C. Bae, H.Y.
Ha, D. Kim // J. of the Electrochemical Society. - 2005. - Vol. 152. - № 7. -
P. A1366-1372.
23.
Андреев, В.Н. Синтез и свойства композитных плёнок полианилин-Нафион,
сформированных на стеклоуглеродной подложке // Электрохимия. - 2001. - Т. 37. -
№ 6. - С. 718-721.
24.
Lai, E.K.W. Electrochemical oxygen reduction at composite films of Nafion,
polyaniline and Pt / E.K.W. Lai, P.D. Beattie, F.P. Orfino, E. Simon, S.
Holdcroft Electrochimica Acta. - 1999. - Vol. 44. - P. 2559-2569.
25.
Costamagna, P. Percolative model of proton conductivity of Nafion membranes P.
Costamagna, S. Grosso, R.D. Felice // Journal of Power Sources. - 2008. - V.
178. - P. 537-546.
26.Заболоцкий,
В.И. Перенос ионов в мембранах / В.И. Заболоцкий, В.В. Никоненко. - М.: Наука,
1996. - 392 с.
27.
Вольфкович, Ю.М. Исследование пористой структуры, гидрофильно-гидрофобных и
сорбционных свойств волокнистых ионообменных мембран "Поликон" и их
влияния на ионную селективность / Ю.М. Вольфкович, Н.А. Кононенко, М.А.
Черняева, М.М. Кардаш, А.И. Шкабара, А.В. Павлов // Серия. Критические
технологии. Мембраны.- 2008.- №3.- С. 35-40.
.
Заболоцкий, В.И. Перенос ионов в мембранах / В.И. Заболоцкий, В.В. Никоненко -
М.: Наука. 1996.− 392 с.
.
Колзунова, Л.Г. Определение характеристик пористой структуры электрохимически
синтезированных ультрафильтрационных мембран по их электросопротивлению / Л.Г.
Колзунова, В.П. Гребень, А.П. Супонина // Электрохимия.- 2003.- Т. 39, №12.- С.
1452-1461.
.
Святченко, В.В. Методика определения пористой структуры ультрафильтрационных
мембран / В.В. Святченко, А.В. Бильдюкевич // Журнал прикладной химии.−
1991.− № 1.− С. 103-106.
.
Ярославцев, А.Б. Композиционные материалы с ионной проводимостью - от неорганических
композитов до гибридных мембран / А.Б. Ярославцев // Успехи химии.- 2009.- Т.
78, №11.- С. 1094-1112.
.
Мулдер, М. Введение в мембранную технологию. - М: Мир, 1999. - 513 с.
.
Пат. 2229325 РФ, МКИ5, B
01 D 15/08.
Электродиализный генератор элюента для ионной хроматографии / В.С. Гурский,
И.А. Шаталов, А.А. Приданцев; ЗАО «Научно-Производственная Коммерческая Фирма
Аквилон». − № 2003132803/28.
34. Пат.
2229326 РФ, МКИ5, B 01 D
15/08. Электродиализный подаватель для ионной хроматографии / В.С. Гурский,
И.А. Шаталов, А.А. Приданцев; ЗАО «Научно-Производственная Коммерческая Фирма
Аквилон». − № 2003132804/28.
. ГОСТ
17553-72. Мембраны ионообменные. Методы подготовки к испытанию. -Введ.
16.02.72. - М.: Изд-во стандартов, 1972. - 3 с.
36. Салдадзе,
К.М. Ионообменные высокомолекулярные соединения / К.М. Салдадзе, А.Б. Пашков,
В.С. Титов. - М.: Госхимиздат, 1960. - 356 с.
37. Березина,
Н.П. Полианилин в структуре нанокомпозитных мембранных материалов / Н.П.
Березина // Всероссийская конференция с международным участием «Ионный перенос
в органических и неорганических мембранах». Туапсе. - 2008. - С. 35-38.
38. Berezina
N., Falina I., Sytcheva A., Shkirskaya S., Timofeyev S. New generation of
nanocomposite materials based on perfluorinated membranes and polyaniline:
Intercalation phenomena, morphology and transport properties // Desalination
and Water Treatment. 2010. V. 14. P.
246-251.
39.Ogumi,
Z. Diffusion of aniline through perfluorosulfonate ion exchange membrane / Z.
Ogumi, K. Toyama, Z.-I. Takehara, K. Katakura, S. Inuta // Journal of Membrane
Science. - 1992. - V. 65, № 3. - P. 205-212.
40.
Протасов, К.В. Применение композитных сульфокатионитовых мембран,
модифицированных полианилином для электродиализного концентрирования солевых
растворов К.В. Протасов, С.А. Шкирская, Н.П. Березина, В.И. Заболоцкий
Электрохимия. - 2010. - Т. 46, № 10 - С. 1209-121.
41.
Munar, A. Performance
of Hydrogen
Fuel Cell
MEAs Based
on Perfluorinated
Nanocomposite
Membranes
Modified
by Polyaniline
/ A. Munar, K. Suarez, O. Solorza, N.P. Berezina, V. Compañ
// Journal of
Electrochemical
Society. - 2010. - V.
4, №1. - P. B1186-B1194.
42.
Фалина И. В. Электропроводящие и диффузионные свойства перфторированных
сульфокатионитовых мембран в процессе их модифицирования полианилином. Дис. …
канд. хим. наук. - Краснодар, 2012. - 147с.
.
Черняева М. А. Структура транспортных каналов и электрохимические свойства
модифицированных ионообменных мембран. Дис. … канд. хим. наук. - Краснодар,
2010. - 156с.
.
Шкирская, С.А. Электрокинетические свойства и морфология нанокомпозитных
материалов на основе сульфокатионитовых мембран и полианилина: Дисс. … канд.
хим. наук. - Краснодар, 2008. - 141 с.