|
Температура,
ºС
|
101
|
208
|
309
|
400
|
505
|
600
|
800
|
|
Содержание COCl2
, %
|
99.55
|
97.17
|
94.39
|
78.64
|
32.81
|
9.00
|
Зависимость константы равновесия Кр от
температуры имеет вид:
lg Кр=5020/Т - 1.75 lgТ - 1.158
где Т - температура, град. К;
. Установка синтеза фосгена в лабораторных
условиях
Центральной частью установки получения фосгена
является реактор, изображенный на рис.1. Он представляет собой кварцевую трубку
с двумя отводами и карманом для термопары. На внешней поверхности трубки
расположена нагревательная спираль, закрытая асбестовой изоляцией.
Реактор имеет следующие основные размеры:
внутренний диаметр D -13 мм;
наружный диаметр кармана термопары d - 8 мм;
высота слоя катализатора L - 110 мм.
Кроме реактора в установку синтеза фосгена (рис.
2)
входят:
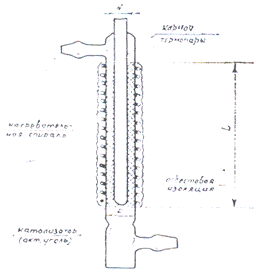
Рисунок 1. Реактор синтеза дихлорангидрида
угольной кислоты Кроме того в установку синтеза фосгена (рис. 2) входят:
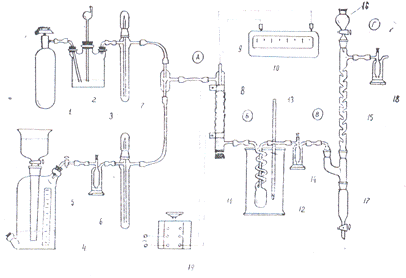
Рисунок 2. Установка синтеза дихлорангидрида
угольной кислоты
система подачи хлора, состоящая из хлорного
баллона 1, предохранительной склянки 2 и реометра 3;
система подачи окиси углерода, состоящая из
газометра 4, склянки Алифанова с Н2 SO4 5 и
реометра 6;
смеситель 7;
реактор 8
термопара 9 с милливольтметром 10;
система конденсации фосгена, включающая в себя
конденсатор 11, охлаждающую баню 12, термометр 13, контрольную склянку с Н2
SO4 13;
щелочная абсорбционная колонка 15 с капельной
воронкой 16, приемником 17 и контрольной склянкой 18.
. Теоретическая часть
Материальный баланс
Материальной баланс - вещественное выражение
закона сохранения массы вещества, согласно которому по всякой замкнутой системе
масса веществ, вступивших во взаимодействие, равна массе веществ образовавшихся
в результате взаимодействии. Применительно к материальному балансу любого
технологического процесса это означает, что масса веществ, поступивших на
технологическую операцию - приход, равна массе полученных веществ - расходу.
Материальный баланс составляют по уравнению основной суммарной реакции с учетом
параллельных и побочных реакций.
Материальный баланс непрерывно действующих
проточных реакторов составляется, как правило, для установившегося
(стационарного) режима при котором общая масса веществ, поступивших в аппарат
за данный период времени, равна массе веществ вышедших из аппарата. Количество
же всех веществ в аппарате постоянно, т. е. накопления или убыли суммарного
количества веществ не происходит.
Равновесие в технологических процессах
Химические процессы делятся на обратимые и
необратимые. Необратимые реакции протекают только в одном направлении.
Химические реакции, обычно, обратимы в том отношении, что в зависимости от
условий могут протекать как в прямом, так и в обратном направлении. Но в
обычных производственных условиях многие реакции практически не обратимы. В
гетерогенных системах обратимыми называют такие процессы, в которых возможен
переход вещества или теплоты как из одной фазы во вторую, так и обратно.
Все обратимые химико-технологические процессы
стремятся к равновесию, при котором скорости прямого и обратного процессов
уравниваются, в результате чего соотношение компонентов во взаимодействующей
системе остается неизменным, пока не изменятся внешние условия. При изменении
температуры, давления или концентрации одного из компонентов равновесие
нарушается, и в системе самопроизвольно происходят химические процессы, ведущие
к восстановлению равновесия уже в новых условиях.
Влияние основных параметров технологического
режима на равновесие в гомогенных и гетерогенных системах определяется
принципом Ле Шателье, согласно которому в системе, выведенной из состояния
равновесия, происходят изменения, направленные на компенсацию воздействий,
выводящих систему из равновесия.
Рассмотрим замкнутую систему:
аА + bB = cC
Скорость прямой реакции:
 (6)
(6)
Cкорость обратной реакции:
 (7)
(7)
где к1 и к2 - константы скорости прямой и
обратной реакции, А, В, С - молярные концентрации реагирующих компонентов в
заданный момент.
Константа равновесия вычисляется как отношение
константы скорости прямой реакции к обратной в состоянии равновесии, то есть
когда U1 = U2:

 (8)
(8)
Химические реакторы
Одним из основных элементов любой
химико-технологической системы (ХТС) является химический реактор. Химический
реактор это аппарат, в котором осуществляется химические процессы, сочетающие
химические реакции с массо- и теплопереносом. Типичными реакторами являются
промышленные печи, контактные аппараты, реакторы с механическим, пневматическим
и струйным перемешивающим устройством, варочные котлы и т. п.
Все аппараты, расположенные до реактора
предназначены для подготовки сырья к химической переработке, а все то, что
находиться после реактора, необходимо для разделения получающихся в реакторе
продуктов. От верности выбора типа реактора и его внутренних устройств напрямую
зависит эффективность всего технологического процесса.
Требования к промышленным реакторам
Основными требованиями к реакторам в
промышленности являются:
1. Максимальные коэффициент полезного действия
(КПД) и интенсивность работы.
2. Высокий выход целевого продукта и
наибольшая селективность процесса (это обеспечивается оптимальным режимом
работы реактора, т.е. необходимо поддерживать заданную температуру, давление,
концентрацию загружаемых веществ и продуктов реакции.)
. Минимальные энергетические затраты на
перемешивание, рациональное использование теплоты экзотермических реакций или
теплоты подводимой к реактору для поддержания оптимальной температуры
реагирующих веществ.
. Безопасность работы и управляемость.
Эти условия обеспечиваются рациональным подходом к выбору конструкции реактора
с малыми колебаниями параметров технологического режима, позволяющими
автоматизировать работу реактора
. Низкие экономические затраты на
изготовление самого реактора, его ремонта и технического обслуживания. Эти
условия достигаются простотой конструкций, применением дешевых сталей и
конструкционных материалов.
. Устойчивость реактора при значительных
изменениях основных параметров технологического процесса - температуры,
давления, концентрация и т.д., устойчивость оболочки реактора к аварийным
ситуациям.
Классификация реакторов
· По временному фактору:
- проточные
периодического действия
· По гидродинамическому фактору:
- смешения (с использованием перемешивающего
устройства)
вытеснения (вытеснение слоя частиц впереди
идущим слоем, т.е. нет продольного смешения частиц)
· По температурному фактору:
- изотермические реакторы ( Т - const)
адиабатические (без теплообмена с окружающей
средой)
политермические( с высокой разностью температур)
Типы идеальных реакторов
Непосредственно на режим работы реактора влияет
степень перемешивания реагирующих веществ. В частности, постоянство параметров
во всем объеме ректора обеспечивается полным смешением, а при полном вытеснении
параметры, как правило, изменяются по высоте реакционного объема. В результате,
в реакторах вытеснения меняется константа скорости реакции, а следовательно и
скорости процесса. При сравнении моделей идеальных реакторов вытеснения и
смешения условно принято постоянство температуры и соответственно константы
скорости реакции для всех типов реакторов.
· Реактор полного смешения, проточный
(РПС)
Проточный реактор представляет собой аппарат, в
котором интенсивно перемешиваются реагенты при помощи перемешивающего
устройства (мешалки). В него непрерывно подаются реагенты и непрерывно
выводятся продукты реакции. Поступающие в такой раствор частицы вещества
мгновенно перемешиваются с находящимися там частицами, то есть равномерно
распределяются по всему объему аппарата Таким образом, во всех точках
реакционного объема мгновенно выравнивается концентрациями все остальные
параметры характеризующие процесс - температура, степени превращения и другие.
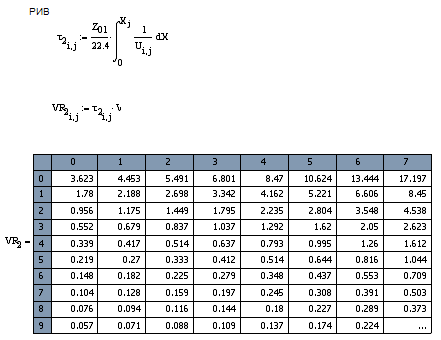
· Реактор идеального вытеснения (РИВ)
В таком реакторе, все частицы движутся
равномерно и в заданном направлении, при этом не перемешиваясь с движущимися
впереди и сзади и полностью вытесняя находящиеся впереди частицы потока
(поршневое движение потока). Время Пребывания всех частиц в аппарате одинаково.
· Реактор периодического действия
(РПД)
Реакторы периодического действия работаю при нестационарном
технологическом режиме. То есть в процессе протекания реакции (независимо от
степени перемешивания ) изменяются не только концентрации реагентов, но и
температура, давление и следовательно и константа скорости реакции. Если
периодический реактор работает в режиме полного смешения, то время для
достижения необходимое для достижения заданной степени превращения
рассчитывается по характеристическому уравнению, которое совпадает с
характеристическим уравнением реактора идеального вытеснения. Таким образом,
если были бы возможны одинаковые условия проведения процесса в реакторах
периодического действия и идеального вытеснения, то их объемы были бы равны
между собой. Но, условия протекания процессов в промышленных проточных
реакторах, как правило, лучше, чем в периодических.
· Каскад реакторов полного смешения
В единичном реакторе полного смешения из-за
того, что концентрации реагентов мгновенно снижаются до конечной величины,
скорость реакции при больших степенях превращения невелика и поэтому для получения
высоких степеней превращения требуются реакторы большого объема. В связи с этим
рациональнее использовать ряд последовательно соединенных реакторов полного
смешения - каскада реакторов. В каскаде реакторов состав реакционной смеси
изменяется при переходе из одного аппарата в другой. При этом в каждой ступени
каскада, как характерно для реакторов полного смешения, параметры процесса
постоянны во всем объеме. Существует несколько методов для определения
теоретического количества ступеней, но в основном используют графический и
алгебраический методы.
Кинетика




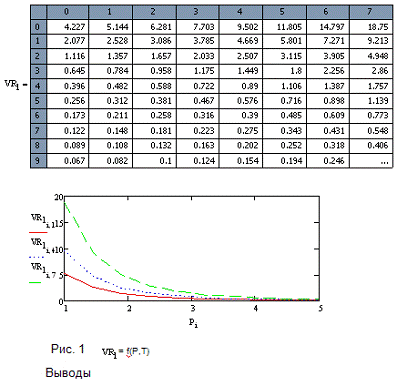
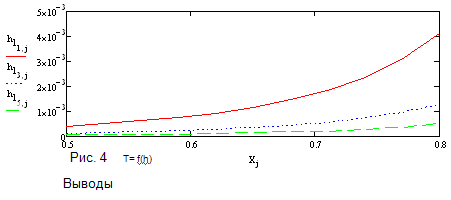
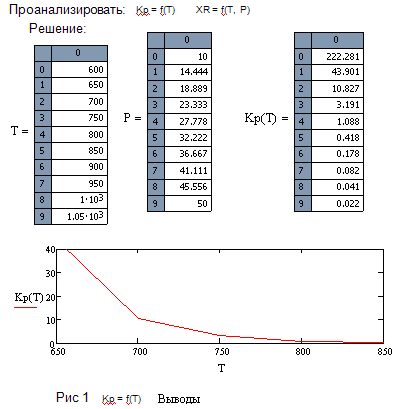
Выводы
С ростом температуры значение величины -Е1\RT
уменьшается, значит К1 - увеличивается. Кр уменьшается с ростом температуры,
тогда 1\Кр увеличивается, величина ΔС
уменьшается, т.е
.График должен иметь форму параболы, но в данном
интервале температур он возрастает
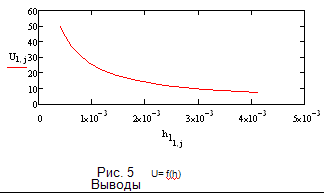
С ростом Х значения U уменьшаются, поэтому
большему значению Х соответствует меньшее значение U .
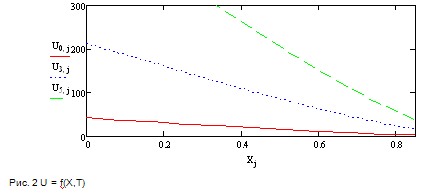
Выводы:
С ростом Х значения U уменьшаются ( функция
убывает)
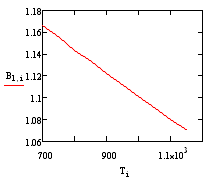
С ростом Т величина Е1\RT уменьшается, К1
увеличивается, Кр с ростом Т - уменьшается, 1\Кр - увеличивается, значит ΔС
уменьшается т.е
В данном интервале температур большему значению
Х соответствуют меньшее значение U.
Реакторы
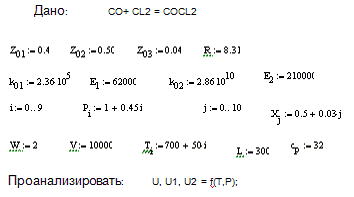
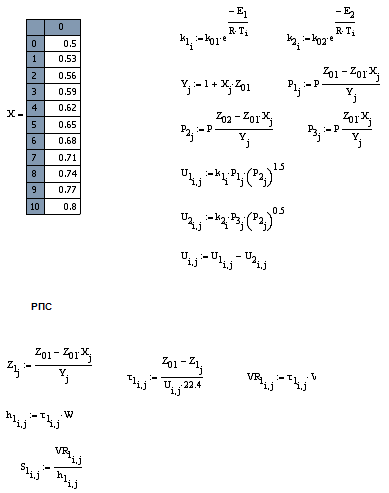
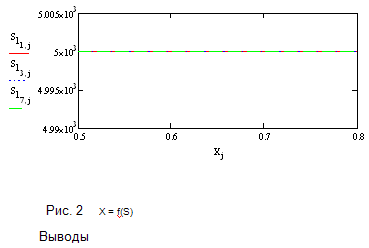

Химическое равновесие
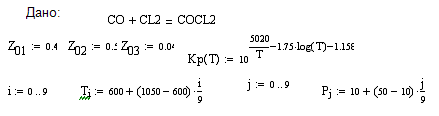
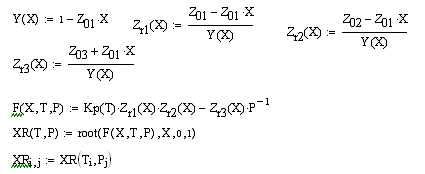


Заключение
Проведя ряд расчетов, мы делаем выбор в пользу
реактора полного смешения (РПС), так как время пребывания в нем реакционной
смеси значительно меньше, чем в реакторе идеального вытеснения, что с
экономической точки зрения гораздо выгоднее. Также чем меньше время пребывания
смеси в реакторе, тем быстрее достигается заданная степень превращения, что нам
и иллюстрирует график(с повышением х-степени превращения, растет время).
Список используемой литературы
. А. М. Кутепов, Т. И. Бондарева, М.
Г. Беренгартен "Общая химическая технология", 2003.
. И. Г. Масленников
"Дихлорангидрид угольной кислоты", Метод. указания, СПб., СПбГТИ(ТУ),
2002.
. Краткий справочник
физико-химических величин.,1983.