D-элементы и их соединения
d-ЭЛЕМЕНТЫ И ИХ
СОЕДИНЕНИЯ
1. Общая характеристика d-элементов
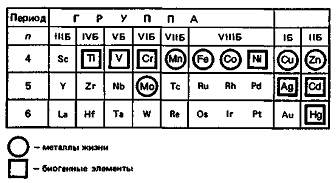
К d-блоку
относятся 32 элемента периодической системы. d-Элементы
входят в 4-7-й большие периоды. У атомов IIIБ-группы
появляется первый электрон на d-орбитали.
В последующих Б-группах происходит заполнение d-подуровня
до 10 электронов (отсюда название d-элементы).
Строение внешних электронных оболочек атомов d-блока
описывается общей формулой (n-1)dansb,
где а = 1-10, b = 1-2.
Особенностью элементов этих
периодов является непропорционально медленное возрастание атомного радиуса с
возрастанием числа электронов. Такое относительно медленное изменение радиусов
объясняется так называемым лантаноидным сжатием вследствие проникновения ns-электронов
под d-электронный слой.
В результате наблюдается незначительное изменение атомных и химических свойств d-элементов
с увеличением атомного номера. Сходство химических свойств проявляется в
характерной особенности d-элементов
образовывать комплексные соединения с разнообразными лигандами.

Важным свойством d-элементов
является переменная валентность и, соответственно, разнообразие степеней
окисления. Эта особенность связана главным образом с незавершенностью
предвнешнего d-электронного слоя
(кроме элементов IБ- и IIБ-групп).
Возможность существования d-элементов
в разных степенях окисления определяет широкий диапазон
окислительно-восстановительных свойств элементов. В низших степенях окисления d-элементы
проявляют свойства металлов. С увеличением атомного номера в группах Б
металлические свойства закономерно уменьшаются.

В растворах кислородсодержащие анионы d-элементов
с высшей степенью окисления проявляют кислотные и окислительные свойства.
Катионные формы низших степеней окисления характеризуются основными и
восстановительными свойствами.
d-элементы
в промежуточной степени окисления проявляют амфотерные свойства. Эти
закономерности можно рассмотреть на примере соединений молибдена:
С изменением свойств меняется
окраска комплексов молибдена в различных степенях окисления (VI
- II):

В периоде с увеличением заряда
ядра наблюдается уменьшение устойчивости соединений элементов в высших степенях
окисления. Параллельно возрастают окислительно-восстановительные потенциалы
этих соединений. Наибольшая окислительная способность наблюдается у
феррат-ионов и перманганат-ионов. Следует отметить, что у d-элементов
при нарастании относительной электроотрицательности усиливаются кислотные и
неметаллические свойства.
С увеличением устойчивости
соединений при движении сверху вниз в Б-группах одновременно уменьшаются их
окислительные свойства.
Можно предположить, что в ходе
биологической эволюции отбирались соединения элементов в промежуточных степенях
окисления, которые характеризуются мягкими окислительно-восстановительными
свойствами. Преимущества такого отбора очевидны: они способствуют плавному
протеканию биохимических реакций. Уменьшение ОВ потенциала создает предпосылки
для более тонкой «регулировки» биологических процессов, что обеспечивает
выигрыш энергии. Функционирование организма становится менее энергоемким, а
значит более экономичным по потреблению пищевых продуктов.
С точки зрения эволюции для
организма становится оправданным существование d-элементов
в низших степенях окисления. Известно, что ионы Мn2+,
Fе2+ , Со2+
при физиологических условиях не являются сильными восстановителями, а ионы Сu2+
и Fе2+
практически не проявляют в организме восстановительных свойств. Дополнительное
снижение реакционной способности происходит при взаимодействии этих ионов с
биоорганическими лигандами.
Может показаться, что
вышесказанному противоречит важная роль биоорганических комплексов молибдена(V)
и (VI) в различных
организмах. Однако и это согласуется с общей закономерностью. Несмотря на
высшую степень окисления такие соединения проявляют слабые окислительные
свойства.
Необходимо отметить высокие
комплексообразующие способности d-элементов,
которые обычно значительно выше, чем у s-
и p-элементов. Это
прежде всего объясняется возможностями d-элементов
быть как донорами, так и акцепторами пары электронов, образующих
координационное соединение.
В случае гидроксокомплекса
хрома [Сr(ОН)6]3-
ион металла является акцептором пары электронов. Гибридизация 3d24sp3-орбиталей
хрома обеспечивает более устойчивое энергетическое состояние, чем при
расположении электронов хрома на орбиталях гидроксогрупп.
Соединение [СrСl4]2-
образуется, наоборот, в результате того, что неподеленные d-электроны
металла занимают свободные d-орбитали
лигандов, поскольку в данном случае энергия этих орбиталей ниже.
Свойства катиона Сr3+
показывают непостоянство координационных чисел d-элементов.
Чаще всего, это четные числа от 4 до 8, реже встречаются числа 10 и 12.
Необходимо отметить, что существуют не только одноядерные комплексы. Известны
многочисленные ди-, три- и тетра-ядерные координационные соединения d-элементов.
Примером может служить
биядерный комплекс кобальта [Со2(NН3)10(О2)](NО3)5,
который может служить моделью переносчика кислорода.
Более 1/3 всех микроэлементов
организма составляют d-элементы.
В организмах они существуют в виде комплексных соединений или гидратированных
ионов со среднем временем обмена гидратной оболочки от 10-1 до 10-10
с. Поэтому можно утверждать, что «свободные» ионы металлов в организме не
существуют: это либо их гидраты, либо продукты гидролиза.
В биохимических реакциях d-элементы
наиболее часто проявляют себя как металлы-комплексообразователи. Лигандами при
этом выступают биологически активные вещества, как правило, органического
характера или анионы неорганических кислот.

Белковые молекулы образуют с d-элементами
бионеорганические комплексы - кластеры или биокластеры. Ион металла
(металл-комплексо-образователь) располагается внутри полости кластера,
взаимодействуя с электроотрицательными атомами связывающих групп белка:
гидроксильных (-ОН), сульфгидрильных (-SН),
карбоксильных (-СООН) и аминогрупп белков (Н2N-).
Для проникновения иона металла в полость кластера необходимо, чтобы диаметр
иона был соизмерим с размером полости. Таким образом, природа регулирует
формирование биокластеров с ионами d-элементов
определенных размеров.
Наиболее известные
металлоферменты: карбоангидраза, ксантиноксидаза, сукцинатдегидрогеназа,
цитохромы, рубредоксин. Они представляют собой биокластеры, полости которых
образуют центры связывания субстратов с ионами металла.
Биокластеры (белковые
комплексы) выполняют различные функции.
Транспортные белковые комплексы
доставляют к органам кислород и необходимые элементы. Координация металла идет
через кислород карбоксильных групп и азот аминогрупп белка. При этом образуется
устойчивое хелатное соединение.
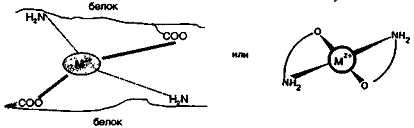
В качестве координирующего металла выступают d-элементы
(кобальт, никель, железо). Пример железосодержащего транспортного белкового
комплекса - трансферрин.
Другие биокластеры могут
выполнять аккумуляторную (накопительную) роль - это железосодержащие белки:
гемоглобин, миоглобин, ферритин. Они будут рассмотрены при описании свойства
группы VIIIБ.
Элементы Zn,
Fе, Со, Мо, Сu
- жизненно необходимы, входят в состав металлоферментов. Они катализируют
реакции, которые можно разделить на три группы:
1.
Кислотно-основные
взаимодействия. Участвует ион цинка, входящий в состав фермента карбоангидразы,
катализирующего обратимую гидратацию СО2 в биосистемах.
2.
Окислительно-восстановительные
взаимодействия. Участвуют ионы Fе,
Со, Сr, Мо. Железо входит
в состав цито-хрома, в ходе процесса происходит перенос электрона:
Fе3+
→ Fе2+
+ е-
3. Перенос кислорода.
Участвуют Fе, Сu.
Железо входит в состав гемоглобина, медь - в состав гемоцианина.
Предполагается, что эти элементы связываются с кислородом, но не окисляются им.
Соединения d-элементов
избирательно поглощают свет с разными длинами волн. Это приводит к появлению
окраски. Квантовая теория объясняет избирательность поглощения расщеплением d-подуровней
ионов металлов под действием поля лигандов.
Хорошо известны следующие
цветные реакции на d-элементы:
Мn2+
+ S2-
= МnS↓ (осадок
телесного цвета)
Нg2+
+ 2I-
= НgI2
↓(желтый или красный осадок)
К2Сr2О7
+ Н2SО4
(конц.) = К2SО4
+ Н2О + 2СrО3↓
(кристаллы оранжевого цвета)
Приведенные выше реакции
используются в аналитической химии для качественного определения
соответствующих ионов. Уравнение реакции с дихроматом показывает, что
происходит при приготовлении «хромовой смеси» для мытья химической посуды. Эта
смесь необходима для удаления как неорганических, так и органических отложений
с поверхности химических склянок. Например, жировых загрязнений, которые всегда
остаются на стекле после прикосновения пальцев.
Необходимо обратить внимание на
то, что d-элементы в
организме обеспечивают запуск большинства биохимических процессов,
обеспечивающих нормальную жизнедеятельность.
. Общая характеристика d-элементов
VIБ-группы
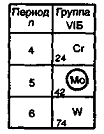
VIБ-группу
составляют элементы (переходные металлы) - хром, молибден и вольфрам. Эти
редкие металлы находятся в природе в небольшом количестве. Однако благодаря
целому ряду полезных химических и физических свойств, широко применяются не
только в машиностроении и химической технологии, но и в медицинской практике
(сплав Сr-Со-Мо используется
в хирургии и стоматологии, молибден и его сплавы применяются как детали
рентгеновских трубок, из вольфрама изготовляют аноды рентгеновских трубок,
сплавы вольфрама - основа экранов для зашиты от γ-лучей).
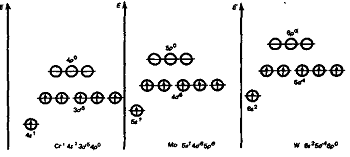
Конфигурация валентных
электронов Сг и Мо - (n-1)d5ns1,
W - 5d46s2.
Сумма валентных электронов хрома, молибдена, вольфрама равна 6, что и
определяет их положение в VIБ-группе.
У Сr и Мо последний
электронный слой занимают 13 электронов, у W
- 12. Как у большинства d-элементов
этот слой неустойчив. Поэтому валентность хрома, молибдена и вольфрама
непостоянна. По этой же причине соединения металлов группы VIБ
характеризуются набором степеней окисления от +2 до +6.
В группе d-элементов
проявляется общая тенденция: с увеличением порядкового номера увеличивается
устойчивость соединений с высшей степенью окисления. Самым сильным окислителем
в состоянии Э6+ является хром. «Пограничный» Мо6+ проявляет
слабые окислительные свойства. Молибде-нат-ион МоО42-
восстанавливается лишь до Мо6О17 («молибденовая синь»),
где часть атомов молибдена имеет степень окисления +5. Эта реакция используется
в аналитической химии для фотометрических определений.
В низших валентных состояниях,
следуя все той же тенденции, более сильные восстановительные свойства проявляет
Сг2+. У ионов Мо2+ и W2+
увеличение энергии ионизации приводит к уменьшению восстановительных и
металлических свойств.
Комплексные соединения данной
группы элементов чаще всего имеют координационное число 6 и гибридизацию типа sр3d2,
которая в пространстве описывается октаэдром.
Характерной особенностью
соединений этой группы является склонность к полимеризации (конденсации)
кислородных форм элементов VI
группы. Это свойство усиливается при движении по группе сверху вниз. При этом
образуются соединения типа М6О2412-,
составленные из октаэдров МоO4
и WO4.
Эти октаэдры образуют полимерные кристаллы. У оксида хрома (VI)
способность к полимеризации проявляется, но слабо. Поэтому у оксидов молибдена
и вольфрама степень полимеризации выше.
По строению электронной
оболочки атомов с незаполненной d-орбиталью,
совокупности физических и химических свойств, по склонности к образованию
электроположительных ионов и координационных соединений элементы VI
группы относятся к переходным металлам.
Химические свойства соединений
хрома. Большинство соединений хрома имеет яркую окраску самых разных цветов.
Название происходит от греч. хромоc
- цвет, окраска.
Соединения трехвалентного хрома
(в отличие от соединений молибдена, а для вольфрама степень окисления +3 вообще
не характерна) химически инертны.
В природе хром находится в
трехвалентном (шпинель - двойной оксид МnСrO4
- магнохромит) и шестивалентном состоянии (РbСrO4
- крокоит). Образует оксиды основного, амфотерного и кислотного характера.
Оксид хрома (II)
СrО - кристаллы
красного (красно-коричневого) цвета или черный пирофорный порошок,
нерастворимый в воде. Соответствует гидроксиду Сr(ОН)2.
Гидроксид желтого (влажный) или коричневого цвета. При прокаливании на воздухе
превращается в Сr2О3
(зеленого цвета):
Сr(ОН)2
+ 0,5О2 = Сr2O3
+ 2Н2О
Катион Сr2+
- бесцветен, его безводные соли белого, а водные - синего цвета. Соли
двухвалентного хрома являются энергичными восстановителями. Водный раствор
хлорида хрома (II)
используется в газовом анализе для количественного поглощения кислорода:
2СrСl2
+ 2НgО + 3Н2O
+ 0,5О2 = 2НgСl2
+ 2Сr(ОН)3↓
(грязно-зеленый осадок)
Гидроксид хрома (III)
обладает амфотерными свойствами. Легко переходит в коллоидное состояние.
Растворяясь в кислотах и щелочах, образует аква- или гидроксокомплексы:
Сr(ОН)3
+ 3Н3О+ = [Сr(Н2О)6]3+
(сине-фиолетовый раствор)
Сr(ОН)3
+ 3ОН- = [Сr(ОН)6]3-
(изумрудно-зеленый раствор)
Соединения трехвалентного
хрома, как и двухвалентного, проявляют восстановительные свойства:
Сr2(SO4)з+КСlО3
+ 10КОН = 2К2СrO4
+
3К2SО4 + КСl
+ 5Н2О
Соединения хрома (VI),
как правило, кислородсодержащие комплексы хрома. Оксид шестивалентного хрома
соответствует хромовым кислотам.
Хромовые кислоты образуются при
растворении в воде СrО3.
Это сильно токсичные растворы желтого, оранжевого и красного цвета, обладающие
окислительными свойствами. СrО3
образует полихромовые кислоты состава Н2СrnО(3n+1):
nCrО3 + Н2О
→ Н2СrnО(3n+1).
Таких соединений может быть несколько: Н2СrО4,
Н2Сr2О7,
Н2Сr3О10,
Н2Сr4О13.
Цвета растворов меняются от желтого до красного. Окраска зависит от содержания
СrО3 в
растворе, концентрация СrО3
влияет на образование полихромовых кислот разной степени полимеризации (от
моно- до полихромовой кислоты).
Государственная фармакопея рекомендует
для определения подлинности раствора пероксида водорода использовать реакцию
К2Сr2О7
+ 4Н2О2 + Н2SО4
= К2SО4
+ 2Н2СrО6
+ 3Н2О
При этом образуется
дипероксохромовая (Н2СrО6)
или пероксохромовая (НСrО5)
кислота - соединение синего цвета. Синяя окраска и подтверждает подлинность
препарата Н2О2.
Хроматометрию применяют также в
санитарно-гигиенической практике для анализа промышленных и сточных вод. В ходе
анализа определяется «окисляемость воды», которая показывает общее содержание
соединений восстановительного характера.
СrО3
обладает прижигающим действием. Это свойство используется в медицине. Тем не
менее, необходимо помнить, что соли хрома (III)
и хрома(VI) токсичны
для человека. Смертельная доза К2Сг2О7
для взрослого человека составляет всего 0,3 г.
3. Биологическая роль d-элементов
VIБ-группы
Их применение в медицине.
Хром Сг, молибден Мо, вольфрам W
- микроэлементы живых организмов.
Хром обнаруживается в
растительных и животных организмах. В организме взрослого человека содержится
примерно 6 г Сr (0,1%).
Металлический хром нетоксичен,
а соединения Сr(III)
и Сr(VI)
опасны для здоровья. Они вызывают раздражение кожи, что приводит к дерматитам.
Есть предположение, что
производные хрома (VI)
обладают канцерогенными свойствами. 0,25-0,3 г дихромата калия вызывают
летальный исход. Соединения хрома (VI)
применяются как фунгициды (протравливающие вещества, фунгис - гриб, цедере -
убивать). Соединения хрома (III)
благоприятно влияют на рост растений.
Нельзя пройти мимо аномальных
свойств металлического хрома. При 37°С у него резко меняется модуль упругости,
коэффициент линейного расширения, внутреннее трение, электросопротивление.
Такое поведение ждет своего объяснения и, возможно, найдет применение в
медицине.
Молибден - относится к металлам жизни, является
одним из важнейших биоэлементов. Его особенное положение было отмечено 20-25
лет назад Ф. Крином и Л. Орилом. Эти ученые выдвинули идею, что возникновение
жизни на Земле происходило не эволюционным путем, а она занесена неведомой
цивилизацией из космоса с молибденовых звезд, где жизнь существовала задолго до
нас.
В биохимических процессах
молибден участвует в степенях окисления V
и VI. В этом состоянии
он создает устойчивые оксоформы.
Молибден образует устойчивые
оксокомплексы (например, [МоО3(ОН)2] и, видимо, поэтому
входит в состав ферментов, обеспечивающих перенос оксогрупп. В крови
преобладает Мо(VI),
если лигандом будет кислород, то образуются устойчивые изополимолибдат-ионы:
МоО42-
МоО72- Мо7О246- Мо12O4110-
Избыточное содержание молибдена
в пище нарушает метаболизм Са2+ и РО43- ,
вызывая снижение прочности костей - остеопорозы.
Возможно, происходит связывание
МоО42- и РО43- в
фосфорномолибденовые комплексы состава [РМо12О40]3-,
[РМо11О39]7-, [Р2Мо17О61]10-.
Такие комплексы можно рассматривать как кислотные остатки
гетерополимолибденовых кислот. С кальцием эти остатки дают нерастворимые
кристаллики. Не исключено, что эти кристаллики инициируют отложение солей
мочевой кислоты и вызывают заболевание подагрой. Подагра деформирует суставы,
оправдывая свой буквальный перевод, как «капкан для ног».
Кроме кислородных комплексов,
молибден образует галогенидные (Наl-),
тиоцианатные (NCS-)
и цианидные (СN-)
комплексы.
Молибден входит в состав
различных ферментов. В организме человека к ним относятся альдегидогидроксидазы,
ксантиндегидрогеназы, ксантиноксидазы.
Молекулярная масса
ксантиноксидазы (КОКС) 250 000. Это молибденсодержащий фермент млекопитающих.
Он может катализировать окисление ксантина и других пуринов, а также
альдегидов. В ходе ферментативной реакции молибден (VI)
переходит в молибден (V),
а потом в молибден (IV).
В общем виде это будет так:

Превращение гипоксантина и ксантина в мочевую
кислоту, катализируемое ксантиноксидазой, происходит по схеме

Предполагается, что в ходе
каталитического процесса молибден образует связь с азотом и кислородом
ксантина.
Молибден является важнейшим
микроэлементом растений, так как биологически активные вещества с его участием
обеспечивают мягкую фиксацию азота: превращают в аммиак или азотсодержащие
продукты.
По сравнению с другими
промышленно важными металлами молибден малотоксичен.
Потребление молибдена с
продуктами питания 0,1-0,3 мг/сут, но необходимое дневное поступление не
установлено. Дефицит молибдена вызывает уменьшение активности ксантиноксидазы в
тканях. Избыточное содержание молибдена вызывает остеопорозы.
Вольфрам - микроэлемент. Его
роль в организме изучена недостаточно. Анионная форма вольфрама легко
абсорбируется в желудочно-кишечном тракте. Металлический вольфрам и его
катионные формы не абсорбируются в организме. О гомеостазе вольфрама у
млекопитающих сведений нет.
4. Общая характеристика d-элементов
VIIБ-группы
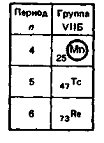
Марганец Мn,
технеций Тс и рений Rе -
элементы-аналоги, образующие группу VIIБ.
Из элементов этой группы
наиболее распространен в природе марганец. Технеций - радиоактивный элемент, в
природе практически не встречается, получен искусственным путем. Рений в земной
коре содержится в незначительном количестве. Он относится к редким и рассеянным
элементам.
Валентные электроны элементов VIIБ-группы
[конфигурация (n-1)d5ns2]
располагаются на энергетических уровнях следующим образом:
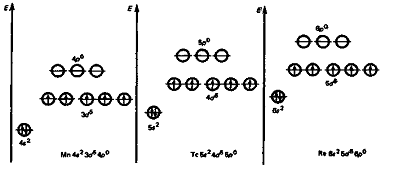
Для марганца характерны степени окисления +2,
+3, +4, -1-6, +7. Для остальных элементов этой группы известны только степени
окисления +4 и +7.
Подобно другим d-элементам,
соединения VIIБ-группы в
низших степенях окисления проявляют восстановительные свойства, об основных
свойствах этих соединений целесообразно говорить только применительно к
соединениям марганца, который в растворах существует в виде катионов Мn2+
и Мn3+.
В высших степенях окисления
элементы VIIБ-группы
существуют в анионной форме (МnО4-,
ТеО4-, RеО4-),
проявляя окислительные и кислотные свойства. Для RеO2
преобладают кислотные свойства.

В промежуточной степени
окисления (IV) явно
выраженная амфотерность проявляется у марганца. Это может быть объяснено
уменьшением устойчивости элементов с увеличением порядкового номера, что
приводит к ослаблению дифференциации кислотно-основных признаков в
промежуточных степенях окисления. Поэтому именно у соединений марганца
отчетливо прослеживается отмечаемая закономерность изменения кислотно-основных
и окислительно-восстановительных свойств.
Реакционная способность
элементных веществ VIIБ-группы
уменьшается в ряду Мn-Тс-Rе.
Без нагревания порошки Мn,
Тс и Rе окисляются во
влажном воздухе, превращаясь в МnО,
ТеО, НRеО4. При
нагревании эти металлы реагируют с О2, F2,
Сl2,
S, Р, Si.
Распространенность в земной
коре: Мn - 0,09%; Тс - нет;
Rе - 10-7%.
Эти элементы относятся к
тяжелым металлам. Наиболее изучен марганец и его соединения.
При взаимодействии марганца с
разбавленными кислотами (особенно при нагревании) выделяется водород. Ион
марганца Мn2+
в воде существует как аквакомплекс. Поэтому в молекулярно-ионном виде реакция
запишется так:
Мn
+ 2Н+ + 6Н2O
→
[Мn(Н2O)6]2+
+ Н2↑
Химические свойства соединений
марганца. Устойчивые степени окисления марганца +2, +4, +7 в соединениях
кислородного и солевого характера. В медицинской практике используются
соединения марганца(II)
и марганца(VII).
Оксид марганца (II)
МnО встречается в
природе в виде мелких зеленых кристаллов, плохо растворимых в воде. При
нагревании на воздухе превращается в разные оксиды:
МnО
+ 3O2
→ 6МnО2 + 3/2
О2 → 3Мn2О3
+4,5 О2 1000°С→ 6МnО3
Оксид марганца (II)
растворяется в кислотах:
МnО
+ 2Н+ + 5Н2О → [Мn(Н2О)6]2+
Обработка аквакомплекса [Мn(Н2О)6]2+
при рН = 8,5 в атмосфере водорода приводит к образованию нерастворимого
гидроксида марганца (II):
[Мn(Н2О)6]2+
+ 2ОН- → Мn(OH)2↓
+ 6Н2О
гидроксид марганца (II)
обладает слабоосновными свойствами, окисляется кислородом воздуха и другими
окислителями до марганцеватистой кислоты или ее солей манганитов:
Мn(ОН)2
+ Н2О2 → Н2МnО3↓
+ Н2О
марганцеватистая кислота (бурый
осадок)
В щелочной среде Мn2+
окисляется до МnО42-,
а в кислой до МnО4-:
МnSО4
+ 2КNО3 +
4КОН → К2МnО4
+ 2КNО2 + К2SО4
+ 2Н2О
Образуются соли марганцовистой
Н2МnО4 и
марганцовой НМnО4
кислот.
Если в опыте in
vitro Мn2+
проявляет восстановительные свойства, то in
vivo восстановительные свойства Мn2+
слабо выражены. В биологических процессах он не меняет степени окисления.
Устойчивые биокомплексы Мn2+
in vivo
стабилизируют эту степень окисления. Стабилизирующее влияние появляется в
большом времени удержания гидратной оболочки. Для Мn2+
это время равно 100 мкс, тогда как для гидрофильного иона Na+
оно составляет 1 мкс.
Оксид марганца (IV)
МnО2
является устойчивым природным соединением марганца, которое встречается в
четырех модификациях. Все модификации имеют амфотерный характер и обладают
окислительно-восстановительной двойственностью.
Примеры
окислительно-восстановительной двойственности МnО2:
МnО2
+ 2КI + 3СО2
+ Н2О → I2
+ МnСО3 +
2КНСО3
МnО2
+ 2NH3
→ 3Мn2О3
+ N2
+ 3Н2О
МnО2
+ 3О2 + 4КОН → 4КМnО4
+ 2Н2О
МnО2
+ 3Сl2
+ 8КОН → 2КМnО4
+ 6КСl + 4Н2О
Последняя реакция ставит под
сомнение расхожее утверждение, что МnО2
в щелочной среде превращается в манганат - соль Мn
(VI), а в кислой - в
перманганат - соль Мn (VII).
Кроме среды на окислительно-восстановительную способность влияют концентрация и
потенциал окислителя.
Соединения Мn
(VI) - неустойчивы. В
растворах могут превращаться в соединения Мn
(II), Мn
(IV) и Мn
(VII): оксид марганца (VI)
МnО3 -
темно-красная масса, вызывающая кашель. Гидратная форма МnО3
- слабая марганцовистая кислота Н2МnO4,
которая существует только в водном растворе. Ее соли (манганаты) легко
разрушаются в результате гидролиза и при нагревании. При 50°С МnО3
разлагается:
МnО3
→ 2МnО2 + О2
и гидролизуется при растворении
в воде:
МnО3
+ Н2О → МnО2
+ 2НМnО4
Мn2О7
→ 2МnО2 + О3
При растворении в холодной воде
образуется кислота
Мn2O7
+ Н2О → 2НМnО4
Соли марганцевой кислоты НМnО4
- перманганаты. Ионы обусловливают фиолетовую окраску растворов. Образуют
кристаллогидраты типа ЭМnО4∙nН2О,
где n = 3-6, Э = Li,
Nа, Мg,
Са, Sr.
Перманганат КМnО4
хорошо растворим в воде. Перманганаты - сильные окислители. Это свойство
используется в медицинской практике для дезинфекции, в фармакопейном анализе
для идентификации Н2О2 путем взаимодействия с КМnО4
в кислой среде. Количественное содержание КМnО4
в препаратах Государственная фармакопея рекомендует определять
иодометрически путем проведения реакции с КI
в кислой среде.
Глубина превращения
перманганата зависит от рН среды, в которой протекает реакция. При сравнении
стандартных окислительно-восстановительных потенциалов видно, что наиболее
сильные окислительные свойства перманганат-ион проявляет в кислой среде.
Вследствие высокой
окислительной способности кислородные соединения марганца в высших степенях
окисления в организме не существуют.
Для организма перманганаты
являются ядами, их обезвреживание может происходить следующим образом:
КМnO4
+ 5Н2O2
+ 6СН3СООН = 2Мn(СН3СОО)2
+ 2СН3СООК + 8Н2О + 5O2
Для лечения острых отравлений
перманганатом используется 3%-ный водный раствор Н2O2,
подкисленный уксусной кислотой.
Калий перманганат окисляет
органические вещества клеток тканей и микробов. При этом КМnО4
восстанавливается до МnО2.
Оксид марганца (IV)
может также взаимодействовать с белками, образуя комплекс бурого цвета.
Под действием перманганата
калия КМnО4 белки
окисляются и свертываются (коагулируют). На этом основано его применение в
качестве наружного препарата, обладающего противомикробными и прижигающими
свойствами. При этом его действие проявляется только на поверхности кожи и
слизистых оболочек. Окислительные свойства водного раствора КМnО4
используют для обезвреживания токсичных органических веществ. В результате
окисления образуются менее токсичные продукты. Например, наркотик морфин превращается
в биологически малоактивный оксиморфин.
Калий перманганат применяют в
титриметрическом анализе для определения содержания различных восстановителей
(перманганатометрия).
Высокую окислительную
способность перманганата используют в экологии для оценки загрязненности
сточных вод (перманганатный метод). По количеству окисленного (обесцвеченного)
перманганата определяют содержание органических примесей в воде.
Перманганатный метод
(перманганатометрию) используют также в клинических лабораториях для определения
содержания мочевой кислоты в крови.
5. Биологическая роль
соединений марганца. Их применение в медицине
Из элементов VIIБ-группы
только марганец является биогенным элементом и одним из десяти металлов жизни,
необходимых для нормального протекания процессов в живых организмах.
В теле взрослого человека
содержится 12 мг (1,6-10-5%). Марганец концентрируется в костях
(43%), остальное - в мягких тканях, в том числе и в мозге.
В организме марганец образует
металлокомплексы с белками, нуклеиновыми кислотами, АТФ, АДФ, отдельными
аминокислотами. Содержащие марганец металлоферменты аргиназа, холинэстераза,
фосфоглюкомутаза, пируваткарбоксилаза.
Связывание аммиака - токсичного
продукта превращения аминокислот в организме млекопитающих осуществляется через
аминокислоту аргинин. Аргиназа - фермент, катализирующий в печени гидролиз
аргинина. В результате аргинин расщепляется на мочевину и циклическую
аминокислоту орнитин. Мочевина - нетоксичное, растворимое в воде вещество. Оно
потоком крови доставляется в почки и выводится с мочой.
Атомный радиус марганца 128 пм.
Это объясняет то обстоятельство, что марганец может замещать магний (атомный
радиус 160 пм) в его соединении с АТФ, существенно влияя на перенос энергии в
организме.
Особенно важной является роль
гидролиза аденозинтрифосфата (АТФ) до аденозиндифосфата (АДФ), обеспечивающего
энергетику жизнедеятельности. В организме этот процесс активируется магнием в
результате образования комплексов МgАТФ2-
и МgАДФ-.
Однако установлено, что активацию могут осуществлять и ионы марганца Мn2+.
При этом оказывается, что эти комплексы более активны. Участие марганца в
гидролизе можно представить в виде:
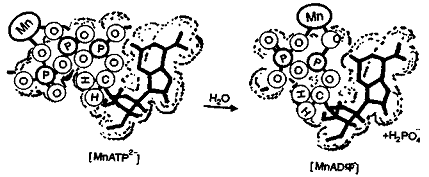
Ионы Мg2+
и марганца Мn2+
осуществляют также активацию ферментов - нуклеаз. Эти ферменты катализируют в
двенадцатиперстной кишке гидролиз нуклеиновых кислот ДНК и РНК. В результате
эти биополимеры расщепляются на мономерные единицы - нуклеотиды. В частности
такой нуклеазой является дезоксирибонуклеаза, которая катализирует гидролиз ДНК
только в присутствии ионов Мg2+
или Мn2+.
Марганец может входить и в
состав неорганических соединений организма. Это, например, малорастворимый
марганец магний пирофосфат МnМgP2О7.
Кристаллы этой соли локализуются на внутренней поверхности мембраны везикул.
Почти одинаковое значение
атомного радиуса марганца (128 пм) и железа (126 пм) объясняет способность
марганца замещать железо в порфириновом комплексе эритроцита. По той же причине
марганец может замещать и цинк (атомный радиус 127 пм) в цинкзависимых ферментах,
изменяя при этом их каталитические свойства.
Калий перманганат КМnО4
- наиболее известное соединение марганца, применяемое в медицине. Используют
водные растворы с содержанием КМnО4
от 0,01 до 5%. В качестве кровоостанавливающего средства применяют 5%-ный
раствор. Растворы калия перманганата обладают антисептическими свойствами,
которые определяются его высокой окислительной способностью.
Из других соединений марганца
следует отметить сульфат марганца (II)
и хлорид марганца (II),
которые используют при лечении малокровия.
О наличии технеция в живых
организмах данных нет. Однако соединения технеция с бисфосфонатами используют
для радиоизотопного метода диагностики.
химический элемент
биологический

Метастабильный изотоп технеция 99Тс
является излучителем лучей. В первые после внутривенного введения препарата
«Технефор», содержащего 99Тс, можно исследовать состояние мягких
тканей, а через 2-3 ч после введения - костных. Ниже приводится формула
строения комплекса 99Тс с бисфосфонатом:
В соединении с бисфосфонатом
технеций обычно четырехвалентен, при этом координационное число может быть
равным 6, что хорошо видно на схеме.
Таким образом, для решения
медико-биологических задач используются не только соединения жизненно
необходимого Мn, но и соединения
искусственного элемента 99Тс.
. Общая характеристика d-элементов
VIIIБ-группы (семейство
железа и семейство платины)

В VIIIБ-группе
периодической системы расположены химические элементы - переходные металлы: Fе,
Со, Ni, Rn,
Rh, Рd,
Оs, Ir,
Рt.
Закономерные изменения свойств
элементов четвертого периода (Fе,
Со, Ni) проявляются
значительно четче, чем у остальных элементов VIIIБ-группы.
Поэтому Fе, Со, Ni
объединены в семейство железа. Другие шесть элементов - в семейство платины.
Элементы семейства железа имеют
близкие по значениям орбитальные радиусы (123, 118, 114 пм). Это можно
объяснить тем, что ns-электроны
частично экранируются (n-1)d-электронами.
При этом увеличение заряда ядра на единицу не вызывает соответствующего роста
экранирования:
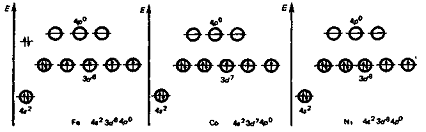
Рост электроотрицательности в
ряду Fе (1,83) - Со
(1,88) - Ni (1,91) показывает,
что от железа к никелю должно происходить уменьшение основных и восстановительных
свойств. В электрохимическом ряду напряжений элементы подгруппы железа стоят
перед водородом.

По распространенности в
природе, применению соединений в медицине и технике и роли в организме железо
стоит на первом месте в VIIIБ-группе.
Элементы семейства железа в соединениях проявляют степень окисления +2, +3.
Соединения элементов со степенью окисления +2 малоустойчивы. Более устойчивы
соединения элементов со степенью окисления +3.
Химические свойства соединений
железа, кобальта, никеля. Оксиды общей формулы МО могут быть получены
восстановлением оксидов более высокой валентности (М2О3,
М3О4), а также окислением металла М, термическим
разложением солей и гидроксидов без доступа воздуха.
Оксиды нерастворимы в воде, растворяются
в кислотах с образованием оксоаквакатионов, придающих раствору зеленую окраску
различных оттенков:
МО + 2Н3О+
+ 3Н2О ⇄
[М(Н2О)6]2+
При подщелачивании этих
растворов выпадают осадки гидроксидов основного характера М(ОН)2.
Гидроксид Fе(ОН)2 -
белого цвета (на воздухе зеленый за счет частичного окисления). Гидроксид
Со(ОН)2 - синего цвета (на холоду, α-форма)
или розового цвета (в теплом растворе, β-форма).
При образовании коллоидного раствора появляется коричневое окрашивание.
Гидроксид Ni(ОН)2
представляет собой зеленые кристаллы.
Из трех перечисленных
гидроксидов в аммиаке и солях аммония растворяется только Ni(ОН)2:
Ni(ОН)2
+ 2NН4Сl
+ 4NН4ОН →
[Ni(NН3)6]Сl2
+ 6Н2О
зеленый синий
Гидроксид никеля (II)
окисляется на воздухе. Гидроксиды железа (II)
и кобальта (II) окисляются
(как и соли) лишь в присутствии влаги:
4Fе(ОН)2
+ O2
+ 2Н2О → 4Fе(ОН)3
Восстановительные свойства
уменьшаются в ряду Fе2+
- Со2+ - Ni2+.
У солей Ni2+
восстановительные свойства практически отсутствуют.
В биогенных соединениях железо
связано в комплекс с органическими лигандами (миоглобин, гемоглобин). Степень
окисления железа в этих комплексах дискутируется. Одни авторы считают, что
степень окисления равна +2, другие предполагают, что она меняется от +2 до +3 в
зависимости от степени взаимодействия с кислородом.
Оксид железа (III).
Fе2О3
в природе существует в виде минерала гематита красного цвета (аналогия с
кровью).
Оксид железа (III)
соответствует гидроксиду Fе(ОН)3,
обладающему слабо выраженными амфотерными свойствами. При его растворении в
щелочи образуется гидроксоанионы:
Fе(ОН)3
+ 3ОН- → [Fе(ОН)6]3-
Fе(ОН)3
может выпасть в осадок при обработке солей железа (III)
раствором КСN низкой концентрации. При более высоких концентрациях образуется
калий гексацианоферрат (III)
К3[Fе(СN)6]:
FеСl3
+ 6КСN + 6Н2О →
2Fе(ОН)3 +
6КСl + 6НСN
Fе(ОН)3
+ 6КСN
→
К3[Fе(СN)6]
+ 3КОН
Это токсичное соединение
упоминается в алхимической литературе (VII-XVII
в.) под названием красная кровяная соль.
Калий гексацианоферрат (III),
как и желтая кровяная соль - калий гексацианоферрат (II)
К4[Fе(СN)6],
применяется в аналитической химии для определения ионов Fе2+
и Fе3+. Оба
иона образуют комплексные соединения, где координационное число металла равно
6. Анионные комплексы Fе
(III) более устойчивы,
чем анионные комплексы Fе
(II).
. Биологическая роль d-элементов
семейства железа. Применение их соединений в медицине
Железо Fе
и кобальт Со - необходимые микроэлементы живых организмов.
Железо - биогенный элемент,
содержится в тканях животных и растений. Общая масса железа в организме
взрослого человека примерно 5г, что составляет 0,007%. Металлическое железо
мало токсично, а соединения Fе(II),
Fе(III)
и Fе(VI)
в больших количествах опасны для здоровья.
Наиболее важными с
физиологической точки зрения являются железосодержащие белки: гемоглобин,
миоглобин, цитохромы, пероксидазы, каталаза. Гемоглобин - главная составная
часть эритроцитов. Обеспечивает внешнее дыхание, являясь переносчиком кислорода
от легких к тканям. Миоглобин, цитохромы, каталаза обеспечивают клеточное
дыхание.

Все эти белки состоят из
собственно белковых частей и связанных с ними активных центров.
Активный центр представляет
собой макроциклическое комплексное соединение - гем (от греч. гема - кровь). В
качестве макроциклического лиганда выступает тетрадентантное соединение -
порфирин. Донорные атомы азота расположены по углам квадрата, в центре которого
расположен ион железа. В целом, комплекс имеет октаэдрическую конфигурацию.
Пятая орбиталь через азот аминокислоты - гистидина используется для связи тема
с белком. Шестая орбиталь свободна и может связывать различные
низкомолекулярные лиганды R:
О2, Н2О2, СО, СN-.
Гемоглобин состоит из четырех
белковых молекул (субъединиц), которые образуют единый макромолекулярный
агрегат. Каждая субъединица по строению аналогична молекуле миоглобина. Таким
образом, гемоглобин может одновременно связывать четыре молекулы О2,
а миоглобин - одну.
На основе законов химического
равновесия нетрудно понять функционирование гемоглобина как переносчика
кислорода от легких к тканям.
Гемоглобин без кислорода
(дезоксигемоглобин) представляет собой слабую кислоту и его химическую формулу
можно представить в виде ННb+.
Присоединение кислорода сопровождается отщеплением протона и образуется
оксигемоглобин НbО2.
При этом имеет место равновесие:
ННb+
+ О2 ⇄
НbО2 + Н+
При поступлении бедной
кислородом венозной крови в легкие, где парциальное давление кислорода велико
(до 20 кПа), его растворимость возрастает согласно закону Генри. Это приводит в
соответствии с принципом Ле Шателье к смещению равновесия вправо и образованию
оксигемоглобина. Дополнительное смещение равновесия вправо обусловлено тем, что
в легких значение рН повышено (до 7,5). В результате в легких дезоксигемоглобин
практически полностью (до 97%) насыщается кислородом и переходит в
оксигемоглобин. В капиллярах, пронизывающих периферические ткани, парциальное
давление кислорода снижается до 5 кПа, а значение рН снижается до 7,2. В
результате равновесие смещается влево. В оттекающей с периферии крови
гемоглобин насыщен кислородом лишь на 65%. Таким образом, при циркуляции крови
в организме равновесие ННb+
+ О2 ⇄
НbО2 + Н+
периодически сильно смещается (на 35%) то вправо, то влево.
Металлокомплексные свойства
гемсодержащих белков проявляются при действии таких токсических веществ как СО
(угарный газ) и МСN (цианиды -
соли синильной кислоты).
Углерод моноксид СО - один из
продуктов неполного сгорания топлива. Значительные количества этого газа
выделяются при работе котельных, двигателей внутреннего сгорания, курении. При
вдыхании СО с воздухом в легких параллельно с оксигемоглобином НbО2
образуется металлокомплексное соединение - карбонилгемоглобин НbСО.
Константа устойчивости НbСО
примерно в двести раз больше, чем у НbО2.
Поэтому даже малые количества СО «перехватывают» значительную долю
дезоксигемоглобина. В результате поступление кислорода к органам уменьшается.
Появляются признаки гипоксии - кислородной недостаточности. В первую очередь
страдают нервные ткани. Для детоксикации - устранения отравляющего действия
углерод моноксида во многих случаях достаточно прекратить его поступление и
усилить кислородную вентиляцию - вывести пострадавшего на «свежий» воздух. При
этом опять работает принцип Ле Шателье - равновесие смещается в сторону
образования оксигемоглобина.
При больших концентрациях
углерод моноксид блокирует гемсодержащие белки клеточного дыхания и трудно
избежать летального исхода.
Аналогичен механизм действия
цианидов. Но их токсичность выше, чем для СО. Поступление в кровь даже очень
небольших количеств этих веществ приводит к остановке дыхания и летальному
исходу. Высокая токсичность цианидов объясняется высокой прочностью связи Fе
- СN-,
что обусловливает большую устойчивость цианидгемоглобина.
Кислородное дыхание приводит к
образованию Н2О2. Это вещество обладает высокой
окислительной способностью. При его взаимодействии с биоорганическими
соединениями клеток образуются радикалы - очень активные молекулярные частицы с
ненасыщенной валентностью и инициируется пероксидное окисление. Под действием
радикалов разрушаются важнейшие составные части клетки - мембраны и ДНК. В ходе
биологической эволюции природа выработала особый белок - фермент каталазу,
которая разрушает водородпероксид. Тем самым ограничивается избыточное
накопление этого вещества и предотвращается разрушение клетки.
Действие каталазы (СаtFе2+)
может быть представлено в виде каталитического цикла из двух последовательных
реакций:
СаtFе2+
+ Н2О2 → СаtFе2+•Н2О2
СаtFе2+•Н2О2
+ Н2О2 → СаtFе2+
+ 2Н2О + О2
В результате разрушаются две
молекулы водородпероксида, а молекула биокатализатора СаtFе2+
освобождается и может вступать в следующий каталитический цикл. Этот процесс
очень быстрый. В течение секунды 1 молекула каталазы может осуществлять до 20
000 циклов.
При недостатке в организме
железа может развиваться болезнь - железодефицитная анемия (малокровие).
Возникает тканевая кислородная недостаточность, связанная с нехваткой железа
для синтеза гемоглобина. В результате доставка кислорода к периферическим
органам снижается, и, соответственно, понижается уровень клеточного дыхания,
замедляется обмен веществ.
Введение в качестве
лекарственных препаратов - хлорида железа (II)
или сульфата железа (II)
ослабляет остроту заболевания. Для этих же целей используется мелкодисперсный
порошок металлического железа (железо восстановленное, до 1г на прием), который
легко растворяется в соляной кислоте желудочного сока. Поэтому действие этого
препарата аналогично действию хлорида железа (II).
Однако более эффективны препараты, представляющие собой бионеорганические
комплексы железа с сахарами, никотинамидом и другими органическими веществами.
Такие комплексы хорошо всасываются в кровь, с чем и связана их
фармакологическая эффективность.
Интересно отметить, что с
древних времен до настоящего времени для лечения железодефицитной анемии применяют
так называемое «железное вино» - напиток, который получают путем настаивания
виноградного вина на железных опилках. Очевидно, железо растворяется в вине
(кислая среда) и образует комплексы с природными органическими веществами,
которые содержатся в нем в больших количествах. Понятно, что механизм действия
древнего напитка примерно тот же, что и у современных препаратов.
Кобальт. Как и железо, кобальт
также является одним из важнейших биогенных элементов. Общая масса кобальта в
организме взрослого человека примерно 1,2 мг, что составляет менее 2∙10-6
%. Около 100 мг из этой массы находится в форме цианокобаламина
(жирорастворимый витамин B12)
и его аналогов. Это вещество, как и гем, представляет собой макроциклическое
комплексной соединение.
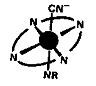
В качестве макроциклического
лиганда выступает тетрадентатное соединение - порфин. R
представляет собой сложный органический заместитель. В аналогах цианокобаламина
вместо аниона СN-
выступают различные органические заместители.
Наиболее важную роль витамин В12
играет в развитии и формировании эритроцитов (эритропоэз). Дефицит витамина В12
(поступление менее 3 мкг в сутки) приводит к тяжелому заболеванию -
злокачественной анемии (малокровии).
Установлено, что аналоги
цианокобаламина являются активаторами - кофакторами различных ферментов,
участвующих в эритропоэзе. Недостаток кофакторов проявляется в дефиците
гемоглобина и эритроцитов.
Растения и животные не могут
синтезировать витамин В12. Его вырабатывают лишь некоторые виды
бактерий. В желудочно-кишечном тракте человека такие бактерии имеются. Они
синтезируют достаточное количество витамина В12. Злокачественная
анемия связана с нарушением всасывания этого витамина в кровь. Поэтому прием
таблеток малоэффективно. Инъекция витамина (100-200 мкг в течение 2 сут) в
кровь существенно улучшает состояние больного при злокачественном малокровии.
8. Общая характеристика d-элементов
IБ-группы
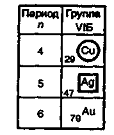
В IБ-группе
(группе меди) находятся переходные металлы Сu,
Аg, Аu,
которые имеют сходное распределение электронов, определяемое феноменом
«проскока» или «провала» электронов.
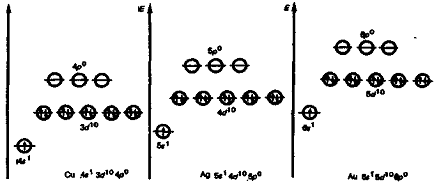
Явление «проскока» представляет
собой символическое перенесение одного из двух валентных s-электронов
на d-подуровень, что
отражает неравномерность удержания ядром внешних электронов.
Переход одного s-электрона
на внешний уровень приводит к стабилизации d-подуровня.
Поэтому в зависимости от степени возбуждения атомы IБ-группы
могут отдавать на образование химической связи от одного до трех электронов.
Вследствие этого элементы IБ-группы
могут образовывать соединения со степенями окисления +1, +2 и +3. Однако
имеются различия: для меди наиболее устойчивы степени окисления +1 и +2; для
серебра +1, а золота +1 и +3. Наиболее характерные координационные числа в этой
группе 2, 3, 4.
Элементы 1Б-группы относительно
инертны. В электрохимическом ряду стоят после водорода, что проявляется в их
слабой восстановительной способности. Поэтому в природе встречаются в
самородном виде. Они относятся к первым металлам, которые нашел и применил
древний человек. В качестве ископаемых находят соединения: Сu2О
- куприт, Сu2S
- халькозин, Аg2S
- аргентит, акантит, АgСl
- кераргирит, АuТe2
- калаверит, (Аu,Аg)Те4
- сильванит.
В группе IБ
восстановительные и основные свойства убывают от меди к золоту.
Химические свойства соединений
меди, серебра, золота.
Оксид серебра (I)
получают при нагревании серебра с кислородом или обработкой растворов АgNО3
щелочами:
АgNО3
+ 2КОН → Аg2О
+ 2КNО3 + Н2О
Оксид серебра (I)
в воде растворяется незначительно, тем не менее, вследствие гидролиза растворы
имеют щелочную реакцию
Аg2О
+ Н2О → 2Аg+
+ 2ОН-
в цианидных растворах
превращается в комплекс:
Аg2О
+ 4КСN + Н2О →
2К[Аg(СN)2]
+ 2КОН
Аg2О
- энергичный окислитель. Окисляет соли хрома (III):
Аg2O
+ 2Сr(ОН)3 +
4NаОН → 2Nа2СrО4
+ 6Аg + 5Н2О,
а также альдегиды и
галогеноуглеводороды.
Окислительные свойства оксида
серебра (I) обусловливают
применение его суспензии как антисептического средства.
В электрохимическом ряду
нормальных окислительно-восстановительных потенциалов серебро стоит после
водорода. Поэтому металлическое серебро реагирует только с окисляющими
концентрированной азотной и серной кислотами:
Аg
+ 2Н2SО4
→ Аg2SО4
+ 5О2 + 2Н2О
Большинство солей серебра мало
или плохо растворимы. Практически нерастворимы галогениды, фосфаты. Плохо
растворимы сульфат серебра и карбонат серебра. Растворы галогенидов серебра
разлагаются под действием ультрафиолетовых и рентгеновских лучей:
АgСl
-hν→
2Аg + Сl2
Еще более чувствительны к
действию ультрафиолетовых и рентгеновских лучей кристаллы АgСl
с примесью бромидов. Под действием кванта света в кристалле протекают реакции
Вr--
+ hν →
Вг° + е-
Аg+
+ е~ → Аg°
АgВr
→
2Аg0
+ Вr2
Это свойство галогенидов
серебра используют при изготовлении светочувствительных материалов, в частности
фотопленок, рентгеновских пленок.
Нерастворимые серебро хлорид и
серебро бромид растворяются в аммиаке с образованием аммиакатов:
АgСl
+ 2NН3 →
[Аg(NH3)2]Сl
Растворение АgСl
возможно потому, что ионы серебра связываются в очень прочный комплексный ион.
В растворе остается настолько мало ионов серебра, что их не хватает для
образования осадка, так как произведение концентраций меньше константы
растворимости.
Бактерицидные свойства АgСl
используются в препаратах для обработки слизистых оболочек газа. Для
стерилизации и консервации пищевых продуктов применяется «серебряная вода» -
обработанная кристаллами АgСl
дистиллированная вода.
Так же, как и серебро, медь (I)
образует нерастворимые галогениды. Эти соли растворяются в аммиаке и образуют
комплексы:
СuСl
+ 2NН3 →
[Сu(NН3)2]Сl
Нерастворимы в воде оксиды и
гидроксиды меди (II),
которые имеют основной характер и растворяются в кислотах:
Сu(ОН)2
+ 2НСl + 4Н2О →
[Сu(Н2О)6]Сl2
Образующийся аквакатион [Сu(Н2О)6]2+
сообщает растворам яркую голубую окраску.
Гидроксид меди (II)
растворяется в аммиаке, образует комплекс, окрашивающий раствор в синий цвет:
Сu(ОН)2
+ 4NН3 + 2Н2О
→ [Сu(NН3)4(Н2О)2](ОН)2
Эта реакция используется для
качественной реакции на ионы меди (II).
Соли меди, серебра и золота
взаимодействуют с сульфидами щелочных металлов и с водородсульфидом с
образованием нерастворимых в воде осадков - Аg2S,
Сu2S,
СuS, Аu2S3.
Высокое сродство металлов
группы IБ к сере определяет
большую энергию связи М-S,
а это, в свою очередь, обусловливает определенный характер их поведения в
биологических системах.
Катионы этих металлов легко
взаимодействуют с веществами, в состав которых входят группы, содержащие серу.
Например, ионы Аg+
и Сu+
реагируют с дитиоловыми ферментами микроорганизмов по схеме:

Включение ионов металлов в
состав белка инактивирует ферменты, разрушает белки.
Такой же механизм лежит и в
основе действия содержащих серебро и золото лекарственных препаратов,
применяемых в дерматологии.
Наиболее распространенным
соединением золота (III)
является хлорид АuСl3,
хорошо растворимый в воде.
Оксид и гидроксид золота (III)
- амфотерные соединения с более выраженными кислотными свойствами. Гидроксид
золота (III) в воде не
растворяется, но растворяется в щелочах с образованием гидроксокомплекса:
Реагирует с кислотами с
образованием ацидокомплекса:
АuО(ОН)
+ 2Н2SО4
→ Н[Аu(SО4)2]
+ 2Н2О
Для золота и его аналогов
известно большое число комплексных соединений. Знаменитая реакция растворения
золота в «царской водке» (1 объем конц. НМОз и 3 объема конц. НСl)
представляет собой образование комплексной кислоты:
Аu
+ 4НСl + НNО3
→ Н[АuСl4]
+ NO + 2Н2О
В организме медь функционирует
в степенях окисления + 1 и +2. Ионы Сu+
и Сu2+
входят в состав «голубых» белков, выделенных из бактерий. Эти белки имеют
сходные свойства и называются азуринами.
Медь (I)
более прочно связывается с серосодержащими лигандами, а медь (II)
с карбоксильными, фенольными, аминогруппами белков. Медь (I)
дает комплексы с координационным числом, равным 4. Образуется тетраэдрическая
структура (если участвует четное число d-электронов).
Для меди (II)
координационное число равно 6, ему соответствует орторомбическая геометрия
комплекса.
. Биологическая роль d-элементов
IБ-группы.
Применение их соединений в медицине
Медь Сu
- необходимый микроэлемент живых организмов. Серебро Аg
и золото Аu - примесные
микроэлементы. Их соединения применяют в медицине.
Медь - биогенный элемент,
содержится в тканях животных и растений. Общая масса меди в организме взрослого
человека примерно 100 мг, что составляет около 0,0001%. Примерно 30% этого
количества содержится в мышцах. Печень и мозг также богаты медью. Металлическая
медь и ее соединения токсичны.
Наиболее важными с
физиологической точки зрения являются медьсодержащие белки - цитохромоксидаза и
супероксиддисмутаза.
Цитохромоксидаза - один из
компонентов дыхательной цепи, локализованной в мембранах митохондрий. Обеспечивает
клеточное дыхание, восстанавливая кислород до воды на конечном участке
дыхательной цепи.
Цитохромоксидаза (М, = 200 000)
состоит из семи белковых субъединиц и четырех связанных с ними активных
центров: двух молекул тема, связывающих ионы железа, и двух ионов меди,
непосредственно связанных с белковыми субъединицами. Такая структура
цитохромоксидазы обеспечивает передачу четырех электронов из дыхательной цепи и
осуществление реакции
О2 + 4Н+
+ 4е~ →Цитохромоксидаза→ 2Н2О
При неполном восстановлении
кислорода в дыхательной цепи образуется анион пероксида:
О2 + е~
-> О2-
Взаимодействие этого аниона с
органическими соединениями клетки приводит к образованию радикалов и нарушению
нормального развития клетки.
Повреждающее действие аниона
предотвращается медьсодержащим ферментом супероксиддисмутазой (СОД). Этот
фермент катализирует реакцию
О2- + О2-
+ 2Н+ → Н2О2 + О2
Образующийся при этом
водородпероксид разлагается каталазой. В результате совместного действия
содержание радикалов в клетке поддерживается на безопасном уровне.
Интересно, что переносчиком
кислорода у моллюсков и членистоногих является не гемоглобин, а гемоцианин (от
греч. кианос - лазурный). Кровь этих животных имеет голубой цвет.
Гемоцианин в зависимости от
биологического вида имеет различную молекулярную массу (у омара Мг =
825000) и состоит из большого числа белковых субъединиц (Мг от 25000
до 35000). Каждая субъединица имеет центры связывания кислорода. Эти центры
представляют собой медьпротеиновые комплексы кислорода (биокластеры) с двумя
ионами меди. Каждая такая пара связывает одну молекулу кислорода.
Ежедневно организму требуется
2,5-5,0 мг меди. При недостатке в организме меди может развиваться болезнь -
медьдефицитная анемия. Медь необходима для усвоения железа, в частности, при синтезе
цитохромоксидазы, которая содержит и железо, и медь. При дефиците меди
нарушается нормальное развитие соединительных тканей и кровеносных сосудов.
Широкое применение меди и ее
соединений в промышленности и сельском хозяйстве повышает риск отравления этими
веществами. Отравления обычно связаны со случайной передозировкой инсектицидов,
вдыханием порошка металла, заглатыванием растворов солей меди. Большую
опасность представляют напитки, хранящиеся в медных сосудах без защитного
покрытия стенок.
Токсическое действие соединений
меди обусловлено тем, что ионы меди взаимодействуют с тиольными -SН-группами
(связывание) и аминогруппами -NH2
(блокирование) белков. При этом могут образовываться биокластеры хелатного
типа:
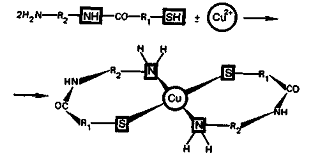
Вследствие таких взаимодействий белки становятся
нерастворимыми, теряют ферментативную активность. В результате нарушается
нормальная жизнедеятельность.
В качестве наружного средства
применяют 0,25%-ный водный раствор сульфата меди СuSО4
при воспалении слизистых оболочек и конъюнктивитах. Малые дозы этого препарата
могут применяться во время приема пищи для усиления эритропоэза при малокровии.
Серебро и золото. В организме
взрослого человека обнаруживается около 1 мг серебра, т.е. примерно 10-6%
(1 ч. на миллион), и до 10 мг золота, т.е. примерно 10-5% (10 ч. на
миллион).
Антисептические свойства
растворимых солей серебра известны с древних времен. Священнослужители давно
знали, что вода («святая») при хранении в серебряных сосудах долго не портится,
т.е. не подвергается микробному загрязнению. В настоящее время это свойство
«серебряной» воды используется моряками в дальних плаваниях.
Сильные токсические проявления
у взрослого человека наблюдаются при приеме внутрь 7 г АgNO3.
Токсическое действие соединений
серебра, как и в случае меди, обусловлено главным образом тем, что ионы серебра
взаимодействуют с тиольными серо- и азотсодержащими группами белков,
нуклеиновых кислот и других биоорганических веществ.
В водном растворе существуют
только комплексные соли золота, например, Nа3[Аu(S2О3)2]
и различные тиоловые бионеорганические комплексы.
Механизм токсического действия
соединений золота аналогичен механизму токсического действия соединений меди и
серебра. В соответствии с общим правилом для тяжелых металлов одной группы
токсичность возрастает с увеличением атомного номера в ряду: Сu
Аg Аu.
В медицине издавна используются
такие препараты, как кристаллический серебро нитрат АgNО3
(ляпис) и его водные растворы. Давно известны также препараты коллоидного
металлического серебра протаргол (8% Аg)
и колларгол (70% Аg), которые
представляют собой мелкодисперсные порошки с металлическим блеском. Каждая
частица таких порошков представляет собой кристаллик восстановленного
металлического серебра размером менее 1 мкм с белковой оболочкой из альбумина
(протаргол) или коллагена (колларгол). Белковая оболочка защищает кристаллики
серебра от слипания и обеспечивает их переход в водную среду (солюбилизирует).
Препараты серебра применяют как
противовоспалительные, антисептические и вяжущие средства.
В качестве эффективных
противовоспалительных средств применяют также препараты золота. Наиболее
известны кризанол (от греч. хризос - золото), с 30%-ным содержанием
благородного металла, и коллоидное золото. Главный компонент кризанола -
комплекс золота с тиоловым органическим соединением Аu-S-СН2СН(ОН)СН2-SО3.
10. Общая характеристика d-элементов
IIБ-группы.
У элементов IIБ-группы
(Zn, Сd,
Нg) предпоследний
электронный слой полностью заполнен, «неспаренных» электронов нет.
Это и определяет стабильность и
особенности химических свойств элементов.
Элементы IIБ-группы
имеют два спаренных электрона на s-подуровне
внешнего уровня. Эти электроны и определяют постоянную валентность, равную
двум.

В соединениях элементы этой
группы имеют степень окисления +2. Для ртути характерна степень окисления +1 в
результате образования атомных димеров Нg22+
(соединения Нg2Сl2,
Нg2(NO3)2).
В этих димерах связь между атомами ртути неполярна +Нg-Нg+.
Поэтому суммарное значение степени окисления равно +1.
Увеличение
электроотрицательности в ряду элементов IIБ-группы
Zn(1,6)-Сd(1,7)-Нg(1,9)
приводит к ослаблению основных и восстановительных свойств, т.е. возрастает
неметалличность элемента. Это, в частности, способствует димеризации атомов
ртути.

По физическим и химическим свойствам ртуть
значительно отличается от цинка и кадмия. Ртуть в электрохимическом ряду
напряжений металлов стоит после водорода, поэтому растворяется лишь в
кислотах-окислителях:
Нg
+ 8НNО3 →
ЗНg(NО3)2
+ 2NО + 4Н2О
Zn,
Сd, Нg
находятся на границе между неметаллами (p-элементами)
и металлами (d-элементами),
поэтому оксо- и гидроксосоединения Zn,
Сd и Нg
проявляют амфотерный характер. Амфотерность соединения от Zn
к Нg резко уменьшается.
Цинк растворяется в щелочи при нагревании.
Zn
+ 2NаОН + 2Н2О → Nа2[Zn(ОН)4]
+ Н2
Кадмий в тех же условиях не
растворяется.
Металлы IIБ-группы
(так же как их оксиды и гидроксиды) хорошо растворяются в кислотах. Zn
и Сd реагируют с
разбавленными (содержание меньше 10%) НСl,
НNО3, Н2SO4
с выделением водорода. Zn,
Сd и Нg
с концентрированными НNО3
и Н2SО4
реагируют с выделением NO
и SО2.
Элементы IIБ-группы
являются своеобразным «экватором», при переходе через которых свойства
элементов меняются от основных к кислотным. Аналогичное явление наблюдается в
случае s-элементов для
бериллия, обладающего амфотерными свойствами. Бериллий расположен между
металлом Li и
неметаллом В.
Близость химических свойств Zn
и
Сd можно объяснить
почти равными значениями электроотрицательности элементов, соответственно 1,6 и
1,7. Амфотерный характер элементов IIБ-группы
проявляется еще и в том, что цинк, кадмий и ртуть могут находиться не только в
гидратированной кати-онной форме [М2+(Н2О)n],
где n = 4, 6, но и в
анионной [М2+(ОН)n],
где n = 4, 6, в том
числе и.в виде аутокомплексов: Сd[СdI3],
Сd[СdI4],
Нg[НgСl3]2,
Нg[НgСl4].
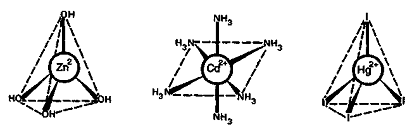
Цинк, кадмий и ртуть, как и все
d-элементы, образуют
большое число комплексных соединений. Комплексообразование идет за счет
свободных орбиталей ионов металлов и за счет неподеленных пар d-электронов
(n-1)-слоя. Для цинка
характерно координационное число, например, К2[Zn(ОН)4],
К2[НgI4]
для кадмия - 4,6, например, [Сd(NН3)6]Сl2.
Химические свойства соединений
цинка, кадмия и ртути.
Металлы IIБ-группы
реагируют при нагревании с галогенами (если без нагревания, то необходимо
увлажнение), кислородом, серой. Цинк и кадмий реагируют также с фосфором.
При взаимодействии с кислородом
образуются оксиды общей формулы МО. Оксиды имеют характерную окраску: ZnО
- белый, СdO -
коричневый, НgО - желтый или
красный. Оксиды не растворяются в воде, но растворяются в кислотах.
Оксидам МО соответствуют
гидроксиды типа М(ОН)2, нерастворимые в воде. Термическая
устойчивость гидроксидов Zn
(II) и Сd(II)
значительно выше гидроксида ртути (II),
который разлагается в момент осаждения из раствора.
При обработке НgО
водным раствором NНз
образуется желтый осадок (основание Миллона):
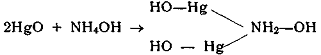
При нагревании этого соединения
до 125°С образуется гидроксид:
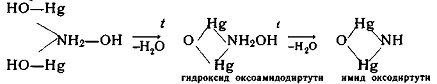
Диспергированный гидроксид
ртути (II) в
коллоидном состоянии служит бактерицидным средством. Антисептическим действием
обладает также белый осадок ртути амидохлорида, который получается
взаимодействием водного раствора аммиака с сулемой (НgСl2)
или каломелью (Нg2Сl2):
НgСl2
+ 2NН3 →
НgNH2Сl
+ NН4Сl
Нg2Сl2
+ 2NН3 →
НgNН2Сl
+ NН4Сl
+ Нg
Обе реакции используются в
химическом анализе для обнаружения ионов Нg2+
и Нg22+.
Амидохлорид ртути НgNН2Сl
может взаимодействовать в биологической системе с сульфогидроксильными группами
белков. Этим объясняется антисептическое действие амидохлорида ртути.
Для обнаружения ионов аммония NH4+
также используются соединения ртути К2[НgI4]
(калий тетраиодомеркурат - реактив Несслера)
К2[НgI4]
+ NН3 +
3КОН → НОНgNННgI
+ 7КI + 2Н2О
Каломель в воде растворяется
незначительно и поэтому менее токсична, чем сулема.
Сулема НgСl2
представляет собой бесцветные кристаллы, достаточно хорошо растворимые в воде,
спирте, эфире, пиридине и др.
Интересно, что в водных
растворах НgСl2
почти не диссоциирует и находится в молекулярной форме. Поэтому водные растворы
сулемы не проводят электрический ток.
11. Биологическая роль d-элементов
IIБ-группы.
Применение их соединений в медицине
Цинк Zn,
кадмий Сd, ртуть Нg
- микроэлементы. В организме взрослого человека содержится 1,8г (0,0024%) Zn,
50 мг (7-10-5%) Cd,
13мг (2-10-5%)Нg.
Кадмий и ртуть - примесные
элементы. Около 70% ртути сосредоточено в жировой и мышечной ткани. Кадмий
локализуется на 30% в почках, остальное в печени, легких, поджелудочной железе.
Цинк - необходимый элемент всех
растений и животных. В организме взрослого человека больше всего цинка в мышцах
(65%), костях (20%). Остальное количество приходится на плазму крови, печень,
эритроциты. Наибольшая концентрация цинка в предстательной железе.
Цинк не проявляет переменной
валентности. Видимо поэтому его биокомплексы принимают участие во многих
биохимических реакциях гидролиза, идущих без переноса электронов. Ион цинка
входит в состав более 40 металлоферментов, катализирующих гидролиз эфиров и
белков.
Одним из наиболее изученных
является бионеорганический комплекс цинка - фермент карбоангидраза (Мг
= 30 000), состоящий, примерно, из 260 аминокислотных остатков.
Ниже схематично представлено
положение иона цинка в полости карбоангидразы (КА). Белковый лиганд, связанный
с Zn2+,
представляет активный центр фермента. Цинка в ферменте всего 0,22%. Тем не
менее наличие цинка - необходимое условие каталитической активности
карбоангидразы, которая обеспечивает гидратацию СО2:
СО2 + Н2О
→ НСО3- + Н+
Протекание этой реакции
обусловливает нормальное дыхание. В отсутствие карбоангидразы нормальный
газообмен был бы затруднен, так как гидратация СО2 замедлилась бы в
10000000 (107) раз.
Как видно из схемы,
координационное число Zn2+
в карбоангидразе равно 4. Три связи заняты аминокислотными остатками (Нis
- гистидил), а четвертая связывает гидроксил - ион ОН- или молекулу
воды.
Единого мнения о действии
карбоангидразы нет. Одни исследователи считают, что цинк координирует молекулу
воды, гидратирующую СО2. Другие полагают (механизм «цинк -
гидроксид»), что цинк координирует гидроксильную группу при гидратации СО2:
ОН-
+ СО2 ⇄
НСО3-
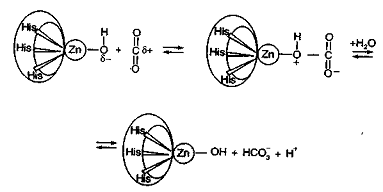
Прежде полагали, что
карбоангидраза катализирует только обратимую гидратацию СО2. Однако
имеются данные о каталическом действии карбоангидразы на превращение
карбонильной группы (С=О) субстрата в карбоксильную (СООН). В этом случае
механизм действия карбоангидразы подобен действию другого цинксодержащего
фермента - карбоксипептидазы (КОП).

Одна из наиболее изученных форм
КОП имеет 307 аминокислотных остатков (содержание цинка 0,19%). Схему реакции
превращения карбонильной группы субстрата в карбоксильную, катализируемой КОП,
можно представить следующим образом:
Механизм действия КОП
окончательно не выяснен, и возможны два варианта.
Механизм «цинк - карбоксил»
предполагает, что субстрат вытесняет молекулу воды, координированную цинком.
Затем карбонильная группа образует связь с ионом цинка. Другой механизм не
предполагает образование связи через карбоксил фермента.
Цинк не входит в состав
дипептидаз - ферментов, катализирующих гидролиз дипептидов - веществ, состоящих
из двух аминокислот.
Цинк образует бионеорганический
комплекс с инсулином - гормоном, регулирующим содержание сахара в крови.
Потребность человека в цинке
полностью удовлетворяется пищевыми продуктами: мясными, молочными, яйцами.
При недостатке цинка в
растениях нарушаются белковый и углеводный обмен, тормозится синтез хлорофилла
и витаминов. Дефицит цинка устраняется при использовании цинксодержащих
удобрений.
Токсичность соединений IIБ-группы
увеличивается от цинка к ртути.
Водорастворимые соединения
оказывают раздражающее действие на кожу. При попадании внутрь организма
вызывают отравление.
Токсичны и сами металлы. При
вдыхании паров цинка (воздух цинковых производств) появляется «металлическая»
лихорадка. Отравление парами ртути в средние века получило название «болезнь
сумасшедшего шляпочника».
Содержание ртути в пищевых
продуктах (в морских, как в Японии) приводит к «болезни миномата».
Токсичность ртути связана с
агглютинацией (склеиванием, слипанием) эритроцитов, ингибированием ферментов.
Например, сулема НgСl2
вызывает изменение размеров, осмотическую хрупкость и снижение деформируемости
эритроцитов, которая необходима для их продвижения по капиллярам.
Токсичность кадмия связана с
его сродством к нуклеиновым кислотам. В результате его присоединения к ДНК
нарушается ее функционирование.
Хроническая интоксикация
кадмием и ртутью может нарушить минерализацию костей. Это связано с близостью
ионных радиусов. Поэтому токсичные элементы могут замещать кальций. Это
приводит к образованию апатита несовершенной структуры вследствие искажения
параметров кристаллического компонента костной ткани. В результате снижается
прочность костей.
Соединения Zn,
Сu, Нg
могут вызывать нарушение белкового обмена, что проявляется в выделении белков
плазмы через почки (протеинурия).
Токсичное действие соединений
группы IIБ на
организм вызывается еще и тем, что ионы этих металлов вступают во
взаимодействие с сульфгидрильными SН-группами
белков, ферментов и аминокислот.

При взаимодействии ионов
металлов с SН-группами
образуются слабодиссоциирующие и, как правило, нерастворимые соединения.
Поэтому блокирование сульфгидрильных групп приводит к подавлению активности
ферментов и свертыванию белков. Ионы двухвалентных металлов блокируют
одновременно две SН-группы.
В реакциях подобного типа ионы
металлов выступают акцептором, а сера - донором электронов.
Наиболее выражено химическое
сродство SН-группам у ртути.
Очевидно, это связано с тем, что комплексообразующие свойства ртути выше и она
образует более прочные связи с серой.
SН-группы
входят в состав более 100 ферментов, активность которых может быть подавлена
из-за блокирования этих групп. Поэтому очевидно, насколько важно знать механизм
блокирования и методы лечения при отравлении организма металлами.
Известно, что токсические
свойства элементов зависят от той химической формы, в какой они попадают в
организм. Наиболее токсичны те формы, которые растворяются в липидах и легко
проникают через мембрану в клетку.
В литературе описан случай
массового отравления ртутью в Японии. Неорганические соединения ртути под
действием ферментов микроорганизмов превращались в метилртуть:
Нg2+
+ СН3- → СН3Нg+
Метилртуть накапливалась в
рыбе, а затем с пищей попадала в организм человека. Из-за того, что СН3Нg+
растворяется в липидах, она накапливается в организме, в том числе и в мозге.
Постепенно концентрируясь, метилртуть вызывает необратимые разрушения в
организме и смерть.
Использование соединений цинка
и ртути в медицине основано на их вяжущем, прижигающем и антисептическом
действии. В качестве глазных капель применяют 0,25%-ный водный раствор цинк
сульфата ZnSО4.
В стоматологии цинк хлорид ZnСl2
используют для прижигания папилом, для лечения воспаленных слизистых.
Применяется также цинк оксид ZnО.
Хлорид ртуть (II)
Нg2Сl2
(сулема) очень ядовита и ее водные растворы при больших разбавлениях (1:1000)
применяются для дезинфекции. Для лечения кожных и венерических заболеваний
применяют мази, содержащие оксид ртути (II)
НgО и сульфид ртути (II)
НgS. Хлорид ртути (I)
Нg2Сl2
(каломель) плохо растворяется в воде и поэтому мало ядовита. Эту соль применяют
в ветеринарии как слабительное средство.
Ртуть при обычных условиях -
жидкий металл, который способен растворять другие металлы. При этом образуются
твердые сплавы - амальгамы. В стоматологии для пломбирования зубов издавна
применяли амальгамы серебра и кадмия. Они химически инертны, легко размягчаются
при нагревании и поэтому легко формуются.
Жидкая ртуть используется в
ряде приборов, применяемых в медицине. Например, для измерения артериального
давления, в медицинских термометрах.
Источники ультрафиолетового
света - ртутно-кварцевые лампы медицинского назначения содержат газообразную
ртуть (пары). При облучении светом этих ламп больничных помещений уничтожаются
микроорганизмы, содержащиеся в воздухе. С помощью ультрафиолетовых лучей лечат
различные кожные заболевания.
Таким образом, по характеру
функционирования и воздействия на организм металлы IIБ-группы
можно разделить на жизненнонеобходимый элемент Zn
и токсичные примесные элементы Сd
и Нg.
. Семейство платины
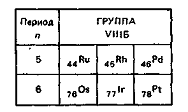
В подгруппу платины входит шесть переходных
металлов. По числу электронов на 4dЗs-орбиталях
(Ru, Rh,
Рd) и 5d6s-орбиталях
(Оs, Ir,
Рt) и по аналогии
физико-химических свойств все элементы VI
IIБ-группы делятся на
три подгруппы: 1) Ru
- Оs; 2) Rh
- Ir; 3) Рd
- Рt. Атомный радиус у
всех шести элементов изменяется в небольшом интервале: 134 пм (Ru)
- 139 пм (Рt).
В электрохимическом ряду все
платиновые металлы стоят после водорода. По значениям электроотрицательности
все элементы группы ближе к неметаллам, чем к металлам. Поэтому соединения этих
металлов проявляют амфотерность, выраженную в разной степени. Гидроксиды не
всех этих элементов растворяются и в кислоте и в щелочи. Тем не менее, элементы
семейства платины образуют не только катионные, но и анионные комплексы.
Устойчивые валентные состояния для элементов семейства платины следующие: Ru
- IV, VI,
VIII; Rh
- III, IV;
Рd - II,
IV; Оs
- IV, VI;
Ir - III,
IV; Рt
- II, IV.
Гидроксиды Ru,
Rh, Рd,
Оs, Ir
и Рt в четырехвалентном
состоянии существуют в форме МО2∙nН2О,
где n = 2 (для платины n
= 2, 3). Содержание воды зависит от температуры.
Гидроксиды Rh,
Рd и Рt
растворяются в кислотах и щелочах:
РtO2∙3Н2О
+ 2NаОН → Na2[Рt(ОН)6]
+ Н2О
РtO2∙3Н2О
+ 6НСl
→
H2[РtСl6]
+ 5Н2О
В обычных условиях платиновые
металлы не взаимодействуют с такими сильными окислителями, как F2,
Сl2
и О2. Низкая реакционная способность элементных веществ определяется
большой энергией связи в кристаллической решетке. Та же причина определяет
высокие температуры плавления и большие значения плотности.
Только платина реагирует без
нагревания с окисляющей смесью кислот
Рt
+ 18НСl + 4НNО3
⇄ 3H2[PtСl6]
+ 4NО + 8Н2О
или с соляной кислотой в
присутствии кислорода
Рt
+ 6НСl + О2 ⇄ Н2[РtСl6]
+ 2Н2О
Все металлы платинового
семейства, кроме иридия, переходят в четырехвалентное состояние при сплавлении
со щелочными окисляющими смесями. Например:
Ru
+ 2КОН + 3КNО3 →
К2RuО4
+ 3КNО2 + Н2О
Иридий переходит в
трехвалентную форму.
При нагревании платиновые
металлы реагируют с NаСl
или НСl в токе хлора, что
приводит к образованию комплекса. Например:
Ir
+ 2NаСl
+ 2Сl2
→ Na2[IrСl6]
Платина при нагревании может
образовывать цианидный комплекс:
Рt
+ 6КСN + 4Н2О →
К2[Рt(СN)6]
+ 4КОН + 2Н2
[Рt(NН3)2Сl2]
+ 2NН3 →
[Рt(NН3)4Сl2]
Нейтральный комплекс:
[Рt(NН3)4]Сl2
+ 2НСl
⇄ [Рt(NН3)2Сl2]
+ 2NН4Сl
Катионно-анионный комплекс:
[Рt(NН3)4]Сl2
+ К2[РtСl4]
→ [Рt(NН3)4]
[РtСl4]
+ 2КСl
Применение соединений платиновых
элементов в медицине. Многочисленные исследования показали, что цис-изомер
дихлородиамминплатины(II)
[Рt(NН3)4]Сl2
оказывает лечебное действие при раковых заболеваниях. Действие этого комплекса
основано на том, что в нем происходит постепенное замещение хлорид-ионов
хелатирующими лигандами. Такими лигандами являются аминокислотные остатки в
белках. Координация идет за счет взаимодействия металла с атомами азота
лиганда. После замещения хлорид-ионов создаются условия для замещения и групп NН3.
В результате платина образует четыре связи с новыми лигандами. Это свойство
цис-дихлородиамминплатины приводит к образованию устойчивого комплекса с
молекулой ДНК. Таким образом, это вещество ингибирует синтез ДНК. Интересно
отметить, что транс-изомер дихлородиамминплатины (II)
токсичен, но противоопухолевым действием не обладает.

Наряду с цис-дихлор-диамминплатиной (II)
противоопухолевой активностью обладают и другие комплексы, содержащие в
качестве лигандов амины и хлорид-ионы. Например, цыс-диамминтетрахлорплатина (IV)
[Рt(NН3)2Сl4]
и цис-дианилиндихлороплатина (II)
[Pt(NH2C6H5)2Cl2]:

Сплавы Рt
- Ir и Рt
- Аu применяются в
ортопедической стоматологии, для изготовления шприцов; сплавы Рd-Аu,
Рd-Аu-Рt,
Рd-Рt-Ir
- для изготовления хирургических инструментов, в ортопедической стоматологии
используют сплавы Рd-Аu
или Рd-Аg,Сu,Ir.
Вживляемые в сердце электроды для стимуляции изготовлены из сплава Рt-Ir;
Ir-Рt
- эталон массы (а раньше и длины). Для дезинфекции питьевой воды применяют О3,
его можно получить по реакции:
 ,
,
где Ir
- катализатор (порошкообразный иридий).
Оксид осмия (VIII)
ОsO4
применяется как фиксатор ткани (липидный стабилизатор) для гистологических
исследований в виде 1%-ного раствора в ацетоне. ОsO4
можно использовать и для электронно-микроскопического выявления ферментов.
Механизм действия ОsO4
может быть представлен в следующем виде:

Восстановление может идти
глубже и будет образовываться Оs2О3
или ОsО. Все эти
соединения имеют темно-коричневый или черный цвет, т.е. обеспечивается эффект
контрастирования участка клетки или ткани (образуются эфиры холестерина и
триглицеридов)
Комплекс [Ru(NН3)4(ОН)Сl]Сl
- рутениевый красный также применят для анатомических и гистологических
исследований. Его раствор (1:5000) окрашивает в розово-красные тона пектин.