Производство стекла
Введение
За последние десятилетия научно-техническая
революция во всех областях науки и техники привела к громадным сдвигам в науке
о стекле, и в технологии стекла.
Характерной чертой развития технологии стекла
является резкое повышение производительности оборудования при одновременном
повышении качества изделий, обуславливающее рост эффективности производства.
Задачи повышения производительности оборудования стекольного производства и
повышения качества стеклянных изделий не могут быть спокойно решены без
правильного определения различных параметров процессов производства стеклянных
изделий. Такие параметры могут быть определены экспериментальными методами, но
более правильным путем является применение наряду с экспериментальными методами
расчетных, дающих возможность значительно ускорить определение различных
параметров. Расчетные методы в химии и технологии стекла получили за последние
годы значительное развитие.
Стекло и стеклянные пленки применяют для термо-,
звуко- и электроизоляции. Большие перспективы открываются перед новыми
материалами - так называемыми стеклопластиками, в которых стекловолокно и
стеклянные пленки сочетаются с различными связующими органическими веществами.
Стеклопластики не уступают по прочности стали и в то же время легче ее более
чем в 4 раза. Из стеклопластиков изготавливают корпусы лодок и кораблей, кузова
машин, цистерны и т.д.
В течение последних лет путем кристаллизации
специальных составов стекол научились получать стеклокристаллические материалы,
которые по своей прочности превосходят обычные стекла в 4-10 раз и выдерживают
резкие смены температур вплоть до 1000 С.
Совсем недавно начались исследовательские работы
в новой области стеклоизделия - в производстве стеклообразных полупроводников,
полученных на основе пятиокиси ванадия, сульфидов и селенидов мышьяка, сурьмы и
т.д.
Каждый знает, что основным недостатком стекла
является его хрупкость. Однако уже сейчас достигнуты поразительные успехи в
повышении прочности стекла. Методами термохимического упрочнения удается
повысить сопротивление стекла статическому изгибу. Широко распространено
производство закаленного стекла, применяемого наряду с триплексом для
остекления автомашин и самолетов в качестве «безопасного стекла».
К сортовому стеклу относят обширный класс
стеклоизделий, вырабатываемых из хрустальных, бесцветных и окрашенных стекол
методами ручного и механизированного выдувания и прессования. Они служат для
употребления в быту, хранения и розлива жидких пищевых продуктов, украшения
жилища, оформление культурно-бытовых учреждений.
Технологическая схема производства
светотехнического стекла
Подготовка сырья
↓
Приготовление шихты
↓
Варка стекла
↓
Формирование поверхности стекла
↓
Отжиг стекла
↓
Резка стекла
Характеристика этапов:
1. Подготовка сырья. Смесь сырьевых
компонентов (куда добавляется стекло для снижения температуры точки плавления)
заряжается в топку и разбавляется водой, чтобы отделить нужные компоненты от
грязи.
2. Расплав сырья. В топке процесс
производства стекла проходит 3 главные стадии:
o плавка, когда сырье плавится при
температуре 1550 С;
o очищение, когда расплавленное стекло
гомогенизируется (становится однородным) и из него удаляются пузырьки газа;
o смена температурного режима, когда
расплав охлаждается до вязкого состояния, удобного для протягивания его через
ванну с оловом.
3. Формирование поверхности стекла. Жидкое
стекло выливается на поверхность ванны, наполненной расплавленным оловом,
температура которого около 1000 С. Ванна сделана в виде ленты, толщина олова
6-7 мм. Благодаря высокой вязкости стекла оно не смешивается с жидким оловом,
при этом обеспечивается очень гладкая контактная поверхность обоих материалов,
что и определяет ровную качественную поверхность стекла. Толщина будущих листов
стекла определяется количеством вылитого в ванну расплава стекла.
4. Отжиг стекла. После ванны с оловом
твердое уже стекло в виде ленты проходит через холодный туннель, называемый
"лер". Температура стекла постепенно понижается с 620 до 250 С.
Процесс охлаждения продолжается до тех пор, пока состояние стекла не позволит
его резать и обрабатывать.
. Резка стекла. Охлажденная стеклянная
лента нарезается на столах-автоматах на листы нужного размера.
Сырьевые материалы для производства стекла
Сырьевые материалы, применяемые для производства
стекла, условно делят на главные и вспомогательные. К главным сырьевым
материалам относят природные или искусственные вещества, которые служат для
введения в стекломассу кислотных, щелочных и щелочноземельных оксидов и
диоксидов, являющихся основой для образования стекол.
Вспомогательными сырьевыми материалами считают
различные соединения химических элементов, используемые для окрашивания и
глушения стекла, улучшения качества стекломассы, ускорения варки стекла.
Введение глушителей в стекломассу позволяет получить непрозрачное стекло.
Общее требование ко всем видам стекольного сырья
- чистота и однородность по составу. Чистота сырьевых материалов определяется,
в частности, количественным содержанием в них окислов железа, снижающих
светопрозрачность стекла.
Химический состав листового стекла
|
Содержание
оксидов, мас. %
|
|
SiO2
|
B2O3
|
Al2O3
|
MgO
|
CaO
|
BaO
|
PbO
|
ZnO
|
Na2O
|
K2O
|
|
73
|
-----
|
1,5
|
2,5
|
9
|
-----
|
-----
|
------
|
14
|
------
|
Сырье для ввода в стекломассу двуокиси кремния
Двуокись кремния (кремнезем) SiO2
- важнейшая составная часть промышленных стекол; большинство из них содержит SiO2
от 60 до 75%.
Сырьем для ввода SiO2
в стекло служит главным образом кварцевый песок. Пригодность песка для
стекловарения определяется химическим составом. Для изготовления стекла
применяют песок с высоким содержанием SiO2
и минимальным содержанием окрашивающих окислов (соединений железа). Окислы
железа FeO и Fe2O3
окрашивают стекло и понижают его общую светопрозрачность. От Fe2O3
стекло приобретает желтую окраску, от FeO
- голубую. Стекло, сваренное из песков, содержащих одновременно FeO
и Fe2O3,
имеет зеленоватый оттенок. К вредным примесям песка, которые придают стеклам
нежелательный оттенок, относят также двуокись титана, окислы хрома и ванадия.
На качество стекла влияют форма зерен кварцевого
песка и его зерновой состав. Зерна песка бывают угловатыми и окатанными.
Быстрее провариваются угловатые зерна, так как они имеют большую активную
поверхность и в меньшей степени, чем окатанные, расслаиваются и выпадают из
шихты.
Размер зерен (диаметр) большинства песков
колеблется от 0,1 до 2 мм. Наиболее пригодны для стекловарения пески с зернами
размером 0,15 - 0,4 мм. Зерновой состав песка подбирают, пропуская песок через
сита с отверстиями определенных размеров.
Сырье для ввода в стекломассу щелочных окислов
Окись натрия Na2O.
Окись натрия - одна из основных составных частей стекла. Окись натрия, как и
окислы других щелочных металлов, выполняет роль плавней. Она ускоряет
стеклообразование и понижает температуру варки стекла. Вместе с тем Na2O
повышает коэффициент термического расширения, снижает термическую и химическую
стойкость стекла. Na2O
вводят в стекломассу в виде кальцинированной соды.
Кальцинированная сода - это углекислый натрий.
Кальцинированная безводная сода представляет собой белый порошок, который при
нагревании разлагается на Na2O
и CO2, причем Na2O
(примерно 58,5%) переходит в стекломассу, а CO2
(оставшиеся 41,5%) улетучиваются в атмосферу печи.
Сырье для ввода в стекломассу щелочноземельных
окислов
Окись магния MgO и окись алюминия Al2O3
Для введения MgO и Al2O3
используют доломит. Минерал доломит, природный карбонат кальция и магния,
CaMg(CO3)2. Цвет белый, серый, блекло-желтый. Блеск на гранях и по спайности в
агрегате - стеклянный, матовый. Твердость 3,5-4. Хрупок. Плотность 2,85-3,0.
Кристаллизуется в тригональной сингонии, образуя ромбоэдрические кристаллы,
грани которых имеют форму ромбов и параллельны направлениям его совершенной
спайности. В отличие от более распространенного карбоната кальция (кальцита) не
образует скаленоэдры. Кристаллы доломита часто «седловидные», с искривленными
гранями. Порошок доломита вскипает в холодной соляной кислоте, куски в ней
растворяются очень медленно, но легко растворимы в горячей кислоте. Доломит -
широко распространенный жильный минерал гидротермальных месторождений.
Образуется также в результате замещения кальцита под воздействием магматогенных
или грунтовых вод.
Горная порода доломит состоит главным образом
(на 95%) из минерала доломита. Цвет обычно белый или серый, но может иметь
любой другой оттенок - желтоватый, красноватый и др. Царапается стальной иглой
и отличается от известняка меньшей растворимостью и более сильным блеском.
Достоверно определить доломит можно лишь путем химического анализа. Содержание
кальцита сильно варьирует, так что существует переходный ряд между доломитом и
известняком. Некоторые доломиты имеют включения ископаемых организмов, как
правило, различимых простым глазом. Органические остатки встречаются в них
гораздо реже, чем в известняках, что, вероятно, обусловлено разрушением
органогенных структур при доломитизации.
Расчёт шихты по листовому стеклу
Расчет состава шихты основан на химическом
анализе применяемых сырьевых материалов и на заданном химическом составе
стекла.
Химический состав листового стекла
|
Содержание
оксидов, мас. %
|
|
SiO2
|
B2O3
|
Al2O3
|
MgO
|
CaO
|
BaO
|
PbO
|
ZnO
|
Na2O
|
K2O
|
|
73
|
-----
|
1,5
|
2,5
|
9
|
-----
|
-----
|
------
|
14
|
------
|
Химический состав сырьевых материалов
Таблица 1. Химический состав сырья (в %)
|
Сырьевые
материалы
|
Содержание
оксидов, маc. %
|
|
SiO2
|
Al2O3
|
CaO
|
MgO
|
Na2O
|
|
Песок
|
99,1
|
0,3
|
-
|
-
|
-
|
|
Пегматит
|
72,9
|
15,3
|
0,85
|
0,5
|
3,9
|
|
Доломит
|
0,7
|
0,3
|
32,0
|
20,5
|
-
|
|
Сода
|
-
|
-
|
-
|
-
|
58,2
|
) Расчет состава шихты на 100
вес.ч.стекла:
· Определяем количество песка:
вес.ч. песка -99,1 вес.ч. SiO2
Х вес.ч. песка - 73вес.ч. SiO2
Х = 100×73/99,1
= 73,66 вес.ч.
С песком в состав стекла перейдет следующее
количество окислов (в вес.ч.):
рSiO2
= 73,66;
рAl2O3
= 73,66×0,3/100
= 0,22;
· Определяем количество пегматита
вес.ч. пегматита - 15,3 вес.ч. Al2O3
b вес.ч. пегматита
-1,5 вес.ч. Al2O3
b =
100×1,5/15,3 = 37,97 вес.ч.
· Определяем количество доломита
вес.ч. доломита - 32,0 вес.ч. CaO
c вес.ч. доломита -
9 вес.ч. CaO
вес.ч. доломита - 20,5 вес.ч. MgO
c вес.ч. доломита
-2,5 вес.ч. MgO
с2 = 100×2,5/20,5
= 12,2 вес.ч.
с = с1 + с2 = 28,1 + 12,2 = 40,3
· Определяем количество соды
вес.ч. соды - 58,2 вес.ч. Na2O
e вес.ч. соды - 14
вес.ч. Na2O
e = 100×14/58,2
= 24,05 вес.ч.
С пегматитом в состав стекла перейдет следующее
количество окислов (в вес.ч.):
рSiO2
=37,97 вес.ч.
рAl2O3
= 37,97
×15,3/100
= 5,81;
рСаО= 37,97×0,85/100=0,32
рMgO
= 37,97
×0,5/100 = 0,19;
рNa2O
= 37,97
×3,9/100
= 1,48.
Таблица 2. Расчетный состав шихты
|
Вес.ча-сти
|
SiO2
|
Al2O3
|
CaO
|
Na2O
|
MgO
|
|
Песок
|
73,88
|
73,66
|
0,22
|
−
|
-
|
−
|
|
Пегматит
|
45,77
|
37,97
|
5,81
|
0,32
|
1,48
|
0,19
|
|
Доломит
|
40,03
|
-
|
-
|
40,3
|
−
|
-
|
|
Сода
|
24,05
|
−
|
−
|
-
|
24,05
|
-
|
|
∑
|
184
|
111,63
|
6,03
|
40,62
|
25,53
|
0,19
|
Таблица 3. Суммарный состав шихты
|
Материал
|
Количество
в вес.ч.
|
Сумма
окислов переходящих в стекло
|
|
Песок
|
73,88
|
73,66
|
|
Пегматит
|
45,77
|
45,77
|
|
Доломит
|
40,3
|
40,3
|
|
Сода
|
24,05
|
|
∑
|
184
|
183,78*
|
|
*
Отклонение этих величин от полученных при решении уравнений объясняется двумя
причинами: во-первых, привлечением в шихту окислов, содержащихся в
загрязненных материалах (Al2O3,
и MgO), и,
во-вторых, округлением при вычислении.
|
Из табл. 3 следует:
вес.ч. шихты - 183,78 вес.ч. стекла
х вес.ч. шихты - 100 вес.ч. стекла
х = 184×100/183,78
= 100,12 вес.ч.
· определяем содержание песка:
184 вес.ч. шихты - 73,88 вес.ч. песка
,12 вес.ч шихты - а вес.ч. песка
а = 100,12×73,88/184
= 40,2 вес.ч
· определяем содержание пегматита:
вес.ч. шихты - 45,77 вес.ч. пегматита
,12 вес.ч. шихты - b
вес.ч. пегматита
b = 100,12×45,77/184
= 24,9 вес.ч.
· определяем содержание доломита:
вес.ч. шихты - 40,3 вес.ч доломита
,12 вес.ч. шихты - c
вес.ч. доломита
c = 100,12×40,3/184
= 21,93 вес.ч.
· определяем содержание соды:
вес.ч. шихты - 24,05 вес.ч соды
,12 вес.ч. шихты - d
вес.ч. соды
d = 100,12×24,05/184
= 13,09вес.ч.
∑ = 100,12
) Расчет состава шихты на 100 вес.ч.
песка.
Количество песка по заданию 100 вес.ч.
· Определим количество пегматита.
,2 вес.ч. песка - 45,77 вес.ч. пегматита
вес.ч. песка - b
вес.ч. пегматита
b = 100×45,77/40,2=
113,85 вес.ч.
· Определим количество доломита.
,2вес.ч. песка - 21,93 вес.ч. доломита
вес.ч. песка - с вес.ч. доломита
с = 100×21,93/40,2
= 54,55 вес.ч.
· Определим количество соды.
,2 вес.ч. песка - 13,09 вес.ч. соды
вес.ч. песка - d
вес.ч. соды
d = 100×13,09/40,2
= 32,56 вес.ч.
∑ = 200,96
) Расчет теоретического состава стекла.
По составу шихты (см. табл. 2) можно определить
теоретический состав стекла (в вес. %):
рSiO2
= 111,63×100/183,78
= 60,74
р Al2O3
= 6,03×100/183,78
= 3,28
рСаО = 40,62×100/183,78
= 22,1
рNa2O
= 25,53×100/183,78
= 13,89
рMgO
= 0,19×100/183,78
= 0,103
Таким образом, листовое стекло имеет следующий
теоретический состав (в вес. %):
SiO2 - 60,74%; Al2O3 - 23,28%; СаО
- 22,1%;O - 13,89%; MgO - 0,103%.
4) Расчет выхода стекла.
,12 вес.ч. шихты - 100 вес.ч. стекла
вес.ч. шихты - х вес.ч. стекла
х = 100×100/100,12
= 99,9 вес.ч.
) Расчет потерь при стеклообразовании
(угар).
Потери при стеклообразовании определяются по
разности
- 99,9 = 0,1 вес.ч.
Общее количество влаги в шихте, складывающееся
из влажности материалов и увлажнения шихты с целью частичного предотвращения
пыления при загрузке ее в печь, с одной стороны, и для получения оптимальной
механической однородности шихты, с другой, составляет по практическим данным в
среднем 5%. В исходном составе шихты материалы взяты без учета содержащейся в
них влаги.
· Количество обратного боя составляет
25%, т.е.
,12 × 0,25 = 25,03
вес.ч.
· Количество вводимой шихты:
100,12 - 25,03 = 75,09 вес.ч. 
· Количество воды в шихте:
,09 × 0,05 =
3,7 вес.ч.
· Количество сухой шихты:
,09 - 3,7 = 71,39 вес.ч
Материальный баланс
|
Приход
|
вес.
ч.
|
Расход
|
|
Шихта
Бой Влага Итого
|
75,09
25,03 3,3 103,7
|
Стекломасса
Угар Влага Итого
|
99,9
0,1 3,7 103,7
|
Расчет свойств стекла
Хотя в настоящее время известно много расчетных
методов определения свойств стекла, при использовании этих методов в
практических целях следует учитывать присущие им специфические недостатки.
Первый недостаток расчетных методов - меньшая по сравнению с экспериментальными
методами точность; второй недостаток - ограничение применения расчетных методов
определенными областями составов стекол.
Известные расчетные методы разработаны в
основном для обычных силикатных стекол, для тех областей составов, в которых
находятся широко применяемые промышленные стекла. Расчетные формулы можно
применять только для тех областей составов, для которых рассчитаны коэффициенты
этих формул.
В настоящее время разработаны, как известно,
помимо обычных силикатных стекол также многочисленные разновидности
несиликатных стекол: фосфатные, боратные и др. с успехом применяемые в технике.
Для стекол этих типов методы расчета свойств по химическому составу практически
отсутствуют. Кроме того, свойства стекла (например, плотность, предел
прочности) в определенной степени зависят от таких факторов, как термическое
прошлое стекла, форма и размеры изделия, состояние поверхности (сильно влияет
на прочность стекла), не учитываемых обычно в расчетных методах. Таким образом,
расчетные методы определения величин свойств относятся скорее к стеклу как к
материалу, к стеклу как к изделию.
Пересчет состава стекла из весовых процентов в
молярные
Для пересчета состава стекла из весовых
процентов в молярные сначала определяют число молей в стекле всех его
компонентов.
Так, для 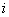 -го
компонента ni=Pi/Mi
-го
компонента ni=Pi/Mi
Затем рассчитывают  по формуле Ni=ni*100/∑
ni
по формуле Ni=ni*100/∑
ni
Состав стекла: SiO2 - 73%; Al2O3 - 1,5%;
СаО - 9%; Na2O - 14%; MgO - 2,5%.
· Определим число молей каждого
компонента стекла:
nSiO2 = 73/60 = 1,217 nCaO = 9/56 =
0,161O3 = 1,5/102 = 0,015 nNa2O = 14/62 = 0,226= 2,5/40 = 0,063
Откуда:
∑ ni= 1,682= 1,217×100/1,682
= 72,35O3 = 0,015 ×100/1,682
= 0,89= 0,161×100/1,682
= 9,57O = 0,226×100/1,682
= 13,44 = 0,063×100/1,682
=3,75
Метод А.А. Аппена
стекло
отжиг производство
А.А. Аппен предложил метод расчета ряда свойств
стекла (плотность, показатель преломления, средняя дисперсия, линейный
коэффициент термического расширения, модули упругости и сдвига, диэлектрическая
проницаемость, поверхностное натяжение). Он получил приближенно усредненные
парциальные величины (аддитивные коэффициенты), которые используют для расчета
свойств стекла.
Для приближенно-усредненных величин, не
являющихся постоянными, выведены уравнения, которые применяют для получения
коэффициентов, пригодных для расчета свойств стекла.
SiO2
· молекулярный объем
VSiO2=27.25+0.035(NSiO2-67)=27.25+0.035(72,35-67)=27.44
cм3/моль;
· показатель преломления
nSiO2=1.489-0.0005(NSiO2-67)=1.489+0.0005(72,35-67)=1.89;
· линейный коэффициент термического
расширения
αSiO2*107=38-1.0(NSiO2-67)=38-1.0(72,35-67)=32,65;
· модуль упругости
ESiO2*10-3=7.15+0.02(NSiO2-67)=7.15+0.02(72,35-67)=7,257
кгс/мм2;
· модуль сдвига
GSiO2*10-3=3.0+0.01(NSiO2-67)=3.0+0.01(72,35-67)=3,05
кгс/мм2;
Для других свойств SiO2
приближенно-усредненные величины принимают постоянными:
· средняя
дисперсия
δSiO2*105=675;
· диэлектрическая проницаемость при частоте 
εSiO2=3.8;
· поверхностное
натяжение при 1300˚С
σSiO2*105=290
дин/см.
Парциальные коэффициенты свойств компонентов в
силикатных щёлочесодержащих стёклах
|
Компонент
|
Молекулярный
обьем,см3/моль,V
|
Показатель
преломления,n
|
Средняя
дисперсия,δ
|
Модуль
сдвига, G*103,кг/мм2
|
ТКЛР,
α
|
Модуль
упругости, Е, кг/мм2
|
|
Na2O
|
20.2
|
1.590
|
1420
|
1.75
|
395
|
5,95
|
|
CaO
|
14.4
|
1.730
|
1480
|
4.95
|
130
|
11,15
|
|
Al2O3
|
40.40
|
1.520
|
850
|
4.95
|
5
|
11,4
|
|
B2O3
|
1.710
|
900
|
7.5
|
-50
|
18
|
Средний линейный коэффициент термического
расширения может быть рассчитан по методу А.А. Аппена с точностью до 2.2*10-7.
Точность расчета других свойств стекла (модуля Юнга и модуля сдвига) лежит в
пределах 3 %.
Таким образом, основные преимущества расчетного
метода А.А. Аппена заключаются в следующем:
· приближенно-усредненные парциальные
величины рассчитаны А.А. Аппеном для большого числа компонентов, в том числе и
неокисных, что дает возможность рассчитывать величины свойств самых
разнообразных стекол;
· метод обеспечивает высокую точность
полученных результатов;
метод позволяет рассчитывать величины восьми
свойств, относящихся к группам механических, оптических, термических и
электрических свойств.
Расчет режима отжига стеклоизделия
Режим отжига стеклоизделия определяется
свойствами стекла, формой и размерами изделий, технологией их изготовления,
конструктивными особенностями печи отжига. Параметры отдельных этапов отжига
(температуры, продолжительности, скорости нагрева) выбирают исходя из
допустимого для каждого конкретного изделия напряжения на основе законов
возникновения, распределения и релаксации напряжений.
Нагрев стекла до температуры отжига (I
этап отжига) проводится с максимальной скоростью, ограниченной возможностью
разрушения изделия. Возникающие при быстром нагреве временные термоупругие
напряжения накладываются на остаточные напряжения, образовавшиеся в изделии при
его формовании. Разрушающие напряжения без учета их знака условно принимают
равными 70 МПа.
· Вычисляем верхнюю температуру отжига
по методу М.В. Охотина:
Тв = - 6,14Na2O+3,15CaO+3,78Al2O3+598,03
=
-6,14×14+3,15×9+3,78×1,5+598,03=
699,11≈ 6990С
Для закрепления формы изделия помещают в печь
отжига, охлаждают до температуры ниже верхней температуры отжига (450…500˚С).
Для расчета принимаем эту температуру 480˚С.
· Скорость на первом этапе отжига
рассчитывается по формуле:
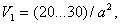
где  - полутолщина листа стекла, см.
- полутолщина листа стекла, см.
Принимаем 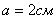 , тогда
, тогда
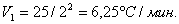
· Время первой стадии
Ι1=(699-480)/6,25=
35,04мин
Выдержка при температуре отжига (II
этап) приводит к выравниванию температур в изделии и релаксации имеющихся в нем
остаточных напряжений.
· Время выдержки при температуре
отжига в зависимости от предшествующей скорости нагрева изделия и его толщины
составляет:

Выдержку можно производить при любой
температуре, лежащей в зоне отжига, однако понижение температуры на каждые 10˚
увеличивает время релаксации напряжений примерно в 2 раза.
· Нижнюю температуру отжига принимают
на 150˚С ниже Тв, то есть
Тн = 699 -150= 549
Ответственное (медленное) охлаждение(III
этап) является важнейшей стадией отжига, поскольку именно на ней в изделии
могут вновь образоваться постоянные напряжения.
· Определяют скорость и время
ответственного охлаждения:


Быстрое охлаждение стекла ниже Тн (IV этап). На
этой стадии - от Тн до комнатной температуры - вероятность релаксации
термоупругих напряжений и появления остаточных напряжений пренебрежимо мало.
· Рассчитываем скорость и время
охлаждения изделий до комнатной температуры (20˚С) на последней стадии процесса
отжига:

Ι3= (549 - 20)/3,75=
141,06мин.
· Таким образом, общая
продолжительность процесса отжига составит:
Ι = 35,04+400+300+141,06= 876,1 мин.
В промышленных условиях температура в
отжигательных печах изменяется настолько плавно, что четкое разграничение
этапов отжига отсутствует.
В соответствии с общими тенденциями развития
технологии стекла исследования в области термической обработки направлены на
интенсификацию отжига стекла. Это достигается сокращением режима отжига (II
и III его этапов).
Заключение
В течение последних десятилетий
научно-техническая революция во всех областях науки и техники привела к
громадным сдвигам и в науке о стекле, и в технологии стекла.
Стекольная промышленность в настоящее время одна
из важнейших отраслей народного хозяйства, оснащенная современной техникой.
За последние годы путем интенсификации процессов
варки стекла, главным образом за счет повышения температуры, увеличения
размеров ванных печей, применяемых в стекольной промышленности, возросло
производство оконного, полированного, теплозащитного и
архитектурно-строительного стекла. Применены новые огнеупорные материалы для
кладки бассейна печей и каналов выработки, что увеличивает срок непрерывной
работы печей. Использование оптимальных химических составов стекла и режимов
выработки позволило повысить скорость вытягивания ленты стекла.
В настоящее время предприятия заняты всемерной
интенсификацией и повышением эффективности производства на базе
научно-технического прогресса.
Принимаются кардинальные меры по созданию
высокопроизводительных машин и технологических линий, оснащенных автоматикой,
по механизации трудоемких работ и транспортных операций. Ведется работа по
экономии материальных и энергетических ресурсов, повышению качества продукции,
увеличению объемов использования отходов и попутных продуктов других
производств, охране окружающей среды.
Cписок литературы
1. Китайгородский И.И. Технология
стекла - М.: Стройиздат, 1967 г., - 564 с., ил.
2. Артамонова М.В., Асланова М.С.,
Бужинский И.М. Химическая технология стекла и ситаллов: учебник для вузов. -
М.: Стройиздат, 1983 г. - 432 с., ил.
3. Жерновая Н.Ф., Онищук В.И.,
Минько Н.И. Физико-химические основы технологии стекла и стеклокристаллических
материалов: учебно-практическое пособие. - Белгород: изд-во БегГТАСМ, 2001 г. -
101 с.
. Матвеев М.А., Матвеев Г.М.,
Френкель Б.Н. Расчеты по химии и технологии стекла: справочное пособие. - М.:
Стройиздат, 1972 г. - 238 с.
5. Роговой М.И., Кондакова М.Н.,
Сагановский М.Н. Расчеты и задачи по теплотехническому оборудованию предприятий
промышленности строительных материалов: учеб. пособие для техникумов. - М.:
Стройиздат, 1975 г. - 320 с.
6. <http://glass2000.by.ru/articles/1_sheetglass.shtml>
. <http://www.starglass.ru/?model=116&page=1&cat=387&m=catalog>
. <http://www.nzsts.ru/>